1.本发明涉及有机合成技术领域,具体涉及一种合成3,3-二取代苯酞的方法。
背景技术:
2.苯酞,又称为异苯并呋喃-1(3h)-酮,为具有γ-内酯与苯稠合的双环结构物质。含有这类结构的天然产物通常具有重要的生物及药物活性。如从芹菜籽里分离出的3-丁基苯酞(nbp),能够抑制血小板凝集、改善微循环、减轻缺血性脑损伤,已成为治疗缺血性脑卒中的有效抗血小板药物;从菊池链格孢中分离出的isoochracinic acid和从多主枝孢中分离出的herbaric acid具有抗菌和抗微生物活性;从皮生球菌中分离出的dermacozined呈现出对不同肿瘤细胞的毒性;从内生真菌炭疽菌cr1535-02中分离出来的化合物对hepg2细胞株具有细胞毒性并且具有强抗氧化性。
[0003][0004]
目前,3,3-二取代苯酞的合成方法鲜有报道。tanaka等人采用rh(cod)2bf4/solphos为催化剂,经1,6-二炔与炔丙醇的[2 2 2]反应和转移酯化,对映体选择性地生成手性3,3-二取代异苯并呋喃-1-酮,但需用到贵金属催化剂。youn等人报道了三唑盐原位脱除质子形成的nhc催化空气对邻烯基苯甲醛的氧化和oxa-michael加成形成3,3-二取代异苯并呋喃-1-酮的方法,采用手性辛可宁代替体系中的三乙胺,以中到高的收率合成了3,3-二取代异苯并呋喃-1-酮,但催化剂用量较高,且反应时间长达6.7-15天。sala等人在koh或k3po4和二苯并-18-冠-6的催化下,以3-芳基苯酞和α,β-不饱和酮的芳基迈克尔反应合成3,3-二取代异苯并呋喃-1-酮化合物,但反应时间较长,多数底物的反应时间在20-164h。
[0005]
带有3-烷基或芳基、3-羧甲基的单取代或二取代的天然产物异苯并呋喃-1-酮具有丰富有效的生物活性,因此人工合成具有相似结构的3,3-二取代异吲哚啉-1-酮化合物具有重要的意义。但合成3,3-二取代异苯并呋喃-1-酮化合物的方法报道较少且仍存在着种种缺陷,如需要贵金属催化剂、催化剂用量较多、反应时间过长。
技术实现要素:
[0006]
为弥补现有技术的不足,本发明提供了一种合成特殊结构的3,3-二取代苯酞的方法,以较为廉价的催化量的cu-膦催化剂,通过级联反应合成3,3-二取代苯酞,不需分离反应中间体,避免了繁琐的操作,反应条件温和、反应较快,以有效解决背景技术中所提及的技术问题,通过以下技术方案实现:
[0007]
本发明在铜盐-膦配体形成的催化剂作用下,使用硅烷作为还原剂,邻酰基苯甲酸
酯(ⅰ)和α,β-不饱和酸酯(ⅱ)进行共轭还原/aldol加成/内酯化级联反应,得到3,3-二取代苯酞(ⅲ)。所述合成路线是:
[0008][0009]
一种合成3,3-二取代苯酞的方法,合成方法为:采用休良克瓶操作,在氮气氛围下,向休良克瓶1中依次加入铜盐-非手性膦配体或手性膦配体的外消旋混合物、式ⅰ底物和溶剂、充分搅拌后向其中加入式ⅱ化合物的溶液,并搅拌;然后向上述混合物中加入硅烷并搅拌反应4-6h即可合成式ⅲ化合物3,3-二取代苯酞;
[0010]
进一步的,所述式ⅰ底物与式ⅲ化合物中的r1为c
1-c
12
的烷基、c
6-c
12
芳基中的一种;式ⅱ化合物与式ⅲ化合物中的r2为c
1-c
12
的烷基;式ⅱ与式ⅲ中r3为h或c
1-c5的烷基;r4为h或c
1-c5的烷基。
[0011]
进一步的,所述的铜盐为cuf(pph3)3·
2meoh、r5co2cu、(r5co2)2cu、(r5co2)2cu
·
mh2o中的一种,m=1或2或3,r5为c
1-c
10
的烷基或c
1-c
10
的取代烷基;或cux、cux2、cui中的一种与naor5的混合物,或cux、cux2、cui中的一种与kor5的混合物,其中x为f、cl、br中的一种。
[0012]
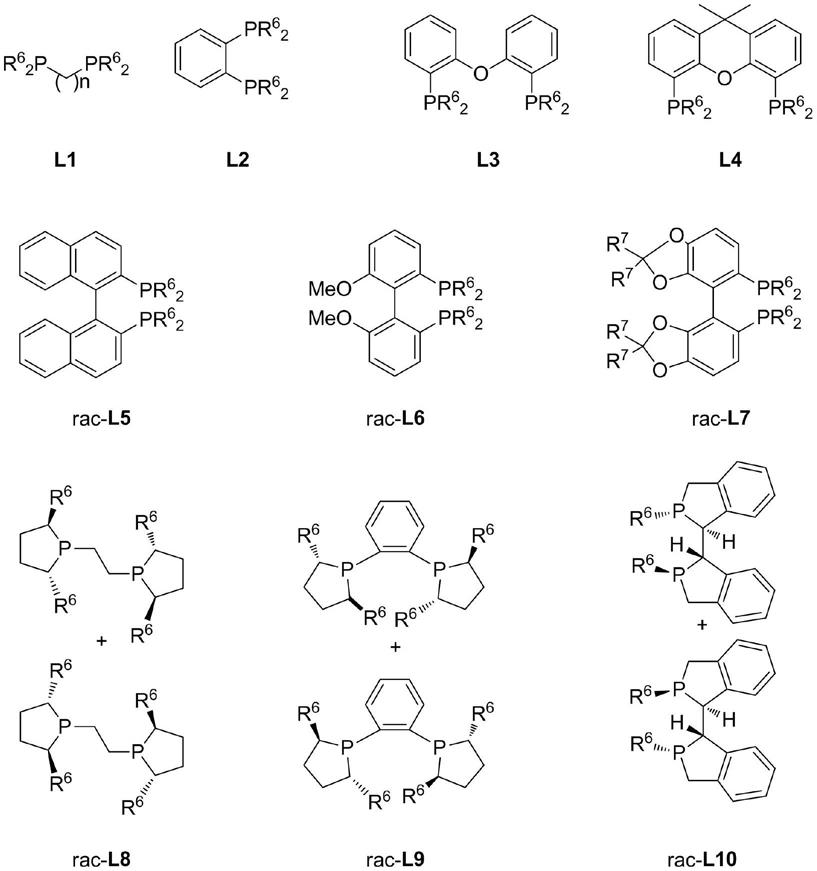
进一步的,所述的配体为非手性膦配体l1-l4或手性膦配体l5-l10的外消旋体(rac-l5-rac-l10)。l1-l10中,r6为苯基或取代苯基中的一种,取代芳基指芳基上的一个到全部h原子被取代的芳基,其中取代基为c
1-c4的直链烷基、c
3-c4的支链烷基、c
1-c4的烷氧基、卤素中的一种或几种;r7为h或甲基或乙基;l1中n=2,3,4,5。
[0013][0014]
进一步的,所述的硅烷包括r8sih3、r
82
sih2、r
83
sih、ph2mesih、(sihme2)2o、(meo)3sih、(sihme2)2nh、((ch3)2osi)n、r9(osihme)
p
or9中的一种;p=1,2,3,
…
,100的整数,r8为me、et或ph,r9为h、si(ch3)3或si(ch3)2bu
t
。
[0015]
进一步的,所述的反应溶剂为醚类或芳烃类或卤代烷类,包括但并不限于乙醚、丁醚、四氢呋喃、1,4-二氧六环、乙二醇二甲醚、乙二醇二乙醚、苯、甲苯、乙苯、二甲苯、三氯甲烷、1,2-二氯乙烷中的一种或一种以上的混合物。
[0016]
进一步的,所述式ⅰ底物的质量为(1-1000)ml/g。
[0017]
进一步的,所述的铜盐、膦配体、硅烷、式i化合物、式ⅱ化合物的摩尔比为(0.02~0.08):(0.02~0.16):(2~5):1:(2-3)。
[0018]
进一步的,所述的反应温度为-20-45℃。
[0019]
本发明与现有技术相比的有益效果是:
[0020]
本发明可以高产率地合成3,3-二取代苯酞,利用廉价的cu-膦催化剂催化反应,性价比较高;反应时间短,4-6h即可完成反应。
[0021]
本发明可以高产率制得3,3-二取代苯酞,所用原料皆为市售原料;该方法只使用了催化量的cu-膦催化剂,反应时间短、反应条件温和、收率高。
附图说明
[0022]
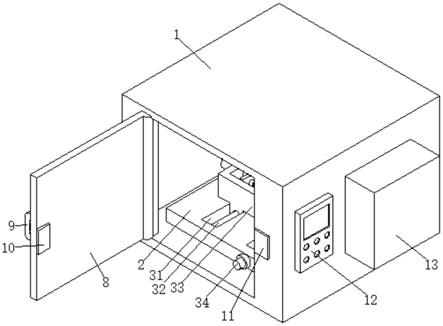
图1为实施例1产物的1hnmr谱图;
[0023]
图2为实施例1产物的
13
cnmr谱图;
[0024]
图3为实施例2产物的1hnmr谱图;
[0025]
图4为实施例2产物的
13
cnmr谱图。
具体实施方式
[0026]
下面通过具体实施例详述本发明,但不限制本发明的保护范围。如无特殊说明,本发明所采用的实验方法均为常规方法,所用实验器材、材料、试剂等均可从商业途径获得。
[0027]
当r
1-r4为相同类型的烷基、芳基和取代芳基时,其制备方法相同,区别仅在于碳的个数不同,不再赘述。
[0028]
实施例1
[0029]
在休良克瓶中加入0.0030g cu(pph3)3f
·
2meoh、0.00125g dppb(l1,n=4,r6=ph)、0.0216g邻苯甲酰苯甲酸甲酯,抽真空/n2置换三次后,加入0.5ml无水甲苯,搅拌10min后给其中加入0.023g甲基丙烯酸甲酯/0.5ml无水甲苯的溶液,降温至0℃并搅拌10min,缓慢加入3equiv的pmhs,反应6h后加入3ml饱和氯化铵水溶液并搅拌1h。过滤、分液,水相用3ml乙酸乙酯萃取两次。合并的有机相经2ml饱和氯化钠溶液洗涤两次,无水硫酸钠干燥、旋蒸、柱层析纯化,得到3-苯基-3-(1-甲基-1-甲氧基酰基)乙基苯酞(
ⅲ‑
1)0.026g,收率93%,无色油状液体。1h-nmr和
13
c-nmr分别见附图1、2。
[0030]
实施例2
[0031]
如实施例1的方法,由0.0094g cu(pph3)3f
·
2meoh、0.0053g rac-l8(r6=ph),0.110g邻苯甲酰苯甲酸甲酯/2ml二甲苯、0.285g甲基丙烯酸苄酯/3ml二甲苯反应4h,经后处理得3-苯基-3-(1-甲基-1-苄氧基酰基)乙基苯酞(
ⅲ‑
2)0.134g,收率76%。1h-nmr和
13
c-nmr分别见附图3、4。
[0032]
实施例3
[0033]
如实施例1的方法,由0.0030g cu(pph3)3f
·
2meoh、0.0016gdpephos(l3,r6=ph)、0.0218g邻甲酰苯甲酸甲酯、0.021g甲基丙烯酸甲酯/0.5ml无水甲苯的溶液、3equiv的pmhs,在0℃反应6h后进行同样的后处理,得到3-苯基-3-(1-甲基-1-甲氧基酰基)乙基苯酞(
ⅲ‑
1)0.026g,收率92%。
[0034]
实施例4
[0035]
如实施例1的方法,由0.0031g cu(pph3)3f
·
2meoh、0.0017gxantphos(l4,r6=ph)、0.0226g邻苯甲酰苯甲酸甲酯、0.023g甲基丙烯酸甲酯/0.5ml无水甲苯的溶液、3equiv的pmhs降温至0℃反应6h,经过同样的后处理,得到3-苯基-3-(1-甲基-1-甲氧基酰基)乙基苯酞(
ⅲ‑
1)0.0265g,收率91%。
[0036]
实施例5
[0037]
如实施例1的方法,由0.0020g cu(oac)2·
h2o、0.0046g dpben(l2,r6=ph)、0.178g邻乙酰苯甲酸甲酯/1.0mlthf混合物、0.200g甲基丙烯酸甲酯/2.0mlthf溶液、2equiv的(meo)3sih,在10℃反应7h后进行同样的后处理,得到3-甲基-3-(1-甲基-1-甲氧基酰基)乙基苯酞(
ⅲ‑
3)0.209g,收率86%。
[0038]
实施例6
[0039]
如实施例1的方法,由0.0125g cu(pph3)3f
·
2meoh、0.0155g l2(r6=ph),0.0880g邻戊酰基苯甲酸甲酯、0.1030g丙烯酸叔丁酯反应,得到3-丁基-3-(1-甲氧基酰基)乙基苯酞(
ⅲ‑
4a和
ⅲ‑
4b)0.104g,dr=97:3(
ⅲ‑
4a:
ⅲ‑
4b),收率82%。
[0040][0041]
对比例1
[0042]
如实施例1的方法,由0.003g cu(pph3)3f
·
2meoh、0.023g邻苯甲酰苯甲酸甲酯、0.022g甲基丙烯酸甲酯/0.5ml无水甲苯的溶液,在0℃反应6h,经同样的后处理,得到3-苯基-3-(1-甲基-1-甲氧基酰基)乙基苯酞(
ⅲ‑
1)0.017g,收率57%。
[0043]
以上所述,仅为本发明创造较佳的具体实施方式,但本发明创造的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明创造披露的技术范围内,根据本发明创造的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明创造的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。