氨基嘧啶酰胺自噬抑制剂及其使用方法
1.相关申请的交叉引用
2.本技术要求2019年6月17日递交的u.s.s.n.62/862,469、2019年6月17日递交的u.s.s.n.62/862,470、2019年10月7日递交的u.s.s.n.62/911,739和2019年10月7日递交的u.s.s.n.62/911,740的优先权,其各自的内容通过引用整体并入本文中。
3.序列表
4.本技术包含已以ascii格式电子提交的序列表,并在此通过引用整体并入。所述ascii副本创建于2020年6月9日,文件名为dcp-081wo_sl.txt,大小为27,190字节。
背景技术:
5.自噬作用(字面含义为“自食”)为出于在应激期下生成营养素的目的使得细胞能够再循环细胞器、蛋白质、储存的脂质、胰高血糖素及其他材料的过程。这些细胞内容物通过在称为自噬小体的囊泡中被吞噬来再循环。随后,自噬小体与降解自噬小体内容物以将营养素再循环至细胞的溶酶体合并。肿瘤细胞倾于活化自噬,这是因为这些细胞具有高代谢需求,经历细胞应激,且通常处于具有有限血流和营养素供应的缺氧环境中。此外,已显示化学疗法和靶向疗法诱导作为治疗耐药机制的自噬作用,且已显示自噬作用抑制(通过自噬基因中的基因功能丧失型突变或通过药理学手段)与化学治疗疗法的组合抑制肿瘤生长且触发肿瘤细胞凋亡达到比单一药剂化学疗法更高的程度。
6.突变ras蛋白驱动约30%所有人类癌症—包括95%胰脏癌和45%结直肠癌,且这些突变ras癌症的治疗为当前高度未满足的医学需要区域。突变ras癌症具有高度增生性并取决于用于生存的基础自噬水平,表明在这些“自噬依赖”癌症中自噬抑制为可行的治疗方法。
7.当前,使用最广泛的自噬抑制剂为作为公认抗疟疾剂的氯喹和羟氯喹。已认为这些抗疟疾药通过在溶酶体区室中被螯合,提高这些溶酶体的ph且因此使降解且再循环营养素的蛋白酶失活来阻断自噬。这些抗疟疾剂除抑制溶酶体以外也具有多个作用机制,且已知其诱发患者的视网膜病变。因此,需要更多选择性地阻断自噬且不展现这些抗疟疾剂的毒性的靶向药剂。ulk1激酶为自噬起始蛋白且为丝氨酸/苏氨酸激酶。ulk1激酶复合物响应于包括营养剥夺和能量耗竭的细胞应激而被活化。营养剥夺通过抑制mtorc1而活化ulk激酶活性,且能量耗竭通过通过amp活化蛋白激酶ampk进行的活化来激活ulk激酶活性。重要地,ulk激酶的激酶失活突变体阻断典型的自噬起始,表明ulk激酶活性的小分子抑制剂应能够阻断自噬。
8.其他机制研究已显示,ulk1基因缺失抑制了癌细胞中的自噬,减轻fox3a转换和促细胞凋亡蛋白puma的上调。除典型自噬的经典活化以外,也已显示ulk1激酶活性需要bcl-2-l-13介导的线粒体自噬(受损线粒体的自噬)。也已证实ulk1和ulk2激酶重塑癌细胞葡萄糖代谢。ulk抑制剂也可发现在阻断这些非典型促肿瘤ulk活性中的效用。
9.自噬也在癌症的宿主细胞和组织中得以上调。证实胰脏组织星形细胞中的自噬支持肿瘤生长。显示胰脏星形细胞通过自噬性丙氨酸分泌来支持胰脏癌肿瘤代谢。证实宿主
组织自噬抑制通过肝脏介导的精氨酸酶分泌增加来引起循环中精氨酸(肿瘤代谢和生长所需氨基酸)耗竭。也显示ulk1激酶活化通过sting抑制性磷酸化来使免疫细胞中的sting通路失活,调节负回馈机制以限制干扰素介导的先天性免疫细胞反应。因此,不仅在肿瘤细胞中活化自噬(癌细胞自发性),而且也在肿瘤微环境或宿主组织中的其他细胞中活化自噬(癌细胞非自发性)以支持肿瘤存活和生长。
10.突变ras癌症依赖自噬。在胰脏癌中,突变ras信号主要通过mapkap通路。突变ras活化raf激酶,之后活化mek激酶,最后活化erk激酶:突变ras
→
raf
→
mek
→
erk。尽管突变ras信号传导通过mapkap通路,该通路的抑制剂在临床试验中用作单一药剂时不提供或提供极少临床效益。最近已报导,mapkap通路抑制诱导了作为补偿性存活机制的自噬。当mek抑制剂与自噬抑制剂羟氯喹组合时,存在引起多种突变ras癌症或突变braf癌症消退的协同活性。类似地,当erk抑制剂与自噬抑制剂羟氯喹或氯喹组合时,存在引起突变ras胰脏癌的抑制的协同活性。已证实,raf激酶(craf和braf)的基因耗竭在自噬也由基因耗竭时在突变ras癌细胞系中引起协同抗肿瘤活性。最近的出版物强调,在复合物中的突变ras癌症中mapkap通路和自噬通路的双重抑制为用于患有突变ras癌症的患者的有前景治疗方案。也已证实,其他靶向疗法和化学治疗剂活化作为抗性机制的肿瘤自噬;因此存在用于组合这些靶向治疗剂或化学治疗剂与自噬抑制剂的理论基础。
11.编码lrrk2激酶的基因中的突变导致帕金森氏病(parkinson'sdisease)。lrrk2点突变见于家族性(遗传性)帕金森氏病患者以及偶发性帕金森氏病患者两者中。帕金森氏病中的最常见lrrk2突变为lrrk2 g2019s。这些lrrk2突变为使得lrrk2信号传导过度活化的功能获得型突变。持续自噬为脑神经元细胞用以维持健康和体内恒定的过程。自噬为使得细胞识别、定位且破坏细胞内老化胞器和结构组件的过程,且具体地,在已知聚集于神经元中的蛋白质的情况下,自噬消除这些毒性蛋白聚集物以维持神经元健康。lrrk2活性抑制了自噬,且lrrk2 g2019s功能获得型突变甚至更能抑制自噬,且已与帕金森氏病的侵袭性形式相关。
12.提高的lrrk2激酶活性也与包括结肠炎和克罗恩氏病(crohn'sdisease)以及炎性肠病的免疫炎性疾病相关。在胃肠道中,lrrk2存在于包括树突状细胞的抗原呈现细胞中。已显示lrrk2活性在患有克罗恩氏病的患者的树突状细胞中凝集素-1介导的先天性免疫反应(包括nfkb通路活化和增加的tnf-α产生)中至关重要。
13.lrrk2抑制剂被探索用于治疗包括帕金森氏病的神经退化性疾病,且也被探索用于治疗包括克罗恩氏病、溃疡性结肠炎和炎性肠病的胃肠道疾病。
14.人们需要抑制自噬且可与mapkap通路抑制剂、化学治疗剂和/或其他靶向治疗剂组合使用的新型靶向疗法。
15.发明概述
16.本文描述了作为自噬抑制剂的化合物、药物组合物及其作为药剂在治疗诸如癌症的病症中的用途、其制备方法以及含有其作为活性成分的药物组合物。这些药物组合物可包含作为单一活性剂或在存在药学上可接受的赋形剂的情况下与其他活性剂组合的化合物。在一个实施方案中,所描述的化合物为包括ulk1和ulk2活性的ulk激酶活性的抑制剂。
17.例如,本文所提供的化合物可描述为式i:
[0018][0019]
或其药学上可接受的盐、对映异构体、立体异构体或互变异构体,其中:a选自:苯基和5或6员杂芳基;w为ch或n;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:卤素、氰基、c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基、c
1-c5烷氧基和c
1-c5烷氧基-c
2-c5烷基,其中各c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基和c
1-c5烷氧基可任选地被一个、两个或三个独立出现的氟或氰基取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r4选自:b、d、nr6r9、nr
6-(c(r
10
)2)
p-nr6r9、c(o)-nr6r9、c(o)-b、c(o)-d和cn;b选自:具有至少一个氮且任选地具有另一环氮或氧的n连接杂环基、及杂芳基,其中b可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;d选自:具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中d可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基、氰基和(c(r
10
)2)
h-nr6r9,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起形成桥氧基;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
10
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选被一或多个独立出现的氟取代,或两个r
10
与其所附接的碳连接在一起以形成c
3-c5环烷基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;l为-(c(r
10
)2)
m-;h为1、2或3;m为0、1、2或3;n为2、3或4;且p为2或3;其限制条件为当m为0时,
r4为c连接至环a,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l;且其他限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0020]
本文也描述一种化合物,其由以下表示:
[0021][0022]
或其药学上可接受的盐、对映异构体、立体异构体或互变异构体,其中:w为ch或n;x为ch或n;y为c(r
33
)或n;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:卤素、氰基、c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基、c
1-c5烷氧基和c
1-c5烷氧基-c
2-c5烷基,其中各c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基和c
1-c5烷氧基可任选地被一个、两个或三个独立出现的氟或氰基取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
33
选自:h、卤素、c
1-c6烷基和c
1-c6烷氧基,其中c
1-c6烷基和c
1-c6烷氧基可任选地被一或多个独立出现的氟取代;r4选自:b、d、nr6r9、nr
6-(c(r
10
)2)
p-nr6r9、c(o)-nr6r9、c(o)-b、c(o)-d和cn;b选自:具有至少一个氮且任选地具有另一环氮或氧的n连接杂环基、及杂芳基,其中b可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;d选自:具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中d可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基、氰基和(c(r
10
)2)
h-nr6r9,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起形成桥氧基;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
10
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
10
与其所附接的碳连接在一起以形成c
3-c5环烷基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;
u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2,或3;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;l为-(c(r
10
)2)
m-;h为1、2或3;m为0、1、2或3;n为2、3或4;且p为2或3;其限制条件为x和y均不为n,当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0023]
在另一方面中,本文描述式id化合物
[0024][0025][0026]
或其药学上可接受的盐、对映异构体、立体异构体或互变异构体,其中:
[0027]
环dd选自:
[0028][0029]
w为ch或n;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:卤素、氰基、c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基、c
1-c5烷氧基和c
1-c5烷氧基-c
2-c5烷基,其中各c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基和c
1-c5烷氧基可任选地被一个、两个或三个独立出现的氟或氰基取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r4选自:b、d、nr6r9、nr
6-(c(r
10
)2)
p-nr6r9、c(o)-nr6r9、c(o)-b、c(o)-d和cn;b选自:具有至少一个氮且任选地具有另一环氮或氧的n连接杂环基、及杂芳基,其中b可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;d选自:具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中d可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基、氰基和(c(r
10
)2)
h-nr6r9,其中c
1-c6烷基和c
3-c6环烷基可任选地
被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起形成桥氧基;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
10
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
10
与其所附接的碳连接在一起以形成c
3-c5环烷基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2,q为1、2或3;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;l为-(c(r
10
)2)
m-;h为1、2或3;m为0、1、2或3;n为2、3或4;且p为2或3;其限制条件为当m为0时,r4为c连接至吡唑基环,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l;且其他限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0030]
发明详述
[0031]
现将本发明的特点及其他细节加以更明确的描述。本说明书、实施例和所附权利要求书中所采用的特定术语在此处汇集。这些定义应根据本发明的其余部分来阅读,且如本领域技术人员所理解。除非另外定义,否则本文所用的所有技术和科学术语具有如本领域技术人员通常理解的相同的含义。
[0032]
定义
[0033]
如本文所用,术语“烷基”是指饱和直链或支链烃。示例性烷基包括但不限于:具有1-6、1-5、1-4、1-3或1-2个碳原子的直链或支链烃,在本文中分别称作c
1-c6烷基、c
1-c5烷基、c
1-c4烷基、c
1-c3烷基和c
1-c2烷基。示例性烷基包括但不限于:甲基、乙基、丙基、异丙基、2-甲基-1-丁基、3-甲基-2-丁基、2-甲基-1-戊基、3-甲基-1-戊基、4-甲基-1-戊基、2-甲基-2-戊基、3-甲基-2-戊基、4-甲基-2-戊基、2,2-二甲基-1-丁基、3,3-二甲基-1-丁基、2-乙基-1-丁基、丁基、异丁基、叔丁基、戊基、异戊基、新戊基、己基等。
[0034]
如本文所用,术语“烯基”是指具有至少一个碳-碳双键的不饱和直链或支链烃。示例性烯基包括但不限于:具有2-6或3-4个碳原子的直链或支链基团,在本文中分别称作c
2-c6烯基和c
3-c4烯基。示例性烯基包括但不限于:乙烯基、烯丙基、丁烯基、戊烯基等。
[0035]
如本文所用,术语“烷氧基”是指连接至氧的直链或支链烷基(烷基-o-)。示例性烷
氧基包括但不限于:具有1-6或2-6个碳原子的烷氧基,在本文中分别称作c
1-c6烷氧基和c
2-c6烷氧基。示例性烷氧基包括但不限于:甲氧基、乙氧基、异丙氧基等。
[0036]
如本文所用,术语“烷氧基烷基”是指附接至氧、附接至第二直链或支链烷基的直链或支链烷基(烷基-o-烷基-)。示例性烷氧基烷基包括但不限于:其中烷基各自独立地含有1-6个碳原子的烷氧基烷基,在本文中称作c
1-c6烷氧基-c
1-c6烷基。示例性烷氧基烷基包括但不限于:甲氧基甲基、2-甲氧基乙基、1-甲氧基乙基、2-甲氧基丙基、乙氧基甲基、2-异丙氧基乙基等。
[0037]
如本文所用,术语“炔基”是指具有至少一个碳-碳三键的不饱和直链或支链烃。示例性炔基包括但不限于:具有2-6或3-6个碳原子的直链或支链基团,在本文中分别称作c
2-c6炔基和c
3-c6炔基。示例性炔基包括但不限于:乙炔基、丙炔基、丁炔基、戊炔基、己炔基、甲基丙炔基等。
[0038]
如本文所用,术语“氰基”是指基团-cn。
[0039]
如本文所用,术语“环烷基”或“碳环基”是指具有例如3-6或4-6个碳的饱和或部分不饱和烃基,在本文中分别称作c
3-c6环烷基或c
4-c6环烷基。示例性环烷基包括但不限于:环己基、环戊基、环戊烯基、环丁基或环丙基。
[0040]
如本文中所使用的术语“环烷氧基”是指附接至氧的环烷基(环烷基-o-)。示例性环烷氧基包括但不限于:具有3-6个碳原子的环烷氧基,在本文中称作c
3-c6环烷氧基。示例性环烷氧基包括但不限于:环丙氧基、环丁氧基、环戊氧基、环己氧基等。
[0041]
如本文所用,术语“卤基”或“卤素”是指f、cl、br或i。
[0042]
如本文所用,术语“杂芳基”是指含有一或多个杂原子(例如1-3个诸如氮、氧和硫的杂原子)的单环芳族5或6员环系统。可能时,该杂芳基环可通过碳或氮连接至相邻基团。杂芳基环的实例包括但不限于:呋喃、噻吩、吡咯、噻唑、恶唑、异噻唑、异恶唑、咪唑、吡唑、三唑、吡啶或嘧啶等。
[0043]
术语“杂环基(heterocyclyl/heterocyclic group)”为该领域公认的且是指饱和或部分不饱和4-10员环结构,包括单环、桥接环或稠环,且这种环结构包括1-3个诸如氮、氧和硫的杂原子。可能时,杂环基环可通过碳或氮连接至相邻基团。杂环基的实例包括但不限于:吡咯烷、哌啶、吗啉、硫代吗啉、哌嗪、氧杂环丁烷、氮杂环丁烷、四氢呋喃或二氢呋喃等。
[0044]
如本文所使用,术语“内酰胺”是指具有1-氮杂环烷-2-酮结构的氨基甲酸的环状酰胺,或具有不饱和或取代该环的一或多个碳原子的杂原子的类似物。“α-内酰胺”是指由3员环构成的内酰胺。“β-内酰胺”是指由4员环构成的内酰胺。“γ-内酰胺”是指由5员环构成的内酰胺。“δ-内酰胺”是指由6员环构成的内酰胺。“ε-内酰胺”是指由7员环构成的内酰胺。
[0045]
如本文所用,术语“桥氧基”是指基团=o。
[0046]“组合疗法”为包括向有需要的患者的施用例如式i化合物和mapkap通路抑制剂的两种或更多种治疗剂的治疗。
[0047]“疾病”、“病症”和“病况”在本文中可互换使用。
[0048]“个体”、“患者”或“受试者”可互换使用且包括任何动物,包括哺乳动物,优选小鼠、大鼠、其他啮齿动物、兔、狗、猫、猪、牛、绵羊、马或灵长类动物,且最优选为人类。本文所描述的化合物可施用于哺乳动物,如人类,但也可施用于其他哺乳动物,诸如需要兽医治疗的动物,例如家畜(例如,狗、猫及其类似动物)、农畜(例如,牛、绵羊、猪、马及其类似动物)
和实验动物(例如,大鼠、小鼠、天竺鼠及其类似动物)。
[0049]“mapkap通路抑制剂”为map激酶信号传导通路抑制剂。该通路抑制剂包括ras抑制剂(例如amg-510、mrtx 849)、raf抑制剂(例如达拉非尼(dabrafenib)、维罗非尼(vemurafenib)、ly3009120)、mek抑制剂(例如曲美替尼(trametinib)、比美替尼(binimetinib)、司美替尼(selumetinib)、考比替尼(cobimetinib))和erk抑制剂(例如优立替尼(ulixertinib)、sch772984、ly3214996)。术语“mapkap通路抑制剂”和“mapkap激酶抑制剂”在本文中可互换使用。
[0050]“药学上或药理学上可接受”包括当按需要向动物或人类施用时不产生不利、过敏或其他不良反应的分子实体和组合物。对于人类施用,制剂应符合fda管理局的生物制剂标准(fda office of biologics standards)所要求的无菌、发热性和通用安全和纯度标准。
[0051]
如本文所用,术语“药学上可接受的载体”或“药学上可接受的赋形剂”是指与药物施用兼容的任何和所有溶剂、分散介质、包衣、等张剂和吸收延迟剂以及其类似物。这些介质和药剂用于药物活性物质的用途在本领域中众所周知。组合物也可含有提供补充、额外或增强治疗功能的其他活性化合物。
[0052]
如本文所用,术语“药物组合物”是指包含与一种或多种药学上可接受的载体一起配制的如本文所公开的至少一种化合物的组合物。
[0053]
如本文所用,术语“药学上可接受的盐”是指具有可存在于组合物中所用化合物中的酸性或碱性基团的盐。在本质上为碱性的本发明组合物中所包括的化合物能够与各种无机酸和有机酸形成广泛多种盐。可用于制备这种碱性化合物的药学上可接受的酸加成盐的酸为形成无毒酸加成盐(也即,含有药理学上可接受的阴离子的盐)的这类酸,包括但不限于:苹果酸盐、草酸盐、氯、溴、碘、硝酸盐、硫酸盐、硫酸氢盐、磷酸盐、酸式磷酸盐、异烟酸盐、乙酸盐、乳酸盐、水杨酸盐、柠檬酸盐、酒石酸盐、油酸盐、丹宁酸盐、泛酸盐、酒石酸氢盐、抗坏血酸盐、琥珀酸盐、顺丁烯二酸盐、龙胆酸盐、反丁烯二酸盐、葡糖酸盐、葡糖醛酸盐、葡糖二酸盐、甲酸盐、苯甲酸盐、谷氨酸盐、甲磺酸盐、乙磺酸盐、苯磺酸盐、对甲苯磺酸盐和双羟萘酸盐(例如1,1'-亚甲基-双-(2-羟基-3-萘甲酸盐))。在本质上为酸性的包含于本发明组合物中的化合物能够与各种药理学上可接受的阳离子形成碱盐。这种盐的实例包括碱金属盐或碱土金属盐,尤其钙盐、镁盐、钠盐、锂盐、锌盐、钾盐和铁盐。包括碱性或酸性部分的包含于本发明组合物中的化合物也可与各种氨基酸形成药学上可接受的盐。本发明化合物可含有酸性和碱性基团两者;例如一个氨基和一个羧酸基团。在此情况下,化合物可以酸加成盐、两性离子或碱盐的形式存在。
[0054]
本发明化合物可含有一或多个手性中心,且因此以立体异构体形式存在。当在本文中使用时,术语“立体异构体”由所有对映异构体或非对映异构体组成。根据手性碳原子周围的取代基的构型,这些化合物可由符号“( )”、“(-)”、“r”或“s”指定,但本领域技术人员将认识到结构可隐含地表示手性中心。本发明所描述的化合物涵盖这些化合物的各种立体异构体及其混合物。在命名法中,对映异构体或非对映异构体的混合物可指定为“(
±
)”,但本领域技术人员将认识到,结构可隐含地指代手性中心。
[0055]
在本说明书中,术语“治疗有效量”是指研究人员、兽医、医生或其他临床师正探索的将引起组织、系统或动物(例如,哺乳动物或人类)发生生物学或医学反应的本发明化合物的量。本文所描述的化合物以治疗有效量施用以治疗病症。
[0056]“治疗”包括引起病况、疾病、病症等的改良的任何作用,例如减轻、减少、调节或排除。
[0057]
本公开也涵盖与本文所述的化合物一致的被同位素标记的化合物,不同的处在于:一或多个原子被原子量或质量数不同于自然界中通常所见的原子量或质量数的原子取代。可并入本发明化合物中的同位素的实例包括氢、碳、氮、氧、磷、硫、氟和氯的同位素,分别诸如2h、3h、
13
c、
14
c、
15
n、
18
o、
17
o、
31
p、
32
p、
35
s、
18
f和
36
cl。例如,本发明化合物可具有被氘取代的一或多个h原子。
[0058]
本发明化合物的单个对映异构体和非对映异构体可由含有不对称或立体对称中心的市售起始材料以合成方式制备,或通过制备外消旋混合物,随后通过本领域技术人员熟知的解析方法来制备。这些解析方法通过以下例示:(1)将对映异构体的混合物附接至手性助剂,通过再结晶或层析分离非对映异构体的所得混合物,且从所述助剂释放光学纯产物,(2)采用光学活性解析剂进行盐形成,(3)在手性液相层析柱上直接分离光学对映异构体的混合物,或(4)使用立体选择性化学或酶试剂进行动力学解析。外消旋混合物也可通过熟知方法解析为其组分对映异构体,这类熟知方法如手性相液相层析或在手性溶剂中结晶化合物。立体选择性合成,在生成新的立构中心期间或在转化预先存在的一种立构中心期间,单一反应物形成立体异构体的不相同混合物的化学或酶反应为本领域中所熟知。立体选择性合成涵盖对映和非对映立体选择性转化两者,且可涉及手性助剂的使用。例如,参见carreira和kvaerno,classics in stereoselective synthesis,wiley-vch:weinheim,2009。
[0059]
化合物
[0060]
在一个方面中,本文所提供的化合物可由以下式i描述:
[0061][0062]
或其药学上可接受的盐、对映异构体、立体异构体或互变异构体,其中a选自:苯基和5或6员杂芳基;w为ch或n;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:卤素、氰基、c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基、c
1-c5烷氧基和c
1-c5烷氧基-c
2-c5烷基,其中各c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基和c
1-c5烷氧基可任选地被一个、两个或三个独立出现的氟或氰基取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r4选自:b、d、nr6r9、nr
6-(c(r
10
)2)
p-nr6r9、c(o)-nr6r9、c(o)-b、c(o)-d和cn;b选自:具有至少一个氮且任选地具有另一环氮或氧的n连接杂环基、及杂芳基,其中b可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;d选自:具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中d可任选地
在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基、氰基和(c(r
10
)2)
h-nr6r9,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起形成桥氧基;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
10
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
10
与其所附接的碳连接在一起以形成c
3-c5环烷基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;l为-(c(r
10
)2)
m-;h为1、2或3;m为0、1、2或3;n为2、3或4;且p为2或3;其限制条件为当m为0时,r4为c连接至环a,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l;且其他限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0063]
例如,本文也描述由式ia表示的化合物:
[0064][0065]
或其药学上可接受的盐、对映异构体、立体异构体或互变异构体,其中:w为ch或n;x为ch或n;y为c(r
33
)或n;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:卤素、氰基、c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基、c
1-c5烷氧基和c
1-c5烷氧基-c
2-c5烷基,其中各c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基和c
1-c5烷氧基可任选地被一个、两个或三个独立出现的氟或氰基取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选
地被一或多个独立出现的氟取代;r
33
选自:h、卤素、c
1-c6烷基和c
1-c6烷氧基,其中c
1-c6烷基和c
1-c6烷氧基可任选地被一或多个独立出现的氟取代;r4选自:b、d、nr6r9、nr
6-(c(r
10
)2)
p-nr6r9、c(o)-nr6r9、c(o)-b、c(o)-d和cn;b选自:具有至少一个氮且任选地具有另一环氮或氧的n连接杂环基、及杂芳基,其中b可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;d选自:具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中d可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基、氰基和(c(r
10
)2)
h-nr6r9,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起形成桥氧基;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
10
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
10
与其所附接的碳连接在一起以形成c
3-c5环烷基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;l为-(c(r
10
)2)
m-;h为1、2或3;m为0、1、2或3;n为2、3或4;且p为2或3;其限制条件为x和y均不为n,当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0066]
在一些实施方案中,w为n。在一些实施方案中,x为ch,且y为n。在一些实施方案中,x为ch,且y为c(r
33
)。
[0067]
在一些实施方案中,r4为b。
[0068]
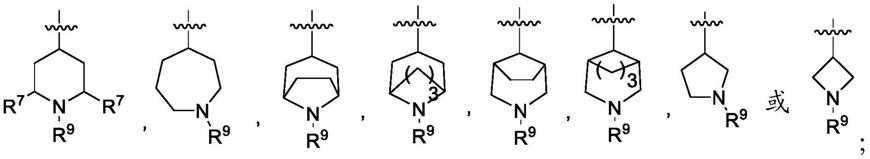
在一些实施方案中,r4选自:
[0069][0070]
其中u为1、2或3。
[0071]
在一些实施方案中,r4选自:
[0072][0073]
在一些实施方案中,r4选自:
[0074][0075]
在一些实施方案中,r4选自:
[0076]
在一些实施方案中,r4为d。
[0077]
在一些实施方案中,r4选自:
[0078][0079]
在一些实施方案中,l为-(ch2)m。在一些实施方案中,m为0。在一些实施方案中,m为1。在一些实施方案中,m为2。在一些实施方案中,m为3。
[0080]
在一些实施方案中,r1选自:卤素、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代。在一些实施方案中,r1为cf3。在一些实施方案中,r1为cf2h。在一些实施方案中,r1选自氯、溴和氟。在一些实施方案中,r1为溴。在一些实施方案中,r1为环丙基。
[0081]
在一些实施方案中,r2选自:c
3-c5环烷基、c
1-c5烷基、卤素、cn、c
2-c5烯基和c
2-c5炔基,其中c
3-c5环烷基、c
1-c5烷基、c
2-c5烯基和c
2-c5炔基可任选地被一个、两个或三个独立出现的氟取代。在一些实施方案中,r2选自:c
1-2
烷基和c
3-4
环烷基。
[0082]
在一些实施方案中,r3选自:h和c
1-c3烷基,其中c
1-c3烷基可任选地被一或多个独立出现的氟取代。
[0083]
在一些实施方案中,r
l
选自:c
1-c6烷基和c
3-c6环烷基,其各自可任选地被1、2或3个独立出现的氟取代。
[0084]
在一些实施方案中,r
l
为环丁基。在一些实施方案中,r
l
为nr
11r12
。
[0085]
在一些实施方案中,r
l
为其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2
或3;r
13
选自:h和c
1-c3烷基;且r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;其限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0086]
在一些实施方案中,n为3。
[0087]
在一些实施方案中,化合物由式ib表示:
[0088][0089]
或其药学上可接受的盐,其中:n为2、3或4;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:c
1-c2烷基和c
3-c4环烷基和卤素,其中c
1-c2烷基和c
3-c4环烷基可任选地被一个、两个或三个独立出现的氟取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r4选自:
[0090][0091]
r9选自:h、c
1-c6烷基、c
3-c6环烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r7在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起以形成桥氧基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;且r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;其限制条件为x和y均不为n,当r为0且q为1
时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0092]
在一些实施方案中,r1选自:卤素、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟和c
3-c5环烷基取代。在一些实施方案中,r1为cf3。在一些实施方案中,r1为cf2h。在一些实施方案中,r1选自:氯、溴和氟。在一些实施方案中,r1为溴。在一些实施方案中,r1为环丙基。
[0093]
在一些实施方案中,r2选自:c
3-c4环烷基、c
1-c5烷基和卤素。在一些实施方案中,r2选自:c
1-c2烷基、c
3-c4环烷基和溴。
[0094]
在一些实施方案中,r3选自:h和c
1-c3烷基,其中c
1-c3烷基可任选地被一或多个独立出现的氟取代。
[0095]
在一些实施方案中,r4选自:
[0096][0097]
在一些实施方案中,r4选自:
[0098][0099]
在一些实施方案中,各r6和r9独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代。
[0100]
在一些实施方案中,r7为h。
[0101]
在一些实施方案中,r
l
选自:c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代。
[0102]
在一些实施方案中,r
l
为环丁基。在一些实施方案中,r
l
为nr
11r12
。
[0103]
在一些实施方案中,r
l
为其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r
13
选自:h和c
1-c3烷基;且r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;其限制条件为当r为0且q为1时,则u不为cr
13
且v不为
o,且当r或q为1时,则u不为n且v不为o或nr6。
[0104]
在一些实施方案中,-n(r3)-c(o)-r
l
选自:
[0105][0106]
在一些实施方案中,-n(r3)-c(o)-r
l
选自:
[0107][0108]
在一些实施方案中,n为3。
[0109]
在一些实施方案中,化合物由选自下组的结构式表示:
[0110][0111]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0112]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0113]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0114]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0115]
在一些实施方案中,化合物由选自下组的结构式表示:
[0116][0117]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0118]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0119]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0120]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0121]
在一些实施方案中,化合物由选自下组的结构式表示:
[0122][0123]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0124]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0125]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0126]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0127]
在一些实施方案中,化合物由式ic表示:
[0128][0129]
或其药学上可接受的盐,其中:n为2、3或4;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:c
1-c2烷基和c
3-c4环烷基和卤素,其中c
1-c2烷基和c
3-c4环烷基可任选地被一个、两个或三个独立出现的氟取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r4选自:
[0130][0131]
r9独立地选自:h、c
1-c6烷基、c
3-c6环烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r7在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起以形成桥氧基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;且r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;其限制条件为x和y均不为n,当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0132]
在一些实施方案中,r1选自:卤素、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟和c
3-c5环烷基取代。在一些实施方案中,r1为cf3。在一些实施方案中,r1为cf2h。在一些实施方案中,r1选自:氯、溴和氟。在一些实施方案中,r1为溴。在一些实施方案中,r1为环丙基。
[0133]
在一些实施方案中,r2选自:c
3-c4环烷基、c
1-c5烷基和卤素。在一些实施方案中,r2选自:c
1-c2烷基、c
3-c4环烷基和溴。
[0134]
在一些实施方案中,r3选自:h和c
1-c3烷基,其中c
1-c3烷基可任选地被一或多个独立出现的氟取代。
[0135]
在一些实施方案中,r4选自:
[0136][0137]
在一些实施方案中,r4选自:
[0138][0139]
在一些实施方案中,各r6和r9独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代。
[0140]
在一些实施方案中,r7为h。
[0141]
在一些实施方案中,r
l
选自:c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代。
[0142]
在一些实施方案中,r
l
为环丁基。在一些实施方案中,r
l
为nr
11r12
。
[0143]
在一些实施方案中,r
l
为其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r
13
选自:h和c
1-c3烷基;且r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;其限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0144]
在一些实施方案中,-n(r3)-c(o)-r
l
选自:
[0145][0146]
在一些实施方案中,-n(r3)-c(o)-r
l
选自:
[0147][0148]
在一些实施方案中,n为3。
[0149]
在一些实施方案中,化合物由选自下组的结构式表示:
[0150][0151]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0152]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立
地选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0153]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0154]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0155]
在一些实施方案中,化合物由选自下组的结构式表示:
[0156][0157]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0158]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0159]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0160]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0161]
在一些实施方案中,化合物由选自下组的结构式表示:
[0162][0163]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;且n为3。
[0164]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0165]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0166]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基、溴和氯;r3在每次出现时独立地选自:h和c
1-c2烷基;r9在每次出现时独立地选自:h和c
1-c3烷基;且n为3。
[0167]
本文也描述式id化合物
[0168][0169]
或其药学上可接受的盐、对映异构体、立体异构体或互变异构体,
[0170]
其中:环dd选自:
[0171][0172]
w为ch或n;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:卤素、氰基、c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基、c
1-c5烷氧基和c
1-c5烷氧基-c
2-c5烷基,其中各c
1-c5烷基、c
3-c6环烷基、c
2-c5烯基、c
2-c5炔基和c
1-c5烷氧基可任选地被一个、两个或三个独立出现的氟或氰基取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r4选自:b、d、nr6r9、nr
6-(c(r
10
)2)
p-nr6r9、c(o)-nr6r9、c(o)-b、c(o)-d和cn;b选自:具有至少一个氮且任选地具有另一环氮或氧的n连接杂环基、及杂芳基,其中b可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;d选自:具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中d可任选地在一或多个可用碳上被r7取代且可任选地在可用氮上被r9取代;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基、氰基和(c(r
10
)2)
h-nr6r9,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起形成桥氧基;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9选自:h、c
1-c6烷基、c
3-c6环烷基、c
1-c5烷氧基-c
2-c5烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
10
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
10
与其所附接的碳连接在一起以形成c
3-c5环烷基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2,q为1、2或3;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被
一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;l为-(c(r
10
)2)
m-;h为1、2或3;m为0、1、2或3;n为2、3或4;且p为2或3;其限制条件为当m为0时,r4为c连接至吡唑基环,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l;且其他限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0173]
在一些实施方案中,w为n。在一些实施方案中,w为ch。
[0174]
在一些实施方案中,环dd选自:
[0175][0176]
在一些实施方案中,环dd选自:
[0177][0178]
在一些实施方案中,环dd为:
[0179][0180]
在一些实施方案中,r4为d。
[0181]
在一些实施方案中,r4选自:
[0182][0183]
在一些实施方案中,r4选自:
[0184][0185]
在一些实施方案中,r4为b。
[0186]
在一些实施方案中,r4选自:
[0187][0188]
其中u为1或2。
[0189]
在一些实施方案中,r4选自:
[0190][0191]
在一些实施方案中,r4选自:
[0192][0193]
在一些实施方案中,l为-(ch2)m。在一些实施方案中,m为0。在一些实施方案中,m为1。在一些实施方案中,m为2。在一些实施方案中,m为3。
[0194]
在一些实施方案中,r4为d,且m为0。在一些实施方案中,r4为d,且m为1。在一些实施方案中,r4选自d和b,且m为2。在一些实施方案中,r4选自d和b,且m为3。
[0195]
在一些实施方案中,r1选自:卤素、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代。在一些实施方案中,r1为cf3。在一些实施方案中,r1为cf2h。在一些实施方案中,r1选自:氯、溴和氟。在一些实施方案中,r1为溴。在一些实施方案中,r1为环丙基。
[0196]
在一些实施方案中,r2选自:c
3-c5环烷基、c
1-c5烷基、卤素、氰基、c
2-c5烯基和c
2-c5炔基,其中c
3-c5环烷基、c
1-c5烷基、c
2-c5烯基和c
2-c5炔基可任选地被一个、两个或三个独立出现的氟取代。在一些实施方案中,r2选自:c
1-2
烷基和c
3-4
环烷基。
[0197]
在一些实施方案中,r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代。
[0198]
在一些实施方案中,r
l
为环丁基。在一些实施方案中,r
l
为nr
11r12
。
[0199]
在一些实施方案中,r
l
为其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r
13
选自:h和c
1-c3烷基;且r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;其限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0200]
在一些实施方案中,n为3。
[0201]
在一些实施方案中,化合物由式ie表示:
[0202][0203]
或其药学上可接受的盐,其中:环dd选自:
[0204][0205]
n为2、3或4;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代;r2选自:c
1-c2烷基和c
3-c4环烷基和卤素,其中c
1-c2烷基和c
3-c4环烷基可任选地被一个、两个或三个独立出现的氟取代;r3选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r4选自:
[0206][0207]
r9选自:h、c
1-c6烷基、c
3-c6环烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r5选自:h、c
1-c6烷基、c
3-c6环烷基和杂环基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r7在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代,或两个r7与其所附接的原子连接在一起以形成桥氧基;r
l
选自:c
1-c6烷基和c
3-c6环烷基、nr
11r12
和其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r6选自:h、c
1-c6烷基、c
3-c6环烷基、c(=o)r5、so2r5、具有至少一个氮且任选地具有另一环氮或氧的c连接杂环基、及杂芳基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r
11
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
12
选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代;r
13
选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;且l为-(c(r
10
)2)
m-;m为0、1、2或3;其限制条件为当m为0时,r4为c连接至吡唑基环,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l;且其他限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0208]
在一些实施方案中,环dd为:
[0209][0210]
在一些实施方案中,r1选自:卤素、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环烷基可任选地被一个、两个或三个独立出现的氟取代。在一些实施方案中,r1为cf3。在一些实施方案中,r1为cf2h。在一些实施方案中,r1选自:氯、溴和氟。在一些实施方案中,r1为溴。在一些实施方案中,r1为环丙基。
[0211]
在一些实施方案中,r2选自:c
3-c4环烷基、c
1-c5烷基和卤素。在一些实施方案中,r2选自:c
1-c2烷基、c
3-c4环烷基和溴。
[0212]
在一些实施方案中,r3选自:h和c
1-c3烷基,其中c
1-c3烷基可任选地被一或多个独立出现的氟取代。
[0213]
在一些实施方案中,r4为d。
[0214]
在一些实施方案中,r4选自:
[0215][0216]
在一些实施方案中,r4选自:
[0217][0218]
在一些实施方案中,各r6和r9独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代。
[0219]
在一些实施方案中,r7为h。
[0220]
在一些实施方案中,r
l
选自:c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代。
[0221]
在一些实施方案中,r
l
为环丁基。在一些实施方案中,r
l
为nr
11r12
。
[0222]
在一些实施方案中,r
l
为其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r
13
选自:h和c
1-c3烷基;且r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;其限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0223]
在一些实施方案中,m为0。在一些实施方案中,m为1。在一些实施方案中,m为2。在一些实施方案中,m为3。
[0224]
在一些实施方案中,-n(r3)-c(o)-r
l
选自:
[0225][0226]
在一些实施方案中,-n(r3)-c(o)-r
l
选自:
[0227][0228]
在一些实施方案中,n为3。
[0229]
在一些实施方案中,化合物由选自下组的结构式表示:
[0230][0231]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0232]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0233]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c1-c6烷基和c
3-c6环烷基;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。在一些实施方案中,化合物由如上文所定义的式ie.1表示。在一些实施方案中,化合物表示选自如上文所定义的式ie.2和式ie.3的结构式。
[0234]
在一些实施方案中,化合物由选自下组的结构式表示:
[0235][0236]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0237]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0238]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0239]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。在一些实施方案中,化合物由如上文所定义的式ie.4表示。在一些实施方案中,化合物表示选自如上文所定义的式ie.5和式ie.6的结构式。
[0240]
在一些实施方案中,化合物由选自下组的结构式表示:
[0241][0242]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0243]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0244]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0245]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。在一些实施方案中,化合物由如上文所定义的式ie.7表示。在一些实施方案中,化合物表示选自如上文所定义的式ie.8和式ie.9的结构式。
[0246]
在一些实施方案中,化合物由式if表示:
[0247][0248]
或其药学上可接受的盐,其中:环dd选自:
[0249][0250]
n为2、3或4;r1选自:卤素、氰基、c
1-c5烷基和c
3-c5环烷基,其中c
1-c5烷基和c
3-c5环
选自:c
1-c2烷基、c
3-c4环烷基和溴。
[0257]
在一些实施方案中,r3选自:h和c
1-c3烷基,其中c
1-c3烷基可任选地被一或多个独立出现的氟取代。
[0258]
在一些实施方案中,r4为d。
[0259]
在一些实施方案中,r4选自:
[0260][0261]
在一些实施方案中,r4选自:
[0262][0263]
在一些实施方案中,各r6和r9独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代。
[0264]
在一些实施方案中,r7为h。
[0265]
在一些实施方案中,r
l
选自:c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代。
[0266]
在一些实施方案中,r
l
为环丁基。在一些实施方案中,r
l
为nr
11r12
。在一些实施方案中,r
l
为其中各c
1-c6烷基和c
3-c6环烷基可任选地被1、2或3个独立出现的氟取代;u为n或cr
13
;v选自:氧、c(r
34
)2和nr6;r为0、1或2;q为1、2或3;r
13
选自:h和c
1-c3烷基;且r
34
在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基,其中c
1-c3烷基和c
3-c5环烷基可任选地被一或多个独立出现的氟取代,或两个r
34
与其所附接的碳连接在一起以形成c
3-c6环烷基;其限制条件为当r为0且q为1时,则u不为cr
13
且v不为o,且当r或q为1时,则u不为n且v不为o或nr6。
[0267]
在一些实施方案中,m为0。在一些实施方案中,m为1。在一些实施方案中,m为2。在一些实施方案中,m为3。
[0268]
在一些实施方案中,-n(r3)-c(o)-r
l
选自:
[0269][0270]
在一些实施方案中,-n(r3)-c(o)-r
l
选自:
[0271][0272]
在一些实施方案中,n为3。
[0273]
在一些实施方案中,化合物由选自下组的结构式表示:
[0274][0275]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0276]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0277]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c1-c6烷基和c
3-c6环烷基;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r7在每次出现时独立地选自:h、c
1-c6烷基、c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。在一些实施方案中,化合物由如上文所定义的式if.1表示。在一些实施方案中,化合物表示选自如上文所定义的式if.2和式if.3的结构式。
[0278]
在一些实施方案中,化合物由选自下组的结构式表示:
[0279][0280]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0281]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0282]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0283]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自:h、c
1-c3烷基、c
3-c5环烷基;且n为3。在一些实施方案中,化合物由如上文所定义的式if.4表示。在一些实施方案中,化合物表示选自如上文所定义的式if.5和式if.6的结构式。
[0284]
在一些实施方案中,化合物由选自下组的结构式表示:
[0285][0286]
其中r1在每次出现时独立地选自:cf3、cf2h、溴、氯或环丙基;r2在每次出现时独立地选自:c
1-c2烷基、c
3-c4环烷基和卤素;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基,其中c
1-c6烷基和c
3-c6环烷基可任选地被一或多个独立出现的氟取代;r9在每次出现时独立地选自:h、c
1-c3烷基和c
3-c5环烷基;r
34
在每次出现时独立地选自h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0287]
在一些实施方案中,r1在每次出现时为溴;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0288]
在一些实施方案中,r1在每次出现时为cf3;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自h、c
1-c3烷基、c
3-c5环烷基;且n为3。
[0289]
在一些实施方案中,r1在每次出现时为cf2h;r2在每次出现时独立地选自:c
1-c2烷基和c
3-c4环烷基;r3在每次出现时独立地选自:h和c
1-c2烷基;r6在每次出现时独立地选自:h、c
1-c6烷基和c
3-c6环烷基;r9在每次出现时选自:h和c
1-c3烷基;r
34
在每次出现时独立地选自h、c
1-c3烷基、c
3-c5环烷基;且n为3。在一些实施方案中,化合物由如上文所定义的式if.7表示。在一些实施方案中,化合物表示选自如上文所定义的式if.8和式if.9的结构式。
[0290]
本文也描述选自下组的化合物:
[0291]
n-(3-((5-环丙基-2-((3-甲基-1-(哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-环丙基-2-((2-甲氧基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-环丙基-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-甲基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)特戊酰胺、n-(3-((5-溴-2-((2-异丙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-环丙基-2-((2-异丙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-环丙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((1-(1-氨基-2-甲基-1-桥氧基丙-2-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-甲氧基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((1-(2-氰基丙-2-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((4-甲基-6-(4-甲基
哌嗪-1-基)吡啶-3-基)氨基)-5-(三氟甲基)吡啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-氯-2-((2-异丙氧基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-氯-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((5-氯-2-((2-甲基-4-(哌啶-4-基)苯基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-甲基-n-(3-((2-((2-甲基-4-(哌啶-4-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-氯-2-((2-甲基-4-(1-甲基哌啶-4-基)苯基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-甲基-n-(3-((2-((2-甲基-4-(1-甲基哌啶-4-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((1-(1-环丙基哌啶-4-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((2-((3-甲基-1-(哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((1-(1-异丙基哌啶-4-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((1-(1-异丁基哌啶-4-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-溴-2-((3-甲基-1-(1-d3-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((3-甲基-1-(1-d3-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-甲基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((4-甲基-6-(4-甲基哌嗪-1-基)吡啶-3-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((4-甲基-6-n-吗啉基吡啶-3-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-异丙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-环丙基-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-溴-2-((2-环丙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-乙基-4-((1r,5s)-8-甲基-3,8-二氮杂二环[3.2.1]辛烷-3-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-乙基-4-(5-甲基-2,5-二氮杂二环[2.2.1]庚烷-2-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((4-(1,4-二氮杂二环[3.2.1]辛烷-4-基)-2-乙基苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-乙基-4-(六氢吡咯并[1,2-a]吡嗪-2(1h)-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-(二氟甲基)-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-3,3-二氟环丁烷-1-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)异丁酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)特戊酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丙烷甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨
基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)四氢呋喃-3-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)四氢-2h-吡喃-4-甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)四氢呋喃-3-甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)四氢-2h-吡喃-4-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((2-((2-乙基-4-((1r,5s)-8-甲基-3,8-二氮杂二环[3.2.1]辛烷-3-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((2-((2-乙基-4-(5-甲基-2,5-二氮杂二环[2.2.1]庚烷-2-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((2-((4-(1,4-二氮杂二环[3.2.1]辛烷-4-基)-2-乙基苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((2-((2-乙基-4-(六氢吡咯并[1,2-a]吡嗪-2(1h)-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((5-(二氟甲基)-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-3,3-二氟-n-甲基环丁烷-1-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基异丁酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基特戊酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基氧杂环丁烷-3-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基四氢呋喃-3-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基四氢-2h-吡喃-4-甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基氧杂环丁烷-3-甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基四氢呋喃-3-甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基四氢-2h-吡喃-4-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((2-((2-乙基-4-((1r,5s)-8-甲基-3,8-二氮杂二环[3.2.1]辛烷-3-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((2-((2-乙基-4-(5-甲基-2,5-二氮杂二环[2.2.1]庚烷-2-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((2-((4-(1,4-二氮杂二环[3.2.1]辛烷-4-基)-2-乙基苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((2-((2-乙基-4-(六氢吡咯并[1,2-a]吡嗪-2(1h)-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨
((2-乙基-4-((1r,5s)-8-甲基-3,8-二氮杂二环[3.2.1]辛烷-3-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-1,3,3-三甲基脲、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-1-甲酰胺、n-(3-((5-溴-2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)嘧啶-4-基)氨基)丙基)吡咯烷-1-甲酰胺、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-3,3-二甲基氮杂环丁烷-1-甲酰胺、3-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-1,1-二甲基脲、n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-2,2-二甲基氮杂环丁烷-1-甲酰胺、3-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)吡啶-4-基)氨基)丙基)-1,1-二甲基脲、1-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)吡啶-4-基)氨基)丙基)-1,3,3-三甲基脲、n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((1-(2-(二甲基氨基)乙基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((3-甲基-1-(1-甲基吡咯烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-溴-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-氯-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)四氢呋喃-3-甲酰胺、n-甲基-n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-溴-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((5-氯-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)四氢-2h-吡喃-4-甲酰胺、n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((2-((1-(2-(二甲基氨基)乙基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((2-((3-甲基-1-(1-甲基吡咯烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-甲基-n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((2-((1-(2-(二甲基氨基)乙基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n-甲基氧杂环丁烷-3-甲酰胺、n-甲基-n-(3-((2-((3-甲基-1-(1-甲基吡咯烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((5-溴-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、1-甲基-n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-3-甲酰胺、n-(3-((2-((1-(2-(二甲基氨基)乙基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、1-甲基-n-(3-((2-((3-甲基-1-(1-甲基吡咯烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-3-甲酰
胺、n,1-二甲基-n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-3-甲酰胺、n-(3-((2-((1-(2-(二甲基氨基)乙基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)-n,1-二甲基氮杂环丁烷-3-甲酰胺、n,1-二甲基-n-(3-((2-((3-甲基-1-(1-甲基吡咯烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-3-甲酰胺、n-(3-((5-溴-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((5-(二氟甲基)-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-(二氟甲基)-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-n-甲基环丁烷甲酰胺、n-(3-((5-(二氟甲基)-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((5-(二氟甲基)-2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-甲基-n-(3-((2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-甲基-n-(3-((2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、1-甲基-n-(3-((2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-3-甲酰胺、n,1-二甲基-n-(3-((2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-3-甲酰胺、n-(3-((5-(二氟甲基)-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-(二氟甲基)-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((5-(二氟甲基)-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((5-溴-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-溴-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((5-溴-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((5-氯-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺、n-(3-((5-氯-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)氧杂环丁烷-3-甲酰胺、n-(3-((5-氯-2-((3-甲基-1-(8-甲基-8-氮杂双环[3.2.1]辛烷-3-基)-1h-吡唑-4-基)氨基)嘧啶-4-基)氨基)丙基)-1-甲基氮杂环丁烷-3-甲酰胺、n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)异丁酰胺、n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)
基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-1-甲酰胺、1,1-二甲基-3-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)脲、n-甲基-n-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)氮杂环丁烷-1-甲酰胺、1,1,3-三甲基-3-(3-((2-((3-甲基-1-(1-甲基哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)脲,及其药学上可接受的盐、对映异构体、立体异构体和互变异构体。
[0292]
治疗方法
[0293]
本文所描述的化合物可充当可用于治疗有需要的患者的病症的自噬抑制剂。例如,病症可为例如实体肿瘤的肿瘤。病症也可为癌症。
[0294]
示例性病症也包括胃肠道基质瘤、食道癌、胃癌、黑色素瘤、神经胶质瘤、神经胶母细胞瘤、卵巢癌、膀胱癌、胰脏癌、前列腺癌、肺癌、乳腺癌、肾癌、肝癌、骨肉瘤、多发性骨髓瘤、子宫颈癌、骨转移癌、乳头状甲状腺癌、非小细胞肺癌和结直肠癌。通过本文所描述的方法治疗的癌症可为转移性癌症。
[0295]
在一些实施方案中,本文所描述的化合物可用于治疗由ras突变引起的癌症。在一些实施方案中,癌症是由kras突变引起。在一些实施方案中,癌症具有肿瘤抑制蛋白中的额外突变,包括tp53、pten、cdn2a/ink4a、p16或stag2中的突变。在一些实施方案中,这些额外突变发生于tp53、pten、cdn2a/ink4a、p16或stag2中的一或多者中。在一些实施方案中,癌症为胰管腺癌。在一些实施方案中,癌症为肺癌。在一些实施方案中,癌症为结直肠癌。
[0296]
在一些实施方案中,通过本文所描述的化合物进行的细胞自噬抑制的测定,是通过监测自噬流(autophagic flux),例如通过监测自噬介导的mcherry/gfp-lc3融合蛋白清除的抑制来测定。在一些实施方案中,通过本文所描述的化合物进行的细胞自噬抑制的测定,是通过监测诸如p62或lc-3的自噬蛋白的积聚来测定。在一些实施方案中,通过本文所描述的化合物进行的细胞自噬抑制的测定,是通过荧光素酶标记的lc3蛋白的减少的清除来测定。在一些实施方案中,通过本文所描述的化合物进行的细胞自噬抑制的测定,是通过监测细胞自噬小体的减少,例如通过测量具有自噬小体标志物cyto-id的荧光斑点来测定。
[0297]
在一些实施方案中,通过本文所描述的化合物进行的ulk激酶细胞抑制,是通过肿瘤细胞或非肿瘤宿主组织中包括atg13、atg14、beclin 1或sting的细胞ulk基质的磷酸化抑制来测定。在一些实施方案中,通过本文所描述的化合物进行的ulk激酶细胞抑制,是在包括免疫细胞的宿主组织中测定。
[0298]
在一些实施方案中,通过本文所描述的化合物进行的自噬活体内抑制,是通过肿瘤细胞或非肿瘤宿主组织中包括atg13、atg14、beclin 1或sting的细胞ulk基质的磷酸化抑制来测定。在一些实施方案中,通过本文所描述的化合物进行的ulk激酶活体内抑制,是,在包括免疫细胞的宿主组织中测定。在一些实施方案中,通过本文所描述的化合物进行的自噬流活体内抑制,可用作监测这种ulk抑制的动力学和程度的药力学模型。在一些实施方案中,通过本文所描述的化合物进行的ulk激酶的活体内抑制,是在携有胰脏癌的动物中测定。在一些实施方案中,通过本文所描述的化合物进行的ulk激酶活体内抑制,是在携有肺癌的动物中测定。在一些实施方案中,ulk激酶活体内抑制,是在携有结直肠癌的动物中测定。在一些实施方案中,通过本文所描述的化合物进行的自噬活体内抑制,是通过利用监测自噬小体形成的抑制进行的肿瘤细胞或非肿瘤宿主组织中的自噬流抑制或通过诸如p62或
lc-iii的自噬蛋白的积聚来测定。在一些实施方案中,自噬活体内抑制,是在包括免疫细胞的宿主组织中测定。在一些实施方案中,自噬流活体内抑制,可用作监测这种ulk抑制的动力学和程度的药力学模型。
[0299]
在一些实施方案中,通过本文所描述的化合物进行的自噬和抗肿瘤活性抑制,是在异种移植研究中利用例如scid或裸小鼠的免疫功能不全小鼠中的人类ras突变细胞系加以评估。在一些实施方案中,通过本文所描述的化合物进行的自噬抑制和抗肿瘤活性,是在异种移植研究中利用例如scid或裸小鼠的免疫功能不全小鼠中的人类ras突变患者来源的肿瘤异种移植物(pdx)加以评估。在一些实施方案中,异种移植研究包括胰脏癌模型中本文所描述的化合物的评估。在一些实施方案中,通过本文所描述的化合物进行的自噬抑制和抗肿瘤活性,是在突变ras癌症的同基因型鼠类经基因工程改造的模型(gem)中加以评估。在一些实施方案中,通过本文所描述的化合物进行的自噬抑制和抗肿瘤活性,是在称为以下名称的鼠类gem同基因型原位胰脏癌模型中加以评估:kpc模型(lsl-kras
g12d/
、lsl-trp53
r172h/
、pdx-1-cre)或kpc模型变化形式。
[0300]
在一些实施方案中,本文所描述的化合物将在异种移植或gem癌症模型中与mek抑制剂组合加以评估。在一些实施方案中,本文所描述的化合物将在异种移植或gem癌症模型中与raf抑制剂组合加以评估。在一些实施方案中,本文所描述的化合物将在异种移植或gem癌症模型中与erk抑制剂组合加以评估。在一些实施方案中,本文所描述的化合物将在异种移植或gem癌症模型中与ras g12c直接抑制剂组合加以评估。
[0301]
在一些实施方案中,通过本文所描述的化合物进行的自噬抑制和抗肿瘤活性,是在用于评估针对ulk抑制剂作用机制的免疫调节组分的免疫活性鼠类癌症模型中加以评估。在一些实施方案中,免疫活性鼠类模型为称为以下的鼠类gem同基因型原位胰脏癌模型:kpc模型(lsl-kras
g12d/
、lsl-trp53
r172h/
、pdx-1-cre)或kpc模型变化形式。在一些实施方案中,本文所描述的化合物的免疫调节特性是结合mek抑制剂加以评估。在一些实施方案中,本文所描述的化合物的免疫调节特性是结合raf抑制剂加以评估。在一些实施方案中,本文所描述的化合物的免疫调节特性是结合erk抑制剂加以评估。在一些实施方案中,本文所描述的化合物的免疫调节特性是结合ras g12c直接抑制剂加以评估。
[0302]
在一些实施方案中,ulk抑制的免疫调节组分为增强型先天性免疫反应。在一些实施方案中,ulk抑制的免疫调节组分为增强型后天性免疫反应。在一些实施方案中,ulk抑制的免疫调节组分为抗原呈递细胞的增强的活性。在一些实施方案中,ulk抑制的免疫调节组分为包括巨噬细胞的骨髓细胞的增强的抗肿瘤活性。在一些实施方案中,ulk抑制的免疫调节组分为自然杀伤细胞的增强的抗肿瘤活性。在一些实施方案中,ulk抑制的免疫调节组分为包括细胞毒性t细胞的效应t细胞的增强的活性。
[0303]
在一个实施方案中,本文提供一种治疗本文所描述的病症的方法,其包括:向需要的患者施用治疗有效量的本文所描述的化合物,且在施用过程期间或之后(例如,在离散时间点,如在预期化合物初始施用之后一周、两周或每月)检测该化合物与ulk激酶的作用,其中检测包含使从该患者获得的样品(包括但不限于:肿瘤、血液、唾液或组织)与磷酸化atg13抗体elisa分析接触以例如基于样品中磷酸化atg13的含量来检测ulk激酶活性的抑制。在一些实施方案中,预期方法包括任选地在施用化合物之前使从患者获得的样品(包括但不限于:肿瘤、血液、唾液或组织)与磷酸化atg13抗体elisa分析接触,且比较在施用前获
得的样品中的磷酸化atg13含量与在施用过程期间或之后获得的样品中的磷酸化atg13含量。在一些实施方案中,磷酸化atg13为p-s318atg13。
[0304]
在一个实施方案中,本文提供一种治疗本文所描述的病症的方法,其包括:向有需要的患者施用治疗有效量的本文所描述的化合物,且在施用过程期间或之后(例如,在离散时间点,如在预期化合物初始施用之后一周、两周或每月)检测该化合物与ulk激酶的作用,其中检测包含使从该患者获得的样品(包括但不限于:肿瘤、血液、唾液或组织)与磷酸化atg14抗体elisa分析接触以例如基于样品中磷酸atg14的含量来检测ulk激酶活性的抑制。在一些实施方案中,预期方法包括任选地在施用化合物之前使从患者获得的样品(包括但不限于:肿瘤、血液、唾液或组织)与磷酸化atg14抗体elisa分析接触,且比较在施用前获得的样品中的磷酸化atg14含量与在施用过程期间或之后获得的样品中的磷酸化atg14含量。在一些实施方案中,磷酸化atg14为p-atg14 ser29。
[0305]
在一个实施方案中,本文提供一种治疗本文所描述的病症的方法,其包括:向有需要的患者施用治疗有效量的本文所描述的化合物,且在施用过程期间或之后(例如,在离散时间点,如在预期化合物初始施用之后一周、两周或每月)检测该化合物与ulk激酶的作用,其中检测包含使从该患者获得的样品(包括但不限于:肿瘤、血液、唾液或组织)与p62抗体elisa分析接触以例如基于样品中p62的含量来检测ulk激酶活性的抑制。在一些实施方案中,预期方法包括任选地在施用化合物之前使从患者获得的样品(包括但不限于:肿瘤、血液、唾液或组织)与p62抗体elisa分析接触,且比较在施用前获得的样品中的p62含量与在施用过程期间或之后获得的样品中的p62含量。
[0306]
在一个实施方案中,本文提供一种治疗本文所描述的病症的方法,其包括:向有需要的患者施用治疗有效量的本文所描述的化合物,且在施用过程期间或之后(例如,在离散时间点,如在预期化合物初始施用之后一周、两周或每月)检测该化合物与ulk激酶的作用,其中检测包含使从该患者获得的样品(包括但不限于:肿瘤、血液、唾液或组织)与pbeclin抗体elisa分析接触以例如基于样品中pbeclin的含量来检测ulk激酶活性的抑制。在一些实施方案中,预期方法包括任选地在施用化合物之前使从患者获得的样品(包括但不限于:肿瘤、血液、唾液或组织)与pbeclin抗体elisa分析接触,且比较在施用前获得的样品中的pbeclin含量与在施用过程期间或之后获得的样品中的pbeclin含量。
[0307]
本文所提供的化合物可以提供最优选药物功效的剂量施用于需要这种治疗的患者(动物和人类)。应了解,任何特定应用中需要使用的剂量将随患者不同而变化,不仅随所选择的特定化合物或组合物而变,而且随施用通路、所治疗病况的性质、患者的年龄和病况、同时服用的药物或患者随后所遵循的特殊饮食和本领域技术人员将意识到的其他因素而变,适当的剂量最终由主治医师酌情处理。对于治疗上文所提和的临床病况和疾病,本文所提供的化合物可以含有常规无毒药学上可接受的载体、佐剂和媒剂的剂量单位制剂的形式经口、皮下、局部、非经肠、通过吸入喷雾或经直肠施用。非经肠施用可包括皮下注射、静脉内或肌内注射或输注技术。
[0308]
治疗可按需要持续尽可能长或尽可能短时间段。组合物可依例如每天一至四次或更多次的方案来施用。合适治疗期可为例如至少约一周、至少约两周、至少约一个月、至少约六个月、至少约1年或无限期时间。治疗期可在实现所需结果时终止。
[0309]
组合疗法
[0310]
本文所述的化合物(例如,如本文所定义的式i化合物),可与一种或多种额外治疗剂组合施用以治疗诸如癌症的本文所描述的病症。例如,本发明提供包含本文所述的化合物(例如,如本文所定义的式i化合物)、一种或多种额外治疗剂和药学上可接受的赋形剂的药物组合物。在一些实施方案中,施用如本文所定义的式i化合物和一种额外治疗剂。在一些实施方案中,施用如本文所定义的式i化合物和两种额外治疗剂。在一些实施方案中,施用如本文所定义的式i化合物和三种额外治疗剂。组合疗法可通过施用两种或更多种治疗剂来实现,该两种或更多种治疗剂各自分开配制和施用。例如,如本文所定义的式i化合物和额外治疗剂可分开配制且施用。组合疗法也可通过施用于单一制剂中的两种或更多种治疗剂来实现,该单一制剂例如包含作为一种治疗剂的式i化合物和诸如mapkap通路抑制剂或化学治疗剂的一种或多种额外治疗剂的药物组合物。例如,如本文所定义的式i化合物和额外治疗剂可在单一制剂中施用。组合疗法也涵盖其他组合。尽管组合疗法中的两种或更多种药剂可同时施用,但其无需如此。例如,第一药剂(或药剂的组合)的施用可比第二药剂(或药剂的组合)的施用提前数分钟、数小时、数天或数周。因此,两种或更多种药剂的施用可以彼此在数分钟内,或彼此在1、2、3、6、9、12、15、18或24小时内,或彼此在1、2、3、4、5、6、7、8、9、10、12、14天内,或彼此在2、3、4、5、6、7、8、9周或数周内。在一些情况下,甚至更长时间间隔也是有可能的。尽管在多数情况下期望用于组合疗法中的两种或更多种药剂同时存在于患者体内,但其无需如此。
[0311]
组合疗法也可包括使用组分药剂的不同定序的组合中进行药剂中一种或多种的两次或更多次施用。例如,若药剂x和药剂y组合使用,则可能将其以任何组合形式依序施用一或多次,例如按x-y-x、x-x-y、y-x-y、y-y-x、x-x-y-y等的次序施用。
[0312]
在一些实施方案中,可与本文所提供的化合物组合施用的一种或多种额外治疗剂可为mapkap通路抑制剂。这种mapkap通路抑制剂包括例如mek抑制剂、erk抑制剂、raf抑制剂和ras抑制剂。
[0313]
示例性mek抑制剂包括但不限于:曲美替尼、司美替尼、考比替尼、比美替尼及其药学上可接受的盐。示例性erk抑制剂包括但不限于:优立替尼、sch772984、ly3214996、拉沃替尼(ravoxertinib)、vx-11e及其药学上可接受的盐。示例性raf抑制剂包括但不限于:ly3009120、lxh254、raf709、达拉非尼、维罗非尼及其药学上可接受的盐。示例性ras抑制剂包括但不限于:amg-510、mrtx849及其药学上可接受的盐。
[0314]
本文所描述的化合物可与已知用于治疗癌症的其他治疗剂组合施用。这种其他治疗剂包括放射线疗法、抗微管蛋白剂、dna烷基化剂、dna合成抑制剂、dna嵌入剂、抗雌激素剂、抗雄激素药、类固醇、抗-egfr剂、激酶抑制剂、mtor抑制剂、pi3激酶抑制剂、周期蛋白依赖型激酶抑制剂、cd4/cd6激酶抑制剂、拓朴异构酶抑制剂、组蛋白去乙酰酶(hdac)抑制剂、dna甲基化抑制剂、抗-her2剂、抗血管生成剂、蛋白酶体抑制剂、沙立度胺(thalidomide)、来那度胺(lenalidomide)、抗体-药物缀合物(adc)、包括免疫调节剂的免疫治疗剂、靶向治疗剂癌症疫苗和car-t细胞疗法。
[0315]
在一些实施方案中,额外治疗剂可为包括但不限于以下的化学治疗剂:抗微管蛋白剂(例如紫杉醇、包括nab-紫杉醇的用于可注射悬浮液的紫杉醇蛋白结合型颗粒、艾瑞布林(eribulin)、多烯紫杉醇、伊沙匹隆(ixabepilone)、长春新碱、奥瑞他汀(auristatins)或类美登素)、长春瑞滨(vinorelbine)、dna烷基化剂(包括顺铂、卡铂、奥沙利铂
(oxaliplatin)、环磷酰胺、异环磷酰胺、替莫唑胺(temozolomide))、dna嵌入剂或dna拓朴异构酶抑制剂(包括蒽环霉素(anthracycline),如阿霉素、聚乙二醇化脂质体阿霉素、道诺霉素(daunorubicin)、伊达比星(idarubicin)、米托蒽醌(mitoxantrone)或表柔比星(epirubicin);喜树碱,如拓朴替康(topotecan)、伊立替康(irinotecan)或依昔替康(exatecan))、5-氟尿嘧啶、卡培他滨(capecitabine)、阿糖胞苷、地西他滨(decitabine)、5-氮杂胞嘧啶核苷、吉西他滨(gemcitabine)和甲胺喋呤。
[0316]
在一些其他实施方案中,额外治疗剂可为包括但不限于以下的激酶抑制剂:埃罗替尼(erlotinib)、吉非替尼(gefitinib)、来那替尼(neratinib)、阿法替尼(afatinib)、奥希替尼(osimertinib)、拉帕替尼(lapatanib)、克唑替尼(crizotinib)、布加替尼(brigatinib)、色瑞替尼(ceritinib)、艾乐替尼(alectinib)、劳拉替尼(lorlatinib)、依维莫司(everolimus)、替西罗莫司(temsirolimus)、阿贝马昔布(abemaciclib)、lee011、帕博昔布(palbociclib)、卡博替尼(cabozantinib)、舒尼替尼(sunitinib)、帕唑帕尼(pazopanib)、索拉非尼(sorafenib)、瑞戈非尼(regorafenib)、舒尼替尼、阿西替尼(axitinib)、达沙替尼(dasatinib)、伊马替尼(imatinib)、尼罗替尼(nilotinib)、艾代拉里斯(idelalisib)、依鲁替尼(ibrutinib)、blu-667、loxo 292、拉罗替尼(larotrectinib)和喹杂替尼(quizartinib);包括但不限于以下的抗雌激素剂:他莫昔芬(tamoxifen)、氟维司群(fulvestrant)、阿那曲唑(anastrozole)、来曲唑(letrozole)和依西美坦(exemestane);包括但不限于以下的抗雄激素剂:乙酸阿比特龙(abiraterone acetate)、恩杂鲁胺(enzalutamide)、尼鲁胺(nilutamide)、比卡鲁胺(bicalutamide)、氟他胺(flutamide)、乙酸环丙孕酮(cyproterone acetate);包括但不限于以下的类固醇药剂:泼尼松(prednisone)和地塞米松(dexamethasone);包括但不限于以下的parp抑制剂:讷拉帕尼(neraparib)、奥拉帕尼(olaparib)、拉唑帕尼(talazoparib)和芦卡帕尼(rucaparib);包括但不限于以下的拓朴异构酶i抑制剂:伊立替康、喜树碱、依昔替康和拓朴替康;包括但不限于以下的拓朴异构酶ii抑制剂:蒽环霉素、依托泊苷(etoposide)、磷酸依托泊苷和米托蒽醌;包括但不限于以下的组蛋白去乙酰酶(hdac)抑制剂:伏立诺他(vorinostat)、罗米地辛(romidepsin)、帕比诺他(panobinostat)、丙戊酸和贝林诺他(belinostat);包括但不限于以下的dna甲基化抑制剂:dznep和5-氮杂-2'-脱氧胞苷;包括但不限于以下的蛋白酶体抑制剂:硼替佐米(bortezomib)和卡非佐米(carfilzomib);沙立度胺;来那度胺;泊利度胺(pomalidomide);包括但不限于以下的生物试剂:曲妥珠单抗(trastuzumab)、阿多曲妥珠单抗(ado-trastuzumab)、帕妥珠单抗(pertuzumab)、西妥昔单抗(cetuximab)、帕尼单抗(panitumumab)、伊匹单抗(ipilimumab)、替西木单抗(tremelimumab);包括以下的抗pd-1药剂:派姆单抗(pembrolizumab)、纳武单抗(nivolumab)、皮立珠单抗(pidilizumab)和赛咪单抗(cemiplimab);包括以下的抗pd-l1药剂:阿特珠单抗(atezolizumab)、阿维鲁单抗(avelumab)、德瓦鲁单抗(durvalumab)和bms-936559;包括以下的抗血管生成剂:贝伐单抗(bevacizumab)和阿柏西普(aflibercept);以及包括以下的抗体-药物缀合物(adc):dm1、dm4、mmae、mmaf或喜树碱有效负载物;本妥昔单抗维多汀(brentuximab vedotin)和曲妥珠单抗-美坦新(trastuzumab emtansine);放射线疗法;包括但不限于:西普鲁塞-t(sipuleucel-t)的治疗性疫苗。
[0317]
在一些实施方案中,额外治疗剂可为包括但不限于以下的免疫调节剂:抗-pd-1或
抗-pdl-1治疗剂,其包括派姆单抗、纳武单抗、阿特珠单抗、德瓦鲁单抗、bms-936559或阿维鲁单抗;抗-tim3(抗-havcr2)治疗剂,其包括但不限于:tsr-022或mbg453;抗-lag3治疗剂,其包括但不限于:瑞拉单抗(relatlimab)、lag525或tsr-033;抗-4-1bb(抗-cd37、抗-tnfrsf9)药;cd40激动剂治疗剂,其包括但不限于:sgn-40、cp-870、cp-893或ro7009789;抗-cd47治疗剂,其包括但不限于:hu5f9-g4;抗-cd20治疗剂;抗-cd38治疗剂;sting激动剂,其包括但不限于:adu-s100、mk-1454、asa404或酰胺基苯并咪唑;蒽环霉素,其包括但不限于:阿霉素或米托蒽醌;低甲基化剂,其包括但不限于:氮杂胞嘧啶核苷或地西他滨;其他免疫调节治疗剂,其包括但不限于:表皮生长因子抑制剂、他汀类(statin)、二甲双胍、血管收缩素受体阻断剂、沙立度胺、来那度胺、泊利度胺、泼尼松或地塞米松。
[0318]
在一些实施方案中,额外治疗剂选自包括戈舍瑞林(goserelin)和亮丙立德(leuprolide)的促黄体素释放激素(lhrh)类似物。在一些实施方案中,额外治疗剂选自:依维莫司、曲贝替定、阿布拉生、tlk 286、av-299、dn-101、帕佐泮尼(pazopanib)、gsk690693、rta 744、on 0910.na、azd 6244(arry-142886)、amn-107、tki-258、gsk461364、azd 1152、恩扎妥林(enzastaurin)、凡德他尼(vandetanib)、arq-197、mk-0457、mln8054、pha-739358、r-763、at-9263、培美曲塞、埃罗替尼、达沙替尼、尼罗替尼、德卡替尼、帕尼单抗、氨柔比星、奥戈伏单抗、lep-etu、诺拉曲特(诺拉曲特)、azd2171、巴他布尔(batabulin)、阿图姆巴布(atumtunab)、扎木单抗、艾特咔林、汉防己碱、卢比替康(rubitecan)、替米利芬(tesmilifene)、奥利默森(oblimersen)、替西单抗、伊匹单抗、棉籽醇、bio 111、131-i-tm-601、alt-110、bio 140、cc 8490、西仑吉肽、吉马替康(gimatecan)、il13-pe38qqr、ino 1001、ipdr1krx-0402、胺甲硫蒽酮、ly 317615、纽拉迪布(neuradiab)、维特斯潘(vitespan)、rta 744、sdx 102、他仑帕奈(talampanel)、阿曲生坦(atrasentan)、xr 311、罗米地辛(romidepsin)、ads-100380、舒尼替尼(sunitinib)、5-氟尿嘧啶、伏立诺他(vorinostat)、依托泊苷、吉西他滨、阿霉素、伊立替康、脂质阿霉素、5'-脱氧-5-氟尿苷、长春新碱、替莫唑胺、zk-304709、塞利希布(seliciclib);pd0325901、azd-6244、卡培他滨、l-谷氨酸、n-[4-[2-(2-氨基-4,7-二氢-4-桥氧基-1h-吡咯并[2,3-d]嘧啶-5-基)-乙基]苯甲酰基]-、二钠盐、七水合物、喜树碱、peg-标记的伊立替康、他莫昔芬(tamoxifen)、托瑞米芬柠檬酸盐、阿那曲唑、依西美坦、来曲唑、des(己烯雌酚)、雌二醇、雌激素、缀合的雌激素、贝伐单抗、imc-1c11、chir-258;3-[5-(甲磺酰哌啶甲基)-吲哚基]-喹啉酮、凡塔蓝尼(vatalanib)、ag-013736、ave-0005、[d-ser(bu t)6,azgly 10](pyro-glu-his-trp-ser-tyr-d-ser(bu t)-leu-arg-pro-azgly-nh2乙酸酯[c
59h84n18o4-(c2h4o2)
x
,其中x=1-2.4]的乙酸盐、乙酸戈舍瑞、乙酸亮丙立德、曲普瑞林双羟萘酸盐、乙酸甲羟孕酮、己酸羟基孕酮、乙酸甲地孕酮、雷诺昔酚、比卡鲁胺、氟烷酰胺、尼鲁胺、乙酸甲地孕酮、cp-724714;tak-165、hki-272、埃罗替尼、拉帕替尼、卡奈替尼、abx-egf抗体、艾必妥(erbitux)、ekb-569、pki-166、gw-572016、爱纳法尼(ionafarnib)、bms-214662、替吡法尼(tipifarnib);阿米福汀(amifostine)、nvp-laq824、辛二酰阿纳里氧肟酸、丙戊酸、曲古霉素a、fk-228、su11248、索拉非尼(sorafenib)、krn951、氨鲁米特、安吖啶、阿那格雷(anagrelide)、l-天冬酰胺酶、卡介苗(bcg)疫苗、博莱霉素、布舍瑞林(buserelin)、白消安、卡铂、卡氯芥、苯丁酸氮芥、顺铂、克拉屈滨(cladribine)、氯膦酸盐、环丙孕酮、阿糖胞苷、达卡巴嗪(dacarbazine)、放线菌素d、道诺霉素、己烯雌酚、表柔比星、氟达拉滨、氟氢可的松、氟甲睾酮、氟他胺、吉西他
滨、格列卫(gleevac)、羟脲、伊达比星、异环磷酰胺、伊马替尼(imatinib)、亮丙瑞林、左旋咪唑、洛莫司汀、氮芥、美法仑、6-巯基嘌呤、美司钠、甲胺喋呤、丝裂霉素、米托坦(mitotane)、米托蒽醌、尼鲁胺、奥曲肽、奥沙利铂、帕米膦酸盐、喷司他汀(pentostatin)、普卡霉素、卟吩姆、丙卡巴肼、雷替曲塞、利妥昔单抗、链脲菌素、替尼泊苷、睾酮、沙立度胺、硫鸟嘌呤、噻替派、维甲酸、长春地辛、13-顺-网膜酸、苯丙氨酸氮芥、尿嘧啶氮芥、雌氮芥、六甲蜜胺、氟尿苷、5-脱氧尿苷、胞嘧啶阿拉伯糖苷、6-巯基嘌呤、脱氧助间型霉素、促钙三醇、伐柔比星、光神霉素、长春碱、长春瑞滨、拓朴替康、拉佐欣(razoxin)、马立马司他(marimastat)、col-3、鲨癌灵、bms-275291、角鲨胺、内皮生长抑素、su5416、su6668、emd121974、介白素-12、im862、血管生长抑素、维他欣(vitaxin)、曲洛昔芬、碘昔芬、螺内酯、非那雄安(finasteride)、西米替丁(cimitidine)、曲妥珠单抗、地尼白介素、吉非替尼、硼替佐米(bortezimib)、伊立替康、拓朴替康、阿霉素、多烯紫杉醇、长春瑞滨、贝伐单抗(单克隆抗体)和艾必妥(erbitux)、不含氢化蓖麻油的紫杉醇、埃博霉素b、bms-247550、bms-310705、曲洛昔芬、4-羟基他莫昔芬、哌喷昔芬、era-923、阿佐昔芬、氟维司群、阿考比芬、拉索昔芬、艾多昔芬、se-424、hmr-3339、zk186619、ptk787/zk 222584、vx-745、pd 184352、雷帕霉素、40-o-(2-羟基乙基)-雷帕霉素、坦罗莫司、ap-23573、rad001、abt-578、bc-210、ly294002、ly292223、ly292696、ly293684、ly293646、渥曼青霉素、zm336372、l-779,450、peg-非格司亭、达贝泊汀(darbepoetin)、红血球生成素、粒细胞集落刺激因子、卓骨祂、泼尼松、西妥昔单抗、粒细胞巨噬细胞集落刺激因子、组胺瑞林、聚乙二醇化干扰素α-2a、干扰素α-2a、聚乙二醇化干扰素α-2b、干扰素α-2b、阿扎胞苷、peg-l天冬酰胺酶、来那度胺、吉妥珠单抗、氢化可的松、介白素-11、右雷佐生、阿仑单抗、全反式维甲酸、酮康唑、介白素-2、甲地孕酮、免疫球蛋白、氮芥子气、甲基泼尼松龙、替伊莫单抗(ibritgumomab tiuxetan)、雄激素、地西他滨、六甲蜜胺、贝瑟罗汀(bexarotene)、托西莫单抗、三氧化二砷、可的松、依替膦酸盐(editronate)、米托坦(mitotane)、环孢素、脂质体道诺霉素、埃德温纳-天门冬酰胺酶(edwina-asparaginase)、锶89、卡索匹坦、奈妥吡坦、nk-1受体拮抗剂、帕洛诺司琼、阿匹坦、苯海拉明、羟嗪、甲氧氯普胺、劳拉西泮(lorazepam)、阿普唑仑、氟哌啶醇、氟哌利多、屈大麻酚、地塞米松、甲基泼尼松龙、丙氯拉嗪、格拉司琼(granisetron)、昂丹司琼(ondansetron)、多拉司琼(dolasetron)、特比司琼(tropisetron)、聚乙二醇化非格司亭(pegfilgrastim)、红血球生成素、阿法依泊汀和阿法达贝泊汀、易普单抗、维罗非尼(vemurafenib)及其混合物。
[0319]
药物组合物和试剂盒
[0320]
本发明的另一方面提供包含与药学上可接受的载体一起配制的如本文所公开的化合物的药物组合物。具体地,本发明提供包含与一种或多种药学上可接受的载体一起配制的如本文所公开的化合物的药物组合物。这些制剂包括适用于经口、经直肠、局部、颊内、非经肠(例如,皮下、肌内、皮内或静脉内)、经直肠、经阴道或气溶胶施用的制剂,但在任何给定情况下,最适合的施用形式将视所治疗病况的程度和严重性而定,且视所使用的特定化合物的性质而定。例如,所公开组合物可以单位剂量形式配制,和/或可经配制用于经口或皮下施用。
[0321]
示例性药物组合物可按药物制剂形式使用,例如以固体、半固体或液体形式,其含有一种或多种本文所描述的化合物作为活性成分,与适用于外部、经肠或非经肠施用的有
机或无机载体或赋形剂掺合。活性成分可与例如常用于片剂、丸剂、胶囊、栓剂、溶液、乳液、悬浮液和任何其他适合使用的形式的无毒、药学上可接受的载体混配。活性目标化合物以足以对疾病的过程或病况产生所需作用的量包括于药物组合物中。
[0322]
对于制备诸如片剂的固体组合物,可将主要活性成分与例如常规制片剂成分(如玉米淀粉、乳糖、蔗糖、山梨糖醇、滑石、硬脂酸、硬脂酸镁、磷酸二钙或胶质)的药物载体和例如水的其他药物稀释剂混合,以形成含有本文所提供的化合物或其无毒药学上可接受的盐的均质混合物的固体预配制组合物。当提和这些预配制组合物为均质时,是指活性成分均匀分散在整个组合物中,使得组合物可易于再分割成同等效力的单位剂型,诸如片剂、丸剂和胶囊。
[0323]
在用于经口施用的固体剂型(胶囊、片剂、丸剂、糖衣药丸、散剂、颗粒及其类似物)中,本发明组合物与一种或多种药学上可接受的载体(如柠檬酸钠或磷酸二钙)和/或以下任一种混合:(1)填充剂或增量剂,如淀粉、乳糖、蔗糖、葡萄糖、甘露糖醇和/或硅酸;(2)粘合剂,如羧甲基纤维素、海藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和/或阿拉伯胶;(3)保湿剂,如甘油;(4)崩解剂,如琼脂、碳酸钙、马铃薯或木薯淀粉、海藻酸、某些硅酸盐和碳酸钠;(5)溶液阻滞剂,如石蜡;(6)吸收促进剂,如季铵化合物;(7)湿润剂,如乙酰醇和单硬脂酸甘油酯;(8)吸附剂,如高岭土和膨润土;(9)润滑剂,如滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、月桂基硫酸钠及其混合物;以及(10)着色剂。在胶囊、片剂和丸剂的情况下,组合物也可包含缓冲剂。也可使用类似类型的固体组合物作为填充剂,用在使用诸如乳糖或牛乳糖类以及高分子量聚乙二醇及其类似物的赋形剂的软式和硬式填充明胶胶囊中。
[0324]
片剂可通过任选地与一种或多种助剂一起压缩或模制来制得。可使用粘合剂(例如明胶或羟丙基甲基纤维素)、润滑剂、惰性稀释剂、防腐剂、崩解剂(例如羟基乙酸淀粉钠或交联羧甲基纤维素钠)、界面活性剂或分散剂来制备压缩片剂。模制片剂可通过在合适机器中模制经惰性液体稀释剂湿润的本发明组合物的混合物来制得。片剂及其他固体剂型,诸如糖衣药丸、胶囊、丸剂和颗粒可任选地刻痕或制备有包衣和外壳,诸如药物配制技术中熟知的肠溶衣及其他包衣。
[0325]
用于吸入或吹入的组合物包括于药学上可接受的水性或有机溶剂或其混合物中的溶液和悬浮液以及散剂。用于经口施用的液体剂型包括药学上可接受的乳液、微乳液、溶液、悬浮液、糖浆和酏剂。除本发明组合物以外,液体剂型可含有常用于本领域的惰性稀释剂,诸如水或其他溶剂;增溶剂和乳化剂,诸如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苯甲酯、丙二醇、1,3-丁二醇、油(具体地,棉籽油、花生油、玉米油、胚芽油、橄榄油、蓖麻油和芝麻)、甘油、四氢呋喃基乙醇、聚乙二醇和脱水山梨糖醇的脂肪酸酯、环糊精及其混合物。
[0326]
除本发明组合物的外,悬浮液也可含有悬浮剂,例如乙氧基化异硬脂醇、聚氧化乙烯山梨糖醇和脱水山梨糖醇酯、微晶纤维素、偏氢氧化铝、膨润土、琼脂和黄芪胶,及其混合物。
[0327]
用于经直肠或经阴道施用的制剂可以栓剂形式呈现,其可通过将本发明组合物与一种或多种适合的无刺激性赋形剂或载体混合来制备,这种赋形剂或载体包含例如可可脂、聚乙二醇、栓剂蜡或水杨酸盐,且其在室温下为固体,但在体温下为液体,且因此,将在体腔中熔融且释放活性剂。
[0328]
用于经皮施用本发明组合物的剂型包括粉剂、喷雾剂、软膏、糊剂、乳膏、乳剂、凝胶、溶液、贴剂和吸入剂。活性组分可在无菌条件下与药学上可接受的载体且与可能需要的任何防腐剂、缓冲剂或推进剂混合。
[0329]
除本发明组合物以外,软膏、糊剂、乳膏和凝胶也可含有诸如动物和植物脂肪、油、蜡、石蜡、淀粉、黄芪胶、纤维素衍生物、聚乙二醇、聚硅酮、膨润土、硅酸、滑石和氧化锌或其混合物的赋形剂。
[0330]
除本发明组合物以外,散剂和喷雾剂也可含有诸如乳糖、滑石、硅酸、氢氧化铝、硅酸钙和聚酰胺粉末或这些物质的混合物的赋形剂。喷雾剂可另外含有习用推进剂,诸如氯氟烃和未被取代的挥发性烃,如丁烷和丙烷。
[0331]
本发明的组合物和化合物可替代地通过气溶胶施用。这通过制备含有化合物的水性气溶胶、脂质体制剂或固体颗粒来完成。可使用非水性(例如碳氟化合物推进剂)悬浮液。可使用音波喷雾器,因为其使暴露于剪切的药剂达到最少,剪切可使得包含在本发明组合物中的化合物降解。通常,水性气溶胶通过将本发明组合物的水性溶液或悬浮液与常规药学上可接受的载体和稳定剂一起配制来制得。载体和稳定剂随特定本发明组合物的需求而变化,但通常包括非离子界面活性剂(吐温类、共聚物pluronics或聚乙二醇);无害蛋白质,如血清白蛋白;脱水山梨糖醇酯;油酸;卵磷脂;氨基酸如甘氨酸;缓冲剂;盐;糖或糖醇。气溶胶一般由等张溶液制备。
[0332]
适用于非经肠施用的本发明药物组合物包含本发明组合物以及一种或多种药学上可接受的无菌等张水性或非水性溶液、分散液、悬浮液或乳液或可在即将使用之前复原成无菌可注射溶液或分散液的无菌散剂,这种无菌散剂可含有抗氧化剂、缓冲剂、抑菌剂、使制剂与预期接受者的血液等张的溶质或悬浮剂或增稠剂。
[0333]
可用于本文所提供的药物组合物中的合适水性和非水性载体的实例包括水、乙醇、多元醇(如甘油、丙二醇、聚乙二醇及其类似物)及其合适混合物、植物油(如橄榄油)和可注射有机酯(如油酸乙酯)以及环糊精。适当的流动性可例如通过使用诸如卵磷脂的包衣材料、通过在分散液的情况下维持所需粒度和通过使用界面活性剂来维持。
[0334]
在另一方面中,提供了经肠药物制剂,其包括所公开化合物和肠溶材料;以及其药学上可接受的载体或赋形剂。肠溶材料是指实质上在胃酸性环境中不溶且在特定ph下主要可溶于肠道流体中的聚合物。小肠为胃与大肠之间的胃肠道(肠)的一部分,且包括十二指肠、空肠和回肠。十二指肠的ph为约5.5,空肠的ph为约6.5,且末端回肠的ph为约7.5。
[0335]
因此,肠溶材料为不可溶的,直至例如ph为约5.0、约5.2、约5.4、约5.6、约5.8、约6.0、约6.2、约6.4、约6.6、约6.8、约7.0、约7.2、约7.4、约7.6、约7.8、约8.0、约8.2、约8.4、约8.6、约8.8、约9.0、约9.2、约9.4、约9.6、约9.8或约10.0。示例性肠溶材料包括邻苯二甲酸乙酸纤维素(cap);邻苯二甲酸羟丙基甲基纤维素(hpmcp);聚乙酸乙烯酯邻苯二甲酸酯(pvap);乙酸琥珀酸羟丙基甲基纤维素(hpmcas);苯偏三酸乙酸纤维素;琥珀酸羟丙基甲基纤维素;乙酸琥珀酸纤维素;乙酸六氢邻苯二甲酸纤维素;丙酸邻苯二甲酸纤维素;乙酸顺丁烯二酸纤维素;乙酸丁酸纤维素;乙酸丙酸纤维素;甲基甲基丙烯酸与甲基丙烯酸甲酯的共聚物;丙烯酸甲酯、甲基丙烯酸甲酯与甲基丙烯酸的共聚物;甲基乙烯基醚与顺丁烯二酸酐的共聚物(gantrez es系列);甲基丙烯酸乙酯-甲基丙烯酸甲酯-氯三甲基铵丙烯酸乙酯共聚物;天然树脂如玉米蛋白、虫胶和柯巴脂松香(copal colophorium);以及若干市售肠
溶分散系统(例如,eudragit l30d55、eudragit fs30d、eudragit l100、eudragit s100、kollicoat emm30d、estacryl 30d、coateric和aquateric)。以上材料各自的溶解性为已知的或可易于活体外测定。前述材料为可能性材料清单,但受益于本发明的本领域技术人员将认识到,其为不全面的且存在满足本文所描述的目标的其他肠溶材料。
[0336]
有利地,本文提供供用于例如需要治疗癌症的消费者使用的试剂盒。这种试剂盒包括适合的剂型,诸如上文所描述的这类剂型;以及描述使用这种剂型以介导、降低或预防发炎的方法的说明书。说明书将引导消费者或医学人员根据熟本领域中本领域技术人员已知的施用模式施用剂型。这种试剂盒可有利地以单或多个试剂盒单元封装且出售。这种试剂盒的实例为所谓的泡壳包装。泡壳包装在封装工业中为人所熟知,且广泛用于封装药物单位剂型(片剂、胶囊及其类似剂型)。泡壳包装一般由用优选透明的塑料材料箔片覆盖的相对刚性材料的薄片组成。在封装过程期间,在塑料箔片中形成凹槽。凹槽具有待封装的片剂或胶囊的大小和形状。随后,将片剂或胶囊置放在凹槽中,且相对于塑料箔片,在箔片上与形成凹槽的方向相反的一面密封相对刚性材料的薄片。因此,将片剂或胶囊密封于塑料箔片与薄片之间的凹槽中。优选地,薄片的强度使得可通过在凹槽上手动施加压力,从而在凹槽置放处的薄片中形成开口来自泡壳包装移除片剂或胶囊。随后,片剂或胶囊可通过该开口来移除。
[0337]
试剂盒上可能需要提供记忆辅助,例如以紧邻片剂或胶囊的编号形式,其中编号对应于用药方案中应摄入这种指定的片剂或胶囊的天数。这种记忆辅助的另一实例为打印于卡上的日程表,例如如下“第一周,星期一、星期二
……
等
……
第二周,星期一、星期二
……
等”。记忆辅助的其他变化形式为显而易见的。“日剂量”可为待于指定日期服用的单一片剂或胶囊或若干丸剂或胶囊。此外,第一化合物的日剂量可由一种片剂或胶囊组成,而第二化合物的日剂量可由若干片剂或胶囊组成,且反之亦然。记忆辅助应反映该情况。
实施例
[0338]
本文所描述的化合物可基于本文所含的教导和本领域中已知的合成程序以多种方式来制备。在下文所描述合成方法的描述中,应理解,除非另有指示,所有提出的反应条件(包括溶剂选择、反应氛围、反应温度、实验持续时间和处理程序)均可被选择作为该反应的标准条件。熟悉有机合成的技术人员应理解,分子多个部分上所存在的官能团应与所提出的试剂和反应物相容。不与反应条件兼容的取代基对于本领域技术人员显而易见,且因此指示替代性方法。实施例中的起始材料可市购或容易通过标准方法从已知材料制备。
[0339]
以下缩写用于本发明中,且具有以下定义:“adp”为二磷酸腺苷,“boc”为叔丁基碳酸酯,“cdi”为羰基二咪唑,“conc.”为浓缩的,“cs2co
3”为碳酸铯,“cui”为碘化铜(i),“dbu”为1,8-二氮杂双环[5.4.0]十一-7-烯,“dcc”为n,n'-二环己基碳二亚胺,“dce”为二氯乙烷,“dcm”为二氯甲烷,“diea”为n,n-二异丙基乙胺,“dma”为n,n-二甲基乙酰胺,“dmap”为4-(二甲氨基)吡啶,“dmf”为n,n-二甲基甲酰胺,“dppf”为1,1'-双(二苯基膦基)二茂铁,“dmem”为经杜尔贝科氏改良伊格尔培养基(dulbecco's modified eagle media),“dmso”为二甲基亚砜,“dppa”为二苯基磷酰叠氮化物,“edc”为1-乙基-3-(3-二甲氨基丙基)碳化二亚胺、“esi”为电喷雾电离,“et2o”为二乙醚,“etoac”为乙酸乙酯,“etoh”为乙醇,“gst”为谷胱甘肽s-转移酶,“h”为一或多个小时,“hbtu”为(2-(1h-苯并三唑-1-基)-1,1,3,3-六
氟磷酸四甲基脲鎓,“h
2”为氢气体,“hcl”为盐酸,“hex”为己烷,“h2o”为水,“hobt”为羟基苯并三唑,“ic
50”为半数最大抑制浓度,“k2co
3”为碳酸钾,“k3po
4”为磷酸钾,“limhds”为双(三甲基硅烷基)酰胺锂,“mecn”为乙腈,“meoh”为甲醇,“me4tbuxphos”为二-叔丁基(2',4',6'-三异丙基-3,4,5,6-四甲基-[1,1'-联苯]-2-基)磷化氢,“mgso
4”为硫酸镁,“mhz”为兆赫兹,“min”为一或多分钟,“ms”为质谱,“mtbe”为甲基叔丁基醚,“nadh”为烟酰胺腺二核苷酸,“nah”为氢化钠,“nahco
3”为碳酸氢钠,“na2so
4”为硫酸钠,“nh4cl”为氯化铵,“nasme”为硫代甲醇钠,“nbs”为n-溴代丁二酰亚胺,“nmr”为核磁共振,“pbs”为磷酸盐缓冲盐水,“pd/c”碳载钯,“pd2(dba)
3”为三(二苯亚甲基丙酮)二钯(0),“pd(oac)
2”为乙酸钯(ii),“pd(pph3)
4”四(三苯基膦)钯(0),“prep-hplc”为制备型高效液相色谱,“pybop”为苯并三唑-1-基-氧基三吡咯烷基鏻六氟磷酸酯,“rt”为室温,其也称为“环境温度”,其应理解为由范围在15-25℃的正常实验室温度的范围组成,“satd.”为饱和的,“t3p”为正丙烷磷酸酸酐,“tea”为三乙胺,“tfa”为三氟乙酸,“thf”为四氢呋喃,“tms”为三甲基甲硅烷基,“tris”为三(羟甲基)氨基甲烷,“xantphos”为4,5-双(二苯膦基)-9,9-二甲基氧杂蒽,“x-phos”为2-二环己基膦基-2',4',6'-三异丙基联苯,以及“zncl
2”为氯化锌。
[0340]
通用化学方法
[0341]
本文所描述的示例性化合物可通过下文流程(scheme)中所例示的通用合成方法,包括中间物制备和随附实施例制备获得。
[0342]
合成流程
[0343]
流程1
[0344][0345]
流程1说明胺d-i-i、d-i-ii和d-i
‑ⅲ
的示例性制备。在碱(例如cs2co3或k2co3)存在下,用胺r
4-h(其可为脂族或杂环的)处理a-i得到化合物b-i。在钯催化剂(铃木偶联)或薗头偶联反应存在下,用市售硼酸酯/硼酸/三氟硼酸盐进一步处理b-i(其中r
2a
为br)得到化合物c-i。中间物c-i可通过轻度还原条件(例如锌或铁金属与氯化铵)选择性转化为胺d-i-i,其中r
2b
为烯基、炔基或环烷基。中间物c-i可通过钯催化的氢化完全还原成d-i-iii。其中r
2a
为cl、br、烷基、cn或烷氧基的中间物b-i,可通过轻度还原条件,例如锌或铁金属与氯化铵还原为d-i-ii。
[0346]
在流程1中,x的实例包括n和ch,y的实例包括n、ch和c-f,其中x和y均不为n,r2的实例包括烷基和环烷基,且r4的实例包括n连接烷基和n连接杂环基,其中适合任选地选用的取代基通过以下中间物的表例示。
[0347]
流程2
[0348][0349]
流程2说明胺d-ii-i、d-ii-ii和d-ii
‑ⅲ
的示例性制备。在还原胺化条件(例如氰基硼氢化钠或三乙酰氧基硼氢化钠,在催化量于极性溶剂如meoh中的乙酸存在下),使a-ii(市售起始材料)与胺r
4-h反应得到化合物b-ii。在钯催化剂(铃木偶联)或薗头偶联反应存在下,用市售硼酸酯/硼酸/三氟硼酸盐进一步处理其中r
2a
为br的b-ii得到化合物c-ii。中间物c-ii可通过轻度还原条件(例如锌或铁金属与氯化铵)选择性转化为胺d-ii-i,其中r
2b
为烯基、炔基或环烷基。中间物c-ii可通过钯催化的氢化完全还原成d-ii-iii。其中r
2a
为cl、br、烷基、cn或烷氧基的中间物b-ii,可通过轻度还原条件(例如锌或铁金属与氯化铵)还原为d-ii-ii。
[0350]
在流程2中,x的实例包括n和ch,y的实例包括n、ch和c-f,其中x和y均不为n,r2的实例包括烷基和环烷基,且r4的实例包括n连接烷基和n连接杂环基,其中适合任选地选用的取代基通过以下中间物的表例示。
[0351]
流程3
[0352][0353]
流程3说明胺d-iii-i、d-iii-ii和d-iii-iii的示例性制备,其中l为-ch
2-ch
2-。用诸如dibal的还原剂还原a-iii-i得到醛a-iii-ii。另一种制备a-iii-ii的方式为,将a-iii-i还原为对应醇,随后为轻度氧化条件,诸如使用mno2。在还原胺化条件(例如氰基硼氢化钠或三乙酰氧基硼氢化钠,在催化量于极性溶剂如meoh中的乙酸存在下),使a-iii-ii与胺r
4-h反应得到化合物b-iii。另一种制备b-iii的方式为,将a-iii-i还原成乙醇,随后将乙醇转化成磺酸盐a-iii-iii。在碱(如三乙胺、惠宁碱或碳酸铯)存在下,a-iii-iii与胺r
4-h的反应得到b-iii。在钯催化剂(铃木偶联)或薗头偶联反应存在下,用市售硼酸酯/硼酸/三氟硼酸盐进一步处理其中r
2a
为br的b-iii得到化合物c-iii。中间物c-iii可通过轻度还原条件(例如锌或铁金属与氯化铵)选择性转化为胺d-iii-iii,其中r
2b
为烯基、炔基或环烷基。中间物c-iii可通过钯催化的氢化完全还原成d-iii-ii。其中r
2a
为cl、br、烷基、cn或烷氧基的中间物b-iii,可通过轻度还原条件(例如锌或铁金属与氯化铵)还原为d-iii-i。
[0354]
在流程3中,x的实例包括n和ch,y的实例包括n、ch和c-f,其中x和y均不为n,r的实例包括甲基和乙基,r2的实例包括烷基和环烷基,r4的实例包括具有任选地选用的取代基的n连接烷基和n连接杂环基,如通过以下中间物的表所例示,且lg的实例包括甲磺酸盐和甲苯磺酸盐。
[0355]
流程4
[0356][0357]
流程4说明胺d-iv的示例性制备,其中l为直接键-ch
2-或-ch
2-ch
2-。在酰胺偶联试剂(例如cdi、dcc、edc、hobt、hbtu、pybop或t3p)下,在催化量的dmap存在下(若必需),a-iii-i与各种胺的反应得到酰胺b-iv。
[0358]
在钯催化剂(铃木偶联)或薗头偶联反应存在下,用市售硼酸酯/硼酸/三氟硼酸盐进一步处理其中r
2a
为br的b-iv得到化合物c-iv。中间物c-iv可通过轻度还原条件(例如锌或铁金属与氯化铵)选择性转化为胺d-iv-i,其中r
2b
为烯基、炔基或环烷基。中间物c-iv可通过钯催化的氢化完全还原成d-iv-iii。其中r
2a
为cl、br、烷基、cn或烷氧基的中间物b-iv可通过轻度还原条件(例如锌或铁金属与氯化铵)还原为d-iv-ii。
[0359]
在流程4中,x的实例包括n和ch,y的实例包括n、ch和c-f,其中x和y均不为n,r的实例包括甲基和乙基,r2的实例包括烷基和环烷基,且r4的实例包括-(ch2)
m-c(o)-b和-(ch2)
m-c(o)-n(r5)r6,其中m为0、1或2。
[0360]
流程5
[0361][0362]
流程5说明胺d-v的示例性制备。在钯催化剂(铃木偶联)存在下,b-v与硼酸酯/硼酸/三氟硼酸盐反应,得到化合物c-v。许多硼酸酯/硼酸/三氟硼酸盐为市售的,且不为市售的这类可容易地由相应羧酸制备(参见流程21)。中间物c-v可通过标准还原条件,例如通过钯催化的氢化或通过包括锌金属和氯化铵的轻度还原条件转化成胺d-v。
[0363]
在流程5中,x的实例包括n和ch,y的实例包括n、ch和c-f,r2的实例包括烷基和环烷基,且r4的实例包括c连接杂环基和杂环基,其中适合任选地选用的取代基通过以下中间物的表例示。
[0364]
流程6
[0365][0366]
流程6说明示例性由c-vi-i制备d-vi,其中在c-vi-i中,r4含有氮保护基,例如boc基团。c-vi-i可在酸性条件下去保护以提供胺盐。在存在催化量的乙酸情况下,在诸如meoh的极性溶剂(还原胺化条件)中,用氰基硼氢化钠或三乙酰氧基硼氢化钠和醛或酮进一步处理盐,得到c-vi。可通过标准还原条件(例如通过钯催化的氢化),或通过包括锌金属和氯化铵的轻度还原条件,将中间物c-vi转化成苯胺d-vi。
[0367]
在流程6中,x的实例包括n和ch,y的实例包括n、ch和c-f,其中x和y均不为n,pg的实例包括boc保护基,r2的实例包括烷基和环烷基,r4的实例包括杂环基,r6的实例包括烷基和环烷基,其中适合任选地选用的取代基通过以下中间物的表例示。
[0368]
流程7
[0369][0370]
在一些实施方案中,通用吡唑胺d-vii-i或d-vii-ii是通过流程7中所示的两种方法来制备。在该流程中,展示r
4-l连接的7-1或7-2的实例。一种方法涉及在存在碱(例如碳酸钾、碳酸铯或氢化钠)和极性非质子溶剂(二甲亚砜、二甲基甲酰胺、四氢呋喃或其类似物)的情况下,在介于环境温度与150℃之间的温度,用市售7-1烷基化b-vii(本领域技术人员可容易地获得),得到硝基-吡唑c-vii-i和/或c-vii-ii。d-vii-i或d-vii-ii的替代性制备涉及b-vii与市售7-2的光延反应,得到硝基-吡唑c-vii-i和c-vii-ii。本领域技术人员应理解,当作为混合物产生时,c-vii-i和c-vii-ii是通过sfc纯化、结晶或层析分离。最后,在存在诸如钯或镍的氢化催化剂或诸如锌或铁和氯化铵的轻度还原条件的情况下,氢化硝基-吡唑c-vii-i和c-vii-ii得到吡唑-胺d-vii-i和d-vii-ii。
[0371]
在流程7中,lg的实例包括cl和br,r2的实例包括烷基、环烷基、烷氧基、卤素和cn,
其中烷基、环烷基或烷氧基可任选地被氟化,r4的实例包括具有通过以下中间物的表例示的适合任选地选用的取代基的杂环基、c(o)nr6r9和nr6r9,其中r6和r9各自可独立地为h或烷基,l的实例包括-(ch2)
m-,其中m可为0、1、2或3,且当m为0时,r4为c连接至吡唑,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l。
[0372]
流程8
[0373][0374]
被单一r2(也即其中r2不为氢)取代的通用吡唑-胺d-viii-i和d-viii-ii的其他实例是如流程8中所描述来制备。使酮-酯a-viii-i与n,n-二甲基甲酰胺二甲缩醛或原甲酸三乙酯/乙酸酐反应,得到a-viii-ii(其中lg为连续环化/吡唑形成反应中所需的适当离去基团)。在存在酸的情况下,使a-viii-ii与肼10-1(本领域技术人员可容易地获得)反应,主要得到b-viii-i或其区位异构体b-viii-ii。环化的区位化学在本领域技术人员所熟悉的条件(如温度和溶剂)下受到控制。用于合成b-viii-i(其中r2不为氢)的条件包括:其中lg为oet,在酸存在下,在质子溶剂(如乙醇)中于低温(-10℃至rt)下。合成b-viii-ii的条件包括:其中lg为nme2,在酸存在下,在质子溶剂(如乙醇)中于回流下。继而,使用本领域技术人员已知的标准条件,将酯b-viii-i或b-viii-ii转化成对应酸c-viii-i或c-viii-ii。通过柯提斯重排(curtius rearrangement)将c-viii-i或c-viii-ii转化为对应胺d-viii-i或d-viii-ii。
[0375]
在流程8中,lg的实例包括ome、oet和n(ch3)2,r2的实例包括烷基和环烷基,其中烷基和环烷基可任选地被氟化,r4的实例包括具有通过以下中间物的表例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,l的实例包括-(ch2)m-,其中m可为0、1、2或3,且当m为0时,r4为c连接至吡唑,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l。
[0376]
流程9
[0377][0378]
r2和r3=烷基、环烷基或支链烷基。均任选地被氟化。
[0379]
以与流程8类似的方式,流程9说明胺d-ix的通用制备。吡唑酯b-ix是通过肼10-1(本领域技术人员容易获得)与中间物a-ix的反应制备。在一些实施方案中,r2和r3部分独立地变化,使得r3与r2相同或不同。使用本领域技术人员已知的标准条件,将酯b-ix转化成对应酸c-ix。在本领域技术人员已知的标准柯提斯重排条件下,酸c-ix转化为胺d-ix。
[0380]
在流程9中,r2和r3的实例可独立地包括烷基和环烷基,其中烷基和环烷基可任选地被氟化,r4的实例包括具有通过以下中间物的表例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,l的实例包括-(ch2)m-,其中m可为0、1、2或3,且当m为0时,r4为c连接至吡唑,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l。
[0381]
流程10
[0382][0383]
在一些实施方案中,非市售肼10-1容易地通过流程10中所示的两种方法来制备。一种方法涉及使胺10-2重氮化,随后使用本领域技术人员熟悉的条件在质子源存在下,例如通过用sn(ii)cl2处理来还原。替代地,肼10-1可通过叔丁氧基羰基的酸催化移除来从相应n-叔丁氧基羰基肼10-3获得。本领域技术人员应认识到,在一些实施方案中,氨基甲酸酯10-3向肼10-1的转化也在反应顺序内原位实现。因此,在其中肼10-1通常在存在酸的情况下使用的所有流程中,氨基甲酸酯10-3均为肼10-1的代替物。n-叔丁氧基羰基肼10-3可通过用市售醛或酮10-4和肼羧酸叔丁酯进行还原胺化来制备。
[0384]
在流程10中,r4的实例包括具有通过以下中间物的表例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,l的实例包括-(c(r7)2)
m-,其中r7的实例为h,且其中m可为0、1、2或3,且当m为0时,r4为c连接至氮,当m为1时,r4为c连接至l,且当m为2或3时,r4为n连接或c连接至l。
[0385]
流程11
[0386][0387]
r2=烷基、环烷基、支链烷基、卤素、cn或烷氧基。均任选地被氟化。
[0388]
在一些实施方案中,通用吡唑胺d-vii-i和d-vii-ii是通过流程11中所示来制备。
在该流程中,展示r
4-l连接的11-1的实例。用11-1烷基化b-vii(本领域技术人员可容易地获得)得到硝基吡唑b-vii-i和b-vii-ii的混合物。这两种异构体b-vii-i和b-vii-ii是通过sfc纯化、结晶或层析来分离。各异构体b-vii-i或b-vii-ii使用mscl或tscl活化,分别得到b-vii-iii或b-vii-iv。用胺r
4-h置换oms或ots,分别得到c-vii-i或c-vii-ii。最后,在存在诸如钯或镍的氢化催化剂或诸如锌或铁和氯化铵的轻度还原条件的情况下,氢化硝基-吡唑c-vii-i或c-vii-ii得到吡唑-胺d-vii-i或d-vii-ii。
[0389]
在流程11中,lg的实例包括cl和br,r的实例包括甲磺酸盐和甲苯磺酸盐,r2的实例包括烷基、环烷基、烷氧基、卤素和cn,其中烷基、环烷基或烷氧基可任选地被氟化,r4的实例包括具有如通过以下中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,l的实例包括-(ch2)m,其中m为2或3,且r4为n连接。
[0390]
流程12
[0391][0392]
流程12说明通用胺d-x-i和d-x-ii的合成。因此,在存在氢氧化铵的情况下,缩合市售醛与乙二醛,得到被r2取代的咪唑a-x。在该流程中,展示r
4-l连接的7-1或7-2的实例。通过本领域技术人员已知的条件(例如在介于0℃至100℃范围温度下的硝酸/浓硫酸),硝化咪唑a-x得到硝基咪唑b-x-i。通过烷基化(7-1)或光延反应(7-2)将b-x-i转化成c-x-i和c-x-ii的混合物。在一些实施方案中,被取代的硝基-咪唑c-x-i和c-x-ii可通过来自a-x的烷基化(7-1)或光延反应(7-2)获得,得到b-x-ii。随后使b-x-ii硝化,得到c-x-i和c-x-ii。这两种区位异构体c-x-i和c-x-ii可通过sfc纯化、结晶或层析来分离。在存在诸如钯或镍的氢化催化剂或诸如锌或铁和氯化铵的轻度还原条件下,还原各硝基咪唑c-x-i和c-x-ii,分别得到对应咪唑胺d-x-i和d-x-ii。
[0393]
在流程12中,试剂7-1中的lg的实例包括cl和br,r2的实例包括烷基和环烷基,其中烷基和环烷基可任选地被氟化,r4的实例包括具有通过以下中间物的表所例示的适合任
选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,l的实例包括-(ch2)
m-,其中m可为2或3,l为n连接至咪唑环。
[0394]
流程13
[0395][0396]
如流程13中所例示,在一些实施方案中,被取代的噻唑胺d-xi可由被适当取代的噻唑a-xi(本领域技术人员可容易地获得)来制备。该方法已描述于wo2006072436中,其内容在此通过引用整体并入本文。使用发烟硝酸或具有硫酸的硝酸,硝化溴噻唑a-xi得到溴硝基噻唑b-xi。可使用本领域技术人员所熟悉的条件(如布赫瓦尔德(buchwald)、ullmann或亲核芳族取代反应),在tea或k2co3存在下,通过各种胺r
4-h置换b-xi上的溴官能团得到c-xi,其中r4为n连接的。使用b-xi与市售或合成硼酸酯t(包括但不限于:其他硼盐)的铃木反应(参见流程21)提供c-xi,其中r4为c连接的。最后,在存在诸如钯或镍的氢化催化剂或诸如锌或铁和氯化铵的轻度还原条件的情况下,氢化c-xi得到对应噻唑胺d-xi。
[0397]
在流程13中,r2的实例包括烷基、环烷基、烷氧基、卤素和cn,其中烷基、环烷基或烷氧基可任选地被氟化,且r4的实例包括具有如通过以下中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基。
[0398]
流程14
[0399][0400]
如流程14中所例示,在一些实施方案中,被取代的噻唑胺d-xii可由被适当取代的噻唑a-xi(本领域技术人员可容易地获得)来制备。该方法已描述于wo2009158373、
wo2016135163和wo2011075515中,其内容在此通过引用整体并入本文。使用发烟硝酸或具有硫酸的硝酸,硝化溴噻唑a-xi得到溴硝基噻唑b-xi。b-xi上的溴官能团可使用诸如羰基化(c-xii-ia)、根岸(negishi)反应(锌介导的偶联条件(c-xii-ib))、薗头(sonogashira)或赫克(heck)偶联反应的本领域技术人员所熟悉的条件,由各种接头(l)合成子置换,接着进行适当还原,得到c-c连接的c-xii-ic。可将c-xii-ia、c-xii-ib和c-xii-ic还原成伯醇,接着进行甲磺酰化或甲苯磺酰化以形成c-xii-ii。用不同亲核试剂r
4-h,亲核取代c-xii-ii得到c-xii-iii。最后,在存在诸如钯或镍的氢化催化剂或诸如锌或铁和氯化铵的轻度还原条件下,还原c-xii-iii得到对应噻唑胺d-xii。
[0401]
在流程14中,lg的实例包括ots和oms,r的实例包括甲基和乙基,r2的实例包括烷基、环烷基、烷氧基、卤素和cn,其中烷基、环烷基或烷氧基可任选地被氟化,r4的实例包括具有通过下文中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,且l的实例包括-(ch2)m-,其中m可为1、2或3。
[0402]
流程15
[0403][0404]
在如流程15中所示的类似反应顺序中,溴噻唑a-xiii(本领域技术人员容易获得)得到噻唑-胺d-xiii(science of synthesis,627,2002)。
[0405]
在流程15中,r2的实例包括烷基、环烷基、烷氧基、卤素或cn,其中烷基、环烷基或烷氧基可任选地被氟化,且r4的实例包括具有如通过以下中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基。
[0406]
流程16
[0407][0408]
如流程16中所例示,在一些实施方案中,被取代的噻唑胺d-xiv可由被适当取代的噻唑a-xiii(本领域技术人员可容易地获得)来制备。该方法已描述于wo2009158373、wo2016135163和wo2011075515中,其内容在此通过引用整体并入本文。使用发烟硝酸或具有硫酸的硝酸,硝化溴噻唑a-xiii得到溴硝基噻唑b-xiii。b-xiii上的溴官能团可使用诸如羰基化(c-xiv-ia)、根岸(negishi)反应(锌介导的偶联条件(c-xiv-ib))、薗头(sonogashira)或赫克(heck)偶联反应的本领域技术人员所熟悉的条件,由各种r4基团置换,接着进行还原,得到c-c连接的c-xiv-ic。可将c-xiv-ia、c-xiv-ib和c-xiv-ic还原成伯醇,接着进行甲磺酰化或甲苯磺酰化以形成c-xiv-ii。用不同亲核试剂r
4-h,亲核取代c-xiv-ii得到c-xiv-iii。最后,在诸如钯或镍的氢气催化剂或诸如锌或铁和氯化铵的轻度还原条件下,还原c-xiv
‑ⅲ
得到对应噻唑-胺d-xiv。
[0409]
在流程16中,lg的实例包括ots和oms,r的实例包括甲基和乙基,r2的实例包括烷基、环烷基、烷氧基、卤素和cn,其中烷基、环烷基或烷氧基可任选地被氟化,r4的实例包括具有通过下文中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,且l的实例包括-(ch2)m-,其中m可为1、2或3。
[0410]
流程17
[0411][0412]
流程17描述如wo2014078378中所报导的被取代的恶唑d-xv的合成,其内容在此通
过引用整体并入本文。使各种酸氯化物a-xv-i与被r2取代的氨基烷腈17-1(本领域技术人员可容易地获得)反应,得到a-xv-ii。在诸如乙酸、硫酸或盐酸的酸性条件下,将a-xv-ii转化成恶唑胺d-xv。
[0413]
在流程17中,r2的实例包括烷基、环烷基和烷氧基,其中烷基、环烷基或烷氧基可任选地被氟化,且r4的实例包括具有如通过以下中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,且l的实例包括-(ch2)
m-,其中m可为0、1、2或3。
[0414]
流程18
[0415][0416]
如流程18中所示,一些被取代的恶唑可由如synlett,1996,1171中所报导的被2-重氮基-3-桥氧基取代的羧酸酯a-xvi制备,其内容在此通过引用整体并入本文。在被rh催化的偶联条件下,用伯酰胺18-1(本领域技术人员可容易地获得)处理重氮酯a-xvi后,得到酰胺b-xvi。在环化脱水条件下,使用脱水剂(例如pocl3、t3p或伯格斯试剂(burgess reagent)),使中间物b-xvi得到恶唑酯c-xvi-i。水解恶唑酯c-xvi-i得到羧酸c-xvi-ii,在柯提斯重排下使用叠氮化钠或dppa将其转化成恶唑胺d-xvi。
[0417]
在流程18中,r2的实例包括烷基、环烷基和烷氧基,其中烷基、环烷基或烷氧基可任选地被氟化,且r4的实例包括具有如通过以下中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,且l的实例包括-(ch2)
m-,其中m可为0、1、2或3。
[0418]
流程19
[0419][0420]
如流程19中所示,在其他实施方案中,恶唑胺d-xvii可由如wo2012033195中所描述的2-卤基恶唑c-xvii-i制备,其内容在此通过引用整体并入本文。在布赫瓦尔德偶联条件下,使c-xvii-i与各种胺r
4-h反应,得到被2-氨基烷基取代的恶唑c-xvii-ii,其中r4为n键联的。c-xvii-i与市售或合成的硼酸酯t(包括但不限于:其他硼盐)的铃木反应(参见流
程21)用于提供c-i-21,其中r4为c连接的。水解恶唑酯c-xvii-i得到羧酸,在柯提斯重排下使用叠氮化钠或dppa将其转化成恶唑胺d-xvii。
[0421]
在流程19中,r2的实例包括烷基、环烷基或烷氧基,其中烷基、环烷基或烷氧基可任选地被氟化,且r4的实例包括具有如通过以下中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基。
[0422]
流程20
[0423][0424]
在一些实施方案中,通用三唑胺d-xviii-i和d-xviii-ii是通过流程20中所示来制备。在该流程中,展示r
4-l连接的7-1或7-2的实例。通过使用asian j.of chem,2014,26,4744和hanneng cailliao,2008,16,49中所描述的程序与醛20-1(本领域技术人员可容易地获得)反应,由二硝基酯a-xviii-i制备三唑b-xviii,其内容在此通过引用整体并入本文。或者,可通过硝化a-xviii-ii来制备b-xviii。通过烷基化(7-1)或光延反应(7-2),将b-xviii转化成c-xviii-i和c-xviii-ii的混合物。这些两种区位异构体c-xviii-i和c-xviii-ii可通过sfc纯化、结晶或层析来分离。在存在诸如钯或镍的氢化催化剂或诸如锌或铁和氯化铵的轻度还原条件下,还原硝基三唑c-i-22或c-i-23,分别得到对应的三唑胺d-xviii-i和d-xviii-ii。
[0425]
在流程20中,r2的实例包括烷基、环烷基、烷氧基、卤素或cn,其中烷基、环烷基或烷氧基可任选地被氟化,r4的实例包括具有如通过以下中间物的表所例示的适合任选地选用的取代基的杂环基和nr6r9,其中r6和r9各自可独立地为烷基,l的实例包括-(ch2)
m-,其中
m为2或3。
[0426]
流程21
[0427][0428]
流程21说明非市售硼酸/硼酸酯t的通用制备。这些化合物可容易地由被取代的羧酸制备。可在偶联剂(例如dci或et3n/hatu)存在下,通过2-羟基异吲哚啉-1,3-二酮活化羧酸得到q。通过用[b2pin2me]li复合物进行镍催化的去羧基硼基化,将中间物q转化为硼酸酯t,其预混合有甲基锂和b2pin2(science,2107,356,1045和jacs,2016,138,2174),其内容在此通过引用整体并入本文。
[0429]
在流程21中,r4的实例包括具有如通过以下中间物的表所例示的适合的任选地选用的取代基的烷基、环烷基和杂环基,且l的实例包括-(ch2)m-,其中m可为0、1、2或3,且当m为0时,r4为c连接至硼酸酯,当m为1时,则r4为c连接至l,且当m为2或3,则r4为n连接或c连接至l。
[0430]
流程22
[0431][0432]
流程19说明l-i-1和l-i-2的通用制备。在存在cui和csf的情况下,使市售2,4-二氯-5-碘嘧啶与tmschf2在诸如nmp或dmf的溶剂中反应,产生二氟甲基嘧啶l-ii-1(us20150284341,其内容在此通过引用整体并入本文)。通过在低于10℃的温度下用含有硫代甲醇钠和氯化锌的二乙醚处理,可将二氟甲基嘧啶l-ii-1转化成甲硫基嘧啶l-i-1(wo2012110773,其内容在此通过引用整体并入本文)。以与l-i-1类似的方式,可由市售2,4-二氯-5-(三氟甲基)嘧啶l-ii-2制备三氟甲基嘧啶l-i-2。
[0433]
流程23
[0434]
[0435]
流程23说明其中r1可为环烷基的磺酰基嘧啶l-iii(t=2)的通用制备。在存在钯催化剂的情况下,用硼酸酯/硼酸/三氟硼酸盐处理市售5-溴-2-氯-6-(甲硫基)嘧啶(铃木偶联),得到被r1取代的硫基嘧啶l-iii(t=0)。此流程中的r1的实例包括诸如环丙基的环烷基。通过氧化,例如通过mcpba,将中间物硫基嘧啶l-iii(t=0)转化成磺酰基嘧啶l-iii(t=2)。
[0436]
流程24
[0437][0438]
流程24说明h-i的通用制备。在碱(et3n或diea)存在下,在dcm中用市售酰基氯化物(f-i)处理市售e-i得到酰胺g-i。许多酰基氯化物(f-i)为市售的,且在碱(et3n或diea)存在下,不为市售的这类可容易地从具有socl2的相应羧酸f-i-1制备。可在暴露于酸,例如hcl或tfa后移除g-i的boc保护基。在流程24中,r
l
的实例可包括烷基和环烷基(例如环丁基)。
[0439]
流程25
[0440][0441]
流程25说明h-ii的通用制备。可通过使胺e-ii与市售异氰酸酯f-ii反应来制备化合物g-ii。多种异氰酸酯为市售的,且不为市售的这类可容易地自相应羧酸或胺制备(参见流程27)。可在暴露于酸,例如hcl或tfa后移除g-ii的boc保护基。在流程25中,r9的实例可包括烷基和环烷基(例如环丁基)且r6的实例可包括h和烷基。
[0442]
流程26
[0443][0444]
流程26说明h-iii的通用制备。可通过使胺e-iii与2,2,2-氨基甲酸三氯乙酯f-iii反应来制备化合物g-iii,该2,2,2-氨基甲酸三氯乙酯f-iii可由胺和酸制备(参见流程27)。可在暴露于酸,例如hcl或tfa后移除g-iii的boc保护基。在流程26中,r9的实例可包括
烷基和环烷基(例如环丁基)且r6的实例可包括h和烷基。
[0445]
流程27
[0446][0447]
流程27说明异氰酸酯f-ii和氨基甲酸酯f-iii的通用制备。非商业异氰酸酯f-ii可由胺或羧酸制备。胺与光气或光气等效物(如双光气、三光气或n,n'-二羰基咪唑)反应提供异氰酸酯f-ii。或者,可通过柯提斯重排直接从羧酸获得异氰酸酯f-ii:在碱(如三乙胺)存在下,将酸与叠氮磷酸二苯酯混合于溶剂(如1,4-二恶烷或二甲基甲酰胺)中,且升高反应物的温度至约80-120℃。也可通过柯提斯重排,在诸如三乙醇的适当乙醇存在下制备某些氨基甲酸酯f-iii。也通过标准条件,用氯甲酸三氯乙酯酰化而容易地从胺制备氨基甲酸三氯乙酯f-iii。
[0448]
流程28
[0449][0450]
流程28说明关键中间物j和k的通用制备。关键中间物j,可在有机碱(例如,三乙胺或diea)存在下任选地进行加热,由h(游离碱或盐)和硫嘧啶l-i制备得到关键中间物j。以类似方式,可通过与l-ii或l-iii反应,由h制备关键中间物k。
[0451]
流程29
[0452][0453]
流程29说明关键中间物m的通用制备。在布赫瓦尔德-哈特维希偶联条件(cs2co3、xantphos和pd(oac)2)下,用市售氯碘吡啶处理h,通常在非质子性溶剂(例如dme、dmf、dmso或nmp)中于环境温度至140℃范围的温度下进行,得到关键中间物m。
[0454]
流程30
[0455][0456]
流程30说明从取代的d通用制备式i-1化合物。可由关键中间物k和j实现式i-1的制备。通常在极性溶剂中于环境温度至150℃范围温度下,k与式d的胺进行第一亲核取代反应,在一些实施方案中,任选地在酸(例如于1,4-二恶烷中的4n hcl)存在下,进行微波加热得到式i-1。非市售的化合物d可易于制备(参见流程1-20)。式i的替代性通用合成是通过两步法,通过使用诸如mcpba的各种氧化剂进行氧化,首先将j(t=0)转化成亚砜j(t=1)。亚砜通过亲核取代反应与胺d反应,通常在极性溶剂中于环境温度至150℃范围温度下,在一些实施方案中,任选地在酸(例如于1,4-二恶烷中的4n hcl)或ptsa存在下进行微波加热。含有诸如r4上的boc基团的氮保护基的式i-1,可在酸性条件下去保护,得到式i-1(r4含有游离胺或盐)。在催化量的乙酸存在下,于诸如meoh的极性溶剂(还原胺化条件)中,用氰基硼氢化钠或三乙酰氧基硼氢化钠和醛或酮进一步处理式i-a(游离碱或盐)得到式i-1,其中r4含有被烷基或环烷基取代的氮。对于酰化和磺酰化,可用市售酰基氯化物或磺酰氯处理游离胺(或盐),得到式i-1,其中r4含有被酰基或磺酰基取代的氮。在流程30中,环a可为苯基或吡啶基(例如,x=含有y的环)或5员杂芳基(例如,含有x
1-y-x2的环)。
[0457]
流程31
[0458][0459]
流程31说明式i-2化合物的通用制备。可通过d与m之间的布赫瓦尔德-哈特维希偶联反应实现式i-2的制备。许多不为市售的胺d可易于制备(参见流程1-12)。在对含有诸如boc基团的氮保护基的式i-2进行去保护之后,可以与流程30中所示类似的方式进行还原烷基化、酰化和磺酰化,得到式i-2。在流程31中,环a可为苯基或吡啶基(例如,x=含有y的环)或5员杂芳基(例如,含有x
1-y-x2的环)。
[0460]
使用本文所描述的合成程序和方法和本领域技术人员已知的方法,制备以下化合物:
[0461]
中间物的制备
[0462]
使用本文所描述的合成程序和方法和本领域技术人员已知的方法,制备以下化合物:
[0463]
通用方法a:芳族亲核型取代:
[0464]
中间物a1:1-(3-溴-4-硝基苯基)-4-甲基哌嗪
[0465][0466]
在室温下用k2co3(63g,455mmol)处理2-溴-4-氟-1-硝基苯(50g,227mmol)和1-甲基哌嗪(24g,250mmol)于dmf(400ml)中的混合物,且在60℃下搅拌反应混合物16小时。反应混合物用冰水(500ml)稀释,并过滤沉淀固体。将该固体进一步用et2o和正戊烷湿磨,获得呈黄色固体状的1-(3-溴-4-硝基苯基)-4-甲基哌嗪(58g,85%产率)。1h nmr(400mhz,dmso-d6):d 7.98(d,j=9.4hz,1h),7.24(d,j=2.1hz,1h),7.01(dd,j=2.2和9.4hz,1h),3.42(m,4h),2.40(m,4h),2.19(s,3h);lc-ms(esi)m/z:299.0(m h
)。
[0467]
通用方法b:去保护和还原胺化:
[0468]
中间物a2:3-(3-溴-4-硝基苯基)-8-甲基-3,8-二氮双环[3.2.1]辛烷
[0469][0470]
用在1,4-二恶烷中的4n hcl(16ml,62mmol)处理3-(3-溴-4-硝基苯基)-3,8-二氮双环[3.2.1]辛烷-8-甲酸叔丁酯(a13,2.57g,6.2mmol)于meoh(30ml)中的溶液,且在室温下搅拌反应混合物16小时。在真空下将反应混合物浓缩至干燥,得到呈白色固体状的3-(3-溴-4-硝基苯基)-3,8-二氮双环[3.2.1]辛烷盐酸盐(2.17g,100%产率)。材料无需进一步纯化即继续使用。用diea(2.9ml,17mmol)和甲醛(1.2ml,17mmol)处理3-(3-溴-4-硝基苯基)-3,8-二氮双环[3.2.1]辛烷盐酸盐(1.92g,5.5mmol)于dce(25ml)中的悬浮液。黄色悬浮液变成澄清橙色溶液。在室温下搅拌反应混合物10分钟,且随后添加乙酸(0.63ml,11mmol)。橙色溶液变成黄色悬浮液,将其搅拌20分钟。添加三乙酰氧基硼氢化钠(2.33g,11mmol),且在室温下搅拌反应混合物4小时。用nahco3水溶液(50ml)稀释反应混合物,且用dcm(3
×
50ml)萃取溶液。合并的有机物经无水na2so4干燥,过滤且浓缩,得到棕色固体。棕色固体使用硅胶柱层析(0-15%meoh/dcm)纯化,得到呈黄色固体状的3-(3-溴-4-硝基苯基)-8-甲基-3,8-二氮双环[3.2.1]辛烷(1.71g,95%产率)。1h nmr(400mhz,dmso-d6):δ7.98(d,j=9.4hz,1h),7.10(d,j=2.7hz,1h),6.89(dd,j=9.5和2.7hz,1h),3.54(d,j=11.6hz,2h),3.22(brs,2h),2.99-3.04(m,2h),2.22(s,3h),1.92-1.95(m,2h),1.52-1.56(m,2h);lc-ms(esi)m/z:326.0(m h
)。
[0471]
通用方法c:烷基化:
[0472]
中间物a3:1-(2-氟乙基)-4-(3-甲基-4-硝基苯基)哌嗪
[0473][0474]
用1-氟-2-碘乙烷(2.0ml,2.6mmol)处理1-(3-甲基-4-硝基苯基)哌嗪盐酸盐(a4的boc去保护产物,1.5g,0.58mmol)和k2co3(4.0g,2.9mmol)于1,4-二恶烷(20ml)中的混合物[注意:所描述的材料易于不稳定—液体中存在一些固体],紧密封盖且加热至100℃持续24小时。将混合物冷却至室温,通过过滤移除固体(k2co3),用dcm冲洗且浓缩滤液至干燥,得到呈黄色油状的1-(2-氟乙基)-4-(3-甲基-4-硝基苯基)哌嗪(1.52g,产率98%),将其静置后固化为琥珀色固体。1h nmr(400mhz,dmso-d6):d 7.97(d,j=9.6hz,1h),6.87-6.89(m,
2h),4.61(t,j=4.9hz,1h),4.52(t,j=4.9hz,1h),3.41(m,4h),2.69(t,j=4.9hz,1h),2.63(t,j=4.9hz,1h),2.54-2.56(m,7h);lc-ms(esi)m/z:268.2(m h
)。
[0475]
使用上述通用方法a-c,制备表a中的以下中间物。
[0476]
表a.
[0477]
[0478]
[0479]
[0480]
[0481]
[0482][0483]
中间物a30:1-(3-溴-4-硝基苯基)-4-甲基哌嗪基2-酮。
[0484][0485]
于室温在n2氛围下用4-氟-2-溴-1-硝基苯(5g,22mmol)处理(2-氨基乙基)(甲基)氨基甲酸叔丁酯(4.3g,24mmol)和碳酸钾(3.8g,27mmol)于dmf(50ml)中的混合物,且在90℃下搅拌混合物16小时。用水(200ml)稀释反应混合物,且用etoac(2
×
100ml)萃取溶液,合并的有机物经无水na2so4干燥,过滤且浓缩。粗产物通过硅胶柱层析(2%meoh/dcm,10份柱体积(cv))纯化,得到呈黄色液体状的(2-((3-溴-4-硝基苯基)氨基)乙基)(甲基)氨基甲酸叔丁酯(5.6g,66%产率)。1h nmr(400mhz,dmso-d6):δ7.98(d,j=9.0hz,1h),6.77(s,1h),6.46(d,j=9.0hz,1h),3.54(s,2h),3.31(t,j=6.0hz,2h),2.90(s,3h),1.47(s,9h);lc-ms(esi)m/z:374.1(m h
)。
[0486]
于0℃在n2氛围下用氯乙酰氯(5.1g,45mmol)处理((2-((3-溴-4-硝基苯基)氨基)乙基)(甲基)氨基甲酸叔丁酯(5.6g,15mmol)和tea(7.6g,75mmol)于dcm(100ml)中的混合物,且在室温下搅拌混合物16小时。用水(100ml)稀释反应混合物,且用dcm(2
×
100ml)萃取溶液。在减压下蒸发合并的有机物,且粗产物通过硅胶柱层析(2%meoh/dcm,10份柱体积(cv))纯化,得到呈黄色液体状的(2-(n-(3-溴-4-硝基苯基)-2-氯乙酰氨基)乙基)(甲基)氨基甲酸叔丁酯(5.6g,66%产率)。1h nmr(400mhz,dmso-d6):δ8.12(d,j=8.6hz,1h),7.97(s,1h),6.66(d,j=7.4hz,1h),4.24(m,2h),3.82(s,2h),3.18(s,2h),2.70(s,3h),1.41
(s,9h);lc-ms(esi)m/z:374.1(m h
)。
[0487]
于0℃在n2氛围下用在1,4-二恶烷中的4n hcl(100ml)处理n-(3-溴-4-硝基苯基)-2-氯-n-(2-(甲基氨基)乙基)乙酰胺盐酸盐(5.6g,12mmol)于二恶烷(100ml)中的溶液,且在室温下搅拌反应混合物16小时。在减压下蒸发反应混合物,且通过在et2o(100ml)中结晶来纯化粗产物,获得呈黄色固体状的n-(3-溴-4-硝基苯基)-2-氯-n-(2-(甲基氨基)乙基)乙酰胺盐酸盐(4.79g,99%产率)。1h nmr(400mhz,dmso-d6):δ8.75(brs,2h),8.16(m,2h),7.83(d,j=7.8hz,1h),4.20(s,2h),3.98(t,2h),3.20(s,2h),2.56(s,3h),1.41(s,9h);lc-ms(esi)m/z:374.1(m h
)。
[0488]
于0℃在n2氛围下向于60%矿物油中的nah(1.1g,25mmol)中添加n-(3-溴-4-硝基苯基)-2-氯-n-(2-(甲基氨基)乙基)乙酰胺盐酸盐(5.0g,12mmol)于dmf(50ml)中的溶液,且在室温下搅拌反应混合物2小时。用水(100ml)稀释反应混合物,且用etoac(2
×
50ml)萃取溶液。在减压下蒸发合并的有机物,且通过硅胶柱层析(2%meoh/dcm,10份柱体积(cv))纯化粗产物,得到呈黄色固体状的1-(3-溴-4-硝基苯基)-4-甲基哌嗪-2-酮(3.1g,76%产率)。1h nmr(400mhz,dmso-d6):δ8.0(d,j=9.4hz,1h),7.24(d,j=2.3hz,1h),6.99(dd,j=2.3和9.3hz,1h),4.0(s,2h),3.72(t,j=5.4hz,2h),3.45(t,j=5.4hz,2h),2.90(s,3h);lc-ms(esi)m/z:314.2(m h
)。
[0489]
中间物a31:1-(3-(甲氧基甲基)-4-硝基苯基)-4-甲基哌嗪:
[0490][0491]
将(5-(4-甲基哌嗪-1-基)-2-硝基苯基)甲醇(1.0g,4.0mmol)于dmf(30ml)中的溶液冷却至0℃。逐份添加氢化钠(0.80g,60%于矿物中),且在相同条件下搅拌混合物。于0℃添加碘甲烷(1.7g,12mmol),且混合物缓慢升温至室温并搅拌2小时。反应物用etoac稀释且小心地用冰水淬灭。混合物用etoac(3
×
30ml)萃取,且合并的有机萃取物经无水na2so4干燥,过滤且在减压下浓缩,获得粗产物。通过硅胶柱层析(己烷/etoac)纯化粗产物,得到1-(3-(甲氧基甲基)-4-硝基苯基)-4-甲基哌嗪(0.76g,72%产率)。1h nmr(400mhz,dmso-d6):δ8.03(m,1h),7.08(s,1h),6.96(m,1h),4.76(s,2h),3.45(brs,4h),3.40(s,3h),2.42(brs,4h),2.22(s,3h);lc-ms(esi)m/z:266.2(m h
)。
[0492]
通用方法d:铃木偶联反应:
[0493]
中间物c1:1-甲基-4-(3-甲基-4-硝基苯基)-1h-咪唑:
[0494]
[0495]
用碳酸钾(1.26g,9.1mmol)处理4,4,5,5-四甲基-2-(3-甲基-4-硝基苯基)-1,3,2-二氧杂硼杂环戊烷(0.80g,3.0mmol)和4-溴-1-甲基-1h-咪唑(0.49g,3.0mmol)于1,4-二恶烷(12ml)和水(0.5ml)的混合物中的悬浮液,且搅拌悬浮液。反应混合物通过鼓泡氩气脱气两分钟,且用pd(dppf)cl2.dcm加合物(0.50g,0.61mmol)处理。在100℃下加热所得反应混合物16小时。反应物用水稀释,且用dcm(4
×
25ml)萃取。合并有机相且经无水na2so4干燥,过滤且在真空下浓缩至干燥,得到黑色油状物。使用硅胶(0-15%meoh/dcm,15份柱体积(cv))纯化黑色油,得到1-甲基-4-(3-甲基-4-硝基苯基)-1h-咪唑(0.31g,47%产率)。1h nmr(400mhz,dmso-d6):δ8.02(d,j=8.6hz,1h),7.84(d,j=7.7hz,2h),7.77(d,j=8.6hz,1h),7.72(s,1h),3.70(s,3h),2.57(s,3h);lc-ms(esi)m/z:218.2(m h
)。
[0496]
使用上述通用方法d,制备表b的以下中间物。
[0497]
表b.
[0498][0499]
通用方法e:烷基化和甲磺酸化:
[0500]
中间物c1:甲磺酸2-(3-甲基-4-硝基-1h-吡唑-1-基)乙酯。
[0501][0502]
(a)用2-溴乙-1-醇(16g,130mmol)和碳酸钾(48.8g,354mmol)处理3-甲基-4-硝基-1h-吡唑(15g,118mmol)于乙腈(200ml)中的溶液。于90℃加热反应混合物16小时。将反
应混合物用水(100ml)稀释,且用乙酸乙酯(3
×
200ml)萃取。合并的有机萃取物用盐水(50ml)洗涤,经无水na2so4干燥,过滤且在减压下浓缩。通过sfc纯化来纯化粗产物,获得2-(3-甲基-4-硝基-1h-吡唑-1-基)乙-1-醇。1hnmr(400mhz,dmso-d6):δ8.72(s,1h),4.96(t,j=5.2,hz,1h),4.12(t,j=5.2hz,2h),3.73(t,j=5.2hz,2h),2.42(s,3h);ms(esi)m/z:172.1(m 1)。
[0503]
(b)于0℃在n2氛围下用三乙胺(5.8g,58mmol),随后用甲磺酰氯(5.0g,44mmol)处理2-(3-甲基-4-硝基-1h-吡唑-1-基)乙-1-醇(5.0g,29mmol)于dcm(50ml)中的溶液。室温搅拌反应混合物4小时。用冷冻水(20ml)淬灭反应混合物。用dcm(2
×
200ml)萃取溶液,且将合并的有机萃取物用盐水(50ml)洗涤,经无水na2so4干燥,过滤且在减压下浓缩,获得呈灰白色固体状的甲磺酸2-(3-甲基-4-硝基-1h-吡唑-1-基)乙酯(6.0g,83%产率)。1h nmr(400mhz,dmso-d6):δ8.88(s,1h),4.57(t,j=5.2,hz,2h),4.46(t,j=5.2hz,2h),3.32(s,3h),2.45(s,3h);ms(esi)m/z:250.2(m h
)。
[0504]
通用方法f:亲核取代反应:
[0505]
实施例c2:n,n-二甲基-2-(3-甲基-4-硝基-1h-吡唑-1-基)乙-1-胺
[0506][0507]
在n2氛围下于10℃用碳酸钾(3.8g,28mmol)和于thf中的2n二甲基胺(60ml,12mmol)处理甲磺酸2-(3-甲基-4-硝基-1h-吡唑-1-基)乙酯(c1,5.0g,20mmol)于无水thf(70ml)中的溶液。用冷冻水(20ml)淬灭反应混合物。溶液用乙酸乙酯(3
×
100ml)萃取,且合并的有机萃取物用盐水(50ml)洗涤,经无水na2so4干燥,过滤且在减压下浓缩,获得n,n-二甲基-2-(3-甲基-4-硝基-1h-吡唑-1-基)乙-1-胺(1.9g,48%产率)。1h nmr(400mhz,dmso-d6):δ8.77(s,1h),4.17(t,j=6.4,hz,2h),2.64(t,j=6.4hz,2h),2.41(s,3h),2.15(s,6h).);ms(esi)m/z:199.2(m h
)。
[0508]
通用方法g:光延反应:
[0509]
中间物c3:1-甲基-4-(3-甲基-4-硝基-1h-吡唑-1-基)哌啶。
[0510][0511]
在氮气氛围下向3-甲基-4-硝基-1h-吡唑(5g,39.4mmol)和1-甲基哌啶-4-醇(4.5g,39.4mmol)于无水thf(60ml)中的溶液中添加三苯基膦(154.7g,59mmol),且将混合物冷却至0℃。逐滴添加偶氮二甲酸二异丙酯(12ml,59mmol)至以上混合物中历经30分钟,且在室温下持续搅拌30小时。在减压下移除thf,且随后添加3n hcl水溶液(30ml)。用etoac(3
×
20ml)洗涤所得溶液,且接着用饱和碳酸钾水溶液碱化水层(直到ph=9)。溶液用10%
甲醇/dcm(3
×
20ml)萃取。合并的有机萃取物经无水na2so4干燥,过滤且在减压下浓缩。采用急骤层析通过硅胶柱层析(0-10%meoh/dcm 15份柱体积(cv))纯化残余物,获得区位异构体的混合物。通过sfc分离这些两种区位异构体,获得期望的区位异构体即呈白色固体的1-甲基-4-(3-甲基-4-硝基-1h-吡唑-1-基)哌啶(2.0g,23%产率)。且也获得另一区位异构体1-甲基-4-(5-甲基-4-硝基-1h-吡唑-1-基)哌啶(1.4g,15%产率)。1h nmr(400mhz,dmso-d6):δ8.84(s,1h),4.16(m,1h),2.91(m,2h),2.42(s,3h),2.26(s,3h),2.13(m,2h),1.98(m,4h);ms(esi)m/z:225.4(m h
)。
[0512]
使用上述通用方法b、c和e-g,制备表c的以下中间物。
[0513]
表c.
[0514]
[0515]
[0516]
[0517]
[0518][0519]
制备实施例c29:
[0520][0521]
于0℃在ar下用氢化钠(0.94g,24mmol)逐份处理5-甲基-4-硝基-1h-吡唑(2.0g,16mmol)于dmf(15ml)中的溶液持续15分钟。在室温下搅拌混合物2小时,随后添加2-溴-2-甲基丙酸甲酯(4.3g,24mmol)。在室温下继续搅拌反应混合物16小时。用饱和nh4cl溶液(100ml)淬灭反应混合物,且用etoac(2
×
80ml)萃取溶液。用水(80ml)、10%licl水溶液(80ml)洗涤合并的有机物,经无水na2so4干燥,过滤并在减压下浓缩。通过急骤层析纯化粗产物,得到呈白色固体状的2-甲基-2-(3-甲基-4-硝基-1h-吡唑-1-基)丙酸甲酯(2.9g,产率81%)。1h nmr(500mhz,dmso-d6):δ8.98(s,1h),3.65(s,3h),2.42(s,4h),1.78(s,6h);lc-ms m/z:228.2(m h
)。
[0522]
用氢氧化锂水合物(0.54g,13mmol)于水(10ml)中的溶液处理2-甲基-2-(3-甲基-4-硝基-1h-吡唑-1-基)丙酸甲酯(2.9g,13mmol)于thf(40ml)中的溶液。在室温下搅拌混合物16小时。浓缩反应混合物,用水(60ml)稀释,且用1n hcl水溶液酸化直到ph为约4。将所得悬浮液过滤,用水(2
×
10ml)洗涤且进行空气干燥,得到呈白色固体状的2-甲基-2-(3-甲基-4-硝基-1h-吡唑-1-基)丙酸(2.2g,81%产率)。lc-ms m/z:214.2(m h
)。
[0523]
用一滴dmf、接着用乙二酰氯(2.8ml,32mmol)处理2-甲基-2-(3-甲基-4-硝基-1h-吡唑-1-基)丙酸(2.3g,11mmol)于dcm(30ml)中的悬浮液。在室温下搅拌悬浮液3小时,随后浓缩澄清溶液。将残余物溶解于thf(30ml)中,且将该溶液缓慢添加至nh4oh溶液(10ml/水(40ml))中。在室温下搅拌悬浮液1小时,随后浓缩。用水(50ml)稀释悬浮液(约10ml),且将固体过滤,用水洗涤且进行空气干燥,得到2-甲基-2-(3-甲基-4-硝基-1h-吡唑-1-基)丙酰胺(2.1g,92%产率)。lc-ms m/z:213.2(m h
)。
[0524]
通用方法h:铃木偶联反应:
[0525]
中间物d1:1-(3-环丙基-4-硝基苯基)-4-甲基哌嗪。
[0526][0527]
用k3po4(43g,200mmol)处理1-(3-溴-4-硝基苯基)-4-甲基哌嗪(a21,20g,67mmol)和环丙基硼酸(8.6g,100mmol)于甲苯:h2o(9:1)(200ml)中的混合物,且用氮气吹扫反应混合物20分钟。将三环己基膦(3.7g,13mmol)和pd(oac)2(2.2g,10mmol)添加至反应混合物中,且随后在100℃下搅拌反应混合物5小时。用水(100ml)稀释反应物,且用etoac(3
×
200ml)萃取溶液。合并的有机萃取物用盐水(50ml)洗涤,经无水na2so4干燥,过滤且浓缩。通过硅胶柱层析(0-80%etoac/己烷,15份柱体积(cv))纯化粗产物,获得呈黄色固体状的1-(3-环丙基-4-硝基苯基)-4-甲基哌嗪(12g,69%产率)。1h nmr(400mhz,dmso-d6):δ7.89(d,
j=9.3hz,1h),6.85(dd,j=2.4和9.4hz 1h),6.55(s,1h),3.36(m,4h),2.45(m,1h),2.40(m,4h),2.20(s,3h),0.94(m,2h),0.75(m,2h);lc-ms(esi)m/z:261.3(m h
)。
[0528]
中间物d12:1-甲基-4-(4-硝基-3-乙烯基苯基)哌嗪。
[0529][0530]
室温下用k2co3(42g,301mmol)处理1-(3-溴-4-硝基苯基)-4-甲基哌嗪(a21,30g,100mmol)和三氟乙烯基硼酸钾(20g,150mmol)于dmso(210ml)中的混合物,且用氮气吹扫反应混合物15分钟。将pdcl2(dppf)(3.7g,5.0mmol)添加至反应混合物中,且在80℃下搅拌反应混合物3小时。反应混合物用冷水(300ml)稀释,且溶液用etoac(3
×
250ml)萃取。合并的有机萃取物用盐水(200ml)洗涤,经无水na2so4干燥,过滤且在减压下浓缩。通过硅胶柱层析(0-80%etoac/己烷,10份柱体积(cv))纯化粗产物,获得呈黄色固体状的1-甲基-4-(4-硝基-3-乙烯基苯基)哌嗪(20g,81%产率)。1h nmr(400mhz,dmso-d6):δ7.96(d,j=9.2hz,1h),7.21(m,1h),6.98(m,2h),5.77(t,j=17.2hz,1h),5.41(d,j=11.2hz,1h),3.44(t,j=4.8hz,4h),2.42(t,j=4.8hz,4h),2.21(s,3h);lc-ms(esi)m/z:247.3(m h
)。
[0531]
使用上述通用方法h,制备表d的以下中间物。
[0532]
表d.
[0533]
[0534]
[0535]
[0536]
[0537]
[0538][0539]
通用方法i:还原
[0540]
(a)中间物e1:2-环丙基-4-(4-甲基哌嗪-1-基)苯胺。
[0541][0542]
于0℃用nh4cl(73g,14mmol)处理1-(3-环丙基-4-硝基苯基)-4-甲基哌嗪(d1,12g,46mmol)于meoh(60ml)中的溶液,且于0℃搅拌反应混合物10分钟。在冰水浴中,将锌粉(30g,459mmol)缓慢添加(内部温度提高至20℃)至反应混合物中。在15分钟搅拌之后,使反应混合物升温至室温,且使其在室温下剧烈搅拌16小时。混合物通过过滤,且用thf(500ml)洗涤。在减压下浓缩滤液,得到呈深棕色粘性固体状的2-环丙基-4-(4-甲基哌嗪-1-基)苯胺(10g,95%)。1h nmr(400mhz,dmso-d6):δ6.52(m,2h),6.43(d,j=2.0hz,1h),4.52(brs,2h),2.88(m,4h),2.42(m,4h),2.20(s,3h),1.65(m,1h),0.813(m,2h),0.47(m,2h);lc-ms(esi)m/z:213.2(m h
)。
[0543]
(b)中间物e11:2-乙基-4-(4-甲基哌嗪基-1-基)苯胺。
[0544][0545]
在氮气氛围下用pd/c(20g,10%w/w,50%水分)处理1-甲基-4-(4-硝基-3-乙烯基苯基)哌嗪(d12,20g,81mmol)于etoac(200ml)中的溶液,且随后在氢气气囊压力下于室温搅拌混合物3小时。在通用处理之后,获得呈棕色粘稠固体状的2-乙基-4-(4-甲基哌嗪-1-基)苯胺(16g,90%产率)。1h nmr(400mhz,dmso-d6):δ6.61(s,1h),6.52(m,2h),4.25(brs,
2h),2.89(t,j=4.4hz,4h),2.41(m,6h),2.19(s,3h),1.09(t,j=7.6hz,3h);lc-ms(esi)m/z:219.3(m h
)。
[0546]
使用上述通用方法i(a)和i(b),制备表e的以下中间物。
[0547]
表e.
[0548]
[0549]
[0550]
[0551]
[0552]
[0553]
[0554]
[0555]
[0556]
[0557]
[0558]
[0559][0560]
偶联方法j(a)和boc基团的去保护:
[0561]
中间物f1:n-(3-氨基丙基)环丁烷甲酰胺盐酸盐。
[0562][0563]
用饱和nahco3(水溶液)(100ml)处理(3-氨基丙基)氨基甲酸叔丁酯(5.0g,29mmol)于etoac(100ml)中的溶液,且用环丁基甲酰氯(3.6ml,32mmol)逐滴处理该两相混合物,且在室温下搅拌18小时。该混合物用etoac(3
×
50ml)萃取,且合并的有机物经无水na2so4干燥且浓缩,得到呈白色固体状的(3-(环丁烷甲酰氨基)丙基)氨基甲酸叔丁酯(5.6g,76%产率)。1h nmr(dmso-d6,500mhz):δ7.57(s,1h),6.73(s,1h),2.85-3.00(m,5h),2.04-2.12(m,2h),1.97(m,2h),1.86(m,1h),1.69-1.76(m,1h),1.47(m,1h),1.36(s,9h);ms(esi)m/z:279.2(m h
)。
[0564]
用1,4-二恶烷中的4n hcl(27ml,0.11mol)逐滴处理(3-(环丁烷甲酰氨基)丙基)氨基甲酸叔丁酯(5.6g,0.022mol)于meoh(100ml)中的溶液,且在室温下搅拌3小时。将溶液浓缩至干燥,再悬浮于meoh中且再次浓缩(此操作两次),得到呈白色固体状的n-(3-氨基丙基)环丁烷甲酰胺盐酸盐(4.7g,100%产率)。1h nmr(dmso-d6,500mhz):δ7.96(brs,3h),7.87(brm,1h),3.09(m,2h),2.96(m,1h),2.74(m,2h),2.13(m,2h),1.5-2.0(m,6h);ms(esi)m/z:140.2(m h
)。
[0565]
偶联方法j(b)和boc基团的去保护:
[0566]
中间物f2:n-(3-氨基丙基)-3,3-二氟-n-甲基环丁烷-1-甲酰胺tfa盐。
[0567][0568]
用hobt(0.52g,2.7mmol),随后edc(0.52g,2.7mmol)处理3,3-二氟环丁烷-1-甲酸
(0.27g,2.0mmol)和diea(1.6ml,9.0mmol)于dcm(5ml)中的溶液,且在室温下搅拌5分钟。添加(3-(甲基氨基)丙基)氨基甲酸叔丁酯(0.34g,1.8mmol)于dcm(5ml)中的溶液,且在室温下搅拌该混合物15小时。将混合物用盐水(30ml)淬灭,且用dcm(3
×
25ml)萃取。合并的有机物经无水na2so4干燥,过滤且浓缩。通过硅胶柱层析(0-10%meoh/dcm,15份柱体积(cv))纯化粗产物,得到(3-(3,3-二氟-n-甲基环丁烷-1-甲酰氨基)丙基)氨基甲酸叔丁酯(0.54g,98%产率),将其溶解于dcm(6ml)中,且随后用tfa(0.18ml)处理。室温下搅拌溶液3小时,且随后浓缩获得n-(3-氨基丙基)-3,3-二氟-n-甲基环丁烷-1-甲酰胺tfa盐(100%产率)。
[0569]
使用上述通用方法j,制备表f的以下中间物。
[0570]
表f.
[0571][0572][0573]
实施例l1:2-氯-5-环丙基-4-(甲磺酰基)嘧啶。
[0574][0575]
用k3po4(66.7g,315mmol)处理5-溴-2-氯-6-(甲硫基)嘧啶(25.0g,105mmol)和环丙基硼酸(13.7g,158mmol)于甲苯:h2o(9:1)(650ml)中的悬浮液。用氮气吹扫反应混合物20分钟,且随后添加三环己基膦(5.9g,21mmol)和pd(oac)2(2.35g,10.50mmol)。于90℃搅拌反应混合物16小时。将反应混合物用水(200ml)稀释,且用etoac(3
×
300ml)萃取。合并的
有机萃取物用盐水(200ml)洗涤,经无水na2so4干燥,过滤且在减压下浓缩。通过硅胶柱层析法(0%-10%etoac/己烷)纯化粗产物,获得呈黄色油状的2-氯-5-环丙基-4-(甲硫基)嘧啶(14.0g,66%产率)。1h nmr(400mhz,dmso-d6):δ7.92(s,1h),2.58(s,3h),1.67(m,1h),1.03(m,2h),0.67(m,2h);ms(esi)m/z:201.0(m h
)。
[0576]
于0℃用m-cpba(4.8g,28mmol)处理2-氯-5-环丙基-6-(甲硫基)嘧啶(4.0g,20mmol)于dcm(60ml)中的溶液。使反应混合物升温至室温且搅拌3小时。反应混合物用饱和nahco3水溶液(2
×
40ml)洗涤。有机层经无水na2so4干燥,过滤且在减压下浓缩,获得呈黄色固体状的2-氯-5-环丙基-6-(甲磺酰基)嘧啶(3.6g,86%产率)。1h nmr(400mhz,dmso-d6):δ8.57(s,1h),2.89(s,3h),2.16(m,1h),1.16(m,2h),0.93(m,2h);ms(esi)m/z:217.0(m h
)。
[0577]
实施例l2:4-氯-2-(甲硫基)-5-(三氟甲基)嘧啶。
[0578][0579]
于0℃用zncl2(1.0n于乙醚中)(555ml,0.56mol)逐滴处理2,4-二氯-5-(三氟甲基)嘧啶(100g,0.46mol)于乙醚(2l)中的溶液,且搅拌反应混合物2小时。于0℃添加硫代甲醇钠(49g,0.94mol),且使反应混合物升温至室温且搅拌48小时。在冰水浴中,用2n hcl淬灭反应混合物,且接着用et2o(3
×
500ml)萃取溶液。合并的有机萃取物用水(500ml)洗涤,经无水na2so4干燥,过滤且于35℃在减压下浓缩,获得呈无色液体状的4-氯-2-(甲硫基)-5-(三氟甲基)嘧啶(100g,95%产率)。1h nmr(400mhz,dmso-d6):δ9.01(s 1h),2.62(s 3h)。
[0580]
通用方法k:取代反应:
[0581]
中间物k20:n-(3-((2-(甲硫基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺
[0582][0583]
将4-氯-2-(甲硫基)-5-(三氟甲基)嘧啶(l2,0.50g,2.1mmol)于dmf(10ml)中的溶液冷却至0℃,用n-(3-氨基丙基)环丁烷甲酰胺hcl盐(f1,0.50g,2.4mmol)和diea(1.1ml,6.4mmol)于dmf(10ml)中的悬浮液处理,且使其缓慢升温至室温且搅拌18小时。将混合物浓缩至干燥,且通过硅胶柱层析(15-40%etoac/己烷,20份柱体积(cv))纯化残余物,得到呈白色固体状的n-(3-((2-(甲硫基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(0.52g,70%产率)。ms(esi)m/z:349.2(m h
)。
[0584]
使用上述通用方法k,制备表g的以下中间物。
[0585]
表g.
[0586]
[0587]
[0588][0589]
制备中间物k21:n-(3-((2-氯-5-(三氟甲基)吡啶-4-基)氨基)丙基)环丁烷甲酰胺
[0590][0591]
用三乙胺(165ml,115mmol)处理(3-氨基丙基)氨基甲酸叔丁酯(100g,57mmol)于dcm(1.5l)中的溶液。将混合物冷却至0℃,且逐滴添加环丁基甲酰氯(68g,57mmol)。在室温
下搅拌反应混合物4小时,且接着用水(1l)稀释。用dcm(2
×
1l)萃取溶液。合并的有机萃取物用盐水(500ml)洗涤,经无水na2so4干燥,过滤且在减压下浓缩,获得呈白色固体状的(3-(环丁烷甲酰氨基)丙基)氨基甲酸叔丁酯(140g,95%产率)。1h nmr(400mhz,dmso-d6):δ7.60(s,1h),6.7(s,1h),3.07(m,2h),2.97(m,1h),2.89(m,2h),2.10(m,2h),1.98(m,2h),1.85(m,1h),1.74(m,1h),1.46(m,2h),1.37(s,9h);ms(esi)m/z:257.4(m h
)。
[0592]
于0℃用1,4-二恶烷中的4n hcl(426ml)处理(3-(环丁烷甲酰氨基)丙基)氨基甲酸叔丁酯(140g,55mmol)于dcm(1.4l)中的溶液,且在室温下搅拌反应混合物16小时。在减压下浓缩溶液,获得hcl盐。依序使用二乙醚(500ml)和戊烷(500ml)湿磨该盐,过滤固体且在真空下干燥,获得呈白色固体状的n-(3-氨基丙基)环丁烷甲酰胺盐酸盐(105g,99%产率)。1h nmr(400mhz,dmso-d6):δ8.00(m,3h),7.90(brs,1h),3.15(m,2h),3.08(m,1h),2.73(m,2h),2.12(m,2h),1.97(m,2h),1.88(m,1h),1.76(m,3h)。
[0593]
用cs2co3(2.6g,8.1mmol)处理2-氯-4-碘-5-(三氟甲基)吡啶(1.0g,3.2mmol)和n-(3-氨基丙基)环丁烷甲酰胺盐酸盐(0.68g,3.58mmol)于甲苯(10ml)中的溶液,且在室温下添加混合物。反应混合物用氮气吹扫15分钟,且接着添加pdcl2(dppf)dcm复合物(0.26g,0.32mmol)。在80℃下加热反应混合物16小时,且接着冷却至室温。反应混合物用水(20ml)稀释,且用dcm(3
×
10ml)萃取。合并的有机萃取物经无水na2so4干燥,过滤且在减压下浓缩。粗产物通过硅胶柱层析(0-3%dcm/meoh,15份柱体积(cv))纯化,获得呈黄色固体状的n-(3-((2-氯-5-(三氟甲基)吡啶-4-基)氨基)丙基)环丁烷甲酰胺(0.2g,18%产率)。1h nmr(400mhz,dmso-d6):δ8.18(s,1h),7.7(brs,1h),6.9(t,j=5.8hz,1h),6.83(s,1h),3.26(m,2h),3.08(m,2h),2.97(m,1h),2.11(m,2h),2.00(m,2h),1.87(m,1h),1.75(m,1h),1.58(m,2h);ms(esi)m/z:336.1(m h
)。
[0594]
通用方法m:氧化
[0595]
中间物m1:n-(3-((2-(甲基亚磺酰基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺。
[0596][0597]
将n-(3-((2-(甲硫基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(k20,0.30g,0.86mmol)于dcm(4.3ml)中的溶液冷却至0℃,用mcpba(0.23g,1.0mmol)处理,且随着冷却槽时间截止而升温至室温。在室温下搅拌混合物3小时。(出现约9:1的亚砜(主要)和砜(次要)的混合物)。用饱和nahco3饱和溶液淬灭混合物,分离有机层,经无水na2so4干燥,过滤且浓缩至干燥,得到呈无色油状的n-(3-((2-(甲基亚磺酰基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(0.314g,100%产率),其在静置后凝固。ms(esi)m/z:365.2(m h
)。
[0598]
使用上述通用方法m,制备表h的以下中间物。
[0599]
表h.
[0600][0601]
通用方法n:取代反应a:
[0602]
实施例1:n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺。
[0603][0604]
用1,4-二恶烷中的4n hcl(0.060ml,0.24mmol)处理2-乙基-4-(4-甲基哌嗪-1-基)苯胺(e11,0.053g,0.24mmol)、n-(3-((2-(甲基亚磺酰基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烯-甲酰胺(m1,0.088g,0.24mol)和若干分子筛于dmf(1.2ml)中的混合物,紧密封盖且在80℃加热15小时。将混合物冷却至室温,且在高度真空下浓缩至干燥。通过硅胶柱层析(3-10%meoh/dcm,11份柱体积(cv))纯化粗产物,获得呈淡色固体状的n-(3-((2-((2-乙基-4-(4-甲基哌嗪-1-基)苯基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(0.068g,54%产率)。1h nmr(400mhz,dmso-d6):δ8.60(s,1h),8.02(s,1h),7.57(brs,1h),7.13(d,j=7.6hz,1h),6.90(t,1h),6.77(d,j=2.3hz,1h),6.73(dd,j=2.8和j=8.8hz,1h),3.26(m,2h),3.10(brs,4h),2.93(m,3h),2.55(m,2h),2.45(brs,4h),2.25(s,3h),2.11(q,2h),2.00(m,2h),1.88(m,1h),1.75(m,1h),1.54(brs,2h),1.07(t,j=7.6hz,3h);ms(esi)m/z:520.3(m h
)。
[0605]
通用方法o:取代反应b:
[0606]
实施例n-boc-21:n-(3-((2-((3-甲基-1-(哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺。
[0607][0608]
用少量分子筛,随后用1,4-二恶烷中的4n hcl(0.086ml,0.35mmol)处理4-(4-氨基-3-甲基-1h-吡唑-1-基)哌啶-1-甲酸叔丁酯(e44,0.097g,0.35mol)和n-(3-((2-(甲基亚磺酰基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(m1,0.13g,0.35mol)于无水dmf(1.7ml)中的混合物,紧密封盖且在80℃加热16小时。将混合物冷却至室温,且接着在高度真空下移除溶剂。通过硅胶柱层析(2-7%meoh/dcm,18份柱体积(cv))纯化残余物,获得呈浅绿色非晶形固体状的4-(4-((4-((3-(环丁烷甲酰氨基)丙基)氨基)-5-(三氟甲基)嘧啶-2-基)氨基)-3-甲基-1h-吡唑-1-基)哌啶-1-甲酸叔丁酯(0.16g,81%产率)。1h nmr(400mhz,dmso-d6):δ8.93(brs,1h),8.08(s,1h),7.86(brs,1h),7.63(brm,1h),7.06(brm,1h),4.20(brm,1h),4.03(m,2h),3.35(m,3h),2.6-3.0(m,7h),1.5-2.2(m,12h),1.39(s,9h);ms(esi)m/z:581.4(m h
)。
[0609]
通用方法p:boc基团的去保护
[0610]
实施例21:n-(3-((2-((3-甲基-1-(哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺。
[0611][0612]
用1,4-二恶烷中的4n hcl(0.7ml,2.8mmol)处理4-(4-((4-((3-(环丁烷甲酰氨基)丙基)氨基)-5-(三氟甲基)嘧啶-2-基)氨基)-3-甲基-1h-吡唑-1-基)哌啶-1-甲酸叔丁酯(n-boc-21,0.16g,81%产率)于meoh(2ml)中的溶液,且在室温下搅拌5小时。将反应混合物浓缩至干燥,且将残余物溶解于meoh/dcm(1:1)中。将该溶液用过量mp-碳酸酯树脂处理且涡旋1小时。树脂通过过滤移除,用meoh冲洗且浓缩滤液,获得呈灰白色非晶形固体状的n-(3-((2-((3-甲基-1-(哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(0.12g,86%产率)。1h nmr(400mhz,dmso-d6):δ8.95(s,1h),8.08(s,1h),7.85(s,1h),7.67(t,j=5.7hz,1h),7.06(s,1h),4.11(brs,1h),3.00-3.15(m,5h),2.66(t,j=12.2hz,2h),2.06-2.11(m,5h),1.90-2.02(m,5h),1.68-1.89(m,5h),1.62(t,j=6.9hz,2h)。(nh质子缺少);ms(esi)m/z:481.4(m h
)。
[0613]
通用方法q:还原烷基化:
[0614]
实施例22:n-(3-((2-((1-(1-异丙基哌啶-4-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺。
[0615][0616]
用氰基硼氢化钠(0.013g,0.21mol),随后用催化性乙酸(1滴)处理n-(3-((2-((3-甲基-1-(哌啶-4-基)-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(21,0.050g,0.1mmol)和丙酮(0.25ml,3.40mmol)于meoh(0.5ml)中的溶液,且在室温下搅拌15小时。将混合物用饱和nahco3饱和溶液稀释,用etoac(3
×
10ml)萃取。合并的有机物用盐水(20ml)洗涤,经无水na2so4干燥且浓缩至干燥。通过硅胶柱层析(4-15%(10%nh4oh/meoh)/dcm,25份柱体积(cv))纯化粗产物,得到呈白色固体状的n-(3-((2-((1-(1-异丙基哌啶-4-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(0.028g,50%产率)。1h nmr(400mhz,dmso-d6):δ8.92(s,1h),8.08(s,1h),7.85(s,1h),7.64(s,1h),7.05(s,1h),3.93(br s,1h),3.37(brs,1h),2.61-2.98(m,6h),2.22(t,j=11.7hz,2h),2.04-2.09(m,5h),1.67-2.03(m,9h),1.55-1.66(m,2h),0.96(d,j=6.6hz,6h);ms(esi)m/z:523.4(m h
)。
[0617]
使用以上通用方法n、o、p和q,制备以下表i的化合物。
[0618]
表i.
[0619]
[0620]
[0621]
[0622]
[0623]
[0624][0625]
制备实施例30:n-(3-((2-((1-(2-氰基丙-2-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺
[0626][0627]
用tea(60mg,0.60mmol)处理n-(3-((2-((1-(1-氨基-2-甲基-1-桥氧基丙-2-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(26,0.12g,0.25mmol)和2,4,6-三丙基-1,3,5,2,4,6-三氧杂三磷杂环己烷(trioxatriphosphinane)2,4,6-三氧化物(0.317g,0.50mmol)于etoac(40ml)中的混合物。在室温下搅拌反应混合物24小时。用饱和nahco3溶液(40ml)淬灭溶液,且用etoac(3
×
20ml)萃取。合并的有机萃取物用盐水洗涤,经无水na2so4干燥,过滤,在减压下浓缩。通过急骤柱层析(etoac/dcm)纯化粗产物,得到n-(3-((2-((1-(2-氰基丙-2-基)-3-甲基-1h-吡唑-4-基)氨基)-5-(三氟甲基)嘧啶-4-基)氨基)丙基)环丁烷甲酰胺(0.036g,31%产率)。1h nmr(400mhz,dmso-d6):δ9.17(brs,1h),8.14(s,2h),7.64(s,1h),7.21(brs,1h),3.39(m,2h),3.03(s,2h),2.95(brs,1h),2.17(s,3h),2.08(m,2h),1.95-2.00(m,2h),1.91(s,6h),1.85(m,1h),1.72(m,1h),1.62(s,2h);ms(esi)m/z:465.2(m h
)。
[0628]
制备实施例31:n-(3-((2-((4-甲基-6-(4-甲基哌嗪-1-基)吡啶-3-基)氨基)-5-(三氟甲基)吡啶-4-基)氨基)丙基)环丁烷甲酰胺
[0629][0630]
在室温下用cs2co3(0.58g,1.78mmol)处理n-(3-((2-氯-5-(三氟甲基)吡啶-4-基)氨基)丙基)环丁烷甲酰胺(k21,0.3g,0.89mmol)和4-甲基-6-(4-甲基哌嗪-1-基)吡啶-3-胺(e39,0.2g,0.98mmol)于1,4-二恶烷(10ml)中的溶液。反应混合物用氮气吹扫15分钟,且接着添加x-phos(0.1g,0.17mmol)和pd2(dba)3(0.081g,0.08mmol)。反应混合物在90℃下加热16小时,且接着冷却至室温。反应混合物用水(5ml)稀释,且用dcm(3
×
10ml)萃取。合并的有机萃取物经无水na2so4干燥,过滤且在减压下浓缩。通过硅胶柱层析(0-5%dcm/meoh,15份柱体积(cv))纯化所得粗产物,得到呈棕色固体状的n-(3-((2-((4-甲基-6-(4-甲基哌嗪-1-基)吡啶-3-基)氨基)-5-(三氟甲基)吡啶-4-基)氨基)丙基)-环丁烷甲酰胺(0.08g,19%产率)。1hnmr(400mhz,dmso-d6):δ8.15(s,1h),7.96(s,1h),7.86(s,1h),7.65(brs,1h),6.73(s,1h),5.92(brs,1h),5.68(s,1h),3.44(brs,4h),3.06(m,4h),2.41(brs,4h),2.23(s,3h),2.10(brs,5h),2.00(m,2h),1.91(s,1h),1.88(m,1h),1.75(m,1h),1.60(m,2h);ms(esi)m/z:506.4(m h
)。
[0631]
实施例31.ulk1.2的生物化学分析
[0632]
使用连续地监测atp水解依赖型nadh氧化的偶联丙酮酸激酶/乳酸脱氢酶分析,以光谱方式测定ulk1激酶的活性(例如schindler等人.science(2000)289:1938-1942)。在384孔板(100μl最终体积)中使用含19nm ulk1(eurofins目录号14-959)、0.25mg/ml髓鞘碱性蛋白、1.5个单位丙酮酸激酶、2.1个单位乳酸脱氢酶、1mm丙酮酸磷酸烯醇、0.28mm nadh和1mm atp的分析缓冲液(100mm tris,ph 7.5、15mm mgcl2、0.5mm dtt、0.1%辛基葡萄糖苷、0.002%(w/v)bsa和0.002%triton x-100)进行分析。通过添加经连续稀释的测试化合物(最终分析浓度为1%dmso)来测量ulk1抑制。于30℃在多模微孔板检测仪(biotek)上,连续地监测340nm处吸光值的减少历时6小时。使用2-3小时的时间范围计算反应速率。使用对照将各浓度下化合物的反应速率转化成抑制百分比(也即,不与测试化合物反应且与已知抑制剂反应),且通过使用prism(graphpad软件)将四参数s形曲线拟合至数据来计算ic
50
值。
[0633]
ulk1蛋白序列(具有n端his标签的残基1-314;seq.id no:1)
[0634]
msyyhhhhhhdydipttenlyfqgamdpffmepgrggtetvgkfefsrkdlighgafavvfkgrhrekhdlevavkcinkknlaksqtllgkeikilkelkhenivalydfqemansvylvmeycnggdladylhamrtlsedtirlflqqiagamrllhskgiihrdlkpqnillsnpagrranpnsirvkiadfgfarylqsnmmaatlcgspmymapevimsqhydgkadlwsigtivyqcltgkapfqasspqdlrlfyeknktlvptipretsaplrqlllallqrnhkdrmdfdeffhhpfldaspsvrksppvpvpsypssgsgssssssstshlas
[0635]
实施例32.ulk1.3的生物化学分析
[0636]
使用连续地监测atp水解依赖型nadh氧化的偶联丙酮酸激酶/乳酸脱氢酶分析,以光谱方式测定ulk1激酶的活性(例如schindler等人.science(2000)289:1938-1942)。在384孔板(100μl最终体积)中,使用含0.1nm ulk1(来自beryllium)、0.075mm肽基质(yanwlaasiyldgkkk(seq id no:5))、1.5个单位丙酮酸激酶、2.1个单位乳酸脱氢酶、1mm丙酮酸磷酸烯醇、0.28mm nadh和1mm atp的分析缓冲液(100mm tris,ph 7.5、15mm mgcl2、0.5mm dtt、0.004%(w/v)bsa和0.004%triton x-100)进行分析。通过添加经连续稀释的测试化合物(最终分析浓度为1%dmso)来测量ulk1抑制。在30℃下,在多模微孔板检测仪(biotek)上,连续地监测340nm处吸光值的减少历时6小时。使用2-3小时的时间范围计算反应速率。使用对照将各浓度下化合物的反应速率转化成抑制百分比(也即,不与测试化合物反应且与已知抑制剂反应),且在prism(graphpad软件)中使用软件例程计算ic
50
值。
[0637]
ulk1蛋白序列(残基1-283;seq.id no:2)
[0638]
mepgrggtetvgkfefsrkdlighgafavvfkgrhraahdlevavkcinkknlaksqtllgkeikilkelkhenivalydfqemansvylvmeycnggdladylhamrtlsedtirlflqqiagamrllhskgiihrdlkpqnillsnpagrranpnsirvkiadfgfarylqsnmmaatlcgspmymapevimsqhydgkadlwsigtivyqcltgkapfqasspqdlrlfyeknktlvptipretsaplrqlllallqrnhkdrmdfdeffhhpfldasps
[0639]
实施例33.ulk2的生物化学分析
[0640]
使用连续地监测atp水解依赖型nadh氧化的偶联丙酮酸激酶/乳酸脱氢酶分析,以光谱方式测定ulk2激酶的活性(例如schindler等人.science(2000)289:1938-1942)。在384孔板(100μl最终体积)中,使用含9.7nm ulk2(eurofins目录号14-772)、0.25mg/ml髓鞘碱性蛋白、1.5个单位丙酮酸激酶、2.1个单位乳酸脱氢酶、1mm丙酮酸磷酸烯醇、0.28mm nadh和1mm atp的分析缓冲液(100mm tris,ph 7.5、15mm mgcl2、0.5mm dtt、0.1%辛基葡萄糖苷、0.002%(w/v)bsa和0.002%triton x-100)进行分析。通过添加经连续稀释的测试化合物(最终分析浓度为1%dmso)来测量ulk2抑制。在30℃下,在多模微孔板检测仪(biotek)上,连续地监测340nm处吸光值的减少历时6小时。使用2-3小时的时间范围计算反应速率。使用对照将各浓度下化合物的反应速率转化成抑制百分比(也即,不与测试化合物反应且与已知抑制剂反应),且通过使用prism(graphpad软件)将四参数s形曲线拟合至数据来计算ic
50
值。
[0641]
ulk2蛋白序列(具有n端gst和his标签的残基1-306;seq.id no:3)
[0642]
mspilgywkikglvqptrllleyleekyeehlyerdegdkwrnkkfelglefpnlpyyidgdvkltqsmaiiryiadkhnmlggcpkeraeismlegavldirygvsriayskdfetlkvdflsklpemlkmfedrlchktylngdhvthpdfmlydaldvvlymdpmcldafpklvcfkkrieaipqidkylksskyiawplqgwqatfgggdhppksdlevlfqgpefmevvgdfeyskrdlvghgafavvfrgrhrqktdwevaiksinkknlsksqillgkeikilkelqhenivalydvqelpnsvflvmeycnggdladylqakgtlsedtirvflhqiaaamrilhskgiihrdlkpqnillsyanrrkssvsgirikiadfgfarylhsnmmaatlcgspmymapevimsqhydakadlwsigtviyqclvgkppfqanspqdlrmfyeknrslmpsipretspylanlllgllqrnqkdrmdfeaffshpfleqgpvkkscpvpvpmysgsvsgsscgsspscrfashhhhhh
[0643]
表1.由表i中的示例性化合物进行的ulk1和ulk2激酶的生物化学活性的抑制.
[0644]
实例(化合物)编号ulk1.2ulk1.3ulk2.21
2
ꢀꢀ
3 4 5 6 7 8 9 10 11
ꢀꢀ
12 13 14 15
ꢀꢀ
16 17
ꢀꢀ
18
ꢀꢀ
19 20 21 22
ꢀꢀ
23 24
ꢀꢀ
25
ꢀꢀ
26 27 28 29
ꢀꢀ
30 31
ꢀꢀ
[0645]
对于表1,“ ”是指大于1nm且小于或等于25nm的ic
50
;“ ”是指大于25nm且小于或等于100nm的ic
50
;“ ”是指大于100nm且小于或等于500nm的ic
50
;且“ ”是指大于500nm且小于20,000nm的ic
50
。
[0646]
实施例34.ulk激酶基质atg13蛋白的细胞抑制
[0647]
在用ulk抑制剂和曲美替尼组合处理后突变kras a549细胞的patg13含量
[0648]
将a549(kras突变)人类肺癌细胞(6,000个细胞/孔)添加至经组织培养物处理384孔板中的补充有10%标准胎牛血清(invitrogen,carlsbad,ca)、100个单位/ml青霉素g和100μg/ml链霉素的50μl预温热dmem培养基中,且使其在37℃、5%co2和95%湿度下生长过夜。第二天,将作为对照的含有曲美替尼或dmso的10μl培养基添加至孔中。所述孔中曲美替
尼的最终浓度为250nm。添加测试化合物的剂量反应(0.6μl/孔)。将dmso(0.6μl)添加至对照孔中。短暂地摇晃所述板以混合所述孔,且随后在37℃下孵育过夜。次日,抽吸培养基,且用杜尔贝科氏磷酸盐缓冲盐水(dulbecco'sphosphate buffered saline)(gibco)洗涤细胞。4℃在摇晃下,使用含有halt磷酸酶和蛋白酶抑制剂(pierce,rockford,il)以及磷酸酶抑制剂混合液2(sigma,st.louis,mo)的mper溶解缓冲液(pierce,rockford,il)溶解细胞10分钟。
[0649]
通过elisa方法测量磷酸丝氨酸318atg13(patg13)的细胞含量。使用全atg13抗体(cell signaling目录号13273)以涂布孔。将所述板在4℃孵育过夜,且用elisa洗涤缓冲液(biolegend目录号421601)洗涤。随后,在室温用分析稀释剂(biolegend目录号421203)封闭所述孔1小时。用elisa洗涤缓冲液洗涤所述板孔。将细胞溶解物添加至孔中,且在室温下孵育2小时。用elisa洗涤缓冲液洗涤所述板孔。将用生物素标记的ps318-atg13抗体(rockland immunochemicals目录号600-401-c49)稀释于分析稀释剂中并添加至各孔中,且在室温下孵育1小时。用elisa洗涤缓冲液洗涤所述板孔。将连接至辣根过氧化酶的链霉亲和素(thermo fisher目录号21140)稀释于分析稀释剂中并添加至各孔中,且在室温下孵育1小时。用elisa洗涤缓冲液洗涤所述板孔。将高敏感度tmb基质(biolegend目录号421101)添加至各孔中,且在室温下孵育20分钟。用2n硫酸终止反应。在测量450nm和540nm处的吸光度(背景)的微孔板检测仪上分析所述板。对于各孔,通过首先自在450nm处的吸光度减去在540nm处的背景吸光度来计算信号。随后,从测试孔减去空白组孔的在450nm处的背景校正吸光度。将数据与对照孔比较以测定atg13磷酸化%。使用graphpad prism以计算ic
50
值。
[0650]
实施例35.用ulk抑制剂和曲美替尼组合处理后突变kras miapaca-2细胞的patg13含量
[0651]
将miapaca-2人类胰脏癌细胞(10000个细胞/孔)添加至于384孔经组织培养物处理的所述板中的补充有10%标准胎牛血清(invitrogen,carlsbad,ca)、100个单位/ml青霉素g、100μg/ml链霉素和2.5%马血清的50μl预温热dmem培养基中,且使其在37℃、5%co2和95%湿度下生长过夜。第二天,将作为对照的含有曲美替尼或dmso的10μl培养基添加至孔中。所述孔中的曲美替尼最终浓度为250nm。添加测试化合物的剂量反应(0.6μl/孔)。将dmso(0.6μl)添加至对照孔中。短暂地摇晃所述板以混合孔,且随后在37℃下孵育过夜。次日,抽吸培养基,且用杜尔贝科氏磷酸盐缓冲盐水(gibco)洗涤细胞。在4℃摇晃的情况下,使用含有halt磷酸酶和蛋白酶抑制剂(pierce,rockford,il)以及磷酸酶抑制剂混合液2(sigma,st.louis,mo)的mper溶解缓冲液(pierce,rockford,il)溶解细胞10分钟。
[0652]
通过elisa方法测量磷酸丝氨酸318atg13(patg13)的细胞含量。使用全atg13抗体(cell signaling目录号13273)包被所述孔。将所述板在4℃孵育过夜,且用elisa洗涤缓冲液(biolegend目录号421601)洗涤。随后,在室温下用分析稀释剂(biolegend目录号421203)封闭所述孔1小时。用elisa洗涤缓冲液洗涤所述板孔。将细胞溶解物添加至孔中,且在室温下孵育2小时。用elisa洗涤缓冲液洗涤所述板孔。将用生物素标记的ps318-atg13抗体(rockland immunochemicals目录号600-401-c49)稀释于分析稀释剂中且添加至各孔中,且在室温下孵育1小时。用elisa洗涤缓冲液洗涤所述板孔。将连接至辣根过氧化酶的链霉亲和素(thermo fisher目录号21140)稀释于分析稀释剂中且添加至各孔中,且在室温下
孵育1小时。用elisa洗涤缓冲液洗涤所述板孔。将高敏感度tmb基质(biolegend目录号421101)添加至各孔中,且在室温下孵育20分钟。用2n硫酸终止反应。在测量在450nm和540nm处吸光度(背景)的微孔板检测仪上分析所述板。对于各孔,通过首先从在450nm处的吸光度减去在540nm处的背景吸光度来计算信号。随后,从测试孔减去空白组孔在450nm处的背景校正吸光度。将数据与对照孔比较以测定atg13磷酸化%。使用graphpad prism以计算ic
50
值。
[0653]
表2.由来自表i的示例性化合物进行的突变ras细胞系中的ulk激酶抑制。
[0654][0655]
对于表2,“ ”是指大于10nm且小于或等于100nm的ic
50
;“ ”是指大于100nm且小于或等于300nm的ic
50
;“ ”是指大于300nm且小于或等于600nm的ic
50
。
[0656]
实施例36.lrrk2的生物化学分析(seq.id no.4)
[0657]
使用连续地监测atp水解依赖型nadh氧化的偶联丙酮酸激酶/乳酸脱氢酶分析,以光谱方式测定lrrk2激酶的活性(例如schindler等人.science(2000)289:1938-1942)。在384孔板(100μl最终体积)中使用含26.4nm lrrk2(thermo fisher)、0.1mm肽基质(rlgrdkyktlrqirq(seq id no:6))、1.5个单位丙酮酸激酶、2.1个单位乳酸脱氢酶、1mm丙酮酸磷酸烯醇、0.28mm nadh和1mm atp的分析缓冲液(100mm tris,ph 7.5、15mm mgcl2、0.5mm dtt、0.004%(w/v)bsa和0.004%triton x-100)进行分析。通过添加经连续稀释的测试化合物(最终分析浓度为1%dmso)来测量lrrk2抑制。在30℃于多模微孔板检测仪(biotek)上,连续地监测340nm处吸光值的减少历时6小时。使用2-3小时的时间范围计算反应速率。使用对照将各浓度化合物的反应速率转化成抑制百分比(也即,不与测试化合物反应且与已知抑制剂反应),且在prism(graphpad软件)中使用软件例程计算ic
50
值。
[0658]
lrrk2蛋白序列(残基970-2528;seq.id no:4)
[0659]
mapilgywkikglvqptrllleyleekyeehlyerdegdkwrnkkfelglefpnlpyyidgdvkltqsmaiiryiadkhnmlggcpkeraeismlegavldirygvsriayskdfetlkvdflsklpemlkmfedrlchktylngdhvthpdfmlydaldvvlymdpmcldafpklvcfkkrieaipqidkylksskyiawplqgwqatfgggdhppksdlvp
rhnqtslykkagtmhsdsisslasereyitsldlsanelrdidalsqkccisvhlehleklelhqnaltsfpqqlcetlkslthldlhsnkftsfpsyllkmscianldvsrndigpsvvldptvkcptlkqfnlsynqlsfvpenltdvvekleqlilegnkisgicsplrlkelkilnlsknhisslsenfleacpkvesfsarmnflaampflppsmtilklsqnkfscipeailnlphlrsldmssndiqylpgpahwkslnlrellfshnqisildlsekaylwsrveklhlshnklkeippeigclenltsldvsynlelrsfpnemgklskiwdlpldelhlnfdfkhigckakdiirflqqrlkkavpynrmklmivgntgsgkttllqqlmktkksdlgmqsatvgidvkdwpiqirdkrkrdlvlnvwdfagreefysthphfmtqralylavydlskgqaevdamkpwlfnikarassspvilvgthldvsdekqrkacmskitkellnkrgfpairdyhfvnateesdalakl
[0660]
rktiineslnfkirdqlvvgqlipdcyvelekiilserknvpiefpvidrkrllqlvrenqlqldenelphavhflnesgvllhfqdpalqlsdlyfvepkwlckimaqiltvkvegcpkhpkgiisrrdvekflskkrkfpknymsqyfkllekfqialpigeeyllvpsslsdhrpvielphcenseiiirlyempyfpmgfwsrlinrlleispymlsgreralrpnrmywrqgiylnwspeayclvgsevldnhpesflkitvpscrkgcillgqvvdhidslmeewfpglleidicgegetllkkwalysfndgeehqkillddlmkkaeegdllvnpdqprltipisqiapdliladlprnimlnndelefeqapefllgdgsfgsvyraayegeevavkifnkhtslrllrqelvvlchlhhpslisllaagirprmlvmelaskgsldrllqqdkasltrtlqhrialhvadglrylhsamiiyrdlkphnvllftlypnaaiiakiadygiaqyccrmgiktsegtpgfrapevargnviynqqadvysfglllydilttggriveglkfpnefdeleiqgklpdpvkeygcapwpmveklikqclkenpqerptsaqvfdilnsaelvcltrrillpknvivecmvathhnsrnasiwlgcghtdrgqlsfldlntegytseevadsrilclalvhlpvekeswivsgtqsgtllvintedgkkrhtlekmtdsvtclycnsfskqskqknfllvgtadgklaifedktvklkgaaplkilnignvstplmclsestnsternvmwggcgtkifsfsndftiqklietrtsqlfsyaafsdsniitvvvdtalyiakqnspvvevwdkkteklcglidcvhflrevmvkenkeskhkmsysgrvktlclqkntalwigtggghillldlstrrlirviynfcnsvrvmmtaqlgslknvmlvlgynrkntegtqkqkeiqscltvwdinlphevqnlekhievrkelaekmrrtsve
[0661]
表3.通过表i中展示的示例性化合物的lrrk2抑制。
[0662][0663]
对于表3,“ ”是指大于1nm且小于或等于100nm的ic
50
;“ ”是指大于100nm且小于或等于300nm的ic
50
;“ ”是指大于300nm且小于或等于600nm的ic
50
;且“ ”是指大于600nm且小于20,000nm的ic
50
。
[0664]
实施例37.活体外和活体内胰管腺癌(pdac)中的ulk抑制剂评估
[0665]
ulk抑制剂在pdac通量分析(flux assay)中加以评估,且在包括来源于trp53
lox/
、lsl-kras
g12d
、rosa-rtta
lsl
、p48cre
的原发性肿瘤的细胞的一组多种pdac细胞系中的化合物的ic
50
,将在不存在或存在曲美替尼的情况下使用集落生成2d分析和3d类器官分析来加以测定。
[0666]
采用同基因型原位模型,使用活体内pdac肿瘤中的通量报告基因,评估在单次剂量和多次剂量后的自噬流抑制。
[0667]
pdac模型中ulk抑制剂的治疗功效应,通过以下来加以评估:(i)皮下评估pdac的肿瘤动力学;(ii)在同基因型模型中,在胰脏内正位地评估pdac(植入kpc的c57黑色小鼠)的肿瘤动力学;(iii)在同基因型模型中,利用ulk抑制剂和mek抑制剂评估肿瘤生长动力学;(iv)在pdac原位模型中评估化合物;(v)在肿瘤微环境中评估组织学变化;(vi)评估ulk抑制剂抑制后肿瘤中的免疫细胞浸润变化;(vii)评估ulk抑制剂和免疫检查点阻断组合的功效。
[0668]
等效物
[0669]
尽管具体实施方案已加以论述,但上述说明书为示例性且非限制性的。本领域技术人员在审阅本说明书后,所述实施方案的许多变化形式将是显而易见的。所公开内容的全部范围应参考权利要求书及其等效物和说明书以及这类变化形式的全部范围来确定。
[0670]
除非另外指示,本说明书和权利要求书中所使用的表示成分数量、反应条件等的所有数字,在所有情况下均应理解为由术语“约”修饰。因此,除非有相反指示,本说明书和所附权利要求书中所列举的数值参数,为可根据试图获得的所需特性而变化的近似值。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。