1.本发明属于荧光探针领域,尤其涉及一种可见光驱动的纳米反应体系及其制备方法。
背景技术:
2.近几年纳米反应器得到快速发展与应用,许多化学反应都成功地在纳米反应器中完成。纳米反应器为化学反应提供了一种纳米尺度的空间,使反应受限于该纳米空间范围,通过控制纳米反应器的尺寸,材质和其他因素从而调节该化学反应。纳米反应器主要有两种,一种是在分散相中能够自组装的分子,形成有序的聚集体如:胶束、囊泡、微乳液等,在聚集体内部制备纳米材料和粒子;另外一种是天然存在或合成的分子,如沸石、层状硅酸盐、金属复合物等,利用分子的层状结构、介孔结构和孔隙作为纳米反应器。
3.羧酸盐型阴离子表面活性剂是亲水基为羧基的阴离子表面活性剂,包括高级脂肪酸的钾、钠、铵盐以及三乙醇铵盐。在水中电离后起表面活性作用的部分是脂肪酸根阴离子。
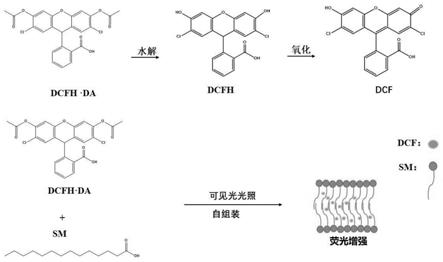
4.dcfh-da(2',7'-二氯二氢荧光素二乙酸酯)是非标记性的氧化敏感的荧光探针,常用于检测细胞内活性氧。dcfh-da本身没有荧光,可以自由穿过细胞膜,进入细胞后,可以被细胞内的酯酶水解生成dcfh(2',7'-二氯二氢荧光素)。而dcfh不能通透细胞膜,从而使dcfh很容易被装载到细胞内,细胞内的活性氧可以氧化无荧光的dcfh生成有荧光的dcf(2',7'-二氯荧光素)。
5.人造细胞在生命医学领域有着重大作用。人造细胞可以更精确地将药物输送到目标、追踪癌细胞、检测有毒化学物质,或者提高诊断测试的准确性。而相互作用的合成细胞阵列可以形成能感知和适应环境的人工组织和智能材料。含有dna、黏土矿物和单个丙烯酸酯分子等原材料的微小液滴是一种典型的人造细胞模型。对于低浓度ros的人造细胞,常规的ros检测方法存在灵敏度低、稳定性差等问题。
技术实现要素:
6.针对上述现有技术中的不足,本发明的目的在于提供一种可见光驱动的纳米反应体系及其制备方法。所述可见光驱动的纳米反应体系包括羧酸盐型阴离子表面活性剂、2',7'-二氯二氢荧光素二乙酸酯,所述羧酸盐型阴离子表面活性剂与2',7'-二氯二氢荧光素二乙酸酯的摩尔比为x,其中,200<x<4000,所述可见光驱动的纳米反应体系中的2',7'-二氯二氢荧光素二乙酸酯水解后在波长不超过580nm的可见光光照条件下发生氧化还原反应。本发明所制备的可见光驱动的纳米反应体系中,2',7'-二氯二氢荧光素二乙酸酯在光照和添加羧酸盐型阴离子表面活性剂的条件下水解后发生氧化还原反应生成有荧光的dcf,从而实现对活性氧的消耗与快速检测。
7.本发明所制备的纳米反应体系可以仅在含有微量的水中,实现dcfh的氧化还原反应产生有荧光的dcf。特别适合于低浓度ros的检测。
8.本方案中,在dcfh-da溶液中加入羧酸盐型阴离子表面活性剂,并给予一定波长的光照使dcfh-da水解后发生氧化还原反应生成有荧光的dcf。dcfh-da分子结构中含有羧基,在dcfh-da中加入羧酸盐型阴离子表面活性剂,溶液中的dcfh-da的羧基、羟基与羧酸盐型阴离子表面活性剂的羧基通过氢键相互作用共组装形成层状纳米结构。dcfh-da水解后有序的排列于羧酸盐型阴离子表面活性剂的层状结构之间(羧酸盐型阴离子表面活性剂与dcfh-da共组装形成层状结构见附图1)。羧酸型阴离子表面活性剂与dcfh-da共组装形成层状结构,进而实现羧酸型阴离子表面活性剂对dcfh-da的富集和稳定。从而使纳米反应体系用于检测低浓度ros时,灵敏度高、稳定性好。将纳米反应体系置于一定波长的光下光照,dcfh-da水解生成dcfh后,低浓度活性氧将有序排列在羧酸型阴离子表面活性剂分子间的dcfh氧化生成有荧光的dcf。
9.进一步的,所述羧酸盐型阴离子表面活性剂与2',7'-二氯二氢荧光素二乙酸酯自组装形成层状结构。
10.所述羧酸盐型阴离子表面活性剂与2',7'-二氯二氢荧光素二乙酸酯的摩尔比为x,其中,400<x<4000。
11.优选地,所述羧酸盐型阴离子表面活性剂与2',7'-二氯二氢荧光素二乙酸酯的摩尔比为1200。
12.优选地,所述羧酸盐型阴离子表面活性剂选自脂肪酸盐、n-酰基氨基羧酸盐、聚醚羧酸盐中的一种或多种。
13.优选地,所述羧酸盐型阴离子表面活性剂选自碳链长度为c14~c18的脂肪酸盐。本方案所采用的羧酸盐型阴离子表面活性剂的疏水碳链越长,羧酸盐型阴离子表面活性剂分子间所形成的层状结构的空间越大,所共组装形成的层状结构中能够容纳2',7'-二氯二氢荧光素二乙酸酯越多,使有序排列的2',7'-二氯二氢荧光素二乙酸酯在层状结构中的浓度越高,光照和水中的活性氧使2',7'-二氯二氢荧光素二乙酸酯水解后发生氧化还原反应生成有荧光的dcf越多,荧光强度越强。
14.优选地,所述羧酸盐型阴离子表面活性剂选自硬脂酸钠、肉豆蔻酸钠、亚油酸钠中的一种或多种。
15.优选地,所述羧酸盐型阴离子表面活性剂选自肉豆蔻酸钠。
16.本发明的另一目的在于提供一种应用β-cd或d2o对所述的阴离子表面活性剂/dcfh-da可见光驱动的纳米反应体系的检测方法。
17.本发明的再一目的在于提供一种可见光驱动的纳米反应体系的制备方法,包括以下步骤:
18.步骤s1.构筑可见光驱动的纳米反应体系:将羧酸盐型阴离子表面活性剂溶液与2',7'-二氯二氢荧光素二乙酸酯溶液配制成混合溶液;
19.步骤s2.在波长不超过580nm的可见光光照步骤s1制得的混合溶液;
20.所述羧酸盐型阴离子表面活性剂与2',7'-二氯二氢荧光素二乙酸酯的摩尔比为x,其中,200<x<4000。
21.相比于现有技术,本发明具有如下有益效果:
22.(1)本发明制备得到的纳米反应体系中,羧酸型阴离子表面活性剂对dcfh-da有富集和稳定作用,在光照条件下,能够促进dcfh-da水解后发生氧化还原反应生成有荧光的
dcf。
23.(2)本发明制备得到的纳米反应体系可以用于低浓度活性氧的检测。
附图说明
24.图1.本发明提供的羧酸盐型阴离子表面活性剂/dcfh-da可见光驱动的纳米反应体系的结构示意图。
25.图2.不同浓度sm对dcfh-da的氧化还原反应影响。
26.图3.实施例3制备的羧酸盐型阴离子表面活性剂/dcfh-da可见光驱动的纳米反应体系的不同区域的透射电镜图。
27.图4.不同光照时间下,sm对dcfh-da氧化还原反应的影响。
28.图5.不同链长羧酸盐表面活性剂对dcfh-da氧化还原反应的影响。
29.图6.β-cd调节可见光驱动的纳米反应体系的形成,对dcfh-da的氧化还原反应的影响。
30.图7.β-cd和淀粉酶调节可见光驱动的纳米反应体系的形成,对dcfh-da的氧化还原反应的影响。
31.图8.d2o调节可见光驱动的纳米反应体系的形成,对dcfh-da的氧化还原反应的影响。
具体实施方式
32.为了使本技术领域的人员更好地理解本发明中的技术方案,下面将结合本发明实施例和附图对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
33.术语:
34.sm:肉豆蔻酸钠。
35.ss:十八酸钠。
36.sp:十六酸钠
37.sl:亚油酸钠。
38.dcfh-da:2',7'-二氯二氢荧光素二乙酸酯。
39.纳米反应器:由阴离子羧酸型表面活性剂 dcfh-da形成的自组装体
40.可见光驱动的纳米反应体系:含有纳米反应器的系统
41.β-cd:β-环糊精。
42.dmso:二甲基亚砜。
43.amylase:淀粉酶。
44.dcf:2',7'-二氯荧光素,荧光激发波长:485nm。
45.检测:所有实施例和对比例均在同一荧光分光光度计的测试条件进行测试。
46.实施例1:不同浓度的sm对dcfh-da氧化还原反应的影响。
47.步骤s1.构筑可见光驱动的纳米反应体系:将dcfh-da溶于dmso配制成浓度为10μmol/l的溶液,用水将sm配制成如下浓度:0mmo/l、2mmo/l、4mmo/l、8mmo/l、12mmo/l、18mmo/
l、20mmo/l、40mmo/l,将10μmol/l的dcfh-da溶液等体积分别与各浓度的sm溶液充分混合,形成混合液,将混合液分别放置于波长420nm下光照10min或不进行光照。
48.步骤s2.荧光的测定:分别使用荧光分光光度计测定各个混合液的荧光,其中,荧光分光光度的激发波长为485nm。结果见图2。
49.由图2可知,在没有光照条件下,dcfh-da水解后不会被氧化生成dcf。而当羧酸盐型阴离子表面活性剂sm与2',7'-二氯二氢荧光素二乙酸酯的摩尔比大于4000时,羧酸盐型阴离子表面活性剂sm在体系中浓度太大,在水中几乎不溶解,将其与dcfh-da的混合溶液进行荧光检测,不溶解的羧酸盐型阴离子表面活性剂sm对荧光强度有干扰,几乎水中没有溶解的羧酸盐型阴离子表面活性剂与dcfh-da共组装所形成的层状结构,荧光强度值为0;其他羧酸盐型阴离子表面活性剂与dcfh-da的摩尔比大于4000时的荧光强度均为0。当羧酸盐型阴离子表面活性剂sm与2',7'-二氯二氢荧光素二乙酸酯的摩尔比在200-400之间,羧酸盐型阴离子表面活性剂在体系中浓度低,与dcfh-da共组装所形成的层状结构少,位于层状结构中的dcfh-da的量少,纳米反应体系的荧光强度较弱;当羧酸盐型阴离子表面活性剂与2',7'-二氯二氢荧光素二乙酸酯的摩尔比在400-4000之间时,可见光驱动的纳米反应体系中的大部分的羧酸盐型阴离子表面活性剂与dcfh-da共组装形成层状结构,光照和水中的活性氧使水解后的dcfh-da氧化生成有荧光的dcf,荧光强度大。
50.将步骤s1中的配制的混合液分别放置于波长580nm下光照10min,最大荧光强度为12000。由此说明,本发明所制备得到的纳米反应体系在波长580nm下的光照可以发荧光。
51.实施例2:羧酸盐型阴离子表面活性剂/dcfh-da纳米反应体系的结构检测。
52.步骤s1.构筑纳米反应体系:将dcfh-da溶于dmso配制成浓度为10μmol/l的溶液,用水将sm配制12mmo/l的溶液,将12mmo/l的sm溶液分别与10μmol/l的dcfh-da溶液等体积充分混合,形成混合液,将配制的混合液分别放置于波长为420nm下光照10min,备用。
53.步骤s2.透射电子显微镜测定结构:样品在室温可控环境玻璃化系统(cevs)中制备。首先,分别将5μl的样品溶液装入带花边的支撑tem网格上,用镊子夹住。用一张吸墨纸吸去多余的液体,在小孔上留下一层薄膜。大约10秒后,将样本放入用液氮冷却的液体乙烷中,迅速冷冻成玻璃态的冰层。然后将陶瓷样品转移到低温样品架(gatan 626)上,并在200kv的thermo scientific低温制样装置talosarctica cryo-tem上测定。结果见图3。
54.由图3可以看出,羧酸盐型阴离子表面活性剂sm与dcfh-da共组装形成层状结构。
55.实施例3:不同光照时间下,对dcfh-da氧化还原反应的影响。
56.步骤s1.构筑可见光驱动的纳米反应体系:将dcfh-da溶于dmso配制成浓度为10μmol/l的溶液,用水将sm配制12mmo/l的溶液,将10μmol/l的dcfh-da溶液等体积与12mmo/l的sm溶液充分混合,形成混合液,将混合液放置于波长为420nm光照下,分别光照0min、1min、2min、3min、4min、5min、6min、7min、8min、9min、10min。
57.步骤s2.测定荧光:使用荧光分光光度计测定不同光照时间下的混合液的荧光,其中,荧光分光光度的激发波长为485nm。结果见图4。
58.由图3可知,随光照时间的延长,更多水解后的dcfh-da被氧化成dcf,混合液中的dcf浓度大,荧光强度增强。
59.实施例4:其他羧酸盐型阴离子离子表面活性剂对dcfh-da氧化还原反应的影响。
60.步骤s1.构筑可见光驱动的纳米反应体系:将dcfh-da溶于dmso配制成浓度为10μ
mol/l的溶液,用水分别将ss、sm、sp、sl配制成如下浓度:4mmo/l、,将10μmol/l的dcfh-da溶液等体积分别与ss、sm、sp、sl溶液充分混合,形成混合液,将混合液分别放置于波长420nm下光照10min。
61.步骤s2.测定荧光:使用荧光分光光度计分别测定各混合液的荧光,其中,荧光分光光度的激发波长为485nm。结果见图5。
62.由此说明,将sm替换成其他羧酸盐型阴离子离子表面活性剂时,可见光驱动的纳米反应体系中,在光照条件下,水中的活性氧可将dcfh-da水解后氧化成dcf。
63.实施例5:β-cd调节可见光驱动的纳米反应体系的形成。
64.步骤s1.将sm溶于水配制为18mmol/l的溶液,将dcfh-da溶于dmso配制成浓度为10μmol/l的溶液,将β-cd溶于dmso配制成如下浓度:0mmol/l、18mmol/l、36mmol/l的溶液,将sm溶液和dcfh-da溶液分别与各浓度的β-cd溶液等体积充分混合,将混合液分别放置在波长为420nm光照下,光照10min或不进行光照,备用。
65.步骤s2.分别使用荧光分光光度计测定各个混合液的荧光,其中,荧光分光光度的激发波长为485nm。结果见图6。
66.由图6可知,β-cd的加入会使可见光驱动的纳米反应体系的荧光强度降低,可能的原因是β-cd的疏水空腔与羧酸盐型阴离子表面活性剂的疏水尾端存在相互作用力,β-cd与羧酸盐型阴离子表面活性剂形成络合物,抑制了羧酸盐型阴离子表面活性剂sm与dcfh-da共组装形成层状结构,破坏了可见光驱动的纳米反应体系的形成,从而使dcfh-da水解后无法被氧化生成dcf。
67.实施例6:β-cd和淀粉酶调节可见光驱动的纳米反应体系的形成。
68.步骤s1.将sm、ss、sl分别溶于水配制为8mmol/l的溶液,将dcfh-da溶于dmso配制成浓度为20μmol/l的溶液,将sm溶液、ss溶液、sl溶液、dcfh-da溶液等体积充分混合,将混合液放置在波长为420nm光照下光照10min或不光照,备用。
69.步骤s2.使用荧光分光光度计分别测定混合液的荧光,其中,荧光分光光度的激发波长为485nm。
70.步骤s3.将sm、ss、sl分别溶于水配制为10mmol/l的溶液,将dcfh-da溶于dmso配制成浓度为25μmol/l的溶液,将β-cd溶于dmso配制成浓度为60mmol/l的溶液,将sm溶液、ss溶液、sl溶液、dcfh-da溶液、β-cd溶液等体积充分混合,将混合液放置在波长为420nm光照下光照10min或不光照,备用。
71.步骤s4.使用荧光分光光度计分别测定混合液的荧光,其中,荧光分光光度的激发波长为485nm。
72.步骤s5.将sm、ss、sl分别溶于水配制为12mmol/l的溶液,将dcfh-da溶于dmso配制成浓度为30μmol/l的溶液,将β-cd溶于dmso配制成浓度为72mmol/l的溶液,将sm溶液、dcfh-da溶液、β-cd溶液等体积充分混合,将混合液加入与sm溶液等体积的60mg/ml淀粉酶,即溶液中的淀粉酶浓度为10mg/ml,放置在波长为420nm光照下光照10min或不光照,备用。
73.步骤s6.使用荧光分光光度计测定混合液的荧光,其中,荧光分光光度的激发波长为485nm。结果见图7。
74.由图7可知,本发明在可见光驱动的纳米反应体系中加入β-cd,β-cd会使可见光驱动的纳米反应体系的荧光强度降低,而淀粉酶的加入则不会使体系重新形成可见光驱动的
纳米反应体系的荧光强度恢复到没有添加β-cd和淀粉酶时的荧光强度值。可能的原因是在羧酸盐型阴离子表面活性剂与dcfh-da所形成的可见光驱动的纳米反应体系中,虽然淀粉酶对β-cd有水解作用,但淀粉酶同时抑制了羧酸盐型阴离子表面活性剂与dcfh-da共组装形成层状结构,破坏了可见光驱动的纳米反应体系的形成,从而使dcfh-da水解后无法被氧化生成dcf。
75.实施例7:重水d2o调节可见光驱动的纳米反应体系的形成
76.步骤s1.将sm溶于重水d2o配制为12mmol/l的溶液,将dcfh-da溶于dmso配制成浓度为10μmol/l的溶液,将sm溶液、dcfh-da溶液等体积充分混合,将混合液放置在波长为420nm光照下光照10min或不光照,备用。
77.步骤s2.使用荧光分光光度计分别测定混合液的荧光,其中,荧光分光光度的激发波长为485nm。结果见图8。
78.由图8可知,sm与dcfh-da自组装形成的纳米反应体系在重水中的荧光强度下降。主要的原因是羧酸盐型阴离子表面活性剂与dcfh-da自组装形成层状结构是由于氢键作用的驱动,在重水中,羧酸盐型阴离子表面活性剂与dcfh-da的氢键作用力弱,羧酸盐型阴离子表面活性剂与dcfh-da自组装形成的层状结构少,所形成的纳米反应体系荧光强度降低。
79.对比例1:不添加羧酸盐型阴离子表面活性剂,dcfh-da的发光情况。
80.将dcfh-da溶于dmso和水配制成浓度为5μmol/l的溶液,将dcfh-da溶液放置于波长为420nm的光照10min,使用荧光分光光度计测定荧光。其中,荧光分光光度的激发波长为485nm。结果无荧光出现。
81.由此可知,在dcfh-da中不添加羧酸盐型阴离子表面活性剂,dcfh-da均匀分散于溶液体系中,体系中无法形成可见光驱动的纳米反应体系。光照和水中的活性氧无法将水解后的dcfh-da氧化成dcf。
82.对比例2:磺酸盐型阴离子表面活性剂对dcfh-da的氧化还原反应影响。
83.将实施例1中的sm替换成磺酸盐型阴离子表面活性剂十八烷基磺酸钠,其余步骤不变,结果无荧光出现。
84.由此可知,将sm替换成磺酸盐型阴离子表面活性剂,dcfh-da水解后无法被氧化生成dcf。可能的原因是dcfh-da与磺酸盐型阴离子表面活性剂的相互作用力弱,磺酸盐型阴离子表面活性剂无法与dcfh-da自组装形成层状结构。
85.对比例3:硫酸酯盐型阴离子表面活性剂对dcfh-da的氧化还原反应影响。
86.将实施例1中的sm替换成硫酸酯盐型阴离子表面活性剂十八烷基硫酸钠,其余步骤不变,结果无荧光出现。
87.由此可知,将sm替换成硫酸酯盐阴离子表面活性剂,dcfh-da无法被氧化生成dcf。可能的原因是dcfh-da与硫酸酯盐型阴离子表面活性剂的相互作用力弱,硫酸盐型阴离子表面活性剂无法与dcfh-da自组装形成层状结构。
88.对比例4:磷酸酯盐型阴离子表面活性剂对dcfh-da的氧化还原反应影响。
89.将实施例1中的sm替换成磷酸酯盐型阴离子表面活性剂十八烷基磷酸钠,其余步骤不变,结果无荧光出现。
90.由此可知,将sm替换成磷酸酯盐型阴离子表面活性剂,dcfh-da无法被氧化生成dcf。可能的原因是dcfh-da与磷酸酯盐型阴离子表面活性剂的相互作用力弱,磷酸盐型阴
离子表面活性剂无法与dcfh-da自组装形成层状结构。
91.最后应当说明的是,以上实施例仅用以说明本发明的技术方案而非对其限制,尽管对照上述实施例对本发明进行了详细的说明,所属领域的普通技术人员应当理解,技术人员阅读本技术说明书后依然可以对本发明的具体实施方式进行修改或者等同替换,但这些修改或变更均未脱离本发明申请待批权利要求保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。