1.本发明属于液流电池储能技术领域。具体涉及到几种具有氧化还原活性的氨基酸衍生物的吩嗪类、醌类、吩噻嗪类和噻嗯类电解质的合成方法,及其在水相液流电池储能系统中的应用。
背景技术:
2.传统能源(例如石油和煤)的迅速消耗及其带来的严重环境污染,迫切地要求我们使用更清洁的能源从而减少对环境的污染。随着科学技术的发展,清洁能源如太阳能、风能的成本已经低于传统能源,然而这两种清洁能源具有强波动性和间歇性,对周围环境要求很高。但人类的日常生产活动对电能的需求却十分规律,因此清洁能源的间歇性与波动性阻碍了它们在电网中大规模的应用。这种供需矛盾,要求我们发展一种大规模的储能技术来调节用电的高峰与低谷,即用电低谷时储存能量,高峰时输出能量,为电网的稳定性提供支持和保障。通过这样的调节作用,减少资源的浪费,使清洁能源得到妥善的存储和利用,使其从低价值、计划外的能源转化为高价值、可靠的产品。
3.现有的大规模储能技术有抽水蓄能、压缩空气储能、电化学储能(二次电池)、超级电容器储能和飞轮储能等。在上述所有储能技术中,前三种储能技术放电时间足够长和容量范围足够大,可用于储存太阳能和风能。抽水蓄能需要在不同海拔上建立两个巨大的蓄水池,是受特殊地理条件限制的大型工程,并可能伴随生态问题,难以在多地推广。压缩空气储能是将电力用于压缩空气,将压缩后的高压空气密封在储气设施中,在需要时释放压缩空气发电的储能方式。因此也需要特殊的地理条件如岩石洞穴、废弃矿井等作为大型储气室,而且在空气压缩与释放的过程中,部分能量转化为热能,导致这项技术效率低下。相比之下,电化学储能因其环境友好、能量效率高、维护成本低、性质可调和不受地理条件限制等优点受到广泛地关注,其中液流电池由于其丰富的电解质储备选择,是液流电池中最有应用前景的储能方式之一。
4.根据电解液使用的溶剂类别,液流电池分为水系液流电池和非水系(有机溶剂)液流电池。非水系液流电池所使用的有机溶剂存在一定的毒性,其成本也远远高于水,并可能对环境造成污染;有机溶剂的易燃易爆性所带来的安全隐患也使得非水系液流电池不适用于大规模储能电站。由此可见,水系液流电池具有更大的应用前景和值得被大规模推广的应用潜力。其中,以有机物作为储能材料的水系液流电池,因其储能物质来源广泛、可利用化学手段对有机物分子进行修饰改造及功能化,是当前的研究热点。
5.综上所述,本领域迫切需要开发新型的有机储能材料。
技术实现要素:
6.本发明的目的是开发一种新型的有机储能材料。
7.本发明的第一方面,提供了一种如下式(i)所示的化合物:
[0008][0009]
其中,y和z各自独立地选自下组:n、nh、c=o或s;
[0010]
虚线为化学键或不存在;
[0011]
m1和m2选自下组:0、1、2、3或4;
[0012]
p1和p2选自下组:0、1、2、3或4;
[0013]
各个r各自独立地选自下组:卤素、取代或未取代的c1-c10的烷基、环烷基、杂环烷基,取代或未取代的c6-c10芳基、羟基、硫醇基团、胺基、羧基、磷酸基、磺酸基或以下基团:
[0014][0015]
r0选自下组:-coox、-so3x、-po3h2、-nh2、-nhch3、-n(ch3)2、-n
(ch3)3m-;其中,x选自下组:h
、nh
4
、li
、na
、k
、mg
2
、al
3
、ca
2
;m选自下组:f、cl、br或i;各个rg各自独立地为功能化基团;其中,所述的功能化基团为其中:
[0016]
ra和rb各自独立地选自下组:h、取代或未取代的c1-c10的烷基、环烷基、杂环烷基,取代或未取代的c6-c10芳基、或ra和rb共同形成取代或未取代的3-8元的含氮杂环或含氮杂芳环;且所述的rg上至少包括一个r0取代基;
[0017]
除特别说明之处,所述的取代指基团上的一个或多个氢原子被选自下组的取代基取代:卤素,c1-c10的烷基、环烷基、杂环烷基,c6-c10芳基、羟基、硫醇基团、胺基、羧基、磷酸基、磺酸基。
[0018]
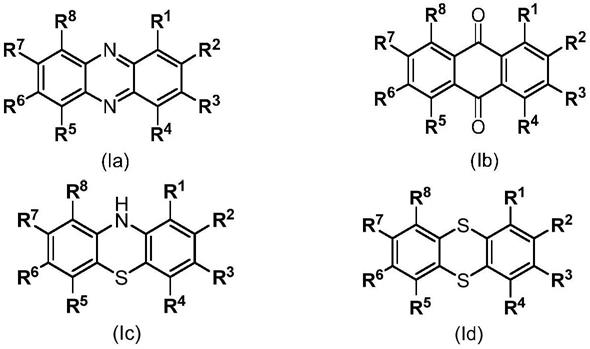
在另一优选例中,所述的化合物具有如下式(ia)、式(ib)、式(ic)或式(id)所示的结构:
[0019][0020]
其中,r1、r2、r3、r4、r5、r6、r7、r8各自独立地选自下组:h、卤素、取代或未取代的c1-c10的烷基、环烷基、杂环烷基,取代或未取代的c6-c10芳基、羟基、硫醇基团、胺基、羧基、磷
酸基、磺酸基,或功能化基团;
[0021]
限定条件是,r1、r2、r3、r4、r5、r6、r7、r8中至少包括一个功能化基团。
[0022]
在另一优选例中,r1、r2、r3、r4、r5、r6、r7、r8各自独立地选自下组:h、取代或未取代的c1-c10的烷基、环烷基、杂环烷基,或功能化基团;其中,所述的功能化基团是选自下组的基团:
[0023][0024]
其中,各个x、x1和x2各自独立地选自下组:h、nh
4
、li
、na
、k
、mg
2
、al
3
、ca
2
;
[0025]
r9、r
10
和r
11
各自独立地选自下组:h、取代或未取代的c1-c10的烷基、环烷基、杂环烷基,或取代或未取代的c6-c10芳基;
[0026]
n为1、2、3、4、5、6、7或8;
[0027]
c1为取代或未取代的3-8元的杂环(包括部分不饱和或饱和环),或取代或未取代
的5-8元的杂芳环。
[0028]
在另一优选例中,所述的ra和rb各自独立地选自下组:h、取代或未取代的c1-c10的烷基、环烷基、杂环烷基,且所述的rg上至少包括一个r0取代基。
[0029]
在另一优选例中,所述的r9、r
10
和r
11
各自独立地选自下组:h、取代或未取代的c1-c10的烷基、环烷基、杂环烷基。
[0030]
在另一优选例中,所述的化合物选自下组:
[0031][0032]
本发明的第二方面,提供了一种如本发明第一方面所述的化合物的制备方法,所述的方法包括步骤:
[0033][0034]
(i)在惰性溶剂中,用式(ii)化合物与rgh反应,得到式(i)化合物;
[0035]
或所述的方法包括步骤:
[0036][0037]
(1)在惰性溶剂中,用式(iii)化合物与ch2=chcooet反应,得到式(iiia)化合物;
[0038][0039]
(2)在氢气气氛下,对式(iiia)化合物进行还原,得到式(iiib)化合物;
[0040][0041]
(3)对式(iiib)化合物进行水解脱保护,得到式(i-1)化合物;
[0042]
其中,m为f、cl、br或i。
[0043]
在另一优选例中,所述的步骤(i)中,所述的方法在钯催化剂,配体和碱存在下进行;优选地,所述的钯催化剂为pd2(dba)3,所述的碱为
t
buok或cs2co3,且所述的配体选自下组:brettphos、ruphos、xphos或pd2(dba)3;
[0044]
在另一优选例中,所述的步骤(1)中,所述的反应在钯催化剂,配体、碱和催化剂存在下进行;优选地,所述的钯催化剂为pdcl2,所述的碱为碳酸钾,所述的配体为p(o-tol)3,且所述的催化剂为bu4nbr。
[0045]
在另一优选例中,所述的步骤(2)中,所述的反应在钯/碳存在下进行。
[0046]
在另一优选例中,所述的步骤(3)中,所述的反应在碱存在下进行;较佳地,所述的碱为naoh。
[0047]
在另一优选例中,所述的步骤(i)中,所述的惰性溶剂选自下组:叔丁醇、正丁醇、甲苯,或其组合。
[0048]
在另一优选例中,所述的步骤(1)中,所述的惰性溶剂选自下组:dmf、水,或其组
合。
[0049]
在另一优选例中,所述的步骤(2)中,所述的惰性溶剂选自下组:乙酸乙酯。
[0050]
在另一优选例中,所述的步骤(2)中,所述的惰性溶剂选自下组:甲醇、水,或其组合。
[0051]
在另一优选例中,所述方法还包括:在反应结束后,过滤并收集滤饼,滤饼用去离子水溶解后再次过滤以除去水中不溶杂质。收集滤液,滤液用hcl酸化至ph=3~4,固体析出后过滤。
[0052]
在另一优选例中,所述方法还包括:在反应结束后,用反相柱对于产物进行提纯。
[0053]
本发明的第三方面,提供了一种液流电池储能材料,其特征在于,所述的液流电池储能材料是用如本发明第一方面所述的化合物作为活性成分制备的。
[0054]
本发明的第四方面,提供了一种液流电池,所述的液流电池包括如本发明第一方面所述的化合物作为储能材料。
[0055]
在另一优选例中,所述的液流电池中,如本发明第一方面所述的化合物作为负极或正极溶液。
[0056]
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
[0057]
图1为化合物3的1h nmr图;
[0058]
图2为化合物3的
13
c nmr图;
[0059]
图3为化合物5的1h nmr图;
[0060]
图4为化合物5的
13
c nmr图;
[0061]
图5为化合物7的1h nmr图;
[0062]
图6为化合物7的
13
c nmr图;
[0063]
图7为化合物9的1h nmr图;
[0064]
图8为化合物9的
13
c nmr图;
[0065]
图9为化合物11的1h nmr图;
[0066]
图10为化合物11的
13
c nmr图;
[0067]
图11为化合物13的1h nmr图;
[0068]
图12为化合物13的
13
c nmr图;
[0069]
图13为化合物14的1h nmr图;
[0070]
图14为化合物14的
13
c nmr图;
[0071]
图15为化合物15的1h nmr图;
[0072]
图16为化合物15的
13
c nmr图;
[0073]
图17为化合物16的1h nmr图;
[0074]
图18为化合物16的
13
c nmr图;
[0075]
图19为化合物19的1h nmr图;
[0076]
图20为化合物20的1h nmr图;
是指具有3、4、5或6个碳原子,依此类推。
[0110]
在本发明中,术语“烷基”表示饱和的线性或支链烃部分,例如术语“c1-c10烷基”是指具有1至10个碳原子的直链或支链烷基,非限制性地包括甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、戊基和已基等;优选乙基、丙基、异丙基、丁基、异丁基、仲丁基和叔丁基。
[0111]
在本发明中,术语“芳基”或“芳环”表示包含一个或多个芳环的烃基部分。芳基的例子包括但不限于苯基(ph)、萘基、芘基、芴基、蒽基和菲基。
[0112]
在本发明中,术语“杂芳基”表示包含一个或多个具有至少一个杂原子(例如n,o或s)的芳环的部分。杂芳基的例子包括呋喃基、吡咯基、噻吩基、噁唑基、咪唑基、噻唑基、吡啶基、嘧啶基、喹唑啉基、喹啉基、异喹啉基和吲哚基等。
[0113]
液流电池
[0114]
在液流电池中,正、负极电解液分别储存在外部的储液罐中,通过蠕动泵传送到电堆里,活性物质在电极表面发生氧化还原反应实现能量的储存与释放。与锂离子电池等传统化学电池相比,液流电池具有能量与功率相互独立的优点,即能量大小取决于储能材料的浓度和体积,而功率大小取决于电极面积。当储能规模越大时,这项技术的成本就越接近储能材料的成本,所以尽管锂离子电池具有更高的能量密度,液流电池则更加适合于大规模的储能电站。根据电解液使用的溶剂类别,液流电池分为水系液流电池和非水系(有机溶剂)液流电池。
[0115]
水系液流电池根据使用的储能材料是无机物或有机物,分为水系无机液流电池和水系有机液流电池。目前研究最多、应用最广泛的储能材料均为无机材料,然而无机材料成本高、资源有限,在使用过程中容易形成枝晶,且电化学反应速率慢等缺点限制了无机液流电池的大规模应用。以有机物作为储能材料,其来源比地壳中储存有限的金属更加广泛,使用成本更低廉,更可以减少重金属对环境的污染。相对于无机材料,有机材料具有质轻、价廉、延展性及可塑性等优点;有机材料的电化学反应速度较快,通常比无机金属高1-2个数量级,无需使用催化剂,也不会形成枝晶破坏隔膜;同时合成化学家可以从分子水平对其进行修饰改造及功能化,通过引入官能团来优化有机材料的溶解度和氧化还原电位,从而调节电池的能量密度和开路电压。因此,研究有机储能材料的结构特性、电化学特性及其可能的降解机理,从而提高水系有机液流电池的性能、能量密度和寿命,同时降低其成本,对于推动液流电池在储能领域的应用、减少环境污染与能源浪费,并且满足人类生产活动对电能的需求具有非常重要的意义。
[0116]
液流电池储能材料
[0117]
本发明中,提供了一种能够用作为水系液流电池的有机储能材料的化合物,具体地,该化合物具有如下式(i)所示的结构:
[0118][0119]
其中,y和z各自独立地选自下组:n、nh、c=o或s;
[0120]
虚线为化学键或不存在;
[0121]
m1和m2选自下组:0、1、2、3或4;
[0122]
p1和p2选自下组:0、1、2、3或4;
[0123]
各个r各自独立地选自下组:卤素、取代或未取代的c1-c10的烷基、环烷基、杂环烷基,取代或未取代的c6-c10芳基、羟基、硫醇基团、胺基、羧基、磷酸基、磺酸基或以下基团:
[0124][0125]
r0选自下组:-coox、-so3x、-po3h2、-nh2、-nhch3、-n(ch3)2、-n
(ch3)3m-;其中,x选自下组:h
、nh
4
、li
、na
、k
、mg
2
、al
3
、ca
2
;m选自下组:f、cl、br或i;各个rg各自独立地为功能化基团;其中,所述的功能化基团为其中:
[0126]
ra和rb各自独立地选自下组:h、取代或未取代的c1-c10的烷基、环烷基、杂环烷基,取代或未取代的c6-c10芳基、或ra和rb共同形成取代或未取代的3-8元的含氮杂环或含氮杂芳环;且所述的rg上至少包括一个r0取代基。
[0127]
在优选的实施方式中,该化合物具有如实施例中所制备的各个化合物所示的结构。
[0128]
所述的化合物溶于溶剂后作为负极或正极溶液,用于组装液流电池。
[0129]
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。
[0130]
实施例1-9吩嗪类氨基酸衍生物的合成
[0131][0132]
氮气氛围下,称取2,7-二溴吩嗪(3mmol,1.014g),甘氨酸(7.2mmol,0.54g),pd2(dba)3(5mol%,137.4mg),brettphos(10mol%,161mg),叔丁醇钾(15mmol,1.68g),叔丁醇30ml于厚壁耐压反应管中。充分搅拌并升温至100℃,反应12h后冷却至室温。过滤并收集滤饼,滤饼用去离子水溶解后再次过滤以除去水中不溶杂质。收集滤液,滤液用hcl酸化至ph=3~4,固体析出后过滤,收集滤饼,滤饼用去离子水洗涤(2
×
5ml),干燥后得到目标化合物3。进一步,通过反相柱(c18)提纯(meoh:h2o=15:85),产率92%.
[0133]
采用上述的通用方法1,通过替换反应原料,得到如下化合物5-16:
[0134][0135]
上述各个化合物的核磁谱图(包括氢谱和碳谱)如图1-图18所示。
[0136]
实施例10吩嗪类丙氨酸衍生物的合成
[0137][0138]
合成步骤如下:
[0139]
氮气氛围下,称取2,7-二溴吩嗪(3mmol,1.014g),3,3'-亚胺二丙腈(12mmol,
1.48g),pd2(dba)3(5mol%,137.4mg),brettphos(10mol%,161mg),碳酸铯(21mmol,6.842g),叔丁醇10ml,于反应管中。充分搅拌并升温至100℃,反应12h后趁热过滤。固体依次用去离子水,etoh洗涤之后于真空干燥箱干燥,得到化合物18。称取化合物18(1mmol,422mg)加入厚壁耐压瓶,加入naoh(4mmol,160mg),去离子水4ml,充分搅拌并升温至150℃,反应12h后冷却过滤,收集固体。进一步,通过反相柱(c18)提纯(meoh:h2o=5:95),得到化合物19。产率90%。
[0140]
实施例11-13蒽醌类氨基酸衍生物的合成
[0141][0142]
氮气氛围下,称取2,6-二碘蒽醌(3mmol,1.38g),甘氨酸(9mmol,0.68g),pd2(dba)3(5mol%,137.4mg),brettphos(10mol%,161mg),叔丁醇钾(15mmol,1.68g),叔丁醇30ml于厚壁耐压反应管中。充分搅拌并升温至120℃,反应12h后冷却至室温。过滤并收集滤饼,滤饼用去离子水溶解后再次过滤以除去水中不溶杂质。收集滤液,滤液用hcl酸化至ph=3~4,固体析出后过滤,收集滤饼,滤饼用去离子水洗涤(2*5ml),干燥后得到目标化合物21。
[0143]
通过上述方法得到化合物20-22,其核磁谱图如图20-22所示。
[0144][0145]
实施例14-17吩嗪类衍生物的合成
[0146][0147]
氮气环境下分别称取1,8-二溴吩嗪(10g,29.8mmol),丙烯酸乙酯(17.9g,178.8mmol),氯化钯(106mg,0.596mmol),三(邻甲基苯基)磷(726mg,2.384mmol),四丁基溴化铵(1.92g,5.96mmol),碳酸钾(16.4g,119.2mmol),n,n-二甲基甲酰胺(8ml),水(80ml)于厚壁耐压反应管中,充分搅拌并升温至100℃反应12h。反应结束后体系冷却至室温,体系中深色不溶固体经减压过滤,蒸馏水及石油醚洗涤后,重新溶解于二氯甲烷中,并加入蒸馏水以及饱和食盐水洗涤。随后体系有机相经分离、无水硫酸钠干燥、过滤以及减压浓缩后进行快速硅胶色谱柱层析(展开剂:二氯甲烷/乙酸乙酯/三乙胺=500/20/3),并得到大量深绿色固体。深绿色固体经乙酸乙酯洗涤及过滤后制备得到纯的黄绿色产物27(11.9g),产率为70.8%。
[0148]
称取黄绿色固体27(4.6g,12.23mmol)及钯/碳(460mg)于反应瓶中,并将反应瓶中的空气置换成氮气,进而置换成氢气。随后150ml乙酸乙酯加入上述体系,并在氢气氛围下
85度搅拌反应12h。反应完成并冷却至室温的体系经硅藻土过滤,减压浓缩以及硅胶色谱柱层析(展开剂:石油醚/乙酸乙酯/三乙胺=400/100/3)后得到纯的目标化合物28(4.4g),产率为94.6%。
[0149]
最后,将上一步制备所得的纯品化合物28(4.4g,11.6mmol)溶于25ml甲醇,并向其中加入氢氧化钠水溶液[氢氧化钠(9.28g,232mmol)溶于25ml水],体系充分搅拌并升温至65℃进行反应。反应12h后冷却至室温,并用盐酸酸化反应体系直至大量黄绿色固体析出。随后通过过滤收集滤饼并用蒸馏水进行充分洗涤,干燥后得到目标化合物24(3.72g),产率为99%。
[0150]
采用上述的通用方法,通过替换反应原料,得到如下化合物25,26:
[0151][0152]
测试实施例
[0153]
测试例1循环伏安法测试(化合物15)
[0154]
循环伏安法测试采用三电极体系。其中,工作电极为5mm玻碳电极,参比电极为水相ag/agcl,对电极为铂丝电极。测试时电压扫描范围:-1.1v~-0.3v,扫描速率为20mv/s。
[0155]
测试化合物15在1m kcl溶液中的循环伏安图,如图23所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.56v,δe=341mv。
[0156]
测试例2电流循环测试
[0157]
液流电池装置主要参数及示意图如图24中所示。使用电化学工作站进行恒流充放循环测试。用化合物15组装电池,采用nafion117阳离子交换膜,sgl39aa碳纸作为电极材料。充放电电流为100ma,电流密度为20ma/cm2。
[0158]
电池循环过程中,其负极溶液为6.9ml 0.1m化合物15溶解在1m kcl溶液中;正极溶液为40ml 0.1m k4fecn6和0.02m k3fecn6溶解在1m kcl溶液中。循环过程采用恒流循环,其电流密度为20ma/cm2。
[0159]
化合物15在1m kcl溶液中的测试结果如图25、26所示。测试结果显示,该化合物具有优异的电池循环稳定性,恒流无间断充放电测试6d,在过程中一直保持稳定的充放电平台,电池容量无衰减,实际容量发挥占理论容量91%,能量效率达73%。研究结果充分表明,该类化合物是理想的水系液流电池储能材料。
[0160]
测试例3循环伏安法测试(化合物3)
[0161]
测试化合物3在1m kcl溶液中的循环伏安图,如图27所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.52v,δe=95mv。
[0162]
测试例4循环伏安法测试(化合物5)
[0163]
测试化合物5在1m kcl溶液中的循环伏安图,如图28所示。结果显示该化合物可在
中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.54v,δe=276mv。
[0164]
测试例5循环伏安法测试(化合物7)
[0165]
测试化合物7在1m kcl溶液中的循环伏安图,如图29所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.52v,δe=115mv。
[0166]
测试例6循环伏安法测试(化合物9)
[0167]
测试化合物9在1m kcl溶液中的循环伏安图,如图30所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.53v,δe=95mv。
[0168]
测试例7循环伏安法测试(化合物11)
[0169]
测试化合物11在1m kcl溶液中的循环伏安图,如图31所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.57v,δe=205mv。
[0170]
测试例8循环伏安法测试(化合物13)
[0171]
测试化合物13在1m kcl溶液中的循环伏安图,如图32所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.52v,δe=376mv。
[0172]
测试例9循环伏安法测试(化合物14)
[0173]
测试化合物14在1m kcl溶液中的循环伏安图,如图33所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.51v,δe=425mv。
[0174]
测试例10循环伏安法测试(化合物16)
[0175]
测试化合物16在1m kcl溶液中的循环伏安图,如图34所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.51v,δe=425mv。
[0176]
测试例11循环伏安法测试(化合物21)
[0177]
测试化合物21在1m kcl溶液中的循环伏安图,如图40所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.56v,δe=44mv。
[0178]
测试例12循环伏安法测试(化合物22)
[0179]
测试化合物22在1m kcl溶液中的循环伏安图,如图41所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.60v,δe=59mv。
[0180]
测试例13循环伏安法测试(化合物23)
[0181]
测试化合物23在1m kcl溶液中的循环伏安图,如图42所示。结果显示该化合物可在中性(kcl)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.60v,δe=48mv。
[0182]
测试例14循环伏安法测试(化合物24)
[0183]
测试化合物24在1m koh溶液中的循环伏安图,如图43所示。结果显示该化合物可在碱性(koh)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.59v,δe=163mv。
[0184]
测试例15循环伏安法测试(化合物25)
[0185]
测试化合物25在1m koh溶液中的循环伏安图,如图44所示。结果显示该化合物可在碱性(koh)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.56v,δe=195mv。
[0186]
测试例16循环伏安法测试(化合物26)
[0187]
测试化合物25在1m koh溶液中的循环伏安图,如图45所示。结果显示该化合物可在碱性(koh)条件下表现出较好的氧化还原性能。且具有较高的负电势,e
1/2
=-0.61v,δe=91mv。
[0188]
测试例17电流循环测试(化合物22)
[0189][0190]
液流电池装置主要参数及示意图如图24中所示。使用电化学工作站进行恒流充放循环测试。用化合物22组装电池,采用nafion117阳离子交换膜,sgl39aa碳纸作为电极材料。充放电电流为100ma,电流密度为20ma/cm2。
[0191]
电池循环过程中,其负极溶液为7.0ml 0.1m化合物22溶解在ph=12的1m kcl溶液中;正极溶液为40ml 0.1m k4fecn6和0.02m k3fecn6溶解在ph=12的1m kcl溶液中。循环过程采用恒流循环,其电流密度为20ma/cm2。
[0192]
化合物22在1m kcl(ph=12)溶液中的测试结果如图46、47所示。测试结果显示,该化合物具有优异的电池循环稳定性,恒流无间断充放电测试总共10天,在过程中一直保持稳定的充放电平台,电池容量为衰减0.61%/day,实际容量发挥占理论容量88%,能量效率达68%。研究结果充分表明,该类化合物是理想的水系液流电池储能材料。
[0193]
测试例18电流循环测试(化合物24)
[0194][0195]
液流电池装置主要参数及示意图如图24中所示。使用电化学工作站进行恒流及恒压充放循环测试。用化合物24组装电池,采用nafion117阳离子交换膜,sgl39aa碳纸作为电极材料。充放电电流为100ma,电流密度为20ma/cm2。
[0196]
电池循环过程中,其负极溶液为7.0ml 0.1m化合物24溶解在ph=12的1m kcl溶液中;正极溶液为40ml 0.1m k4fecn6和0.02m k3fecn6溶解在ph=12的1m kcl溶液中。循环过程采用恒流与恒压循环,其电流密度为20ma/cm2。
[0197]
化合物24在1m kcl(ph=12)溶液中的测试结果如图48、49所示。测试结果显示,该
化合物具有优异的电池循环稳定性,恒流与恒压无间断充放电测试总共20天,在过程中一直保持稳定的充放电平台,电池容量为衰减0.0033%/day,实际容量发挥占理论容量96%,能量效率达66%。研究结果充分表明,该类化合物是理想的水系液流电池储能材料。
[0198]
测试例19电流循环测试(化合物25)
[0199][0200]
液流电池装置主要参数及示意图如图24中所示。使用电化学工作站进行恒流及恒压充放循环测试。用化合物25组装电池,采用nafion117阳离子交换膜,sgl39aa碳纸作为电极材料。充放电电流为100ma,电流密度为20ma/cm2。
[0201]
电池循环过程中,其负极溶液为7.0ml 0.1m化合物25溶解在ph=12的1m kcl溶液中;正极溶液为40ml 0.1m k4fecn6和0.02m k3fecn6溶解在ph=12的1m kcl溶液中。循环过程采用恒流与恒压循环,其电流密度为20ma/cm2。
[0202]
化合物25在1m kcl(ph=12)溶液中的测试结果如图50、51所示。测试结果显示,该化合物具有优异的电池循环稳定性,恒流与恒压无间断充放电测试总共20d,在过程中一直保持稳定的充放电平台,电池容量为衰减0.0044%/day,实际容量发挥占理论容量99%,能量效率达65%。研究结果充分表明,该类化合物是理想的水系液流电池储能材料。
[0203]
测试例20电流循环测试(化合物26)
[0204][0205]
液流电池装置主要参数及示意图如图24中所示。使用电化学工作站进行恒流及恒压充放循环测试。用化合物26组装电池,采用nafion117阳离子交换膜,sgl39aa碳纸作为电极材料。充放电电流为100ma,电流密度为20ma/cm2。
[0206]
电池循环过程中,其负极溶液为7.0ml 0.1m化合物26溶解在ph=12的1m kcl溶液中;正极溶液为40ml 0.1m k4fecn6和0.02m k3fecn6溶解在ph=12的1m kcl溶液中。循环过程采用恒流与恒压循环,其电流密度为20ma/cm2。
[0207]
化合物26在1m kcl(ph=12)溶液中的测试结果如图52、53所示。测试结果显示,该化合物具有优异的电池循环稳定性,恒流与恒压无间断充放电测试总共18d,在过程中一直保持稳定的充放电平台,电池容量为衰减0.1110%/day,实际容量发挥占理论容量96%,能量效率达70%。研究结果充分表明,该类化合物是理想的水系液流电池储能材料。
[0208]
上述各个实施例的结果显示,本发明的化合物用作为液流电池的储能材料时,具有较高的负电势和较好的氧化还原性能,因此是一种理想的水系液流电池储能材料。
[0209]
在本发明提及的所有文献都在本技术中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。