1.本发明涉及医疗器械技术领域,具体地说,是一种基于图像分割的自动化瓣膜支架输送系统。
背景技术:
2.二尖瓣关闭不全(mitral regurgitation,mr)是最为常见的瓣膜疾病,在一般人群中的发病率约为1.7%。据统计,中国患有严重二尖瓣关闭不全的人约有2000万。严重的mr将严重损害心脏功能,增加心力衰竭的风险,从而威胁人的健康和寿命。未经手术治疗的严重mr患者中,5年内的死亡率高达50%,且存活的患者中有90%将会发展至心衰阶段。
3.在当前的诊疗实践中,研究的热点为经导管二尖瓣瓣膜置入术(tmvi)。tmvi是一种借助介入技术,将人工瓣膜置入心脏以完成瓣膜置换的微创手术,具有创伤小,恢复快的特点。其中,输送系统是进行tmvi手术时的重要部分,主要作用是携带压缩后的瓣膜支架进入心脏,完成释放和固定。输送系统的优劣决定着tmvi手术的成败。
4.在现有技术中,tmvi手术过程均为全手动操作。术前,医生通过ct进行二尖瓣瓣环分析,确定最佳入路及相关信息。术中,医生还需要全程在左心室食道超声造影的引导下进行瓣膜植入,同时辅以数字减影血管造影(digital subtraction angiography,dsa)进行判断。然而,在dsa下进行瓣膜置换术,术者须长期处于辐射环境中,有害身体健康。此外,二尖瓣瓣膜支架的置入过程较复杂,手动操作易带来控制不稳定、定位不精确的问题,且由于患者的解剖参数不同,现有技术也无法做到预先调节。
5.中国专利文献:cn201721010385.5,申请日20170814,专利名称为:一种二尖瓣膜支架输送系统。公开了一种二尖瓣膜支架输送系统,包括:设有第一按钮的手柄;外管,可移动地设置在手柄上,与第一按钮连接,第一按钮控制外管在手柄上滑动;内管,位于外管中,其第一端固定在手柄上,内外管之间具有间隙;锥形尖头,设置在内管的第二端处;瓣膜支架连接结构,包括多个条形结构,条形结构的第一端固定在内管上,第二端为自由端,其自由端处设有用于固定二尖瓣膜支架的夹持部。
6.上述专利文献中的一种二尖瓣膜支架输送系统,当第一按钮处于打开状态时,瓣膜支架连接结构露出外管,且条形结构的自由端处于向远离所述内管的方向弯曲的状态,该实用新型的输送系统在输送瓣膜支架的过程中可以有效保证瓣膜支架的稳定装载及准确释放瓣膜支架,有效提高了手术成功率;但是该瓣膜支架输送系统仍然为手动操作,故易带来控制不稳定、定位不精确的问题。另外,本技术人曾申请过发明专利名称(公开日2021.07.16)为:一种基于远程控制的电动支架输送装置。该电动支架输送系统解决目前二尖瓣瓣膜置换技术上,操作复杂,精准度低,手术失败率高的问题,切实减少患者创伤、降低术者难度、提高手术成功率、减少术后并发症,能够简化操作过程,保证二尖瓣瓣膜置入的精确定位以及精准释放,为二尖瓣瓣膜置换技术的发展做出贡献,但是其在操作过程中同样需要手动操作,未达到自动化级别的瓣膜支架输送。
7.综上所述,亟需一种能够实时监测输送装置位置、二尖瓣活动状态、人工支架释放
阶段等,并将相应信息反馈给控制器和机械臂,高度自动化、分阶段地完成心脏瓣膜支架的置入和释放,解决现有瓣膜输送系统可控性、精确性、安全性低的问题,同时保护术者免于辐射危害的一种基于图像分割的自动化瓣膜支架输送系统。而关于该系统目前则没有相关的报道。
技术实现要素:
8.本发明的目的是克服现有技术的不足,提供一种能够实时监测输送装置位置、二尖瓣活动状态、人工支架释放阶段等,并将相应信息反馈给控制器和机械臂,高度自动化、分阶段地完成心脏瓣膜支架的置入和释放,解决现有瓣膜输送系统可控性、精确性、安全性低的问题,同时保护术者免于辐射危害的一种基于图像分割的自动化瓣膜支架输送系统。
9.为实现上述目的,本发明采取的技术方案是:
10.一种基于图像分割的自动化瓣膜支架输送系统,由以下3个部分组成:远程控制软件、机械臂、支架输送装置;
11.所述远程控制软件主要有2个功能;其一,术前设置;允许术者根据每个患者的个人情况预设手术参数,并根据识别对象设置图像分割所需的预选框。其二,术中干预;由于在使用本系统时,手术过程是高度自动化的,故远程控制软件为人工干预提供了可能;在界面中设置了超声心动图及dsa影像监测窗口,使得术者在手术进程中可以及时发现意外情况,并进行暂停、调整等操作,增强了手术的可控性和安全性;
12.所述机械臂用于夹持支架输送装置,可以在手术过程中进行瓣膜支架的位置调整;
13.所述支架输送装置,其主要作用是携带压缩后的瓣膜支架进入心脏,完成释放和固定。
14.本说明书实施例提供的一种基于图像分割的自动化瓣膜支架输送系统的输送方法,包括以下步骤:
15.从外接超声设备输入的二维和三维dicom数据中,解析所需信息,将二维超声心动图、三维超声心动图实时显示在远程控制软件的控制界面中;
16.术前,须调整好超声探头的位置,采用胸骨旁左室长轴切面,使得二尖瓣的前尖瓣、后尖瓣均显示完整,且能较完整地看到左心房的顶部;
17.手术开始后,做胸壁小切口(2
‑
3cm),切开心包,在心尖处做荷包缝合,使用穿刺鞘管做心尖穿刺,置入软导丝,逆行跨过二尖瓣进入左心房,建立输送通路,将软导丝更换为硬导丝,将输送装置顺导丝置入左心;术者此时可离开手术台,进入远程控制室,进行瓣膜置换的远程精细操控。
18.术者进入远程控制室后,须在远程控制软件的参数设置页面上设置患者的个性化参数,以便手术过程可以依据患者的个人情况进行调整;此外,术者须设置预选框,即框选出左心房、二尖瓣的前尖瓣、二尖瓣的后尖瓣和输送装置的大致位置。预选框为椭圆形,各预选框之间允许重叠。
19.进一步地,自动采用c
‑
v模型对二维超声心动图进行实时处理。
20.进一步地,进入输送装置置入的第一阶段。根据处理结果,当所述支架输送装置的头端距离二尖瓣较远时,控制器控制输送装置以较快的速度向前运动;当所述支架输送装
置的头端位于二尖瓣附近时,输送装置置入的第一阶段结束。
21.进一步地,进入输送装置置入的第二阶段;根据处理结果,当二尖瓣舒张时,所述支架输送装置小幅度向前运动;当二尖瓣收缩时,所述支架输送装置停止运动;当所述支架输送装置的头端到达左心房内的目标位置时,输送装置置入的第二阶段结束;
22.输送装置置入后,暂停对二维超声心动图的识别;术者须在三维超声心动图中,手动框选出二尖瓣环和输送装置头端,以便系统自动识别出二尖瓣环的准确轮廓,以及输送装置头端的准确轮廓。
23.进一步地,自动采用c
‑
v模型对三维超声心动图进行实时处理。
24.进一步地,根据处理结果,将人工瓣膜调整到合适的释放位置,并向输送装置的控制器发送信息,释放瓣膜的心房侧。释放完成后,输送装置向后运动,使人工瓣膜与二尖瓣原有的瓣叶贴合紧密。
25.进一步地,将信息发送至控制器,控制输送装置将瓣膜完全释放;
26.瓣膜释放完成后,暂停对三维超声心动图的识别。术者须在二维超声心动图上重新设置预选框,分别框选出输送装置、人工瓣膜的前尖瓣和后尖瓣。
27.进一步地,自动采用c
‑
v模型对二维超声心动图进行实时处理。
28.进一步地,进入输送装置撤出的第一阶段;根据处理结果,当所述支架输送装置的头端未完全撤出左心房时,所述支架输送装置小幅度向后运动;当所述支架输送装置的头端完全撤出左心房时,输送装置撤出的第一阶段结束。
29.进一步地,进入输送装置撤出的第二阶段;根据处理结果,控制器控制输送装置以较快的速度向后运动,直至输送装置完全撤出;
30.输送装置完全撤出心脏后,自动输送过程结束;术者由远程控制室进入手术室,对心尖切口处进行加压缝合处理后,即可完成手术。
31.本发明优点在于:
32.1、远程控制,保护术者安全:允许术者在远程控制室中通过远程控制软件进行相关操作,避免术者长期处于手术室的辐射环境中。
33.2、精准释放,提高手术成功率:根据瓣膜输送过程的不同阶段,设计不同的输送策略,借助图像分割技术,配合心脏搏动实现精准自动释放。
34.3、合理人工干预,提高手术可靠性和安全性:在远程控制软件中设计手动控制模式,并设置手动控制面板,允许医生远程进行手动控制,防止意外情况的发生。
35.4、基于图像分割技术,实现了高度自动化的tmvi手术,解决了现有瓣膜输送系统可控性,精确性,安全性低的问题,同时保护术者免于辐射危害,并使远程手术成为可能;特别地,本系统也可以应用于其他瓣膜置换术,以及血管外科和肝胆外科的介入治疗等。
附图说明
36.附图1为本发明提供的一种基于图像分割的自动化瓣膜支架输送系统的远程控制软件的参数设置页面示意图。
37.图2为本发明提供的一种基于图像分割的自动化瓣膜支架输送系统的远程控制软件的超声图像预选标记页面示意图。
38.图3为本发明提供的一种基于图像分割的自动化瓣膜支架输送系统的远程控制软
件的过程控制页面示意图。
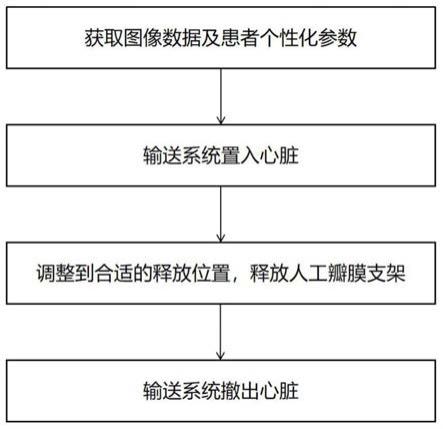
39.图4为本发明提供的一种基于图像分割的自动化瓣膜支架输送系统的输送方法的流程图。
40.图5为本发明提供的一种基于c
‑
v模型的预选标记对象的实时识别流程图。
41.图6为本发明涉及的一种c
‑
v模型的算法流程图。
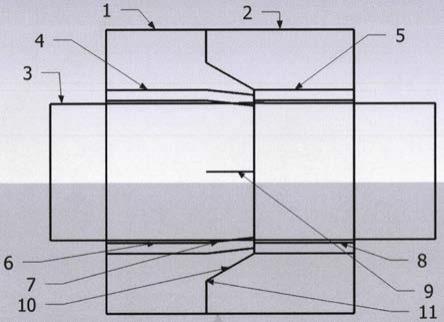
42.图7为本发明提供的一种输送装置置入心脏过程的参数定义示意图(1)。
43.图8为本发明提供的一种输送装置置入心脏过程的参数定义示意图(2)。
44.图9为本发明提供的一种输送装置位置调整过程的参数定义示意图。
45.图10为本发明提供的一种输送装置撤出心脏过程的参数定义示意图。
具体实施方式
46.下面结合实施例并参照附图对本发明作进一步描述。
47.实施例1
48.为了使本技术领域的人员更好地理解本说明书中的技术方案,下面将结合本说明书实施例中的附图,对本说明书实施例中的技术方案进行清晰、完整的描述。显然,所描述的实施例仅仅是本技术的一部分实施例,而不是全部的实施例。基于本说明书实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都应当属于本技术的保护范围。
49.本说明书提供的一种基于图像分割的自动化瓣膜支架输送系统,由以下3个部分组成:远程控制软件、机械臂、支架输送装置;
50.所述远程控制软件以visual studio 2019为开发平台,采用c#语言编写;该软件通过wi
‑
fi与输送装置和机械臂分别建立远程连接,进行自动或手动的运动控制;自动控制以图像分割为基础,采用了c
‑
v(chan
‑
vese)算法,实现了输送装置位置、二尖瓣活动状态、人工支架释放阶段等的实时监测;软件主要由三个页面组成:控制页面、超声图像预选标记页面以及参数设置页面;
51.如图1,在参数设置页面,术者可以根据经验和术前分析,设置输送装置在不同输送阶段的理想运动速度和临界停止距离;所有参数设置完成后点击“保存”即设置成功,系统将按照该组参数运行直至下次修改;此外,术者可通过“设为默认”按钮将本次设置的参数保存为默认参数,并在下次手术时通过“恢复默认”按钮自动填充所有参数;
52.如图2,在超声图像预选标记页面,当超声数据接入后,该页面将实时显示超声探头捕获的图像;术者可以在识别过程开始前,通过鼠标移动标记左心房、二尖瓣前尖瓣、二尖瓣后尖瓣和输送装置的预选框;标记完成后点击下方“确认”按钮提交;若中途出现绘制错误,可点击“重绘”按钮重新进行标记;
53.如图3,控制页面可以监控手术过程,并允许术者对手术过程进行适当干预,以避免意外的危险情况发生,保证手术过程安全可靠;在左上角的监控窗口中,可以选择查看二维超声心动图、三维超声心动图或dsa影像;其中,二维和三维超声心动图均可选择是否显示识别结果;在右上角的状态检测模块中,可以进行机械臂、输送装置和远程控制软件的连接,并查看连接状态;当连接状态均显示为“已连接”,工作状态均显示为“就绪”时,系统工作正常;由于在使用本系统时,手术过程是高度自动化的,故本页面下方为机械臂和输送装
置分别单独设置了手动控制按钮;其中,在机械臂的手动控制模块中,末端执行器平面系二尖瓣环平面,即垂直于输送装置运动方向的平面;绝对坐标平面系竖直平面;
54.所述机械臂可采用一般六轴机械臂,用于夹持支架输送装置,在手术过程中进行瓣膜支架的位置调整;六轴机械臂满足三维空间中的六个自由度,理论上其末端可以到达空间中的任何位置及角度,适合于几乎任何轨迹的工作;
55.所述支架输送装置,其主要作用是携带压缩后的瓣膜支架进入心脏,完成释放和固定;
56.图4为本说明书提供的一种基于图像分割的自动化瓣膜支架输送系统的输送流程;该流程包括:
57.步骤s101:从外接超声设备输入的二维和三维dicom数据中,解析所需信息,将二维超声心动图、三维超声心动图实时显示在远程控制软件的控制界面中;
58.支架输送装置在心脏内的实时位置,可以通过图像分割的方法,利用二维和三维超声心动图进行监测;二维超声心动图,即利用超声波从人体反射回来的回波信号,以光点的形式组成切面图像,可从二维空间清晰、直观地实时显示心脏各结构的形态、空间位置及连续关系等,适合于各种类型心血管疾病的检查;从系列二维图像重建的三维图像能提供准确的解剖信息,因此,三维超声心动图可以作为二维超声心动图的补充,提供准确的三维形态、空间位置关系等方面的参考;
59.dicom是医学图像及其相关信息传输的国际标准协议,广泛应用于心血管成像以及如超声、x射线、ct等的放射诊疗设备中;在dicom标准中,详细定义了医学影像及其相关信息的组成格式和交换方法;利用该标准,人们可以通过在医疗影像设备上建立一个接口,来完成影像数据的输入、输出工作;
60.在dicom数据结构标准中,定义了数据集来保存单次诊断的全部信息(患者信息 图像数据);根据内容,可以将dicom文件的数据元素大致分为patient,study,series和image四类;其中,image类数据中包含图像的大小和高度等信息,并以像素阵列的形式存储医学影像画面,阵列中的第一个字节表示图像左上角的像素,而最后一个字节表示图像右下角的像素;
61.所述远程控制软件对dicom数据进行读取和解析,提取图像大小、高度、宽度、每像素字节数等所需信息,并将二维和三维超声心动图实时显示在控制页面中;
62.步骤s102:获取术前术者设置的患者个性化参数,以便手术过程可以依据患者的个人情况进行调整;
63.记输送装置置入第一阶段的理想前进速度为v1,临界停止距离为d1;第二阶段的理想前进速度为v2,临界停止距离为d2;记输送装置回撤第一阶段的理想后撤速度为v3,临界停止距离为d3;第二阶段的理想后撤速度为v4;记人工瓣膜位置调整时的输送装置理想运动速度为v5;
64.步骤s201:进入自动输送过程;术者须在二维超声心动图中设置预选框,即框选出左心房、二尖瓣的前尖瓣、二尖瓣的后尖瓣和输送装置的大致位置;预选框为椭圆形,应尽可能贴合目标边缘,且各预选框之间允许重叠;
65.步骤s202:以术者标注的四个预选框为首帧图像的初始化边界,采用c
‑
v模型对二维超声心动图进行实时分割;
66.c
‑
v(chan
‑
vese)模型是基于区域的水平集方法,运行速度快、对噪声和对初始演化曲线的状态不敏感,且针对背景与分割对象的像素平均值明显不同的图像,具有良好的分割效果;该算法采用水平集方法表示演化曲线,并构造能量函数,求其euler
‑
lagrange方程,也即演化方程;最后,演化曲线会在能量函数的作用下开始演化,当能量函数的值达到最小时,即可实现对图像的分割;具体分割步骤如下:
67.步骤s202
‑
1:确定初始演化曲线;
68.由于c
‑
v模型具有对初始演化曲线不敏感的优点,因此,直接选取术者手动标注的预选框作为首帧图像的初始演化曲线;此外,考虑到视频的连续性,对于首帧外的其他帧,取每帧图像的输出结果作为下一帧图像的初始演化曲线;
69.具体地,为减少迭代次数并提高分割的准确性,术者手动标注预选框时,应尽量使椭圆形的预选框与识别对象贴合;手动标注完成后,将自动根据预选框的相对位置检验是否标注完全或存在误标注,同时确定各预选框所标注的具体内容:根据人体结构和所述超声探头的放置要求,相对位置按照从上至下、从左至右的顺序,应当依次为左心房、前尖瓣、后尖瓣和输送装置;
70.步骤s202
‑
2:构建能量函数;
71.能量函数由长度约束项、面积约束项和保真项构成;其中,长度约束项和面积约束项用于保证演化曲线在演化过程中的平滑性;保真项则与演化曲线内、外的灰度值有关,系曲线演化的动力;
[0072][0073]
式中,c表示演化曲线,u0(x,y)表示待识别图像中某点处的灰度值,inside(c)表示演化曲线内部,outside(c)表示演化曲线外部;参数c1、c2分别表示演化曲线内部、外部的平均灰度值,μ、v、λ1、λ2分别表示长度约束项、面积约束项和保真项的系数;通常取μ≥0,v≥0,λ1、λ2>0;
[0074]
将上述关于曲线c的能量函数写成关于水平集函数φ(x,y)的能量函数;当(x,y)位于演化曲线内部时,φ(x,y)>0;当(x,y)位于演化曲线外部时,φ(x,y)<0;
[0075][0076]
其中,ω表示待识别图像,h
ε
(z)和δ
ε
(z)是规整化后的海氏(heaviside)函数和狄拉克(dirac)函数;
[0077][0078][0079]
最小化上述能量函数可得到c1、c2的表达式:
[0080][0081][0082]
步骤s202
‑
3:获得演化方程;
[0083]
针对c
‑
v模型的能量函数,求其欧拉
‑
拉格朗日方程:
[0084][0085]
φ(o,x,y)=φ0(x,y)inω,
[0086][0087]
步骤s202
‑
4:迭代求解及验证;
[0088]
根据事先设置的迭代次数,重复进行求解;对迭代得到的轮廓进行检验,统计其位于预选框内的像素点个数占总像素点个数的百分比;若结果大于80%则认为识别正确,否则认为迭代失败;迭代失败的帧将再次重新尝试求解,若仍迭代失败,则该帧丢弃;
[0089]
此时,已完成单帧图像单个轮廓的识别任务;在本系统中,每帧图像有多个轮廓待识别,故按照从上至下、从左至右的顺序,串行识别每帧中的多个轮廓;
[0090]
步骤s203:根据每帧图像中的四个识别轮廓,计算出输送装置置入过程的各参数;
[0091]
具体地,记左心房的轮廓线为曲线s1,分别画出后尖瓣、前尖瓣、输送装置的最小外接矩形,并分别记为r1、r2、r3;
[0092]
识别5个测点;后尖瓣最小外接矩形r1的右下角为测点1,前尖瓣最小外接矩形r2的左下角为测点2,输送装置最小外接矩形r3靠近心房端的边的中点为测点3,输送装置最小外接矩形r3远离心房端的边的中点为测点4;根据测点3和测点4确定一条直线,与左心房的轮廓线s1交与两点,其中上方的点记为测点5;
[0093]
计算4个距离;记测点1和测点2之间的距离为l1,测点3和测点5之间的距离为l2,测点1和测点3之间的距离为l3,测点2和测点3之间的距离为l4;
[0094]
特别地,在开始的一段时间内,不断计算并记录l1的大小变化;记二尖瓣舒张时l1的大小为舒张距离ol,记二尖瓣收缩时l1的大小为收缩距离cl;
[0095]
步骤s204:进入输送装置置入的第一阶段;当所述支架输送装置的头端距离二尖瓣较远时,控制器控制输送装置以较快的速度向前运动;当所述支架输送装置的头端位于二尖瓣附近时,输送装置置入的第一阶段结束;
[0096]
在该阶段中,当距离l3和l4始终(即无论瓣膜舒张还是收缩)均大于临界距离d1时,将信息发送至控制器,控制输送装置以速度v1匀速向前运动;当检测到距离l3或l4小于d1时,发送停止信息,输送装置已抵达位置1,位于瓣膜附近,第一阶段运动结束;
[0097]
步骤s205:进入输送装置置入的第二阶段;当二尖瓣舒张时,所述支架输送装置小幅度向前运动;当二尖瓣收缩时,所述支架输送装置停止运动;当所述支架输送装置的头端到达左心房内的目标位置时,输送装置置入的第二阶段结束;
[0098]
在该阶段中,当检测到l1约等于舒张距离ol,且l2大于临界距离d2时,向控制器发
送相应信息,控制输送装置以速度v2匀速向前运动;当检测到l1约等于收缩距离cl时,即使l2大于临界距离d2,输送装置也需要停止运动;当检测到l2小于临界距离d2时,无论l1为何值,输送装置均立刻停止运动,同时标志着第二阶段结束;
[0099]
步骤s301:输送装置置入后,暂停对二维超声心动图的识别;术者须在三维超声心动图中,手动框选出二尖瓣环和输送装置头端,以便系统自动识别出二尖瓣环的准确轮廓,以及输送装置头端的准确轮廓;
[0100]
调整三维超声心动图的视角,使得二尖瓣环与观察平面平行,即输送装置外鞘与观察平面垂直;由于三维超声心动图立体成像的特点,在瓣膜舒张时,二尖瓣环和输送装置的轮廓较易分辨;因此,本系统首先逐帧判定瓣膜的活动状态,提取出瓣膜舒张状态的图像帧,再对其中二尖瓣环和输送装置的轮廓进行识别;
[0101]
具体地,首先逐帧判定瓣膜的活动状态;将图像转化为灰度图,记术者标注的二尖瓣环预选框为c';根据三维超声心动图的特点,当瓣膜舒张时,c'内的图像颜色较深,灰度值较小;当瓣膜收缩时,c'内的图像颜色较浅,灰度值较大;因此,在一个周期内,c'内的平均灰度值将由最小逐渐增大至最大,后又减小至最小;根据这一规律,一个周期内c'的像素平均灰度值,对时间求平均并记为参考值e;参考值e确定后,逐帧计算c'内的像素平均灰度值并与e进行比较,当灰度值小于e时,认为瓣膜处于舒张状态;
[0102]
提取出瓣膜舒张状态的图像帧,采用所述c
‑
v模型分割二尖瓣环轮廓及输送装置轮廓;
[0103]
步骤s302:根据每帧图像中的d形二尖瓣环和输送装置头端,计算出人工瓣膜和二尖瓣环共轴调整过程的各参数,并依据这些参数进行位置调整;
[0104]
识别4个测点;记二尖瓣环的轮廓线为曲线s2,支架输送装置头端的中心像素点为a;过a点画水平线交瓣膜轮廓线s2于测点6和测点7,画竖直线交瓣膜轮廓线s2于测点8和测点9;
[0105]
计算4个距离;计算点a与测点6之间的距离并记为l5,计算点a与测点7之间的距离并记为l6,计算点a与测点8之间的距离并记为l7,计算点a与测点9之间的距离并记为l8;
[0106]
进一步地,将所述l5,l6,l7,l8的距离信息发送至机械臂,通过远程控制软件控制机械臂在垂直于输送装置运动方向的平面(即二尖瓣环平面)内,进行人工瓣膜和二尖瓣环的共轴调整;当人工瓣膜和二尖瓣环共轴时,系瓣膜释放的最佳位置;
[0107]
步骤s303:将人工瓣膜调整到合适的释放位置后,向输送装置的控制器发送信息,释放瓣膜的心房侧;释放完成后,输送装置向后运动,使人工瓣膜与二尖瓣原有的瓣叶贴合紧密;
[0108]
在该阶段中,调整三维超声心动图的视角,使得二尖瓣环所在平面与观察平面呈一定角度;此时,术者须重新手动框选出识别框,该识别框内应包含二尖瓣环及人工瓣膜;
[0109]
求解识别框内的像素方差;当方差较大时,向控制器发送相应信息,控制输送装置以速度v5匀速向后运动;当方差较小时,遍历识别框内的所有像素点,若所有像素点的灰度值均较大,则认为人工瓣膜与二尖瓣叶已贴合紧密,输送装置停止运动;
[0110]
步骤s304:将信息发送至控制器,控制输送装置将瓣膜完全释放;
[0111]
步骤s401:瓣膜释放完成后,暂停对三维超声心动图的识别;术者须在二维超声心动图上重新设置预选框,分别框选出输送装置、人工瓣膜的前尖瓣和后尖瓣;
[0112]
步骤s402:以术者标注的三个预选框为首帧图像的初始化边界,采用c
‑
v模型对二维超声心动图进行实时处理;
[0113]
步骤s403:根据每帧图像中的三个识别轮廓,计算出输送装置撤出过程的各参数;
[0114]
具体地,分别画出人工瓣膜的后尖瓣、人工瓣膜的前尖瓣、输送装置的最小外接矩形,并分别记为r1’、r2’、r3’;
[0115]
识别3个测点;人工瓣膜的后尖瓣的最小外接矩形r1’的右下角为测点1’,人工瓣膜的前尖瓣的最小外接矩形r2’的左下角为测点2’,输送装置最小外接矩形r3’靠近心房端的边的中点为测点3’;
[0116]
计算3个距离;记测点1’和测点2’之间的距离为l1’,测点1’和测点3’之间的距离为l3’,测点2和测点3之间的距离为l4’;
[0117]
特别地,在开始的一段时间内,不断计算并记录l1’的大小变化;记人工瓣膜舒张时l1’的大小为人工瓣膜舒张距离ol’,记人工瓣膜收缩时l1的大小为人工瓣膜收缩距离cl’;
[0118]
步骤s404:进入输送装置撤出的第一阶段;当所述支架输送装置的头端未完全撤出左心房时,所述支架输送装置小幅度向后运动;当所述支架输送装置的头端完全撤出左心房时,输送装置撤出的第一阶段结束;
[0119]
在该阶段中,当检测到l1’约等于舒张距离ol’时,向控制器发送相应信息,控制输送装置以速度v3匀速向后运动;当检测到测点1’和测点2’均位于测点3’的上方,且l3’和l4’的大小均大于临界距离d3时,标志着输送装置已完全撤出左心房,输送装置撤出的第一阶段结束;
[0120]
步骤s405:进入输送装置撤出的第二阶段;在该阶段中,控制器控制输送装置以较快的速度向后运动,直至输送装置完全撤出;
[0121]
在该阶段中,控制器控制输送装置以速度v4匀速向后运动,直至在二维超声心动图中无法再检测到输送装置,输送装置撤出的第二阶段结束;至此,自动化输送流程结束;
[0122]
本说明书描述了一种基于图像分割的自动化瓣膜支架输送系统的使用实例;在实例中,输送装置在食道超声造影的引导下,自动完成经导管二尖瓣瓣膜置入术;由超声引导、输送装置和机械臂执行的自动化手术,使术者能够远程操作,避免辐射伤害,同时提高手术的可控性和安全性,具有较高的社会价值。
[0123]
本说明书中对该系统使用实例的描述按照基本操作步骤进行,各步骤间原理相同的部分为避免重复不再赘述,可参照上文描述;系统中,部分涉及的编程算法底层实现,考虑到其通用性,未进行详细描述,采用常规方法达到要求即可。
[0124]
本说明书中所述仅为本系统的一种具体使用实例,本系统也可以应用于其他瓣膜置换术,以及血管外科和肝胆外科的介入治疗等。
[0125]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明原理的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。