mirna联合标志物在制备诊断或检测hbv 且lc
‑
原发性hcc的试剂盒中的应用
技术领域
1.本发明涉及分子生物学和医学诊断领域,具体涉及一种mirna联合标志物在制备诊断或检测hbv 且lc
‑
原发性hcc的试剂盒中的应用。
背景技术:
2.原发性肝癌是世界范围内发病率和死亡率最高的恶性肿瘤之一。肝细胞癌(hcc)是原发性肝癌的主要形式,通常由肝硬化、hbv感染等慢性肝病演化而来。早期hcc五年生存率为50%
‑
70%,而晚期肝癌患者仅为10%
‑
19%,因此,早诊早筛是肝癌治疗的关键。由于缺乏有效区分早期肝癌患者和慢性肝病患者的早期诊断方法,目前hcc的诊断主要还是依赖于影像学、血清afp和组织活检,具有一定的滞后性,大多数患者在初诊时已经是晚期。因此,临床上亟需开发新型生物标志物用于肝癌患者的早期诊断。
3.外泌体(exosome)是一类直径大小在40
‑
160nm(平均100nm),能被大多数细胞分泌,进入血液循环系统的胞外囊泡。外泌体携带了膜蛋白、核蛋白、dna、mrna、非编码rna等生物信息,参与细胞活动的重要调控,在肿瘤转移、免疫调控机制、疾病发生发展中发挥重要作用。微小rna(microrna,mirna)是一类长度在19
‑
24nt的非编码单链rna,一般通过与目标信使rna(mrna)部分或完全的互补配对,导致mrna的降解或翻译的抑制,起到转录后调控的作用,在生物发育的各个环节,以及包括肿瘤在内的多种疾病的发生发展中发挥功能。同时,相比于外泌体中其他类型的生物信息,mirna片段更小,更为稳定。因此,来源于外泌体的mirna可作为一类潜在的肿瘤分子标志物。
4.本领域已发现has
‑
mir
‑
29a、has
‑
mir
‑
29c、has
‑
mir
‑
133a、has
‑
mir
‑
143、has
‑
mir
‑
145、has
‑
mir
‑
192、has
‑
mir
‑
505等7个mirna组成的panel可用于肝癌的动态监测。本领域也发现基于has
‑
mir
‑
122、has
‑
mir
‑
192、has
‑
mir
‑
21、has
‑
mir
‑
223、has
‑
mir
‑
26a、has
‑
mir
‑
27a、has
‑
mir
‑
801的检测可用于肝癌的早期诊断。但是,原发性肝癌发病机理较为复杂,不同类型的患者生物标志物可能不尽相同,现有panel一般针对所有类型肝癌患者,缺乏针对性。本发明基于来源于外周血外泌体中异常表达的mirna,针对hbv阳性(hbv )且肝硬化(lc
‑
)的hcc患者提出针对性panel用于肝癌的早期诊断。
技术实现要素:
5.本发明的第一个目的是针对现有技术的不足,提供mirna联合标志物在制备诊断或检测hbv阳性(hbv )且肝硬化阴性(lc
‑
)的原发性hcc的试剂盒中的应用,其中mirna联合标志物为来源于血浆外泌体的hsa
‑
mir
‑
146a
‑
5p和hsa
‑
mir
‑
154
‑
5p。
6.本发明的第二个目的是提供诊断或检测hbv阳性(hbv )且肝硬化阴性(lc
‑
)的原发性hcc试剂盒,包括:特异性检测人hsa
‑
mir
‑
146a
‑
5p和hsa
‑
mir
‑
154
‑
5p的检测试剂。
7.本发明的第三个目的是提供外周血外泌体mirna联合标志物作为hbv阳性(hbv )且肝硬化阴性(lc
‑
)的原发性hcc辅助诊断指标的应用,其中mirna联合标志物为来源于血
浆外泌体的hsa
‑
mir
‑
146a
‑
5p和hsa
‑
mir
‑
154
‑
5p。
8.本发明的第四个目的是提供一种hbv阳性(hbv )且肝硬化阴性(lc
‑
)的原发性hcc血清外泌体标志物,包括hsa
‑
mir
‑
146a
‑
5p和hsa
‑
mir
‑
154
‑
5p。
9.本发明的第五个目的是提供一种hbv阳性(hbv )且肝硬化阴性(lc
‑
)的原发性hcc诊断制剂,包括mirna联合标志物hsa
‑
mir
‑
146a
‑
5p和hsa
‑
mir
‑
154
‑
5p。
10.本发明的优点和有益效果如下:
11.1.外泌体mirnas是一种新型的液体活检生物标志物,更为灵敏、稳定、无创,且需要的样本量较少,患者更容易接受,其成功开发有助于肝癌的辅助诊断。
12.2.基于多个mirnas设计的产品相较于单一mirnas的产品,在灵敏度和特异性上会更优,且可以减少因单一指标个体表达差异导致的误差,使结果更加准确。
13.3.肝癌发病因素很多,本发明针对hbv阳性(hbv )的非肝硬化(lc
‑
)原发性hcc予以检测,针对性更强,检测结果也更有说服力。
附图说明
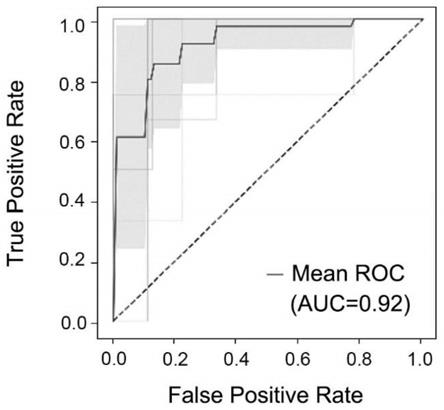
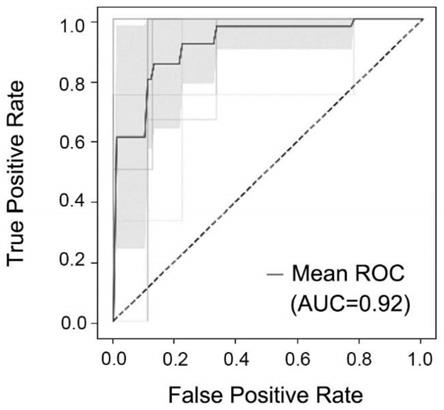
14.图1为roc曲线分析采用mirnapanel鉴定hbv /lc
‑
的hcc患者和hbv /lc
‑
患者的检测结果。
15.图2为roc曲线分析采用肝癌血清学标志物甲胎蛋白(afp)鉴定hbv /lc
‑
的hcc患者和hbv /lc
‑
患者的检测结果。
具体实施方式
16.下面结合具体实施例对本发明做进一步的分析。
17.外泌体提取试剂盒exo
‑
quick exosome precipitation solution(exoq5sa
‑
1,sbi,united states),mirneasy serum/plasma kit试剂盒(217184,qiagen,germany)、mgieasy small rnalibrary prep kit(1071073,mgi,china)试剂盒以及ngs测序仪用于mirna测序。
18.本发明hsa
‑
mir
‑
1307
‑
3p、hsa
‑
mir
‑
221
‑
3p、hsa
‑
mir
‑
323b
‑
3p、hsa
‑
mir
‑
150
‑
5p、hsa
‑
mir
‑
134
‑
5p、hsa
‑
mir
‑
4433b
‑
3p、hsa
‑
mir
‑
222
‑
3序列可通过公开网站http://www.mirbase.org/获知,并由对应的accession number确定。
19.实施例1受试者及样本提取
20.样本由新加坡中央医院(singapore general hospital)提供(经新加坡singhealth cirb b审批,审批号cirb ref:2007/447/b)。其中hbv /lc
‑
的hcc患者34例,hbv /lc
‑
的非hcc患者89例。
21.实施例2外泌体的提取
22.用一次性针筒采集受试者外周血2ml,迅速转入edta抗凝管,混匀。在采集的2h内分离血浆,具体步骤为:1)转移全血至2ml离心管,室温,500g离心10min;2)取上层血浆,4℃,2000g离心10min;3)取上层血浆,4℃,16000g离心10min;4)分离出的血浆直接用于外泌体提取或冻存于
‑
80℃冰箱。
23.按照外泌体提取试剂盒exo
‑
quick exosome precipitation solution(exoq5sa
‑
1,sbi,united states)操作说明提取外泌体。1)将血浆加入离心管,按每250μl血浆加入63
μl的比例加入exo
‑
quick;2)1500g,4℃离心30分钟,弃上清;3)1500g,4℃离心5分钟,弃上清;4)200μl pbs重悬,冻存于
‑
20℃。
24.实施例3外泌体mirna的提取
25.按照mirneasy serum/plasmakit试剂盒(217184,qiagen,germany)的操作说明书提取mirna。具体步骤为:1)在实施例2分离出的血浆添加5倍体积的qiazol lysis reagent,涡旋混匀或吸打混匀;2)室温孵育5min;3)加入等体积氯仿,震荡15s;4)室温孵育2
‑
3min;5)4℃,12000g离心15min;6)转移上层液体至新的离心管,加入1.5倍体积无水乙醇,吸打混匀,得到样本;7)取700μl样本至rneasy minelute spin column(置于2ml收集管中),盖上盖子,室温>8000g离心15s,弃去;8)重复步骤7一次;9)加入700μl rwtbuf至rneasy minelute spin column,室温>8000g离心15s,弃去;10)加入500μl rpe buf至rneasy minelute spin column,室温>8000g离心15s,弃去;11)加入500μl 80%乙醇(现配)至rneasy minelute spin column,室温>8000g离心2min,弃去;12)将rneasy minelute spin column置于新的收集管,开盖,高速离心5min;13)将rneasy minelute spin column置于1.5ml收集管,加入14μl rnase
‑
free水,高速离心1min。
26.实施例4ngs测序分析mirna
27.提取的mirna经nanodrop 2000spectrophotometer(thermo fisher scientific,usa)检测浓度后,采用mgieasy small rnalibrary prep kit(1071073,mgi,china)构建文库,采用bgiseq
‑
500进行测序。所得数据采用deseq2、limma和edger等三个r语言包分析mirna表达水平,将|log2 fold change|>
‑
1.5且adjustedp
‑
value<0.05的视为差异表达mirna:hsa
‑
mir
‑
146a
‑
5p和hsa
‑
mir
‑
154
‑
5p。
28.实施例5验证mirna组合对hbv阳性(hbv )且非肝硬化(lc
‑
)的原发性hcc发生的预测
29.以hsa
‑
mir
‑
146a
‑
5p和hsa
‑
mir
‑
154
‑
5p作为检测对象,通过spss软件的“roc曲线图”功能,绘制roc曲线。分析显示,若2个基因均显著下调(|log
2 fold change|>1.5,p
‑
value<0.05),在区分hcc组和非hcc组时,其auc值为0.92(图1)。而以血清学标志物甲胎蛋白(afp)作为指标的区分hcc和非hcc患者的auc值仅为0.80(图2)。
30.上述实施例并非是对于本发明的限制,本发明并非仅限于上述实施例,只要符合本发明要求,均属于本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。