1.本发明属于水杨酸检测技术领域,特别是一种荧光微米探针检测水杨酸的方法和应用。
背景技术:
2.水杨酸(salicylic acid,sa),化学名称为邻羟基苯甲酸,是植物体内常见的一种小分子酚类化合物,由于水杨酸具有广谱、稳定性好、不挥发等特点,在许多医药产品中被广泛用作抗微生物和抗真菌剂,通常用于治疗常见的皮肤病,如痤疮、愈伤组织和牛皮癣,以及缓解疼痛和退烧,但长期使用高剂量的水杨酸会引起恶心和头晕以及胃肠道不良反应。此外,由于sa具有抗粉刺和美白作用,化妆品中也已被广泛添加使用,用于日常生活中的护肤、美容和皮肤病治疗。然而,过度使用这种化合物会对消费者的健康产生负面影响如刺激,并可能对皮肤造成伤害,测定药品以及化妆品中的水杨酸对于质量保证和消费者安全尤为重要。
3.现有技术中,检测sa浓度的方法主要有紫外分光光度法、荧光分光光度法、比色度法、电化学分析法、气相色谱法和高效液相色谱法等,但这些方法往往需要昂贵的仪器、耗时、复杂的操作等,很少适合常规分析。近年来,由于荧光探针具有选择性好、灵敏度高、便于观察、能够实时检测等良好的特性,可以利用荧光探针对sa进行检测,但大多数荧光探针响应时间慢和灵敏度差。
技术实现要素:
4.本发明的主要目的是提供一种荧光微米探针。
5.本发明的另一目的是提供上述荧光微米探针在检测水杨酸中的应用,响应时间快且灵敏度高,尤其是药品或化妆品中水杨酸的快速检测。
6.为实现上述目的,本发明采用如下技术方案:
7.一种荧光微球,是姜黄素与六氯环三磷腈形成的共聚物,其中姜黄素的羟基与六氯环三磷腈的氯缩合形成共聚物。
8.优选地,荧光微球的粒径为0.5
–
2微米。
9.上述荧光微球的制备方法,包括以下步骤:
10.(1)环三磷腈和姜黄素溶于有机溶剂;
11.(2)加入三乙胺,反应4
–
12小时。
12.步骤(1)的有机溶剂为乙腈、甲苯、四氢呋喃或dmf,优选为乙腈。
13.步骤(1)中,六氯环三磷腈与姜黄素的摩尔比为1:1.5
–
5,优选为1:2
–
4,在本发明的优选方式中,六氯环三磷腈与姜黄素的摩尔比为1:3。
14.步骤(2)中,六氯环三磷腈摩尔比为1:50
–
150,优选为1:80
–
100,在本发明的优选方式中,六氯环三磷腈与三乙胺的摩尔比为1:90。
15.步骤(2)反应结束后,离心或过滤、抽滤收集沉淀,用水和乙醇洗涤并干燥。
16.一种荧光微米探针,为上述荧光微球与铝离子的混合物。
17.将上述荧光微球溶解于乙醇溶液,再与铝盐溶液混合形成荧光微米探针,混合体系中的荧光微球与铝离子的质量比为1:1
–
2,优选为1:1.7。
18.一种检测水杨酸的方法,步骤如下:
19.(1)将上述荧光微球溶解于乙醇溶液中,再与铝盐溶液混合;混合体系中的pc与al(iii)的质量比为1:1
–
2,优选为1:1.7;然后加入待测样品混合;
20.(2)步骤(1)的混合物与待测样品混合,以313nm为激发波长,测定400nm处的荧光发射强度,进行定性或定量检测。
21.步骤(1)中,荧光微球的乙醇溶液与铝盐溶液混合后,用乙醇溶液稀释至荧光微球的含量为50
–
100μg/ml。
22.本发明中检测水杨酸的浓度线性范围为0.5
‑5×
10
‑5mol/l,最低检出限为0.1μmol/l。
23.荧光微米探针识别水杨酸的机理:由于水杨酸与金属离子良好的配位能力,水杨酸与探针中的al(ii)结合形成pc
‑
al(iii)
‑
sa的三元体系,释放出荧光信号,使体系荧光增强。
24.本发明的有益效果在于:
25.(1)本发明所获得的荧光微球、探针可以用于水杨酸检测,是一种荧光增强型探针,相对于荧光淬灭型探针具有较好的专一选择、抗干扰性和较高的灵敏度;本发明利用水杨酸与金属离子良好的配位能力,在探针与水杨酸结合后释放出强烈的紫色荧光,溶液体系荧光显著增强,从而实现对水杨酸的检测。
26.(2)本发明提出一种基于络合机制的聚磷腈超支化微米级荧光探针,通过水杨酸与金属离子的络合能力来实现荧光增强识别水杨酸,利用姜黄素作为荧光团,通过荧光团的羰基实现与金属离子的络合并调制荧光变化,聚磷腈的超支化骨架有利于“姜黄素
‑
金属离子
‑
水杨酸”微反应器的构建,以提高复杂背景干扰下的荧光信号稳定性和传感性能,在多种金属离子和水杨酸类物质的复杂模拟样品环境中实用性强。
27.(3)本发明对水杨酸小分子的最低检测限为0.1μmol/l,并实现1min内的快速响应,检测过程简便、抗干扰能力强、快速、灵敏,检测结果准确,可用于水杨酸的检测,尤其是药品和化妆品中水杨酸的快速检测。
附图说明
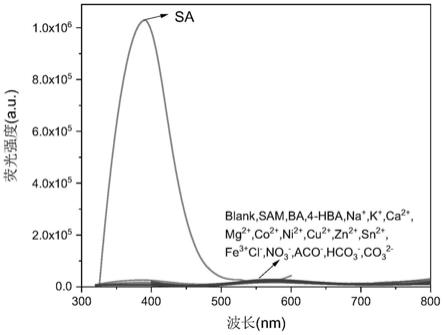
28.图1为实施例中荧光微米探针pc
‑
al(iii)荧光选择性图,激发波长为313nm。
29.图2为实施例中荧光微米探针pc
‑
al(iii)识别水杨酸的抗干扰性图,激发波长为313nm。
30.图3为实施例中荧光微米探针pc
‑
al(iii)对水杨酸的响应时间图。
31.图4为实施例中荧光微米探针pc
‑
al(iii)识别水杨酸的稳定性。
32.图5为实施例中荧光微米探针pc
‑
al(iii)识别水杨酸的荧光滴定图,激发波长为313nm。
33.图6为实施例中荧光微米探针pc
‑
al(iii)识别水杨酸的最低检测限图,激发波长为313nm。
具体实施方式
34.下面将结合本发明实施例,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有付出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
35.制备荧光微米探针pc
‑
al(iii)的过程中所使用的化学试剂、溶剂均购自探索公司,金属离子等均购自阿拉丁试剂公司,采用英国爱丁堡fs
‑
5荧光分析仪记录荧光光谱。
36.实施例1荧光微球和荧光微米探针的制备
37.(一)荧光微球的制备
38.250ml圆底烧瓶中,将0.10g(0.30mmol)六氯环三磷腈(hccp)和0.32g(0.90mmol)姜黄素溶于50ml乙腈中,待六氯环三磷腈和姜黄素完全溶解于至乙腈溶液后,加入2ml三乙胺(约27mmol),室温下搅拌8h。反应完全后离心得到下层沉淀物,用乙醇和纯净水洗涤至上清液澄清为止,将所得到的沉淀物50℃真空干燥12h,得到颗粒粒径在0.5
–
2微米的淡黄色粉末,技术路线为:
[0039][0040]
(二)荧光微米探针pc
‑
al(iii)的制备
[0041][0042]
用乙醇溶液配制浓度为12mg/ml的pc溶液,用纯净水配制浓度为100mg/ml的al(no3)3·
9h2o水溶液(铝离子浓度7mg/ml),在2ml的乙醇溶液中加入10μl的pc溶液和10μl的al(iii)溶液,混合均匀,即制备完成探针。
[0043]
实施例2荧光专一选择性
[0044]
配制12mg/ml的pc的乙醇溶液和100mg/ml的al(iii)水溶液,在比色皿中加入2ml的乙醇溶液、10μl的pc溶液以及10μl的al(iii)水溶液,用荧光光谱仪考察探针pc
‑
al(iii)对水杨酸等小分子的选择性。如图1所示,在313nm处激发条件下,单独的探针pc
‑
al(iii)在乙醇溶液中在400nm处具有微弱的荧光发射强度,当加入水杨酸后,在400nm处的荧光发射强度明显增强,加入其它物质时,溶液体系的荧光发射强度与单独探针体系的荧光发射强度相比没有明显变化,表明探针pc
‑
al(iii)对水杨酸在乙醇溶液中具有较好的荧光专一选择性。
[0045]
实施例3抗干扰性测试
[0046]
配制12mg/ml的pc的乙醇溶液和100mg/ml的al(iii)水溶液,在18个干净的荧光比色皿中,分别加入2ml的乙醇溶液和10μl的pc溶液和10μl的al(iii)溶液,再分别加入10μm的水杨酸和100μm的其他分析物,如:
[0047]
其它类小分子:水杨酰胺(sam)、苯甲酸(ba)、对羟基苯甲酸(4
‑
hba);
[0048]
阳离子:na
、k
、ca
2
、mg
2
、co
2
、ni
2
、cu
2
、zn
2
、sn
2
、fe
3
;
[0049]
阴离子:cl
‑
、no3‑
、aco
‑
、hco3‑
、co
32
‑
,在荧光光谱仪上检测,绘制不同分析物对应的最高荧光强度的荧光发射柱状图,如图2所示,证明探针pc
‑
al(iii)对水杨酸在乙醇溶液中的识别不受上述其他分析物的干扰,具有较好的抗干扰性。
[0050]
实施例4响应时间测试
[0051]
配制12mg/ml的pc的乙醇溶液和100mg/ml的al(iii)水溶液,在比色皿中加入2ml的乙醇溶液,10μl的pc溶液以及10μl的al(iii)溶液,用荧光光谱仪考察了探针pc
‑
al(iii)对水杨酸小分子的响应时间。pc
‑
al(iii)可以在1min内实现对水杨酸的检测,如图3所示,证明探针pc
‑
al(iii)对水杨酸能够快速响应可以在乙醇溶液中实现对水杨酸的快速检测。
[0052]
实施例5稳定性测试
[0053]
配制12mg/ml的pc的乙醇溶液和100mg/ml的al(iii)水溶液,在比色皿中加入2ml的乙醇溶液、10μl的pc溶液以及10μl的al(iii)溶液并保持在0
‑
120min内测定其对水杨酸的检测效果。如附图4所示,探针pc
‑
al(iii)的荧光和探针pc
‑
al(iii)对水杨酸检测的荧光强度在2h内几乎没有变化,结果表明探针pc
‑
al(iii)在乙醇溶液体系中表现出良好的稳定性。
[0054]
实施例6线性回归方程
[0055]
配制12mg/ml的pc的乙醇溶液和100mg/ml的al(iii)水溶液,配制2mmol/l浓度的水杨酸溶液,把2ml的乙醇溶液、10μl的pc和10μl的al(iii)水溶液加到干净的荧光比色皿中,逐渐加入水杨酸溶液的体积分别为0、5μl、10μl、15μl、20μl、25μl、30μl、35μl、40μl、45μl、50μl、55μl同时以313nm为激发波长,在荧光光谱仪上测定400nm处的荧光发射强度,以水杨酸的浓度为横坐标,以400nm处的荧光强度为纵坐标,得到水杨酸浓度的工作曲线,线性回归方程为f
400nm
=3.58
×
10
10
c
‑
1.05
×
10
‑5,c的单位为mol/l,如图5所示。
[0056]
实施例7最低检出限实验
[0057]
良好的检出限是检验一个探针分子是否具有应用价值的标准之一,配制12mg/ml的pc的乙醇溶液和100mg/ml的al(iii)水溶液,把2ml的乙醇溶液和10μl的pc和10μl的al(iii)水溶液加到干净的荧光比色皿中,测定其对不同浓度的水杨酸的响应强度,随着水杨酸浓度的增加,体系荧光发射强度在400nm处不断增强,发现溶液荧光发射强度在水杨酸浓度线性范围为0.5
‑5×
10
‑5mol/l(r2=0.986),经计算(3σ/k)得出该探针分子对水杨酸的检出限为0.1μmol/l(图6),表明该探针pc
‑
al(iii)对水杨酸的检测具有潜在的应用价值。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。