涉及白介素
‑
2(il2)和干扰素(ifn)的治疗
技术领域
1.本公开内容涉及用于增强免疫效应细胞之作用的方法和药剂,所述免疫效应细胞特别是响应于白介素
‑
2(interleukin
‑
2,il2)的免疫效应细胞(例如效应t细胞,例如cd8 t细胞)。特别地,这些方法和药剂可用于治疗以表达所述免疫效应细胞所针对的抗原的病变细胞为特征的疾病。具体地,本公开内容涉及包括向对象施用以下的方法:包含il2或其功能性变体(本文中通常称为“il2”)的多肽或者编码包含il2或其功能性变体的多肽的多核苷酸,以及包含i型干扰素(interferon,ifn)或其功能性变体(本文中通常称为“干扰素”或“ifn”)的多肽或者编码包含i型干扰素或其功能性变体的多肽的多核苷酸。提供给对象的il2作用于免疫效应细胞,例如效应t细胞,并导致免疫效应细胞作用的增强,例如通过促进免疫效应细胞的扩增;而干扰素阻止或降低il2介导的调节性t细胞(treg)的扩增,这将抵消免疫效应细胞的作用。本公开内容的方法还可包括向对象施用疫苗抗原或编码其的多核苷酸,以提供(任选地在适当的靶细胞表达多核苷酸之后)抗原用于刺激、引发和/或扩增免疫效应细胞。在一个实施方案中,免疫效应细胞携带对抗原或其加工产物具有结合特异性的抗原受体,例如t细胞受体(t cell receptor,tcr)或嵌合抗原受体(chimeric antigen receptor,car)。在一个实施方案中,免疫效应细胞经遗传修饰以表达抗原受体。作为替代或补充,免疫效应细胞经遗传修饰以表达il2受体(il2 receptor,il2r)。这样的遗传修饰可离体或在体外实现并随后可将免疫效应细胞施用于需要治疗的对象,和/或这样的遗传修饰可在需要治疗的对象中在体内实现。免疫效应细胞可以来自需要治疗的对象,并且可以是在需要治疗的对象中内源性的。免疫效应细胞的抗原受体可靶向与疾病相关的抗原。在一个特别优选的实施方案中,根据本公开内容施用的编码il2的多核苷酸、编码ifn的多核苷酸和/或编码疫苗抗原的多核苷酸是rna。
背景技术:
2.免疫系统在癌症、自身免疫、变态反应以及病原体相关疾病中起着重要作用。t细胞和nk细胞是抗肿瘤免疫应答的重要介导物。cd8
t细胞和nk细胞可直接裂解肿瘤细胞。在另一方面,cd4
t细胞可介导不同的免疫亚群(包括cd8
t细胞和nk细胞)向肿瘤的流入。cd4
t细胞能够允许树突细胞(dendritic cell,dc)引发抗肿瘤cd8
t细胞应答,并且可通过ifnγ介导的mhc上调和生长抑制而直接作用于肿瘤细胞。可通过疫苗接种或通过t细胞的过继性转移来诱导cd8
以及cd4
肿瘤特异性t细胞应答。在基于mrna的疫苗平台的情况下,mrna可通过脂质体制剂(rna
‑
脂质复合体(rna
‑
lipoplex),rna
‑
lpx)被递送到位于次级淋巴器官中的抗原呈递细胞中,而无需任何另外的佐剂进行免疫刺激(kreiter,s.et al.nature 520,692
–
696(2015);kranz,l.m.et al.nature 534,396
–
401(2016))。
3.进一步改善t细胞临床效力的一个潜在途径是通过影响细胞存活和功能的细胞因子支持和调节所述细胞。例如,白介素
‑
2(il2)是活化免疫系统的多种细胞的强效免疫刺激物。已知il2支持t细胞和nk细胞的分化、增殖、存活和效应子功能(blattman,j.nnat.med.9,540
–
7(2003)),并且已用于晚期恶性黑素瘤的治疗数十年(maas,r.a.,
dullens,h.f.&den otter,w.cancer immunother.36,141
–
8(1993))。
4.然而,存在一些与细胞因子施用相关的困难。重组细胞因子的血浆半衰期很短,产生了频繁注射大量细胞因子的需求。对于il2,这导致严重的副作用,例如血管渗漏综合征(vascular leak syndrome,vls)(rosenberg,s.n.engl.j.med.316,889
–
97(1987))。此外,细胞因子施用可对免疫细胞造成不期望的影响。例如,已知il2能够比效应t细胞更强效地刺激调节性t细胞(treg)(todd,j.plos med.13,e1002139(2016)),因为由cd25(il2rα)、cd122(il2rβ)和cd132(il2rγ)组成的高亲和力il2受体(il2rαβγ)在treg以及活化的cd4
和cd8
t细胞上表达,而缺乏cd25的中等亲和力受体(il2rβγ)在初始t细胞和记忆t细胞以及nk细胞上普遍存在。treg与癌症患者的存活降低相关,因为它们可抑制抗肿瘤效应t细胞和nk细胞的功能(nishikawa,h.&sakaguchi.curr.opin27,1
–
7(2014))。以使il2失去对表达cd25的细胞的偏好这样的方式来改变il2,从而相对提高对初始t细胞和记忆t细胞以及nk细胞的刺激潜力的尝试显示出提高了其抗肿瘤潜力(arenas
‑
ramirez,n.et al.sci.transl.med.8,1
–
13(2016))。
5.显然,需要新的策略来提高免疫治疗的有效性,特别是疫苗(例如癌症疫苗)和/或基于细胞的免疫治疗(例如基于细胞的癌症免疫治疗)的有效性,包括(初始或t细胞受体转基因或嵌合抗原受体转基因)t细胞和nk细胞的过继性转移。
6.为了解决细胞因子治疗存在的局限性,我们在本文中提供了新的策略来提高涉及il2治疗的免疫治疗的有效性。
7.本公开内容提供了用于阻止il2介导的treg扩增同时保留il2治疗的有益效果例如抗原特异性t细胞应答的扩增的手段和方法。
8.我们证明了编码与用于延长全身可用性的血清白蛋白融合的il2(alb
‑
il2)的mrna显著活化cd8 t细胞,并在小鼠体内强烈扩增疫苗诱导的抗原特异性t细胞。同时,alb
‑
il2导致treg的大量扩增,这强烈限制了抗原特异性t细胞的后续扩增。与alb
‑
il2一起同时施用编码ifnα的mrna阻止treg扩增,并允许持续增强疫苗诱导的抗原特异性t细胞。用分离的人t细胞进行的体外研究证实,ifnα阻止il2介导的treg活化,但不会强烈影响cd8 t细胞的活化。
技术实现要素:
9.本发明一般包括对对象的免疫治疗性治疗,其包括:施用包含il2或其功能性变体的多肽或者编码包含il2或其功能性变体的多肽的多核苷酸以提高免疫治疗的有效性,以及施用包含i型干扰素或其功能性变体的多肽或者编码包含i型干扰素或其功能性变体的多肽的多核苷酸以降低或阻止il2介导的不期望的作用,特别是treg扩增。免疫治疗可包括疫苗治疗和/或基于细胞的癌症免疫治疗,例如基于til或t细胞的治疗,例如使用例如自体细胞的基于tcr或car转基因t细胞的治疗。一般而言,使用本文中所述的治疗刺激的免疫效应细胞可靶向表达抗原的细胞,例如病变细胞,特别是表达肿瘤抗原的癌细胞。靶细胞可在细胞表面表达抗原或可呈递抗原的加工产物。在一个实施方案中,抗原为肿瘤相关抗原且疾病为癌症。这样的治疗提供了对表达抗原的细胞的选择性根除,从而使对不表达该抗原的正常细胞的不利影响最小化。待通过il2施用刺激且优选具有内源性il2受体(il2r)(或任选地经遗传修饰以表达il2r)的免疫效应细胞(任选地经遗传修饰以表达抗原受体)靶向
抗原或其加工产物,并且因此靶向表达该抗原的靶细胞群或靶组织。这样的免疫效应细胞可施用于需要治疗的对象,或者在需要治疗的对象中可以是内源性的。在一个实施方案中,免疫效应细胞携带il2受体(il2r)。在一个实施方案中,免疫效应细胞经遗传修饰以表达il2r。在一个实施方案中,免疫效应细胞携带对靶抗原或其加工产物具有结合特异性的抗原受体,例如t细胞受体(tcr)或嵌合抗原受体(car)。在一个实施方案中,免疫效应细胞经遗传修饰以表达抗原受体。用于表达il2r和/或抗原受体的这样的遗传修饰可离体或在体外实现并随后可将免疫效应细胞施用于需要治疗的对象,或者这样的遗传修饰可在需要治疗的对象中在体内实现,或者可通过离体或体外和体内修饰的组合实现。在一个实施方案中,施用疫苗抗原或编码其的多核苷酸以提供(任选地在通过适当的靶细胞表达多核苷酸之后)抗原用于刺激、引发和/或扩增靶向靶抗原或其加工产物的免疫效应细胞。在一个实施方案中,根据本公开内容的待诱导的免疫应答是针对表达免疫效应细胞所针对的抗原的靶细胞群或靶组织的免疫应答。在一个实施方案中,根据本公开内容的待诱导的免疫应答是t细胞介导的免疫应答。在一个实施方案中,免疫应答是抗肿瘤免疫应答,并且靶细胞群或靶组织是肿瘤细胞或肿瘤组织。
10.如果il2与改变药代动力学的基团连接(以下称为“药代动力学(pharmacokinetic,pk)延长的il2”),则本文中所述的方法和药剂特别有效。如果编码il2(例如pk延长的il2)的多核苷酸是rna和/或编码i型干扰素的多核苷酸是rna,则本文中所述的方法和药剂特别有效。在一个实施方案中,所述rna靶向肝以获得全身可用性。肝细胞可被有效地转染并且能够产生大量的蛋白质。编码疫苗抗原的rna优选靶向次级淋巴器官。
11.在一个方面中,本文中提供了用于在对象中诱导免疫应答的方法,其包括向所述对象施用:
12.a.包含il2或其功能性变体的多肽,或者编码包含il2或其功能性变体的多肽的多核苷酸;和
13.b.包含i型干扰素或其功能性变体的多肽,或者编码包含i型干扰素或其功能性变体的多肽的多核苷酸。
14.在一个实施方案中,该方法还包括向所述对象施用:
15.c.肽或蛋白质,其包含用于在所述对象中诱导针对抗原的免疫应答的表位,或者编码所述肽或蛋白质的多核苷酸。
16.在一个实施方案中,编码包含il2或其功能性变体的多肽的多核苷酸是rna,编码包含i型干扰素或其功能性变体的多肽的多核苷酸是rna,并且任选地,编码所述肽或蛋白质的多核苷酸是rna。
17.在一个方面中,本文中提供了用于在对象中诱导免疫应答的方法,其包括向所述对象施用:
18.a.编码包含il2或其功能性变体的多肽的rna;和
19.b.编码包含i型干扰素或其功能性变体的多肽的rna。
20.在一个实施方案中,该方法还包括向所述对象施用:
21.c.编码肽或蛋白质的rna,所述肽或蛋白质包含用于在所述对象中诱导针对抗原的免疫应答的表位。
22.在一个实施方案中,免疫应答是t细胞介导的免疫应答。
23.在一个实施方案中,对象患有与抗原表达或抗原表达升高相关的疾病、障碍或病症。
24.在一个方面中,本文中提供了用于治疗患有与抗原表达或抗原表达升高相关的疾病、障碍或病症的对象的方法,其包括向所述对象施用:
25.a.包含il2或其功能性变体的多肽,或者编码包含il2或其功能性变体的多肽的多核苷酸;
26.b.包含i型干扰素或其功能性变体的多肽,或者编码包含i型干扰素或其功能性变体的多肽的多核苷酸;和
27.c.肽或蛋白质,其包含用于在所述对象中诱导针对所述抗原的免疫应答的表位,或者编码所述肽或蛋白质的多核苷酸。
28.在一个实施方案中,编码包含il2或其功能性变体的多肽的多核苷酸是rna,编码包含i型干扰素或其功能性变体的多肽的多核苷酸是rna,并且编码所述肽或蛋白质的多核苷酸是rna。
29.在一个方面中,本文中提供了用于治疗患有与抗原表达或抗原表达升高相关的疾病、障碍或病症的对象的方法,其包括向所述对象施用:
30.a.编码包含il2或其功能性变体的多肽的rna;
31.b.编码包含i型干扰素或其功能性变体的多肽的rna;和
32.c.编码肽或蛋白质的rna,所述肽或蛋白质包含用于在所述对象中诱导针对所述抗原的免疫应答的表位。
33.在一个实施方案中,所述疾病、障碍或病症是癌症且所述抗原是肿瘤相关抗原。
34.在一个实施方案中,包含il2或其功能性变体的多肽是药代动力学(pk)延长的il2。在一个实施方案中,pk延长的il2包含融合蛋白。在一个实施方案中,融合蛋白包含il2或其功能性变体的部分和选自血清白蛋白、免疫球蛋白片段、转铁蛋白、fn3及其变体的部分。在一个实施方案中,血清白蛋白包括小鼠血清白蛋白或人血清白蛋白。在一个实施方案中,免疫球蛋白片段包含免疫球蛋白fc结构域。
35.在一个实施方案中,任一方面的方法是用于在对象中治疗或预防癌症的方法,任选地其中所述抗原是肿瘤相关抗原。
36.在一个实施方案中,以下的施用诱导抗原特异性t细胞:包含il2或其功能性变体的多肽或者编码包含il2或其功能性变体的多肽的多核苷酸,特别是rna,以及任选地包含用于在所述对象中诱导针对抗原的免疫应答的表位的肽或蛋白质或者编码所述肽或蛋白质的多核苷酸,特别是rna。
37.在一个实施方案中,以下的施用降低调节性t细胞的数量:包含i型干扰素或其功能性变体的多肽或者编码包含i型干扰素或其功能性变体的多肽的多核苷酸,特别是rna。
38.在一个实施方案中,以下的施用降低il2介导的调节性t细胞的扩增:包含i型干扰素或其功能性变体的多肽或编码包含i型干扰素或其功能性变体的多肽的多核苷酸,特别是rna。
39.在一个实施方案中,以下的施用提高抗原特异性t细胞与t调节细胞的比例:包含i型干扰素或其功能性变体的多肽或编码包含i型干扰素或其功能性变体的多肽的多核苷酸,特别是rna。
40.在所有方面的一个实施方案中,i型干扰素是干扰素
‑
α。
41.在一个方面中,本文中提供了药物制剂,其包含:
42.a.包含il2或其功能性变体的多肽,或者编码包含il2或其功能性变体的多肽的多核苷酸;和
43.b.包含i型干扰素或其功能性变体的多肽,或者编码包含i型干扰素或其功能性变体的多肽的多核苷酸。
44.在一个实施方案中,所述药物制剂还包含:
45.c.肽或蛋白质,其包含用于在对象中诱导针对抗原的免疫应答的表位,或者编码所述肽或蛋白质的多核苷酸。
46.在一个实施方案中,编码包含il2或其功能性变体的多肽的多核苷酸是rna,编码包含i型干扰素或其功能性变体的多肽的多核苷酸是rna,并且任选地,编码所述肽或蛋白质的多核苷酸是rna。
47.在一个实施方案中,所述药物制剂是药盒。
48.在一个实施方案中,所述药物制剂在单独的容器中包含:包含il2或其功能性变体的多肽,或者编码包含il2或其功能性变体的多肽的多核苷酸;包含i型干扰素或其功能性变体的多肽,或者编码包含i型干扰素或其功能性变体的多肽的多核苷酸;和任选地所述肽或蛋白质或者编码所述肽或蛋白质的多核苷酸。
49.在一个实施方案中,所述药物制剂还包含所述药物制剂用于治疗或预防癌症的用途的说明,任选地其中所述抗原是肿瘤相关抗原。
50.在一个实施方案中,所述药物制剂是药物组合物。
51.在一个实施方案中,所述药物组合物还包含一种或更多种可药用载体、稀释剂和/或赋形剂。
52.在一个方面中,本文中提供了药物制剂,其包含:
53.a.编码包含il2或其功能性变体的多肽的rna;和
54.b.编码包含i型干扰素或其功能性变体的多肽的rna。
55.在一个实施方案中,所述药物制剂还包含:
56.c.编码肽或蛋白质的rna,其包含用于在对象中诱导针对抗原的免疫应答的表位。
57.在一个实施方案中,药物制剂是药盒。
58.在一个实施方案中,所述药物制剂在单独的容器中包含编码包含il2或其功能性变体的多肽的rna、编码包含i型干扰素或其功能性变体的多肽的rna和任选地编码肽或蛋白质的rna。
59.在一个实施方案中,所述药物制剂还包含所述药物制剂用于治疗或预防癌症的用途的说明,任选地其中所述抗原是肿瘤相关抗原。
60.在一个实施方案中,药物制剂是药物组合物。
61.在一个实施方案中,药物组合物还包含一种或更多种可药用载体、稀释剂和/或赋形剂。
62.在药物制剂的一个实施方案中,免疫应答是t细胞介导的免疫应答。
63.在一个实施方案中,包含il2或其功能性变体的多肽是药代动力学(pk)延长的il2。在一个实施方案中,pk延长的il2包含融合蛋白。在一个实施方案中,融合蛋白包含il2
或其功能性变体的部分和选自血清白蛋白、免疫球蛋白片段、转铁蛋白、fn3及其变体的部分。在一个实施方案中,血清白蛋白包括小鼠血清白蛋白或人血清白蛋白。在一个实施方案中,免疫球蛋白片段包含免疫球蛋白fc结构域。
64.在一个方面中,本文中提供了本文中所述的用于药物用途的药物制剂。
65.在一个实施方案中,药物用途包括疾病或病症的治疗性或预防性治疗。
66.在一个方面中,本文中提供了本文中所述的用于在对象中治疗或预防癌症的方法中的药物制剂,任选地其中所述抗原是肿瘤相关抗原。
67.在所有方面的一个实施方案中,i型干扰素是干扰素
‑
α。
附图说明
68.图1:malb
‑
mil2和t细胞疫苗接种的组合治疗导致卵清蛋白特异性cd8 t细胞的暂时性增强
69.a,实验概要。b至d,在第7(b)、14(c)和21(d)天在外周血中卵清蛋白(ovalbumin,ova)特异性cd8 t细胞的数量。e,ova特异性t细胞随时间的频率。f,cd4 t细胞中cd4 cd25 foxp3 treg随时间的频率。对于统计分析,应用了双尾非配对student’s t检验(b至d)或双因素方差分析和sidak’s多重比较检验(e、f)。ns;p>0.05,*:p≤0.05,**:p≤0.01,***;p≤0.001,***;p≤0.0001。显示平均值
±
s.e.m.。
70.图2:malb
‑
mil2和t细胞疫苗接种的组合治疗导致gp70特异性cd8 t细胞的暂时性增强
71.a,实验概要。b至d,在第7(b)、14(c)和21(d)天在外周血中gp70特异性cd8 t细胞的数量。e,gp70特异性t细胞随时间的频率。f,cd4 t细胞中cd4 cd25 foxp3 treg随时间的频率。对于统计分析,应用了双尾非配对student’s t检验(b至d)或双因素方差分析和sidak’s多重比较检验(e、f)。ns;p>0.05,*:p≤0.05,**:p≤0.01,***;p≤0.001,***;p≤0.0001。显示平均值
±
s.e.m.。
72.图3:在体内,ifnα限制il2介导的treg扩增,这导致了ova特异性t细胞的稳健引发
73.a,实验概要。b、d,在第7(b)和14(d)天在外周血中ova特异性cd8 t细胞的频率。c,在第7天cd4 t细胞中cd4 cd25 foxp3 treg的频率。对于统计分析,应用了单因素方差分析随后是sidak’s多重比较检验。ns;p>0.05,*:p≤0.05,**:p≤0.01,***;p≤0.001,***;p≤0.0001。显示平均值
±
s.e.m.。
74.图4:在体内,ifnα限制il2介导的treg扩增,这导致了gp70特异性t细胞的稳健引发
75.a,实验概要。b、d,在第7(b)和21(d)天在外周血中gp70特异性cd8 t细胞的数量。c,在第7天cd4 t细胞中cd4 cd25 foxp3 treg的频率。对于统计分析,应用了单因素方差分析随后是sidak’s多重比较检验。ns;p>0.05,*:p≤0.05,**:p≤0.01,***;p≤0.001,***;p≤0.0001。显示平均值
±
s.e.m.。
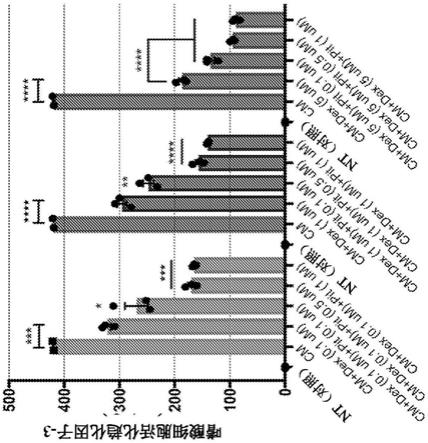
76.图5:在体外,ifnα限制il2介导的treg扩增,但不限制cd8 t细胞扩增
77.将celltrace farred标记的分离的treg(cd4 cd25 )与自体的cfse标记的pbmc以1:1的比例在次优浓度的抗cd3抗体(克隆ucht1)的存在下共培养,并用5%含halb
‑
hil2的上清液进行处理。将共培养物与10,000u/ml hifnα2b、625u/ml hifnα2b一起孵育或在没有
hifnα2b的情况下保持。孵育4天之后,通过流式细胞术测量cd4 cd25 treg和cd8 t细胞的增殖。将来自两个不同pbmc供体(a、b)的数据显示为使用flowjo v10.5软件计算的扩增指数平均值。误差棒表示实验中的变化(两个重复)。
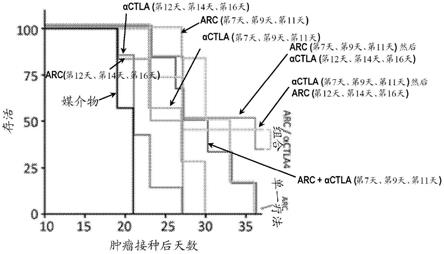
78.图6:在小鼠中ifnα和il2组合治疗导致协同抗肿瘤作用。a,处理方案和分析计划表。b,每组的中位肿瘤尺寸。对于统计分析,进行了双因素anova随后是dunnett’s检验来将所有组与malb对照进行比较。c,单只小鼠的肿瘤生长曲线。垂直虚线表示处理。d,小鼠的存活。为了统计学地比较il2和ifnα组合组与il2单一治疗组之间的存活,进行了对数秩检验。e,在第29天(左)和第35天(右)时cd45
细胞中cd8
t细胞的分数。显示了平均值(线)和单个值(符号)。水平虚线表示malb组的平均值。进行tukey’s检验随后是单因素anova来鉴定显著差异。ns;p>0.05,*:p≤0.05,**:p≤0.01,***;p≤0.001,***;p≤0.0001。
具体实施方式
79.尽管以下详细描述了本公开内容,但是应理解,本公开内容不限于本文中所述的特定方法、方案和试剂,因为这些可变化。还应理解,本文中使用的术语仅出于描述一些具体实施方案的目的,并且不旨在限制本公开内容的范围,本公开内容的范围将仅受所附权利要求书限制。除非另外限定,否则本文中使用的所有技术和科学术语均具有与本领域普通技术人员通常所理解的相同的含义。
80.优选地,本文中使用的术语如“amultilingual glossary of biotechnological terms:(iupac recommendations)”,h.g.w.leuenberger,b.nagel和h.编辑,helvetica chimica acta,ch
‑
4010basel,switzerland,(1995)中所述进行定义。
81.除非另外指出,否则本公开内容的实施将采用化学、生物化学、细胞生物学、免疫学和重组dna技术的常规方法,其在本领域的文献中进行了说明(参见例如molecular cloning:alaboratory manual,2nd edition,j.sambrook et al.eds.,cold spring harbor laboratory press,cold spring harbor 1989)。
82.在下文中,将描述本公开内容的一些要素。这些要素与一些具体实施方案一起列出,然而,应理解,其可以以任何方式且以任何数量组合以产生另外的实施方案。不同描述的一些实例和实施方案不应被解释为将本公开内容仅限于明确描述的一些实施方案。本说明书应理解为公开和涵盖将明确描述的实施方案与任何数量的所公开要素组合的实施方案。此外,除非上下文另外指出,否则所有描述要素的任何排列和组合应被认为被本说明书所公开。
83.术语“约”意指大约或接近,并且在一个实施方案中在本文中所列的数值或范围的情况下意指所列举或要求保护的数值或范围的
±
20%、
±
10%、
±
5%、或
±
3%。
84.除非本文中另外指出或者与上下文明显矛盾,否则在描述本公开内容的上下文中(尤其是在权利要求书的上下文中)使用的没有数量词修饰的名词应解释为涵盖一个/种和/或更多个/种。本文中数值范围的记载仅旨在用作单独提及落入所述范围内的每个单独值的简写方法。除非本文中另外指出,否则每个单独值均被并入本说明书中,如同其在本文中被单独记载一样。除非本文中另外指出或者另外与上下文明显矛盾,否则本文中所述的所有方法均可以以任何合适的顺序进行。本文中提供的任何和所有实例或示例性语言(例如“例如”)的使用仅旨在更好地举例说明本公开内容,而不对权利要求书的范围构成限制。
本说明书中的语言均不应被解释为指示实施本公开内容所必需的任何未要求保护的要素。
85.除非另有明确说明,否则在本文件的上下文中使用术语“包含/包括”以指示除由“包含/包括”引入的列表的成员之外还可任选地存在其他成员。然而,考虑了作为本公开内容的具体实施方案,术语“包含/包括”涵盖不存在其他成员的可能性,即,出于这个目的,实施方案“包含/包括”应理解为具有“由......组成”的含义。
86.在本说明书的正文通篇引用了数篇文件。本文中无论是在上文还是在下文引用的每篇文件(包括所有专利、专利申请、科学出版物、制造商说明书、指南等)均在此通过引用整体并入。本文中的内容均不应解释为承认本公开内容无权早于这样的公开内容。
87.下面将提供适用于本公开内容的所有方面的定义。除非另外指出,否则以下术语具有以下含义。任何未经定义的术语均具有其本领域公认的含义。
88.定义
89.本文中使用的例如“减少”、“降低”、“抑制”或“减弱”的术语涉及水平(例如,结合水平)的总体降低或导致总体降低的能力,优选5%或更大、10%或更大、20%或更大,更优选50%或更大,并且最优选75%或更大。
90.例如“提高”、“增强”或“超过”的术语优选涉及提高或增强约至少10%,优选至少20%,优选至少30%,更优选至少40%,更优选至少50%,甚至更优选至少80%,并且最优选至少100%,至少200%,至少500%,或甚至更多。
91.根据本公开内容,术语“肽”是指包含通过肽键彼此连接的约两个或更多个、约3个或更多个、约4个或更多个、约6个或更多个、约8个或更多个、约10个或更多个、约13个或更多个、约16个或更多个、约20个或更多个,并且多至约50个、约100个、或约150个连续氨基酸的物质。术语“蛋白质”或“多肽”是指大肽,特别是具有至少约150个氨基酸的肽,但是术语“肽”、“蛋白质”和“多肽”在本文中通常作为同义词使用。
[0092]“治疗性蛋白质”当以治疗有效量提供给对象时,对该对象的病症或疾病状态具有积极或有利作用。在一个实施方案中,治疗性蛋白质具有治愈性或姑息治疗性(palliative)特性并且可被施用以改善、缓解、减轻、逆转、延迟疾病或病症发作,或者减轻疾病或病症的一种或更多种症状的严重程度。治疗性蛋白质可具有预防特性,并且可用于延迟疾病发作或减轻这样的疾病或病理状况的严重程度。术语“治疗性蛋白质”包括完整的蛋白质或肽,并且也可指其治疗活性片段。其还可包括蛋白质的治疗活性变体。治疗活性蛋白质的一些实例包括但不限于细胞因子以及用于疫苗接种的抗原。
[0093]
关于氨基酸序列(肽或蛋白质),“片段”涉及氨基酸序列的一部分,即该序列表示在n端和/或c端缩短的氨基酸序列。在c端缩短的片段(n端片段)可例如通过翻译缺少开放阅读框的3’端的截短的开放阅读框来获得。在n端缩短的片段(c端片段)可例如通过翻译缺少开放阅读框的5’端的截短的开放阅读框来获得,只要截短的开放阅读框包含用于起始翻译的起始密码子即可。氨基酸序列的片段包含来自氨基酸序列的例如至少50%、至少60%、至少70%、至少80%、至少90%的氨基酸残基。氨基酸序列的片段优选包含来自氨基酸序列的至少6个、特别地至少8个、至少12个、至少15个、至少20个、至少30个、至少50个或至少100个连续氨基酸。
[0094]
本文中的“变体”或“变体蛋白质”或“变体多肽”意指由于至少一种氨基酸修饰而不同于野生型蛋白质的蛋白质。亲本多肽可以是天然存在的或野生型(wild type,wt)多
肽,或者可以是野生型多肽的经修饰形式。优选地,变体多肽与亲本多肽相比具有至少一种氨基酸修饰,例如与亲本相比,具有1至约20种氨基酸修饰,并且优选1至约10或1至约5种氨基酸修饰。
[0095]
本文中使用的“亲本多肽”、“亲本蛋白质”、“前体多肽”或“前体蛋白质”意指随后被修饰以产生变体的未经修饰多肽。亲本多肽可以是野生型多肽,或者野生型多肽的变体或经改造形式。
[0096]
本文中的“野生型”或“wt”或“天然的”意指在自然界中存在的氨基酸序列,包括等位基因变化。野生型蛋白质或多肽具有未经有意修饰的氨基酸序列。
[0097]
出于本公开内容的目的,氨基酸序列(肽、蛋白质或多肽)的“变体”包括氨基酸插入变体、氨基酸添加变体、氨基酸缺失变体和/或氨基酸替换变体。术语“变体”包括所有剪接变体、翻译后修饰的变体、构象体、异构体和物种同源物,特别是由细胞天然表达的那些。术语“变体”特别地包括氨基酸序列片段。
[0098]
氨基酸插入变体包括在特定氨基酸序列中单个或两个或更多个氨基酸的插入。在具有插入的氨基酸序列变体的情况下,一个或更多个氨基酸残基被插入氨基酸序列中的特定位点中,尽管随机插入并合适筛选所得产物也是可以的。氨基酸添加变体包含一个或更多个氨基酸,例如1、2、3、5、10、20、30、50个或更多个氨基酸的氨基和/或羧基端融合物。氨基酸缺失变体的特征在于从序列中去除一个或更多个氨基酸,例如,去除1、2、3、5、10、20、30、50个或更多个氨基酸。缺失可在蛋白质的任何位置中。在蛋白质的n端和/或c端末端包含缺失的氨基酸缺失变体也称为n端和/或c端截短变体。氨基酸替换变体的特征在于去除序列中的至少一个残基,并在其位置中插入另一个残基。优先考虑的是在同源蛋白质或肽之间非保守的氨基酸序列中的位置中的修饰和/或用具有相似特性的另一些氨基酸来替换氨基酸。优选地,肽和蛋白质变体中的氨基酸变化是保守的氨基酸变化,即类似带电荷或不带电荷氨基酸的替换。保守的氨基酸变化涉及其侧链相关联的氨基酸的家族之一的替换。天然存在的氨基酸通常分为四个家族:酸性氨基酸(天冬氨酸、谷氨酸);碱性氨基酸(赖氨酸、精氨酸、组氨酸);非极性氨基酸(丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、甲硫氨酸、色氨酸)和不带电荷的极性氨基酸(甘氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、丝氨酸、苏氨酸、酪氨酸)。苯丙氨酸、色氨酸和酪氨酸有时被共同分类为芳香族氨基酸。在一个实施方案中,保守氨基酸替换包括以下组内的替换:
[0099]
甘氨酸、丙氨酸;
[0100]
缬氨酸、异亮氨酸、亮氨酸;
[0101]
天冬氨酸、谷氨酸;
[0102]
天冬酰胺、谷氨酰胺;
[0103]
丝氨酸、苏氨酸;
[0104]
赖氨酸、精氨酸;以及
[0105]
苯丙氨酸、酪氨酸。
[0106]
优选地,给定氨基酸序列与作为所述给定氨基酸序列的变体的氨基酸序列之间的相似性,优选同一性的程度将为至少约60%、70%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、或99%。相似性或同一性的程度优选地针对为参考氨基酸序列的全长的至少约10%、至少约20%、至少
约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约90%或约100%的氨基酸区域给出。例如,如果参考氨基酸序列由200个氨基酸组成,则相似性或同一性的程度优选地针对至少约20个、至少约40个、至少约60个、至少约80个、至少约100个、至少约120个、至少约140个、至少约160个、至少约180个或约200个氨基酸,优选连续氨基酸给出。在一些优选实施方案中,相似性或同一性的程度针对参考氨基酸序列的全长给出。用于确定序列相似性,优选序列同一性的比对可使用本领域已知的工具,优选地使用最佳序列比对,例如,使用align,使用标准设置,优选emboss::needle,矩阵:blosum62,空位开放(gap open)10.0,空位延伸(gap extend)0.5来完成。
[0107]“序列相似性”表明相同的或表示保守氨基酸替换的氨基酸的百分比。两个氨基酸序列之间的“序列同一性”表明序列之间相同氨基酸的百分比。
[0108]
术语“百分比同一性”旨在表示待比较的两个序列之间在最佳比对之后获得的相同的氨基酸残基的百分比,该百分比是纯统计学的,并且两个序列之间的差异是随机分布的并且在其全长内随机分布。两个氨基酸序列之间的序列比较常规上是通过在最佳地对其比对之后对这些序列进行比较来进行的,所述比较是通过区段或通过“比较窗口”进行的,以便鉴定和比较序列相似性的局部区域。用于比较的序列的最佳比对除了人工之外,可借助于smith and waterman,1981,ads app.math.2,482的局部同源性算法、借助于neddleman and wunsch,1970,j.mol.biol.48,443的局部同源性算法,借助于pearson and lipman,1988,proc.natl acad.sci.usa 85,2444的相似性检索方法,或者借助于使用这些算法的计算机程序(wisconsin genetics software package,genetics computer group,575science drive,madison,wis.中的gap、bestfit、fasta、blast p、blast n和tfasta)来产生。
[0109]
百分比同一性通过确定待比较的两个序列之间相同位置的数目,将该数目除以所比较的位置的数目,并将获得的结果乘以100来计算,以便获得这两个序列之间的百分比同一性。
[0110]
根据本公开内容,同源氨基酸序列显示出氨基酸残基的至少40%,特别地至少50%、至少60%、至少70%、至少80%、至少90%,并且优选地至少95%、至少98%或至少99%同一性。
[0111]
本文中所述的氨基酸序列变体可由技术人员例如通过重组dna操作来容易地制备。用于制备具有替换、添加、插入或缺失的肽或蛋白质的dna序列的操作在例如sambrook et al.(1989)中详细描述。此外,本文中所述的肽和氨基酸变体可借助于已知的肽合成技术例如如通过固相合成和类似方法来容易地制备。
[0112]
在一个实施方案中,氨基酸序列(肽或蛋白质)的片段或变体优选是“功能性片段”或“功能性变体”。术语氨基酸序列的“功能性片段”或“功能性变体”涉及表现出与该片段或变体所来源的氨基酸序列的功能特性相同或相似的一个或更多个功能特性(即,其是功能等同的)的任何片段或变体。关于细胞因子例如il2,一种特定功能是由该片段或变体所来源的氨基酸序列所表现出的一种或更多种免疫调节活性和/或与该片段或变体所来源的氨基酸序列所结合的受体的结合。本文中使用的术语“功能性片段”或“功能性变体”特别是指包含与母体分子或序列的氨基酸序列相比改变一个或更多个氨基酸并且仍然能够实现母体分子或序列的一种或更多种功能(例如,与靶分子结合或有助于与靶分子结合)的氨基酸
序列的变体分子或序列。在一个实施方案中,母体分子或序列的氨基酸序列中的修饰不显著影响或改变该分子或序列的结合特性。在不同的实施方案中,功能性片段或功能性变体的结合可降低但仍显著存在,例如,功能性变体的结合可为母体分子或序列的至少50%、至少60%、至少70%、至少80%或至少90%。然而,在另一些实施方案中,与母体分子或序列相比,功能性片段或功能性变体的结合可以是增强的。
[0113]“来源于”指定氨基酸序列(肽、蛋白质或多肽)的氨基酸序列(肽、蛋白质或多肽)是指第一氨基酸序列的来源。优选地,来源于特定氨基酸序列的氨基酸序列具有与该特定序列或其片段相同、基本上相同或同源的氨基酸序列。来源于特定氨基酸序列的氨基酸序列可以是该特定序列或其片段的变体。例如,本领域普通技术人员将理解,适用于本文中的抗原和细胞因子(例如,il2)可以被改变,使得它们的序列与它们所来源的天然存在或天然的序列不同,同时保留天然序列的期望活性。
[0114]
本文中使用的“说明材料”或“说明”包括出版物、记录、图表或可用于传达本发明的组合物和方法的有用性的任何其他表达媒介。例如,本发明的药盒的说明材料可标附到含有本发明组合物的容器上,或者与含有所述组合物的容器一起运输。或者,说明材料可以与容器分开运输,目的是让接受者合作使用说明材料和组合物。
[0115]“分离”意指从天然状态中改变或取出。例如,天然存在于活体动物中的核酸或肽不是“分离”的,但部分或完全从其天然状态的共存物质中分离的相同的核酸或肽是“分离”的。分离的核酸或蛋白质可以以充分纯化的形式存在,或者可以存在于非天然环境,例如宿主细胞中。
[0116]
在本发明的上下文中,术语“重组”意指“通过遗传工程制备”。优选地,在本发明的上下文中,“重组物质”例如重组细胞是非天然存在的。
[0117]
本文中使用的术语“天然存在的”是指物体可在自然界中存在的事实。例如,存在于生物体(包括病毒)中并且可以从天然来源中分离且没有在实验室中被人有意修饰的肽或核酸是天然存在的。
[0118]
术语“遗传修饰”包括用核酸转染细胞。术语“转染”涉及将核酸,特别是rna引入细胞中。出于本发明的目的,术语“转染”还包括将核酸引入细胞中或由这样的细胞摄入核酸,其中细胞可存在于对象例如患者中。因此,根据本发明,用于转染本文中所述核酸的细胞可存在于体外或体内,例如,细胞可形成患者的器官、组织和/或生物体的一部分。根据本发明,转染可以是瞬时的或稳定的。对于转染的一些应用,如果仅瞬时表达所转染的遗传物质就已足够。由于在转染过程中引入的核酸通常不会整合至核基因组中,因此外源核酸将通过有丝分裂而被稀释或者降解。允许核酸进行游离扩增的细胞大大降低了稀释率。如果期望所转染的核酸实际上保留在细胞及其子细胞的基因组中,则必须发生稳定的转染。这样的稳定转染可通过使用用于转染的基于病毒的系统或基于转座子的系统来实现。通常,经遗传修饰以表达受体多肽例如抗原受体或il2受体的细胞稳定地用编码受体的核酸转染,而通常将编码细胞因子例如il2或i型干扰素的核酸和/或编码抗原的核酸瞬时转染到细胞中。可将rna转染到细胞中以瞬时表达其编码的蛋白质。
[0119]
免疫效应细胞
[0120]
待在本文中使用的免疫效应细胞,特别是il2响应性免疫效应细胞(含有il2r的免疫效应细胞),可施用于需要治疗的对象,或者可内源性地存在于需要治疗的对象中。向对
象施用il2或编码il2的多核苷酸允许刺激免疫效应细胞。特别地,本文中所述的方法和药剂可用于治疗以表达所述免疫效应细胞所针对的抗原的病变细胞为特征的疾病。在一个实施方案中,免疫效应细胞携带对抗原或其加工产物具有结合特异性的抗原受体,例如t细胞受体(tcr)或嵌合抗原受体(car)。在一个实施方案中,免疫效应细胞在待治疗的对象中存在并且在对象中在体内进行遗传修饰以表达抗原受体。在一个实施方案中,将来自待治疗对象或来自不同对象的免疫效应细胞施用于待治疗对象。施用的免疫效应细胞可在施用之前进行离体遗传修饰,或者在施用之后在对象中在体内进行遗传修饰,以表达抗原受体。在一个实施方案中,抗原受体对于免疫效应细胞是内源性的。在一个实施方案中,免疫效应细胞离体或在体内进行遗传修饰以表达il2r。因此,关于il2r的这样的遗传修饰可在体外(任选地与抗原受体的遗传修饰一起)实现并随后将免疫效应细胞施用于需要治疗的对象,或者这样的遗传修饰可在需要治疗的对象中在体内(任选地与抗原受体的遗传修饰一起)实现。
[0121]
因此,待由il2刺激的免疫效应细胞包括天然的或在用一种或更多种il2r多肽转染之后对il2有应答的任何细胞。这样的应答性包括活化、分化、增殖、存活和/或一种或更多种免疫效应功能的指征。特别地,所述细胞包括具有裂解潜能的细胞,特别是淋巴细胞,并且优选t细胞,特别是细胞毒性淋巴细胞,优选选自细胞毒性t细胞、自然杀伤(natural killer,nk)细胞和淋巴因子活化的杀伤(lak)细胞。一旦活化,这些细胞毒性淋巴细胞中的每一种都触发靶细胞的破坏。例如,细胞毒性t细胞通过以下方式中的任一种或两种触发靶细胞的破坏。首先,一旦活化,t细胞释放细胞毒素,例如穿孔素、颗粒酶(granzyme)和颗粒溶素(granulysin)。穿孔素和颗粒溶素在靶细胞中产生孔,而颗粒酶进入细胞并在细胞质中触发胱天蛋白酶级联,其诱导细胞的凋亡(程序性细胞死亡)。其次,凋亡可以通过t细胞和靶细胞之间的fas
‑
fas配体相互作用诱导。尽管可以使用异源细胞或同种异体细胞,但结合本发明使用的细胞优选是自体细胞。在一个实施方案中,待由il2刺激的免疫效应细胞对于待治疗的对象是内源性的。
[0122]
本发明上下文中的术语“效应子功能”包括由免疫系统组分介导的任何功能,这些功能导致例如杀伤病变细胞如肿瘤细胞,或抑制肿瘤生长和/或抑制肿瘤发展,包括抑制肿瘤散播和转移。优选地,本发明上下文中的效应子功能是t细胞介导的效应子功能。在辅助t细胞(cd4
t细胞)的情况下,这样的功能包括释放细胞因子和/或活化cd8
淋巴细胞(ctl)和/或b细胞,并且在ctl的情况下包括例如通过凋亡或穿孔素介导的细胞裂解来消除细胞(即以表达抗原为特征的细胞),产生细胞因子如ifn
‑
γ和tnf
‑
α,以及抗原表达靶细胞的特异性细胞裂解杀伤。
[0123]
在本发明上下文中,术语“免疫效应细胞”或“免疫反应性细胞”涉及在免疫反应期间发挥效应子功能的细胞。在一个实施方案中,“免疫效应细胞”能够结合抗原,例如在细胞上的mhc的情况下呈递或在细胞表面上表达的抗原并介导免疫应答的抗原。例如,免疫效应细胞包括t细胞(细胞毒性t细胞、辅助t细胞、肿瘤浸润t细胞)、b细胞、自然杀伤细胞、嗜中性粒细胞、巨噬细胞和树突细胞。优选地,在本发明的上下文中,“免疫效应细胞”是t细胞,优选cd4
和/或cd8
t细胞。根据本发明,术语“免疫效应细胞”还包括可以在适当的刺激下成熟为免疫细胞(例如t细胞,特别是t辅助细胞或细胞裂解t细胞)的细胞。免疫效应细胞包括cd34
造血干细胞,未成熟和成熟t细胞以及未成熟和成熟b细胞。当暴露于抗原时,t细胞
前体分化为细胞裂解t细胞类似于免疫系统的克隆选择。
[0124]
优选地,“免疫效应细胞”以一定程度的特异性识别抗原,特别是如果在mhc的情况下呈递或存在于病变细胞(例如癌细胞)的表面上时。优选地,所述识别使得识别抗原的细胞具有响应性或反应性。如果细胞是辅助t细胞(cd4
t细胞),则这样的响应性或反应性可涉及细胞因子的释放和/或cd8
淋巴细胞(ctl)和/或b细胞的活化。如果细胞是ctl,则这样的响应性或反应性可涉及例如通过凋亡或穿孔素介导的细胞裂解来消除细胞(即以表达抗原为特征的细胞)。根据本发明,ctl响应性可包括持续的钙通量,细胞分裂,细胞因子如ifn
‑
γ和tnf
‑
α的产生,活化标志物如cd44和cd69的上调以及抗原表达靶细胞的特异性细胞裂解杀伤。ctl响应性也可以使用精确指示ctl响应性的人工报告物来确定。这样的识别抗原并且是响应性或反应性的ctl在本文中也称为“抗原响应性ctl”。
[0125]
在一个实施方案中,免疫效应细胞是表达car的免疫效应细胞。在一个实施方案中,免疫效应细胞是表达tcr的免疫效应细胞。
[0126]
根据本发明使用的免疫效应细胞可表达内源性抗原受体,例如t细胞受体或b细胞受体,或者可缺乏内源性抗原受体的表达。
[0127]“淋巴样细胞”是任选地在适当修饰后,例如在转移抗原受体例如tcr或car后,能够产生免疫应答(例如细胞免疫应答)的细胞,或者这样的细胞的前体细胞,并且包括淋巴细胞(优选t淋巴细胞)、成淋巴细胞和浆细胞。淋巴样细胞可以是如本文中所述的免疫效应细胞。优选的淋巴样细胞是可以被修饰以在细胞表面上表达抗原受体的t细胞。在一个实施方案中,淋巴样细胞缺少t细胞受体的内源性表达。
[0128]
术语“t细胞”和“t淋巴细胞”在本文中可互换使用,并且包括t辅助细胞(cd4
t细胞)和包括细胞裂解t细胞的细胞毒性t细胞(ctl,cd8
t细胞)。术语“抗原特异性t细胞”或类似术语涉及识别t细胞所靶向的抗原的t细胞,并且优选地发挥t细胞的效应子功能。如果t细胞杀伤表达抗原的靶细胞,则认为该细胞对抗原具有特异性。可以使用多种标准技术中的任何一种(例如在铬释放测定或增殖测定中)来评价t细胞特异性。或者,可以测量淋巴因子(例如ifn
‑
γ)的合成。
[0129]
t细胞属于被称为淋巴细胞的一组白细胞,并且在细胞介导的免疫中起着关键作用。它们可以通过其细胞表面上被称为t细胞受体(tcr)的特殊受体的存在与其他淋巴细胞类型(例如b细胞和自然杀伤细胞)区分开来。胸腺是负责t细胞成熟的主要器官。已经发现了多种不同的t细胞亚群,每种具有独特的功能。
[0130]
t辅助细胞在免疫过程中辅助其他白细胞,包括b细胞成熟为浆细胞以及细胞毒性t细胞和巨噬细胞的活化等功能。这些细胞也被称为cd4 t细胞,因为它们在其表面上表达cd4糖蛋白。当辅助t细胞通过在抗原呈递细胞(antigen presenting cell,apc)表面上表达的mhc ii类分子呈递肽抗原时,其被活化。一旦活化,其迅速分裂并分泌被称为细胞因子的小蛋白,这些小蛋白调节或协助主动免疫应答。
[0131]
细胞毒性t细胞破坏病毒感染的细胞和肿瘤细胞,也参与移植排斥。这些细胞也被称为cd8 t细胞,因为它们在其表面上表达cd8糖蛋白。这些细胞通过结合与存在于几乎身体的每个细胞的表面上的mhc i类缔合的抗原来识别它们的靶标。
[0132]“调节性t细胞”或“treg”是调节免疫系统、维持对自身抗原的耐受性以及预防自身免疫病的t细胞亚群。treg是免疫抑制的,并且通常抑制或下调效应t细胞的诱导和增殖。
treg表达生物标志物cd4、foxp3和cd25。
[0133]
本文中使用的术语“初始t细胞”是指不同于活化t细胞或记忆t细胞,在外周内未接触其同源抗原的成熟t细胞。初始t细胞的特征通常在于l
‑
选择素(cd62l)的表面表达,不存在活化标志物cd25、cd44或cd69,以及不存在记忆cd45ro同种型。
[0134]
本文中使用的术语“记忆t细胞”是指先前已接触并响应于其同源抗原的t细胞亚组或亚群。在与抗原第二次接触时,记忆t细胞可复制以产生比第一次免疫系统响应于抗原更快且更强的免疫应答。记忆t细胞可以是cd4
或cd8
并且通常表达cd45ro。
[0135]
所有t细胞都具有作为几种蛋白质的复合体存在的t细胞受体(tcr)。t细胞的tcr能够与同主要组织相容性复合体(major histocompatibility complex,mhc)分子结合并呈递在靶细胞表面上的免疫原性肽(表位)相互作用。tcr的特异性结合触发t细胞内的信号级联,导致增殖和分化成成熟的效应t细胞。在大多数t细胞中,实际的t细胞受体由两条独立的肽链构成,它们由独立的t细胞受体α和β(tcrα和tcrβ)基因产生,并被称为α
‑
tcr链和β
‑
tcr链。γδt细胞(gamma delta t细胞)是一类很不常见(t细胞总数的2%)的t细胞,其表面上具有独特的由一条γ链和一条δ链形成的t细胞受体(tcr)。
[0136]
所有t细胞都来源于骨髓中的造血干细胞。源自造血干细胞的造血祖细胞存在于胸腺中并通过细胞分裂扩增以产生大量未成熟胸腺细胞。最早的胸腺细胞既不表达cd4也不表达cd8,因此分类为双阴性(cd4
‑
cd8
‑
)细胞。随着它们在发育过程中的进展,它们变成双阳性胸腺细胞(cd4
cd8
),并且最终成熟为单阳性(cd4
cd8
‑
或cd4
‑
cd8
)胸腺细胞,然后从胸腺释放到外周组织。
[0137]
通常可以使用标准程序在体外或离体制备t细胞。例如,可以使用市售的细胞分离系统从哺乳动物(如患者)的骨髓、外周血或者骨髓或外周血的级分中分离t细胞。或者,t细胞可以来源于相关或不相关的人、非人动物、细胞系或培养物。包含t细胞的样品可以例如是外周血单个核细胞(peripheral blood mononuclear cell,pbmc)。
[0138]
本文中使用的术语“nk细胞”或“自然杀伤细胞”是指由cd56或cd16的表达和t细胞受体的缺失定义的外周血淋巴细胞亚群。如本文中提供的,nk细胞也可由干细胞或祖细胞分化。
[0139]
核酸
[0140]
本文中使用的术语“多核苷酸”或“核酸”旨在包括dna和rna,例如基因组dna、cdna、mrna、重组产生的和化学合成的分子。核酸可以是单链或双链的。rna包括体外转录的rna(in vitro transcribed rna,ivt rna)或合成的rna。根据本发明,多核苷酸优选为经分离的。
[0141]
核酸可包含在载体中。本文中使用的术语“载体”包括技术人员已知的任何载体,其包括质粒载体、黏粒载体、噬菌体载体(例如λ噬菌体)、病毒载体(例如逆转录病毒、腺病毒或杆状病毒载体),或人工染色体载体(例如细菌人工染色体(bacterial artificial chromosome,bac)、酵母人工染色体(yeast artificial chromosome,yac)或p1人工染色体(p1 artificial chromosome,pac))。所述载体包括表达载体以及克隆载体。表达载体包括质粒以及病毒载体并且一般含有用于在特定宿主生物体(例如,细菌、酵母、植物、昆虫或哺乳动物)或者在体外表达系统中可操作地连接的编码序列之表达所必需的期望编码序列和合适的dna序列。克隆载体一般用于改造和扩增某期望dna片段,并可缺乏表达所期望dna片
段所需要的功能性序列。
[0142]
在本发明所有方面的一个实施方案中,例如编码细胞因子(例如il2或ifn)的核酸、编码il2r的核酸、编码抗原受体的核酸或编码疫苗抗原的核酸的核酸在经处理以提供细胞因子、il2r、抗原受体或疫苗抗原的对象细胞中表达。在本发明所有方面的一个实施方案中,在对象的细胞中瞬时表达核酸。因此,在一个实施方案中,核酸未整合到细胞的基因组中。在本发明所有方面的一个实施方案中,核酸为rna,优选体外转录的rna。
[0143]
本文中所述核酸可为重组分子和/或经分离的分子。
[0144]
在本公开内容中,术语“rna”涉及包含核糖核苷酸残基的核酸分子。在一些优选实施方案中,rna包含全部或大部分核糖核苷酸残基。本文中使用的“核糖核苷酸”是指在β
‑
d
‑
呋喃核糖基的2
’‑
位具有羟基的核苷酸。rna包括但不限于双链rna、单链rna、经分离的rna(例如部分纯化的rna)、基本上纯的rna、合成的rna、重组产生的rna以及通过添加、缺失、替换和/或改变一个或更多个核苷酸而不同于天然存在的rna之经修饰的rna。这样的改变可以是指将非核苷酸物质添加至内部rna核苷酸或rna端。本文中还考虑了rna中的核苷酸可以是非标准核苷酸,例如化学合成的核苷酸或脱氧核苷酸。对于本公开内容,这些改变的rna被认为是天然存在rna的类似物。
[0145]
在本公开内容的某些实施方案中,rna是与编码肽或蛋白质的rna转录物相关的信使rna(mrna)。如本领域中认可的,mrna通常包含5’非翻译区(5
’‑
utr)、肽编码区和3’非翻译区(3
’‑
utr)。在一些实施方案中,rna通过体外转录或化学合成产生。在一个实施方案中,mrna通过使用dna模板的体外转录产生,其中dna是指包含脱氧核糖核苷酸的核酸。
[0146]
在一个实施方案中,rna是体外转录的rna(ivt
‑
rna),并且可通过合适dna模板的体外转录获得。用于控制转录的启动子可以是任何rna聚合酶的任何启动子。用于体外转录的dna模板可通过克隆核酸,特别是cdna,并将其引入用于体外转录的合适载体中而获得。cdna可通过rna的反转录获得。
[0147]
在一个实施方案中,本文中所述的rna可具有经修饰的核苷。在一些实施方案中,rna包含代替至少一个(例如,每个)尿苷的经修饰的核苷。
[0148]
本文中使用的术语“尿嘧啶”描述了可存在于rna的核酸中的核碱基之一。尿嘧啶的结构是:
[0149][0150]
本文中使用的术语“尿苷”描述了可存在于rna中的核苷之一。尿苷的结构是:
[0151][0152]
utp(5
’‑
三磷酸尿苷)具有以下结构:
[0153][0154]
假
‑
utp(5
’‑
三磷酸假尿苷)具有以下结构:
[0155][0156]“假尿苷”是经修饰的核苷的一个实例,其是尿苷的异构体,其中尿嘧啶通过碳
‑
碳键而不是氮
‑
碳糖苷键与戊糖环连接。
[0157]
另一示例性的经修饰的核苷是n1
‑
甲基
‑
假尿苷(m1ψ),其具有以下结构:
[0158][0159]
n1
‑
甲基
‑
假
‑
utp具有以下结构:
[0160][0161]
另一示例性的经修饰的核苷为5
‑
甲基
‑
尿苷(m5u),其具有以下结构:
[0162][0163]
在一些实施方案中,本文中所述的rna中的一个或更多个尿苷被经修饰的核苷替代。在一些实施方案中,经修饰的核苷是经修饰的尿苷。
[0164]
在一些实施方案中,rna包含代替至少一个尿苷的经修饰的核苷。在一些实施方案中,rna包含代替每个尿苷的经修饰的核苷。
[0165]
在一些实施方案中,经修饰的核苷独立地选自假尿苷(ψ)、n1
‑
甲基
‑
假尿苷(m1ψ)和5
‑
甲基
‑
尿苷(m5u)。在一些实施方案中,经修饰的核苷包括假尿苷(ψ)。在一些实施方案中,经修饰的核苷包括n1
‑
甲基
‑
假尿苷(m1ψ)。在一些实施方案中,经修饰的核苷包括5
‑
甲基
‑
尿苷(m5u)。在一些实施方案中,rna可包含多于一种类型的经修饰的核苷,并且经修饰的核苷独立地选自假尿苷(ψ)、n1
‑
甲基
‑
假尿苷(m1ψ)和5
‑
甲基
‑
尿苷(m5u)。在一些实施方案中,经修饰的核苷包括假尿苷(ψ)和n1
‑
甲基
‑
假尿苷(m1ψ)。在一些实施方案中,经修饰的核苷包括假尿苷(ψ)和5
‑
甲基
‑
尿苷(m5u)。在一些实施方案中,经修饰的核苷包括n1
‑
甲基
‑
假尿苷(m1ψ)和5
‑
甲基
‑
尿苷(m5u)。在一些实施方案中,经修饰的核苷包括假尿苷(ψ)、n1
‑
甲基
‑
假尿苷(m1ψ)和5
‑
甲基
‑
尿苷(m5u)。
[0166]
在一些实施方案中,替代rna中的一个或更多个尿苷的经修饰的核苷可以是以下中的一种或更多种:3
‑
甲基
‑
尿苷(m3u)、5
‑
甲氧基
‑
尿苷(mo5u)、5
‑
氮杂
‑
尿苷、6
‑
氮杂
‑
尿苷、2
‑
硫代
‑5‑
氮杂
‑
尿苷、2
‑
硫代
‑
尿苷(s2u)、4
‑
硫代
‑
尿苷(s4u)、4
‑
硫代
‑
假尿苷、2
‑
硫代
‑
假尿苷、5
‑
羟基
‑
尿苷(ho5u)、5
‑
氨基烯丙基
‑
尿苷、5
‑
卤代
‑
尿苷(例如,5
‑
碘
‑
尿苷或5
‑
溴
‑
尿苷)、尿苷5
‑
羟乙酸(cmo5u)、尿苷5
‑
羟乙酸甲酯(mcmo5u)、5
‑
羧甲基
‑
尿苷(cm5u)、1
‑
羧甲基
‑
假尿苷、5
‑
羧羟甲基
‑
尿苷(chm5u)、5
‑
羧羟甲基
‑
尿苷甲酯(mchm5u)、5
‑
甲氧基羰基甲基
‑
尿苷(mcm5u)、5
‑
甲氧基羰基甲基
‑2‑
硫代
‑
尿苷(mcm5s2u)、5
‑
氨基甲基
‑2‑
硫代
‑
尿苷(nm5s2u)、5
‑
甲基氨基甲基
‑
尿苷(mnm5u)、1
‑
乙基
‑
假尿苷、5
‑
甲基氨基甲基
‑2‑
硫代
‑
尿苷(mnm5s2u)、5
‑
甲基氨基甲基
‑2‑
硒基
‑
尿苷(mnm5se2u)、5
‑
氨甲酰基甲基
‑
尿苷(ncm5u)、5
‑
羧甲基氨基甲
基
‑
尿苷(cmnm5u)、5
‑
羧甲基氨基甲基
‑2‑
硫代
‑
尿苷(cmnm5s2u)、5
‑
丙炔基
‑
尿苷、1
‑
丙炔基
‑
假尿苷、5
‑
牛磺酸甲基
‑
尿苷(τm5u)、1
‑
牛磺酸甲基
‑
假尿苷、5
‑
牛磺酸甲基
‑2‑
硫代
‑
尿苷(τm5s2u)、1
‑
牛磺酸甲基
‑4‑
硫代
‑
假尿苷、5
‑
甲基
‑2‑
硫代
‑
尿苷(m5s2u)、1
‑
甲基
‑4‑
硫代
‑
假尿苷(m1s4ψ)、4
‑
硫代
‑1‑
甲基
‑
假尿苷、3
‑
甲基
‑
假尿苷(m3ψ)、2
‑
硫代
‑1‑
甲基
‑
假尿苷、1
‑
甲基
‑1‑
脱氮
‑
假尿苷、2
‑
硫代
‑1‑
甲基
‑1‑
脱氮
‑
假尿苷、二氢尿苷(d)、二氢假尿苷、5,6
‑
二氢尿苷、5
‑
甲基
‑
二氢尿苷(m5d)、2
‑
硫代
‑
二氢尿苷、2
‑
硫代
‑
二氢假尿苷、2
‑
甲氧基
‑
尿苷、2
‑
甲氧基
‑4‑
硫代
‑
尿苷、4
‑
甲氧基
‑
假尿苷、4
‑
甲氧基
‑2‑
硫代
‑
假尿苷、n1
‑
甲基
‑
假尿苷、3
‑
(3
‑
氨基
‑3‑
羧丙基)尿苷(acp3u)、1
‑
甲基
‑3‑
(3
‑
氨基
‑3‑
羧丙基)假尿苷(acp3ψ)、5
‑
(异戊烯基氨基甲基)尿苷(inm5u)、5
‑
(异戊烯基氨基甲基)
‑2‑
硫代
‑
尿苷(inm5s2u)、α
‑
硫代
‑
尿苷、2
’‑
o
‑
甲基
‑
尿苷(um)、5,2
’‑
o
‑
二甲基
‑
尿苷(m5um)、2
’‑
o
‑
甲基
‑
假尿苷(ψm)、2
‑
硫代
‑2’‑
o
‑
甲基
‑
尿苷(s2um)、5
‑
甲氧基羰基甲基
‑2’‑
o
‑
甲基
‑
尿苷(mcm5um)、5
‑
氨甲酰基甲基
‑2’‑
o
‑
甲基
‑
尿苷(ncm5um)、5
‑
羧甲基氨基甲基
‑2’‑
o
‑
甲基
‑
尿苷(cmnm5um)、3,2
’‑
o
‑
二甲基
‑
尿苷(m3um)、5
‑
(异戊烯基氨基甲基)
‑2’‑
o
‑
甲基
‑
尿苷(inm5um)、1
‑
硫代
‑
尿苷、脱氧胸苷、2
’‑
f
‑
阿糖
‑
尿苷(2
’‑
f
‑
ara
‑
uridine)、2
’‑
f
‑
尿苷、2
’‑
oh
‑
阿糖
‑
尿苷、5
‑
(2
‑
甲酯基乙烯基)尿苷、5
‑
[3
‑
(1
‑
e
‑
丙烯基氨基)尿苷或本领域已知的任何其他经修饰的尿苷。
[0167]
在一些实施方案中,根据本公开内容的rna包含5
’‑
帽。在一个实施方案中,本公开内容的rna不具有未加帽的5
’‑
三磷酸。在一个实施方案中,rna可被5
’‑
帽类似物修饰。术语“5
’‑
帽”是指见于mrna分子的5
’‑
端的结构,并且通常由通过5’至5’三磷酸连接与mrna连接的鸟苷核苷酸组成。在一个实施方案中,该鸟苷在7位被甲基化。提供具有5
’‑
帽或5
’‑
帽类似物的rna可通过体外转录来实现,其中5
’‑
帽共同转录表达到rna链中,或者可使用加帽酶转录后与rna连接。
[0168]
在一些实施方案中,rna的构建单元(building block)帽为m
27,3
’‑
o
gppp(m
12
’‑
o
)apg(有时也称为m
27,3’o
g(5’)ppp(5’)m2’‑
o
apg),其具有以下结构:
[0169][0170]
下面是示例性cap1 rna,其包含rna和m
27,3`o
g(5’)ppp(5’)m2’‑
o
apg:
[0171][0172]
下面是另一示例性cap1 rna(无cap类似物):
[0173][0174]
在一些实施方案中,用“cap0”结构修饰rna,所述“cap0”结构在一个实施方案中使用了具有以下结构的帽类似物反逆转帽(arca帽(m
27,3`o
g(5’)ppp(5’)g)):
[0175][0176]
下面是包含rna和m
27,3`o
g(5’)ppp(5’)g的一个示例性cap0 rna:
[0177][0178]
在一些实施方案中,使用具有以下结构的帽类似物β
‑
s
‑
arca(m
27,2`o
g(5’)ppsp(5’)g)产生“cap0”结构:
[0179][0180]
下面是包含β
‑
s
‑
arca(m
27,2`o
g(5’)ppsp(5’)g)和rna的一个示例性cap0 rna:
[0181][0182]
在一些实施方案中,根据本公开内容的rna包含5
’‑
utr和/或3
’‑
utr。术语“非翻译区”或”utr”涉及dna分子中被转录但未被翻译成氨基酸序列的区域,或涉及rna分子(例如mrna分子)中的相应区域。非翻译区(utr)可存在于开放阅读框的5’(上游)(5
’‑
utr)和/或开放阅读框的3’(下游)(3
’‑
utr)。5
’‑
utr(如果存在的话)位于5’端,蛋白质编码区的起始密码子的上游。5
’‑
utr位于5
’‑
帽(如果存在的话)的下游,例如直接与5’帽相邻。3
’‑
utr(如果存在的话)位于3’端,蛋白质编码区的终止密码子的下游,但是术语“3
’‑
utr”优选不包含
poly(a)序列。因此,3
’‑
utr位于poly(a)序列(如果存在的话)的上游,例如直接与poly(a)序列相邻。
[0183]
在一些实施方案中,根据本公开内容的rna包含3
’‑
poly(a)序列。本文中使用的术语“poly(a)序列”或“poly
‑
a尾”是指腺苷酸残基的不间断或间断的序列,其通常位于rna分子的3’端。poly(a)序列为本领域技术人员已知的,并且可在本文中所述rna中紧接3’utr。poly(a)序列可以是任意长度。在一些实施方案中,poly(a)序列包含以下或由以下组成:至少20、至少30、至少40、至少80或至少100且至多500、至多400、至多300、至多200或至多150个核苷酸,特别是约110个核苷酸。在一些实施方案中,poly(a)序列仅由a核苷酸组成。在一些实施方案中,poly(a)序列基本上由a核苷酸组成,但被四种核苷酸(a、c、g和u)的随机序列间断,如通过引用在此并入的wo 2016/005324 a1中所公开的。这样的随机序列的长度可以是5至50、10至30或10至20个核苷酸。存在于dna编码链中、基本上由da核苷酸组成但被具有平均分布的四种核苷酸(da、dc、dg、dt)的随机序列间断、并且具有例如5至50个核苷酸的长度的poly(a)盒在dna水平上显示出质粒dna在大肠杆菌(e.coli)中的恒定增殖,并且在rna水平上仍然与关于支持rna稳定性和翻译效率的有益特性相关。在一些实施方案中,除a核苷酸之外,没有核苷酸在其3’端侧接poly(a)序列,即poly(a)序列在其3’端未被除a之外的核苷酸掩蔽或紧接。
[0184]
在本公开内容的上下文中,术语“转录”涉及其中dna序列中的遗传密码转录成rna的过程。随后,rna可被翻译成肽或蛋白质。
[0185]“编码”是指多核苷酸(例如基因、cdna或mrna)中特定核苷酸序列的用作在生物过程中合成其他聚合物和大分子的模板的固有特性,所述其他聚合物和大分子具有限定的核苷酸序列(即rrna、trna和mrna)或限定的氨基酸序列和由其产生的生物学特性。因此,如果与该基因对应的mrna的转录和翻译在细胞或其他生物系统中产生蛋白质,则该基因编码蛋白质。核苷酸序列与mrna序列相同且通常在序列表中提供的编码链和用作基因或cdna转录模板的非编码链二者均可称为该基因或cdna编码蛋白质或其他产物。
[0186]
本文中使用的“内源性”是指来自或产生于有机体、细胞、组织或系统内部的任何物质。
[0187]
本文中使用的术语“外源性”是指从有机体、细胞、组织或系统外部引入或产生的任何物质。
[0188]
本文中使用的术语“表达”定义为特定核苷酸序列的转录和/或翻译。
[0189]
本文中使用的术语“连接的”、“融合的”或“融合/融合物”可互换使用。这些术语是指将两个或更多个要素或组成或结构域连接在一起。
[0190]
细胞因子
[0191]
细胞因子是一类在细胞信号传导中重要的小蛋白质(约5至20kda)。它们的释放对它们周围细胞的行为有影响。细胞因子作为免疫调节剂参与自分泌信号传导、旁分泌信号传导和内分泌信号传导。细胞因子包括趋化因子、干扰素、白介素、淋巴因子和肿瘤坏死因子,但通常不包括激素或生长因子(尽管术语有些重叠)。细胞因子由广泛多种的细胞产生,所述细胞包括免疫细胞,例如巨噬细胞、b淋巴细胞、t淋巴细胞和肥大细胞,以及内皮细胞、成纤维细胞和多种基质细胞。给定的细胞因子可由多于一种的细胞类型产生。细胞因子通过受体起作用,并且在免疫系统中尤为重要;细胞因子调节体液免疫应答和基于细胞的免
疫应答之间的平衡,并且它们调节特定细胞群体的成熟、生长和反应性。一些细胞因子以复杂的方式增强或抑制另一些细胞因子的作用。
[0192]
il2和il2r
[0193]
白介素
‑
2(il2)是一种细胞因子,其诱导抗原活化的t细胞的增殖并刺激自然杀伤(nk)细胞。il2的生物活性是通过跨细胞膜的以下三个多肽亚基的多亚基il2受体复合体(il2r)介导的:p55(il2rα,α亚基,在人中也称为cd25)、p75(il2rβ,β亚基,在人中也称为cd122)和p64(il2rγ,γ亚基,在人中也称为cd132)。t细胞对il2的响应取决于多种因素,包括:(1)il2的浓度;(2)细胞表面上il2r分子的数目;以及(3)il2占据的il2r的数目(即,il2和il2r之间的结合相互作用的亲和力(smith,“cell growth signal transduction is quantal”in receptor activation by antigens,cytokines,hormones,and growth factors 766:263
‑
271,1995))。il2:il2r复合体在配体结合之后被内化,并且不同组分进行差异分选。当作为静脉内(intravenous,i.v.)推注施用时,il2具有快速的全身清除(半衰期为12.9分钟的初始清除阶段,接着是半衰期为85分钟的较慢清除阶段)(konrad et al.,cancer res.50:2009
‑
2017,1990)。
[0194]
在真核细胞中,人il2被合成为153个氨基酸的前体多肽,从中去除20个氨基酸以生成成熟的分泌型il2。重组人il2已在大肠杆菌中、昆虫细胞中和哺乳动物cos细胞中产生。
[0195]
癌症患者全身性il2施用的结果远非理想。尽管15%至20%的患者客观地响应于高剂量il2,但大多数患者没有响应,并且许多患者遭受严重的、危及生命的副作用,包括恶心、意识错乱、低血压和感染性休克。与高剂量il2治疗相关的严重毒性很大程度上归因于自然杀伤(nk)细胞的活性。已尝试了通过降低剂量和调整给药方案来降低血清浓度,并且尽管毒性较低,但是这样的治疗的效果也甚小。
[0196]
根据本公开内容,il2(任选地作为pk延长的il2的一部分)可以是天然存在的il2或其片段或变体。il2可以是人il2,并且可以源自任何脊椎动物,特别是任何哺乳动物。本文中使用的“人il2”或“野生型人il2”(无论是天然的还是重组的)具有天然人il2的正常存在的133个氨基酸的序列(少了信号肽,其由另外的20个n端氨基酸组成),其氨基酸序列描述于fujita,et.al,pnas usa,80,7437
‑
7441(1983)中,具有或不具有另外的n端甲硫氨酸,当蛋白质在大肠杆菌中表达为胞内级分时,必须包含所述甲硫氨酸。
[0197]
在一个实施方案中,il2包含seq id no:1或2的氨基酸序列。在一个实施方案中,il2的功能性变体包含与seq id no:1或2具有至少80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的氨基酸序列。在一个实施方案中,il2的功能性变体与il2受体或il2受体的亚基(例如α亚基和/或β/γ亚基)结合。一般而言,出于本公开内容的目的,除非与环境相矛盾,否则本文中使用的术语“il2”包括包含天然存在的il2部分或其功能性变体的任何多肽。
[0198]
根据本公开内容,在某些实施方案中,il2与药代动力学修饰基团连接。相对于游离il2,所得的分子(下文称为“药代动力学(pk)延长的il2”)具有延长的循环半衰期。pk延长的il2的延长的循环半衰期使体内血清il2的浓度维持在治疗范围内,从而有可能导致许多类型的免疫细胞(包括t细胞)的活化增强。由于pk延长的il2的有利的药代动力学谱,其与未经修饰的il2相比可以以较低的频率给药并且持续更长的时间。
[0199]
因此,在本文中所述的某些实施方案中,il2部分与异源多肽(即,不是il2且优选地不是il2的变体的多肽)融合,并且因此是pk延长的il2。在某些实施方案中,pk延长的il2的il2部分是人il2。在另一些实施方案中,pk延长的il2的il2部分是人il2的片段或变体。异源多肽可提高il2的循环半衰期。如下文进一步详细讨论的,提高循环半衰期的多肽可以是血清白蛋白,例如人或小鼠血清白蛋白。
[0200]
根据本公开内容,il2受体(il2r)可以是天然存在的il2r或其片段或变体。il2r可以是人il2r,并且可来源于任何脊椎动物,特别是任何哺乳动物。如果本文中使用的il2包含il2变体,则il2r可以是与il2变体结合的变体受体。
[0201]
干扰素
[0202]
干扰素(ifn)是由宿主细胞响应于多种病原体(例如病毒、细菌、寄生虫以及肿瘤细胞)的存在而产生和释放的一组信号传导蛋白。在典型情况下,病毒感染的细胞将释放干扰素,导致附近的细胞增强其抗病毒防御。
[0203]
基于受体(通过其干扰素发出信号)的类型,干扰素通常分为三类:i型干扰素、ii型干扰素和iii型干扰素。
[0204]
所有i型干扰素均与称为ifn
‑
α/β受体(ifnar)的特定细胞表面受体复合体结合,所述ifn
‑
α/β受体(ifnar)由ifnar1和ifnar2链组成。
[0205]
人中存在的i型干扰素为ifnα、ifnβ、ifnε、ifnκ和ifnω。一般来说,i型干扰素是在身体识别入侵身体的病毒时产生的。它们由成纤维细胞和单核细胞产生。一旦释放,i型干扰素会与靶细胞上的特定受体结合,从而导致表达将阻止病毒产生和复制其rna和dna的蛋白质。
[0206]
ifnα蛋白主要由浆细胞样树突细胞(pdc)产生。它们主要参与针对病毒感染的先天免疫。负责其合成的基因以被称为以下的13种亚型出现:ifna1、ifna2、ifna4、ifna5、ifna6、ifna7、ifna8、ifna10、ifna13、ifna14、ifna16、ifna17、ifna21。这些基因在9号染色体上的簇中一起被发现。
[0207]
ifnβ蛋白由成纤维细胞大量产生。它们具有主要涉及先天免疫应答的抗病毒活性。已经描述了两种类型的ifnβ,ifnβ1和ifnβ3。ifnβ1的天然和重组形式具有抗病毒、抗菌和抗癌特性。
[0208]
ii型干扰素(人中的ifnγ)也称为免疫干扰素,并且由il12活化。此外,ii型干扰素由细胞毒性t细胞和t辅助细胞释放。
[0209]
iii型干扰素通过由il10r2(也称为crf2
‑
4)和ifnlr1(也称为crf2
‑
12)组成的受体复合体发出信号。尽管iii型干扰素比i型和ii型干扰素发现得更晚,但最近的信息表明了iii型干扰素在一些类型的病毒或真菌感染中的重要性。
[0210]
一般来说,i型和ii型干扰素负责调节和活化免疫应答。
[0211]
根据本公开内容,i型干扰素优选为ifnα或ifnβ,更优选为ifnα。
[0212]
根据本公开内容,ifnα可为天然存在的ifnα或其片段或变体。ifnα可以是人ifnα,并且可源自任何脊椎动物,特别是任何哺乳动物。在一个实施方案中,ifnα包含seq id no:3的氨基酸序列。在一个实施方案中,ifnα的功能性变体包含与seq id no:3具有至少80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的氨基酸序列。在一个实施方案中,ifnα的功能性变体与
pharmacists and in peters et al.,pharmacokinetic analysis:a practical approach(1996)中提供另外的细节。也参考gibaldi,m.et al.,pharmacokinetics,2nd rev.edition,marcel dekker(1982)。
[0218]
在某些实施方案中,pk延长基团包括血清白蛋白或其片段或者血清白蛋白或其片段的变体(出于本公开内容的目的,所有这些均由术语“白蛋白”包括)。本文中所述的多肽可以与白蛋白(或其片段或变体)融合以形成白蛋白融合蛋白。这样的白蛋白融合蛋白在美国公开no.20070048282中描述。
[0219]
本文中使用的“白蛋白融合蛋白”是指通过将至少一个白蛋白分子(或其片段或变体)与至少一个蛋白质分子(例如治疗性蛋白质,特别是il2(或其变体))融合而形成的蛋白质。白蛋白融合蛋白可通过翻译核酸来产生,其中编码治疗性蛋白质的多核苷酸与编码白蛋白的多核苷酸框内连接。治疗性蛋白质和白蛋白(曾经是白蛋白融合蛋白的一部分)可各自被称为白蛋白融合蛋白的“部分(portion)”、“区域”或“部分(moiety)”(例如“治疗性蛋白质部分”或“白蛋白蛋白质部分”)。在一个高度优选的实施方案中,白蛋白融合蛋白包含至少一个治疗性蛋白质分子(包括但不限于治疗性蛋白质的成熟形式)和至少一个白蛋白分子(包括但不限于白蛋白的成熟形式)。在一个实施方案中,白蛋白融合蛋白由用于所施用rna的宿主细胞(例如靶器官的细胞(例如肝细胞))加工并被分泌到循环中。在用于表达rna的宿主细胞分泌途径中发生的新生白蛋白融合蛋白的加工可包括但不限于:信号肽切割;二硫键形成;适当折叠;碳水化合物的添加和加工(例如如n
‑
和o
‑
连接糖基化);特定的蛋白水解切割;和/或组装成多聚体蛋白质。白蛋白融合蛋白优选由rna以特别地在其n端具有信号肽的非加工形式编码,并且在由细胞分泌之后优选以加工的形式存在,其中特别地信号肽已被切割掉。在一个最优选的实施方案中,“白蛋白融合蛋白的加工形式”是指已经经历了n端信号肽切割的白蛋白融合蛋白产物,在本文中也称为“成熟的白蛋白融合蛋白”。
[0220]
在一些优选实施方案中,包含治疗性蛋白质的白蛋白融合蛋白与不与白蛋白融合的相同治疗性蛋白质的血浆稳定性相比,具有更高的血浆稳定性。血浆稳定性通常是指当体内施用治疗性蛋白质并带入血流中与当治疗性蛋白质被降解并从血流中被清除至器官(例如肾或肝)(最终从身体清除治疗性蛋白质)之间的时间段。根据治疗性蛋白质在血流中的半衰期来计算血浆稳定性。治疗性蛋白质在血流中的半衰期可通过本领域已知的常规测定法容易地确定。
[0221]
本文中使用的“白蛋白”统指具有白蛋白的一种或更多种功能活性(例如,生物活性)的白蛋白蛋白质或氨基酸序列,或白蛋白片段或变体。特别地,“白蛋白”是指人白蛋白或其片段或变体,特别是人白蛋白的成熟形式,或者来自其他脊椎动物的白蛋白或其片段,或这些分子的变体。白蛋白可来源于任何脊椎动物,特别是任何哺乳动物,例如人、牛、绵羊或猪。非哺乳动物白蛋白包括但不限于母鸡和鲑鱼。白蛋白融合蛋白的白蛋白部分可来自与治疗性蛋白质部分不同的动物。
[0222]
在某些实施方案中,白蛋白是人血清白蛋白(hsa)或其片段或变体,例如在us 5,876,969、wo 2011/124718、wo 2013/075066和wo 2011/0514789中公开的那些。
[0223]
术语人血清白蛋白(hsa)和人白蛋白(ha)在本文中可互换使用。术语“白蛋白”和“血清白蛋白”更广泛,并且涵盖人血清白蛋白(及其片段和变体)以及来自其他物种的白蛋白(及其片段和变体)。
[0224]
本文中使用的足以延长治疗性蛋白质的治疗活性或血浆稳定性的白蛋白片段是指这样的白蛋白片段:长度或结构足以稳定或延长蛋白质的治疗活性或血浆稳定性,使得白蛋白融合蛋白的治疗性蛋白质部分的血浆稳定性与非融合状态下的血浆稳定性相比延长或延伸。
[0225]
白蛋白融合蛋白的白蛋白部分可包含白蛋白序列的全长,或者可包含其一个或更多个能够稳定或延长治疗活性或血浆稳定性的片段。这样的片段的长度可以是10个或更多个氨基酸,或者可包含来自白蛋白序列的约15、20、25、30、50或更多个连续氨基酸,或者可包含白蛋白的特定结构域的一部分或全部。例如,可使用跨越前两个免疫球蛋白样结构域的hsa的一个或更多个片段。在一个优选实施方案中,hsa片段是hsa的成熟形式。
[0226]
一般而言,白蛋白片段或变体将是至少100个氨基酸长,优选至少150个氨基酸长。
[0227]
根据本公开内容,白蛋白可以是天然存在的白蛋白或其片段或变体。白蛋白可以是人白蛋白,并且可来源于任何脊椎动物,特别是任何哺乳动物。在一个实施方案中,白蛋白包含seq id no:4或5的氨基酸序列或与seq id no:4或5具有至少80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同一性的氨基酸序列。
[0228]
优选地,白蛋白融合蛋白包含白蛋白作为n端部分并且包含治疗性蛋白质作为c端部分。或者,也可使用包含白蛋白作为c端部分并且包含治疗性蛋白质作为n端部分的白蛋白融合蛋白。在另一些实施方案中,白蛋白融合蛋白具有与白蛋白的n端和c端二者融合的治疗性蛋白质。在一个优选实施方案中,在n端和c端融合的治疗性蛋白质是相同的治疗性蛋白质。在另一个优选实施方案中,在n端和c端融合的治疗性蛋白质是不同的治疗性蛋白质。在一个实施方案中,不同的治疗性蛋白质均是细胞因子。
[0229]
在一个实施方案中,治疗性蛋白质通过肽接头与白蛋白连接。融合的部分之间的接头肽可在部分之间提供更大的物理分离,并因此使治疗性蛋白质部分的可及性最大化,例如,用于与其同源受体结合。接头肽可由氨基酸组成使得它是柔性的或更刚性的。接头序列可被蛋白酶或化学地切割。
[0230]
本文中使用的术语“fc区”是指天然免疫球蛋白的由其两条重链的各自的fc结构域(或fc部分)形成的部分。本文中使用的术语“fc结构域”是指单个免疫球蛋白(ig)重链的部分或片段,其中fc结构域不包含fv结构域。在某些实施方案中,fc结构域在正好位于木瓜蛋白酶切割位点上游的铰链区中开始,并终止于抗体的c端。因此,完整的fc结构域包含至少铰链结构域、ch2结构域和ch3结构域。在某些实施方案中,fc结构域包含以下至少之一:铰链(例如,上部、中间和/或下部铰链区)结构域,ch2结构域,ch3结构域,ch4结构域,或者其变体、部分或片段。在某些实施方案中,fc结构域包含完整的fc结构域(即,铰链结构域、ch2结构域和ch3结构域)。在某些实施方案中,fc结构域包含与ch3结构域(或其部分)融合的铰链结构域(或其部分)。在某些实施方案中,fc结构域包含与ch3结构域(或其部分)融合的ch2结构域(或其部分)。在某些实施方案中,fc结构域由ch3结构域或其部分组成。在某些实施方案中,fc结构域由铰链结构域(或其部分)和ch3结构域(或其部分)组成。在某些实施方案中,fc结构域由ch2结构域(或其部分)和ch3结构域组成。在某些实施方案中,fc结构域由铰链结构域(或其部分)和ch2结构域(或其部分)组成。在某些实施方案中,fc结构域缺少ch2结构域的至少一部分(例如,ch2结构域的全部或部分)。本文中的fc结构域通常是指包
含免疫球蛋白重链的fc结构域的全部或部分的多肽。这包括但不限于包含完整的ch1、铰链、ch2和/或ch3结构域的多肽,以及仅包含例如铰链、ch2和ch3结构域的这样的肽的片段。fc结构域可来源于任何物种和/或任何亚型的免疫球蛋白,包括但不限于:人igg1、igg2、igg3、igg4、igd、iga、ige或igm抗体。fc结构域涵盖天然fc和fc变体分子。如本文中所述,本领域普通技术人员将理解,任何fc结构域可被修饰,使得其氨基酸序列与天然存在的免疫球蛋白分子的天然fc结构域不同。在某些实施方案中,fc结构域具有降低的效应子功能(例如,fcγr结合)。
[0231]
本文中所述的多肽的fc结构域可来源于不同的免疫球蛋白分子。例如,多肽的fc结构域可包含来源于igg1分子的ch2和/或ch3结构域和来源于igg3分子的铰链区。在另一个实例中,fc结构域可包含部分地来源于igg1分子且部分地来源于igg3分子的嵌合铰链区。在另一个实例中,fc结构域可包含部分地来源于igg1分子且部分地来源于igg4分子的嵌合铰链。
[0232]
在某些实施方案中,pk延长基团包含fc结构域或其片段或者fc结构域或其片段的变体(出于本公开内容的目的,所有这些均由术语“fc结构域”包括)。fc结构域不包含与抗原结合的可变区。适用于本公开内容的fc结构域可获自许多不同的来源。在某些实施方案中,fc结构域来源于人免疫球蛋白。在某些实施方案中,fc结构域来自人igg1恒定区。然而,应理解,fc结构域可来源于其他哺乳动物物种的免疫球蛋白,所述物种包括例如啮齿动物(例如,小鼠、大鼠、兔、豚鼠)或非人灵长类(例如,黑猩猩、猕猴)物种。
[0233]
此外,fc结构域(或其片段或变体)可来源于任何免疫球蛋白种类,包括igm、igg、igd、iga和ige,并且可来源于任何免疫球蛋白同种型,包括igg1、igg2、igg3和igg4。
[0234]
多种fc结构域基因序列(例如,小鼠和人恒定区基因序列)均可以以公共可获得的保藏物的形式得到。可选择缺乏特定效应子功能和/或具有特定修饰以降低免疫原性的包含fc结构域序列的恒定区结构域。许多抗体和抗体编码基因的序列已被公布,并且可使用本领域公认的技术从这些序列中得到合适的fc结构域序列(例如,铰链、ch2和/或ch3序列或其片段或变体)。
[0235]
在某些实施方案中,pk延长基团是血清白蛋白结合蛋白,例如在us2005/0287153、us2007/0003549、us2007/0178082、us2007/0269422、us2010/0113339、wo2009/083804和wo2009/133208中描述的那些,其通过引用整体并入本文。在某些实施方案中,pk延长基团是转铁蛋白,如在us 7,176,278和us 8,158,579中公开的,其通过引用整体并入本文。在某些实施方案中,pk延长基团是血清免疫球蛋白结合蛋白,例如在us2007/0178082、us2014/0220017和us2017/0145062中公开的那些,其通过引用整体并入本文。在某些实施方案中,pk延长基团是与血清白蛋白结合的基于纤连蛋白(fn)的支架结构域蛋白,例如us2012/0094909中公开的那些,其通过引用整体并入本文。在us2012/0094909中还公开了制备基于纤连蛋白的支架结构域蛋白的方法。基于fn3的pk延长基团的一个非限制性实例是fn3(hsa),即与人血清白蛋白结合的fn3蛋白。
[0236]
在某些方面中,适合于根据本公开内容使用的pk延长的il,可采用一种或更多种肽接头。本文中使用的术语“肽接头”是指在多肽链的线性氨基酸序列中连接两个或更多个结构域(例如,pk延长的部分和il部分,例如il2)的肽或多肽序列。例如,肽接头可用于将il2部分与hsa结构域连接。
[0237]
适合于将pk延长基团与例如il2融合的接头是本领域公知的。一些示例性的接头包括甘氨酸
‑
丝氨酸
‑
多肽接头、甘氨酸
‑
脯氨酸
‑
多肽接头和脯氨酸
‑
丙氨酸多肽接头。在某些实施方案中,接头是甘氨酸
‑
丝氨酸
‑
多肽接头,即由甘氨酸和丝氨酸残基组成的肽。
[0238]
除上述异源多肽之外或代替上述异源多肽,本文中所述的il2变体多肽可包含编码“标志物”或“报道子”的序列。标志物或报道子基因的一些实例包括β
‑
内酰胺酶、氯霉素乙酰转移酶(chloramphenicol acetyltransferase,cat)、腺苷脱氨酶(adenosine deaminase,ada)、氨基糖苷磷酸转移酶、二氢叶酸还原酶(dihydrofolate reductase,dhfr)、潮霉素
‑
b
‑
磷酸转移酶(hygromycin
‑
b
‑
hosphotransferase,hph)、胸苷激酶(thymidine kinase,tk)、β
‑
半乳糖苷酶以及黄嘌呤鸟嘌呤磷酸核糖基转移酶(xanthine guanine phosphoribosyltransferase,xgprt)。
[0239]
抗原受体
[0240]
本文中所述的免疫效应细胞可表达结合抗原或其加工产物的抗原受体,例如t细胞受体(tcr)或嵌合抗原受体(car),特别是当存在于靶细胞上或由靶细胞呈递时。细胞可天然表达抗原受体或经修饰(例如,离体/体外或在待治疗对象中在体内)以表达抗原受体。此外,免疫效应细胞可表达il2r或可经修饰(例如,离体/体外或在待治疗对象中在体内)以表达il2r。在一个实施方案中,同时或在不同时间点进行离体/体外修饰以表达il2r和进行离体/体外修饰以表达抗原受体。随后,可向患者施用经修饰的细胞。在一个实施方案中,表达il2r的修饰离体/体外发生,并且在向患者施用细胞之后,表达抗原受体的修饰在体内发生。在一个实施方案中,表达抗原受体的修饰离体/体外发生,并且在向患者施用细胞之后,表达il2r的修饰在体内发生。在一个实施方案中,表达il2r的修饰和表达抗原受体的修饰同时或在不同时间点在体内发生。该细胞可以是患者的内源性细胞,或者可以已经施用于患者。
[0241]
嵌合抗原受体
[0242]
由于car修饰的t细胞可以被改造以靶向几乎任何肿瘤抗原,因此用表达嵌合抗原受体的car改造t细胞进行过继性细胞转移治疗是有前景的抗癌治疗。例如,可以将患者的t细胞遗传改造(遗传修饰)成表达特异性针对患者肿瘤细胞上的抗原的car,然后输注回患者中。
[0243]
根据本发明,术语“car”(或“嵌合抗原受体”)与术语“嵌合t细胞受体”和“人工t细胞受体”同义,并且涉及包含单一分子或分子复合体的人工受体,其识别靶细胞(例如癌细胞)上的靶结构(例如抗原)(即与其结合)(例如通过抗原结合结构域与靶细胞表面上表达的抗原结合)并且可赋予免疫效应细胞例如在细胞表面上表达所述car的t细胞以特异性。优选地,靶结构被car识别使得表达所述car的免疫效应细胞被活化。car可以包含一个或更多个蛋白质单元,所述蛋白质单元包含如本文中所述的一个或更多个结构域。术语“car”不包括t细胞受体。
[0244]
car包含靶标特异性结合元件,或者称为抗原结合部分或抗原结合结构域,其通常是car胞外结构域的一部分。抗原结合结构域识别充当靶细胞上与特定疾病状态相关的细胞表面标志物的配体。具体地,本发明的car靶向病变细胞(例如肿瘤细胞)上的抗原(例如肿瘤抗原)。
[0245]
在一个实施方案中,car中的结合结构域与抗原特异性结合。在一个实施方案中,
与car中的结合结构域结合的抗原在癌细胞中表达(肿瘤抗原)。在一个实施方案中,抗原在癌细胞表面上表达。在一个实施方案中,结合结构域与抗原的胞外结构域或胞外结构域中的表位结合。在一个实施方案中,结合结构域与存在于活细胞表面的抗原的天然表位结合。
[0246]
在本发明的一个实施方案中,抗原结合结构域包含对抗原具有特异性的免疫球蛋白重链可变区(vh)和对抗原具有特异性的免疫球蛋白轻链可变区(vl)。在一个实施方案中,免疫球蛋白是抗体。在一个实施方案中,所述重链可变区(vh)和相应的轻链可变区(vl)通过肽接头连接。优选地,car中的抗原结合部分是scfv。
[0247]
car被设计为包含与car胞外结构域融合的跨膜结构域。在一个实施方案中,跨膜结构域不与car中的结构域之一天然缔合。在一个实施方案中,跨膜结构域与car中的结构域之一天然缔合。在一个实施方案中,通过氨基酸替换来修饰跨膜结构域以避免这样的结构域与具有相同或不同表面膜蛋白的跨膜结构域结合,以使与受体复合体的其他成员的相互作用最小化。跨膜结构域可源自天然或合成来源。在来源是天然的情况下,结构域可来源于任何膜结合蛋白或跨膜蛋白。在本发明中具有特定用途的跨膜区可来源于以下(即至少包含以下的跨膜区):t细胞受体的α、β或ζ链、cd28、cd3ε、cd45、cd4、cd5、cd8、cd9、cd16、cd22、cd33、cd37、cd64、cd80、cd86、cd134、cd137、cd154。或者,跨膜结构域可以是合成的,在这种情况下其将主要包含疏水性残基例如亮氨酸和缬氨酸。优选地,苯丙氨酸、色氨酸和缬氨酸的三联体将存在于合成跨膜结构域的每个末端。
[0248]
在一些实例中,本发明的car包含形成跨膜结构域和胞外结构域之间的连接的铰链结构域。
[0249]
car的胞质结构域或另外的胞内信号传导结构域负责活化其中已放置car的免疫细胞的至少一种正常效应子功能。术语“效应子功能”是指细胞的特化功能。例如,t细胞的效应子功能可以是细胞裂解活性或辅助活性,包括分泌细胞因子。因此,术语“胞内信号传导结构域”是指转导效应子功能信号并指导细胞进行特化功能的蛋白质的部分。虽然通常可以使用整个胞内信号传导结构域,但是在许多情况下不需要使用整个链。就使用胞内信号传导结构域的截短部分来说,这样的截短部分可用于代替完整链,只要其转导效应子功能信号即可。术语胞内信号传导结构域因此意味着包括胞内信号传导结构域的足以转导效应子功能信号的任何截短部分。
[0250]
已知通过单独tcr产生的信号不足以完全活化t细胞并且还需要次级信号或共刺激信号。因此,t细胞活化可以被认为由两种不同种类的胞质信号传导序列介导:通过tcr起始抗原依赖性初级活化的那些(初级胞质信号传导序列)和以抗原独立性方式作用以提供次级或共刺激信号的那些(次级胞质信号传导序列)。
[0251]
在一个实施方案中,car包含来源于cd3ζ的初级胞质信号传导序列。此外,car的胞质结构域可包含与共刺激信号传导区结合的cd3ζ信号传导结构域。
[0252]
共刺激结构域的特性仅限于其具有在car与靶向部分结合之后增强细胞增殖和存活的能力。合适的共刺激结构域包括cd28、cd137(4
‑
1bb)(肿瘤坏死因子受体(tnfr)超家族成员)、cd134(ox40)(tnfr受体超家族成员)和cd278(icos)(在活化的t细胞上表达的cd28超家族共刺激分子)。技术人员将理解,可以使用这些提及的共刺激结构域的序列变体而对本发明无不利影响,其中所述变体与其模拟的结构域具有相同或类似的活性。这样的变体与其来源于的结构域的氨基酸序列具有至少约80%的序列同一性。在本发明的一些实施方
案中,car构建体包含两个共刺激结构域。虽然一些具体组合包括四种提及的结构域的所有可能变化方案,但是一些具体实例包括cd28 cd137(4
‑
1bb)和cd28 cd134(ox40)。
[0253]
car的胞质信号传导部分内的胞质信号传导序列可以以随机或特定的顺序相互连接。任选地,短的寡肽接头或多肽接头(优选长度为2至10个氨基酸)可形成连接。甘氨酸
‑
丝氨酸双联体提供特别合适的接头。
[0254]
在一个实施方案中,car包含将新生蛋白质导入内质网的信号肽。在一个实施方案中,信号肽在抗原结合结构域之前。在一个实施方案中,信号肽源自例如igg的免疫球蛋白。
[0255]
术语“抗体”包括包含通过二硫键相互连接的至少两条重(h)链和两条轻(l)链的免疫球蛋白。每条重链由重链可变区(本文中缩写为vh)和重链恒定区构成。每条轻链由轻链可变区(本文中缩写为vl)和轻链恒定区构成。vh和vl区可进一步细分为高变区,称为互补决定区(complementarity determining region,cdr),其间散布着更为保守的区域,称为框架区(framework region,fr)。每个vh和vl由从氨基端到羧基端按以下顺序排列的三个cdr和四个fr构成:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4。重链和轻链的可变区包含与抗原相互作用的结合结构域。抗体的恒定区可介导免疫球蛋白与宿主组织或因子的结合,所述宿主组织或因子包括免疫系统的多种细胞(例如,效应细胞)和经典补体系统的第一组分(clq)。抗体与抗原结合,优选与抗原特异性结合。抗体可以是源自天然来源或重组来源的完整免疫球蛋白,并且可以是完整免疫球蛋白的免疫反应性部分或片段。抗体通常是免疫球蛋白分子的四聚体。本发明中的抗体可以以多种形式存在,包括例如多克隆抗体、单克隆抗体、fv、fab和f(ab’)2,以及单链抗体和人源化抗体(harlow et al.,1999,in:using antibodies:a laboratory manual,cold spring harbor laboratory press,ny;harlow et al.,1989,in:antibodies:a laboratory manual,cold spring harbor,new york;houston et al.,1988,proc.natl.acad.sci.usa 85:5879
‑
5883;bird et al.,1988,science 242:423
‑
426)。
[0256]
b细胞表达的抗体有时被称为bcr(b细胞受体)或抗原受体。这类蛋白质包括五个成员:iga、igg、igm、igd和ige。iga是存在于身体分泌物中的一级抗体,所述身体分泌物例如唾液、泪、母乳、胃肠道分泌物以及呼吸道和泌尿生殖道的黏液分泌物。igg是最常见的循环抗体。igm是大多数对象中初级免疫应答中产生的主要免疫球蛋白。它是在凝集、补体固定和其他抗体应答方面最高效的免疫球蛋白,并且在抵御细菌和病毒方面很重要。igd是没有已知的抗体功能但可以作为抗原受体的免疫球蛋白。ige是在暴露于变应原时通过引起肥大细胞和嗜碱性粒细胞释放介质介导速发型超敏反应的免疫球蛋白。
[0257]
术语“抗体片段”是指完整抗体的一部分,并且通常包含完整抗体的抗原决定可变区。
[0258]
抗体片段的一些实例包括但不限于fab、fab’、f(ab’)2和fv片段、线性抗体、scfv抗体和由抗体片段形成的多特异性抗体。
[0259]
本文中使用的“抗体重链”是指抗体分子中以其天然存在的构象存在的两种类型的多肽链中较大的一者。
[0260]
本文中使用的“抗体轻链”是指抗体分子中以其天然存在的构象存在的两种类型的多肽链中较小的一者,κ和λ轻链是指两种主要的抗体轻链同种型。
[0261]
根据本公开内容,car当存在于t细胞上时识别抗原(例如抗原呈递细胞或病变细
胞(例如癌细胞)表面上的抗原),使得该t细胞被刺激,和/或扩增或发挥如上所述的效应子功能。
[0262]
免疫效应细胞的遗传修饰
[0263]
可使用多种方法将il2受体和/或抗原受体(例如car构建体)引入例如t细胞的细胞中,以产生经遗传修饰以表达il2受体和/或抗原受体的细胞。这样的方法包括基于非病毒的dna转染、基于非病毒的rna转染,例如mrna转染、基于转座子的系统和基于病毒的系统。基于非病毒的dna转染具有低插入诱变风险。与不包含整合元件的质粒相比,基于转座子的系统可以更高效地整合转基因。基于病毒的系统包括使用γ
‑
逆转录病毒和慢病毒载体。γ
‑
逆转录病毒相对容易生产,高效且永久地转导t细胞,并且从原代人t细胞的整合观点来看已被初步证明是安全的。慢病毒载体也高效且永久地转导t细胞,但是制造更加昂贵。它们相比于基于逆转录病毒的系统还可能更加安全。
[0264]
在本发明所有方面的一个实施方案中,用编码il2受体的核酸和/或编码抗原受体的核酸离体或体内转染t细胞或t细胞祖细胞。在一个实施方案中,可使用离体和体内转染的组合。在本发明所有方面的一个实施方案中,t细胞或t细胞祖细胞来自待治疗的对象。在本发明所有方面的一个实施方案中,t细胞或t细胞祖细胞来自与待治疗的对象不同的对象。
[0265]
可以使用靶向t细胞的纳米粒在体内并因此几乎瞬时地产生car t细胞。例如,基于聚(β
‑
氨基酯)的纳米粒可以与抗cd3e f(ab)片段偶联以结合t细胞上的cd3。与t细胞结合之后,这些纳米粒被内吞。它们的内容物,例如编码抗肿瘤抗原car的质粒dna,可定向到t细胞核,由于包含含有微管相关序列(microtubule
‑
associated sequence,mtas)和核定位信号(nuclear localization signal,nls)的肽。包含car基因表达盒侧翼的转座子和编码过度活跃转座酶的单独质粒可允许car载体有效整合到染色体中。smith et al.(2017)nat.nanotechnol.12:813
‑
820中描述了这样的允许在纳米粒输注之后在体内产生car t细胞的系统。
[0266]
另一种可能性是使用crispr/cas9方法有意将car编码序列置于特定基因座处。例如,现有的t细胞受体(tcr)可被敲除,同时敲入car并将其置于内源性启动子的动态调节控制下,否则其会弱化tcr的表达;参考例如,eyquem et al.(2017)nature 543:113
‑
117。
[0267]
在本发明所有方面的一个实施方案中,经遗传修饰以表达一种或更多种il2受体多肽和/或抗原受体的细胞用编码il2受体多肽的核酸和/或编码抗原受体的核酸稳定或瞬时转染。在一个实施方案中,将细胞用一些核酸稳定转染,并用其他核酸瞬时转染。因此,编码il2受体多肽的核酸和/或编码抗原受体的核酸被整合或未被整合到细胞的基因组中。
[0268]
在本发明所有方面的一个实施方案中,使经遗传修饰以表达抗原受体的细胞失活以表达内源性t细胞受体和/或内源性hla。
[0269]
在本发明所有方面的一个实施方案中,本文中所述的细胞相对于待治疗的对象可以是自体的、同种异体的或同基因的。在一个实施方案中,本公开内容设想了从患者中去除细胞并随后将所述细胞重新递送至该患者。在一个实施方案中,本发明没有设想从患者中去除细胞。在后一种情况下,细胞的遗传修饰(如果存在的话)的所有步骤都可在体内进行。
[0270]
术语“自体”用于描述来源于同一对象的任何事物。例如,“自体移植”是指来源于同一对象的组织或器官的移植。这样的程序是有利的,因为它们克服了免疫屏障,否则会导
致排斥。
[0271]
术语“同种异体的”用于描述来源于相同物种的不同个体的任何事物。当一个或更多个基因座处的基因不相同时,两个或更多个个体被认为彼此是同种异体的。
[0272]
术语“同基因的”用于描述来源于具有相同基因型的个体或组织(即同卵双胞胎或相同近交品系的动物,或其组织)的任何事物。
[0273]
术语“异源的”用于描述由多个不同要素组成的事物。作为一个实例,将一个个体的骨髓转移到不同个体中构成异源移植。异源基因是来源于除对象之外的来源的基因。
[0274]
抗原
[0275]
在一个实施方案中,本文中所述的方法还包括这样的步骤:无论是离体还是在受治疗的对象中,将免疫效应细胞与同源抗原分子接触,所述免疫效应细胞特别是表达抗原受体的免疫效应细胞,例如经遗传操作以表达抗原受体的免疫效应细胞,其中抗原分子或其加工产物(例如,其片段)与免疫效应细胞携带的抗原受体(例如tcr或car)结合。这样的同源抗原分子在本文中也称为“疫苗抗原”或“包含用于诱导针对抗原的免疫应答的表位的肽或蛋白质”。在一个实施方案中,同源抗原分子选自免疫效应细胞靶向的靶细胞表达的抗原或其片段,或者抗原或片段的变体。在一个实施方案中,免疫效应细胞在发生免疫效应细胞扩增和/或活化的条件下与同源抗原分子接触。在一个实施方案中,免疫效应细胞与同源抗原分子接触的步骤在体内或离体发生。
[0276]
在一个实施方案中,本文中所述方法包括向对象施用同源抗原分子或编码其的核酸的步骤。在一个实施方案中,编码同源抗原分子的核酸在对象的细胞中表达以提供同源抗原分子。在一个实施方案中,同源抗原分子的表达在细胞表面。在一个实施方案中,编码同源抗原分子的核酸在对象的细胞中瞬时表达。在一个实施方案中,编码同源抗原分子的核酸为rna。在一个实施方案中,全身性地施用同源抗原分子或编码其的核酸。在一个实施方案中,在全身性施用编码同源抗原分子的核酸之后,在脾中发生编码同源抗原分子的核酸的表达。在一个实施方案中,在全身性施用编码同源抗原分子的核酸之后,在抗原呈递细胞(优选专职性抗原呈递细胞)中发生编码同源抗原分子的核酸的表达。在一个实施方案中,抗原呈递细胞选自树突细胞、巨噬细胞和b细胞。在一个实施方案中,在全身性施用编码同源抗原分子的核酸之后,在肺和/或肝中不发生或基本上不发生编码同源抗原分子的核酸的表达。在一个实施方案中,在全身性施用编码同源抗原分子的核酸之后,编码同源抗原分子的核酸在脾中的表达是在肺中表达量的至少5倍。
[0277]
根据本发明向对象提供的肽和蛋白质抗原(通过施用肽和蛋白质抗原或者编码所述肽和蛋白质抗原的核酸,特别是rna),即疫苗抗原,优选在施用该肽或蛋白质抗原或核酸的对象中导致免疫效应细胞的刺激、引发和/或扩增。所述刺激、引发和/或扩增的免疫效应细胞优选针对靶抗原,特别是由病变细胞、组织和/或器官表达的靶抗原,即疾病相关抗原。因此,疫苗抗原可包含疾病相关抗原或其片段或变体。在一个实施方案中,这样的片段或变体与疾病相关抗原免疫学上等同。在本公开内容的上下文中,术语“抗原的片段”或“抗原的变体”意指导致免疫效应细胞的刺激、引发和/或扩增的物质,该刺激、引发和/或扩增的免疫效应细胞靶向抗原,即疾病相关抗原,特别是当由病变细胞、组织和/或器官呈递时。因此,疫苗抗原可对应于或可包含疾病相关抗原,可对应于或可包含疾病相关抗原的片段,或者可对应于或可包含与疾病相关抗原或其片段同源的抗原。如果疫苗抗原包含疾病相关抗
原的片段或与疾病相关抗原的片段同源的氨基酸序列,则所述片段或氨基酸序列可包含免疫效应细胞的抗原受体所靶向的疾病相关抗原的表位或与疾病相关抗原的表位同源的序列。因此,根据本公开内容,疫苗抗原可包含疾病相关抗原的免疫原性片段或与疾病相关抗原的免疫原性片段同源的氨基酸序列。根据本公开内容的“抗原的免疫原性片段”优选地涉及这样的抗原片段:能够刺激、引发和/或扩增携带与抗原或表达抗原的细胞结合的抗原受体的免疫效应细胞。优选的是疫苗抗原(类似于疾病相关抗原)提供相关表位用于通过存在于免疫效应细胞中的抗原结合结构域结合。在一个实施方案中,疫苗抗原(类似于疾病相关抗原)在细胞例如抗原呈递细胞的表面上表达,以提供相关表位用于通过免疫效应细胞结合。疫苗抗原可以是重组体抗原。
[0278]
在本发明所有方面的一个实施方案中,编码疫苗抗原的核酸在对象的细胞中表达,以提供抗原或其加工产物,用于通过免疫效应细胞表达的抗原受体结合,所述结合导致免疫效应细胞的刺激、引发和/或扩增。
[0279]
术语“免疫学上等同的”意指例如关于免疫效应类型表现出相同或基本上相同的免疫学特性和/或发挥相同或基本上相同的免疫学效应的免疫学上等同的分子,例如免疫学上等同的氨基酸序列。在本公开内容的上下文中,术语“免疫学上等同的”优选地关于抗原或抗原变体用于免疫接种的免疫学效应或特性使用。例如,如果氨基酸序列在暴露于对象的免疫系统(例如与参考氨基酸序列结合的t细胞或表达该参考氨基酸序列的细胞)时诱导具有与参考氨基酸序列反应的特异性的免疫反应,则所述氨基酸序列与该参考氨基酸序列免疫学上等同。因此,在免疫学上等同于抗原的分子在t细胞的刺激、引发和/或扩增方面表现出与t细胞所靶向的抗原相同或基本上相同的特性和/或发挥相同或基本上相同的作用。
[0280]
本文中使用的“活化”或“刺激”是指免疫效应细胞(例如t细胞)的已被充分刺激以诱导可检测的细胞增殖的状态。活化也可与信号传导途径的启动、诱导的细胞因子的产生和可检测的效应子功能有关。术语“活化的免疫效应细胞”尤其是指正在经历细胞分裂的免疫效应细胞。
[0281]
术语“引发”是指其中免疫效应细胞例如t细胞首次与其特异性抗原接触并导致分化为效应细胞例如效应t细胞的过程。
[0282]
术语“克隆扩增”或“扩增”是指其中特定实体扩增的过程。在本公开内容的上下文中,该术语优选在免疫应答的情况下使用,在所述免疫应答中淋巴细胞被抗原刺激,增殖,并且扩增识别所述抗原的特异性淋巴细胞。优选地,克隆扩增导致淋巴细胞分化。
[0283]
术语“抗原”涉及包含这样的表位的物质:针对该表位可产生免疫应答。特别地,术语“抗原”包含蛋白质和肽。在一个实施方案中,抗原由免疫系统的细胞(例如抗原呈递细胞如树突细胞或巨噬细胞)呈递或在其表面上存在。在一个实施方案中,抗原或其加工产物例如t细胞表位,通过抗原受体结合。因此,抗原或其加工产物可与免疫效应细胞例如t淋巴细胞(t细胞)特异性反应。在一个实施方案中,抗原是疾病相关抗原,例如肿瘤抗原、病毒抗原或细菌抗原,并且表位来源于这样的抗原。
[0284]
术语“疾病相关抗原”以其最广泛的含义使用,是指与疾病相关的任何抗原。疾病相关抗原是这样的分子:其包含刺激宿主的免疫系统以产生针对该疾病的细胞抗原特异性免疫应答和/或体液抗体应答的表位。因此,疾病相关抗原或其表位可用于治疗性目的。疾
病相关抗原可与微生物(通常是微生物抗原)感染相关或者与癌症(通常是肿瘤)相关。
[0285]
术语“肿瘤抗原”是指癌细胞的成分,其可来源于细胞质、细胞表面和细胞核。特别地,它是指在细胞内产生或在肿瘤细胞上作为表面抗原产生的那些抗原。肿瘤抗原通常优先地由癌细胞表达(例如,与非癌细胞相比,在癌细胞中其以更高的水平表达),并且在一些情况下,其仅由癌细胞表达。肿瘤抗原的一些实例包括但不限于:p53,art
‑
4,bage,β
‑
联蛋白/m,bcr
‑
ablcamel,cap
‑
1,casp
‑
8,cdc27/m,cdk4/m,cea,密蛋白家族的细胞表面蛋白例如密蛋白
‑
6、密蛋白
‑
18.2和密蛋白
‑
12,c
‑
myc,ct,cyp
‑
b,dam,elf2m,etv6
‑
aml1,g250,gage,gnt
‑
v,gap 100,hage,her
‑
2/neu,hpv
‑
e7,hpv
‑
e6,hast
‑
2,htert(或htrt),lage,ldlr/fut,mage
‑
a,优选mage
‑
a1、mage
‑
a2、mage
‑
a3、mage
‑
a4、mage
‑
a5、mage
‑
a6、mage
‑
a7、mage
‑
a8、mage
‑
a9、mage
‑
a10、mage
‑
a11或mage
‑
a12,mage
‑
b,mage
‑
c,mart
‑
1/melan
‑
a,mc1r,肌球蛋白/m,muc1,mum
‑
1,mum
‑
2,mum
‑
3,na88
‑
a,nf1,ny
‑
eso
‑
1,ny
‑
br
‑
1,pl90小bcr
‑
abl,pml/rara,prame,蛋白酶3,psa,psm,rage,ru1或ru2,sage,sart
‑
1或sart
‑
3,scgb3a2,scp1,scp2,scp3,ssx,存活蛋白,tel/aml1,tpi/m,trp
‑
1,trp
‑
2,trp
‑
2/int2,tpte,wt和wt
‑
1。
[0286]
术语“病毒抗原”是指具有抗原特性,即能够在个体中引起免疫应答的任何病毒组分。病毒抗原可以是病毒核糖核蛋白或包膜蛋白。
[0287]
术语“细菌抗原”是指具有抗原特性,即能够在个体中引起免疫应答的任何细菌组分。细菌抗原可来源于细菌的细胞壁或细胞质膜。
[0288]
术语“在细胞表面上表达”或“与细胞表面相关”意指例如受体或抗原的分子与细胞质膜相关并位于细胞质膜上,其中该分子的至少一部分朝向所述细胞的胞外空间并且可从所述细胞的外部接近,例如,通过位于细胞外的抗体。在该背景下,部分为优选至少4个、优选至少8个、优选至少12个、更优选至少20个氨基酸。该相关可以是直接的或间接的。例如,该相关可以是通过一个或更多个跨膜结构域、一个或更多个脂质锚的,或者是通过与可在细胞质膜外小叶上发现的任何其他蛋白质、脂质、糖类或其他结构的相互作用的。例如,与细胞表面相关的分子可以是具有胞外部分的跨膜蛋白质,或者可以是通过与另一种是跨膜蛋白质的蛋白质相互作用而与细胞表面相关的蛋白质。
[0289]“细胞表面”或“细胞的表面”根据其在本领域中的通常含义使用,并因此包括可由蛋白质和其他分子结合的细胞外部。
[0290]
在本发明的上下文中,术语“胞外部分”或“外结构域”是指朝向细胞的胞外空间并且优选地从所述细胞的外部接近(例如通过位于细胞外部的结合分子,例如抗体)的分子(例如,蛋白质)的部分。优选地,该术语是指一个或更多个胞外环或结构域或者其片段。
[0291]
术语“表位”是指分子(例如抗原)被免疫系统识别的部分或片段。例如,表位可以被t细胞、b细胞或抗体识别。抗原的表位可包含抗原的连续或不连续部分,并且长度可为约5至约100,例如约5至约50,更优选约8至约30,最优选约10至约25个氨基酸,例如,表位的长度可优选为9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或25个氨基酸。在一个实施方案中,表位的长度为约10至约25个氨基酸。术语“表位”包含t细胞表位。
[0292]
术语“t细胞表位”是指当在mhc分子的情况下存在时被t细胞识别的蛋白质的部分或片段。术语“主要组织相容性复合体”和缩写“mhc”包括i类mhc和ii类mhc分子,并且涉及存在于所有脊椎动物中的基因复合体。mhc蛋白或分子对于免疫反应中淋巴细胞与抗原呈
递细胞或病变细胞之间的信号传导是重要的,其中mhc蛋白或分子结合肽表位并呈递它们以被t细胞上的t细胞受体识别。由mhc编码的蛋白质在细胞表面上表达,并将自身抗原(来自细胞本身的肽片段)和非自身抗原(例如,侵入的微生物的片段)二者展示给t细胞。在i类mhc/肽复合体的情况下,结合肽通常长约8至约10个氨基酸,尽管更长或更短的肽可以是有效的。在ii类mhc/肽复合体的情况下,结合肽通常长约10至约25个氨基酸,并且特别地长约13至约18个氨基酸,尽管更长或更短的肽可以是有效的。
[0293]
在一个实施方案中,靶抗原是肿瘤抗原,并且疫苗抗原或其片段(例如,表位)来源于肿瘤抗原。肿瘤抗原可以是“标准”抗原,通常已知其在多种癌症中表达。肿瘤抗原也可以是“新抗原”,其对个体的肿瘤具有特异性,并且先前未被免疫系统识别。新抗原或新表位可以是由癌细胞基因组中导致氨基酸变化的一种或更多种癌症特异性突变导致的。如果肿瘤抗原是新抗原,则疫苗抗原优选包含含有一个或更多个氨基酸变化的所述新抗原的表位或片段。
[0294]
癌症突变因个体而异。因此,编码的新的表位(新表位)的癌症突变在疫苗组合物和免疫治疗的开发中代表有吸引力的靶标。肿瘤免疫治疗的效力取决于能够在宿主内诱导强效免疫应答的癌症特异性抗原和表位的选择。rna可用于将患者特异性肿瘤表位递送至患者。存在于脾中的树突细胞(dc)代表对免疫原性表位或抗原(例如肿瘤表位)的rna表达特别感兴趣的抗原呈递细胞。已示出多种表位的使用促进肿瘤疫苗组合物中的治疗效力。肿瘤突变组的快速测序可为个体化疫苗提供多个表位,其可由本文中所述的rna编码,例如作为单一多肽,在其中表位任选地被接头分开。在本公开内容的某些实施方案中,rna编码至少一个表位、至少两个表位、至少三个表位、至少四个表位、至少五个表位、至少六个表位、至少七个表位、至少八个表位、至少九个表位或至少十个表位。一些示例性的实施方案包括编码至少五个表位(称为“五表位(pentatope)”)的rna和编码至少十个表位(称为“十表位(decatope)”)的rna。
[0295]
根据本发明的多个方面,目的优选是提供针对表达肿瘤抗原的癌细胞的免疫应答,以及治疗涉及表达肿瘤抗原的细胞的癌症疾病。在一个实施方案中,本发明涉及施用靶向表达肿瘤抗原的癌细胞的、抗原受体改造的免疫效应细胞,例如t细胞。
[0296]
肽和蛋白质抗原的长度可以为2至100个氨基酸,包括例如5个氨基酸、10个氨基酸、15个氨基酸、20个氨基酸、25个氨基酸、30个氨基酸、35个氨基酸、40个氨基酸、45个氨基酸或50个氨基酸。在一些实施方案中,肽可大于50个氨基酸。在一些实施方案中,肽可大于100个氨基酸。
[0297]
根据本发明,疫苗抗原应可被免疫效应细胞识别。优选地,抗原如果被免疫效应细胞识别,则该抗原能够在存在适当的共刺激信号的情况下诱导携带识别该抗原的抗原受体的免疫效应细胞的刺激、引发和/或扩增。在本发明一些实施方案的情况下,抗原优选存在于细胞表面上,优选抗原呈递细胞的表面上。病变细胞表面上的抗原的识别可导致针对该抗原(或表达该抗原的细胞)的免疫反应。
[0298]
在本发明所有方面的一个实施方案中,抗原在病变细胞(例如癌细胞)中表达。在一个实施方案中,抗原在病变细胞(例如癌细胞)的表面上表达。在一个实施方案中,抗原受体是与抗原的胞外结构域或胞外结构域中的表位结合的car。在一个实施方案中,car与存在于活细胞表面上的抗原的天然表位结合。在一个实施方案中,当由t细胞表达和/或存在
于t细胞上时,car与存在于细胞(例如抗原呈递细胞)上的抗原的结合导致所述t细胞的刺激、引发和/或扩增。在一个实施方案中,当由t细胞表达和/或存在于t细胞上时,car与存在于病变细胞(例如癌细胞)上的抗原的结合导致病变细胞的细胞裂解和/或凋亡,其中所述t细胞优选释放细胞毒性因子,例如穿孔素和颗粒酶。
[0299]
免疫检查点抑制剂
[0300]
在某些实施方案中,免疫检查点抑制剂与本文中所述的其他治疗剂组合使用。
[0301]
本文中使用的“免疫检查点”是指调节抗原的t细胞受体识别的幅度和质量的共刺激和抑制性信号。在某些实施方案中,免疫检查点是抑制性信号。在某些实施方案中,抑制性信号是pd
‑
1与pd
‑
l1之间的相互作用。在某些实施方案中,抑制性信号是ctla
‑
4与cd80或cd86之间的相互作用以取代cd28结合。在某些实施方案中,抑制性信号是lag3与ii类mhc分子之间的相互作用。在某些实施方案中,抑制性信号是tim3与半乳糖凝集素9之间的相互作用。
[0302]
本文中使用的“免疫检查点抑制剂”是指完全或部分降低、抑制、干扰或调节一种或更多种检查点蛋白质的分子。在某些实施方案中,免疫检查点抑制剂阻止与免疫检查点相关的抑制性信号。在某些实施方案中,免疫检查点抑制剂是破坏与免疫检查点相关的抑制性信号传导的抗体或其片段。在某些实施方案中,免疫检查点抑制剂是破坏抑制性信号传导的小分子。在某些实施方案中,免疫检查点抑制剂是阻止检查点阻断剂蛋白质之间的相互作用的抗体、其片段或抗体模拟物,例如,阻止pd
‑
1与pd
‑
l1之间的相互作用的抗体或其片段。在某些实施方案中,免疫检查点抑制剂是阻止ctla
‑
4与cd80或cd86之间的相互作用的抗体或其片段。在某些实施方案中,免疫检查点抑制剂是阻止lag3与其配体或tim
‑
3与其配体之间的相互作用的抗体或其片段。检查点抑制剂也可以以分子(或其变体)自身的可溶性形式的形式,例如可溶性pd
‑
l1或pd
‑
l1融合物。
[0303]“程序性死亡
‑
1(programmed death
‑
1,pd
‑
1)”受体是指属于cd28家族的免疫抑制性受体。pd
‑
1主要在体内先前活化的t细胞上表达,并且与两种配体(pd
‑
l1和pd
‑
l2)结合。本文中使用的术语“pd
‑
1”包含人pd
‑
1(hpd
‑
1)、hpd
‑
1的变体、同种型和物种同源物,以及与hpd
‑
1具有至少一个共同表位的类似物。
[0304]“程序性死亡配体
‑
1(programmed death ligand
‑
1,pd
‑
l1)”是pd
‑
1(另一个是pd
‑
l2)的两个细胞表面糖蛋白配体之一,其与pd
‑
1结合时下调t细胞活化和细胞因子分泌。本文中使用的术语“pd
‑
l1”包含人pd
‑
l1(hpd
‑
l1)、hpd
‑
l1的变体、同种型和物种同源物,以及与hpd
‑
l1具有至少一个共同表位的类似物。
[0305]“细胞毒性t淋巴细胞相关抗原
‑
4(ctla
‑
4)”是t细胞表面分子并且是免疫球蛋白超家族的成员。该蛋白质通过与cd80和cd86结合而下调免疫系统。本文中使用的术语“ctla
‑
4”包含人ctla
‑
4(hctla
‑
4)、hctla
‑
4的变体、同种型和物种同源物,以及与hctla
‑
4具有至少一个共同表位的类似物。
[0306]“淋巴细胞活化基因3(lymphocyte activation gene
‑
3,lag3)”是通过与ii类mhc分子结合而与淋巴细胞活性的抑制相关的抑制性受体。该受体增强treg细胞的功能并抑制cd8
效应t细胞功能。本文中使用的术语“lag3”包含人lag3(hlag3)、hlag3的变体、同种型和物种同源物,以及具有至少一个共同表位的类似物。
[0307]“t细胞膜蛋白
‑
3(tim3)”是通过抑制th1细胞应答而参与淋巴细胞活性的抑制的
抑制性受体。其配体是在多种类型的癌症中均被上调的半乳糖凝集素9。本文中使用的术语“tim3”包含人tim3(htim3)、htim3的变体、同种型和物种同源物,以及具有至少一个共同表位的类似物。
[0308]“b7家族”是指具有未定义受体的抑制性配体。b7家族涵盖b7
‑
h3和b7
‑
h4,二者在肿瘤细胞和肿瘤浸润细胞上均上调。
[0309]
在某些实施方案中,适用于本文所公开的方法的免疫检查点抑制剂是抑制性信号的拮抗剂,例如靶向例如pd
‑
1、pd
‑
l1、ctla
‑
4、lag3、b7
‑
h3、b7
‑
h4或tim3的抗体。这些配体和受体在pardoll,d.,nature.12:252
‑
264,2012中综述。
[0310]
在某些实施方案中,免疫检查点抑制剂是破坏或抑制来自抑制性免疫调节剂的信号传导的抗体或其抗原结合部分。在某些实施方案中,免疫检查点抑制剂是破坏或抑制来自抑制性免疫调节剂的信号传导的小分子。
[0311]
在某些实施方案中,抑制性免疫调节剂是pd
‑
1/pd
‑
l1信号传导途径的组分。因此,本公开内容的某些实施方案提供了向对象施用破坏pd
‑
1受体与其配体pd
‑
l1之间的相互作用的抗体或其抗原结合部分。与pd
‑
1结合并破坏pd
‑
1与其配体pd
‑
l1之间的相互作用的抗体是本领域中已知的。在某些实施方案中,抗体或其抗原结合部分与pd
‑
1特异性结合。在某些实施方案中,抗体或其抗原结合部分与pd
‑
l1特异性结合并抑制其与pd
‑
1的相互作用,从而提高免疫活性。
[0312]
在某些实施方案中,抑制性免疫调节剂是ctla4信号传导途径的组分。因此,本公开内容的某些实施方案提供了向对象施用靶向ctla4并破坏其与cd80和cd86的相互作用的抗体或其抗原结合部分。
[0313]
在某些实施方案中,抑制性免疫调节剂是lag3(淋巴细胞活化基因3)信号传导途径的组分。因此,本公开内容的某些实施方案提供了向对象施用靶向lag3并破坏其与ii类mhc分子的相互作用的抗体或其抗原结合部分。
[0314]
在某些实施方案中,抑制性免疫调节剂是b7家族信号传导途径的组分。在某些实施方案中,b7家族成员是b7
‑
h3和b7
‑
h4。因此,本公开内容的某些实施方案提供了向对象施用靶向b7
‑
h3或h4的抗体或其抗原结合部分。b7家族没有任何定义的受体,但是这些配体在肿瘤细胞或肿瘤浸润细胞上均被上调。临床前小鼠模型已示出这些配体的阻断可增强抗肿瘤免疫。
[0315]
在某些实施方案中,抑制性免疫调节剂是tim3(t细胞膜蛋白3)信号传导途径的组分。因此,本公开内容的某些实施方案提供了向对象施用靶向tim3并破坏其与半乳糖凝集素9的相互作用的抗体或其抗原结合部分。
[0316]
本领域普通技术人员将理解,其他免疫检查点靶标也可被拮抗剂或抗体靶向,前提是这种靶向导致刺激免疫应答,例如抗肿瘤免疫应答,如反映在例如,t细胞增殖的提高、t细胞活化的增强和/或细胞因子(例如,ifn
‑
γ、il2)产生的提高。
[0317]
rna靶向
[0318]
根据本发明,特别优选的是,本文中所述的肽、蛋白质或多肽,特别是il2多肽、ifn多肽和/或疫苗抗原,以编码本文中所述的肽、蛋白质或多肽的rna的形式施用。在一个实施方案中,不同的本文中所述的肽、蛋白质或多肽由不同的rna分子编码。
[0319]
在一个实施方案中,rna在递送载剂中配制。在一个实施方案中,递送载剂包含颗
粒。在一个实施方案中,递送载剂包含至少一种脂质。在一个实施方案中,所述至少一种脂质包含至少一种阳离子脂质。在一个实施方案中,脂质与rna形成复合体和/或包封rna。在一个实施方案中,脂质包含在包封rna的囊泡中。在一个实施方案中,rna在脂质体中配制。
[0320]
根据本公开内容,在施用本文中所述的rna之后,至少一部分rna被递送至靶细胞。在一个实施方案中,至少一部分rna被递送至靶细胞的胞质溶胶。在一个实施方案中,rna被靶细胞翻译以产生所编码的肽或蛋白质。
[0321]
本公开内容的一些方面涉及靶向递送本文中所公开的rna(例如编码il2多肽的rna、编码ifn多肽的rna和/或编码疫苗抗原的rna)。
[0322]
在一个实施方案中,本公开内容涉及靶向淋巴系统,特别是次级淋巴器官,更特别地是脾。如果施用的rna是编码疫苗抗原的rna,则特别优选靶向淋巴系统,特别是次级淋巴器官,更特别地是脾。
[0323]
在一个实施方案中,靶细胞是脾细胞。在一个实施方案中,靶细胞是抗原呈递细胞,例如脾中的专职性抗原呈递细胞。在一个实施方案中,靶细胞是脾中的树突细胞。
[0324]“淋巴系统”是循环系统的一部分并且是免疫系统的重要部分,包含运送淋巴的淋巴管网络。淋巴系统由淋巴器官、淋巴管的传导网络和循环淋巴组成。原发性或中央淋巴器官从未成熟的祖细胞产生淋巴细胞。胸腺和骨髓构成原发性淋巴器官。次级或外周淋巴器官(包括淋巴结和脾)维持成熟的初始淋巴细胞并启动适应性免疫应答。
[0325]
rna可通过所谓的脂质复合体制剂递送至脾,其中rna与包含阳离子脂质和任选地另外的或辅助脂质(helper lipid)的脂质体结合以形成可注射的纳米粒制剂。脂质体可通过将脂质在乙醇中的溶液注入到水或合适的水相中而获得。rna脂质复合体颗粒可通过将脂质体与rna混合来制备。靶向rna脂质复合体颗粒的脾在wo 2013/143683中描述,其通过引用并入本文。已发现具有净负电荷的rna脂质复合体颗粒可用于优先靶向脾组织或脾细胞,例如抗原呈递细胞,特别是树突细胞。因此,在施用rna脂质复合体颗粒之后,在脾中发生rna积聚和/或rna表达。因此,本公开内容的rna脂质复合体颗粒可用于在脾中表达rna。在一个实施方案中,在施用rna脂质复合体颗粒之后,在肺和/或肝中没有或基本上没有rna积聚和/或rna表达发生。在一个实施方案中,在施用rna脂质复合体颗粒之后,在脾中在抗原呈递细胞(例如专职性抗原呈递细胞)中发生rna积聚和/或rna表达。因此,本公开内容的rna脂质复合体颗粒可用于在这样的抗原呈递细胞中表达rna。在一个实施方案中,抗原呈递细胞是树突细胞和/或巨噬细胞。
[0326]
在本公开内容的上下文中,术语“rna脂质复合体颗粒”涉及包含脂质(特别是阳离子脂质)和rna的颗粒。带正电荷的脂质体和带负电荷的rna之间的静电相互作用导致rna脂质复合体颗粒的络合和自发形成。带正电荷的脂质体通常可使用阳离子脂质(例如dotma)和另外的脂质(例如dope)合成。在一个实施方案中,rna脂质复合体颗粒是纳米粒。
[0327]
本文中使用的“阳离子脂质”是指具有净正电荷的脂质。阳离子脂质结合带负电荷的rna,通过与脂质基质的静电相互作用。通常来说,阳离子脂质具有亲脂性部分,例如甾醇、酰基或二酰基链,并且脂质的头基通常携带正电荷。阳离子脂质的一些实例包括但不限于:1,2
‑
二
‑
o
‑
十八碳烯基
‑3‑
三甲基铵丙烷(dotma)、二甲基双二十八烷基铵(ddab)、1,2
‑
二油酰基
‑3‑
三甲基铵丙烷(dotap)、1,2
‑
二油酰基
‑3‑
二甲基铵丙烷(dodap)、1,2
‑
二酰氧基
‑3‑
二甲基铵丙烷、1,2
‑
二烷氧基
‑3‑
二甲基铵丙烷、双十八烷基二甲基氯化铵(dodac)、
2,3
‑
二(十四烷氧基)丙基
‑
(2
‑
羟乙基)
‑
二甲基铵(dmrie)、1,2
‑
二豆蔻酰基
‑
sn
‑
甘油基
‑3‑
乙基磷酸胆碱(dmepc)、1,2
‑
二豆蔻酰基
‑3‑
三甲基铵丙烷(dmtap)、1,2
‑
二油氧基丙基
‑3‑
二甲基
‑
羟乙基溴化铵(dorie)、和2,3
‑
二油酰氧基
‑
n
‑
[2(精胺甲酰胺)乙基]
‑
n,n
‑
二甲基
‑1‑
三氟乙酸丙铵(dospa)。优选的是dotma、dotap、dodac和dospa。在一些具体实施方案中,阳离子脂质是dotma和/或dotap。
[0328]
可并入另外的脂质以调整总的正负电荷比和rna脂质复合体颗粒的物理稳定性。在某些实施方案中,所述另外的脂质是中性脂质。本文中使用的“中性脂质”是指净电荷为零的脂质。中性脂质的一些实例包括但不限于1,2
‑
二
‑
(9z
‑
十八烯酰基)
‑
sn
‑
甘油基
‑3‑
磷酸乙醇胺(dope)、1,2
‑
二油酰基
‑
sn
‑
甘油基
‑3‑
磷酸胆碱(dopc)、二酰基磷脂酰胆碱、二酰基磷脂酰乙醇胺、神经酰胺、鞘磷脂、脑磷脂、胆固醇和脑苷脂。在一些具体实施方案中,另外的脂质是dope、胆固醇和/或dopc。
[0329]
在某些实施方案中,rna脂质复合体颗粒包含阳离子脂质和另外的脂质二者。在一个示例性实施方案中,阳离子脂质是dotma,并且另外的脂质是dope。
[0330]
在一些实施方案中,至少一种阳离子脂质与至少一种另外的脂质的摩尔比为约10:0至约1:9、约4:1至约1:2、或约3:1至约1:1。在一些具体实施方案中,摩尔比可以为约3:1、约2.75:1、约2.5:1、约2.25:1、约2:1、约1.75:1、约1.5:1、约1.25:1、或约1:1。在一个示例性实施方案中,至少一种阳离子脂质与至少一种另外的脂质的摩尔比为约2:1。
[0331]
在一个实施方案中,本文中所述的rna脂质复合体颗粒的平均直径为约200nm至约1000nm、约200nm至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm、或约350nm至约400nm。在一些具体实施方案中,rna脂质复合体颗粒的平均直径为约200nm、约225nm、约250nm、约275nm、约300nm、约325nm、约350nm、约375nm、约400nm、约425nm、约450nm、约475nm、约500nm、约525nm、约550nm、约575nm、约600nm、约625nm、约650nm、约700nm、约725nm、约750nm、约775nm、约800nm、约825nm、约850nm、约875nm、约900nm、约925nm、约950nm、约975nm、或约1000nm。在一个实施方案中,rna脂质复合体颗粒的平均直径为约250nm至约700nm。在另一个实施方案中,rna脂质复合体颗粒的平均直径为约300nm至约500nm。在一个示例性实施方案中,rna脂质复合体颗粒的平均直径为约400nm。
[0332]
本公开内容的rna脂质复合体颗粒的电荷是至少一种阳离子脂质中存在的电荷与rna中存在的电荷的总和。电荷比是至少一种阳离子脂质中存在的正电荷与rna中存在的负电荷的比。至少一种阳离子脂质中存在的正电荷与rna中存在的负电荷的电荷比通过以下方程来计算:电荷比=[(阳离子脂质浓度(mol))*(阳离子脂质中正电荷总数)]/[(rna浓度(mol))*(rna中负电荷总数)]。
[0333]
本文中所述的靶向脾的rna脂质复合体颗粒在生理ph下优选具有净负电荷,例如正电荷与负电荷的电荷比为约1.9:2至约1:2。在一些具体实施方案中,在生理ph下rna脂质复合体颗粒中正电荷与负电荷的电荷比为约1.9:2.0、约1.8:2.0、约1.7:2.0、约1.6:2.0、约1.5:2.0、约1.4:2.0、约1.3:2.0、约1.2:2.0、约1.1:2.0或约1:2.0。
[0334]
细胞因子,例如pk延长的细胞因子,特别是pk延长的白介素,例如本文中所述的那些,可通过以下来提供给对象:向对象施用在制剂中的编码细胞因子的rna,用于将rna优先递送至肝或肝组织。优选将rna递送至这样的靶器官或靶组织,特别是如果期望表达大量细胞因子和/或如果期望或需要细胞因子全身性存在,特别是大量存在。
[0335]
rna递送系统对肝具有固有的偏好。这涉及基于脂质的颗粒、阳离子和中性纳米粒,特别是生物缀合物中的脂质纳米粒,例如脂质体、纳米胶束和亲脂性配体。肝积聚是由肝血管系统或脂质代谢(脂质体和脂质或胆固醇缀合物)的不连续性质引起的。
[0336]
为了在体内将rna递送至肝,可使用药物递送系统通过防止其降解将rna运送到肝中。例如,由聚(乙二醇)(peg)包被的表面和包含mrna的核心组成的复合纳米胶束是有用的系统,因为纳米胶束在生理条件下提供了优异的体内rna稳定性。此外,由密集的peg栅栏构成的复合纳米胶束表面所提供的隐身特性有效地规避了宿主免疫防御。
[0337]
药物组合物
[0338]
本文中所述的药剂可以以药物组合物或药物施用,并且可以以任何合适的药物组合物的形式施用。
[0339]
在本发明所有方面的一个实施方案中,在一起或彼此分开的本文中所述的组分,例如编码细胞因子(il2或ifn)的核酸或编码抗原的核酸,可以以药物组合物施用,该药物组合物可包含可药用载体且可任选地包含一种或更多种佐剂、稳定剂等。在一个实施方案中,药物组合物用于治疗性或预防性治疗,例如用于治疗或预防涉及抗原的疾病,例如癌症疾病,例如本文中所述的那些。
[0340]
术语“药物组合物”涉及包含治疗有效剂,优选与可药用载体、稀释剂和/或赋形剂一起的治疗有效剂的制剂。通过将所述药物组合物施用于对象,所述药物组合物可用于治疗、预防或者减轻疾病或病症的严重程度。药物组合物在本领域中也称为药物制剂。
[0341]
本公开内容的药物组合物可包含一种或更多种佐剂或可与一种或更多种佐剂一起施用。术语“佐剂”涉及延长、增强或加速免疫应答的化合物。佐剂包括化合物例如油乳剂(例如,弗氏佐剂(freund’s adjuvant))、矿物质化合物(例如明矾)、细菌产品(例如百日咳鲍特菌毒素)或免疫刺激复合物的非均质组。佐剂的一些实例包括但不限于:lps、gp96、cpg寡脱氧核苷酸、生长因子和细胞因子,例如单核因子、淋巴因子、白介素、趋化因子。细胞因子可以是il1、il2、il3、il4、il5、il6、il7、il8、il9、il10、il12、ifnα、ifnγ、gm
‑
csf、lt
‑
a。另一些已知的佐剂是氢氧化铝、弗氏佐剂或油类,例如isa51。用于本公开内容的另一些合适的佐剂包括脂肽,例如pam3cys。
[0342]
根据本公开内容的药物组合物通常以“药学有效量”和“可药用制剂”施加。
[0343]
术语“可药用的”是指不与药物组合物的活性组分的作用相互作用的物质的无毒性。
[0344]
术语“药学有效量”或“治疗有效量”是指单独或与另外的剂量一起实现期望的反应或期望的效果的量。在治疗特定疾病的情况下,期望的反应优选地涉及对疾病进程的抑制。这包括减缓疾病的进展,并且特别是中断或逆转疾病的进展。疾病治疗中的期望反应还可以是延迟所述疾病或所述病症的发生或预防其发生。本文中所述的组合物的有效量将取决于:待治疗的病症,疾病的严重程度,患者的个体参数包括年龄、生理状况、身材大小和体重,治疗持续时间,伴随治疗(如果存在的话)的类型,具体施用途径以及类似因素。因此,本文中所述的组合物的施用剂量可取决于多种这样的参数。在采用初始剂量患者的反应不足的情况下,可使用更高的剂量(或通过不同的、更局部的施用途径实现有效地更高的剂量)。
[0345]
本公开内容的药物组合物可包含盐、缓冲剂、防腐剂和任选地其他治疗剂。在一个实施方案中,本公开内容的药物组合物包含一种或更多种可药用载体、稀释剂和/或赋形
剂。
[0346]
用于本公开内容的药物组合物中的合适的防腐剂包括但不限于:苯扎氯铵、氯丁醇、对羟基苯甲酸酯和硫柳汞。
[0347]
本文中使用的术语“赋形剂”是指可存在于本公开内容的药物组合物中但不是活性成分的物质。赋形剂的一些实例包括但不限于:载体、黏合剂、稀释剂、润滑剂、增稠剂、表面活性剂、防腐剂、稳定剂、乳化剂、缓冲剂、矫味剂或着色剂。
[0348]
术语“稀释剂”涉及稀释剂(diluting agent)和/或冲淡剂(thinning agent)。此外,术语“稀释剂”包括流体、液体或固体混悬剂和/或混合介质中的任何一种或更多种。合适的稀释剂的一些实例包括乙醇、甘油和水。
[0349]
术语“载体”是指可以是天然的、合成的、有机的、无机的组分,在其中将活性组分组合以促进、增强或实现药物组合物的施用。本文中使用的载体可以是适合于施用于对象的一种或更多种相容的固体或液体填充剂、稀释剂或包封物质。合适的载体包括但不限于:无菌水、林格液(ringer)、乳酸林格液、无菌氯化钠溶液、等张盐水、聚亚烷基二醇、氢化萘以及特别是生物相容性丙交酯聚合物、丙交酯/乙交酯共聚物或聚氧乙烯/聚氧丙烯共聚物。在一个实施方案中,本公开内容的药物组合物包含等张盐水。
[0350]
用于治疗用途的可药用载体、赋形剂或稀释剂在药学领域中是公知的,并且描述于例如remington’s pharmaceutical sciences,mack publishing co.(a.r gennaro edit.1985)中。
[0351]
可根据预期的施用途径和标准药物实践来选择药用载体、赋形剂或稀释剂。
[0352]
在一个实施方案中,本文中所述的药物组合物可静脉内、动脉内、皮下、皮内或肌内施用。在某些实施方案中,将药物组合物配制成用于局部施用或全身性施用。全身性施用可包括涉及通过胃肠道吸收的肠施用,或肠胃外施用。本文中使用的“肠胃外施用”是指以除通过胃肠道之外的任何方式的施用,例如通过静脉内注射。在一个优选实施方案中,将药物组合物配制成用于全身性施用。在另一个优选实施方案中,全身性施用是通过静脉内施用。在本发明所有方面的一个实施方案中,全身性施用编码本文中所述的细胞因子的rna和任选地编码抗原的rna。
[0353]
本文中使用的术语“共施用”意指其中将不同的化合物或组合物(例如,编码il2多肽的rna、编码ifn多肽的rna和任选地编码疫苗抗原的rna)施用于同一患者的过程。不同的化合物或组合物可同时、基本上同时或依次施用。在一个实施方案中,首先施用il2多肽或编码il2多肽的核酸,然后施用ifn多肽或编码ifn多肽的核酸。
[0354]
治疗
[0355]
本文中所述的药剂、组合物和方法可用于治疗患有疾病(例如,以存在表达抗原的病变细胞为特征的疾病)的对象。特别优选的疾病为癌症疾病。例如,如果抗原来源于病毒,则所述药剂、组合物和方法可用于治疗由所述病毒引起的病毒性疾病。如果抗原是肿瘤抗原,则所述药剂、组合物和方法可用于治疗癌症疾病,其中癌细胞表达所述肿瘤抗原。
[0356]
术语“疾病”是指影响个体身体的异常状况。疾病通常被解释为与特定症状和体征相关的医学病症。疾病可由最初来自外部来源的因素引起,例如感染性疾病,或者疾病可由内部功能障碍引起,例如自身免疫病。在人中,“疾病”通常被更广泛地用于是指引起患病个体的疼痛、功能障碍、痛苦、社会问题或死亡或者与该个体有关的那些的类似问题的任何病
症。在此更广泛的意义上,疾病有时包括损伤、失能、障碍、综合征、感染、孤立症状、异常行为以及结构和功能的非典型变化,而在另一些情况下和出于另一些目的,这些可被视为可区分的类别。疾病通常不仅在身体上而且在情感上影响个体,因为对许多疾病的感染和经历可改变个体对生活的看法和个体的性格。
[0357]
在本发明背景下,术语“治疗”或“治疗性干预”涉及出于对抗病症例如疾病或障碍目的的对对象的管理和护理。该术语旨在包括针对对象所遭受的给定病症的全谱治疗,例如施用治疗有效的化合物以减轻症状或并发症,延缓疾病、障碍或病症的进展,减轻或缓解症状和并发症,和/或治愈或消除疾病、障碍或病症以及预防病症,其中预防应理解为出于对抗疾病、病症或障碍目的的对个体的管理和护理,并且包括施用活性化合物以预防症状或并发症的发作。
[0358]
术语“治疗性治疗”涉及改善健康状况和/或延长(提高)个体寿命的任何治疗。所述治疗可在个体中消除疾病、在个体中阻止或减缓疾病的发生、在个体中抑制或减缓疾病的发生,在个体中降低症状的频率或严重程度,和/或在目前患有或以前曾患有疾病的个体中降低复发。
[0359]
术语“预防性治疗”或“防止性治疗”涉及旨在防止疾病在个体中发生的任何治疗。术语“预防性治疗”或“防止性治疗”在本文中可互换使用。
[0360]
术语“个体”和“对象”在本文中可互换使用。它们是指可受疾病或病症(例如,癌症)折磨或易于患有疾病或病症(例如,癌症)但是可患有或可未患有疾病或病症的人或其他哺乳动物(例如小鼠、大鼠、兔、犬、猫、牛、猪、绵羊、马或灵长类)。在许多实施方案中,个体是人。除非另有说明,否则术语“个体”和“对象”不表示特定年龄,并且因此涵盖成年人、老年人、儿童和新生儿。在本公开内容的一些实施方案中,“个体”或“对象”是“患者”。
[0361]
术语“患者”意指治疗的个体或对象,特别是患病的个体或对象。
[0362]
在本公开内容的一个实施方案中,目的是提供针对表达抗原的病变细胞(例如表达肿瘤抗原的癌细胞)的免疫应答,并且治疗涉及表达抗原例如肿瘤抗原的细胞的疾病例如癌症疾病。
[0363]
本文中使用的“免疫应答”是指对抗原或表达抗原的细胞的整合的身体应答,并且是指细胞免疫应答和/或体液免疫应答。
[0364]“细胞介导的免疫”、“细胞免疫”、“细胞免疫应答”或类似术语意在包括针对以表达抗原为特征,特别是以用i类或ii类mhc呈递抗原为特征的细胞的细胞应答。细胞应答与称为t细胞或t淋巴细胞的细胞有关,这些细胞充当“辅助”或“杀伤”。辅助t细胞(也称为cd4
t细胞)通过调节免疫应答发挥中心作用,并且杀伤细胞(也称为细胞毒性t细胞、细胞裂解t细胞、cd8
t细胞或ctl)杀伤病变细胞,例如癌细胞,从而阻止更多病变细胞的产生。
[0365]
本公开内容考虑了可以是保护性、防止性、预防性和/或治疗性的免疫应答。本文中使用的“诱导免疫应答”可指示在诱导之前不存在针对特定抗原的免疫应答,或者可指示在诱导之前存在针对特定抗原的基础水平的免疫应答,其在诱导之后增强。因此,“诱导免疫应答”包括“增强免疫应答”。
[0366]
术语“免疫治疗”涉及通过诱导或增强免疫应答来治疗疾病或病症。术语“免疫治疗”包括抗原免疫接种或抗原疫苗接种。
[0367]
术语“免疫接种”或“疫苗接种”描述了以诱导免疫应答为目的例如出于治疗性或
预防性的原因而向个体施用抗原的过程。
[0368]
术语“巨噬细胞”是指通过单核细胞的分化产生的吞噬细胞的亚组。被炎症、免疫细胞因子或微生物产物活化的巨噬细胞在巨噬细胞内通过水解和氧化攻击非特异性地吞噬并杀伤外来病原体,从而导致病原体的降解。来自降解的蛋白质的肽显示在巨噬细胞表面上,在这里其可被t细胞识别,并且其可直接与b细胞表面上的抗体相互作用,从而导致t细胞和b细胞活化并进一步刺激免疫应答。巨噬细胞属于抗原呈递细胞的类别。在一个实施方案中,巨噬细胞是脾巨噬细胞。
[0369]
术语“树突细胞”(dc)是指吞噬细胞的另一亚型,其属于抗原呈递细胞的类别。在一个实施方案中,树突细胞来源于造血骨髓祖细胞。这些祖细胞最初转化为未成熟的树突细胞。这些未成熟细胞的特征在于高吞噬活性和低t细胞活化潜能。未成熟的树突细胞不断采样周围环境中的病原体,例如病毒和细菌。一旦其与可呈递的抗原接触,其就被活化成为成熟的树突细胞,并且开始迁移至脾或淋巴结。未成熟的树突细胞吞噬病原体并将其蛋白质降解为小块(piece),并且在成熟之后,这些片段使用mhc分子呈现在其细胞表面处。同时,其上调了在t细胞活化中充当共受体的细胞表面受体,例如cd80、cd86和cd40,极大地增强了其活化t细胞的能力。其还上调了ccr7,所述ccr7是诱导树突细胞穿过血流到达脾,或穿过淋巴系统到达淋巴结的趋化性受体。在此其充当抗原呈递细胞,并通过与非抗原特异性共刺激信号一起呈递其抗原来活化辅助t细胞和杀伤t细胞以及b细胞。因此,树突细胞可主动诱导t细胞或b细胞相关的免疫应答。在一个实施方案中,树突细胞是脾树突细胞。
[0370]
术语“抗原呈递细胞”(apc)是能够在其细胞表面上(或在其表面处)展示、获得和/或呈递至少一种抗原或抗原性片段的多种细胞中的细胞。抗原呈递细胞可以区分为专职性抗原呈递细胞和非专职性抗原呈递细胞。
[0371]
术语“专职性抗原呈递细胞”涉及组成性表达与初始t细胞相互作用所需的主要组织相容性复合体ii类(ii类mhc)分子的抗原呈递细胞。如果t细胞与抗原呈递细胞膜上的ii类mhc分子复合体相互作用,则抗原呈递细胞产生诱导t细胞活化的共刺激分子。专职性抗原呈递细胞包括树突细胞和巨噬细胞。
[0372]
术语“非专职性抗原呈递细胞”是指不组成性表达ii类mhc分子,但是在受到某些细胞因子例如干扰素
‑
γ刺激之后组成性表达ii类mhc分子的抗原呈递细胞。一些示例性的非专职性抗原呈递细胞包括成纤维细胞、胸腺上皮细胞、甲状腺上皮细胞、胶质细胞、胰腺β细胞或血管内皮细胞。
[0373]“抗原加工”是指抗原降解为加工产物,其是所述抗原的片段(例如,蛋白质降解为肽),并且是指这些片段中的一个或更多个与mhc分子的缔合(例如,通过结合)用于由细胞例如抗原呈递细胞呈递到特定的t细胞。
[0374]
术语“涉及抗原的疾病”是指与抗原相关的任何疾病,例如以抗原的存在为特征的疾病。涉及抗原的疾病可以是感染性疾病、或癌症疾病或仅是癌症。如上所述,抗原可以是疾病相关抗原,例如肿瘤相关抗原、病毒抗原或细菌抗原。在一个实施方案中,涉及抗原的疾病是涉及优选在细胞表面上表达抗原的细胞的疾病。
[0375]
术语“感染性疾病”是指可在个体之间或生物体之间传播并且由微生物原(microbial agent)引起的任何疾病(例如,普通感冒)。感染性疾病是本领域中已知的,并且包括例如病毒性疾病、细菌性疾病或寄生物性疾病,这些疾病分别由病毒、细菌和寄生物
引起。在这方面中,感染性疾病可以是例如肝炎、性传播疾病(例如衣原体或淋病)、结核病、hiv/获得性免疫缺陷综合征(acquired immune deficiency syndrome,aids)、白喉、乙型肝炎、丙型肝炎、霍乱、严重急性呼吸综合征(severe acute respiratory syndrome,sars)、禽流感和流感。
[0376]
术语“癌症疾病”或“癌症”是指或描述个体中通常以不受调节的细胞生长为特征的生理状况。癌症的一些实例包括但不限于:上皮癌(carcinoma)、淋巴瘤、母细胞瘤、肉瘤和白血病。更特别地,这样的癌症的一些实例包括骨癌、血癌肺癌、肝癌、胰腺癌、皮肤癌、头颈癌、皮肤或眼内黑素瘤、子宫癌、卵巢癌、直肠癌、肛区癌、胃癌、结肠癌、乳腺癌、前列腺癌、子宫癌、性器官和生殖器官癌、霍奇金病(hodgkin's disease)、食管癌、小肠癌、内分泌系统癌、甲状腺癌、甲状旁腺癌、肾上腺癌、软组织肉瘤、膀胱癌、肾癌、肾细胞癌、肾盂癌、中枢神经系统(central nervous system,cns)赘生物、神经外胚层癌症、脊椎轴肿瘤(spinal axis tumor)、胶质瘤、脑脊膜瘤和垂体腺瘤。根据本公开内容的术语“癌症”还包括癌症转移。
[0377]
由于产生的协同作用,在癌症治疗中的组合策略可以是理想的,其可比单一治疗方法的影响要强得多。在一个实施方案中,药物组合物与免疫治疗剂一起施用。本文中使用的“免疫治疗剂”涉及可参与活化特异性免疫应答和/或免疫效应功能的任何药剂。本公开内容考虑了抗体作为免疫治疗剂的用途。不希望受到理论的束缚,抗体能够通过多种机制实现针对癌细胞的治疗效果,包括诱导凋亡、阻断信号转导途径的组分或抑制肿瘤细胞的增殖。在某些实施方案中,抗体是单克隆抗体。单克隆抗体可通过抗体依赖性细胞介导的细胞毒性(antibody
‑
dependent cell mediated cytotoxicity,adcc)诱导细胞死亡,或结合补体蛋白,导致直接的细胞毒性,称为补体依赖性细胞毒性(complement dependent cytotoxicity,cdc)。可与本公开内容组合使用的抗癌抗体和潜在抗体靶标(在括号里)的一些非限制性实例包括:阿巴伏单抗(ca
‑
125)、阿昔单抗(cd41)、阿达木单抗(epcam)、阿夫土珠单抗(afutuzumab)(cd20)、培化阿珠单抗(alacizumab pegol)(vegfr2)、喷替酸阿妥莫单抗(cea)、阿麦妥昔单抗(amatuximab)(morab
‑
009)、马安那莫单抗(tag
‑
72)、阿泊珠单抗(hla
‑
dr)、阿昔莫单抗(cea)、阿特珠单抗(atezolizumab)(pd
‑
l1)、巴维昔单抗(磷脂酰丝氨酸)、贝妥莫单抗(cd22)、贝利木单抗(baff)、贝伐珠单抗(vegf
‑
a)、莫比伐单抗(bivatuzumab mertansine)(cd44 v6)、博纳吐单抗(blinatumomab)(cd 19)、布妥昔单抗(cd30 tnfrsf8)、莫坎妥珠单抗(黏蛋白canag)、雷坎妥珠单抗(muc1)、卡罗单抗喷地肽(前列腺癌细胞)、卡鲁单抗(carlumab)(cnt0888)、卡妥索单抗(epcam、cd3)、西妥昔单抗(egfr)、泊西他珠单抗(citatuzumab bogatox)(epcam)、西妥木单抗(igf
‑
1受体)、克劳西单抗(claudiximab)(密蛋白)、替坦司可利妥珠单抗(clivatuzumab tetraxetan)(muc1)、西他土珠单抗(trail
‑
r2)、达西珠单抗(cd40)、达罗土珠单抗(dalotuzumab)(胰岛素样生长因子i受体)、地诺单抗(rankl)、地莫单抗(b
‑
淋巴瘤细胞)、多兹图单抗(drozitumab)(dr5)、依美昔单抗(gd3神经节苷脂)、依决洛单抗(epcam)、埃罗妥珠单抗(slamf7)、依那妥珠单抗(pdl192)、恩司昔单抗(ensituximab)(npc
‑
1c)、依帕珠单抗(cd22)、厄妥索单抗(her2/neu、cd3)、伊瑞西珠单抗(整合素ανβ3)、法勒珠单抗(farletuzumab)(叶酸受体1)、fbta05(cd20)、芬克拉妥珠单抗(ficlatuzumab)(sch 900105)、芬妥木单抗(figitumumab)(igf
‑
1受体)、弗拉伏妥单抗(flanvotumab)(糖蛋白75)、夫苏木单抗(fresolimumab)(tgf
‑
β)、加利昔单抗(galiximab)(cd80)、盖尼塔单抗(igf
‑
i)、吉妥单抗奥唑米星(cd33)、吉伏珠单抗(gevokizumab)(iliβ)、吉瑞妥昔单抗(girentuximab)(碳酸酐酶9(ca
‑
ix))、格莱木单抗维多汀(glembatumumab vedotin)(gpnmb)、替伊莫单抗(cd20)、依库单抗(icrucumab)(vegfr
‑
1)、伊戈伏单抗(ca
‑
125)、依坦希单抗(indatuximab ravtansine)(sdc1)、英妥木单抗(intetumumab)(cd51)、奥英妥珠单抗(cd22)、伊匹单抗(cd 152)、伊妥木单抗(iratumumab)(cd30)、拉贝珠单抗(cea)、来沙木单抗(trail
‑
r2)、利韦单抗(乙型肝炎表面抗原)、林妥珠单抗(cd33)、洛妥珠单抗(lorvotuzumab mertansine)(cd56)、鲁卡木单抗(cd40)、鲁昔单抗(cd23)、马帕木单抗(trail
‑
r1)、马妥珠单抗(egfr)、美泊利单抗(il5)、米拉珠单抗(milatuzumab)(cd74)、米妥莫单抗(gd3神经节苷脂)、莫加珠单抗(mogamulizumab)(ccr4)、莫妥莫单抗(moxetumomab pasudotox)(cd22)、他那可单抗(c242抗原)、他那莫单抗(5t4)、纳那妥单抗(namatumab)(ron)、耐昔妥珠单抗(necitumumab)(egfr)、尼妥珠单抗(egfr)、纳武单抗(igg4)、奥法木单抗(cd20)、奥拉单抗(olaratumab)(pdgf
‑
r a)、奥纳珠单抗(onartuzumab)(人分散因子受体激酶)、莫奥珠单抗(oportuzumab monatox)(epcam)、奥戈伏单抗(ca
‑
125)、欧西鲁单抗(oxelumab)(ox
‑
40)、帕尼单抗(egfr)、帕曲妥单抗(patritumab)(her3)、培妥莫单抗(pemtumomab)(muc1)、帕妥珠单抗(her2/neu)、平妥单抗(腺癌抗原)、普托木单抗(波形蛋白)、雷妥莫单抗(racotumomab)(n
‑
羟乙酰神经氨酸)、雷德图单抗(radretumab)(纤连蛋白额外结构域
‑
b)、雷韦单抗(狂犬病病毒糖蛋白)、雷莫芦单抗(vegfr2)、利妥木单抗(rilotumumab)(hgf)、利妥昔单抗(cd20)、罗妥木单抗(robatumumab)(igf
‑
1受体)、沙玛立珠单抗(samalizumab)(cd200)、西罗珠单抗(fap)、司妥昔单抗(il6)、他贝鲁单抗(tabalumab)(baff)、他珠单抗(甲胎蛋白)、帕他普莫单抗(cd 19)、替妥莫单抗(tenatumomab)(生腱蛋白c)、替妥木单抗(teprotumumab)(cd221)、西木单抗(ctla
‑
4)、替加珠单抗(trail
‑
r2)、tnx
‑
650(il13)、托西莫单抗(cd20)、曲妥珠单抗(her2/neu)、trbs07(gd2)、替西木单抗(ctla
‑
4)、西莫白介素图考珠单抗(tucotuzumab celmoleukin)(epcam)、优利妥昔单抗(ublituximab)(ms4a1)、乌瑞鲁单抗(urelumab)(4
‑
1bb)、伏洛昔单抗(整合素α5β1)、伏妥莫单抗(肿瘤抗原ctaa16.88)、扎妥木单抗(egfr)和扎木单抗(cd4)。
[0378]
本文中所引用的文件和研究的引证并不旨在承认任何前述内容是相关的现有技术。关于这些文件内容的所有陈述都是基于申请人可获得的信息,并且不构成对这些文件内容正确性的任何承认。
[0379]
呈现以下描述以使本领域普通技术人员能够制造和使用多种实施方案。特定装置、技术和应用的描述仅作为实例提供。对本文中所述的实施例的多种修改对于本领域普通技术人员而言将是明显的,并且在不脱离多种实施方案的精神和范围的情况下,本文中定义的一般原理可应用于另一些实施例和应用。因此,多种实施方案不旨在限于本文中描述和示出的实施例,而是与符合权利要求书的范围相一致。
[0380]
实施例
[0381]
实施例1:构建体设计和mrna产生
[0382]
编码细胞因子的mrna的体外转录基于pst1
‑
t7
‑
aga
‑
deari
‑
hag
‑
mcs
‑
fi
‑
a30la70质粒
‑
骨架和衍生的dna
‑
构建体。这些质粒构建体包含5’utr(非翻译区,智人(homo sapiens)血红蛋白亚基α1(hag)的5
’‑
utr的衍生物)、3’fi元件(其中f是分裂的mrna的氨基
端增强子的136个核苷酸长的3
’‑
utr片段,并且i是线粒体编码的12s rna的142个核苷酸长的片段,二者均在智人中鉴定;wo 2017/060314)和100个核苷酸的poly(a)尾,在70个核苷酸之后有接头。细胞因子和血清白蛋白(alb)编码序列来源于小鼠(mus musculus)(缩写为m,即malb、mil2或mifnα)或智人(缩写为h,即halb、hil2 hifnα),在所得氨基酸序列中没有引入变化。在成熟il2序列(il2的信号肽没被编码)的n端引入alb。仅在最c端部分引入终止密码子。细胞因子与halb融合构建体中的不同蛋白质部分被编码甘氨酸和丝氨酸残基的30个核苷酸长的接头序列隔开。如kreiter et al.所述,通过体外转录产生mrna。(kreiter,s.et al.cancer immunol.immunother.56,1577
–
87(2007))。对于所有编码细胞因子/白蛋白的rna,正常核苷尿苷被1
‑
甲基
‑
假尿苷替换。所得mrna配备有cap1结构并且双链(dsrna)分子被耗尽。经纯化的细胞因子/白蛋白mrna在h2o中洗脱,并储存在
‑
80℃下直至进一步使用。所有所描述的mrna构建体的体外转录均在biontech rnapharmaceuticals gmbh处进行。表1中示出了用于后续实验的所有构建体的列表。
[0383]
表1:mrna编码和表达的蛋白质的氨基酸序列。
[0384]
[0385]
[0386][0387]
实施例2:在体内rna编码的il2对疫苗诱导的t细胞应答的影响
[0388]
雌性c57bl/6(9周龄)(每组n=8只小鼠)购自envigo,并在第0天、第7天和第14天用10μg编码鸡卵清蛋白(ova)来源的h2
‑
kb限制性cd8
t细胞表位siinfekl的mrna脂质复合体(rna
‑
l)(kranz,l.m.et al.nature 534,396
–
401(2016))静脉内(i.v.)进行疫苗接种。每次疫苗接种之后三天,i.v.施用1μg用transit(mirrus)配制的编码malb
‑
融合蛋白的mrna。小鼠接受malb或与malb融合的mil2(malb
‑
mil2)。在第7天、第14天和第21天提取小鼠的血液,并通过流式细胞术分析抗原特异性t细胞应答以及调节性t细胞(treg)。在2至8℃下用荧光色素标记的抗体或mhc四聚体对50μl血液进行染色持续30分钟。通过cd45(30
‑
f11,bd)和cd8(克隆5h10,bd)特异性抗体以及与siinfekl肽结合的mhc四聚体(mbl international)共染色检测抗原特异性t细胞。使用ebioscience的foxp3染色试剂盒,根据制造者的说明,通过对cd45(30
‑
f11,bd)、cd4(克隆rm4
‑
5,biolegend)、cd25(克隆pc61,bd)和foxp3(克隆fjk
‑
16s,ebioscience)具有特异性的抗体来鉴定treg。使用裂解溶液(bd facs
tm
)裂解血液。为了确定绝对细胞数,将细胞转移到管(bd)中。在lsrfortessa流式细胞仪(bd)上获得流式细胞数据,并用flowjo x软件(tree star)进行分析。使用graphpad prism 7对结果进行描绘和统计分析。图1a给出了处理和分析计划表的概述。与仅接受rna
‑
l疫苗接种和malb的对照组相比,rna
‑
l疫苗接种和用malb
‑
mil2进行的处理的组合导致在第7天和第14天ova特异性t细胞显著升高(图1b、c)。然而,在第21天的分析揭示,在经malb
‑
mil2处理的动物中,抗原特异性t细胞应答显著降低,其频率甚至显著低于malb对照(图1d、e)。我们假设抗原特异性t细胞的这种降低是由malb
‑
mil2诱导的treg引起的。事实上,经malb
‑
mil2处理的小鼠在每个测量的时间点都显示出显著更高的treg频率,并且在第14天具有峰值(图1f)。推测在早期时间点malb
‑
mil2的刺激电位超过了treg的抑制电位。在较晚的时间点,treg数量增加,导致对活化的cd8 t细胞的抑制信号更强,破坏malb
‑
mil2的刺激电位。
[0389]
为了在不同背景的第二模型中证实这些结果,用20μg编码h2
‑
kd限制性cd8 t细胞抗原spsyayhqf的gp70 rna
‑
l疫苗接种(kranz,l.m.et al.nature 534,396
–
401(2016))结
lambda inc.,目录号a25761)的iscove’s改良杜氏培养基(imdm;life technologies gmbh,目录号12440
‑
053)中,将每孔30,000个cfse标记的pbmc和30,000个farred标记的treg共培养,并与次优浓度的抗cd3抗体(ucht1;r&d systems,目录号mab100;最终浓度0.09μg/ml)一起孵育。用含halb
‑
hil2的上清液(最终浓度为5%)处理pbmc:treg共培养物,并且不添加、添加625u/ml或添加10,000u/ml重组ifnα2b(pbl assay science,目录号:11105
‑
1)。在37℃、5%co2下刺激共培养物四天。收获细胞并通过流式细胞术分析,通过efluor780染色(ebioscience,目录号65
‑
0865
‑
18)排除死细胞。通过用在facs缓冲液(dpbs 2%fbs 2mm edta)中以1:100稀释的抗人cd8 pe
‑
cy7抗体(tonbo biosciences,目录号60
‑
0088)染色来鉴定cd8 t细胞。在bd facs canto ii流式细胞仪(becton dickinson)上进行流式细胞术分析,其中cfse稀释(cd8 t细胞)和farred稀释(treg)作为增殖读出。使用flowjo 10.5软件(treestar,inc.)分析所获得的增殖数据,并在graphpad prism 6(graphpad software,inc.)中绘制输出的扩增指数值。
[0395]
在组合的抗cd3和halb
‑
hil2处理之后,cd8 t细胞和cd4 cd25 treg均具有强烈的增殖响应。虽然添加重组ifnα使treg的增殖降低约50%至55%,但cd8 t细胞的增殖仅降低约10%至20%。对于两个受试的pbmc供体,均观察到treg而不是cd8 t细胞的选择性增殖抑制的作用(图5a、b),并且其很大程度上独立于所使用的ifnα浓度。
[0396]
实施例5:ifnα和il2组合治疗导致小鼠中的协同抗肿瘤作用
[0397]
接下来,我们评估了向il2治疗添加ifnα是否会导致改善的抗肿瘤作用。雌性balb/c小鼠(9周龄,每组n=12只小鼠)购自janvier labs s.a.s.并皮下注射(s.c.)5
×
105个ct26结肠癌细胞。肿瘤细胞接种之后15天,基于肿瘤尺寸对每组10至11只小鼠进行分层。用100μl用transit(mirrus)单独配制的1μg编码malb
‑
mil2的rna和2μg编码ifnα的mrna处理小鼠5次。对照组接受用transit配制的ifnα、il2或无关rna(1μg编码malb的rna)。肿瘤尺寸用卡尺每周三次地测量,并使用公式(a2×
b)/2(a,宽度;b,长度)进行计算。当动物表现出健康受损迹象或当肿瘤体积超过1500mm3时,对动物进行安乐死。在第29天和第35天提取小鼠的血液并通过流式细胞术分析cd8
t细胞,如实施例2中所述。图6a说明了实验概要。
[0398]
值得注意的是,本实验中未添加疫苗,因为ct26肿瘤本身具有免疫原性,并且肿瘤特异性t细胞可在没有疫苗的情况下引发,特别是在il2处理下。此外,在鼠肿瘤中,特别是早期干预决定了治疗结果。il2介导的疫苗诱导的t细胞的增强将因此导致强大的肿瘤控制,并且随后il2刺激的treg对t细胞的抑制不会产生影响。相反,在没有疫苗接种的情况下,il2对肿瘤特异性t细胞的增强作用不太明显,并且因此treg对肿瘤特异性t细胞的抑制作用更为重要。
[0399]
在ifnα和il2的组合处理的组中检测到显著的治疗活性,而il2或ifnα单一治疗不影响肿瘤生长(图6b)。总的来说,在组合治疗下,11只小鼠中有4只(36%)抵制其肿瘤,而在分别用ifnα或il2进行的单一治疗之后,仅两只(18%)或没有小鼠无肿瘤(图6c)。与il2单一治疗相比,il2和ifnα处理导致显著的存活受益(图6d)。重要的是,il2和ifnα组合治疗的治疗活性伴随着血液中cd8
t细胞的持续和显著的提高。与图2e和图3d类似,il2单一治疗在第29天介导cd8
t细胞的仅暂时性升高,其直到第35天才正常(图6e)。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。