组合物、膜、近红外线截止滤波器、层叠体、图案形成方法
1.本技术是申请人提交的申请号为201780006291.7、发明名称为“组合物、膜、近红外线截止滤波器、层叠体、图案形成方法、固体成像元件、图像显示装置、红外线传感器及滤色器板”的申请的分案申请。母案申请日为2017年1月19日,最早优先权日为2016年1月29日。
技术领域
2.本发明涉及一种组合物、膜、近红外线截止滤波器、层叠体、图案形成方法、固体成像元件、图像显示装置、红外线传感器及滤色器。
背景技术:
3.在摄影机、数码静态照相机、带有照相机功能的移动电话等中,使用作为彩色图像的固体成像元件的ccd(电荷耦合元件)或cmos(互补式金属氧化膜半导体)。该些固体成像元件在该受光部中使用对红外线具有感度的硅光电二极管,因此有时通过使用近红外线截止滤波器来进行可见度校正。
4.作为近红外线吸收化合物,已知有吡咯并吡咯化合物和花青化合物等(例如,专利文献1、专利文献2)。
5.专利文献2中,记载有一种使用包含两种以上的水溶性花青化合物的近红外线吸收组合物来制作近红外线截止滤波器的例子。
6.以往技术文献
7.专利文献
8.专利文献1:日本特开2009
‑
263614号公报
9.专利文献2:日本特开2009
‑
185161号公报
技术实现要素:
10.发明要解决的技术课题
11.近年来,关于近红外线截止滤波器等包含近红外线吸收化合物的膜,要求屏蔽较宽波长范围的红外线,并要求进一步提高红外线屏蔽性。而且,关于近红外线截止滤波器等包含近红外线吸收化合物的膜,有时也在高温高湿的环境下使用,因此要求即使在高温高湿的环境下曝光,光谱也很难产生变化。
12.用于解决技术课题的手段
13.本发明的目的在于提供一种红外线屏蔽性优异,并能够形成不易产生光谱变化的膜的组合物。并且,本发明的目的在于提供一种膜、近红外线截止滤波器、层叠体、图案形成方法、固体成像元件、图像显示装置、红外线传感器及滤色器。
14.在上述状况下,本发明人等进行深入研究的结果发现,通过使用两种以上的近红外线吸收化合物能够实现上述目的,并完成了本发明,所述近红外线吸收化合物在波长650~1000nm的范围内具有极大吸收波长,且相对于23℃的水的溶解度为0.1质量%以下。本发
明提供以下内容。
15.<1>一种组合物,包含两种以上的近红外线吸收化合物,该近红外线吸收化合物在波长650~1000nm的范围内具有极大吸收波长,且相对于23℃的水的溶解度为0.1质量%以下,
16.两种以上的近红外线吸收化合物包含:
17.第1近红外线吸收化合物,在波长650~1000nm的范围内具有极大吸收波长;及
18.第2近红外线吸收化合物,在比第1近红外线吸收化合物的极大吸收波长更靠短波长侧的波长650~1000nm的范围内具有极大吸收波长,
19.第1近红外线吸收化合物的极大吸收波长与第2近红外线吸收化合物的极大吸收波长之差为1~150nm。
20.<2>根据<1>所述的组合物,其中,第1近红外线吸收化合物及第2近红外线吸收化合物的波长500nm下的吸光度a1与极大吸收波长下的吸光度a2的比率a1/a2分别为0.04以下。
21.<3>根据<1>或<2>所述的组合物,其中,第1近红外线吸收化合物及第2近红外线吸收化合物的至少一个包含选自吡咯并吡咯化合物、花青化合物、方酸化合物、酞菁化合物、萘酞菁化合物及萘嵌苯(rylene)化合物中的至少一种。
22.<4>根据<1>至<3>中任一个所述的组合物,其中,第1近红外线吸收化合物为吡咯并吡咯化合物。
23.<5>根据<1>至<4>中任一个所述的组合物,其中,第1近红外线吸收化合物及第2近红外线吸收化合物的至少一个包含由下述式(i)表示的化合物,
24.[化学式1]
[0025][0026]
式(i)中,a1及a2分别独立地表示杂芳基,
[0027]
b1及b2分别独立地表示
‑
br1r2基,r1及r2分别独立地表示取代基,r1与r2可以相互键合而形成环,
[0028]
c1及c2分别独立地表示烷基、芳基、或杂芳基,
[0029]
d1及d2分别独立地表示取代基。
[0030]
<6>根据<1>至<4>中任一个所述的组合物,其中,第1近红外线吸收化合物及第2近红外线吸收化合物中的至少一个包含选自由下述式(ii)表示的化合物及由下述式(iii)表示的化合物中的至少一种,
[0031]
[化学式2]
[0032][0033]
式(ii)中,x1及x2分别独立地表示o、s、nr
x1
或cr
x2
r
x3
,r
x1
~r
x3
分别独立地表示氢原子或取代基,
[0034]
r3~r6分别独立地表示氢原子或取代基,
[0035]
r3与r4或r5与r6可以相互键合而形成环,
[0036]
b1及b2分别独立地表示
‑
br1r2基,r1及r2分别独立地表示取代基,r1与r2可以相互键合而形成环,
[0037]
c1及c2分别独立地表示烷基、芳基或杂芳基,
[0038]
d1及d2分别独立地表示取代基,
[0039]
式(iii)中,y1~y8分别独立地表示n或cr
y1
,y1~y4中的至少两个为cr
y1
,y5~y8中的的至少两个为cr
y1
,r
y1
表示氢原子或取代基,相邻的r
y1
彼此可以相互键合而形成环,
[0040]
b1及b2分别独立地表示
‑
br1r2基,r1及r2分别独立地表示取代基,r1与r2可以相互键合而形成环,
[0041]
c1及c2分别独立地表示烷基、芳基或杂芳基,
[0042]
d1及d2分别独立地表示取代基。
[0043]
<7>根据<1>至<6>中任一项所述的组合物,其中,第1近红外线吸收化合物和第2近红外线吸收化合物为具有共同的色素骨架的化合物。
[0044]
<8>根据<1>至<3>中任一项所述的组合物,其中,第1近红外线吸收化合物和第2近红外线吸收化合物均为吡咯并吡咯化合物或均为花青化合物。
[0045]
<9>根据<1>至<8>中任一项所述的组合物,其中,第1近红外线吸收化合物的极大吸收波长与第2近红外线吸收化合物的极大吸收波长之差为1~90nm。
[0046]
<10>根据<1>至<9>中任一项所述的组合物,其还包含固化性化合物。
[0047]
<11>根据<1>至<10>中任一项所述的组合物,其还包含树脂及溶剂。
[0048]
<12>根据<1>至<11>中任一项所述的组合物,其还包含彩色着色剂。
[0049]
<13>一种膜,其包含<1>至<12>中任一项所述的组合物。
[0050]
<14>一种近红外线截止滤波器,其包含<1>至<12>中任一项所述的组合物。
[0051]
<15>根据<14>所述的近红外线截止滤波器,其还具有含铜的层。
[0052]
<16>一种层叠体,其具有<14>或<15>所述的近红外线截止滤波器和包含彩
色着色剂的滤色器。
[0053]
<17>一种图案形成方法,其包含:在支撑体上形成包含<1>~<12>中任一个所述的组合物的组合物层的工序;及通过光刻法或干式蚀刻法在组合物层上形成图案的工序。
[0054]
<18>一种固体成像元件,其具有<13>所述的膜。
[0055]
<19>一种图像显示装置,其具有<13>所述的膜。
[0056]
<20>一种红外线传感器,其具有<13>所述的膜。
[0057]
<21>一种滤色器,其具有包含<1>至<12>中任一项所述的组合物的像素和选自红、绿、蓝、品红、黄、青、黑及无色的像素。
[0058]
发明效果
[0059]
根据本发明,可提供一种能够形成红外线屏蔽性及耐湿性优异的膜的组合物。并且,可提供一种膜、近红外线截止滤波器、层叠体、图案形成方法、固体成像元件、图像显示装置、红外线传感器及滤色器。
附图说明
[0060]
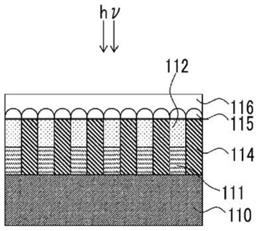
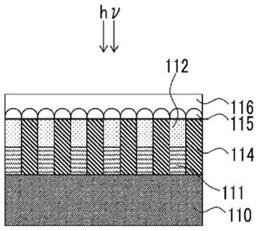
图1是表示红外线传感器的一实施方式的概略图。
[0061]
图2是表示图案的形成工序的图(俯视图)。
[0062]
图3是图2的a
‑
a剖视图。
[0063]
图4是表示图案的形成工序的图(俯视图)。
[0064]
图5是图4的a
‑
a剖视图。
[0065]
图6是表示图案的形成工序的图(俯视图)。
[0066]
图7是图6的a
‑
a剖视图。
[0067]
图8是表示红外线传感器的另一实施方式的概略图。
具体实施方式
[0068]
以下,对本发明的内容进行详细说明。
[0069]
本说明书中,“~”是以将记载于其前后的数值作为下限值及上限值而包含的含义使用。
[0070]
本说明书中的基团(原子团)的标记中,未记载有取代及未取代的标记一同包含不具有取代基的基团(原子团)和具有取代基的基团(原子团)。例如,“烷基”不仅包含不具有取代基的烷基(未取代烷基),还包含具有取代基的烷基(取代烷基)。
[0071]
本说明书中,光是指光化射线或放射线。而且,“光化射线”或“放射线”是指例如以水汞灯的明线光谱、准分子激光为代表的远紫外线、极紫外线(euv光)、x射线、电子束等。
[0072]
本说明书中,在并无特别限制的范围内、“曝光”不仅包含使用以水汞灯的明线光谱、准分子激光为代表的远紫外线、x射线、euv光等的曝光,还包含使用电子束、离子束等粒子束。
[0073]
本说明书中,“(甲基)丙烯酸酯”表示丙烯酸酯及甲基丙烯酸酯,“(甲基)丙烯酸”表示丙烯酸及甲基丙烯酸,“(甲基)丙烯酰基”表示丙烯酰基及甲基丙烯酰基。
[0074]
本说明书中,将重量均分子量及数均分子量定义为通过凝胶渗透色谱法(gpc)测
定的聚苯乙烯换算值而定义。本说明书中,重量均分子量(mw)及数均分子量(mn)例如能够通过使用hlc
‑
8220(tosoh corporation制),作为柱而使用tskgel super awm―h(tosoh corporation制、6.0mmid(内径)
×
15.0cm),作为洗脱液而使用10mmol/l的溴化锂nmp(n
‑
甲基吡咯啶酮)溶液来求出。
[0075]
本说明书中,化学式中的me表示甲基,et表示乙基,bu表示丁基,ph表示苯基。
[0076]
近红外线是指极大吸收波长区域为波长700~2500nm的光(电磁波)。
[0077]
本说明书中,总固体成分是指从组合物的所有成分去除溶剂之后的成分的总质量。
[0078]
本说明书中,“工序”该一术语不仅包含独立的工序,即使于无法与其他工序明确区分的情况下只要可实现对该工序所期待的作用,也包含于本术语中。
[0079]
<组合物>
[0080]
本发明的组合物包含两种以上的近红外线吸收化合物,该近红外线吸收化合物在波长650~1000nm的范围内具有极大吸收波长,且相对于23℃的水的溶解度为0.1质量%以下,
[0081]
两种以上的近红外线吸收化合物包含:
[0082]
第1近红外线吸收化合物,在波长650~1000nm的范围内具有极大吸收波长;及
[0083]
第2近红外线吸收化合物,在比第1近红外线吸收化合物的极大吸收波长更靠短波长侧的波长650~1000nm的范围内具有极大吸收波长,
[0084]
第1近红外线吸收化合物的极大吸收波长与第2近红外线吸收化合物的极大吸收波长之差为1~150nm。
[0085]
另外,本说明书中,“在波长650~1000nm的范围内具有极大吸收波长”是指在近红外线吸收化合物的溶液中的吸收光谱中,在波长650~1000nm的范围内具有表示最大吸光度的波长。关于用于测定近红外线吸收化合物的溶液中的吸收光谱的测定溶剂,可举出氯仿、甲醇、二甲基亚砜、乙酸乙酯、四氢呋喃。当为溶解于氯仿的化合物的情况下,将氯仿用作测定溶剂。当为不溶解于氯仿的化合物的情况下,使用甲醇。并且,均不溶解于氯仿及甲醇的情况下,使用二甲基亚砜。并且,本说明书中,近红外线吸收化合物相对于23℃的水的溶解度是指通过后述的实施例中所示的方法测定而得到的值。
[0086]
本发明的组合物包含上述第1近红外线吸收化合物和第2近红外线吸收化合物,因此能够形成红外线屏蔽性优异,且很难产生光谱变化的膜。
[0087]
即,第1近红外线吸收化合物和第2近红外线吸收化合物在波长650~1000nm的范围内,在不同波长范围具有极大吸收波长,并且两者的极大吸收波长之差为1~150nm,因此与使用一种红外线吸收化合物的情况相比,波长650~1000nm的范围内的膜的吸收光谱的波形得到扩大,能够屏蔽较宽波长范围的红外线。
[0088]
并且,得知包含两种以上的近红外线吸收化合物的膜轻松地产生光谱变化。对光谱变化的产生进行研究的结果,推测其原因在于膜中所包含的近红外线吸收化合物渗出至膜表面,或近红外线吸收化合物的缔合状态发生变化。
[0089]
本发明中,作为近红外线吸收化合物,使用相对于23℃的水的溶解度为0.1质量%以下的化合物,因此可提高所得到的膜的耐湿性。即使将通过使用本发明的组合物而得到的膜置于高温高湿的环境下,也能够抑制近红外线吸收化合物的渗出和缔合状态的变化
等,并能够抑制光谱变化。
[0090]
并且,作为第1近红外线吸收化合物,使用耐光性优异的化合物(例如吡咯并吡咯化合物)的情况下,即使作为第2近红外线吸收化合物而使用耐光性较差的化合物,也能够制作出耐光性优异的膜。推测可得到这种效果的机理的原因在于通过将第2近红外线吸收化合物所吸收的能量移动至耐光性优异的第1近红外线吸收化合物侧,从而能够抑制第2近红外线吸收化合物的分解等,该第2近红外线吸收化合物在比第1近红外线吸收化合物更靠近短波长侧具有极大吸收波长。
[0091]
以下,对组合物的各成分进行说明。
[0092]
<<近红外线吸收化合物>>
[0093]
本发明的组合物包含两种以上的近红外线吸收化合物(以下,还称为近红外线吸收化合物a),该近红外线吸收化合物在波长650~1000nm的范围内具有极大吸收波长,且相对于23℃的水的溶解度为0.1质量%以下。
[0094]
关于近红外线吸收化合物a的极大吸收波长,优选在660~1000nm的范围具有极大吸收波长,更优选在670~1000nm的范围具有极大吸收波长,尤其优选在710~1000nm的范围具有极大吸收波长。
[0095]
近红外线吸收化合物a相对于23℃的水的溶解度为0.1质量%以下,更优选为0.05质量%以下,进一步优选为0.01质量%以下。根据该方式,能够制作出光谱变化进一步得到抑制的膜。尤其,即使在高温高湿的环境下进行曝光,也能够进一步有效地抑制光谱变化。
[0096]
在近红外线吸收化合物a中,波长500nm下的吸光度a1与极大吸收波长下的吸光度a2的比率a1/a2优选为0.08以下,更优选为0.04以下。根据该方式,能够制作出可见透明性和红外线屏蔽性优异的膜。
[0097]
另外,波长500nm下的吸光度a1及极大吸收波长下的吸光度a2为依据近红外线吸收化合物的溶液中的吸收光谱求出的值。
[0098]
两种以上的近红外线吸收化合物a至少包含如下化合物:第1近红外线吸收化合物,在波长650~1000nm的范围内具有极大吸收波长;第2近红外线吸收化合物,在波长650~1000nm的范围内具有极大吸收波长,且在比第1近红外线吸收化合物的极大吸收波长更靠短波长侧,第1近红外线吸收化合物的极大吸收波长与第2近红外线吸收化合物的极大吸收波长之差为1~150nm。
[0099]
作为第1近红外线吸收化合物与第2近红外线吸收化合物的优选组合的一方式,第1近红外线吸收化合物的极大吸收波长与第2近红外线吸收化合物的极大吸收波长之差优选为5~100nm,更优选为30~90nm。根据该方式,适合制作出能够屏蔽较宽的波长范围的红外线的膜等。
[0100]
作为第1近红外线吸收化合物与第2近红外线吸收化合物的优选组合的又一方式,第1近红外线吸收化合物的极大吸收波长与第2近红外线吸收化合物的极大吸收波长之差优选为5~100nm,更优选为20~60nm。根据该方式,适合制作可选择性屏蔽特定波长范围的红外线的膜等。
[0101]
另外,还可以包含3种以上的在上述波长范围具有极大吸收波长的近红外线吸收化合物。该情况下,波长650~1000nm的范围中,将在最长的长波长侧具有极大吸收波长的近红外线吸收化合物作为第1近红外线吸收化合物,并将在比第1近红外线吸收化合物更靠
短波长侧具有极大吸收波长的所有近红外线吸收化合物作为第2近红外线吸收化合物。并且,存在两种以上的、在最长的长波长侧具有极大吸收波长的近红外线吸收化合物的情况下,将这些视为第1近红外线吸收化合物。
[0102]
近红外线吸收化合物a只要是在波长650~1000nm的范围内具有极大吸收波长,且相对于23℃的水的溶解度为0.1质量%以下的化合物,则并无特别限定。例如,可举出吡咯并吡咯化合物、花青化合物、方酸(squarylium)化合物、酞菁化合物、萘酞菁化合物、萘嵌苯(rylene)化合物、部花青化合物、克酮鎓(croconium)化合物、氧杂菁(oxonol)化合物、二亚铵化合物、二硫酚(dithiol)化合物、三芳甲烷化合物、吡咯亚甲基化合物、甲亚氨(azomethine)化合物、蒽醌化合物及二苯并呋喃酮化合物等。其中,优选吡咯并吡咯化合物、花青化合物、方酸化合物、酞菁化合物、萘酞菁化合物及萘嵌苯(rylene)化合物,更优选吡咯并吡咯化合物、花青化合物及方酸化合物,进一步优选吡咯并吡咯化合物。
[0103]
第1近红外线吸收化合物和第2近红外线吸收化合物可以为具有共同的色素骨架的化合物,也可以为具有不同的色素骨架的化合物。另外,具有共同的色素骨架的化合物是指相同的化合物种类。例如,第1近红外线吸收化合物和第2近红外线吸收化合物均为吡咯并吡咯化合物(具有吡咯并吡咯色素骨架的化合物)的情况下,第1近红外线吸收化合物和第2近红外线吸收化合物相当于具有共同的色素骨架的化合物。
[0104]
第1近红外线吸收化合物优选吡咯并吡咯化合物。第2近红外线吸收化合物可以为吡咯并吡咯化合物,也可以为吡咯并吡咯化合物以外的化合物。作为吡咯并吡咯化合物以外的化合物,可举出花青化合物、方酸化合物、酞菁化合物、萘酞菁化合物及萘嵌苯(rylene)化合物等,优选花青化合物及方酸化合物。从耐光性的观点考虑,第2近红外线吸收化合物更优选吡咯并吡咯化合物。即,优选第1近红外线吸收化合物为吡咯并吡咯化合物,并且第2近红外线吸收化合物为选自吡咯并吡咯化合物、方酸化合物及花青化合物中的至少一种方式。该方式中,第2近红外线吸收化合物优选吡咯并吡咯化合物或方酸化合物,尤其优选吡咯并吡咯化合物。吡咯并吡咯化合物的耐光性优异,因此如上所述,作为第1近红外线吸收化合物,使用吡咯并吡咯化合物的情况下,即使作为第2近红外线吸收化合物而使用耐光性比吡咯并吡咯化合物差的化合物的情况下,也能够制作出耐光性优异的膜。其中,第1近红外线吸收化合物和第2近红外线吸收化合物双方均使用吡咯并吡咯化合物的情况下,尤其能够制作出耐光性优异的膜。
[0105]
并且,第1近红外线吸收化合物优选方酸化合物。第2近红外线吸收化合物可以为方酸化合物,也可以为方酸化合物以外的化合物。作为方酸化合物以外的化合物,可举出吡咯并吡咯化合物、花青化合物、酞菁化合物、萘酞菁化合物及萘嵌苯(rylene)化合物等,优选吡咯并吡咯化合物及花青化合物。第2近红外线吸收化合物更优选吡咯并吡咯化合物或方酸化合物。即,更优选第1近红外线吸收化合物为方酸化合物,并且第2近红外线吸收化合物为选自吡咯并吡咯化合物、方酸化合物及花青化合物中的至少一种的方式。该方式中,第2近红外线吸收化合物更优选吡咯并吡咯化合物或方酸化合物。
[0106]
并且,第1近红外线吸收化合物优选花青化合物。第2近红外线吸收化合物可以为花青化合物,也可以为花青化合物以外的化合物。作为花青化合物以外的化合物,可举出吡咯并吡咯化合物、方酸化合物、酞菁化合物、萘酞菁化合物及萘嵌苯(rylene)化合物等,优选吡咯并吡咯化合物及方酸化合物。第2近红外线吸收化合物更优选吡咯并吡咯化合物或
方酸化合物。即,更优选第1近红外线吸收化合物为花青化合物,并且第2近红外线吸收化合物为选自吡咯并吡咯化合物、方酸化合物及花青化合物中的至少一种的方式。该方式中,第2近红外线吸收化合物更优选吡咯并吡咯化合物或花青化合物,进一步优选花青化合物。
[0107]
组合物中的近红外线吸收化合物a的含量(第1近红外线吸收化合物和第2近红外线吸收化合物的合计量)相对于组合物的总固体成分优选为0.01~60质量%。下限优选为0.1质量%以上,更优选为0.5质量%以上。上限优选为30质量%以下,更优选为15质量%以下。通过设在该范围内,能够赋予良好的近红外线吸收性。
[0108]
关于第1近红外线吸收化合物与第2近红外线吸收化合物的比例,并无特别限定。相对于第1近红外线吸收化合物的100质量份,优选为含有5~500质量份的第2近红外线吸收化合物,更优选为10~300质量份,进一步优选为30~200质量份。
[0109]
第1近红外线吸收化合物可以仅为一种,也可以包含两种以上。包含两种以上的第1近红外线吸收化合物和/或第2近红外线吸收化合物的情况下,这些合计优选在上述范围内。
[0110]
并且,第2近红外线吸收化合物可以仅为一种,也可以包含两种以上。从分光的观点考虑,优选包含两种以上的第2近红外线吸收化合物。包含两种以上的n个第2近红外线吸收化合物的情况下,n个第2近红外线吸收化合物中,在第a个长波长侧具有极大吸收波长的化合物a
a
的极大吸收波长与在第(a 1)个长波长侧具有极大吸收波长的化合物a
a 1
的极大吸收波长之差优选为1~90nm,更优选为5~60nm。其中,a表示1~n
‑
1的整数,n表示2以上的整数。
[0111]
并且,例如包含3种第2近红外线吸收化合物的情况下,在第1个长波长侧具有极大吸收波长的化合物a1(在最长的长波长侧具有极大吸收波长的化合物)的极大吸收波长与在第2个长波长侧具有极大吸收波长的化合物a2(在比化合物a1更靠短波长侧具有极大吸收波长的化合物)的极大吸收波长之差优选为1~90nm,更优选为5~60nm。并且,在第2个长波长侧具有极大吸收波长的化合物a2的极大吸收波长与在第3个长波长侧具有极大吸收波长的化合物a3(在比化合物a2更靠短波长侧具有极大吸收波长的化合物)的极大吸收波长之差优选为1~90nm,更优选为5~60nm。
[0112]
也优选将第1近红外线吸收化合物及第2近红外线吸收化合物用作色素多聚体(multimer)。色素多聚体在一分子中具有两个以上的近红外线吸收性色素结构,优选具有3个以上的近红外线吸收性色素结构。一分子中的近红外线吸收性色素结构的数量的上限并无特别限定,能够设为100以下。
[0113]
(吡咯并吡咯化合物)
[0114]
用作近红外线吸收化合物a的吡咯并吡咯化合物优选由式(i)表示的化合物。
[0115]
[化学式3]
[0116]
[0117]
式(i)中,a1及a2分别独立地表示杂芳基,
[0118]
b1及b2分别独立地表示
‑
br1r2基,r1及r2分别独立地表示取代基,r1与r2可以相互键合而形成环,
[0119]
c1及c2分别独立地表示烷基、芳基或杂芳基,
[0120]
d1及d2分别独立地表示取代基。
[0121]
式(i)中,a1及a2分别独立地表示杂芳基。a1与a2可以为相同的基团,也可以为不同的基团。a1与a2优选相同的基团。
[0122]
杂芳基优选单环或稠环,单环或稠合数更优选为2~8的稠环,单环或稠合数进一步优选为2~4的稠环。构成杂芳基的杂原子的数量为优选1~3。构成杂芳基的杂原子优选氮原子、氧原子或硫原子。构成杂芳基的碳原子的数量优选为3~30,更优选为3~18,进一步优选为3~12,尤其优选为3~10。杂芳基优选为5元环或6元环。
[0123]
杂芳基优选由下述式(a
‑
1)表示的基团及由(a
‑
2)表示的基团。
[0124]
[化学式4]
[0125][0126]
式(a
‑
1)中,x1分别独立地表示o、s、nr
x1
或cr
x2
r
x3
,r
x1
~r
x3
分别独立地表示氢原子或取代基,r3及r4分别独立地表示氢原子或取代基,r3与r4可以相互键合而形成环。*表示式(i)中的键合位置。
[0127]
关于r3、r4及r
x1
~r
x3
所表示的取代基,可举出烷基、烯基、芳基、杂芳基、烷氧基、芳氧基、杂芳氧基、酰基、烷氧羰基、芳氧羰基、杂芳氧基羰基、酰氧基、氨基、酰氨基、烷氧羰基氨基、芳氧羰基氨基、杂芳氧基羰基氨基、磺酰基氨基、氨磺酰基、氨基甲酰基、烷硫基、芳硫基、杂芳硫基、烷基磺酰基、芳基磺酰基、杂芳基磺酰基、烷基亚磺酰基、芳基亚磺酰基、杂芳基亚磺酰基、脲基、磷酸酰氨基、巯基、磺酸基、羧基、硝基、羟肟酸(hydroxamic acid)基、亚磺酸基、肼基、亚氨基、甲硅烷基、羟基、卤素原子、氰基等,优选为烷基、芳基及卤素原子。
[0128]
烷基的碳数优选为1~20,更优选为1~15,进一步优选为1~8。烷基可以为直链、分支、环状中的任意一个,优选为直链或分支。烷基可以具有取代基,也可以未取代。作为取代基,可举出上述的基团,例如,可举出卤素原子、芳基等。
[0129]
芳基的碳数优选为6~30,更优选为6~20,进一步优选为6~12。芳基可以具有取代基,也可以未取代。作为取代基,可举出上述的基团,例如,可举出卤素原子、烷基等。
[0130]
关于卤素原子,可举出氟原子、氯原子、溴原子、碘原子等。
[0131]
r3与r4键合而形成的环优选为芳香族环。r3与r4形成环的情况下,(a
‑
1)可举出由下述(a
‑1‑
1)表示的基团,由(a
‑1‑
2)表示的基团等。
[0132]
[化学式5]
[0133][0134]
式中,x1分别独立地表示o、s、nr
x1
或cr
x2
r
x3
,r
x1
~r
x3
分别独立地表示氢原子或取代基,r
101
~r
109
分别独立地表示氢原子或取代基。*表示式(i)中的键合位置。
[0135]
式(a
‑
2)中,y1~y4分别独立地表示n或cr
y1
,y1~y4的至少两个为cr
y1
,r
y1
表示氢原子或取代基,相邻的r
y1
彼此可以相互键合而形成环。*表示式(i)中的键合位置。
[0136]
关于r
y1
所表示的取代基,可举出上述的取代基,优选为烷基、芳基及卤素原子。烷基的碳数优选为1~20,更优选为1~15,进一步优选为1~8。烷基可以为直链、分支、环状中的任意一个,优选为直链或分支。烷基可以具有取代基,也可以未取代。作为取代基,可举出上述的取代基,例如可举出卤素原子、芳基等。
[0137]
芳基的碳数优选为6~30,更优选为6~20,进一步优选为6~12。芳基可以具有取代基,也可以未取代。作为取代基,可举出上述的取代基,例如可举出卤素原子、烷基等。
[0138]
关于卤素原子,可举出氟原子、氯原子、溴原子、碘原子等。
[0139]
y1~y4的至少两个为cr
y1
,相邻的r
y1
彼此可以相互键合而形成环。相邻的r
y1
彼此键合而形成的环优选为芳香族环。相邻的r
y1
彼此形成环的情况下,(a
‑
2)可举出由下述(a
‑2‑
1)~(a
‑2‑
5)表示的基团等。
[0140]
[化学式6]
[0141][0142]
式中,r
201
~r
227
分别独立地表示氢原子或取代基,*表示式(i)中的键合位置。
[0143]
作为a1及a2的具体例,可举出以下。以下,bu表示丁基。*表示式(i)中的键合位置。
[0144]
[化学式7]
[0145][0146]
式(i)中,b1及b2分别独立地表示
‑
br1r2基,r1及r2分别独立地表示取代基。r1与r2可以相互键合而形成环。作为取代基,可举出以上述的a1及a2进行说明的基团,优选为卤素原子、烷基、烯基、烷氧基、芳基或杂芳基,更优选为卤素原子、芳基或杂芳基,进一步优选为芳基或杂芳基。r1与r2可以为相同的基团,也可以为不同的基团。r1与r2优选为相同基团。而
且,b1与b2可以为相同基团,也可以为不同的基团。优选b1与b2为相同的基团。
[0147]
作为卤素原子,优选为氟原子、氯原子、溴原子、碘原子,尤其优选为氟原子。
[0148]
烷基的碳数优选为1~40。下限例如,更优选为3以上。上限例如,更加为30以下,进一步优选为25以下。烷基可以为直链、分支、环状中的任意一个,优选直链或分支。
[0149]
烯基的碳数优选为2~40。下限例如,更优选为3以上,进一步优选为5以上,更进一步优选为8以上,尤其优选为10以上。上限更优选为35以下,进一步优选为30以下。烯基可以为直链、分支、环状中的任意一个。
[0150]
烷氧基的碳数优选为1~40。下限例如,更优选为3以上。上限例如,更优选为30以下,进一步优选为25以下。烷氧基可以为直链、分支、环状中的任意一个。
[0151]
芳基的碳数优选为6~20,更优选为6~12。芳基可以具有取代基,也可以未取代。作为取代基,可举出烷基、烷氧基、卤素原子等。关于这些详细内容,可举出前述取代基。
[0152]
杂芳基可以为单环,也可以为多环。构成杂芳基的杂原子的数量优选为1~3。构成杂芳基的杂原子为氮原子、优选为氧原子或硫原子。构成杂芳基的碳原子的数量优选为3~30,更优选为3~18,进一步优选为3~12,尤其优选为3~5。杂芳基优选为5元环或6元环。杂芳基可以具有取代基,也可以未取代。作为取代基,可举出烷基、烷氧基、卤素原子等。关于这些详细内容,可举出前述取代基。
[0153]
‑
br1r2基的r1与r2可以相互键合而形成环。例如,可举出由下述(b
‑
1)~(b
‑
4)表示的结构等。以下,r表示取代基,r
a1
~r
a4
分别独立地表示氢原子或取代基,m1~m3分别独立地表示0~4的整数,*表示式(i)中的键合位置。作为由r及r
a1
~r
a4
表示的取代基,可举出以r1及r2进行说明的取代基,优选为卤素原子及烷基。
[0154]
[化学式8]
[0155][0156]
作为b1及b2的具体例,可举出以下。以下,me表示甲基,bu表示丁基。*表示式(i)中的键合位置。
[0157]
[化学式9]
[0158][0159]
式(i)中,c1及c2分别独立地表示烷基、芳基或杂芳基。c1和c2可以为相同的基团,也可以为不同的基团。c1和c2优选为相同的基团。c1及c2分别独立地优选为芳基或杂芳基,更优选为芳基。
[0160]
烷基的碳数优选为1~40,更优选为1~30,尤其优选为1~25。烷基可以为直链、分支、环状中的任意一个,优选为直链或分支,尤其优选为分支。
[0161]
芳基优选为碳数6~20的芳基,更优选为碳数6~12的芳基。尤其优选为苯基或萘基。
[0162]
杂芳基可以为单环也可以为多环。构成杂芳基的杂原子的数量优选为1~3。构成杂芳基的杂原子优选为氮原子、氧原子或硫原子。构成杂芳基的碳原子的数量优选为3~30,更优选为3~18,进一步优选为3~12。
[0163]
上述的烷基、芳基及杂芳基可以具有取代基,也可以未取代。优选为具有取代基。并且,可以具有两个以上的取代基。例如,c1及c2为苯基的情况下,相对于吡咯并吡咯环可以在两处间位或邻位分别具有取代基,也可以仅在一处间位或邻位具有取代基。而且,可以在间位或邻位中的任一处和对位具有取代基。而且,可以在间位或邻位这两处和对位具有取代基。
[0164]
作为取代基,可举出可以含有氧原子的烃基、氨基、酰氨基、烷氧羰基氨基、芳氧羰基氨基、杂芳氧基羰基氨基、磺酰基氨基、氨磺酰基、氨基甲酰基、烷硫基、芳硫基、杂芳硫
基、烷基磺酰基、芳基磺酰基、杂芳基磺酰基、烷基亚磺酰基、芳基亚磺酰基、杂芳基亚磺酰基、脲基、磷酸酰氨基、巯基、磺酸基、羧基、硝基、羟肟酸基、亚磺酸基、肼基、亚氨基、甲硅烷基、羟基、卤素原子、氰基等。
[0165]
作为卤素原子,可举出氟原子、氯原子、溴原子、碘原子等。
[0166]
作为烃基,可举出烷基、烯基、芳基等。
[0167]
烷基的碳数优选为1~40。下限更优选为3以上,进一步优选为5以上,更进一步优选为8以上,尤其优选为10以上。上限更优选为35以下,进一步优选为30以下。烷基可以为直链、分支、环状中的任意一个,优选为直链或分支,尤其优选为分支。分支烷基的碳数优选为3~40。下限例如,更优选为5以上,进一步优选为8以上,更进一步优选为10以上。上限更优选为35以下,进一步优选为30以下。分支烷基的分支数例如,优选为2~10,更优选为2~8。
[0168]
烯基的碳数优选为2~40。下限例如,更优选为3以上,进一步优选为5以上,更进一步优选为8以上,尤其优选为10以上。上限更优选为35以下,进一步优选为30以下。烯基可以为直链、分支、环状中的任意一个,优选为直链或分支,尤其优选为分支。优选为分支烯基的碳数为3~40。下限例如更优选为5以上,进一步优选为8以上,更进一步优选为10以上。上限更优选为35以下,进一步优选为30以下。分支烯基的分支数优选为2~10,更优选为2~8。
[0169]
芳基的碳数优选为6~30,更优选为6~20,进一步优选为6~12。
[0170]
作为含有氧原子的烃基,可举出由
‑
l
‑
r
x1
表示的基团。
[0171]
l表示
‑
o
‑
、
‑
co
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
(or
x2
)
m
‑
或
‑
(r
x2
o)
m
‑
。r
x1
表示烷基、烯基或芳基。r
x2
表示伸烷基或伸芳基。m表示2以上的整数,m个r
x2
可以相同,也可以不同。
[0172]
l优选为
‑
o
‑
、
‑
(or
x2
)
m
‑
或
‑
(r
x2
o)
m
‑
,更优选为
‑
o
‑
。
[0173]
r
x1
所表示的烷基、烯基、芳基与上述者含义相同,优选范围也相同。r
x1
优选为烷基或烯基,更优选为烷基。
[0174]
r
x2
所表示的伸烷基的碳数优选为1~20,更优选为1~10,进一步优选为1~5。伸烷基可以为直链、分支、环状中的任意一个,优选为直链或分支。r
x2
所表示的伸芳基的碳数优选为6~20,更优选为6~12。r
x2
优选为伸烷基。
[0175]
m表示2以上的整数,优选为2~20,更优选为2~10。
[0176]
烷基、芳基及杂芳基可具有的取代基优选为具有分支烷基结构的基团。并且,取代基也可以优选为含有氧原子的烃基,更优选为含有氧原子的烃基。含有氧原子的烃基优选为由
‑
o
‑
r
x1
表示的基团。r
x1
优选为烷基或烯基,更优选为烷基,尤其优选为分支烷基。即,取代基优选为烷氧基,尤其优选为分支烷氧基。取代基为烷氧基,由此可轻松地得到耐热性及耐光性优异的膜。烷氧基的碳数优选为1~40。下限例如,更优选为3以上,进一步优选为5以上,更进一步优选为8以上,尤其优选为10以上。上限更优选为35以下,进一步优选为30以下。烷氧基可以为直链、分支、环状中的任意一个,优选为直链或分支,尤其优选为分支。分支烷氧基的碳数优选为3~40。下限例如,更优选为5以上,进一步优选为8以上,更进一步优选为10以上。上限更优选为35以下,进一步优选为30以下。分支烷氧基的分支数优选为2~10,更优选为2~8。
[0177]
作为c1及c2的具体例,可举出以下。以下,me表示甲基,bu表示丁基。*表示式(i)中的键合位置。而且,还能够优选使用以下结构的光学异构体。
[0178]
[化学式10]
[0179][0180]
[化学式11]
[0181][0182]
式(i)中,d1及d2分别独立地表示取代基。d1与d2可以为相同的基团,也可以为不同的基团。d1与d2优选为相同的基团。
[0183]
作为取代基,例如可举出烷基、烯基、芳基、杂芳基、烷氧基、芳氧基、杂芳氧基、酰基、烷氧羰基、芳氧羰基、杂芳氧基羰基、酰氧基、氨基、酰氨基、烷氧羰基氨基、芳氧羰基氨基、杂芳氧基羰基氨基、磺酰基氨基、氨磺酰基、氨基甲酰基、烷硫基、芳硫基、杂芳硫基、烷基磺酰基、芳基磺酰基、杂芳基磺酰基、烷基亚磺酰基、芳基亚磺酰基、杂芳基亚磺酰基、脲基、磷酸酰氨基、巯基、磺酸基、羧基、硝基、羟肟酸基、亚磺酸基、肼基、亚氨基、甲硅烷基、羟
基、卤素原子、氰基等。d1及d2优选为吸电子基团。
[0184]
hammett的σp值(sigma para value)为正的取代基作用为吸电子基团。本发明中,能够将hammett的σp值为0.2以上的取代基例示为吸电子基团。σp值优选为0.25以上,更优选为0.3以上,尤其优选为0.35以上。关于上限,并无特别限制,优选为0.80。作为吸电子基团的具体例,可举出氰基(σp值=0.66)、羧基(
‑
cooh:σp值=0.45)、烷氧羰基(例如,
‑
coome:σp值=0.45)、芳氧羰基(例如,
‑
cooph:σp值=0.44)、氨基甲酰基(例如,
‑
conh2:σp值=0.36)、烷基羰基(例如,
‑
come:σp值=0.50)、芳基羰基(例如,
‑
coph:σp值=0.43)、烷基磺酰基(例如,
‑
so2me:σp值=0.72)、芳基磺酰基(例如,
‑
so2ph:σp值=0.68)等。作为吸电子基团,优选为氰基、烷基羰基、烷基磺酰基及芳基磺酰基,更优选为氰基。在此,me表示甲基,ph表示苯基。关于hammett的σp值,能够参照日本特开2009
‑
263614号公报的0024~0025段,并将该内容并入本说明书中。
[0185]
作为d1及d2的具体例,可举出以下。*表示式(i)中的键合位置。
[0186]
[化学式12]
[0187][0188]
吡咯并吡咯化合物优选为由下述式(ii)表示的化合物或由下述式(iii)表示的化合物。根据该方式,能够制作出红外线屏蔽性及耐光性优异的膜。
[0189]
[化学式13]
[0190][0191]
式(ii)中,x1及x2分别独立地表示o、s、nr
x1
或cr
x2
r
x3
,r
x1
~r
x3
分别独立地表示氢原子或取代基,
[0192]
r3~r6分别独立地表示氢原子或取代基,
[0193]
r3与r4或r5与r6可以相互键合而形成环,
[0194]
b1及b2分别独立地表示
‑
br1r2基,r1及r2分别独立地表示取代基,r1与r2可以相互键合而形成环,
[0195]
c1及c2分别独立地表示烷基、芳基或杂芳基,
[0196]
d1及d2分别独立地表示取代基。
[0197]
式(ii)的b1、b2、c1、c2、d1及d2与式(i)的b1、b2、c1、c2、d1及d2含义相同,优选范围也相同。式(ii)的x1及x2与上述式(a
‑
1)的x1含义相同,优选范围也相同。式(ii)的r3~r6与上述式(a
‑
1)的r3及r4含义相同,优选范围也相同。
[0198]
式(iii)中,y1~y8分别独立地表示n或cr
y1
,y1~y4的至少两个为cr
y1
,y5~y8的至少两个为cr
y1
,r
y1
表示氢原子或取代基,相邻的r
y1
彼此可以相互键合而形成环,
[0199]
b1及b2分别独立地表示
‑
br1r2基,r1及r2分别独立地表示取代基,r1与r2可以相互键合而形成环,
[0200]
c1及c2分别独立地表示烷基、芳基或杂芳基,
[0201]
d1及d2分别独立地表示取代基。
[0202]
式(iii)的b1、b2、c1、c2、d1及d2与式(i)的b1、b2、c1、c2、d1及d2含义相同,优选范围也相同。式(iii)的y1~y8与上述式(a
‑
2)的y1~y4含义相同,优选范围也相同。
[0203]
作为吡咯并吡咯化合物的具体例,可举出下述化合物。以下表中的b1、b2结构、c1、c2结构中所记载的记号为上述的b1、b2、c1、c2的具体例中所示的基团。并且,作为吡咯并吡咯化合物的具体例,还可举出日本特开2009
‑
263614号公报的0049~0058段中所记载的化合物,并将该内容并入本说明书中。
[0204]
[表1]
[0205][0206]
[表2]
[0207][0208][0209]
[表3]
[0210][0211][0212]
[表4]
[0213][0214][0215]
[表5]
[0216][0217]
[0218]
[表6]
[0219][0220]
[0221]
[表7]
[0222]
[0223][0224]
[表8]
[0225]
[0226][0227]
[表9]
[0228]
[0229][0230]
[表10]
[0231][0232]
[0233]
[表11]
[0234][0235]
[表12]
[0236][0237]
[表13]
[0238]
[0239]
[表14]
[0240][0241]
[0242]
[表15]
[0243][0244]
[0245]
[表16]
[0246][0247]
[0248]
[表17]
[0249][0250]
[表18]
[0251][0252]
[表19]
[0253]
[0254]
[表20]
[0255][0256]
[表21]
[0257][0258]
[表22]
[0259][0260]
[表23]
[0261][0262]
[表24]
[0263][0264]
[表25]
[0265][0266]
[表26]
[0267][0268]
[表27]
[0269][0270]
[表28]
[0271][0272]
[表29]
[0273][0274]
[表30]
[0275][0276][0277]
[表31]
[0278][0279][0280]
[表32]
[0281][0282][0283]
[表33]
[0284][0285][0286]
[表34]
[0287][0288][0289]
[表35]
[0290][0291][0292]
[表36]
[0293][0294]
[表37]
[0295][0296]
[表38]
[0297][0298]
[表39]
[0299][0300]
[表40]
[0301][0302]
[表41]
[0303][0304]
[表42]
[0305][0306]
[表43]
[0307][0308]
[表44]
[0309][0310]
[表45]
[0311][0312]
[表46]
[0313][0314]
[表47]
[0315][0316]
[表48]
[0317][0318]
[表49]
[0319]
[0320][0321]
[表50]
[0322][0323][0324]
[表51]
[0325][0326][0327]
[表52]
[0328][0329]
[表53]
[0330][0331]
[表54]
[0332]
[0333][0334]
(方酸化合物)
[0335]
用作近红外线吸收化合物a的方酸化合物优选为由式(sq)表示的化合物。
[0336]
[化学式14]
[0337][0338]
式中,a1及a2分别独立地表示芳基、杂芳基或由下述式(2)表示的基团,
[0339]
[化学式15]
[0340][0341]
式(2)中,z1表示形成含氮杂环的非金属原子团,r2表示烷基、烯基或芳烷基,d表示0或1,波线表示与式(sq)中的4元环的连接键。
[0342]
式(sq)中的a1及a2分别独立地表示芳基、杂芳基或由式(2)表示的基团,优选为由式(2)表示的基团。
[0343]
a1及a2所表示的芳基的碳数优选为6~48,更优选为6~24,尤其优选为6~12。作为具体例,可举出苯基、萘基等。另外,芳基具有取代基的情况下的上述芳基的碳数表示去除取代基的碳数之后的数量。
[0344]
作为a1及a2所表示的杂芳基,优选为5元环或6元环。并且,杂芳基优选为单环或稠
环,单环或稠合数更优选为2~8的稠环,单环或稠合数进一步优选为2~4的稠环,单环或稠合数尤其优选为2或3的稠环。作为杂芳基中所包含的杂原子,例示出氮原子、氧原子、硫原子,优选为氮原子、硫原子。杂原子的数量优选为1~3,更优选为1~2。具体而言,可举出从含有氮原子、氧原子及硫原子中的至少一个的5元环或6元环等的单环、多环芳香族环衍生的杂芳基等。
[0345]
芳基及杂芳基可以具有取代基。芳基及杂芳基具有两个以上的取代基的情况下,复数个取代基可以相同,也可以不同。
[0346]
作为取代基,可举出卤素原子、氰基、硝基、烷基、烯基、炔基、芳基、杂芳基、芳烷基、
‑
or
10
、
‑
cor
11
、
‑
coor
12
、
‑
ocor
13
、
‑
nr
14
r
15
、
‑
nhcor
16
、
‑
conr
17
r
18
、
‑
nhconr
19
r
20
、
‑
nhcoor
21
、
‑
sr
22
、
‑
so2r
23
、
‑
so2or
24
、
‑
nhso2r
25
或
‑
so2nr
26
r
27
。r
10
~r
27
分别独立地表示氢原子、烷基、烯基、炔基、芳基、杂芳基或芳烷基。另外,
‑
coor
12
的r
12
为氢的情况(即,羧基)下,氢原子可以解离(即,碳酸盐基),也可以为盐的状态。并且,
‑
so2or
24
的r
24
为氢原子的情况(即,磺酸基)下,氢原子可以解离(即,磺酸盐基),也可以为盐的状态。
[0347]
作为卤素原子,可举出氟原子、氯原子、溴原子、碘原子。
[0348]
烷基的碳数优选为1~20,更优选为1~15,进一步优选为1~8。烷基可以为直链、分支、环状中的任意一个,优选为直链或分支。
[0349]
烯基的碳数优选为2~20,更优选为2~12,尤其优选为2~8。烯基可以为直链、分支、环状中的任意一个,优选为直链或分支。
[0350]
炔基的碳数优选为2~40,更优选为2~30,尤其优选为2~25。炔基可以为直链、分支、环状中的任意一个,优选为直链或分支。
[0351]
芳基的碳数优选为6~30,更优选为6~20,进一步优选为6~12。
[0352]
芳烷基的烷基部分与上述烷基相同。芳烷基的芳基部分与上述芳基相同。芳烷基的碳数优选为7~40,更优选为7~30,进一步优选为7~25。
[0353]
杂芳基优选为单环或稠环,单环或稠合数更优选为2~8的稠环,单环或稠合数进一步优选为2~4的稠环。构成杂芳基的环的杂原子的数量优选为1~3。构成杂芳基的环的杂原子为氮原子、优选为氧原子或硫原子。杂芳基优选为5元环或6元环。构成杂芳基的环的碳原子的数量优选为3~30,更优选为3~18,进一步优选为3~12。
[0354]
烷基、烯基、炔基、芳烷基、芳基及杂芳基可以具有取代基,也可以未取代。作为取代基,可举出上述的取代基。
[0355]
接着,对a1及a2所表示的由式(2)表示的基团进行说明。
[0356]
式(2)中,r2表示烷基、烯基或芳烷基,优选为烷基。
[0357]
烷基的碳数优选为1~30,更优选为1~20,进一步优选为1~12,尤其优选为2~8。
[0358]
烯基的碳数优选为2~30,更优选为2~20,进一步优选为2~12。
[0359]
烷基及烯基可以为直链、分支、环状的任意一个,优选为直链或分支。
[0360]
芳烷基的碳数优选为7~30,更优选为7~20。
[0361]
式(2)中,作为由z1而形成的含氮杂环,优选为5元环或6元环。并且,含氮杂环优选为单环或稠环,单环或稠合数更优选为2~8的稠环,单环或稠合数进一步优选为2~4的稠环,稠合数尤其优选为2或3的稠环。除了氮原子以外,含氮杂环还可以含有硫原子。而且,含氮杂环也可以具有取代基。作为取代基,可举出上述的取代基。例如,优选为卤素原子、烷
基、羟基、氨基、酰氨基,更优选为卤素原子及烷基。优选为卤素原子为氯原子。烷基的碳数优选为1~30,更优选1~20,进一步优选为1~12。烷基优选为直链或分支。
[0362]
由式(2)表示的基团优选为由下述式(3)或式(4)表示的基团。
[0363]
[化学式16]
[0364][0365]
式(3)及式(4)中,r
11
表示烷基、烯基或芳烷基,r
12
表示取代基。m表示0~4的整数,m为2以上的情况下,r
12
彼此可以连结而形成环。x表示氮原子或cr
13
r
14
,r
13
及r
14
分别独立地表示氢原子或取代基。波线表示与式(sq)中的4元环的连接键。
[0366]
式(3)及式(4)中的r
11
与式(2)中的r2含义相同,优选范围也相同。
[0367]
式(3)及式(4)中的r
12
表示取代基。作为取代基,可举出以上述式(sq)进行说明的取代基。例如,优选为卤素原子、烷基、羟基、氨基、酰氨基,更优选为卤素原子、烷基。卤素原子优选为氯原子。烷基的碳数优选为1~30,更优选为1~20,进一步优选为1~12。烷基优选为直链或分支。
[0368]
m为2以上的情况下,r
12
彼此可以连结而形成环。作为环,可举出脂环(非芳香性烃环)、芳香环、杂环等。环可以为单环,也可以为多环。作为取代基彼此连结而形成环的情况下的连结基,能够由选自包含
‑
co
‑
、
‑
o
‑
、
‑
nh
‑
、2价脂肪族基、2价芳香族基及它们的组合的群组中的2价连结基而连结。例如,r
12
优选为彼此连接而形成苯环。
[0369]
式(3)中的x表示氮原子或cr
13
r
14
,r
13
及r
14
分别独立地表示氢原子或取代基。作为取代基,可举出以上述式(sq)进行说明的取代基。例如,可举出烷基等。烷基的碳数优选为1~20,更优选为1~10,进一步优选为1~5,尤其优选为1~3,最优选为1。烷基优选为直链或分支,尤其优选为直链。
[0370]
m表示0~4的整数,优选为0~2。
[0371]
另外,式(sq)中,阳离子如下以非定域化的方式存在。
[0372]
[化学式17]
[0373]
[0374]
用作近红外线吸收化合物a的方酸化合物优选为由式(sq
‑
1)表示的化合物。
[0375]
式(sq
‑
1)
[0376]
[化学式18]
[0377][0378]
式(sq
‑
1)中,环a及环b分别独立地表示芳香族环,
[0379]
x
a
及x
b
分别独立地表示取代基,
[0380]
g
a
及g
b
分别独立地表示取代基,
[0381]
ka表示0~na的整数,kb表示0~nb的整数,
[0382]
na表示可取代为环a的最大的整数,nb表示可取代为环b的最大的整数,
[0383]
x
a
与g
a
、x
b
与g
b
可以相互键合而形成环,g
a
及g
b
分别存在复数个的情况下,可以相互键合而形成环。
[0384]
式(sq
‑
1)中,g
a
及g
b
分别独立地表示取代基。
[0385]
作为取代基,可举出卤素原子、氰基、硝基、烷基、烯基、炔基、芳烷基、芳基、杂芳基、
‑
orc1、
‑
corc2、
‑
coor
c3
、
‑
ocor
c4
、
‑
nr
c5
r
c6
、
‑
nhcor
c7
、
‑
conr
c8
r
c9
、
‑
nhconrc
10
rc
11
、
‑
nhcoorc
12
、
‑
src
13
、
‑
so2rc
14
、
‑
so2orc
15
、
‑
nhso2rc
16
或
‑
so2nrc
17
rc
18
。rc1~rc
18
分别独立地表示氢原子、烷基、烯基、炔基、芳基或杂芳基。另外,
‑
coor
c3
的r
c3
为氢原子的情况(即,羧基)下,氢原子可以解离(即,碳酸盐基),也可以为盐的状态。而且,
‑
so2orc
15
的rc
15
为氢原子的情况(即,磺酸基)下,氢原子可以解离(即,磺酸盐基),也可以为盐的状态。
[0386]
作为卤素原子,可举出氟原子、氯原子、溴原子、碘原子。
[0387]
烷基的碳数优选为1~20,更优选为1~12,尤其优选为1~8。烷基可以为直链、分支、环状中的任意一个。烷基可以未取代,也可以具有取代基。
[0388]
烯基的碳数优选为2~20,更优选为2~12,尤其优选为2~8。烯基可以为直链、分支、环状中的任意一个。
[0389]
炔基的碳数优选为2~20,更优选为2~12,尤其优选为2~8。炔基可以为直链、分支、环状中的任意一个。
[0390]
芳基的碳数优选为6~25,更优选为6~15,最优选为6~10。
[0391]
芳烷基的烷基部分与上述烷基相同。芳烷基的芳基部分与上述芳基相同。芳烷基的碳数优选7~40,更优选为7~30,进一步优选为7~25。
[0392]
杂芳基优选为单环或稠环,单环或稠合数更优选为2~8的稠环,单环或稠合数进一步优选为2~4的稠环。构成杂芳基的环的杂原子的数量优选为1~3。构成杂芳基的环的杂原子优选为氮原子、氧原子或硫原子。杂芳基优选为5元环或6元环。构成杂芳基的环的碳原子的数量优选为3~30,更优选为3~18,进一步优选为3~12。
[0393]
烷基、烯基、炔基、芳烷基、芳基及杂芳基可以具有取代基,也可以未取代。作为取代基,可举出上述的以g
a
及g
b
例举的取代基,例如,可举出卤素原子、羟基、羧基、磺酸基、烷氧基、氨基等。
[0394]
式(sq
‑
1)中,x
a
及x
b
分别独立地表示取代基。取代基优选为具有活性氢的基团,优选为
‑
oh、
‑
sh、
‑
cooh、
‑
so3h、
‑
nhr
x1
、
‑
nr
x1
r
x2
、
‑
nhcor
x1
、
‑
conr
x1
r
x2
、
‑
nhconr
x1
r
x2
、
‑
nhcoor
x1
、
‑
nhso2r
x1
、
‑
b(oh)2、
‑
po(oh)3及
‑
nhbr
x1
r
x2
,更优选为
‑
oh、
‑
nhcor
x1
、
‑
nhconr
x1
r
x2
、
‑
nhcoor
x1
、
‑
nhso2r
x1
及
‑
nhbr
x1
r
x2
。
[0395]
r
x1
及r
x2
分别独立地表示取代基。作为取代基,可举出烷基、芳基等,优选为烷基。烷基的碳数优选为1~20,更优选为1~15,进一步优选为1~8,尤其优选为1~5。烷基可以为直链、分支、环状中的任意一个,优选为直链或分支。芳基的碳数优选为6~30,更优选为6~20,进一步优选为6~12。烷基及芳基可以具有取代基,也可以未取代,优选为具有取代基。作为取代基,可举出上述的以g
a
及g
b
例举的取代基。例如,可举出卤素原子、芳基、烷氧基等。
[0396]
式(sq
‑
1)中,环a及环b分别独立地表示芳香族环。芳香族环可以为单环,也可以为稠环。芳香族环可以为芳香族烃环,也可以为芳香族杂环。作为芳香族环的具体例,可举出苯环、萘环、并环戊二烯(pentalene)环、茚环、薁环、庚搭烯(heptalene)环、茚烯(indacene)环、苝环、稠五苯(pentacene)环、苊烯环、菲环、蒽环、稠四苯环、(chrysene)环、联伸三苯环、茀环、联苯环、吡咯环、呋喃环、噻吩环、咪唑环、噁唑环、噻唑环、吡啶环、吡嗪环、嘧啶环、哒嗪环、吲哚嗪环、吲哚环、苯并呋喃环、苯并噻吩环、异苯并呋喃环、喹嗪(quinolizine)环、喹啉环、酞嗪环、萘啶(naphthyridine)环、喹噁啉环、喹噁唑啉环、异喹啉环、咔唑环、啡啶环、吖啶环、啡啉环、噻嗯环、色烯环、呫吨环、啡噁噻环、啡噻嗪环及啡嗪环,优选为苯环或萘环,更优选为萘环。
[0397]
芳香族环可以未取代,也可以具有取代基。作为取代基,可举出以g
a
及g
b
进行说明的取代基。
[0398]
式(sq
‑
1)中,x
a
与g
a
、x
b
与g
b
可以相互键合而形成环,g
a
及g
b
分别存在复数个的情况下,g
a
彼此或g
b
彼此可以相互键合而形成环。作为环,优选为5元环或6元环。环可以为单环,也可以为多环。x
a
与g
a
、x
b
与g
b
、g
a
彼此或g
b
彼此键合而形成环的情况下,它们可以直接键合而形成环,也可以经由选自包含伸烷基、
‑
co
‑
、
‑
o
‑
、
‑
nh
‑
、
‑
br
‑
及它们的组合的组中的2价连结基键合而形成环。x
a
与g
a
、x
b
与g
b
、g
a
彼此或g
b
彼此优选经由
‑
br
‑
键合而形成环。r表示氢原子或取代基。作为取代基,可举出烷基、烯基、炔基、芳基或杂芳基。关于烷基、烯基、炔基、芳基及杂芳基的详细内容,与以g
a
及g
b
进行说明的范围含义相同。
[0399]
式(sq
‑
1)中,ka表示0~na的整数,kb表示0~nb的整数,na表示可取代为环a的最大的整数,nb表示可取代为环b的最大的整数。ka及kb分别独立地优选为0~4,0~2,尤其优选为0~1。
[0400]
方酸化合物优选为由下述式(sq
‑
a)表示的化合物。该化合物的耐热性及耐光性优异。
[0401]
式(sq
‑
a)
[0402]
[化学式19]
[0403][0404]
式中,r1及r2分别独立地表示烷基、烯基、芳基或杂芳基,
[0405]
r3及r4分别独立地表示氢原子或烷基,
[0406]
x1及x2分别独立地表示氧原子或
‑
n(r5)
‑
,
[0407]
r5表示氢原子、烷基、芳基或杂芳基,
[0408]
y1~y4分别独立地表示取代基,y1与y2及y3与y4可以相互键合而形成环,
[0409]
y1~y4分别存在复数个的情况下,可以相互键合而形成环,
[0410]
p及s分别独立地表示0~3的整数,
[0411]
q及r分别独立地表示0~2的整数。
[0412]
式(sq
‑
a)中,r1及r2所表示的烷基的碳数优选为1~40。下限更优选为3以上,进一步优选为5以上,更进一步优选为10以上,尤其优选为13以上。上限更优选为35以下,进一步优选为30以下。烷基可以为直链、分支、环状中的任意一个,优选为直链或分支,尤其优选为分支。分支烷基的分支数例如,优选为2~10,更优选为2~8。
[0413]
r1及r2所表示的烯基的碳数优选为2~40。下限例如,更优选为3以上,进一步优选为5以上,更进一步优选为8以上,尤其优选为10以上。上限优选为35以下,进一步优选为30以下。烯基优选为直链或分支,尤其优选为分支。分支烯基的分支数优选为2~10,更优选为2~8。
[0414]
r1及r2所表示的芳基的碳数优选为6~30,更优选为6~20,进一步优选为6~12。
[0415]
r1及r2所表示的杂芳基可以为单环也可以为多环。构成杂芳基的环的杂原子的数量优选为1~3。构成杂芳基的环的杂原子优选为氮原子、氧原子或硫原子。构成杂芳基的环的碳原子的数量优选为3~30,更优选为3~18,进一步优选为3~12。
[0416]
r1及r2所表示的烷基、烯基、芳基及杂芳基可以未取代,也可以具有取代基。作为取代基,可举出以上述的g
a
及g
b
进行说明的取代基,优选为烷氧基。
[0417]
式(sq
‑
a)中,r3及r4分别独立地表示氢原子或烷基。r3与r4可以相同,也可以为不同的基团。r3与r4优选为相同的基团。r3及r4所表示的烷基的碳数优选为1~20,更优选为1~10,进一步优选为1~4,尤其优选为1~2。烷基可以为直链、分支中的任意一个。r3及r4优选为分别独立地表示氢原子、甲基或乙基,更优选为氢原子或甲基,尤其优选为氢原子。
[0418]
式(sq
‑
a)中,x1及x2分别独立地表示氧原子或
‑
n(r5)
‑
。x1与x2可以相同,也可以不同,优选为相同。
[0419]
r5优选为表示氢原子、烷基、芳基或杂芳基,氢原子、烷基或芳基。r5所表示的烷基、
芳基及杂芳基的详细内容与以r3及r4进行说明的范围相同。r5所表示的烷基、芳基及杂芳基可以未取代,也可以具有取代基。作为取代基,可举出上述的以g
a
及g
b
进行说明的取代基。
[0420]
式(sq
‑
a)中,y1~y4分别独立地表示取代基。作为取代基,可举出以上述的g
a
及g
b
进行说明的取代基。
[0421]
式(sq
‑
a)中,y1与y2及y3与y4可以相互键合而形成环。例如,y1与y2相互键合并与直接连结到y1及y2的萘环的组合,由此例如可成为乙烷合萘(acenaphthene)环、苊烯环等3环等。
[0422]
y1~y4分别存在复数个的情况下,可以相互键合而形成环结构。例如,当y1存在复数个的情况下,y1彼此相互键合并与直接连结y1及y2的萘环组合,由此例如可成为蒽环、菲环等3环等。另外,y1彼此相互键合而形成环结构的情况下,作为y1以外的取代基的y2~y4无需存在复数个。而且,y2~y4还可以不存在。y2彼此、y3彼此及y4彼此键合而形成环结构的情况下也相同。
[0423]
p及s分别独立地表示0~3的整数,分别优选为0~1,尤其优选为0。
[0424]
q及r分别独立地表示0~2的整数,分别优选为0~1,尤其优选为0。
[0425]
作为方酸化合物的具体例,可举出以下所示的化合物。并且,可举出日本特开2011
‑
208101号公报的0044~0049段中所记载的化合物,并将该内容并入本说明书中。
[0426]
[化学式20]
[0427][0428]
(花青化合物)
[0429]
用作近红外线吸收化合物a的花青化合物优选为由式(c)表示的化合物。
[0430]
式(c)
[0431]
[化学式21]
[0432][0433]
式(c)中,z1及z2分别独立地为可以稠环的形成5员或6员的含氮杂环的非金属原子团,
[0434]
r
101
及r
102
分别独立地表示烷基、烯基、炔基、芳烷基或芳基,
[0435]
l1表示具有奇数个次甲基的次甲基链,
[0436]
a及b分别独立地为0或1,
[0437]
a为0的情况下,碳原子与氮原子以双键键合,b为0的情况下,碳原子与氮原子以单键键合,
[0438]
式中的由cy表示的部位为阳离子部的情况下,x1表示阴离子,c表示使电荷平衡时所需的数,式中由cy表示的部位为阴离子部的情况下,x1表示阳离子,c表示电荷平衡时所需的数,式中以cy表示的部位的电荷在分子内中和的情况下,c为0。
[0439]
式(c)中,z1及z2分别独立地表示可以稠环的形成5员或6员的含氮杂环的非金属原子团。含氮杂环中,可以稠合其他杂环、芳香族环或脂肪族环。含氮杂环优选为5元环。进一步优选5员的含氮杂环中稠合有苯环或萘环的结构。作为含氮杂环的具体例,可举出噁唑环、异噁唑环、苯并噁唑环、萘并恶唑环、噁唑并咔唑(oxazolo carbazole)环、噁唑并二苯并呋喃环、噻唑环、苯并噻唑环、萘并噻唑环、假吲哚环、苯并假吲哚环、咪唑环,苯并咪唑环、萘并咪唑环、喹啉环、吡啶环、吡咯并吡啶环、呋喃并吡咯环,吲哚嗪环,咪唑并喹噁啉环,喹噁啉环等,优选为喹啉环、假吲哚环、苯并假吲哚环、苯并噁唑环、苯并噻唑环、苯并咪唑环,尤其优选为假吲哚环、苯并噻唑环、苯并咪唑环。含氮杂环及与其稠合的环可以具有取代基。作为取代基,可举出以式(sq)进行说明的取代基。
[0440]
式(c)中,r
101
及r
102
分别独立地表示烷基、烯基、炔基、芳烷基或芳基。
[0441]
烷基的碳数优选为1~20,更优选为1~12,尤其优选为1~8。烷基可以为直链、分支、环状中的任意一个。
[0442]
烯基的碳数优选为2~20,更优选为2~12,尤其优选为2~8。烯基可以为直链、分支、环状中的任意一个。
[0443]
炔基的碳数优选为2~20,更优选为2~12,尤其优选为2~8。炔基可以为直链、分支、环状中的任意一个。
[0444]
芳基的碳数优选为6~25,更优选为6~15,最优选为6~10。芳基可以未取代,也可以具有取代基。
[0445]
芳烷基的烷基部分与上述烷基相同。芳烷基的芳基部分与上述芳基相同。芳烷基的碳数优选为7~40,更优选为7~30,进一步优选为7~25。
[0446]
烷基、烯基、炔基、芳烷基及芳基可以具有取代基,也可以未取代。作为取代基,可
举出卤素原子、羟基、羧基、磺酸基、烷氧基、氨基等,优选为羧基及磺酸基,尤其优选为磺酸基。羧基及磺酸基中,氢原子可以解离,也可以为盐的状态。
[0447]
式(c)中,l1表示具有奇数个次甲基的次甲基链。l1优选为具有3、5或7个次甲基的次甲基链。
[0448]
次甲基可以具有取代基。具有取代基的次甲基优选为中央的(中位的)次甲基。作为取代基的具体例,可举出可以具有z1及z2的含氮杂环的取代基及以式(a)表示的基团等。而且,可以由次甲基链的两个取代基键合而形成5或6元环。
[0449]
[化学式22]
[0450][0451]
式(a)中,*表示与次甲基链的连结部,a1表示氧原子或硫原子。
[0452]
式(c)中,a及b分别独立地为0或1。a为0的情况下,碳原子与氮原子以双键键合,b为0的情况下,碳原子与氮原子以单键键合。a与b均为0为较佳。另外,a与b均为0的情况下,式(c)表示为如下。
[0453]
[化学式23]
[0454][0455]
式(c)中,式中的以cy表示的部位为阳离子部的情况下,x1表示阴离子,c表示使电荷平衡时所需的数。作为阴离子的例,可举出卤素离子(cl
‑
、br
‑
、i
‑
)、对甲苯磺酸离子、乙基硫酸离子、pf6‑
、bf4‑
或clo4‑
、三(卤代烷磺酰基)甲基化物阴离子(例如,(cf3so2)3c
‑
)、二(卤代烷磺酰基)亚氨阴离子(例如(cf3so2)2n
‑
)、四氰基硼酸阴离子等。
[0456]
式(c)中,式中的以cy表示的部位为阴离子部的情况下,x1表示阳离子,c表示使电荷平衡时所需的数。作为阳离子,可举出碱金属离子(li
、na
、k
等)、碱土类金属离子(mg
2
、ca
2
、ba
2
、sr
2
等)、过渡金属离子(ag
、fe
2
、co
2
、ni
2
、cu
2
、zn
2
等)、其他金属离子(al
3
等)、铵离子、三乙基铵离子、三丁基铵离子、吡啶鎓离子、四丁基铵离子、鈲离子、四甲基胍离子、二氮杂双环十一碳烯等。作为阳离子,优选为na
、k
、mg
2
、ca
2
、zn
2
、二氮杂双环十一碳烯。
[0457]
式(c)中,式中的以cy表示的部位的电荷在分子内中和的情况下,不存在x1。即,c为0。
[0458]
花青化合物也优选为由下述(c
‑
1)~(c
‑
3)表示的化合物。
[0459]
[化学式24]
[0460][0461]
式中,r
1a
、r
2a
、r
1b
及r
2b
分别独立地表示烷基、烯基、炔基、芳烷基或芳基,
[0462]
l
1a
及l
1b
分别独立地表示具有奇数个次甲基的次甲基链,
[0463]
y1及y2分别独立地表示
‑
s
‑
、
‑
o
‑
、
‑
nr
x1
‑
或
‑
cr
x2
r
x3
‑
,
[0464]
r
x1
、r
x2
及r
x3
分别独立地表示氢原子或烷基,
[0465]
v
1a
、v
2a
、v
1b
及v
2b
分别独立地表示取代基,
[0466]
m1及m2分别独立地表示0~4,
[0467]
式中的以cy表示的部位为阳离子部的情况下,x1表示阴离子,c表示使电荷平衡时所需的数,
[0468]
式中的以cy表示的部位为阴离子部的情况下,x1表示阳离子,c表示使电荷平衡时所需的数,
[0469]
式中的以cy表示的部位的电荷在分子内中和的情况下,不存在x1。
[0470]
r
1a
、r
2a
、r
1b
及r
2b
所表示的基团与以式(c)的r
101
及r
102
进行说明的烷基、烯基、炔基、
芳烷基及芳基含义相同,优选范围也相同。这些基团可以未取代,也可以具有取代基。作为取代基,可举出卤素原子、羟基、羧基、磺酸基、烷氧基、氨基等,优选为羧基及磺酸基,尤其优选为磺酸基。羧基及磺酸基中,氢原子可以解离,也可以为盐的状态。r
1a
、r
2a
、r
1b
及r
2b
表示烷基的情况下,更优选为直链烷基。
[0471]
y1及y2优选为分别独立地表示
‑
s
‑
、
‑
o
‑
、
‑
nr
x1
‑
或
‑
cr
x2
r
x3
‑
,
‑
nr
x1
‑
。r
x1
、r
x2
及r
x3
分别独立地表示氢原子或烷基,优选为烷基。烷基的碳数优选为1~10,更优选为1~5,尤其优选为1~3。烷基可以为直链、分支、环状中的任意一个,优选为直链或分支,尤其优选为直链。烷基尤其优选为甲基或乙基。
[0472]
l
1a
及l
1b
与式(c)的l1含义相同,优选范围也相同。
[0473]
关于v
1a
、v
2a
、v
1b
及v
2b
所表示的取代基,可举出以式(sq)进行说明的取代基,优选范围也相同。
[0474]
m1及m2优选为分别独立地表示0~4,0~2。
[0475]
x1所表示的阴离子及阳离子与以式(c)的x1进行说明的范围含义相同,优选范围也相同。
[0476]
作为花青化合物的具体例,可举出以下所示的化合物。而且,可举出日本特开2015
‑
172004号公报及日本特开2015
‑
172102号公报中所记载的化合物。
[0477]
[化学式25]
[0478][0479]
[化学式26]
[0480][0481]
<<其他近红外线吸收化合物>>
[0482]
组合物可以进一步包含上述的近红外线吸收化合物a以外的近红外线吸收化合物(还称为其他近红外线吸收化合物)。
[0483]
作为其他近红外线吸收化合物,例如可举出铜化合物、花青化合物、方酸化合物、酞菁化合物、萘酞菁化合物、萘嵌苯(rylene)化合物、部花青化合物、克酮鎓化合物、氧杂菁
化合物、二亚铵化合物、二硫酚化合物、三芳甲烷化合物、吡咯亚甲基化合物、甲亚氨化合物、蒽醌化合物及二苯并呋喃酮化合物等。
[0484]
铜化合物优选为铜络合物。铜络合物能够使用由式(cu
‑
1)表示的铜络合物。该铜络合物为在中心金属的铜配位有配位子l的铜化合物,铜通常为2价铜。例如能够由对铜成分混合成为配位子l的化合物或其盐或使该些进行反应等而得到。
[0485]
cu(l)
n1
·
(x)
n2
……
式(cu
‑
1)
[0486]
上述式中,l表示配位于铜的配位子,x表示相对离子。n1表示1~4的整数。n2表示0~4的整数。
[0487]
x表示相对离子。除了不具有电荷的中性络合物以外,铜化合物有时还成为阳离子络合物、阴离子络合物。该情况下,根据需要而存在相对离子,以使中和铜化合物的电荷。
[0488]
相对离子为负的相对离子(相对阴离子)的情况下,例如,可以为无机阴离子也可以为有机阴离子。作为具体例,可举出氢氧化物离子、卤素阴离子(例如,氟化物离子、氯化物离子、溴化物离子、碘化物离子等)、取代或未取代的烷基羧酸离子(乙酸离子、三氟乙酸离子等)、取代或未取代的芳基羧酸离子(苯甲酸离子等)、取代或未取代的烷基磺酸离子(甲磺酸离子、三氟甲磺酸离子等)、取代或未取代的芳基磺酸离子(例如对甲苯磺酸离子、对氯苯磺酸离子等)、芳基二磺酸离子(例如1,3
‑
苯二磺酸离子、1,5
‑
萘二磺酸离子、2,6
‑
萘二磺酸离子等)、烷基硫酸离子(例如甲基硫酸离子等)、硫酸离子、硫氰酸离子、硝酸离子、高氯酸离子、四氟硼酸离子、四芳基硼酸离子、四(五氟苯基)硼酸离子(b
‑
(c6f5)4)、六氟磷酸离子、苦味酸离子、酰氨离子(包含被酰基或磺酰基取代的酰氨)、甲基化物离子(包含被酰基或磺酰基取代的甲基化物),优选为卤素阴离子、取代或未取代的烷基羧酸离子、硫酸离子、硝酸离子、四氟硼酸离子、四芳基硼酸离子、六氟磷酸离子、酰氨离子(包含被酰基或磺酰基取代的酰氨)、甲基化物离子(包含被酰基或磺酰基取代的甲基化物离子)。
[0489]
相对阴离子优选为低亲核阴离子。低亲核阴离子通常被称为超强酸(super acid)的pka较低的酸解离质子而成的阴离子。关于超强酸的定义,根据文献而不同,为pka比甲磺酸低的酸的总称,已知有j.org.chem.2011,76,391
‑
395equilibrium acidities of super acids中所记载的结构。低亲核阴离子的pka例如,优选为
‑
11以下,更优选为
‑
11~
‑
18。pka例如能够通过j.org.chem.2011,76,391
‑
395中所记载的方法来测定。本说明书中的pka值在并无特别说明的情况下,为1,2
‑
二氯乙烷中的pka。
[0490]
低亲核阴离子更优选为四氟硼酸离子、四芳基硼酸离子(作为烷基,包含具有被卤素原子或全氟烷基取代的芳基的四芳基硼酸离子)、六氟磷酸离子、酰亚氨离子(包含被酰基或磺酰基取代的酰亚氨)、甲基化物离子(包含被酰基或磺酰基取代的甲基化物离子),尤其优选为四芳基硼酸离子、酰亚氨离子、甲基化物离子。
[0491]
相对离子为正的相对离子(相对阳离子)的情况下,例如可举出无机或有机铵离子(例如,四丁基铵离子等四烷基铵离子、三乙基苄基铵离子、吡啶离子等)、鏻离子(例如,四丁基鏻离子等四烷基鏻离子、烷基三苯鏻离子、三乙基苯鏻离子等)、碱金属离子或质子。
[0492]
而且,相对离子可以为金属络合物离子,尤其相对离子可以为铜络合物、即,阳离子性铜络合物和阴离子性铜络合物的盐。
[0493]
配位子l为针对铜具有配位部位的化合物,可举出具有选自针对铜以阴离子配位的配位部位及针对铜以非共用电子对配位的配位原子中的一种以上的化合物。以阴离子配
位的配位部位可以解离,也可以为非解离。配位子l优选为具有两个以上的相对于铜的配位部位的化合物(多牙配位子)。并且,配位子l中,为了提高可见透明性,优选芳香族等π共轭系并不连续性地键合有复数个。配位子l还能够并用具有一个针对铜的配位部位的化合物(单牙配位子)和具有两个以上的针对铜的配位部位的化合物(多牙配位子)。作为单座配位子,可举出以阴离子或非共用电子对配位的单牙配位子。作为以阴离子配位的配位子,可举出卤化物阴离子、羟化物阴离子、烷氧化物阴离子、苯氧化物阴离子、酰氨阴离子(包含被酰基或磺酰基取代的酰氨)、酰亚氨阴离子(包含被酰基或磺酰基取代的酰亚氨)、苯氨阴离子(包含被酰基或磺酰基取代的苯氨)、硫醇盐阴离子、碳酸氢阴离子、羧酸阴离子、硫羧酸阴离子、二硫羧酸阴离子、硫酸氢阴离子、磺酸阴离子、磷酸二氢阴离子、磷酸二酯阴离子、膦酸单酯阴离子、膦酸氢阴离子、次膦酸阴离子、含氮杂环阴离子、硝酸阴离子、次氯酸阴离子、氰化物阴离子、氰酸盐阴离子、异氰酸盐阴离子、硫氰酸盐阴离子、异硫氰酸盐阴离子、叠氮化物阴离子等。作为以非共用电子对配位的单座配位子,可举出水、醇、苯酚、酯、氨、苯氨、酰氨、酰亚氨、亚氨、腈、异腈、硫醇、硫醚、羰基化合物、硫羰基化合物、亚砜、杂环或碳酸、羧酸、硫酸、磺酸、磷酸、膦酸、次膦酸、硝酸或其酯。
[0494]
铜络合物中,作为配位子优选具有如下化合物,即至少具有两个配位部位的化合物(以下,还称为化合物(a))。化合物(a)更优选至少具有3个配位部位,进一步优选具有3~5个。化合物(a)相对于铜成分,作为螯合配位子而发挥作用。即,可认为由化合物(a)所具有的至少两个配位原子与铜螯合配位,铜络合物的结构歪斜,并得到可见区域的较高的透射性,能够提高红外线的吸光能力,色价也得到提高。铜络合物可以具有两个以上的化合物(a)。具有两个以上的化合物(a)的情况下,各自的化合物(a)可以相同,也可以不同。作为化合物(a)所具有的配位部位,可举出以阴离子配位的配位部位、以非共用电子对配位的配位部位。铜络合物中,例示了4配位、5配位及6配位,更优选为4配位及5配位,进一步优选为5配位。而且,铜络合物优选由铜和配位子而形成5元环和/或6元环。这种铜络合物的形状稳定,络合物的稳定性优异。
[0495]
铜络合物能够通过对例如铜成分(铜或包含铜的化合物)混合化合物(a)和/或与该混合物反应等来得到。铜成分优选为包含2价铜的化合物。铜成分可以仅使用一种,也可以使用两种以上。
[0496]
作为铜成分,例如能够使用氧化铜或铜盐。关于铜盐,例如,优选为羧酸铜(例如,乙酸铜、乙基乙酰乙酸铜、甲酸铜、苯甲酸铜、硬脂酸铜、环烷酸铜、柠檬酸铜、2
‑
乙基己酸铜等)、磺酸铜(例如,甲磺酸铜等)、磷酸铜、磷酸酯铜、膦酸铜、膦酸酯铜、次膦酸铜、酰氨铜、磺酰氨铜、酰亚氨铜、酰基磺酰亚氨铜、双磺酰亚氨铜、甲基化物铜、烷氧基铜、苯氧基铜、氢氧化铜、碳酸铜、硫酸铜、硝酸铜、高氯酸铜、氟化铜、氯化铜、溴化铜,更优选为羧酸铜、磺酸铜、磺酰氨铜、酰亚氨铜、酰基磺酰亚氨铜、双磺酰亚氨铜、烷氧基铜、苯氧基铜、氢氧化铜、碳酸铜、氟化铜、氯化铜、硫酸铜、硝酸铜,进一步优选为羧酸铜、酰基磺酰亚氨铜、苯氧基铜、氯化铜、硫酸铜、硝酸铜,尤其优选为羧酸铜、酰基磺酰亚氨铜、氯化铜、硫酸铜。与化合物(a)反应的铜成分的量以摩尔比(化合物(a):铜成分)计优选为1:0.5~1:8,更优选为1:0.5~1:4。而且,使铜成分与化合物(a)反应时的反应条件例如,优选为以20~100℃进行0.5小时以上。
[0497]
铜络合物可以具有化合物(a)以外的配位子。作为化合物(a)以外的配位子,可举
出以阴离子或非共用电子对配位的单座配位子。作为以阴离子配位的配位子,可举出卤化物阴离子、羟化物阴离子、烷氧化物阴离子、苯氧化物阴离子、酰氨阴离子(包含被酰基或磺酰基取代的酰氨)、酰亚氨阴离子(包含被酰基或磺酰基取代的酰亚氨)、苯氨阴离子(包含被酰基或磺酰基取代的苯氨)、硫醇盐阴离子、碳酸氢阴离子、羧酸阴离子、硫羧酸阴离子、二硫羧酸阴离子、硫酸氢阴离子、磺酸阴离子、磷酸二氢阴离子、磷酸二酯阴离子、膦酸单酯阴离子、膦酸氢阴离子、次膦酸阴离子、含氮杂环阴离子、硝酸阴离子、次氯酸阴离子、氰化物阴离子、氰酸盐阴离子、异氰酸盐阴离子、硫氰酸盐阴离子、异硫氰酸盐阴离子、叠氮化物阴离子等。作为以非共用电子对配位的单座配位子,可举出水、醇、苯酚、酯、氨、苯氨、酰氨、酰亚氨、亚氨、腈、异腈、硫醇、硫醚、羰基化合物、硫羰基化合物、亚砜、杂环、或碳酸、羧酸、硫酸、磺酸、磷酸、膦酸、次膦酸、硝酸或其酯。单座配位子的种类及数量能够根据配位于铜络合物的化合物(a)而适当进行选择。
[0498]
铜络合物可根据以阴离子配位的配位部位的数量,除了不具有电荷的中性络合物以外,有时还成为阳离子络合物、阴离子络合物。该情况下,依需要而存在相对离子,以使中和铜化合物的电荷。相对离子为负的相对离子的情况下,例如,可以为无机阴离子也可以为有机阴离子。作为具体例,可举出氢氧化物离子、卤素阴离子(例如,氟化物离子、氯化物离子、溴化物离子、碘化物离子等)、取代或未取代的烷基羧酸离子(乙酸离子、三氟乙酸离子等)、取代或未取代的芳基羧酸离子(苯甲酸离子等)、取代或未取代的烷基磺酸离子(甲磺酸离子、三氟甲磺酸离子等)、取代或未取代的芳基磺酸离子(例如对甲苯磺酸离子、对氯苯磺酸离子等)、芳基二磺酸离子(例如1,3
‑
苯二磺酸离子、1,5
‑
萘二磺酸离子、2,6
‑
萘二磺酸离子等)、烷基硫酸离子(例如甲基硫酸离子等)、硫酸离子、硫氰酸离子、硝酸离子、高氯酸离子、四氟硼酸离子、四芳基硼酸离子、六氟磷酸离子、苦味酸离子、酰氨离子(包含被酰基或磺酰基取代的酰氨)、甲基化物离子(包含被酰基或磺酰基取代的甲基化物),优选为卤素阴离子、取代或未取代的烷基羧酸离子、硫酸离子、硝酸离子、四氟硼酸离子、四芳基硼酸离子、六氟磷酸离子、酰氨离子(包含被酰基或磺酰基取代的酰氨)、甲基化物离子(包含被酰基或磺酰基取代的甲基化物)。相对离子为正的相对离子的情况下,例如可举出无机或有机铵离子(例如,四丁基铵离子等四烷基铵离子、三乙基苄基铵离子、吡啶离子等)、鏻离子(例如,四丁基鏻离子等四烷基鏻离子、烷基三苯鏻离子、三乙基苯鏻离子等)、碱金属离子或质子。而且,相对离子可以为金属络合物离子。
[0499]
铜络合物中,例如作为优选的一例可举出以下(1)~(5)的方式,更优选(2)~(5),进一步优选(3)~(5),更进一步优选(4)。
[0500]
(1)作为配位子而具有一个或两个化合物的铜络合物,该化合物具有两个配位部位
[0501]
(2)作为配位子而具有化合物的铜络合物,该化合物具有3个配位部位
[0502]
(3)作为配位子而具有如下化合物的铜络合物,该化合物为具有3个配位部位的化合物和具有两个配位部位的化合物
[0503]
(4)作为配位子而具有化合物的铜络合物,该化合物具有4个配位部位
[0504]
(5)作为配位子而具有化合物的铜络合物,该化合物具有5个配位部位
[0505]
作为铜络合物的具体例,例如可举出以下内容。并且,铜络合物可以使用日本特开2014
‑
41318号公报的0013~0056段、日本特开2014
‑
32380号公报的0012~0030段中所记载
的铜络合物,并将该内容并入本说明书中。
[0506]
[化学式27]
[0507][0508]
而且,作为其他近红外线吸收化合物,还能够使用无机粒子。从红外线屏蔽性更加优异的方面考虑,无机粒子优选为金属氧化物粒子或金属粒子。作为金属氧化物粒子,例如可举出氧化铟锡(ito)粒子、氧化锑锡(ato)粒子、氧化锌(zno)粒子、al掺杂氧化锌(al掺杂zno)粒子、氟掺杂二氧化锡(f掺杂sno2)粒子、铌掺杂二氧化钛(nb掺杂tio2)粒子等。作为金属粒子,例如可举出银(ag)粒子、金(au)粒子、铜(cu)粒子、镍(ni)粒子等。关于无机粒子的形状,并无特别限制,不仅可以是球状、非球状,还可以是片状、线状、管状。
[0509]
而且,作为无机粒子,能够使用氧化钨系化合物。具体而言,更优选为由下述通式(组合式)(w
‑
1)表示的氧化钨系化合物。
[0510]
mxwyoz
……
(w
‑
1)
[0511]
m表示金属,w表示钨,o表示氧。
[0512]
0.001≤x/y≤1.1
[0513]
2.2≤z/y≤3.0
[0514]
作为m所表示的金属,可举出碱金属、碱土类金属、mg、zr、cr、mn、fe、ru、co、rh、ir、ni、pd、pt、cu、ag、au、zn、cd、al、ga、in、tl、sn、pb、ti、nb、v、mo、ta、re、be、hf、os、bi,优选为碱金属,更优选为rb或cs,尤其优选为cs。m的金属可以为一种也可以为两种以上。
[0515]
x/y为0.001以上,由此能够充分屏蔽红外线,为1.1以下,由此能够更加确切地避免在氧化钨系化合物中生成杂质相。
[0516]
z/y为2.2以上,由此能够进一步提高作为材料的化学稳定性,且为3.0以下,由此能够充分屏蔽红外线。
[0517]
作为氧化钨系化合物的具体例,可举出cs
0.33
wo3、rb
0.33
wo3、k
0.33
wo3、ba
0.33
wo3等,优选为cs
0.33
wo3或rb
0.33
wo3,更优选为cs
0.33
wo3。
[0518]
氧化钨系化合物例如可作为sumitomo metal mining co.,ltd.制ymf
‑
02等钨微粒子的分散物而得到。
[0519]
无机粒子的平均粒径优选为800nm以下,更优选为400nm以下,进一步优选为200nm以下。无机粒子的平均粒径为在种范围内,由此能够更加确保可见区域中的透光性。从避免光散射的观点考虑,无机粒子的平均粒径越小越优选。从制作时的易操作性等理由考虑,无机粒子的平均粒径通常为1nm以上。
[0520]
其他近红外线吸收化合物的含量相对于组合物的总固体成分优选为0.01~50质量%。下限优选为0.1质量%以上,更优选为0.5质量%以上。上限优选为30质量%以下,更优选为15质量%以下。
[0521]
<<彩色着色剂>>
[0522]
组合物能够含有彩色着色剂。本发明中,彩色着色剂是指白色着色剂及黑色着色剂以外的着色剂。彩色着色剂优选在波长400nm以上且小于650nm的范围具有极大吸收的着色剂。
[0523]
彩色着色剂可以为颜料,也可以为染料。颜料平均粒径(r)优选满足如下:优选为20nm≤r≤300nm,更优选为25nm≤r≤250nm,尤其优选为30nm≤r≤200nm。在此“平均粒径”是指针对集合有颜料的一次粒子的二次粒子的平均粒径。并且,可使用的颜料的二次粒子的粒径分布(以下,简称为“粒径分布”。)优选为如下:(平均粒径
±
100)nm范围内的所有二次粒子的70质量%以上,优选为80质量%以上。另外,二次粒子的粒径分布能够通过使用散射强度分布来测定。另外,关于一次粒子的平均粒径,以扫描型电子显微镜(sem)或穿透型电子显微镜(tem)进行观察,在未凝聚有粒子的部分测定100个粒子的尺寸,并求出平均值,从而能够求出平均粒径。
[0524]
颜料优选为有机颜料,能够举出以下颜料。然而,本发明并不限定于这些。
[0525]
比色指数(c.i.)pigment yellow 1、2、3、4、5、6、10、11、12、13、14、15、16、17、18、20、24、31、32、34、35、35:1、36、36:1、37、37:1、40、42、43、53、55、60、61、62、63、65、73、74、77、81、83、86、93、94、95、97、98、100、101、104、106、108、109、110、113、114、115、116、117、118、119、120、123、125、126、127、128、129、137、138、139、147、148、150、151、152、153、154、155、156、161、162、164、166、167、168、169、170、171、172、173、174、175、176、177、179、180、181、182、185、187、188、193、194、199、213、214等(以上为黄色颜料)
[0526]
c.i.pigment orange 2、5、13、16、17:1、31、34、36、38、43、46、48、49、51、52、55、59、60、61、62、64、71、73等(以上为橙色颜料)
[0527]
c.i.pigment red 1、2、3、4、5、6、7、9、10、14、17、22、23、31、38、41、48:1、48:2、48:3、48:4、49、49:1、49:2、52:1、52:2、53:1、57:1、60:1、63:1、66、67、81:1、81:2、81:3、83、88、90、105、112、119、122、123、144、146、149、150、155、166、168、169、170、171、172、175、176、177、178、179、184、185、187、188、190、200、202、206、207、208、209、210、216、220、224、226、242、246、254、255、264、270、272、279等(以上为红色颜料)
[0528]
c.i.pigment green 7、10、36、37、58、59等(以上为绿色颜料)
[0529]
c.i.pigment violet 1、19、23、27、32、37、42等(以上为紫色颜料)
[0530]
c.i.pigment blue 1、2、15、15:1、15:2、15:3、15:4、15:6、16、22、60、64、66、79、80等(以上为蓝色颜料)
[0531]
该些有机颜料能够单独使用或组合复数种来使用。
[0532]
作为染料,并无特别限制,能够使用公知的染料。作为化学结构,能够使用吡咯并吡唑偶氮系、苯氨偶氮系、三芳甲烷系、蒽醌系、蒽吡啶酮系、亚苄基系、氧杂菁系、吡唑并三唑偶氮系、吡啶酮偶氮系、花青系、吩噻嗪系、吡咯并吡唑偶氮次甲基系、呫吨系、酞菁系、苯并吡喃系、靛蓝系、吡咯亚甲基系等染料。而且,还可以使用该些染料的多聚体。并且,能够使用日本特开2015
‑
028144号公报、日本特开2015
‑
34966号公报中所记载的染料。
[0533]
组合物含有彩色着色剂的情况下,彩色着色剂的含量优选为组合物的总固体成分的0.1~70质量%。下限优选为0.5质量%以上,更优选为1.0质量%以上。上限优选为60质量%以下,更优选为50质量%以下。
[0534]
彩色着色剂的含量相对于近红外线吸收化合物a100质量份,优选为10~1000质量份,更优选为50~800质量份。
[0535]
而且,彩色着色剂与近红外线吸收化合物a的合计量优选为组合物的总固体成分的1~80质量%。下限优选为5质量%以上,更优选为10质量%以上。上限优选为70质量%以下,更优选为60质量%以下。
[0536]
组合物包含两种以上的彩色着色剂的情况下,其合计量优选为上述范围内。
[0537]
<<透射红外区域的至少一部分光,且对可见区域的光进行遮光的色材(对可见光进行遮光的色材)>>
[0538]
组合物还能够含有对可见光进行遮光的色材。对可见光进行遮光的色材中,颜料的含量相对于对可见光进行遮光的色材的总质量优选为90质量%以上,更优选为95质量%以上,进一步优选为99质量%以上。对可见光进行遮光的色材因组合复数种色材,而优选呈现黑色、灰色或接近这些颜色。而且,对可见光进行遮光的色材优选为吸收从紫色至红色波长域的光的材料。并且,对可见光进行遮光的色材优选为对波长450~650nm的波长域的光进行遮光的色材。
[0539]
对可见光进行遮光的色材优选满足以下(1)及(2)的至少一个要求,更优选满足(1)的要求。
[0540]
(1):包含两种以上的彩色着色剂的方式
[0541]
(2):包含有机系黑色着色剂的方式
[0542]
另外,本发明中,作为对可见光进行遮光的色材的有机系黑色着色剂是指吸收可见区域的光,且透射红外区域的至少一部分光的材料。从而,本发明中,作为对可见光进行遮光的色材的有机系黑色着色剂并不包含吸收红外区域的光及可见区域的光这两者的黑色着色剂,即不包含碳黑或钛黑。
[0543]
作为彩色着色剂,可举出上述的彩色着色剂。作为有机系黑色着色剂,例如可举出双苯并呋喃酮化合物、甲亚氨化合物、苝化合物、偶氮系化合物等,优选为双苯并呋喃酮化合物、苝化合物。作为双苯并呋喃酮化合物,可举出日本特表2010
‑
534726号公报、日本特表2012
‑
515233号公报、日本特表2012
‑
515234号公报等中所记载的化合物,例如,可作为basf公司制“irgaphor black”而得到。作为苝化合物,可举出c.i.pigment black 31、32等。作为甲亚氨化合物,可举出日本特开平1
‑
170601号公报、日本特开平2
‑
34664号公报等中所记载的化合物,例如能够作为dainichiseika color&chemicals mfg.co.,ltd.制“chromofine黑a1103”而得到。
[0544]
对可见光进行遮光的色材中,例如作为波长450~650nm的范围内的吸光度的最小值a与波长900~1300nm的范围内的吸光度的最小值b的比的a/b优选为4.5以上。
[0545]
关于上述特性,可以以一种原材料满足,也可以组合复数种原材料来满足。例如,上述(1)的方式的情况下,优选组合复数种彩色着色剂来满足上述光谱特性。
[0546]
作为对可见光进行遮光的色材而包含两种以上的彩色着色剂的情况下,彩色着色剂优选为选自红色着色剂、绿色着色剂、蓝色着色剂、黄色着色剂、紫色着色剂及橙色着色剂的着色剂。
[0547]
组合两种以上的彩色着色剂来形成对可见光进行遮光的色材的情况下,作为彩色着色剂的组合,例如可举出以下方式。
[0548]
(1)含有黄色着色剂、蓝色着色剂、紫色着色剂及红色着色剂的方式
[0549]
(2)含有黄色着色剂、蓝色着色剂及红色着色剂的方式
[0550]
(3)含有黄色着色剂、紫色着色剂及红色着色剂的方式
[0551]
(4)含有黄色着色剂及紫色着色剂的方式
[0552]
(5)含有绿色着色剂、蓝色着色剂、紫色着色剂及红色着色剂的方式
[0553]
(6)含有紫色着色剂及橙色着色剂的方式
[0554]
(7)含有绿色着色剂、紫色着色剂及红色着色剂的方式
[0555]
(8)含有绿色着色剂及红色着色剂的方式
[0556]
作为各着色剂的比率(质量比),例如可举出以下示例。
[0557]
[表55]
[0558]
no.黄色着色剂绿色着色剂蓝色着色剂紫色着色剂红色着色剂橙色着色剂10.1~0.4 0.1~0.60.01~0.30.1~0.6 20.1~0.4 0.1~0.6 0.2~0.7 30.1~0.6
ꢀꢀ
0.1~0.60.1~0.6 40.2~0.8
ꢀꢀ
0.2~0.8
ꢀꢀ
5 0.1~0.40.1~0.40.1~0.40.1~0.4 6
ꢀꢀꢀ
0.2~0.6 0.4~0.87 0.1~0.5 0.2~0.70.1~0.4 8 0.5~0.8
ꢀꢀ
0.2~0.5 [0559]
组合物含有对可见光进行遮光的色材的情况下,对可见光进行遮光的色材的含量相对于组合物的总固体成分优选为30质量%以下,更优选为20质量%以下,进一步优选为5质量%以下。下限例如能够设为0.01质量%以上,也能够设为0.5质量%以上。
[0560]
而且,组合物能够为实质上并不含有对可见光进行遮光的色材的方式。实质上并不含有对可见光进行遮光的色材的情况是指,对可见光进行遮光的色材的含量优选为组合物的总固体成分的0.005质量%以下,更优选为0.001质量%以下,进一步优选不含有对可见光进行遮光的色材。
[0561]
<<颜料衍生物>>
[0562]
组合物包含颜料的情况下,能够进一步含有颜料衍生物。作为颜料衍生物,优选颜料的一部分具有被酸性基、碱性基或邻苯二甲酰亚氨甲基取代的结构的化合物,更优选由式(b1)表示的颜料衍生物。
[0563]
[化学式28]
[0564][0565]
式(b1)中,p表示色素结构,l表示单键或连结基,x表示酸性基、碱性基、具有盐结构的基团或邻苯酰亚氨基。m表示1以上的整数,n表示1以上的整数。m为2以上的情况下,复数个l及x可以彼此不同,n为2以上的情况下,复数个x可以彼此不同。
[0566]
式(b1)中,p表示色素结构,优选选自吡咯并吡咯色素结构、二酮吡咯并吡咯色素结构、喹吖啶酮色素结构、蒽醌色素结构、二蒽醌色素结构、苯并异吲哚色素结构、噻嗪靛蓝色素结构、偶氮色素结构、喹酞酮色素结构、酞菁色素结构、萘酞菁色素结构、二噁嗪色素结
构、苝色素结构、紫环酮色素结构、苯并咪唑酮色素结构、苯并噻唑色素结构、苯并咪唑色素结构及苯并噁唑色素结构中的至少一种,更优选选自吡咯并吡咯色素结构、二酮吡咯并吡咯色素结构、喹吖啶酮色素结构及苯并咪唑酮色素结构中的至少一种,尤其优选吡咯并吡咯色素结构。
[0567]
式(b1)中,l表示单键或连结基。作为连结基,优选由1~100个碳原子、0~10个氮原子、0~50个氧原子、1~200个氢原子及0~20个硫原子构成的基团,可以未取代也可以进一步具有取代基。
[0568]
式(b1)中,x表示酸性基、碱性基、具有盐结构的基团或邻苯酰亚氨基。
[0569]
组合物含有颜料衍生物的情况下,颜料衍生物的含量相对于组合物中所包含的颜料100质量份,优选为1~50质量份。下限值优选为3质量份以上,更优选为5质量份以上。上限值优选为40质量份以下,更优选为30质量份以下。若颜料衍生物的含量为上述范围,则可提高颜料分散性,并有效地抑制粒子的凝聚。颜料衍生物可以仅为一种,也可以为两种以上,两种以上的情况下,优选合计量成为上述范围。
[0570]
<<固化性化合物>>
[0571]
组合物优选含有固化性化合物。作为固化性化合物,能够使用由自由基、酸、热而可固化的公知的化合物。例如,可举出具有包含烯属不饱和键的基团的化合物、具有环氧基的化合物、具有羟甲基的化合物、具有烷氧基甲硅烷基的化合物等。作为包含烯属不饱和键的基团,可举出乙烯基、(甲基)烯丙基、(甲基)丙烯酰基、(甲基)丙烯酰氧基等。作为烷氧基甲硅烷基,可举出单烷氧基甲硅烷基、二烷氧基甲硅烷基、三烷氧基甲硅烷基。包含烯属不饱和键的基团优选为(甲基)丙烯酰基、(甲基)丙烯酰氧基。烷氧基甲硅烷基优选为二烷氧基甲硅烷基、三烷氧基甲硅烷基。而且,烷氧基甲硅烷基中的烷氧基的碳数优选为1~5,更优选为1~3,尤其优选为1或2。
[0572]
固化性化合物可以为单体、聚合物中的任一形态,优选为单体。单体类型固化性化合物的分子量优选为100~3000。上限优选为2000以下,更优选为1500以下。下限优选为150以上,进一步优选为250以上。而且,固化性化合物也优选实质上不具有分子量分布的化合物。在此,实质上不具有分子量分布是指,化合物的分散度(重量均分子量(mw)/数均分子量(mn))优选为1.0~1.5,更优选为1.0~1.3。
[0573]
(具有包含烯属不饱和键的基团的化合物)
[0574]
作为固化性化合物,能够使用具有包含烯属不饱和键的基团的化合物。具有包含烯属不饱和键的基团的化合物优选为单体。具有包含烯属不饱和键的基团的化合物的分子量优选为100~3000。上限优选为2000以下,更优选为1500以下。下限优选为150以上,更优选为250以上。具有包含烯属不饱和键的基团的化合物优选为3~15官能(甲基)丙烯酸酯化合物,更优选为3~6官能(甲基)丙烯酸酯化合物。
[0575]
作为上述化合物的例子,可参考日本特开2013
‑
253224号公报的0033~0034段中所记载的化合物,并将该内容并入本说明书中。作为上述化合物,优选乙烯氧基改质季戊四醇四丙烯酸酯(作为市售品,nk酯atm
‑
35e;shin
‑
nakamura chemical co.,ltd.制)、双季戊四醇三丙烯酸酯(作为市售品,kayarad d
‑
330;nippon kayaku co.,ltd.制)、双季戊四醇四丙烯酸酯(作为市售品,kayarad d
‑
320;nippon kayaku co.,ltd.制)、双季戊四醇五(甲基)丙烯酸酯(作为市售品,kayarad d
‑
310;nippon kayaku co.,ltd.制)、双季戊四醇六
(甲基)丙烯酸酯(作为市售品,kayarad dpha;nippon kayaku co.,ltd.制、a
‑
dph
‑
12e;shin
‑
nakamura chemical co.,ltd.制)、及它们的(甲基)丙烯酰基经由乙二醇、丙二醇残基而键合的结构。且还可使用这些寡聚物类型。而且,能够参考日本特开2013
‑
253224号公报的0034~0038段的有关聚合性化合物的记载,并将该内容并入本说明书中。而且,能够举出日本特开2012
‑
208494号公报的0477(相对应的美国专利申请公开第2012/0235099号说明书的0585段)段中所记载的聚合性单体等,并将该些内容并入本说明书中。
[0576]
而且,优选双甘油eo(环氧乙烷)改质(甲基)丙烯酸酯(作为市售品,m
‑
460;toagosei co.,ltd.制)。也优选季戊四醇四丙烯酸酯(shin
‑
nakamura chemical co.,ltd.制、a
‑
tmmt)、1,6
‑
己二醇二丙烯酸酯(nippon kayaku co.,ltd.制、kayarad hdda)。还能够使用该些寡聚物类型。例如,可举出rp
‑
1040(nippon kayaku co.,ltd.制)等。
[0577]
具有包含烯属不饱和键的基团的化合物可以具有羧基、磺酸基、磷酸基等酸基。作为具有酸基的上述化合物,可举出脂肪族多羟基化合物与不饱和羧酸的酯等。优选使脂肪族多羟基化合物的未反应羟基与非芳香族羧酸酐反应而具有酸基的化合物,尤其优选在该酯中,脂肪族多羟基化合物为季戊四醇和/或双季戊四醇的化合物。作为市售品,例如作为toagosei co.,ltd.制多元酸改质丙烯酸寡聚物,可举出aronix系列的m
‑
305、m
‑
510、m
‑
520等。具有酸基的化合物的酸值优选为0.1~40mgkoh/g。下限优选为5mgkoh/g以上。上限优选为30mgkoh/g以下。
[0578]
具有包含烯属不饱和键的基团的化合物为具有己内酯结构的化合物也为优选的方式。作为具有己内酯结构的化合物,在分子内具有己内酯结构的范围内并无特别限定。例如,能够举出可由将三羟甲基、二三羟甲基、三羟甲基丙烷、二三羟甲基丙烷、季戊四醇、二季戊四醇、三季戊四醇、甘油、双甘油、羟甲基三聚氰氨等多元醇、(甲基)丙烯酸酸及ε
‑
己内酯酯化而得到的、ε
‑
己内酯改质多官能(甲基)丙烯酸酯。作为具有己内酯结构的化合物,能够参考日本特开2013
‑
253224号公报的0042~0045段中所记载的化合物,并将该内容并入本说明书中。关于具有己内酯结构的化合物,例如可举出有nippon kayaku co.,ltd.作为kayarad dpca系列而市售的、dpca
‑
20、dpca
‑
30、dpca
‑
60、dpca
‑
120等、sartomer company,inc制的作为具有4个伸乙氧基链的4官能丙烯酸酯的sr
‑
494、作为具有3个异伸丁氧基链的3官能丙烯酸酯的tpa
‑
330等。
[0579]
作为具有包含烯属不饱和键的基团的化合物,日本特公昭48
‑
41708号公报、日本特开昭51
‑
37193号公报、日本特公平2
‑
32293号公报、日本特公平2
‑
16765号公报中所记载的氨基甲酸酯丙烯酸酯类,也优选日本特公昭58
‑
49860号公报、日本特公昭56
‑
17654号公报、日本特公昭62
‑
39417号公报、日本特公昭62
‑
39418号公报中所记载的具有环氧乙烷系骨架的氨基甲酸酯化合物类。而且,能够使用日本特开昭63
‑
277653号公报、日本特开昭63
‑
260909号公报、日本特开平1
‑
105238号公报中所记载的、在分子内具有氨基结构或硫醚结构的加成聚合性化合物类。
[0580]
作为市售品,可举出氨基甲酸酯寡聚物uas
‑
10、uab
‑
140(sanyo kokusaku pulp co.,ltd制)、ua
‑
7200(shin
‑
nakamura chemical co.,ltd.制)、dpha
‑
40h(nippon kayaku co.,ltd.制)、ua
‑
306h、ua
‑
306t、ua
‑
306i、ah
‑
600、t
‑
600、ai
‑
600(kyoeisha chemical co.,ltd.制)等。
[0581]
(具有环氧基的化合物)
[0582]
作为固化性化合物,还能够使用具有环氧基的化合物。作为具有环氧基的化合物,单官能或多官能缩水甘油醚化合物、多官能脂肪族缩水甘油醚化合物等。而且,能够使用缩水甘油基(甲基)丙烯酸酯或烯丙基缩水甘油醚等具有缩水甘油基的化合物、具有脂环式环氧基的化合物。
[0583]
关于具有环氧基的化合物,可举出在一分子内具有一个以上的环氧基的化合物,优选具有两个以上的化合物。在一分子内优选具有1~100个环氧基。上限例如能够设为10个以下。也能够设为5个以下。下限优选为两个以上。
[0584]
具有环氧基的化合物中,环氧基当量(=具有环氧基的化合物的分子量/环氧基的数)优选为500g/eq以下,更优选为100~400g/eq,进一步优选为100~300g/eq。
[0585]
具有环氧基的化合物可以为低分子化合物(例如,分子量小于2000,进而分子量小于1000)、高分子化合物(macromolecule)(例如,分子量1000以上,聚合物时,重量均分子量为1000以上)中的任意一个。具有环氧基的化合物的重量均分子量优选为200~100000,更优选为500~50000。重量均分子量的上限优选为10000以下,更优选为5000以下,进一步优选为3000以下。
[0586]
具有环氧基的化合物还能够使用日本特开2013
‑
011869号公报的0034~0036段、日本特开2014
‑
043556号公报的0147~0156段、日本特开2014
‑
089408号公报的0085~0092段中所记载的化合物。将该些内容并入本说明书中。作为市售品,为如下市售品,例如,作为双酚a型环氧树脂,为jer825、jer827、jer828、jer834、jer1001、jer1002、jer1003、jer1055、jer1007、jer1009、jer1010(以上为mitsubishi chemical co.,ltd.制)、epiclon860、epiclon1050、epiclon1051、epiclon1055(以上为dic corporation制)等,作为双酚f型环氧树脂,为jer806、jer807、jer4004、jer4005、jer4007、jer4010(以上、mitsubishi chemical co.,ltd.制)、epiclon830、epiclon835(以上为dic corporation制)、lce
‑
21、re
‑
602s(以上为nippon kayaku co.,ltd.制)等,作为苯酚酚醛清漆型环氧树脂,为jer152、jer154、jer157s70、jer157s65(以上为mitsubishi chemical co.,ltd.制)、epiclon n
‑
740、epiclon n
‑
770、epiclon n
‑
775(以上为dic corporation制)等,作为甲酚酚醛清漆型环氧树脂,为epiclon n
‑
660、epiclon n
‑
665、epiclon n
‑
670、epiclon n
‑
673、epiclon n
‑
680、epiclon n
‑
690、epiclon n
‑
695(以上为dic corporation制)、eocn
‑
1020(nippon kayaku co.,ltd.制)等,作为脂肪族环氧树脂,为adeka resin ep
‑
4080s、adeka resin ep
‑
4085s、adeka resin ep
‑
4088s(以上为adeka corporation制)、celloxide 2021p、celloxide 2081、celloxide 2083、celloxide2085、ehpe3150、epolead pb 3600、epolead pb 4700(以上为daicel corporation制)、denacol ex
‑
212l、ex
‑
214l、ex
‑
216l、ex
‑
321l、ex
‑
850l(以上为nagase chemtex corporation制)等。除此以外,还可举出adeka resin ep
‑
4000s、adeka resin ep
‑
4003s、adeka resin ep
‑
4010s、adeka resin ep
‑
4011s(以上为adeka corporation制)、nc
‑
2000、nc
‑
3000、nc
‑
7300、xd
‑
1000、eppn
‑
501、eppn
‑
502(以上为adeka corporation制)、jer1031s(mitsubishi chemical co.,ltd.制)、oxt
‑
221(toagosei co.,ltd.制)等。
[0587]
作为具有环氧基的化合物,可使用缩水甘油基(甲基)丙烯酸酯或烯丙基缩水甘油醚等作为环氧基而具有缩水甘油基的化合物,优选具有脂环式环氧基的不饱和化合物。作为这种化合物,例如能够参考日本特开2009
‑
265518号公报的0045段等的记载,并将该内容
并入本说明书中。
[0588]
(具有烷氧基甲硅烷基的化合物)
[0589]
作为固化性化合物,还能够使用具有烷氧基甲硅烷基的化合物。烷氧基甲硅烷基中的烷氧基的碳数优选为1~5,更优选为1~3,尤其优选为1或2。烷氧基甲硅烷基在一分子中优选具有两个以上,进一步优选具有2~3个。作为具有烷氧基甲硅烷基的化合物的具体例,可举出甲基三甲氧基硅烷、二甲基二甲氧基硅烷、苯基三甲氧基硅烷、甲基三乙氧基硅烷、二甲基二乙氧基硅烷、苯基三乙氧基硅烷、正丙基三甲氧基硅烷、正丙基三乙氧基硅烷、己基三甲氧基硅烷、己基三乙氧基硅烷、辛基三乙氧基硅烷、癸基三甲氧基硅烷、1,6
‑
双(三甲氧基硅烷基)己烷、三氟丙基三甲氧基硅烷、六甲基二硅氮烷、乙烯基三甲氧基硅烷、乙烯基三乙氧基硅烷、2
‑
(3,4
‑
环氧基环己基)乙基三甲氧基硅烷、3
‑
环氧丙氧基丙基甲基二甲氧基硅烷、3
‑
环氧丙氧基丙基三甲氧基硅烷、3
‑
环氧丙氧基丙基甲基二乙氧基硅烷、3
‑
环氧丙氧基丙基三乙氧基硅烷、对苯乙烯基三甲氧基硅烷、3
‑
甲基丙烯酰氧基丙基甲基二甲氧基硅烷、3
‑
甲基丙烯酰氧基丙基三甲氧基硅烷、3
‑
甲基丙烯酰氧基丙基甲基二乙氧基硅烷、3
‑
甲基丙烯酰氧基丙基三乙氧基硅烷、3
‑
丙烯酰氧基丙基三甲氧基硅烷、n
‑2‑
(氨基乙基)
‑3‑
氨基丙基甲基二甲氧基硅烷、n
‑2‑
(氨基乙基)
‑3‑
氨基丙基三甲氧基硅烷、3
‑
氨基丙基三甲氧基硅烷、3
‑
氨基丙基三乙氧基硅烷、3
‑
三乙氧基甲硅烷基
‑
n
‑
(1,3
‑
二甲基
‑
亚丁基)丙基氨、n
‑
苯基
‑3‑
氨基丙基三甲氧基硅烷、n
‑
(乙烯基苄基)
‑2‑
氨基乙基
‑3‑
氨基丙基三甲氧基硅烷的盐酸盐、三
‑
(三甲氧基甲硅烷基丙基)异氰脲酸酯、3
‑
脲丙基三乙氧基硅烷、3
‑
巯基丙基甲基二甲氧基硅烷、3
‑
巯基丙基三甲氧基硅烷、双(三乙氧基甲硅烷基丙基)四硫醚、3
‑
异氰酸酯丙基三乙氧基硅烷等。而且,上述以外还能够使用烷氧基寡聚物。而且,还能够使用下述化合物。
[0590]
[化学式29]
[0591][0592]
作为市售品,可举出shin
‑
etsu silicone co.,ltd.制kbm
‑
13、kbm
‑
22、kbm
‑
103、kbe
‑
13、kbe
‑
22、kbe
‑
103、kbm
‑
3033、kbe
‑
3033、kbm
‑
3063、kbm
‑
3066、kbm
‑
3086、kbe
‑
3063、kbe
‑
3083、kbm
‑
3103、kbm
‑
7103、sz
‑
31、kpn
‑
3504、kbm
‑
1003、kbe
‑
1003、kbm
‑
303、kbm
‑
402、kbm
‑
403、kbe
‑
402、kbe
‑
403、kbm
‑
1403、kbm
‑
502、kbm
‑
503、kbe
‑
502、kbe
‑
503、kbm
‑
5103、
kbm
‑
602、kbm
‑
603、kbm
‑
903、kbe
‑
903、kbe
‑
9103、kbm
‑
573、kbm
‑
575、kbm
‑
9659、kbe
‑
585、kbm
‑
802、kbm
‑
803、kbe
‑
846、kbe
‑
9007、x
‑
40
‑
1053、x
‑
41
‑
1059a、x
‑
41
‑
1056、x
‑
41
‑
1805、x
‑
41
‑
1818、x
‑
41
‑
1810、x
‑
40
‑
2651、x
‑
40
‑
2655a、kr
‑
513,kc
‑
89s,kr
‑
500、x
‑
40
‑
9225、x
‑
40
‑
9246、x
‑
40
‑
9250、kr
‑
401n、x
‑
40
‑
9227、x
‑
40
‑
9247、kr
‑
510、kr
‑
9218、kr
‑
213、x
‑
40
‑
2308、x
‑
40
‑
9238等。
[0593]
而且,具有烷氧基甲硅烷基的化合物能够使用在侧链具有烷氧基甲硅烷基的聚合物。
[0594]
(具有羟甲基的化合物)
[0595]
作为固化性化合物,也能够使用具有羟甲基的化合物。作为具有羟甲基的化合物,可举出羟甲基与氮原子或形成芳香族环的碳原子键合而成的化合物。
[0596]
作为羟甲基与氮原子键合而成的化合物,优选为烷氧基甲基化三聚氰氨、羟甲基化三聚氰氨、烷氧基甲基化苯并胍氨、羟甲基化苯并胍氨、烷氧基甲基化甘脲、羟甲基化甘脲、烷氧基甲基化尿素及羟甲基化尿素等。而且,特优选为1,3,4,6
‑
四甲氧基甲基甘脲。而且,能够参考日本特开2004
‑
295116号公报的0134~0147段、日本特开2014
‑
089408的0095~0126段的记载,并将该些内容并入本说明书中。
[0597]
作为具有羟甲基的化合物的优选结构,能够举出由下述式(8
‑
1)~式(8
‑
4)表示的化合物。
[0598]
[化学式30]
[0599][0600]
(式(8
‑
1)~式(8
‑
4)中,x2表示2价有机基团,r7~r
11
分别独立地表示氢原子或一价有机基团。)
[0601]
作为具有羟甲基的化合物的例子,能够举出例如由下述式(4)~式(5)表示的化合物。
[0602]
[化学式31]
[0603][0604]
(式(4)中,x表示单键或1~4价有机基团,r
11
、r
12
分别独立地表示氢原子或一价有机基团,n为1~4的整数,p及q分别独立地为0~4的整数。其中,n为1的情况下,p为1~4的整数。n为2~4的整数的情况下,p为0~4的整数,且式(4)中包含一个以上的
‑
ch2or
11
。)
[0605]
[化学式32]
[0606][0607]
(式(5)中,两个y分别独立地表示氢原子或碳数1~10的烷基,也可以含有氧原子、氟原子。r
13
~r
16
分别独立地表示氢原子或一价有机基团。m及n分别独立地为1~3的整数,p及q分别独立地为0~4的整数)
[0608]
作为具有羟甲基的化合物的市售品,例如,能够优选使用cymel300、301、303、370、325、327、701、266、267、238、1141、272、202、1156、1158、1123、1170、1174、ufr65、300(以上为mitsui
‑
cyanamid,ltd.制)、nikalac mx
‑
750、
‑
032、
‑
706、
‑
708、
‑
40、
‑
31、
‑
270、
‑
280、
‑
290、
‑
750lm、nikalac ms
‑
11、nikalac mw
‑
30hm、
‑
100lm、
‑
390(以上为sanwa chemical co.,ltd.制)等。
[0609]
组合物含有固化性化合物的情况下,固化性化合物的含量相对于组合物的总固体成分优选为0.1~40质量%。下限例如,更优选为0.5质量%以上,进一步优选为1质量%以上。上限例如,更优选为30质量%以下,进一步优选为20质量%以下。固化性化合物可以单独使用一种,也可以并用两种以上。并用两种以上的情况下,合计量优选为上述范围。
[0610]
<<树脂>>
[0611]
组合物能够含有树脂。树脂例如以将颜料等分散于组合物中的用途、粘结剂的用途进行配合。另外,还将主要为了分散颜料等而使用的树脂称为分散剂。然而,该种用途为一例,也能够作为该种用途以外的目的而使用树脂。
[0612]
树脂的重量均分子量(mw)优选为2,000~2,000,000。上限优选为1,000,000以下,更优选为500,000以下。下限优选为3,000以上,更优选为5,000以上。并且,为环氧树脂的情况下,环氧树脂的重量均分子量(mw)优选为100以上,更优选为200~2,000,000。上限优选为1,000,000以下,更优选为500,000以下。下限优选为100以上,更优选为200以上。
[0613]
作为树脂,可举出(甲基)丙烯酸树脂、环氧树脂、烯硫醇树脂、聚碳酸酯树脂、聚醚树脂、聚芳酯树脂、聚砜树脂、聚醚砜树脂、聚对亚苯基树脂、聚亚芳基醚氧化膦树脂、聚酰亚氨树脂、聚酰氨酰亚氨树脂、聚烯烃树脂、环状烯烃树脂、聚脂树脂、苯乙烯树脂等。该些树脂可单独使用一种,也可以混合两种以上来使用。
[0614]
作为(甲基)丙烯酸树脂,可举出包含(甲基)丙烯酸和/或来源于其酯的结构单元的聚合物。具体而言,可举出聚合选自(甲基)丙烯酸、(甲基)丙烯酸酯类、(甲基)丙烯酰氨及(甲基)丙烯腈中的至少一种来得到的聚合物。
[0615]
作为聚酯树脂,可举出由多元醇(例如,乙二醇、丙二醇、丙三醇、三羟甲基丙烷)与多元酸(例如,对苯二甲酸、间苯二甲酸、萘二甲酸等芳香族二羧酸及该些芳香族环的氢原子被甲基、乙基、苯基等取代的芳香族二羧酸、己二酸、癸二酸、十二烷二羧酸等碳数2~20的脂肪族二羧酸、及环己烷二羧酸等的脂肪族二羧酸等)的反应而得到的聚合物、及由己内酯单体等的环状酯化合物的开环聚合而得到的聚合物(例如,聚己内酯)。
[0616]
作为苯乙烯树脂,可举出聚羟基苯乙烯等。
[0617]
而且,树脂可以具有酸基。作为酸基,例如可举出羧基、磷酸基、磺酸基、苯酚性羟基等。该些酸基可以仅为一种,也可以为两种以上。具有酸基的树脂能够用作碱溶性树脂。而且,也能够用作分散剂。
[0618]
作为具有酸基的树脂,优选在侧链具有羧基的聚合物,甲基丙烯酸共聚物、丙烯酸共聚物、衣康酸共聚物、巴豆酸共聚物、马来酸共聚物、部分酯化马来酸共聚物、酚醛清漆树脂等的碱可溶性酚醛树脂等,以及在侧链具有羧基的酸性纤维素衍生物、在具有羟基的聚合物加成酸酐而得到者。尤其,优选(甲基)丙烯酸、及可与其共聚的与其他单体的共聚物。作为可与(甲基)丙烯酸共聚的其他单体,可举出烷基(甲基)丙烯酸酯、芳基(甲基)丙烯酸酯、乙烯基化合物等。作为烷基(甲基)丙烯酸酯及芳基(甲基)丙烯酸酯,可举出(甲基)丙烯酸甲酯、(甲基)丙烯酸乙酯、(甲基)丙烯酸丙酯、(甲基)丙烯酸丁酯、(甲基)丙烯酸异丁酯、(甲基)丙烯酸戊酯、(甲基)丙烯酸己酯、(甲基)丙烯酸辛酯、苯基(甲基)丙烯酸酯、苄基(甲基)丙烯酸酯、甲苯基(甲基)丙烯酸酯、萘基(甲基)丙烯酸酯、环己基(甲基)丙烯酸酯等,作为乙烯基化合物,可举出苯乙烯、α
‑
甲基苯乙烯、乙烯基甲苯、甲基丙烯酸缩水甘油酯、丙烯腈、乙酸乙烯酯、n
‑
乙烯基吡咯啶酮、丙烯酸四氢糠酯、聚苯乙烯大分子单体、聚甲基丙烯酸甲酯大分子单体等。而且,作为上述其他单体,可举出日本特开平10
‑
300922号公报所记载的n位取代马来酰亚氨单体。例如,可举出n
‑
苯基马来酰亚氨、n
‑
环己基马来酰亚氨等。可与这些(甲基)丙烯酸共聚的其他单体可以仅为一种,也可以为两种以上。
[0619]
具有酸基的树脂,能够优选使用包括苄基(甲基)丙烯酸酯/(甲基)丙烯酸共聚物、苄基(甲基)丙烯酸/(甲基)丙烯酸/2
‑
羟乙基(甲基)丙烯酸酯共聚物、苄基(甲基)丙烯酸/(甲基)丙烯酸/其他单体的多元共聚物。而且,也能够优选使用将2
‑
羟乙基(甲基)丙烯酸酯聚合者,日本特开平7
‑
140654号公报所记载的2
‑
羟丙基(甲基)丙烯酸酯/聚苯乙烯大分子单体/甲基丙烯酸苄酯/甲基丙烯酸共聚物、2
‑
羟基
‑3‑
苯氧基丙酯/聚甲基丙烯酸甲酯大分子单体/甲基丙烯酸苄酯/甲基丙烯酸共聚物、丙烯酸2
‑
羟基乙酯/聚苯乙烯大分子单体/甲基丙烯酸甲酯/甲基丙烯酸共聚物、丙烯酸2
‑
羟基乙酯/聚苯乙烯大分子单体/甲基丙烯酸苄酯/甲基丙烯酸共聚物。
[0620]
也优选具有酸基的树脂包含如下聚合物,该聚合物由聚合包含由下述式(ed1)表示的化合物和/或由下述式(ed2)表示的化合物(以下,有时将该些化合物称为“醚二聚体”。)的单体成分而成。
[0621]
[化学式33]
[0622][0623]
式(ed1)中,r1及r2分别独立地表示氢原子或可以具有取代基的碳数1~25的烃基。
[0624]
[化学式34]
[0625][0626]
式(ed2)中,r表示氢原子或碳数1~30的有机基团。作为式(ed2)的具体例,能够参考日本特开2010
‑
168539号公报的记载。
[0627]
式(ed1)中,作为由r1及r2表示的可以具有取代基的碳数1~25的烃基,并无特别限定,例如可举出,甲基、乙基、正丙基、异丙基、正丁基、异丁基、第三级丁基、第三级戊基、硬脂基、月桂基、2
‑
乙基己基等的直链状或分支状烷基;苯基等的芳基;环己基、第三级丁基环己基、二环戊二烯基、三环癸基、异冰片基、金刚烷基、2
‑
甲基
‑2‑
金刚烷基等脂环族基;被1
‑
甲氧基乙基、1
‑
乙氧基乙基等烷氧基取代的烷基;被苄基等芳基取代的烷基等。其中,从耐热性方面考虑,尤其优选如甲基、乙基、环己基、苄基等不易因酸和热而脱离的1级或2级碳的取代基。
[0628]
作为醚二聚体的具体例,例如,能够参考日本特开2013
‑
29760号公报的0317段,并将该内容并入本说明书中。醚二聚体可以仅为一种,也可以为两种以上。
[0629]
具有酸基的树脂可以含有源自由下述式(x)表示的化合物的结构单元。
[0630]
[化学式35]
[0631][0632]
式(x)中,r1表示氢原子或甲基,r2表示碳数2~10的伸烷基,r3表示氢原子或可以含有苯环的碳数1~20的烷基。n表示1~15的整数。
[0633]
上述式(x)中,r2的伸烷基的碳数优选为2~3。并且,r3的烷基的碳数为1~20,更优选为1~10,r3的烷基可以含有苯环。作为由r3表示的含有苯环的烷基,能够举出苄基、2
‑
苯基(异)丙基等。
[0634]
作为具有酸基的树脂,能够参考日本特开2012
‑
208494号公报的0558~0571段(相对应的美国专利申请公开第2012/0235099号说明书的0685~0700段)的记载、日本特开2012
‑
198408号公报的0076~0099段的记载,并将该内容并入本说明书中。而且,还可举出以下的树脂。
[0635]
[化学式36]
[0636][0637]
具有酸基的树脂的酸值优选为30~200mgkoh/g。下限优选为50mgkoh/g以上,更优选为70mgkoh/g以上。上限优选为150mgkoh/g以下,更优选为120mgkoh/g以下。
[0638]
树脂可以具有固化性基团。作为固化性基团,可举出具有烯属不饱和键的基团、环氧基、羟甲基、烷氧基甲硅烷基等。作为具有烯属不饱和键的基团,可举出乙烯基、(甲基)烯丙基、(甲基)丙烯酰基、(甲基)丙烯酰氧基等。作为烷氧基甲硅烷基,可举出单烷氧基甲硅烷基、二烷氧基甲硅烷基、三烷氧基甲硅烷基。作为具有固化性基团的结构单元,可举出下述式(a2
‑
1)~式(a2
‑
4)等。
[0639]
[化学式37]
[0640][0641]
r1表示氢原子或烷基。烷基的碳数优选为1~5,更优选为1~3,尤其优选为1。r1优选为氢原子或甲基。
[0642]
l
51
表示单键或2价连结基。作为2价连结基,可举出伸烷基、伸芳基、
‑
o
‑
、
‑
s
‑
、
‑
co
‑
、
‑
coo
‑
、
‑
oco
‑
、
‑
so2‑
、
‑
nr
10
‑
(r
10
表示氢原子或烷基,优选为氢原子)或包含它们的组合的基团,优选包含伸烷基、伸芳基及伸烷基的至少一个与
‑
o
‑
的组合的基团。伸烷基的碳数优选为1~30,更优选为1~15,进一步优选为1~10。伸烷基可以具有取代基,优选为未取代。伸烷基可以为直链、分支、环状中的任意一个。而且,环状伸烷基可以为单环、多环中的任意一个。伸芳基的碳数优选为6~18,更优选为6~14,进一步优选为6~10。
[0643]
p1表示固化性基团。作为固化性基团,可举出具有烯属不饱和键的基团、环氧基、羟甲基、烷氧基甲硅烷基等。作为具有烯属不饱和键的基团,可举出乙烯基、(甲基)烯丙基、(甲基)丙烯酰基、(甲基)丙烯酰氧基等。作为烷氧基甲硅烷基,可举出单烷氧基甲硅烷基、二烷氧基甲硅烷基、三烷氧基甲硅烷基。
[0644]
作为含有固化性基团的树脂,可举出dianal nr系列(mitsubishi rayon co.,ltd.制)、photomer6173(含cooh聚氨酯丙烯酸低聚物.diamond shamrock co.,ltd.制)、viscote r
‑
264、ks resist106(均为osaka organic chemical industry ltd.制)、cyclomer p系列(例如,aca230aa)、placcel cf200系列(均为daicel corporation co.,ltd.制)、ebecryl3800(daicel u c b kk制)、acrycure
‑
rd
‑
f8(nippon shokubai co.,ltd.制)等。又,可举出上述的环氧树脂或下述树脂等。
[0645]
[化学式38]
[0646][0647]
树脂也优选具有由下述式(a3
‑
1)~式(a3
‑
7)表示的结构单元。
[0648]
[化学式39]
[0649][0650]
式中,r5表示氢原子或烷基,l4~l7分别独立地表示单键或2价连结基,r
10
~r
13
分别独立地表示烷基或芳基。r
14
及r
15
分别独立地表示氢原子或取代基。
[0651]
r5与式(a2
‑
1)~式(a2
‑
4)的r1含义相同,优选范围也相同。
[0652]
l4~l7与式(a2
‑
1)~式(a2
‑
4)的l
51
含义相同,优选范围也相同。
[0653]
r
10
所表示的烷基可以为直链状、分支状或环状中的任意一个,优选为环状。烷基可以具有上述的取代基,也可以未取代。烷基的碳数优选为1~30,更优选为1~20,进一步优选为1~10。r
10
所表示的芳基的碳数优选为6~18,更优选为6~12,进一步优选为6。r
10
优选为环状烷基或芳基。
[0654]
r
11
、r
12
所表示的烷基可以为直链状、分支状或环状中的任意一个,优选为直链状或分支状。烷基可以具有上述的取代基,也可以未取代。烷基的碳数优选为1~12,更优选为1~6,进一步优选为1~4。r
11
,r
12
所表示的芳基的碳数优选为6~18,更优选为6~12,进一步优选为6。r
11
、r
12
优选为直链状或分支状烷基。
[0655]
r
13
所表示的烷基可以为直链状、分支状或环状的任意一个,优选为直链状或分支状。烷基可以具有上述的取代基,也可以未取代。烷基的碳数优选为1~12,更优选为1~6,进一步优选为1~4。r
13
所表示的芳基的碳数优选为6~18,更优选为6~12,进一步优选为6。r
13
优选为直链状或分支状烷基或芳基。
[0656]
关于r
14
及r
15
所表示的取代基,可举出以上述式(sq)进行说明的基团。其中,优选
为r
14
及r
15
的至少一个表示氰基或、
‑
coora。ra表示氢原子或取代基。作为取代基可举出上述的取代基。例如,优选为烷基、芳基。
[0657]
作为具有由上述式(a3
‑
7)表示的结构单元的树脂的市售品,可举出arton f4520(jsr corporation制)等。
[0658]
而且,树脂也优选使用marproof g
‑
0150m、g
‑
0105sa、g
‑
0130sp、g
‑
0250sp、g
‑
1005s、g
‑
1005sa、g
‑
1010s、g
‑
2050m、g
‑
01100、g
‑
01758(nof corporation.制、含环氧基的聚合物)。
[0659]
组合物包含颜料的情况下,优选树脂包含分散剂。
[0660]
作为分散剂而发挥作用的树脂优选为酸性型的树脂和/或碱性基型的树脂。
[0661]
在此,酸性类树脂表示酸基量比碱性基的量多的树脂。酸性类树脂为将树脂中的酸基的量与碱性基的量的合计量设为100摩尔%时,优选酸基量占70摩尔%以上的树脂,更优选实质上仅包含酸基。酸性类树脂所具有的酸基优选为羧基。酸性类树脂的酸值优选为40~105mgkoh/g,更优选为50~105mgkoh/g,进一步优选为60~105mgkoh/g。
[0662]
而且,碱性类树脂表示碱性基的量比酸基的量多的树脂。碱性基类树脂为将树脂中的酸基的量与碱性基的量的合计量设为100摩尔%时,碱性基的量优选占50摩尔%以上的树脂。碱性类树脂所具有的碱性基优选为氨。
[0663]
树脂根据其结构能够进一步分类为直链状高分子、末端改质型高分子、接枝型高分子、嵌段型高分子。
[0664]
作为末端改质型高分子,例如可以举出日本特开平3
‑
112992号公报、日本特表2003
‑
533455号公报等中所记载的末端具有磷酸基的高分子、日本特开2002
‑
273191号公报等中所记载的末端具有磺酸基的高分子、日本特开平9
‑
77994号公报等中所记载的具有有机色素的部分骨架或杂环的高分子等。并且,日本特开2007
‑
277514号公报中所记载的在高分子末端导入有两个以上的对颜料表面的锚定(anchor)部位(酸基、碱性基、有机色素的部分骨架或杂环等)的高分子的分散稳定性也优异,因此优选。
[0665]
作为接枝型高分子,例如可以举出日本特开昭54
‑
37082号公报、日本特表平8
‑
507960号公报、日本特开2009
‑
258668公报等中所记载的聚(低级伸烷基亚氨)与聚酯的反应产物、日本特开平9
‑
169821号公报等中所记载的聚烯丙基氨与聚酯的反应产物、日本特开平10
‑
339949号公报、日本特开2004
‑
37986号公报等中所记载的大分子单体与含氮原子单体的共聚物、日本特开2003
‑
238837号公报、日本特开2008
‑
9426号公报、日本特开2008
‑
81732号公报等中所记载的具有有机色素的部分骨架或杂环的接枝型高分子、日本特开2010
‑
106268号公报等中所记载的大分子单体与含酸基单体的共聚物等。作为大分子单体,例如可举出toagosei co.,ltd.制的大分子单体aa
‑
6(末端基为甲基丙烯酰基的聚甲基丙烯酸甲酯)、as
‑
6(末端基为甲基丙烯酰基的聚苯乙烯)、an
‑
6s(末端基为甲基丙烯酰基的苯乙烯与丙烯腈的共聚物)、ab
‑
6(末端基为甲基丙烯酰基的聚丙烯酸丁酯)、daicel corporation制的placcel fm5(甲基丙烯酸2
‑
羟基乙酯的ε
‑
己内酯5摩尔当量加成物)、fa10l(丙烯酸2
‑
羟基乙酯的ε
‑
己内酯10摩尔当量加成物)及日本特开平2
‑
272009号公报中所记载的聚酯系大分子单体等。
[0666]
作为嵌段型高分子,优选日本特开2003
‑
49110号公报、日本特开2009
‑
52010号公报等中所记载的嵌段型高分子。
[0667]
分散剂也能够使用包含由下述式(1)~式(4)的任一个表示的结构单元的接枝共聚物。
[0668]
[化学式40]
[0669][0670]
x1、x2、x3、x4及x5分别独立地表示氢原子或1价有机基团。氢原子或碳数优选为1~12的烷基,更优选为氢原子或甲基,尤其优选为甲基。w1、w2、w3及w4分别独立地表示氧原子或nh,优选为氧原子。r3表示分支或直链的伸烷基(碳数优选为1~10,更优选为2或3),从分散稳定性的观点考虑,优选
‑
ch2‑
ch(ch3)
‑
所表示的基团或
‑
ch(ch3)
‑
ch2‑
所表示的基团。r4表示氢原子或1价基团。y1、y2、y3及y4分别独立地表示2价连结基。z1、z2、z3、及z4分别独立地表示1价基团。n、m、p、及q分别独立地表示1~500的整数,j及k分别独立地表示2~8的整数。
[0671]
关于上述接枝共聚物,能够参考日本特开2012
‑
255128号公报的0025~0069段的记载,并将上述内容并入本说明书中。
[0672]
作为上述接枝共聚物的具体例,例如可举出以下。并且,能够使用日本特开2012
‑
255128号公报的0072~0094段中所记载的树脂。
[0673]
[化学式41]
[0674][0675]
分散剂也能够使用在主链及侧链的至少一者上含有氮原子的寡聚亚氨系树脂。作为寡聚亚氨系树脂,具有如下结构单元及侧链,且优选在主链及侧链的至少一者上具有碱性氮原子的树脂,该结构单元包含具有pka14以下的官能基的部分结构x,该侧链包含原子数40~10,000的侧链y。碱性氮原子若为呈碱性的氮原子,则并无特别限制。
[0676]
关于寡聚亚氨系树脂,例如可举出含有由下述式(i
‑
1)表示的结构单元、及由式(i
‑
2)表示的结构单元和/或由式(i
‑
2a)表示的结构单元的树脂等。
[0677]
[化学式42]
[0678][0679]
r1及r2分别独立地表示氢原子、卤素原子或烷基(碳数优选为1~6)。a分别独立地表示1~5的整数。*表示结构单元之间的连结部。
[0680]
r8及r9为含义与r1相同的基团。
[0681]
l是单键、伸烷基(碳数优选为1~6)、伸烯基(碳数优选为2~6)、伸芳基(碳数优选为6~24)、杂伸芳基(碳数优选为1~6)、亚氨基(碳数优选为0~6)、醚基、硫醚基、羰基或该等的组合的连结基。其中,优选单键或
‑
cr5r6‑
nr7‑
(亚氨基成为x或y的一者)。其中,r5及r6分别独立地表示氢原子、卤素原子、烷基(碳数优选为1~6)。r7是氢原子或碳数1~6的烷基。
[0682]
l
a
是与cr8cr9和n一同形成环结构的结构部位,优选组合cr8cr9的碳原子而形成碳数3~7的非芳香族杂环的结构部位。更优选组合cr8cr9的碳原子及n(氮原子)而形成5员~7员的非芳香族杂环的结构部位,进一步优选形成5员的非芳香族杂环的结构部位,尤其优选形成吡咯烷的结构部位。该结构部位可以进一步具有烷基等取代基。
[0683]
x表示具有pka14以下的官能基的基团。
[0684]
y表示原子数40~10,000的侧链。
[0685]
上述树脂(寡聚亚氨系树脂)可进一步含有选自由式(i
‑
3)、式(i
‑
4)及式(i
‑
5)表示的结构单元中的1种以上来作为共聚成分。上述树脂包含该种结构单元,由此能够进一步提高颜料的分散性能。
[0686]
[化学式43]
[0687][0688]
r1、r2、r8、r9、l、la、a及*的含义与式(i
‑
1)、(i
‑
2)、(i
‑
2a)中的规定相同。
[0689]
ya表示具有阴离子基的原子数40~10,000的侧链。由式(i
‑
3)表示的结构单元可通过在主链部具有一级或二级氨基的树脂中添加具有与氨反应而形成盐的基团的寡聚物或聚合物并进行反应来形成。
[0690]
关于上述的寡聚亚氨系树脂,能够参考日本特开2012
‑
255128号公报的0102~0166段的记载,并将上述内容并入本说明书中。作为寡聚亚氨系树脂的具体例,例如可举出以下。并且,能够使用日本特开2012
‑
255128号公报的0168~0174段中所记载的树脂。
[0691]
[化学式44]
[0692][0693]
分散剂也能够使用包含由式(p1)表示的结构单元的树脂。
[0694]
[化学式45]
[0695][0696]
式(p1)中,r1表示氢或甲基,r2表示伸烷基,z表示含氮杂环结构。
[0697]
作为r2所表示的伸烷基,并无特别限定,例如可优选举出亚甲基、伸乙基、三亚甲基、四亚甲基、六亚甲基、2
‑
羟基伸丙基、亚甲氧基、伸乙氧基、亚甲氧基羰基、亚甲基硫基(methylene thio group)等,更优选为亚甲基、亚甲氧基、亚甲氧基羰基、亚甲基硫基。
[0698]
z所表示的含氮杂环结构例如可以举出具有吡啶环、吡嗪环、嘧啶环、吡咯环、咪唑环、三唑环、四唑环、吲哚环、喹啉环、吖啶环、吩噻嗪环、吩噁嗪(phenoxazine)环、吖啶酮环、苯并咪唑结构、苯并三唑结构、苯并噻唑结构、环状酰氨结构、环状脲结构及环状酰亚氨结构者。该些中,作为z所表示的含氮杂环结构,优选由下述式(p2)或(p3)表示的结构。
[0699]
[化学式46]
[0700][0701]
式中,x为选自包含单键、伸烷基(例如,亚甲基、伸乙基、伸丙基、三亚甲基、四亚甲基等)、
‑
o
‑
、
‑
s
‑
、
‑
nr
‑
及
‑
c(=o)
‑
的群组中的任一个。另外,在此r表示氢原子或烷基。r表示烷基的情况下,例如可举出甲基、乙基、正丙基、异丙基、正丁基、第三级丁基、正己基、正辛基、2
‑
乙基己基、正十八烷基等。
[0702]
x优选为单键、亚甲基、
‑
o
‑
、
‑
c(=o)
‑
,尤其优选为
‑
c(=o)
‑
。
[0703]
式中,环a、环b及环c分别独立地表示芳香环。作为芳香环,例如可以举出苯环、萘环、茚环、薁环、芴环、蒽环、吡啶环、吡嗪环、嘧啶环、吡咯环、咪唑环、吲哚环、喹啉环、吖啶环、吩噻嗪环、吩噁嗪环、吖啶酮环、蒽醌环等,其中,优选苯环、萘环、蒽环、吡啶环、吩噁嗪环(phenoxazine ring)、吖啶环、吩噻嗪环、吖啶酮环、蒽醌环,尤其优选苯环、萘环、吡啶环。
[0704]
作为由式(p1)表示的结构单元的具体例,例如可举出以下。此外,能够参考日本特开2008
‑
009426号公报的0023段的记载并将上述内容并入本说明书中。
[0705]
[化学式47]
[0706][0707]
作为包含由式(p1)表示的结构单元的树脂的具体例,可举出以下。
[0708]
[化学式48]
[0709][0710]
分散剂可作为市售品而得到,作为该等的具体例,可举出kusumoto chemicals,ltd.制“da
‑
7301”、bykchemie公司制“disperbyk
‑
101(聚酰氨氨磷酸盐)、107(羧酸酯)、110(含有酸基的共聚物)、111(磷酸系分散剂)、130(聚酰氨)、161、162、163、164、165、166、170
(高分子共聚物)”、bykchemie公司制“byk
‑
p104、p105(高分子量不饱和聚羧酸)”、efka公司制“efka4047、4050~4165(聚氨基甲酸酯系)、efka4330~4340(嵌段共聚物)、4400~4402(改质聚丙烯酸酯)、5010(聚酯酰氨)、5765(高分子量聚羧酸盐)、6220(脂肪酸聚酯)、6745(酞菁衍生物)、6750(偶氮颜料衍生物)”、ajinomoto fine
‑
techno co.,inc.制“ajisper pb821、pb822、pb880、pb881”、kyoeisha chemical co.,ltd.制“flowlen tg
‑
710(氨基甲酸酯寡聚物)”、“polyflow no.50e、no.300(丙烯酸系共聚物)”、kusumoto chemicals,ltd.制“disparon ks
‑
860、873sn、874、#2150(脂肪族多元羧酸)、#7004(聚醚酯)、da
‑
703
‑
50、da
‑
705、da
‑
725”、kao corporation制“demo rn、n(萘磺酸福马林缩聚物)、ms、c、sn
‑
b(芳香族磺酸福马林缩聚物)”、kao corporation.制“homogenol l
‑
18(高分子聚羧酸)”、kao corporation.制“emulgen 920、930、935、985(聚氧乙烯壬基苯基醚)”、kao corporation.制“acetamin 86(硬脂氨乙酸盐)”、lubrizol japan limited制“solsperse 5000(酞菁衍生物)、22000(偶氮颜料衍生物)、13240(聚酯氨)、3000、12000、17000、20000、27000(末端部具有功能部的高分子)、24000、28000、32000、38500(接枝型高分子)”、nikko chemicals co.,ltd.制“nikkol t106(聚氧乙烯脱水山梨糖醇单油酸酯)、mys
‑
iex(聚氧乙烯单硬脂酸酯)”、kawaken fine chemicals co.,ltd.制“hinoact t
‑
8000e“、shin
‑
etsu chemical co.,ltd.制“有机硅氧烷聚合物kp341”、morishita&co.,ltd.制“efka
‑
46、efka
‑
47、efka
‑
47ea、efka polymer 100、efka polymer 400、efka polymer 401、efka polymer 450”、san nopco limited制“disperse aid6、disperse aid 8、disperse aid 15、disperse aid 9100”、adeka corporation制“adeka pluronic l31、f38、l42、l44、l61、l64、f68、l72、p95、f77、p84、f87、p94、l101、p103、f108、l121、p
‑
123”及sanyo chemical industries,ltd.制“ionet s
‑
20”等。
[0711]
组合物中的树脂的含量相对于组合物的总固体成分优选为1~80质量%。下限优选为5质量%以上,更优选为7质量%以上。上限优选为50质量%以下,更优选为30质量%以下。
[0712]
<<光聚合起始剂>>
[0713]
组合物能够含有光聚合起始剂。尤其,组合物包含具有如下基团的树脂或固化性化合物等、自由基聚合性成分的情况下,优选含有光聚合起始剂,该基团具有烯属不饱和键。作为光聚合起始剂,并无特别限制,能够从公知的光聚合起始剂中适当选择。例如,优选对从紫外线区域至可见区域的光线具有感光性者。光聚合起始剂优选为光自由基聚合起始剂。而且,光聚合起始剂优选含有至少1种在约300nm~800nm(更优选为330nm~500nm。)的范围内具有至少约50摩尔吸光数的化合物。
[0714]
作为光聚合起始剂,例如可举出卤化烃衍生物(例如,具有三嗪骨架者、具有噁二唑骨架者等)、酰基氧化膦等酰基膦化合物、六芳基双咪唑、肟衍生物等肟化合物、有机过氧化物、硫化合物(thio compound)、酮化合物、芳香族鎓盐、酮肟醚、氨基苯乙酮化合物、羟基苯乙酮等。作为具有三嗪骨架的卤化烃化合物,例如可以举出,若林等着、bull.chem.soc.japan,42,2924(1969)中所记载的化合物、英国专利1388492号说明书中所记载的化合物、日本特开昭53
‑
133428号公报中所记载的化合物、德国专利3337024号说明书中所记载的化合物、基于f.c.schaefer等的有机化学期刊(j.org.chem.),29,1527(1964)中所记载的化合物、日本特开昭62
‑
58241号公报中所记载的化合物、日本特开平5
‑
281728号公报中所记载的化合物、日本特开平5
‑
34920号公报中所记载的化合物、美国专利第4212976号说明书中所记载的化合物等。
[0715]
而且,从曝光感度的观点考虑,优选选自包含三卤甲基三嗪(trihalo methyl triazine)化合物、苄基二甲基缩酮化合物、α
‑
羟基酮化合物、α
‑
氨基酮化合物、酰基膦化合物、氧化膦化合物、茂金属化合物、肟化合物、三芳基咪唑(triallyl imidazole)二聚体、鎓化合物、苯并噻唑化合物、二苯甲酮化合物、苯乙酮化合物及其衍生物、环戊二烯
‑
苯
‑
铁络合物及其盐、卤甲基噁二唑化合物、3
‑
芳基取代香豆素化合物的群组中的化合物。
[0716]
作为光聚合起始剂,也能够优选使用羟基苯乙酮化合物(α
‑
羟基酮化合物)、氨基苯乙酮化合物(α
‑
氨基酮化合物)及酰基膦化合物。例如,还能够使用日本特开平10
‑
291969号公报中所记载的氨基苯乙酮系起始剂、日本专利第4225898号公报中所记载的酰基膦系起始剂。作为羟基苯乙酮化合物(α
‑
羟基酮化合物),能够使用irgacure
‑
184、darocur
‑
1173、irgacure
‑
500、irgacure
‑
2959,irgacure
‑
127(产品名、均为basf公司制)。作为氨基苯乙酮系化合物(α
‑
氨基酮化合物),能够使用作为市售品的irgacure
‑
907、irgacure
‑
369及irgacure
‑
379eg(产品名,均为basf公司制)。氨基苯乙酮系化合物(α
‑
氨基酮化合物)也能够使用吸收波长与365nm或405nm等光源匹配的日本特开2009
‑
191179号公报中所记载的化合物。
[0717]
作为酰基膦化合物,可以使用作为市售品的irgacure
‑
819及darocur
‑
tpo(产品名、均为basf公司制)。
[0718]
作为光聚合起始剂,可优选举出肟化合物。作为肟化合物的具体例,能够使用日本特开2001
‑
233842号公报中所记载的化合物、日本特开2000
‑
80068号公报中所记载的化合物、日本特开2006
‑
342166号公报中所记载的化合物。
[0719]
作为能够优选使用的肟化合物,例如可以举出3
‑
苯甲酰氧基亚氨基丁烷
‑2‑
酮、3
‑
乙酰氧基亚氨基丁烷
‑2‑
酮、3
‑
丙酰氧基亚氨基丁烷
‑2‑
酮、2
‑
乙酰氧基亚氨基戊烷
‑3‑
酮、2
‑
乙酰氧基亚氨基
‑1‑
苯基丙烷
‑1‑
酮、2
‑
苯甲酰氧基亚氨基
‑1‑
苯基丙烷
‑1‑
酮、3
‑
(4
‑
甲苯磺酰氧基)亚氨基丁烷
‑2‑
酮及2
‑
乙氧基羰氧基亚氨基
‑1‑
苯基丙烷
‑1‑
酮等。并且,也可以举出j.c.s.perkin ii(1979年)pp.1653
‑
1660、j.c.s.perkin ii(1979年)pp.156
‑
162、光聚合物科学与技术杂志(journal of photopolymer science and technology)(1995年)pp.202
‑
232、日本特开2000
‑
66385号公报、日本特开2000
‑
80068号公报、日本特表2004
‑
534797号公报、日本特开2006
‑
342166号公报的各公报中所记载的化合物等。市售品中,也能够优选使用irgacure
‑
oxe01(basf公司制)、irgacure
‑
oxe02(basf公司制)、irgacure
‑
oxe03(basf公司制)、irgacure
‑
oxe04(basf公司制)。并且,也可以使用tr
‑
pbg
‑
304(changzhou tronly new electronic materials co.,ltd.制)、adeka arkls nci
‑
930(adeka corporation制)。
[0720]
而且,作为上述记载以外的肟化合物,可以使用在咔唑环的n位上连结有肟的日本特表2009
‑
519904号公报中所记载的化合物、在二苯甲酮部位导入有杂取代基的美国专利第7626957号公报中所记载的化合物、在色素部位导入有硝基的日本特开2010
‑
15025号公报及美国专利公开2009
‑
292039号公报中所记载的化合物、国际公开wo2009/131189号公报中所记载的酮肟化合物、在同一分子内含有三嗪骨架和肟骨架的美国专利7556910号公报中所记载的化合物、对在405nm下具有吸收极大且对g射线光源具有良好的感度的日本特开
2009
‑
221114号公报中所记载的化合物、日本特开2014
‑
137466号公报的0076~0079段中所记载的化合物等。
[0721]
优选地、例如,能够参考日本特开2013
‑
29760号公报的0274~0275段,并将该内容并入本说明书中。
[0722]
具体而言,作为肟化合物,优选由下述式(ox
‑
1)所表示的化合物。肟化合物可以为肟的n
‑
o键是(e)体的肟化合物,也可以为肟的n
‑
o键是(z)体的肟化合物,也可以是(e)体与(z)体的混合物。
[0723]
[化学式49]
[0724][0725]
式(ox
‑
1)中,r及b分别独立地表示一价取代基,a表示二价有机基团,ar表示芳基。
[0726]
式(ox
‑
1)中,作为r所表示的一价取代基,优选为一价非金属原子团。
[0727]
作为一价非金属原子团,可举出烷基、芳基、酰基、烷氧基羰基、芳氧基羰基、杂环基、烷硫基羰基、芳硫基羰基等。并且,该些基团可以具有1个以上的取代基。而且,所述取代基可以进一步被其他取代基取代。
[0728]
作为取代基,可举出卤素原子、芳氧基、烷氧基羰基或芳氧基羰基、酰氧基、酰基、烷基、芳基等。
[0729]
式(ox
‑
1)中,作为b所表示的一价取代基,优选为芳基、杂环基、芳基羰基或杂环羰基。该些基团可以具有1个以上的取代基。作为取代基,能够例示出所述取代基。
[0730]
式(ox
‑
1)中,作为a所表示的二价有机基团,优选为碳数1~12的伸烷基、环伸烷基、伸炔基。该些基团可以具有1个以上的取代基。作为取代基,能够例示出所述取代基。
[0731]
作为光聚合起始剂,还能够使用具有芴环的肟化合物。作为具有芴环的肟化合物的具体例,可举出日本特开2014
‑
137466号公报中所记载的化合物。并将该内容并入本说明书中。
[0732]
作为光聚合起始剂也能够使用具有氟原子的肟化合物。作为具有氟原子的肟化合物的具体例,可以举出日本特开2010
‑
262028号公报记载的化合物、日本特表2014
‑
500852号公报中记载的化合物24、36~40、日本特开2013
‑
164471号公报中记载的化合物(c
‑
3)等。将该内容并入本说明书中。
[0733]
作为光聚合起始剂,能够使用具有硝基的肟化合物。也优选将具有硝基的肟化合物作为二聚体。作为具有硝基的肟化合物的具体例,可举出日本特开2013
‑
114249号公报的0031~0047段、日本特开2014
‑
137466号公报的0008~0012段、0070~0079段中所记载的化合物、日本专利4223071号公报的0007~0025段中所记载的化合物、adeka arkls nci
‑
831(adeka corporation制)。
[0734]
以下示出优选使用的肟化合物的具体例,但本发明并不限定在此。
[0735]
[化学式50]
[0736][0737]
[化学式51]
[0738][0739]
肟化合物优选为在350nm~500nm的波长区域具有极大吸收波长的化合物,更优选在360nm~480nm的波长区域具有吸收波长的化合物,尤其优选在365nm及405nm下的吸光度较高的化合物。
[0740]
从感度的观点考虑,肟化合物的365nm或405nm下的摩尔吸光是数优选为1,000~300,000,更优选为2,000~300,000,尤其优选为5,000~200,000。化合物的摩尔吸光是数的测定中能够使用公知的方法,具体而言,例如优选利用紫外可见分光光度计(varian公司制cary
‑
5分光光度计(spectrophotometer)),并使用乙酸乙酯溶剂以0.01g/l的浓度进行测定。
[0741]
光聚合起始剂的含量相对于组合物的总固体成分优选为0.1~50质量%,更优选为0.5~30质量%,进一步优选为1~20质量%。在该范围内可得到更加良好的感度和图案形成性。组合物可以仅含有一种光聚合起始剂,也可以含有两种以上。含有两种以上的情况下,其合计量优选成为上述范围内。
[0742]
<<酸产生剂>>
[0743]
组合物能够含有酸产生剂。尤其,作为固化性化合物而使用具有环氧基的化合物或具有羟甲基的化合物的情况下,优选含有酸产生剂。酸产生剂是优选为由光照射而产生酸的化合物(光酸产生剂)。关于酸产生剂,可举出由光照射而分解并产生酸的、重氮盐、鏻
盐、锍盐、錪鎓盐等鎓盐化合物、酰亚氨磺酸盐、肟磺酸盐、重氮二砜、二砜、o
‑
硝基苄基磺酸盐等磺酸盐化合物等。作为酸产生剂的种类、具体化合物、及优选例子,能够举出日本特开2008
‑
13646号公报的0066~0122段中所记载的化合物等,且能够将该化合物应用于本发明中。例如,能够举出三乙基铵九氟丁烷磺酸盐等。
[0744]
关于作为酸产生剂而优选的化合物,能够举出由下述式(b1)、式(b2)、式(b3)表示的化合物。
[0745]
[化学式52]
[0746][0747]
式(b1)~式(b3)中,r
201
~r
207
分别独立地表示有机基团。x
‑
表示非亲核性阴离子,可优选举出磺酸阴离子、羧酸阴离子、双(烷基磺酰基)酰氨阴离子、三(烷基磺酰基)甲基化物阴离子、bf4‑
、pf6‑
、sbf6‑
或以下所示的基团等,优选为bf4‑
、pf6‑
、sbf6‑
。
[0748]
作为酸产生剂的市售品,可举出wpag
‑
469(wako pure chemical co.,ltd.制)、cpi
‑
100p(san
‑
apro ltd.制)等。
[0749]
酸产生剂的含量相对于组合物的总固体成分优选为0.1~50质量%,更优选为0.5~30质量%,进一步优选为1~20质量%。组合物可以仅包含一种酸产生剂,也可以包含两种以上。包含两种以上的情况下,优选其合计量为上述范围。
[0750]
<<催化剂>>
[0751]
组合物能够进一步含有催化剂。尤其,作为固化性化合物而使用具有烷氧基甲硅烷基的化合物的情况下,通过含有催化剂,溶胶
‑
凝胶反应得到促进,从而可得到坚固的固化膜。作为催化剂,可举出酸催化剂、碱催化剂等。作为酸催化剂,可举出盐酸、硝酸、硫酸、亚硫酸、硫化氢、高氯酸、过氧化氢、碳酸、甲酸或乙酸等羧酸、以其他元素或取代基取代rcooh所表示的结构式r的取代羧酸、苯磺酸等磺酸、磷酸等。进而,还可使用氯化铝、乙酰丙酮铝、氯化锌、氯化锡、三氟化硼二乙醚络合物、三甲基碘硅烷等路易斯酸。而且,作为碱催化剂,可举出氨水等氨性碱化合物、乙氨或苯氨等有机氨等。而且,催化剂还能够使用日本特开2013
‑
201007号公报的0070~0076段中所记载的催化剂。
[0752]
催化剂的含量相对于固化性化合物的100质量份(优选具有烷氧基甲硅烷基的化合物的100质量份)优选为0.1~100质量份,更优选为0.1~50质量份,进一步优选为0.1~20质量份。组合物可以仅包含一种催化剂,也可以包含两种以上。包含两种以上的情况下,其合计量优选为上述范围。
[0753]
<<溶剂>>
[0754]
组合物能够含有溶剂。作为溶剂,可举出有机溶剂。关于溶剂,若满足各成分的溶解性或组合物的涂布性,则基本上并无特别限制,优选考虑组合物的涂布性、安全性而进行选择。
[0755]
作为有机溶剂的例子,例如可举出以下者。
[0756]
作为酯类,例如可优选举出乙酸乙酯、乙酸正丁酯、乙酸异丁酯、乙酸环己酯、甲酸
戊酯、乙酸异戊酯、丙酸丁酯、丁酸异丙酯、丁酸乙酯、丁酸丁酯、乳酸甲酯、乳酸乙酯、烷氧基乙酸烷基酯(例如,烷氧基乙酸甲酯、烷氧基乙酸乙酯、烷氧基乙酸丁酯(例如,甲氧基乙酸甲酯、甲氧基乙酸乙酯、甲氧基乙酸丁酯、乙氧基乙酸甲酯、乙氧基乙酸乙酯等))、3
‑
烷氧基丙酸烷基酯类(例如,3
‑
烷氧基丙酸甲酯、3
‑
烷氧基丙酸乙酯等(例如,3
‑
甲氧基丙酸甲酯、3
‑
甲氧基丙酸乙酯、3
‑
乙氧基丙酸甲酯、3
‑
乙氧基丙酸乙酯等))、2
‑
烷氧基丙酸烷基酯类(例如,2
‑
烷氧基丙酸甲酯、2
‑
烷氧基丙酸乙酯、2
‑
烷氧基丙酸丙酯等(例如,2
‑
甲氧基丙酸甲酯、2
‑
甲氧基丙酸乙酯、2
‑
甲氧基丙酸丙酯、2
‑
乙氧基丙酸甲酯、2
‑
乙氧基丙酸乙酯))、2
‑
烷氧基
‑2‑
甲基丙酸甲酯及2
‑
烷氧基
‑2‑
甲基丙酸乙酯(例如,2
‑
甲氧基
‑2‑
甲基丙酸甲酯、2
‑
乙氧基
‑2‑
甲基丙酸乙酯等)、丙酮酸甲酯、丙酮酸乙酯、丙酮酸丙酯、乙酰乙酸甲酯、乙酰乙酸乙酯、2
‑
氧代丁酸甲酯、2
‑
氧代丁酸乙酯等,以及作为醚类,例如可优选举出二乙二醇二甲醚、四氢呋喃、乙二醇单甲醚、乙二醇单乙醚、甲基纤溶剂乙酸酯、乙基纤溶剂乙酸酯、二乙二醇单甲醚、二乙二醇单乙醚、二乙二醇单丁醚、丙二醇单甲醚、丙二醇单甲醚乙酸酯、丙二醇单乙醚乙酸酯、丙二醇单丙醚乙酸酯等,以及作为酮类,例如可优选举出甲乙酮、环己酮、环戊酮、2
‑
庚酮、3
‑
庚酮等,以及作为芳香族烃类,例如可优选举出甲苯、二甲苯等。
[0757]
有机溶剂可以单独使用一种,也可以组合使用两种以上。组合使用两种以上的有机溶剂的情况下,尤其优选由选自上述3
‑
乙氧基丙酸甲酯、3
‑
乙氧基丙酸乙酯、乙基纤溶剂乙酸酯、乳酸乙酯、二乙二醇二甲醚、乙酸丁酯、3
‑
甲氧基丙酸甲酯、2
‑
庚酮、环己酮、乙基卡必醇乙酸酯、丁基卡必醇乙酸酯、丙二醇甲醚及丙二醇甲醚乙酸酯中的两种以上构成的混合溶液。
[0758]
优选使用金属含量较少的溶剂,溶剂的金属含量优选例如10ppb以下。依需要可以使用ppt级溶剂,该种高纯度溶剂例如由toyo gosei co.,ltd.提供。
[0759]
作为从溶剂去除金属等杂质的方法,例如能够举出蒸馏(分子蒸馏或薄膜蒸馏等)或使用滤波器来进行的过滤。作为使用滤波器进行的过滤中的滤波器孔径,孔径尺寸优选为10nm以下,更优选为5nm以下,进一步优选为3nm以下。作为滤波器的材质,优选为聚四氟乙烯制、聚乙烯制、尼龙制滤波器。
[0760]
溶剂可以包含异构体(原子数相同但结构不同的化合物)。可以仅包含一种异构体,也可以包含复数种。
[0761]
有机溶剂的过氧化物的含有率优选为0.8mmol/l以下,更优选实质上不含过氧化物。
[0762]
溶剂的含量相对于组合物的总量优选为10~90质量%,更优选为20~80质量%,进一步优选为25~75质量%。
[0763]
<<聚合抑制剂>>
[0764]
组合物中,为了在制作或保存组合物时阻止固化性化合物的不必要的热聚合,可以含有聚合抑制剂。
[0765]
作为聚合抑制剂,可举出对苯二酚、对甲氧基苯酚、二
‑
第三丁基
‑
对甲酚、五倍子酚、第三丁基邻苯二酚、苯醌、4,4
’‑
硫双(3
‑
甲基
‑6‑
第三丁基苯酚)、2,2
’‑
亚甲基双(4
‑
甲基
‑6‑
第三丁基苯酚)、n
‑
亚硝基苯基羟基氨盐(铵盐、第一铈盐等)。其中,优选对甲氧基苯酚
[0766]
聚合抑制剂的含量相对于组合物的总固体成分优选为0.01~5质量%。
[0767]
<<界面活性剂>>
[0768]
从进一步提高涂布性的观点考虑,组合物可以含有各种界面活性剂。作为界面活性剂,能够使用氟系界面活性剂、非离子系界面活性剂、阳离子系界面活性剂、阴离子系界面活性剂、硅酮系界面活性剂等各种界面活性剂。
[0769]
使上述组合物中含有氟系界面活性剂,由此作为涂布液而进行制备时的液体特性(尤其流动性)得到进一步提高,且能够进一步改善涂布厚度的均匀性或省液性。即,使用应用了含有氟系界面活性剂的组合物的涂布液来形成膜的情况下,被涂布面与涂布液之间的界面张力下降,对被涂布面的润湿性得到改善,且对被涂布面的涂布性得到提高。因此,能够更优选形成厚度不均较小的厚度均匀的膜。
[0770]
氟系界面活性剂中的氟含有率优选为3~40质量%,更优选为5~30质量%,尤其优选为7~25质量%。从涂布膜的厚度的均匀性及省液性方面考虑,氟含有率在该范围内的氟系界面活性剂较有效,在组合物中的溶解性也为良好。
[0771]
作为氟系界面活性剂,具体而言可举出日本特开2014
‑
41318号公报的0060~0064段(相对应的国际公开wo2014/17669号公报的0060~0064段)等中所记载的截面活性剂、日本特开2011
‑
132503号公报的0117~0132段中所记载的界面活性剂,并将该内容并入本说明书中。作为氟系界面活性剂的市售品,例如可以举出megaface f171、megaface f172、megaface f173、megaface f176、megaface f177、megaface f141、megaface f142、megaface f143、megaface f144、megaface r30、megaface f437、megaface f475、megaface f479、megaface f482、megaface f554、megaface f780、rs
‑
72
‑
k(以上为dic corporation制)、fluorad fc430、fluorad fc431、fluorad fc171(以上为sumitomo 3m limited制)、surflon s
‑
382、surflon sc
‑
101、surflon sc
‑
103、surflon sc
‑
104、surflon sc
‑
105、surflon sc1068、surflon sc
‑
381、surflon sc
‑
383、surflon s393、surflon kh
‑
40(以上为asahi glass co.,ltd.制)、polyfox pf636、pf656、pf6320、pf6520、pf7002(omnova公司制)等。
[0772]
氟系界面活性剂还能够使用嵌段聚合物,作为具体例,例如可举出日本特开2011
‑
89090号公报中所记载的化合物。氟系界面活性剂还能够优选使用含氟高分子化合物,该含氟高分子化合物包含源自具有氟原子的(甲基)丙烯酸酯化合物的重复单元和源自具有2个以上(优选为5个以上)伸烷氧基(优选为伸乙氧基、伸丙氧基)的(甲基)丙烯酸酯化合物的重复单元。下述化合物也作为在本发明中所使用的氟系界面活性剂而例示。
[0773]
[化学式53]
[0774][0775]
上述化合物的重量均分子量优选为3,000~50,000,例如,为14,000。
[0776]
而且,氟系界面活性剂也能够使用在侧链具有烯属不饱和基团的含氟聚合物。作为具体例,可举出日本特开2010
‑
164965号公报的0050~0090段及0289~0295段中所记载的化合物、例如dic corporation制的megaface rs
‑
101、rs
‑
102、rs
‑
718k、rs
‑
72
‑
k等。氟系界面活性剂还能够使用日本特开2015
‑
117327号公报的0015~0158段中所记载的化合物。
[0777]
而且,氟系界面活性剂也能够优选使用丙烯酸系化合物,其为具有含氟原子的官能基的分子结构,若施加热则含氟原子的官能基的一部分被切断而氟原子挥发。作为该种氟系界面活性剂,可使用如下:dic corporation制的megaface ds系列(化学工业日报、2016年2月22日)(日经产业新闻、2016年2月23日),例如megaface ds
‑
21,并能够使用该些。
[0778]
作为非离子是界面活性剂,具体而言可举出甘油、三羟甲基丙烷、三羟甲基乙烷及该些乙氧基化物及丙氧基化物(例如,甘油丙氧基化物、甘油乙氧基化物等)、聚氧乙烯月桂基醚、聚氧乙烯硬脂基醚、聚氧乙烯油基醚,聚氧乙烯辛基苯基醚、聚氧乙烯壬基苯基醚、聚乙二醇二月桂酸酯、聚乙二醇二硬脂酸酯、脱水山梨醇脂肪酸酯(basf公司制的pluronicl10、l31、l61、l62、10r5、17r2、25r2、tetronic304、701、704、901、904、150r1)、solsperse20000(lubrizol japan limited制)等。而且,还能够使用wako pure chemical industries,ltd.制的ncw
‑
101、ncw
‑
1001、ncw
‑
1002。
[0779]
作为阳离子系界面活性剂,具体而言可举出有机硅氧烷聚合物kp341(shi n
‑
etsu chemical co.,ltd.制)、(甲基)丙烯酸系(共)聚合物polyflow no.75、no.90、no.95(kyoeisha chemical co.,ltd.制)、w001(yusho co.,ltd.)等。
[0780]
作为阴离子系界面活性剂,具体而言,可以举出w004、w005、w017(yush o co.,ltd.制)、sandetto bl(sanyo chemical industries,ltd.制)等。
[0781]
作为硅酮系界面活性剂,例如可以举出toray silicone dc3pa、toray silicone sh7pa、toray silicone dc11pa、toray silicone sh21pa、toray silicone sh28pa、toray silicone sh29pa、toray silicone sh30pa、toray silicone sh8400(以上为dow corning toray co.,ltd.制)、tsf
‑
4440、tsf
‑
4300、tsf
‑
4445、tsf
‑
4460、tsf
‑
4452(以上为momentive performance materials inc.制)、kp341、kf6001、kf6002(以上为shin
‑
etsu silicone co.,ltd.制)、byk307、byk323、byk330(以上为byk
‑
chemie corporation制)等。
[0782]
界面活性剂可以仅使用一种,也可以组合两种以上。
[0783]
界面活性剂的含量相对于组合物总固体成分优选为0.001~2.0质量%,更优选为0.005~1.0质量%。
[0784]
<<紫外线吸收剂>>
[0785]
组合物可以含有紫外线吸收剂。紫外线吸收剂优选为共轭二烯系化合物,更优选为由下述式(1)表示的化合物。
[0786]
[化学式54]
[0787][0788]
r1及r2分别独立地表示氢原子、碳数1~20的烷基、或碳数6~20的芳基,r1与r2可以彼此相同也可以不同,但不会同时表示氢原子。
[0789]
r3及r4表示吸电子基团。吸电子基团是,哈米特取代基常数σp值(以下,简称为“σp
值”。)优选为0.20以上且1.0以下的基团,σp值更优选为0.30以上且0.8以下的基团。作为r3、r4,优选为酰基、氨基甲酰基、烷氧基羰基、芳氧羰基、氰基、硝基、烷基磺酰基、芳基磺酰基、磺酰氧基、氨磺酰基,尤其优选为酰基、氨基甲酰基、烷氧基羰基、芳氧羰基、氰基、烷基磺酰基、芳基磺酰基、磺酰氧基、氨磺酰基。关于上述式(1),能够参考日本特开2010
‑
049029号公报的0148~0158段的记载,并将该内容并入本说明书中。
[0790]
作为上由述式(1)表示的化合物的具体例,可举出日本特开2010
‑
049029号公报的0160~0162段中所记载的化合物,并将该内容并入本说明书中。
[0791]
作为紫外线吸收剂的市售品,例如可举出uv503(daito chemical co.,ltd.)等。
[0792]
紫外线吸收剂的含量相对于组合物的总固体成分优选为0.01~10质量%,更优选为0.01~5质量%。
[0793]
<<其他成分>>
[0794]
组合物可以依需要而含有分散剂、增感剂、固化促进剂、填料、热固化促进剂、热聚合抑制剂、增塑剂、粘附促进剂及其他助剂类(例如,导电性粒子、填充剂、消泡剂、阻燃剂、调平剂、剥离促进剂、抗氧化剂、香料、表面张力调节剂、链转移剂等)。通过适当地含有该些成分,能够调整作为目标的近红外线截止滤波器等光学滤波器的稳定性、膜物性等性质。关于该些成分,例如能够参考日本特开2012
‑
003225号公报的0183段(相对应的美国专利申请公开第2013/0034812号说明书的0237段)的记载,日本特开2008
‑
250074号公报的0101~0104、0107~0109段等的记载,并将该些内容并入本说明书中。而且,作为抗氧化剂,可举出苯酚化合物、亚磷酸酯化合物、硫醚化合物等。更优选分子量500以上的苯酚化合物、分子量500以上的亚磷酸酯化合物或分子量500以上的硫醚化合物。该些可以混合使用两种以上。作为苯酚化合物,能够使用作为苯酚系抗氧化剂而周知的任意苯酚化合物。作为优选的苯酚化合物,可举出受阻酚化合物。尤其,优选在与苯酚性羟基相邻的部位(邻位)具有取代基的化合物。作为所述取代基,优选碳数1~22的取代或未取代的烷基,更优选甲基、乙基、丙酰基、异丙酰基、丁基、异丁基、第三级丁基、戊基、异戊基、第三级戊基、己基、辛基、异辛基、2
‑
乙基己基。而且,也优选铜一分子内具有苯酚基和亚磷酸酯基的化合物(抗氧化剂)。而且,抗氧化剂还能够优选使用磷系抗氧化剂。作为磷系抗氧化剂,可举出选自包含三[2
‑
[[2,4,8,10
‑
四(1,1
‑
二甲基乙基)二苯并[d,f][1,3,2]二噁磷环庚烷
‑6‑
基]氧基]乙基]氨、三[2
‑
[(4,6,9,11
‑
四叔丁基二苯并[d,f][1,3,2]二噁磷环庚烷
‑2‑
基)氧基]乙基]氨及亚磷酸酯乙基双(2,4
‑
二叔丁基
‑6‑
甲基苯基)的群组的至少一种化合物。该些可作为市售品而轻易获得,可举出adkstab ao
‑
20、adkstab ao
‑
30、adkstab ao
‑
40、adkstab ao
‑
50、adkstab ao
‑
50f、adkstab ao
‑
60、adkstab ao
‑
60g、adkstab ao
‑
80、adkstab ao
‑
330(adeka corporation)等。抗氧化剂的含量相对于组合物的总固体成分优选为0.01~20质量%,更优选为0.3~15质量%。抗氧化剂可以仅为一种,也可以为两种以上。两种以上的情况下,合计量优选为上述范围。
[0795]
(组合物的制备方法)
[0796]
组合物能够由混合所述成分来制备。
[0797]
制备组合物时,可以一次性配合各成分,也能够将各成分溶解和/或分散于溶剂之后逐一进行配合。并且,关于配合时的投入顺序和作业条件,并不受特别限制。例如,可以将所有成分同时溶解和/或分散于溶剂来制备组合物,也可以依需要,将各成分适当地作为两
个以上的溶液或分散液,且使用时(涂布时)将该些进行混合来制备组合物。
[0798]
制备组合物时,以去除杂质或减少缺陷等为目的,优选利用过滤器进行过滤。若过滤器为从先前就使用于过滤用途等者,则并无特别限定。例如,可以举出使用了聚四氟乙烯(ptfe)等氟树脂、尼龙(例如尼龙
‑
6、尼龙
‑
6,6)等聚酰氨系树脂、聚乙烯、聚丙烯(pp)等聚烯烃树脂(包含高密度、超高分子量的聚烯烃树脂)等原材料的过滤器。该等原材料中,优选为聚丙烯(包含高密度聚丙烯)及尼龙。
[0799]
过滤器的孔径是0.01~7.0μm左右为适当,优选为0.01~3.0μm左右,更优选为0.05~0.5μm左右。通过设为该范围内,能够可靠地去除在后制程中可阻碍均匀的组合物的制备和平滑的膜的形成等的微细的杂质。而且,也优选使用纤维状滤材,作为滤材例如可举出聚丙烯纤维、尼龙纤维、玻璃纤维等,具体而言能够使用roki techno co.,ltd.制的sbp类型系列(sbp008等)、tpr类型系列(tpr002、tpr005等)、shpx类型系列(shpx003等)滤芯。
[0800]
使用过滤器时,可以组合不同的过滤器。此时,利用第1过滤器的过滤可以仅进行一次,也可以进行两次以上。
[0801]
而且,也可以在上述范围内组合不同孔径的第1过滤器。此处的孔径能够参考过滤器制作商的标称值。作为市售的过滤器,例如能够从由nihon pall ltd.(dfa4201nxey等)、advantec toyo kaisha,ltd.、japan entegris inc.(旧japan microlis co.,ltd.)或kitz micro filter corporation等提供的各种过滤器中选择。
[0802]
第2滤波器能够使用以与上述的第1滤波器相同的材料等形成者。
[0803]
例如,利用第1滤波器的过滤可以过滤分散液,并混合其他成分之后,可以利用第2滤波器的过滤进行。
[0804]
关于组合物的粘度(23℃),例如通过涂布来形成膜的情况下,优选在1~3000mpa
·
s的范围。下限优选为3mpa
·
s以上,更优选为5mpa
·
s以上。上限优选为2000mpa
·
s以下,更优选为1000mpa
·
s以下。
[0805]
本发明的组合物还能够使用于固体成像元件的受光侧中的近红外线截止滤波器(例如,针对晶圆级透镜的近红外线截止滤波器等)、固体成像元件的背面侧(与受光侧相反一侧)中的近红外线截止滤波器等。而且,可以将组合物直接涂布于图像传感器上形成涂膜后使用。
[0806]
组合物由于能够以可涂布状态供给,因此能够轻松地在固体成像元件的所希望的部件或位置形成近红外线截止滤波器。
[0807]
而且,还可将本发明的组合物应用于玻璃基材或含铜的层中。
[0808]
而且,组合物包含彩色着色剂的情况下,还能够使用于滤色器的像素形成中。
[0809]
而且,可以组合使用组合物的像素和选自红、绿、蓝、品红、黄、青、黑及无色的像素来作为滤色器。
[0810]
<膜、近红外线截止滤波器、层叠体>
[0811]
接着,对本发明的膜进行说明。本发明的膜为使用上述的组合物而形成者。本发明的膜的红外线屏蔽性及可见透明性优异,且很难产生光谱变化,(尤其,即使暴露于高温高湿的环境下也很难产生光谱变化),因此能够优选用作近红外线截止滤波器、红外线透射滤波器。而且,也能够用作热射线屏蔽滤波器。膜是可以具有图案,也可以是不具有图案的膜(平坦膜)。并且,膜可以以积层在支撑体上的状态使用,也可以从支撑体剥离膜。另外,将本
发明的膜用作红外线透射滤波器的情况下,红外线透射滤波器例如可举出屏蔽可见光,并透射波长900nm以上的波长的光的滤波器。另外,将膜用作红外线透射滤波器的情况下,使用包含上述近红外线吸收化合物a、及屏蔽可见光的色材(优选为含有两种以上的彩色着色剂的色材或至少含有有机系黑色着色剂的色材)的组合物的滤波器、或除了包含近红外线吸收化合物a的层的外,还优选另有屏蔽可见光的色材的层的滤波器。将膜用作红外线透射滤波器的情况下,近红外线吸收化合物a具有将所透射的光(近红外线)限定在更靠长波长侧的作用。
[0812]
而且,本发明的近红外线截止滤波器为使用上述的组合物而形成者。
[0813]
本发明的膜的膜厚能够依目的而适当调整。膜厚优选为20μm以下,更优选为10μm以下,进一步优选为5μm以下。膜厚的下限优选为0.1μm以上,更优选为0.2μm以上,进一步优选为0.3μm以上。
[0814]
本发明的膜(近红外线截止滤波器)能够与包含彩色着色剂的滤色器组合来使用。滤色器能够通过使用包含彩色着色剂的着色组合物来制作。作为彩色着色剂,能够举出以上述组合物进行说明的彩色着色剂。着色组合物能够进一步含有树脂、固化性化合物、光聚合起始剂、界面活性剂、溶剂、聚合抑制剂、紫外线吸收剂等。关于该等详细内容,可举出以上述组合物进行说明的材料。而且,也可将本发明的膜(近红外线截止滤波器)设为如下滤波器,即含有彩色着色剂,并具备作为近红外线截止滤波器和滤色器的功能。
[0815]
而且,本发明的层叠体具有本发明的近红外线截止滤波器和包含彩色着色剂的滤色器。层叠体中,近红外线截止滤波器与滤色器可以在厚度方向上相邻,也可以不相邻。近红外线截止滤波器与滤色器在厚度方向上不相邻的情况下,可以在与形成有滤色器的基材不同的基材上形成近红外线截止滤波器,也可以在近红外线截止滤波器与滤色器之间夹有构成固体成像元件的其他部件(例如,微透镜、平坦化层等)。
[0816]
另外,本发明中,近红外线截止滤波器是指,透射可见光域的波长的光(可见光),且屏蔽近红外域的波长的光(近红外线)的至少一部分的滤波器。近红外线截止滤波器可以为透射可见光域的所有波长的光者,也可以为透射可见光域的波长的光中的特定波长域的光,且屏蔽特定波长域的光者。而且,本发明中,滤色器是指,透射可见光域的波长的光中的特定波长域的光,且屏蔽特定波长域的光的滤波器。而且,红外线透射滤波器是指,屏蔽可见区域的波长的光,且透射近红外域的波长的光(近红外线)的至少一部分的滤波器。
[0817]
将本发明的膜用作近红外线截止滤波器的情况下,除了本发明的膜的外,还可以进一步具有含铜的层、介电质多层膜、紫外线吸收层等。
[0818]
近红外线截止滤波器进一步具有含铜的层和/或介电质多层膜,由此能够得到视角较广,且红外线屏蔽性优异的近红外线截止滤波器。而且,近红外线截止滤波器进一步具有紫外线吸收层,由此能够得到紫外线屏蔽性优异的近红外线截止滤波器。作为紫外线吸收层,例如能够参考国际公开wo2015/099060号公报的0040~0070段、0119~0145段中所记载的吸收层,并将该内容并入本说明书中。作为介电质多层膜,能够参考日本特开2014
‑
41318号公报的0255~0259段中的记载,并将该内容并入本说明书中。作为含铜的层,能够使用由含铜的玻璃构成的玻璃基材(含铜的玻璃基材)或含铜络合物的层(含铜络合物的层)。作为含铜的玻璃基材,可举出含铜的磷酸盐玻璃、含铜的氟磷酸盐玻璃等。作为含铜的玻璃的市售品,可举出nf
‑
50(agc techno glass co.,ltd.制产品名)、bg
‑
60、bg
‑
61(以上
为schott ag制产品名)、cd5000(hoya group制产品名)等。作为含铜络合物的层,可举出通过使用含铜络合物的组合物而形成的层。铜络合物优选为在700~1200nm的波长区域具有极大吸收波长的化合物。关于铜络合物的极大吸收波长,更优选为在720~1200nm的波长区域具有极大吸收波长,进一步优选为在800~1100nm的波长区域具有极大吸收波长。关于铜络合物,可举出以上述的其他近红外线吸收化合物进行说明的材料等。
[0819]
将本发明的膜用作近红外线截止滤波器的情况下,优选膜在波长650~1000nm的范围内具有极大吸收波长。
[0820]
而且,近红外线截止滤波器的可见透明性的优选范围中,优选在波长400~550nm的平均透射率为70%以上,更优选为80%以上,进一步优选为85%以上,尤其优选为90%以上。而且,优选在波长400~550nm的所有范围内的透射率为70%以上,更优选为80%以上,进一步优选为90%以上。
[0821]
而且,近红外线截止滤波器的红外线屏蔽性的优选范围根据用途而不同,优选在波长700~1000nm的范围的至少一处的透射率为20%以下,更优选15%以下,进一步优选为10%以下。
[0822]
例如,使用于屏蔽较宽的波长区域的红外线的近红外线截止滤波器的情况下,近红外线截止滤波器的红外线屏蔽性优选在波长700~800nm的范围内的透射率最低的值为20%以下,更优选为10%以下,进一步优选为5%以下,尤其优选为1%以下。具有该种光谱特性的近红外线截止滤波器中,在波长700~800nm的范围的红外线屏蔽性优异。关于具有该种光谱特性的近红外线截止滤波器,可以仅由实现本发明的膜来实现,也可以将本发明的膜与其他层组合来实现。例如,可将本发明的膜与含铜的层的组合作为优选的一例而举出。
[0823]
而且,使用于选择性地屏蔽规定的波长范围内的红外线的近红外线截止滤波器的情况下,关于近红外线截止滤波器的红外线屏蔽性的优选范围,近红外线截止滤波器的极大吸收波长
±
25nm的范围内的平均透射率优选为20%以下,更优选为15%以下,进一步优选为10%以下。关于该种光谱特性,可以仅由本发明的膜来实现,也可以将本发明的膜与其他层组合来实现。
[0824]
将本发明的膜用作红外线透射滤波器的情况下,优选具有以下(1)的光谱特性。根据该方式,可设为能够以源自可见光线的杂讯较少的状态透射红外线的膜。
[0825]
(1)波长400~830nm的范围内的膜的厚度方向上的光的透射率的最大值为20%以下,波长1000~1300nm的范围内的膜的厚度方向上的光的透射率的最小值为80%以上。具有该种光谱特性的膜能够优选用作屏蔽波长400~750nm的范围的光,且透射波长900nm以上的光的红外线透射滤波器。
[0826]
膜的光谱特性为使用紫外可见近红外分光光度计(hitachi high
‑
technologies corporation.制u
‑
4100),在波长300~1300nm的范围内测定透射率的值。
[0827]
将本发明的膜用作近红外线截止滤波器或红外线透射滤波器的情况下,能够组合使用近红外线截止滤波器与红外线透射滤波器。组合使用近红外线截止滤波器与红外线透射滤波器,由此能够优选使用于检测特定波长的红外线的红外线传感器的用途。组合使用两个滤波器的情况下,能够使用本发明的组合物来形成近红外线截止滤波器及红外线透射滤波器该两者,也能够使用本发明的组合物来仅形成任意一个。
[0828]
本发明的膜能够使用于ccd(电荷耦合元件)或cmos(互补型金属氧化膜半导体)等固体成像元件或红外线传感器、图像显示装置等各种装置中。而且,本发明的膜可使用于如下机构:具有吸收或截止近红外线的功能的透镜(数码相机、行动电话、车载相机等相机用透镜、f
‑
θ透镜、拾取透镜等光学透镜)及半导体受光元件用的光学滤波器、以选择性利用太阳光为目的的农业用涂层剂、利用近红外线的吸收热的记录介质、电子设备用或照片用近红外线滤波器、护眼镜、太阳镜、热射线遮断滤波器、读取记录光学文字用、机密文件防影印用、电子照片感光体、激光焊接等。且作为ccd相机用杂讯截止滤波器、cmos图像传感器用滤波器也有用。
[0829]
<图案形成方法>
[0830]
本发明的图案形成方法包含使用本发明的组合物在支撑体上形成组合物层的工序、通过光刻法或干式蚀刻法在组合物层上形成图案的工序。
[0831]
制作积层本发明的膜和滤色器而成的层叠体的情况下,可以分别进行膜的图案形成和滤色器的图案形成。而且,也可以在本发明的膜与滤色器的层叠体上进行图案形成。即,可以同时进行膜和滤色器的图案形成。
[0832]
分别进行膜(近红外线截止滤波器)和滤色器的图案形成的情况是指如下方式。仅对膜(近红外线截止滤波器)及滤色器中的任意一个进行图案形成。接着,在图案已形成的滤波器层上形成另一滤波器层。接着,对未进行图案形成的滤波器层进行图案形成。
[0833]
图案形成方法可以是基于光微影的图案形成方法,也可以是基于干式蚀刻的图案形成方法。
[0834]
若为基于光微影的图案形成方法,则无需进行干式蚀刻工序,因此可得到能够削减工序数的效果。
[0835]
若为基于干式蚀刻的图案形成方法,则本发明的组合物无需具有光微影功能,因此可得到能够提高近红外线吸收剂等的浓度的效果。
[0836]
分别进行膜(近红外线截止滤波器)的图案形成和滤色器的图案形成的情况下,各滤波器层的图案形成方法可以仅通过光刻法或仅通过干式蚀刻法来进行。而且,还可以通过光刻法对一个滤波器层进行图案形成,且通过干式蚀刻法对另一滤波器层进行图案形成。并用干式蚀刻法和光刻法来进行图案形成的情况下,对第1层的图案,通过干式蚀刻法来进行图案形成,且对第2层以后的图案,优选通过光刻法来进行图案形成。
[0837]
基于光刻法的图案形成优选包含如下工序:使用各组合物,在支撑体上形成组合物层的工序;将组合物层曝光成图案状的工序;及对未曝光部进行显影去除而形成图案的工序。可依需要来设置对组合物层进行烘烤的工序(预烘烤工序)及对经显影的图案进行烘烤的工序(后烘烤工序)。
[0838]
而且,基于干式蚀刻法的图案形成优选包含如下工序:使用各组合物,在支撑体上形成组物层并进行固化来形成固化物层的工序;在固化物层上形成光阻剂层的工序;通过进行曝光及显影而将光阻剂层图案化来得到抗蚀剂图案的工序;将抗蚀剂图案作为蚀刻遮罩而对固化物层进行干式蚀刻来形成图案的工序。
[0839]
<<形成组合物层的工序>>
[0840]
形成组合物层的工序中,使用各组合物在支撑体上形成组合物层。
[0841]
作为支撑体,例如能够使用在基板(例如,硅基板)上设有ccd或cmos等的固体成像
元件(受光元件)的固体成像元件用基板。
[0842]
图案可以形成于固体成像元件用基板的固体成像元件形成面侧(表面),也可以形成于固体成像元件非形成面侧(背面)。
[0843]
在支撑体上,可根据需要,为了改善与上部层的粘结、防止物质的扩散或基板表面的平坦化而设置底涂层。
[0844]
作为将组合物应用于支撑体的方法,能够利用公知的方法。例如,可举出:滴加法(滴落涂布);狭缝涂布法;喷涂法;辊涂法;旋转涂布法(旋涂);流延涂布法;狭缝及旋转法;预湿法(例如,日本特开2009
‑
145395号公报中所记载的方法);喷墨法(例如,按需喷涂方式、压电方式、热方式)、喷嘴喷涂等吐出型印刷、柔性版印刷、网版印刷、凹版印刷、反转胶版印刷、金属遮罩印刷等各种印刷法;使用模具等的转引法、纳米压印法等。基于喷墨的应用方法,若可吐出组合物则并无特别限定,例如可举出“扩散、可使用的喷墨
‑
在专利中看到的无限可能性
‑
、2005年2月发行、s.b.research co.,ltd”中所示出的专利公报中所记载的方法(尤其,115页~133页)或日本特开2003
‑
262716、日本特开2003
‑
185831、日本特开2003
‑
261827、日本特开2012
‑
126830、日本特开2006
‑
169325等中所记载的方法。
[0845]
形成于支撑体上的组合物层可进行干燥(预烘)。通过低温工艺而形成图案的情况下,可以不进行预烘。
[0846]
进行预烘的情况下,预烘温度优选为150℃以下,更优选为120℃以下,进一步优选为110℃以下。下限例如能够设为50℃以上,还能够设为80℃以上。通过将预烘温度设为150℃以下来进行,例如在以有机原材料构成图像传感器的光电转换膜的情况下,能够更有效地维持该些特性。
[0847]
预烘时间优选为10秒~300秒钟,更优选为40~250秒钟,进一步优选为80~220秒钟。干燥能够通过加热板、烤箱来进行。
[0848]
(通过光刻法形成图案的情况)
[0849]
<<曝光工序>>
[0850]
接着,将组合物层以图案状曝光(曝光工序)。例如,对组合物层,使用步进机等的曝光装置并经由具有规定的遮罩图案的遮罩而进行曝光,由此能够进行图案曝光。由此,能够固化曝光部分。
[0851]
作为曝光时能够使用的放射线(光线),可优选使用g线、i线等紫外线(尤其优选i线)。照射量(曝光量)例如优选为0.03~2.5j/cm2,更优选为0.05~1.0j/cm2,最优选为0.08~0.5j/cm2。
[0852]
曝光时的氧浓度可适当选择,除了在大气压下进行,例如还可以在氧浓度为19体积%以下的低氧气氛下(例如,15体积%、5体积%、实质上为无氧)进行曝光,也可以在氧浓度大于21体积%的高氧浓度气氛下(例如,22体积%、30体积%、50体积%)进行曝光。而且,曝光照度可适当设定,通常能够选自1000w/m2~100000w/m2(例如,5000w/m2、15000w/m2、35000w/m2)的范围。氧浓度和曝光照度可以组合适当条件,例如,能够设为氧浓度10体积%且照度10000w/m2,氧浓度35体积%且照度20000w/m2等。
[0853]
<<显影工序>>
[0854]
接着,显影去除未曝光部来形成图案。未曝光部的显影去除能够使用显影液来进行。由此,曝光工序中的未曝光部的组合物层溶出于显影液,而只残留光固化后的部分。
[0855]
作为显影液,优选对基底的固体成像元件或线路等中不会引起损伤的有机碱显影液。
[0856]
显影液的温度优选例如20~30℃。显影时间优选为20~180秒。而且,为了提高残渣去除性,可以反覆进行将显影液按每60秒喷涂一次,进而重新供给显影液的工序。
[0857]
作为显影液中所使用的碱性试剂,例如可举出氨水、乙氨、二乙氨、二甲基乙醇氨、四甲基氢氧化铵、四乙基氢氧化铵、四丙基氢氧化铵、四丁基氢氧化铵、氢氧化苄基三甲铵、胆碱、吡咯、哌啶、1,8
‑
二氮杂双环[5.4.0]
‑7‑
十一碳烯等有机碱性化合物。可将以该些碱性试剂的浓度成为0.001~10质量%,优选为0.01~1质量%的方式,利用纯水进行稀释之后的碱性水溶液优选用作显影液。而且,显影液还可以使用无机碱。作为无机碱,例如,优选为氢氧化钠、氢氧化钾、碳酸钠、碳酸氢钠、硅酸钠、偏硅酸钠等。而且,显影液还可以使用界面活性剂。作为界面活性剂的例子,可举出以上述的组合物进行说明的界面活性剂,优选为非离子界面活性剂。显影液从方便移送或保管等的观点出发,也可以暂且制作成浓缩液,使用时稀释成所需的倍率。稀释倍率并无特别限定,但例如能够设定在1.5~100倍的范围。另外,使用包含该种碱性水溶液的显影液的情况下,通常在显影后优选以纯水清洗(冲洗)。
[0858]
显影后、能够在实施干燥后进行加热处理(后烘)。后烘为用于使膜完全固化的显影后的加热处理。进行后烘的情况下,后烘温度例如优选为100~240℃。从膜固化的观点考虑,更优选为200~230℃。而且,作为发光光源而使用有机电致发光(有机el)元件的情况,或以有机原材料构成图像传感器的光电转换膜的情况下,后烘温度优选为150℃以下,更优选为120℃以下,进一步优选为100℃以下,尤其优选为90℃以下。下限例如能够设为50℃以上。后烘是将能够对显影后的膜,以成为上述条件的方式使用加热板或对流式烘箱(热风循环式干燥机)、高频加热机等加热机构,并以连续式或间歇式进行。而且,通过低温工艺形成图案的情况下,可以不进行后烘。
[0859]
(通过干式蚀刻法形成图案的情况)
[0860]
关于通过干式蚀刻法进行的图案形成,将形成于支撑体上的组合物层固化来形成固化物层,接着,能够对所得到的固化物层,形成经图案化的光阻层,将该光阻层作为遮罩而相对于固化物层使用蚀刻气体来进行蚀刻。作为光阻层的形成方法,优选在固化物层上涂布正型或负型感放射线性组合物,并对其进行干燥来形成。光阻层的形成中,优选进一步实施预烘处理。尤其,作为光阻的形成工艺,优选实施曝光后的加热处理、显影后的加热处理(后烘处理)。关于通过干式蚀刻法进行的图案形成,能够参考日本特开2013
‑
064993号公报的0010~0067段的记载,并将该内容并入本说明书中。
[0861]
<固体成像元件>
[0862]
本发明的固体成像元件具有上述的本发明的膜。作为固体成像元件的构成,是具有本发明的膜(近红外线截止滤波器)的构成,且作为固体成像元件而发挥功能,则并无特别限定,例如可举出如以下构成。
[0863]
该构成为如下:在支撑体上具有包含构成固体成像元件的受光区的复数个光电二极体及多晶硅等的转移电极,在光电二极体及转移电极上具有仅光电二极体的受光部开口的包含钨等的遮光膜,遮光膜上具有以覆盖整个遮光膜及光电二极体受光部的方式形成的包含氮化硅等的设备保护膜,且在设备保护膜上具有本发明的膜。
[0864]
进而,还可以为在设备保护膜上,且本发明的近红外线截止滤波器的下侧(靠近支
撑体一侧)具有聚光机构(例如,微透镜等。以下相同)的构成有,或在本发明的膜(近红外线截止滤波器)上具有聚光机构的构成等。
[0865]
而且,滤色器可以具有如下结构:在由隔壁例如以方格状隔开的空间,嵌入有形成各色像素的固化膜。该情况下的隔壁对各色像素优选为低屈折率。作为具有该种结构的摄像装置的例子,可举出日本特开2012
‑
227478号公报、日本特开2014
‑
179577号公报中所记载的装置。
[0866]
<图像显示装置>
[0867]
本发明的膜也能够用于液晶显示装置或有机电致发光(有机el)显示装置等图像显示装置。例如,通过同时使用各着色像素(例如红色、绿色、蓝色),可以屏蔽显示装置的背光(例如白色发光二极体(白色led))中所含有的红外光,可以防止外围设备的误动作和除了形成各着色显示像素以外,也可以以形成红外的像素的目的来使用。
[0868]
关于显示装置的定义或各显示装置的详细内容,例如记载于“电子显示器件(佐佐木昭夫着、kogyo chosakai publishing co.,ltd.1990年发行)”、“显示器件(伊吹顺章着、sangyo tosho publishingco.,ltd.平成元年(1989年)发行)”等。并且,关于液晶显示装置,例如记载于“下一代液晶显示技术(内田龙男编集、工业调査会1994年发行)”。本发明能够应用的液晶显示装置并没有特别限制,例如,能够应用于上述“下一代液晶显示技术”中所记载的各种方式的液晶显示装置。
[0869]
图像显示装置可以为具有白色有机el元件者。作为白色有机el元件,优选为串联结构。关于有机el元件的串联结构,记载于日本特开2003
‑
45676号公报、三上明义监修、“有机el技术开发的最前线
‑
高亮度、高精度、长寿命化、技术秘密集
‑”
,技术资讯协会、326
‑
328页、2008年等。有机el元件所发出的白色光的光谱优选为在蓝色区域(430nm
‑
485nm)、绿色区域(530nm
‑
580nm)及黄色区域(580nm
‑
620nm)具有较强的极大发光峰值。除了该等发光峰值以外更优选进一步在红色区域(650nm
‑
700nm)具有极大发光峰值。
[0870]
<红外线传感器>
[0871]
本发明的红外线传感器具有上述的本发明的膜。作为红外线传感器的构成,若是具有本发明的膜,且作为红外线传感器而发挥功能的构成,则并无特别限定。
[0872]
以下,利用图式对红外线传感器的一实施方式进行说明。
[0873]
图1中,元件符号110为固体成像元件。设置于固体成像元件110上的摄像区域具有近红外线截止滤波器111和红外线透射滤波器114。而且,近红外线截止滤波器111上积层有滤色器112。滤色器112及红外线透射滤波器114的入射光hν侧配置有微透镜115。以覆盖微透镜115的方式形成有平坦化层116。
[0874]
近红外线截止滤波器111的特性可通过后述的红外发光二极体(红外led)的发光波长而选择。
[0875]
例如,红外led的发光波长为850nm的情况下,优选近红外线截止滤波器111为透射可见光(例如,波长400~700nm的光),且屏蔽波长大于850nm的波长的光的滤波器。
[0876]
而且,红外led的发光波长为940nm的情况下,优选近红外线截止滤波器111为透射可见光(例如,波长400~700nm的光),且屏蔽波长大于940nm的波长的光的滤波器。
[0877]
滤色器112为形成有透射及吸收可见区域中的特定波长的光的像素的滤色器,并无特别限定,能够使用以往公知的像素形成用滤色器。例如,科室员工可使用形成有红色
(r)、绿色(g)、蓝色(b)像素的滤色器等。例如,能够参考日本特开2014
‑
043556号公报的0214~0263段的记载,并将该内容并入本说明书中。
[0878]
红外线透射滤波器114的特性可通过后述的红外led的发光波长而选择。
[0879]
例如,红外led的发光波长为850nm的情况下,红外线透射滤波器114的波长400~650nm的范围内的膜厚度方向上的光透射率的最大值优选为30%以下,更优选为20%以下,进一步优选为10%以下,尤其优选为0.1%以下。优选该透射率在波长400~650nm的范围的所有区域满足上述条件。波长400~650nm的范围内的光透射率的最大值通常为0.1%以上。
[0880]
红外线透射滤波器114,波长800nm以上(优选为800~1300nm)的范围内的膜的厚度方向上的光透射率的最小值优选为70%以上,更优选为80%以上,进一步优选为90%以上。优选该透射率在波长800nm以上的范围的一部分满足上述条件,优选在与红外led的发光波长相对应的波长满足上述条件。波长900~1300nm的范围内的光透射率的最小值通常为99.9%以下。
[0881]
红外线透射滤波器114的膜厚优选为100μm以下,更优选为15μm以下,进一步优选为5μm以下,尤其优选为1μm以下。下限值优选为0.1μm。若膜厚为上述范围内,则能够作为满足上述的光谱特性的膜。
[0882]
以下示出红外线透射滤波器114的光谱特性、膜厚等的测定方法。
[0883]
关于膜厚,使用探针式表面形状测定器(ulvac,inc.制dektak150)测定了具有膜的干燥后的基板。
[0884]
膜的光谱特性为使用紫外可见近红外分光光度计(hitachi high
‑
technologies corporation.制u
‑
4100),在波长300~1300nm的范围内测定透射率的值。
[0885]
具有上述的光谱特性的红外线透射滤波器114能够藉由使用包含对可见光进行遮光的色材的组合物而形成。关于对可见光进行遮光的色材的详细内容,与以上述的组合物进行说明的范围相同。
[0886]
而且,例如,红外led的发光波长为940nm的情况下,红外线透射滤波器114中,波长450~650nm的范围内的膜的厚度方向上的光透射率的最大值为20%以下,波长835nm的膜的厚度方向上的光的透射率为20%以下,波长1000~1300nm的范围内的膜的厚度方向上的光的透射率的最小值优选为70%以上。
[0887]
具有上述的光谱特性的红外线透射滤波器114能够由使用组合物来制作,该组合物包含对可见光进行遮光的色材和在波长750~950nm的范围具有极大吸收的近红外线吸收化合物。关于对可见光进行遮光的色材的详细内容,与以上述的组合物进行说明的范围相同。作为近红外线吸收化合物,可举出以上述的组合物进行说明的近红外线吸收化合物。
[0888]
用于图1所示的红外线传感器的近红外线截止滤波器、滤色器及红外线透射滤波器的图案例如能够通过如下方式形成。
[0889]
首先,在支撑体151上应用近红外线截止滤波器形成用组合物(近红外线吸收组合物)来形成近红外线吸收组合物层。接着,如图2、图3所示,对近红外线吸收组合物层进行图案形成。图案形成方法可通过光刻法及干式蚀刻法中的任意一个来进行。另外,图2、图3中,在近红外线吸收组合物层形成了bayer(方格)图案,但图案的形状能够依用途而适当选择。
[0890]
接着,在近红外线吸收组合物层的bayer图案(近红外线截止滤波器111)上,应用滤色器形成用的组合物(着色组合物)来形成着色组合物层。接着,如图4、图5所示,对着色
组合物层进行图案形成,并在近红外线吸收组合物层的bayer图案(近红外线截止滤波器111)上对着色组合物层的bayer图案(滤色器112)进行图案形成。图案形成方法可通过光刻法及干式蚀刻法的任意一个来进行,优选为光刻法。
[0891]
接着,在形成了滤色器112的膜上,应用红外线透射滤波器形成用组合物来形成组合物层。接着,如图6、图7所示,对组合物层进行图案形成,并在近红外线截止滤波器111的bayer图案的缺陷部分形成红外线透射滤波器114的图案。
[0892]
另外,图1所示的实施方式中,滤色器112比近红外线截止滤波器111更靠入射光hν侧而设置,但可以替换近红外线截止滤波器111和滤色器112的顺序在比滤色器112更靠入射光hν侧设置近红外线截止滤波器111。而且,图1所示的实施方式中,红外线透射滤波器114为单层膜,但也可以由两层以上的膜构成。而且,图1所示的实施方式中,近红外线截止滤波器111与滤色器112相邻地积层,但并不一定要与滤波器相邻,可以在形成有滤色器112的支撑体不同的支撑体上形成近红外线截止滤波器111。若上述支撑体为透明基材,则能够优选使用任意支撑体。而且,还能够使用含铜的透明基材、具有含铜的透明层的基材、形成有带通滤波器的基材。
[0893]
而且,作为近红外线截止滤波器111,除了近红外线吸收化合物以外,还使用包含彩色着色剂者,且近红外线截止滤波器111具有作为滤色器的功能的情况下,如图8所示,能够省略滤色器112。图8中,元件符号111a为包含彩色着色剂的近红外线截止滤波器,且为兼具滤色器的功能的近红外线截止滤波器。
[0894]
实施例
[0895]
以下举出实施例来更具体地说明本发明。以下实施例中所示出的材料、使用量、比例、处理内容、处理顺序等只要不脱离本发明的主旨,能够适当进行变更。因此,本发明的范围并不限定于以下所示出的具体例。另外,并无特别说明的范围内,“%”及“份”为质量基准。而且,化学式中,me表示甲基,bu表示丁基,ph表示苯基。nmr为核磁共振的缩写。
[0896]
<合成例>
[0897]
(合成例1)化合物ii
‑
186的合成
[0898]
参考chem.eur.j.2009,15,4857来合成了化合物ii
‑
186。
[0899]
将18.2质量份的60质量%的氢氧化钠和200质量份的四氢呋喃放入烧瓶中,在冰浴下滴加60质量份的氰基乙酸叔丁酯。在室温下搅拌1小时之后,添加25质量份的2
‑
氯
‑6‑
甲基
‑
苯并噁唑,并搅拌12小时。将反应液注入于1000质量份的水中,添加100质量份的乙酸来滤取析出物,并以己烷进行清洗。将该结晶于50℃下风干,由此得到了39质量份的中间物a。
[0900]
将39质量份的中间物a、50质量份的三氟乙酸、及300质量份的氯仿加入烧瓶中,在60℃下搅拌1小时。反应后,添加碳酸钠水溶液,且通过分液操作来提取有机相。将有机相以饱和氯化钠水溶液清洗之后,对溶剂进行减压蒸馏来得到了淡黄色固体。将所得到的淡黄色固体通过硅胶柱色谱法(己酮/氯仿溶剂)来提纯,从而得到了13质量份的中间物a
‑
1。
[0901]
[化学式5]
[0902][0903]
将21.6质量份的异十八醇(fineoxoco l
1 80、nissan chemical industries,ltd.制)、三乙氨在80质量份的甲苯中进行搅拌,并在
‑
10℃下滴加10质量份的甲磺酰氯。滴加结束后,在30℃下反应2小时。通过分液操作提取有机相,且对溶剂进行减压蒸馏。对溶剂进行蒸馏之后,添加于10.5质量份的3
‑
氰基苯酚、13.9质量份的碳酸钠、16质量份的二甲基乙酰氨,在100℃下反应24小时。通过分液操作来提取有机相,将有机相以氢氧化钠水溶液清洗之后,对溶剂进行减压蒸馏来得到了28质量份的作为淡黄色液体的化合物a。
[0904]
将30质量份的化合物a、9质量份的琥珀酸二异丙基、40质量份的第三级戊醇、16.5质量份的第三级丁醇钾放入烧瓶中,在120℃下搅拌3小时。反应后,添加100质量份的甲醇、100质量份的水来滤取析出物。将该结晶在50℃下风干,由此得到了20质量份的化合物b。
[0905]
将20质量份的化合物b和9.4质量份的中间物a
‑
1在400质量份的甲苯中进行搅拌,接着添加20.9质量份的三氯氧磷来经4.5小时进行加热还流。反应后,冷却至室温,添加800质量份的甲醇,在室温下搅拌30分钟。滤除所析出的结晶,且以400质量份的甲醇清洗。将所得到的结晶在40℃下风干12小时,由此得到了13质量份的化合物c。
[0906]
向含有7.5质量份的二苯基硼酸2
‑
氨基乙酯的甲苯90质量份中添加10.5质量份的氯化钛,在35℃下搅拌30分钟。接着,添加9质量份的化合物c,进而经2小时在加热还流条件进行搅拌。冷却至室温,添加100质量份的甲醇,进而搅拌30分钟。虑取所析出的结晶,并通过硅胶柱层析法(氯仿溶剂)来提纯,从而得到了8.8质量份的化合物ii
‑
186。
[0907]1h
‑
nmr(cdcl3):δ0.75
‑
1.88(m,70h)、2.13(s,6h)、3.75(m,4h)、6.20(s,2h)、6.42(d,4h)、6.64(d,4h)、6.93(d,2h)7.12
‑
7.22(m,22h)
[0908]
[化学式56]
[0909][0910]
(合成例2)
[0911]
以与化合物ii
‑
186相同的方法合成了化合物ii
‑
9、ii
‑
10、ii
‑
27、ii
‑
43、ii
‑
44、ii
‑
167、ii
‑
168、ii
‑
184、ii
‑
185、ii
‑
201、ii
‑
202、ii
‑
325、ii
‑
507、ii
‑
508、ii
‑
524、ii
‑
525、ii
‑
541、ii
‑
673、ii
‑
697、ii
‑
715、iii
‑
9、iii
‑
28、iii
‑
29、iii
‑
167、iii
‑
328、iii
‑
349、iii
‑
358及iii
‑
365。
[0912]
(合成例3)化合物ii
‑
408的合成
[0913]
使用以与中间物a
‑
1相同的方法合成的中间物a
‑
2合成了化合物d。
[0914]
向含有10质量份的2
‑
氯
‑
1,3,2
‑
苯并二氧杂硼杂环戊二烯(benzodioxaborole)的甲苯200质量份中添加20质量份的化合物d之后,添加11质量份的二异丙基乙氨,在100℃下搅拌1小时。冷却至室温之后,加入400质量份的甲醇,进而搅拌30分钟。滤取所析出的结晶,并通过硅胶柱层析法(氯仿溶剂)进行提纯,从而得到了13质量份的化合物ii
‑
408。
[0915]1h
‑
nmr(cdcl3):δ0.85
‑
2.02(m,70h)、3.70(m,4h)、6.44(m,4h)、6.63(m,8h)、6.95(m,6h)、7.29(m,2h)7.41(dd,2h)
[0916]
[化学式57]
[0917][0918]
(合成例4)
[0919]
以与化合物ii
‑
408相同的方法合成了化合物ii
‑
91、ii
‑
269、ii
‑
274、ii
‑
275、ii
‑
589及ii
‑
590。
[0920]
(合成例5)化合物ii
‑
92的合成
[0921]
向20质量份的化合物b添加35质量份的三氯氧磷来经2小时进行加热还流。反应后,对过剩的三氯氧磷进行减压蒸馏,之后添加200质量份的甲苯、4.7质量份的2
‑
(2
‑
苯并噻唑)乙腈来经1小时进行加热还流。冷却至室温,添加200质量份的氯仿、200质量份的水,
通过分液操作来取出有机相。将有机相以饱和氯化钠水溶液清洗之后,对溶剂进行减压蒸馏,由此得到了11质量份的化合物e。将8质量份的化合物e和2.2质量份的中间物a
‑
1在80质量份的甲苯中进行搅拌,接着,添加4质量份的三氯氧磷来经2小时进行加热还流。反应后,冷却至室温,添加150质量份的甲醇来在室温下搅拌30分钟。滤除所析出的结晶,并以100质量份的甲醇清洗。将所得到的结晶在40℃下经12小时进行风干,由此得到了6质量份的化合物f。
[0922]
向含有2.5质量份的2
‑
氯
‑
1,3,2
‑
苯并二氧杂硼杂环戊二烯的甲苯50质量份中添加4.5质量份的化合物f。接着,添加2.5质量份的二异丙基乙氨,在100℃下搅拌1小时。冷却至室温之后,加入90质量份的甲醇,进而搅拌30分钟。滤取所析出的结晶,并通过硅胶柱层析法(氯仿溶剂)进行提纯,从而得到了3质量份的化合物iv
‑
92。
[0923]1h
‑
nmr(cdcl3):δ0.85
‑
2.02(m,70h)、2.14(s,3h)、3.60
‑
3.87(m,4h)、6.40(m,4h)、6.45(s,1h)、6.60(m,6h)、6.86(m,1h)、6.89
‑
[0924]
7.00(m,5h)、7.10(d,2h)、7.19(t,1h)、7.30(t,1h)、7.34(d,1h)
[0925]
[化学式58]
[0926][0927]
(合成例6)
[0928]
以与化合物iii
‑
92相同的方法合成了化合物iv
‑
7及化合物iv
‑
91。
[0929]
(合成例7)化合物iii
‑
168的合成
[0930]
将21.6质量份的异十八醇(fineoxocol180、nissan chemical industries,ltd.制)、9.7质量份的三乙氨、80质量份的甲苯进行搅拌,并在10℃以下的液温下滴加10质量份的甲磺酰氯。滴加结束后,在30℃下反应2小时。通过分液操作提取有机相,且对溶剂进行减
压蒸馏。对溶剂进行蒸馏之后,添加10.5质量份的4
‑
氰基苯酚、13.3质量份的碳酸钾、24质量份的二甲基乙酰氨,在110℃下反应24小时。通过分液操作来提取有机相,将有机相以氢氧化钠水溶液清洗之后,对溶剂进行减压蒸馏来得到了28质量份的作为淡黄色液体的化合物g。
[0931]
接着,将13质量份的化合物g、4.2质量份的琥珀酸二异丙基酯、18质量份的第三级戊醇、7.7质量份的第三级丁醇钾放入烧瓶中,在120℃下搅拌6小时。反应后,添加36质量份的甲醇、36质量份的水来滤取析出物。将该结晶在50℃下风干,由此得到了5.1质量份的化合物h。
[0932]
接着,将5质量份的化合物h和利用于国际公开wo2015/166873号公报中记载的方法合成的3.5质量份的中间物a
‑
3在100质量份的甲苯中进行加热搅拌,接着添加3.8质量份的三氯氧磷来经4小时进行加热还流。反应后,将反应液冷却至室温,接着添加200质量份的甲醇,在室温下搅拌30分钟。滤除所析出的结晶,且以400质量份的甲醇清洗。将所得到的结晶在50℃下风干12小时,由此得到了3.1质量份的化合物i。
[0933]
接着,向含有2.2质量份的二苯基硼酸2
‑
氨基乙酯的甲苯20质量份中添加3.1质量份的氯化钛,在35℃下搅拌30分钟。接着,添加1.7质量份的化合物i,进而经3小时在加热还流条件进行搅拌。冷却至室温,添加40质量份的甲醇,进而搅拌30分钟。虑取所析出的结晶,并通过硅胶柱层析法(氯仿溶剂)来提纯,从而得到了1.8质量份的化合物iii
‑
168。
[0934]1h
‑
nmr(cdcl3):δ8.99(s,2h)、8.16(s,2h)、7.78(s,2h)、7.26(s,10h)、7.19(s,10h)、6.58(d,4h)、6.18(d,4h)、3.95
‑
3.82(m,4h)、1.98
‑
1.67(m,4h)、1.45
‑
1.08(m,18h)、1.03
‑
0.95(m,48h)
[0935]
[化学式59]
[0936][0937]
<极大吸收波长、吸光度比的评价>
[0938]
将各化合物溶解于下述表中所记载的测定溶剂(浓度2.5
×
10
‑6mol/l)来测定了吸收光谱(光路长度10mm)。
[0939]
将各化合物的吸收光谱的极大吸收波长(λmax)示于下述表。
[0940]
且依据以下基准评价了作为将波长500nm的吸光度除以极大吸收波长的吸光度的值的吸光度比(500nm/λmax)。
[0941]
a:吸光度比(500nm/λmax)为0.04以下
[0942]
b:吸光度比(500nm/λmax)大于0.04,且0.08以下
[0943]
c:吸光度比(500nm/λmax)大于0.08
[0944]
<溶解度的评价>
[0945]
将各化合物在大气压下添加至23℃的水中,搅拌1小时之后求出各化合物针对水的溶解度。依据以下基准评价了化合物的溶解性。
[0946]
a:针对23℃的水的溶解度为0.1质量%以下
[0947]
b:针对23℃的水的溶解度大于0.1质量%,且1质量%以下
[0948]
c:针对23℃的水的溶解度大于1质量%
[0949]
[表56]
[0950]
化合物分类化合物序号溶液极大吸收波长(nm)吸光度比溶解性吡咯并吡咯化合物ii
‑
9氯仿740aa吡咯并吡咯化合物ii
‑
10氯仿740aa吡咯并吡咯化合物ii
‑
27氯仿743aa吡咯并吡咯化合物ii
‑
29氯仿743aa吡咯并吡咯化合物ii
‑
43氯仿732aa吡咯并吡咯化合物ii
‑
44氯仿732aa吡咯并吡咯化合物ii
‑
91氯仿679aa吡咯并吡咯化合物ii
‑
167氯仿745aa吡咯并吡咯化合物ii
‑
168氯仿745aa吡咯并吡咯化合物ii
‑
184氯仿749aa吡咯并吡咯化合物ii
‑
185氯仿748aa吡咯并吡咯化合物ii
‑
186氯仿748aa吡咯并吡咯化合物ii
‑
201氯仿737aa吡咯并吡咯化合物ii
‑
202氯仿737aa吡咯并吡咯化合物ii
‑
269氯仿685aa吡咯并吡咯化合物ii
‑
274氯仿685aa吡咯并吡咯化合物ii
‑
275氯仿685aa吡咯并吡咯化合物ii
‑
325氯仿738aa吡咯并吡咯化合物ii
‑
408氯仿680aa吡咯并吡咯化合物ii
‑
507氯仿780aa吡咯并吡咯化合物ii
‑
508氯仿780aa吡咯并吡咯化合物ii
‑
524氯仿779aa吡咯并吡咯化合物ii
‑
525氯仿783aa吡咯并吡咯化合物ii
‑
541氯仿772aa吡咯并吡咯化合物ii
‑
673氯仿794aa吡咯并吡咯化合物ii
‑
589氯仿719aa吡咯并吡咯化合物ii
‑
590氯仿719aa吡咯并吡咯化合物ii
‑
697氯仿743aa
吡咯并吡咯化合物ii
‑
715氯仿769aa吡咯并吡咯化合物iii
‑
9氯仿863aa吡咯并吡咯化合物iii
‑
28氯仿863aa吡咯并吡咯化合物iii
‑
29氯仿863aa吡咯并吡咯化合物iii
‑
167氯仿885aa吡咯并吡咯化合物iii
‑
168氯仿885aa吡咯并吡咯化合物iii
‑
328氯仿872aa吡咯并吡咯化合物iii
‑
349氯仿752aa吡咯并吡咯化合物iii
‑
358氯仿814aa吡咯并吡咯化合物iii
‑
365氯仿735aa吡咯并吡咯化合物iv
‑
7氯仿698aa吡咯并吡咯化合物iv
‑
91氯仿701aa吡咯并吡咯化合物iv
‑
92氯仿701aa吡咯并吡咯化合物pp
‑
1氯仿739ba吡咯并吡咯化合物v
‑
1氯仿740aa吡咯并吡咯化合物v
‑
25氯仿794aa吡咯并吡咯化合物v
‑
33氯仿863aa吡咯并吡咯化合物v
‑
42氯仿885aa
[0951]
[表57]
[0952]
化合物分类化合物序号溶液极大吸收波长(nm)吸光度比溶解性方酸化合物q
‑
3氯仿737aa方酸化合物q
‑
36氯仿704aa方酸化合物q
‑
39氯仿822aa方酸化合物q
‑
54氯仿698aa花青化合物cy
‑
1氯仿698aa花青化合物cy
‑
2氯仿758aa花青化合物cy
‑
3氯仿761aa花青化合物cy
‑
4甲醇758ac花青化合物cy
‑
5甲醇682ac花青化合物cy
‑
6氯仿844aa花青化合物cy
‑
7氯仿764aa花青化合物cy
‑
8氯仿764aa花青化合物cy
‑
9氯仿681aa花青化合物cy
‑
10氯仿702aa花青化合物cy
‑
11氯仿788aa花青化合物cy
‑
12氯仿829aa花青化合物cy
‑
13氯仿831aa
[0953]
[化学式60]
[0954][0955]
[化学式61]
[0956][0957]
[化学式62]
[0958][0959]
[化学式63]
[0960][0961]
[化学式64]
[0962][0963]
方酸化合物
[0964]
[化学式65]
[0965][0966]
花青化合物
[0967]
[化学式66]
[0968]
[0969]
[化学式67]
[0970][0971]
<试验例1>
[0972]
(含铜的层的制作)
[0973]
将6.55质量份的下述铜络合物1、19.65质量份的下述铜络合物2、61.9质量份的以下所示的树脂1、5质量份的irgacure
‑
oxe02(basf公司制)、0.025质量份的三(2,4
‑
戊二酮)铝(iii)(tokyo chemical industry co.,ltd.制)、6.875质量份kbm
‑
3066(shin
‑
etsu chemical co.,ltd.制)、24.344质量份的环戊酮、75.656质量份的乙酸丁酯、0.1质量份的水进行混合,并搅拌之后,以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤而制备了含铜络合物的组合物1。
[0974]
铜络合物1
[0975]
[化学式68]
[0976][0977]
铜络合物2
[0978]
[化学式69]
[0979][0980]
树脂1(mw=1.5万、在主链标记的数值为各结构单元的摩尔比)
[0981]
[化学式70]
[0982][0983]
以干燥后的膜厚成为100μm的方式使用旋转涂布机将所得到的含铜络合物的组合物1涂布于玻璃晶圆上,并使用150℃的加热板来经3小时进行加热处理,从而制作了含铜的层。
[0984]
(组合物的制备)
[0985]
将下述组合进行混合及撹拌之后,以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤而制备了组合物。
[0986]
<组合1>
[0987]
第1近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[0988]
第2近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[0989]
树脂1、树脂2或树脂3(下述表所示的树脂)
……
7.51份
[0990]
树脂1:下述结构的树脂(mw=40,000)
[0991]
[化学式71]
[0992][0993]
树脂2:arton f4520(jsr corporation制)
[0994]
树脂3:下述结构的树脂(结构单元中的比为摩尔比)、mw=11500
[0995]
以日本特开2012
‑
198408号公报的0247~0249段中所记载的方法进行合成。
[0996]
[化学式72]
[0997]
[0998]
固化性化合物1(双季戊四醇六丙烯酸酯(nippon kayaku co.,ltd.制,产品名kayarad dpha))
……
1.28份
[0999]
光聚合起始剂(irgacure
‑
oxe02,basf公司制)
……
1.40份
[1000]
界面活性剂1(megaface rs
‑
72
‑
k(dic corporation制,30%丙二醇单甲醚乙酸酯溶液))
……
1.59份
[1001]
环己酮
……
86.3份
[1002]
<组合2>
[1003]
第1近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[1004]
第2近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[1005]
树脂4(甲基丙烯酸缩水甘油酯骨架无规共聚物,nof corporation.制,marproof g
‑
0150m,mw=10,000)
……
12.9份
[1006]
固化性化合物2(oxt
‑
221,toagosei co.,ltd.制)
……
12.9份
[1007]
酸产生剂1(cpi
‑
100p,san
‑
apro ltd.制)
……
2.5份
[1008]
界面活性剂2(下述混合物,mw=14000)
……
0.04份
[1009]
[化学式73]
[1010][1011]
环己酮
……
49.6份
[1012]
丙二醇单甲醚乙酸酯
……
19.3份
[1013]
<组合3>
[1014]
第1近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[1015]
第2近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[1016]
树脂5(下述结构的树脂(结构单元中的比为摩尔比)、mw=18,000)
……
12.9份
[1017]
[化学式74]
[1018][1019]
酸催化剂(磷酸)
……
2.5份
[1020]
界面活性剂2
……
0.04份
[1021]
环己酮
……
58.9份
[1022]
丙二醇单甲醚乙酸酯
……
22.9份
[1023]
<组合4>
[1024]
第1近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[1025]
第2近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[1026]
树脂6:聚羟基苯乙烯(sigma
‑
aldrich co.llc制、mw=10,000)
……
12.9份
[1027]
固化性化合物3:1,3,4,6
‑
四甲氧基甲基甘脲(tokyo chemical industry co.,ltd.制)
……
12.9份
[1028]
酸产生剂2(三乙基铵九氟丁烷磺酸盐)
……
2.5份
[1029]
界面活性剂3(fc
‑
4430、sumitomo 3m limited制)
……
0.04份
[1030]
环己酮
……
49.6份
[1031]
丙二醇单甲醚乙酸酯
……
19.3份
[1032]
<组合5>
[1033]
第1近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[1034]
第2近红外线吸收化合物(下述表所示的化合物)
……
0.96份
[1035]
树脂1
……
7.51份
[1036]
固化性化合物1(双季戊四醇六丙烯酸酯(nippon kayaku co.,ltd.制,产品名kayarad dpha))
……
1.28份
[1037]
界面活性剂1(megaface rs
‑
72
‑
k(dic corporation制,30%丙二醇单甲醚乙酸酯溶液))
……
1.59份
[1038]
环己酮
……
86.3份
[1039]
另外,实施例1
‑
10中,作为第2近红外线吸收化合物,将ii
‑
590和iv
‑
92各使用了0.48份(以质量比计,使用比例为ii
‑
590:iv
‑
92=1:1)。
[1040]
而且,实施例1
‑
11中,作为第2近红外线吸收化合物,分别将ii
‑
589、iv
‑
91及ii
‑
274各使用了0.32份(以质量比计,使用比例为ii
‑
589:iv
‑
91:ii
‑
274=1:1:1)。
[1041]
而且,实施例1
‑
30中,作为第2近红外线吸收化合物,将ii
‑
408和ii
‑
91各使用了0.48份(以质量比计,使用比例为ii
‑
408:ii
‑
91=1:1)。
[1042]
而且,实施例1
‑
31中,作为第2近红外线吸收化合物,分别将ii
‑
29、ii
‑
408及ii
‑
91各使用了0.32份(以质量比计,使用比例为ii
‑
29:ii
‑
408:ii
‑
91=1:1:1)。
[1043]
而且,比较例1
‑
1中,将第1近红外线吸收化合物的含量设为1.92份。
[1044]
而且,比较例1
‑
2中,将第1近红外线吸收化合物的含量设为3.84份。
[1045]
<<近红外线截止滤波器的制作>>
[1046]
(实施例1
‑
1~实施例1
‑
18、实施例1
‑
20~实施例1
‑
31、比较例1
‑
1~比较例1
‑
6)
[1047]
以干燥后的膜厚成为0.8μm的方式使用旋转涂布机将各组合物涂布于上述含铜的层上,并使用100℃的加热板来经120秒钟进行加热处理(预烘)。
[1048]
接着,使用i线步进机,且以1000mj/cm2进行全面曝光。其次,在200℃下、经300秒钟进行后加热(后烘),从而制作了近红外线截止滤波器。
[1049]
(实施例1
‑
19)
[1050]
以干燥后的膜厚成为0.8μm的方式使用旋转涂布机来将实施例1
‑
19的组合物涂布于上述含铜的层上,并使用100℃的加热板经120秒钟进行加热处理(预烘),从而制作了近红外线截止滤波器。
[1051]
<<红外线屏蔽性评价>>
[1052]
使用分光光度计u
‑
4100(hitachi high
‑
technologies corporation.制)来测定了近红外线截止滤波器的波长700nm~800nm的透射率。依据以下基准评价了红外线屏蔽性。将结果示于以下表。
[1053]
a:波长700~800nm时,透射率最低的值≤1%
[1054]
b:1%<波长700~800nm时,透射率最低的值≤5%
[1055]
c:5%<波长700~800nm时,透射率最低的值≤10%
[1056]
d:10%<波长700~800nm时,透射率最低的值≤20%
[1057]
e:20%<波长700~800nm时,透射率最低的值
[1058]
<<可见透明性评价>>
[1059]
使用分光光度计u
‑
4100(hitachi high
‑
technologies corporation.制)来测定了如上述般得到的近红外线截止滤波器中的波长400~550nm的平均透射率。依据以下基准评价了可见透明性。将结果示于以下表。
[1060]
a:90%≤波长400~550nm的平均透射率
[1061]
b:85%≤波长400~550nm的平均透射率<90%
[1062]
c:波长400~550nm的平均透射率<85%
[1063]
<<光谱变化性评价>>
[1064]
将近红外线截止滤波器在85℃、相对湿度85%的高温高湿的环境下放置1小时。分别在耐湿性试验前和耐湿性试验后,使用分光光度计u
‑
4100(hitachi high
‑
technologies corporation.制)测定近红外线截止滤波器的波长700~1400nm下的最大吸光度(absλmax)和波长400~700nm下的最小吸光度(absλmin),并求出以“absλmax/absλmin”表示的吸光度比。依据以下基准评价了以|(试验前的吸光度比
‑
试验后的吸光度比)/试验前的吸光度比
×
100|(%)表示的吸光度比变化率。将结果示于以下表。
[1065]
a:吸光度比变化率≤2%
[1066]
b:2%<吸光度比变化率≤4%
[1067]
c:4%<吸光度比变化率≤7%
[1068]
d:7%<吸光度比变化率
[1069]
<<耐光性>>
[1070]
针对近红外线截止滤波器,将氙气灯以5万lux照射20小时(相当于100万l ux
·
h)之后,测定了耐光试验前后的色差的δeab值。δeab值越小则表示耐光性越良好。将结果示于以下表。另外,δeab值为以基于cie1976(l*,a*,b*)空间颜色系统的自以下色差公式求出的值(日本色彩学会编着新编色彩科学手册(昭和60年)p.266)。
[1071]
δeab={(δl*)2 (δa*)2 (δb*)2}
1/2
[1072]
a:δeab值<5
[1073]
b:5≤δeab值<10
[1074]
c:10≤δeab值<20
[1075]
d:20≤δeab值
[1076][1077]
如上述表,实施例的光谱变化性、红外线屏蔽性及可见透明性优异。而且,作为第1近红外线吸收化合物而使用吡咯并吡咯化合物的实施例的耐光性尤其优异。
[1078]
另一方面,比较例中,光谱变化性及红外线屏蔽性至少一个比实施例差。
[1079]
实施例中,即使在含铜的层的两面使用实施例的组合物来形成膜,也可得到与实施例相同的效果。
[1080]
而且,实施例中,替代含铜的层,即使在含铜的磷酸盐玻璃或含铜的氟磷酸盐玻璃上使用实施例的组合物来形成膜,也可得到与实施例相同的效果。
[1081]
而且,对实施例的组合物进一步配合使用于含铜的层的形成中的铜络合物的组合物,且即使在玻璃基材上使用所述组合物来形成膜,也可得到与实施例相同的效果。
[1082]
而且,在玻璃基板上使用实施例的组合物来形成层,且即使在所得到的层上形成上述含铜的层,也可得到与实施例相同的效果。
[1083]
而且,替代上述含铜的层,即使在使用以下含铜络合物的组合物2来形成的含铜的层的单面或两面,使用实施例的组合物来形成膜,也可得到与实施例相同的效果。
[1084]
(含铜络合物的组合物2)
[1085]
在室温下将28.9质量份的四乙氧基硅烷、28.9质量份的苯基三乙氧基硅烷、30.6质量份的10质量%盐酸混合4小时来得到了溶胶。该溶液通过在室温下将26.0质量份的铜络合物1在85.5质量份的环戊酮,经20分钟进行溶解来得到溶液,将溶液添加在所述溶胶中,并以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤来制备了含铜络合物的组合物2。
[1086]
而且,即使在实施例的组合物的膜上,以以下方法形成组合含铯氧化钨的组合物的膜的情况下,也可得到与实施例相同的效果。
[1087]
在含铜的层上积层实施例的组合物而成的膜上,以旋转涂布法涂布以下含铯氧化钨的组合物,之后使用加热板在100℃下加热2分钟来得到了涂布层。使用i线步进机或对准仪来将所得到的涂布层以500mj/cm2的曝光量进行曝光。接着,使用加热板在220℃下对曝光后的涂布层经5分钟进行固化处理,从而形成了厚度3.0μm的膜。
[1088]
(含铯氧化钨的组合物)
[1089]
将49.84质量份的yms
‑
01a
‑
2(sumitomo metal mining co.,ltd.制:铯氧化钨粒子分散液)、39.5质量份的下述树脂(固形分40%pgmea溶液)、6.80质量份的kayarad dpha(nippon kayaku co.,ltd.制)、2.18质量份的irgacure 369(basf公司制)、1.68质量份的pgmea进行混合并搅拌来制备了含铯氧化钨的组合物。
[1090]
树脂:下述结构的树脂(酸值:70mgkoh/g、mw=11000、结构单元中的比为摩尔比)
[1091]
[化学式75]
[1092][1093]
(实施例1
‑
32)
[1094]
即使以以下方法,形成由两层膜构成的近红外线截止滤波器,也可得到与实施例1
‑
30相同的效果。
[1095]
以干燥后的膜厚成为0.8μm的方式使用旋转涂布机,将组合6的组合物涂布于上述含铜的层上,并使用100℃的加热板进行120秒钟的加热处理(预烘)。接着,使用i线步进机,且以1000mj/cm2进行全面曝光。其次,在200℃下、进行300秒钟之后加热(后烘),从而制作
了第1近红外线截止滤波器。
[1096]
接着,以干燥后的膜厚成为0.8μm的方式使用旋转涂布机,将组合7的组合物涂布于上述第1近红外线截止滤波器层上,并使用100℃的加热板进行120秒钟的加热处理(预烘)。接着,使用i线步进机,且以1000mj/cm2进行全面曝光。其次,在200℃下、进行300秒钟之后加热(后烘),从而制作了由两层构成的近红外线截止滤波器。
[1097]
<组合6>
[1098]
第1近红外线吸收化合物(ii
‑
186)
……
0.96份
[1099]
第2近红外线吸收化合物(ii
‑
408)
……
0.48份
[1100]
树脂1
……
7.51份
[1101]
固化性化合物1
……
1.28份
[1102]
光聚合起始剂(irgacure
‑
oxe02、basf公司制)
……
1.40份
[1103]
界面活性剂1
……
1.59份
[1104]
环己酮
……
86.3份
[1105]
<组合7>
[1106]
近红外线吸收化合物(ii
‑
91)
……
0.48份
[1107]
树脂1
……
7.51份
[1108]
固化性化合物1
……
1.28份
[1109]
光聚合起始剂(irgacure
‑
oxe02、basf公司制)
……
1.40份
[1110]
界面活性剂1
……
1.59份
[1111]
环己酮
……
86.3份
[1112]
(实施例1
‑
33)
[1113]
即使以以下方法,形成由两层膜构成的近红外线截止滤波器,也可得到与实施例1
‑
31相同的效果。
[1114]
以干燥后的膜厚成为0.8μm的方式使用旋转涂布机,将组合8的组合物涂布于上述含铜的层上,并使用100℃的加热板进行120秒钟的加热处理(预烘)。接着,使用i线步进机,且以1000mj/cm2进行全面曝光。其次,在200℃下、进行300秒钟之后加热(后烘),从而制作了第1近红外线截止滤波器。
[1115]
接着,以干燥后的膜厚成为0.8μm的方式使用旋转涂布机将组合9的组合物涂布于上述第1近红外线截止滤波器层上,并使用100℃的加热板来经120秒钟进行加热处理(预烘)。接着,使用i线步进机,且以1000mj/cm2进行全面曝光。其次,在200℃下、经300秒钟进行后加热(后烘),从而制作了由两层构成的近红外线截止滤波器。
[1116]
<组合8>
[1117]
第1近红外线吸收化合物(ii
‑
186)
……
0.96份
[1118]
第2近红外线吸收化合物(ii
‑
408)
……
0.32份
[1119]
树脂1
……
7.51份
[1120]
固化性化合物1
……
1.28份
[1121]
光聚合起始剂(irgacure
‑
oxe02、basf公司制)
……
1.40份
[1122]
界面活性剂1
……
1.59份
[1123]
环己酮
……
86.3份
[1124]
<组合9>
[1125]
第1近红外线吸收化合物(ii
‑
29)
……
0.32份
[1126]
第2近红外线吸收化合物(ii
‑
91)
……
0.32份
[1127]
树脂1
……
7.51份
[1128]
固化性化合物1
……
1.28份
[1129]
光聚合起始剂(irgacure
‑
oxe02、basf公司制)
……
1.40份
[1130]
界面活性剂1
……
1.59份
[1131]
环己酮
……
86.3份
[1132]
<试验例2>
[1133]
(组合物的制备)
[1134]
将下述组合混合并分散之后,以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤来制备了组合物。
[1135]
[组合]
[1136]
第1近红外线吸收化合物(表中所示的化合物)
……
2.38份
[1137]
第2近红外线吸收化合物(表中所示的化合物)
……
0.98份
[1138]
表中所示的树脂1、树脂2或树脂3(下述表所示的树脂)
……
6.86份
[1139]
树脂1:下述结构的树脂(mw=40,000、结构单元中的比为摩尔比)
[1140]
[化学式76]
[1141][1142]
树脂2:arton f4520(jsr corporation制)
[1143]
树脂3:下述结构的树脂(结构单元中的比为摩尔比)、mw=11500
[1144]
以日本特开2012
‑
198408号公报的0247~0249段中所记载的方法进行合成。
[1145]
[化学式77]
[1146][1147]
固化性化合物(二季戊四醇六丙烯酸酯(nippon kayaku co.,ltd.制,产品名kayarad dpha))
……
1.41份
[1148]
光聚合起始剂(下述化合物)
……
1.55份
[1149]
[化学式78]
[1150]
[1151]
界面活性剂(megaface rs
‑
72
‑
k(dic corporation制、30%丙二醇单甲醚乙酸酯溶液))
……
2.71份
[1152]
聚合抑制剂(对甲氧基苯酚)
……
0.001份
[1153]
环戊酮
……
84.11份
[1154]
另外,使用3种色素的实施例2
‑
20中,作为第1近红外线吸收化合物而使用1.12份的ii
‑
507,且作为第2近红外线吸收化合物,将ii
‑
186和iv
‑
91各使用1.12份。(以质量比计,使用比例为ii
‑
507:ii
‑
186:iv
‑
91=1:1:1。)
[1155]
而且,使用了3种色素的实施例2
‑
21中,作为第1近红外线吸收化合物而使用1.12份的ii
‑
507,且作为第2近红外线吸收化合物,将ii
‑
43和ii
‑
589各使用1.12份。(以质量比计,使用比例为ii
‑
507:ii
‑
43:ii
‑
589=1:1:1。)
[1156]
而且,使用了3种色素的实施例2
‑
22中,作为第1近红外线吸收化合物而使用1.12份的iii
‑
9,且作为第2近红外线吸收化合物,将ii
‑
673和ii
‑
9各使用1.12份。(以质量比计,使用比例为iii
‑
9:ii
‑
673:ii
‑
9=1:1:1。)
[1157]
而且,使用了3种色素的实施例2
‑
23中,作为第1近红外线吸收化合物而使用了1.12份的ii
‑
673,且作为第2近红外线吸收化合物,将ii
‑
507和ii
‑
43各使用1.12份。(以质量比计,使用比例为ii
‑
673:ii
‑
507:ii
‑
43=1:1:1。)
[1158]
而且,使用了4种色素的实施例2
‑
24中,作为第1近红外线吸收化合物而使用0.84份的iii
‑
9,且作为第2近红外线吸收化合物,将iii
‑
673、ii
‑
167,iv
‑
92各使用0.84份。(以质量比计,使用比例为iii
‑
9:iii
‑
673:ii
‑
167:iv
‑
92=1:1:1:1。)
[1159]
而且,实施例2
‑
34中不含有光聚合起始剂。
[1160]
而且,比较例2
‑
1中,将第1近红外线吸收化合物的含量设为2.38份。
[1161]
而且,比较例2
‑
2中,将第1近红外线吸收化合物的含量设为4.0份。
[1162]
而且,实施例2
‑
39中,作为第1近红外线吸收化合物而使用了17.6份的以如下方式制备的颜料分散液。
[1163]
·
颜料分散液的制备。
[1164]
使用直径为0.3mm的氧化锆珠,且通过珠磨机(带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制))来直至吡咯并吡咯化合物的平均粒径(二次粒子)成为75nm以下为止混合下述组合的混合物,并进行分散来制备了颜料分散液。使用nikkiso co.,ltd.制的microtracupa 150,并依据体积基准测定了颜料分散液中的颜料的平均粒径。
[1165]
·
吡咯并吡咯化合物(ii
‑
524)
……
13.5质量份
[1166]
·
树脂(disperbyk
‑
111(bykchemie公司制))
……
4质量份
[1167]
·
丙二醇单甲醚乙酸酯(pgmea)
……
82.5质量份
[1168]
<<近红外线截止滤波器的制作>>
[1169]
(实施例2
‑
1~实施例2
‑
33、实施例2
‑
35~实施例2
‑
39、比较例2
‑
1~比较例2
‑
6)
[1170]
以干燥后的膜厚成为1.0μm的方式使用旋转涂布机,将各组合物涂布于玻璃基板(corning incorporated co.,ltd.制1737)上,并使用100℃的加热板进行120秒钟的加热处理(预烘)来制作了近红外线截止滤波器。
[1171]
接着,使用i线步进机曝光装置fpa
‑
3000i5 (canon inc.制),以500mj/cm2进行了
曝光。进而,使用200℃的加热板来进行300秒钟的加热处理(后烘)来制作了近红外线截止滤波器。
[1172]
(实施例2
‑
34)
[1173]
以干燥后的膜厚成为1.0μm的方式使用旋转涂布机,将实施例2
‑
34的组合物涂布于玻璃基板(corning incorporated co.,ltd.制1737)上,并使用100℃的加热板进行120秒钟的加热处理(预烘)来制作了近红外线截止滤波器。
[1174]
<<红外线屏蔽性评价>>
[1175]
使用分光光度计u
‑
4100(hitachi high
‑
technologies corporation.制)测定了近红外线截止滤波器的透射率。依以下基准评价了红外线屏蔽性。将结果示于以下表。
[1176]
a:极大吸收波长λmax
±
25nm的范围的平均透射率≤10%
[1177]
b:10%<极大吸收波长λmax
±
25nm的范围的平均透射率≤15%
[1178]
c:15%<极大吸收波长λmax
±
25nm的范围的平均透射率≤20%
[1179]
d:20%<极大吸收波长λmax
±
25nm的范围的平均透射率
[1180]
<<可见透明性评价>>
[1181]
使用分光光度计u
‑
4100(hitachi high
‑
technologies corporation.制)测定了近红外线截止滤波器的波长400~550nm的平均透射率。依以下基准评价了可见透明性。将结果示于以下表。
[1182]
a:90%≤波长400~550nm的平均透射率
[1183]
b:85%≤波长400~550nm的平均透射率<90%
[1184]
c:波长400~550nm的平均透射率<85%
[1185]
<<光谱变化性评价>>
[1186]
将近红外线截止滤波器于85℃、相对湿度85%的高温高湿的环境下放置1小时。分别在耐湿性试验前和耐湿性试验后,使用分光光度计u
‑
4100(hitachi high
‑
technologies corporation.制)测定近红外线截止滤波器的波长700~1400nm下的最大吸光度(absλmax)和波长400~700nm下的最小吸光度(absλmin),并求出以“absλmax/absλmin”表示的吸光度比。依据以下基准评价了以|(试验前的吸光度比
‑
试验后的吸光度比)/试验前的吸光度比
×
100|(%)表示的吸光度比变化率。将结果示于以下表。
[1187]
a:吸光度比变化率≤2%
[1188]
b:2%<吸光度比变化率≤4%
[1189]
c:4%<吸光度比变化率≤7%
[1190]
d:7%<吸光度比变化率
[1191]
<<耐光性>>
[1192]
针对近红外线截止滤波器,将氙气灯以5万lux照射20小时(相当于100万lux/h)之后,测定了耐光试验前后的色差的δeab值。δeab值小时表示耐光性良好。将结果示于以下表。另外,δeab值为以基于cie1976(l*,a*,b*)空间颜色系统的自以下色差公式求出的值(日本色彩学会编着新编色彩科学手册(昭和60年)p.266)。
[1193]
δeab={(δl*)2 (δa*)2 (δb*)2}
1/2
[1194]
a:δeab值<5
[1195]
b:5≤δeab值<10
[1196]
c:10≤δeab值<20
[1197]
d:20≤δeab值
[1198]
[1199]
如上述表所示,实施例中,光谱变化性、红外线屏蔽性及可见透明性优异。而且,作为第1近红外线吸收化合物而使用吡咯并吡咯化合物的实施例中,耐光性尤其优异。
[1200]
另一方面,比较例中,光谱变化性及红外线屏蔽性至少一个比实施例差。
[1201]
实施例2
‑
1~实施例2
‑
39中,进一步配合彩色着色剂,由此可得到特定可见光以外的透过性及红外线屏蔽性为良好,且光谱变化性优异的滤波器。
[1202]
而且,组合介电质多层膜与通过实施例2
‑
1~实施例2
‑
39的组合物得到的膜而成的积层膜也可以得到优选的效果。
[1203]
实施例2
‑
1~实施例2
‑
39中,进一步配合对可见光进行遮光的色材,由此可得到光谱变化性优异的红外线透射滤波器。
[1204]
实施例2
‑
1~实施例2
‑
39中,即使将固化性化合物(二季戊四醇六丙烯酸酯(nippon kayaku co.,ltd.制、产品名kayarad dpha))改变成二甘油eo(环氧乙烷)改质(甲基)丙烯酸酯(toagosei co.,ltd.制、产品名m
‑
460)也可得到相同的效果。
[1205]
实施例2
‑
1~实施例2
‑
19、实施例2
‑
25~实施例2
‑
39中,即使使用以下组合10来形成膜,也可得到与实施例相同的效果。
[1206]
(组合10)
[1207]
将下述组合混合并搅拌之后,以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤来制备了组合物。
[1208]
[组合]
[1209]
第1近红外线吸收化合物(表中所示的化合物)
……
2.38份
[1210]
第2近红外线吸收化合物(表中所示的化合物)
……
0.98份
[1211]
树脂1、树脂2或树脂3
……
7.52份
[1212]
固化性化合物(二季戊四醇六丙烯酸酯(nippon kayaku co.,ltd.制、产品名kayarad dpha))
……
1.41份
[1213]
光聚合起始剂(下述化合物)
……
1.55份
[1214]
[化学式79]
[1215][1216]
界面活性剂(megaface rs
‑
72
‑
k(dic corporation制、30%丙二醇单甲醚乙酸酯溶液))
……
0.467份
[1217]
聚合抑制剂(对甲氧基苯酚)
……
0.001份
[1218]
环戊酮
……
85.68份
[1219]
<试验例3>
[1220]
以制膜后的膜厚成为1.0μm的方式利用旋转涂布法,将实施例2
‑
5或实施例2
‑
26的组合物涂布于硅晶圆上。之后使用加热板在100℃下加热2分钟。接着,使用加热板,在200℃下加热5分钟。接着通过干式蚀刻法形成了2μm的bayer图案(近红外线截止滤波器)。
[1221]
接着,以制膜后的膜厚成为1.0μm的方式利用旋转涂布法,将red组合物涂布于近红外线截止滤波器的bayer图案上。接着,使用加热板在100℃下加热2分钟。接着,使用i线步进机曝光装置fpa
‑
3000i5 (canon inc.制),且经由遮罩以1000mj/cm2曝光2μm的点图案。接着使用氢氧化四甲铵(tmah)0.3质量%水溶液,在23℃下进行60秒钟的搅拌式(paddle)显影。之后,通过旋转喷淋进行冲洗,进而用纯水来进行水洗。接着,使用加热板,在200℃下加热5分钟,由此在近红外线截止滤波器的bayer图案上将red组合物进行图案化。同样地,依次对green组合物、blue组合物进行图案化,从而形成了红、蓝及绿色着色图案。
[1222]
接着,以制膜后的膜厚成为2.0μm的方式利用旋转涂布法,将红外线透射滤波器形成用组合物(组合100或组合101)涂布于上述图案形成的膜上。接着,使用加热板在100℃下加热2分钟。接着,使用i线步进机曝光装置fpa
‑
3000i5 (canon inc.制),且将2μm的bayer图案经由遮罩以1000mj/cm2进行曝光。接着。使用氢氧化四甲铵(tmah)0.3质量%水溶液,在23℃下进行60秒钟的搅拌式(paddle)显影。之后,通过旋转喷淋进行清洗,进而用纯水进行水洗。接着,使用加热板在200℃下加热5分钟,由此对近红外线截止滤波器的bayer图案的缺陷部分以红外线透射滤波器进行图案化。根据该些公知的方法组装了固体成像元件。所得到的固体成像元件的入射角依赖性良好。进而,识别评价也良好。
[1223]
另外,使用实施例2
‑
5的组合物来制作近红外线截止滤波器的情况下,使用了组合100的红外线透射滤波器形成用组合物。使用实施例2
‑
26的组合物来制作近红外线截止滤波器的情况下,使用了组合101的红外线透射滤波器形成用组合物。
[1224]
试验例3中所使用的red组合物、green组合物、blue组合物及红外线透射滤波器形成用组合物如以下。
[1225]
(red组合物)
[1226]
将下述成分混合并进行撹拌之后,以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤而制备了red组合物。
[1227]
red颜料分散液
……
51.7质量份
[1228]
树脂4(40%pgmea溶液)
……
0.6质量份
[1229]
固化性化合物4
……
0.6质量份
[1230]
光聚合起始剂1
……
0.3质量份
[1231]
界面活性剂1
……
4.2质量份
[1232]
pgmea
……
42.6质量份
[1233]
(green组合物)
[1234]
将下述成分混合并搅拌之后,以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤而制备了green组合物。
[1235]
green颜料分散液
……
73.7质量份
[1236]
树脂4(40%pgmea溶液)
……
0.3质量份
[1237]
固化性化合物1
……
1.2质量份
[1238]
光聚合起始剂1
……
0.6质量份
[1239]
界面活性剂1
……
4.2质量份
[1240]
紫外线吸收剂1
……
0.5质量份
[1241]
pgmea
……
19.5质量份
[1242]
(blue组合物)
[1243]
将下述成分混合并搅拌之后,以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤而制备了blue组合物。
[1244]
blue颜料分散液
……
44.9质量份
[1245]
树脂4(40%pgmea溶液)
……
2.1质量份
[1246]
固化性化合物1
……
1.5质量份
[1247]
固化性化合物4
……
0.7质量份
[1248]
光聚合起始剂1
……
0.8质量份
[1249]
界面活性剂1
……
4.2质量份
[1250]
pgmea
……
45.8质量份
[1251]
(红外线透射滤波器形成用组合物)
[1252]
将下述组合中的成分混合并搅拌之后,以孔径0.45μm的尼龙制滤波器(nihon pall ltd.制)进行过滤而制备了红外线透射滤波器形成用组合物。
[1253]
(组合100)
[1254]
颜料分散液1
‑1……
46.5质量份
[1255]
颜料分散液1
‑2……
37.1质量份
[1256]
固化性化合物5
……
1.8质量份
[1257]
树脂4
……
1.1质量份
[1258]
光聚合起始剂2
……
0.9质量份
[1259]
界面活性剂1
……
4.2质量份
[1260]
聚合抑制剂1
……
0.001质量份
[1261]
基板粘结剂
……
0.6质量份
[1262]
pgmea
……
7.8质量份
[1263]
(组合101)
[1264]
颜料分散液2
‑1……
22.67质量份
[1265]
颜料分散液3
‑1……
11.33质量份
[1266]
颜料分散液3
‑2……
22.67质量份
[1267]
颜料分散液3
‑3……
10.34质量份
[1268]
颜料分散液3
‑4……
6.89质量份
[1269]
固化性化合物6
……
1.37质量份
[1270]
树脂5
……
3.52质量份
[1271]
光聚合起始剂1
……
0.86质量份
[1272]
界面活性剂1
……
0.42质量份
[1273]
聚合抑制剂1
……
0.001质量份
[1274]
pgmea
……
19.93质量份
[1275]
red组合物、green组合物、blue组合物及红外线透射滤波器形成用组合物中所使用的原料为如下。
[1276]
·
red颜料分散液
[1277]
通过珠磨机(直径为0.3mm的氧化锆珠,将包含9.6质量份的c.i.pigment red 254、4.3质量份的c.i.pigment yellow 139、6.8质量份的分散剂(disperbyk
‑
161、bykchemie公司制)、79.3质量份的pgmea的混合液混合并分散3小时,从而制备了颜料分散液。之后,进一步使用带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制)在2000kg/cm3的压力下以流量500g/min进行了分散处理。将该分散处理重复10次而得到了red颜料分散液。
[1278]
·
green颜料分散液
[1279]
通过珠磨机(直径为0.3mm的氧化锆珠),将包含6.4质量份的c.i.pigment green 36、5.3质量份的c.i.pigment yellow 150、5.2质量份的分散剂(disperbyk
‑
161,bykchemie公司制)、83.1质量份的pgmea的混合液混合并分散3小时,从而制备了颜料分散液。之后,进一步使用带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制)在2000kg/cm3的压力下以流量500g/min进行了分散处理。将该分散处理重复10次而得到了green颜料分散液。
[1280]
·
blue颜料分散液
[1281]
通过珠磨机(直径为0.3mm的氧化锆珠),将包含9.7质量份的c.i.pigment blue 15:6、2.4质量份的c.i.pigment violet 23、5.5份的分散剂(disperbyk
‑
161、bykchemie公司制)、82.4份的pgmea的混合液混合和并分散3小时,从而制备了颜料分散液。之后,进一步使用带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制),在2000kg/cm3的压力下以流量500g/min进行了分散处理。将该分散处理重复10次而得到了blue颜料分散液。
[1282]
·
颜料分散液1
‑1[1283]
使用直径为0.3mm的氧化锆珠,且通过珠磨机(带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制))来将下述组合的混合液混合并分散3小时,从而制备了颜料分散液1
‑
1。
[1284]
·
包含红色颜料(c.i.pigment red 254)及黄色颜料(c.i.pigment yellow 139)的混合颜料
……
11.8质量份
[1285]
·
树脂(disperbyk
‑
111,bykchemie公司制)
……
9.1质量份
[1286]
·
pgmea
……
79.1质量份
[1287]
·
颜料分散液1
‑2[1288]
使用直径为0.3mm的氧化锆珠,且通过珠磨机(带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制))来将下述组合的混合物混合并分散3小时,从而制备了颜料分散液1
‑
2。
[1289]
·
包含蓝色颜料(c.i.pigment blue 15:6)及紫色颜料(c.i.pigment violet 23)的混合颜料
……
12.6质量份
[1290]
·
树脂(disperbyk
‑
111,bykchemie公司制)
……
2.0质量份
[1291]
·
树脂10
……
3.3质量份
[1292]
·
环己酮
……
31.2质量份
[1293]
·
pgmea
……
50.9份
[1294]
树脂10:下述结构的树脂(mw=14,000,结构单元中的比为摩尔比)
[1295]
[化学式80]
[1296][1297]
·
颜料分散液2
‑1[1298]
使用直径为0.3mm的氧化锆珠,且通过珠磨机(带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制))来将下述组合的混合物混合并分散,直至吡咯并吡咯颜料的平均粒径(二次粒子)成为75nm以下为止,从而制备了颜料分散液。使用nikkiso co.,ltd.制的microtracupa 150,并依据体积基准测定了颜料分散液中的颜料的平均粒径。
[1299]
·
吡咯并吡咯颜料
……
13.5质量份
[1300]
·
树脂(disperbyk
‑
111,bykchemie公司制)
……
4质量份
[1301]
·
pgmea
……
82.5质量份
[1302]
·
吡咯并吡咯颜料:下述结构的化合物
[1303]
[化学式81]
[1304][1305]
·
颜料分散液3
‑1[1306]
使用直径为0.3mm的氧化锆珠,且通过珠磨机(带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制))来混合并分散下述组合的混合液,从而制备了颜料分散液。
[1307]
·
c.i.pigment red 254
……
13.5质量份
[1308]
·
树脂11
……
2质量份
[1309]
·
树脂12
……
2质量份
[1310]
·
pgmea
……
82.5质量份
[1311]
·
树脂11:下述结构的树脂(mw:7950,在主链标记的数值为摩尔比,在侧链标记的数值为重复单元的数量)
[1312]
[化学式82]
[1313][1314]
·
树脂12:下述结构的树脂(mw:12000、结构单元中的比为摩尔比)
[1315]
[化学式83]
[1316][1317]
·
颜料分散液3
‑2[1318]
使用直径为0.3mm的氧化锆珠,且通过珠磨机(带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制))来混合并分散下述组合的混合液,而制备了颜料分散液。
[1319]
·
c.i.pigment blue 15:6
……
13.5质量份
[1320]
·
树脂13
……
4质量份
[1321]
·
pgmea
……
82.5质量份
[1322]
·
树脂13:下述结构的树脂(mw:30000,在主链标记的数值为摩尔比,在侧链标记的数值为重复单元的数量)
[1323]
[化学式84]
[1324][1325]
·
颜料分散液3
‑3[1326]
使用直径为0.3mm径的氧化锆珠,且通过珠磨机(带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制))来混合并分散下述组合的混合液,从而制备了颜料分散液。
[1327]
·
c.i.pigment yellow 139
……
14.8质量份
[1328]
·
树脂(disperbyk
‑
111,bykchemie公司制)
……
3质量份
[1329]
·
树脂12
……
2.2质量份
[1330]
·
pgmea
……
80质量份
[1331]
·
颜料分散液3
‑4[1332]
使用直径为0.3mm的氧化锆珠,且通过珠磨机(带减压机构的高压分散机nano
‑
3000
‑
10(nippon bee chemical co.,ltd.制))来混合并分散下述组合的混合液,从而制备了颜料分散液。
[1333]
·
c.i.pigment violet 23
……
14.8质量份
[1334]
·
树脂(disperbyk
‑
111、bykchemie公司制)
……
3质量份
[1335]
·
树脂12
……
2.2质量份
[1336]
·
pgmea
……
80质量份
[1337]
·
固化性化合物1:kayarad dpha(nippon kayaku co.,ltd.制)
[1338]
·
固化性化合物4:下述结构的化合物
[1339]
[化学式85]
[1340][1341]
·
固化性化合物5:下述结构的化合物(左侧化合物与右侧化合物的摩尔比为7:3的混合物)
[1342]
[化学式86]
[1343][1344]
·
固化性化合物6:m
‑
305(三丙烯酸酯为55~63质量%、toagosei co.,ltd.制)
[1345]
·
树脂4:下述结构的树脂(酸值:70mgkoh/g、mw=11000、结构单元中的比为摩尔比)
[1346]
[化学式87]
[1347][1348]
·
树脂5:下述结构的树脂(mw=40,000、结构单元中的比为摩尔比)
[1349]
[化学式88]
[1350][1351]
·
光聚合起始剂1:irgacure
‑
oxe01(basf公司制)
[1352]
·
光聚合起始剂2:下述结构的化合物
[1353]
[化学式89]
[1354][1355]
·
界面活性剂1:下述混合物(mw=14000、1%pgmea溶液)
[1356]
[化学式90]
[1357][1358]
·
基板粘结剂:下述结构的化合物
[1359]
[化学式91]
[1360][1361]
·
聚合抑制剂1:对甲氧基苯酚
[1362]
·
紫外线吸收剂:下述结构的化合物
[1363]
[化学式92]
[1364][1365]
符号说明
[1366]
110
‑
固体成像元件,111、111a
‑
近红外线截止滤波器,112
‑
滤色器,114
‑
红外线透射滤波器,115
‑
微透镜,116
‑
平坦化层,151
‑
支撑体。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。