本申请要求于2019年2月26日提交的美国临时专利第62/810,866号(代理案卷号56027-703.101)的权益,其全部内容通过引用并入本文。
背景技术
1.技术领域。本发明总体上涉及医疗装置、系统和方法。更具体地,本发明涉及用于向患有晚期心力衰竭的患者提供心脏辅助的系统。
已经提出了多种心室辅助装置(VAD)用于支持患有严重心力衰竭的患者的血液循环。VAD还用于让患者存活,直到供体心脏可以用于移植,作为“移植的桥梁”。在美国,由于终末期心力衰竭,每年有多达50,000名患者需要心脏移植。供体心脏每年仅可用于2,000至2,500名患者。许多无法接受移植的患者可以通过接受VAD存活下来。
然而,目前可用的VAD的放置(典型地是胸骨切开术或开胸术)通常地需要大的外科切口。心力衰竭患者很难接受如此大的外科手术。尽管已经提出了许多微创VAD,诸如血管内旋转泵和外部压缩装置,但是此类微创系统通常需要大的经皮“脐带”来提供驱动植入的泵辅助部件的动力。此类绳索不方便、不舒服,并且存在很大的感染风险。此外,当感染时,移除大脐带通常需要外科干预。
由于这些原因,期望提供用于向患有晚期心力衰竭的患者提供心脏辅助的改善的设备、系统和方法。特别期望提供此类系统,所述系统可以通过剑突下和其他已建立的微创途径植入。还期望提供具有经皮连接器的VAD系统,其降低了感染的风险,并且如果它们被感染,则更容易更换和消毒。本文描述和要求保护的发明将满足这些要求中的至少一些。
2.背景技术的描述。相关专利和出版物包括US2019/0076250;US2008/0275295;US2007/0073218;US10391216;US10220128;US9259318;US8092363;US7468029;US6602182;US6432039;US6238334;US5713954;US4957477;和WO1998/005289。
技术实现要素:
本发明为患有心力衰竭或其他心脏功能受损的患者提供一种微创心脏辅助装置。所述装置包括可植入的心脏辅助导管,所述可植入的心脏辅助导管典型地被配置为通过导丝推进到患者心包囊中位于心肌表面和心包内表面之间的位置。可植入心脏辅助导管在其远侧端部具有球囊或其他气动执行器,并且通常提供外部驱动单元以使球囊充气与患者自然心动周期的心室收缩同步,从而压缩心脏并且提供心室辅助,从而增加患者的心输出量。纤维心包囊的相对不灵活提供限制性约束,导致充气的球囊压缩心室。此外,胸骨还覆盖心脏并且提供骨性外壳以增强球囊充气时的心脏压缩。心脏辅助装置可以与传感器一起使用以获得用于同步球囊充气的心电图信号。
心包内心脏辅助导管可以仅锚定在心包的进入点。替代地,它可在心尖附近进入心包,并且在更上方离开心包,朝向心脏底部,并且在导管的远侧尖端附近可以存在扩张锚定件,诸如小球囊,位于心包外部并且维持心室压缩球囊的位置。心室压缩球囊在形状上可以是椭圆形的,其长度的大小可以沿着心室腔的主要部分延伸。心室压缩球囊可以用流体(气体或液体,通常是气体)充气,以便减少充气/放气时间。气体可以是优选的,因为它允许球囊充气和球囊放气的快速响应时间。球囊充气的频率应等于生理心率,约为70bpm。小的贮存器可以附接到导管的近侧端部。贮存器的一个表面可以含有隔膜或其他弹性部分,针可以通过隔膜或其他弹性部分插入以用于球囊充气,同时密封插入的针。替代地,整个贮存器可由自密封针穿刺的弹性材料构成。在放置导管后,可以经由小的皮肤切口、心脏辅助和取向将贮液器植入皮下,使得弹性表面面向皮肤。球囊导管和附接的皮下贮存器保持植入,而充气泵、控制器和电池位于患者皮肤外部,其中经皮针用于经由植入的贮存器对心室压缩球囊进行充气和放气。此配置便于泵和电池的更换,同时因为小直径的针穿过皮肤而降低了导管感染的可能性。针穿刺位置也可以定期更换,以降低针道感染的可能性。
心室压缩球囊可以借助于位于患者身体外的外部电池操作泵来充气和放气。泵可以是双向流动的,具有附接的流体贮存器;或在心室压缩球囊充气的情况下,泵的入口和出口可以直接通向室内空气。心室压缩球囊充气借助于电子传感器与心动周期同步,所述电子传感器感测患者的ECG(心电图)信号,并且在QRS复合波开始时启动球囊充气。患者ECG感测可以经由来自外部单元的导电针来执行,所述导电针刺穿患者的皮肤以执行球囊充气。替代地,ECG电极或其他传感器可以设置在可植入端口和/或导管中,并且针用于提供与外部控制器中的ECG电路的连接。外部泵模块中的控制单元接收ECG信号并且在心脏收缩期间触发球囊充气。在心脏舒张期间,由泵执行主动球囊放气。还可以使用液压系统执行球囊充气,所述液压系统含有在心脏收缩期间提供球囊充气的加压流体罐和在心脏舒张期间允许球囊放气的压力释放阀。流体罐可以定期重新加压,或电池操作的压缩机可以是位于患者身体外的单元的部分。
尽管上面描述了经皮方法,但是心室压缩球囊装置可以经由微创外科方法插入,使用4cm的剑突下小切口进入并且穿刺心尖附近的心包。导丝和锥形扩张器可在心尖部位插入心脏前方的心包内空间,并且在心包左侧的较高位置推进以离开心包。然后,扩张器可以从患者移除,并且心室压缩球囊导管可在导丝上方推进到跨过左心室的位置以用于心脏辅助。
在一些实施方式中,经皮心室辅助装置可以包括球囊导管,所述球囊导管经由剑突下穿刺部位插入患者心尖附近的心包中。含有弹性面的贮存器附接到导管的近侧端部。执行4cm的切口以延伸剑突下穿刺部位,并且将贮液器皮下植入腹壁的上腹部区域中。在此类装置中,单个针会穿透患者的皮肤和贮存器的弹性面,以允许患者体外的泵单元对球囊导管进行充气和放气,从而在心脏收缩期间压缩患者的心室。球囊充气由患者的ECG触发,如实时感测。
获得ECG信号至少需要两个电极。在以前的装置中,充气针形成一个电极,并且第二个电极由表面电极组成,表面电极带有用于皮肤附接在患者腹部或胸部的粘性贴片。从穿过身体组织插入的针获得的ECG信号优于从表面电极获得的ECG信号,因为与表面电极相比,针更不容易受到运动伪影和噪声的影响。所提出的设计将一个、两个或多个电极集成到可植入贮存器,其中导电网从每个电极延伸,以提供扩张的目标来适应针的放置。网中开口的尺寸与针的圆周干涉配合;使得在针插入时,网抵靠针的外表面施加压力,确保最佳的ECG信号传导。针可以含有一系列球形物或倒钩,以便于锚定在目标电极的网状部件中,防止无意中的针脱离。
贮存器的主体可由可植入的聚合物材料构成,诸如聚碳酸酯或聚氯乙烯。电极可由导电金属诸如不锈钢构成。如果将单个电极被并入一个贮存器中,则所述电极可以是附接到聚合物贮存器外径的金属环。如果两个电极并入单个贮存器中,则一个电极可以附接到贮存器的外径,并且另一个电极可以是附接到贮存器的弹性面的小直径同心金属环。不锈钢网可以从外电极朝向内电极径向向内延伸,在网的内边缘和内电极的外边缘之间存在圆周间隙,以充当两个电极之间的绝缘体。替代地,两个电极可由贮存器外径上的两个径向相对的弧形成,钢网在每个弧的两端之间延伸,从而在两个导电网区域之间保留非导电区域。可以应用多个贮存器上的多个电极的组合;例如,两个电极可以位于一个植入的贮存器上,单个电极可以位于第二个植入的贮存器上,以产生三导联EKG传感阵列。
在本发明的另一个实施方式中,接收EKG信号并且控制外部泵单元的激活的电路板定位在贮存器中。来自控制板的信号经由光纤传输来传输到外部泵单元,确保因患者运动而产生的信号噪声最小。由围绕其中一个充气针的圆周阵列组成的光纤连接与电路板中的对应的圆形阵列匹配。漏斗导向器被并入贮存器的内同心电极中,以确保针插入导致针上的相应光纤阵列和贮存器中的控制板接合。通过网状电极插入的两个针携载来自外部单元的电流,以便为贮存器内的电路板供电。
在第一方面,本发明提供一种心脏辅助系统,其包括气动执行器,所述气动执行器被配置为植入患者的心包囊下方和心肌表面上方,典型地覆盖患者左心室。所述系统还包括可植入端口,所述可植入端口被配置为接收经皮引入的套管,其中所述套管向气动执行器供应驱动气体。典型地,气动执行器可以是位于导管或其他管状主体的远侧端部附近的球囊,其中可植入端口在近侧端部附近连接到导管或其他管。
心脏辅助系统还包括外部驱动单元,所述外部驱动单元包含泵组件和控制电路。泵组件包含至少一个泵,用于将气体(典型地是环境空气)输送到套管。控制电路典型地被配置为响应于患者感测到的心律来操作泵以致动气动执行器。通常,连接管具有可连接到泵组件的泵的泵端和附接到套管的套管端。
在特定实施方式中,气动执行器可以包括可膨胀的球囊,诸如医疗球囊,典型地是导管上的不可膨胀的医疗球囊,其中球囊被配置为位于患者左心室上方和心包囊内表面下方。当完全充气时,球囊将典型地具有在50ml至200ml的范围内,典型地在76ml至125ml的范围内的体积。在其他情况下,气动执行器可以包括一些其他可气动致动机械装置,诸如活塞和气缸装置。
在本发明的其他示例和示例中,可植入端口可以包括针可穿透的隔膜,其中套管包括针或其他尖锐的管或中空探针,所述针或其他尖锐的管或中空探针被配置为经皮穿透覆盖在隔膜上的患者组织(典型地是腹壁),并且进一步穿透隔膜以将泵组件和外部驱动单元与端口内部流体连接,使得空气或其他气体可在压力下输送以充气或以其他方式致动气动执行器。
在特定情况下,隔膜将具有足够大的面积以提供用于针穿透的多个部位。当经皮插入部位被感染时,这是一个特别的优点。通过具有多个针穿透部位,可以从接受治疗的患者的感染区域移除针,并且新的或消毒的针可以通过隔膜上的替代部位引入可植入端口。以此方式,为了治疗感染,可植入端口和气动执行器都不需要被移出或以其他方式受到显著干扰。
然而,在替代实施方式中,可植入端口可以包括用于接收针或其他套管的机械阀。此类机械端口对于血液透析通路和其他目的是众所周知的。例如,参见US 6,120,492,其全部公开内容通过引用并入本文。
在此外其他实施方式中,本发明的系统将还包括至少一个心电图(ECG)电极,所述至少一个心电图(ECG)电极被定位并且被配置为检测患者的心律。与常规的ECG检测系统一样,ECG电极可以位于外部,并且可以包括一个、两个、三个、四个或更多个外部电极。然而,方便的是,一个或多个ECG电极可以并入心脏辅助系统中。例如,电极可由用于进入可植入端口的针或其他套管提供或并入所述针或其他套管中。替代地或另外地,一个或多个ECG电极可以位于或耦合到可植入端口本身。例如,一个、两个、三个、四个或更多个ECG电极可以附接到端口壳体的外表面、端口隔膜或其他膜,或端口上的其他地方。进一步替代地或另外地,一个或多个ECG电极可以位于连接管上和/或气动执行器本身上。
在具有ECG电极的系统中,外部驱动单元典型地将还包括ECG电路,以便检测心律并且使泵组件的致动与心律同步。当ECG电极存在于可植入端口或连接管的任何部分上时,电导体可以设置在针或其他套管中或穿过针或其他套管设置,以便将电信号输送到ECG电路。当针或其他套管本身包括ECG电极时,针或其他套管可以通过将套管连接到外部电极的导管或其他结构中的导体连接到ECG电路。常规的外部ECG电极可以通过常规的ECG导线连接到外部控制器。
外部驱动单元中的控制电路将典型地被配置为与由ECG测量的患者的心律同步地致动气动执行器。例如,控制电路可以被配置为在每次出现R波峰值时致动气动执行器。通常,控制电路将被进一步被配置为检测异常心律。例如,控制电路可以比较连续的单个R峰值之间的时间,并且基于时间增加或减少超过预定阈值百分比,诸如300%,通常是250%,来确定异常心律的出现。替代地或另外地,控制电路可以比较连续的累积R峰值之间的时间,并且基于超过预定阈值百分比(典型地为300%,通常为250%)的总变异性来确定是否存在异常心律。
当控制电路检测到异常心律时,它可以采取若干措施中的任一种。例如,控制电路可以简单地停止气动执行器的致动,直到心律恢复到正常模式。替代地,控制电路可以以预定的固定速率致动气动执行器,所述固定速率典型地在从50跳动/分钟(bpm)到80跳动/分钟的范围内,并且继续此类致动,直到重新建立正常的心律。进一步替代地,控制电路可以被配置为当检测到异常心律时,以相对于患者的心律“成比例地”修改的速率致动气动执行器。也就是说,尽管当心律正常时,气动执行器的致动典型地是1:1的比率,但是当检测到异常心律时,所述比率可以改变为另一个比率。例如,如果患者经历异常高的心率(心动过速),则气动执行器被触发的速率可能降低。气动执行器可以每两次心跳触发一次(1:2),每三次心跳触发一次(1:3),等等。
在此外其他实施方式中,心脏辅助系统的泵组件可以被配置为交替地将驱动气体输送到气动执行器和从气动执行器中抽出驱动气体。每个输送和抽出周期将对应于来自外部控制器的控制电路的单个触发事件。泵输送和泵抽出的周期将对应于从ECG检测到的患者心率,对于心率为60bpm的患者,单个周期典型地持续约一秒钟。应理解,此类快速充气和放气需要快速作用的系统,并且可用的气体传输体积、流体传输腔尺寸等将需要符合所需的充气和放气时间。为了实现快速的输送和抽取时间,被输送的流体典型地是气体,通常是环境空气。
泵组件可以采取多种配置中的任一种,用于将流体输送和抽出到气动执行器。例如,泵组件可以包含在单个流动方向上操作的单个泵,其还包括将气体从充气方向转向放气方向所需的阀。替代地,泵组件可以包括一对泵,一个在流体输送方向上操作,并且另一个在流体抽取方向上操作。还应理解,泵组件可以连接到单个套管,所述套管提供从可植入泵的流体输送和流体抽取。替代地,泵组件可以连接到一对套管,一个用于输送充气流体,并且一个用于抽取充气流体。
在第二方面,本发明提供一种用于辅助患有心力衰竭的患者的心脏功能的方法。所述方法可以包括检测患者的ECG以确定心律。患者内的植入端口通过套管经皮进入,驱动气体通过套管输送到连接的端口,然后输送到植入患者左心室的气动执行器。驱动气体的输送和抽取与感测到的心律同步,以使得气动执行器以通常与患者的自然心律相匹配的速率压缩心脏。
在特定实施方式中,气动执行器将被植入患者心包囊下方和心肌表面上方。在进一步的特定实施方式中,气动执行器将在心脏辅助导管上,所述心脏辅助导管在入口位置处通过心包进入,并且在一些情况下,具有在出口位置处穿过心包而出去的远侧尖端。可在心脏辅助导管的远侧尖端上提供锚定件(诸如小锚定球囊),以便将气动执行器稳定在心包囊中的期望位置。
在又一特定实施方式中,可以以多种方式检测ECG。例如,一个或多个ECG电极可以位于植入端口上、植入气动执行器上或系统的植入部分上的其他地方。在此类情况下,可以使用套管作为经皮传输元件或导体将来自植入的ECG电极的信号输送到外部控制器中的ECG电路。在其他特定实施方式中,套管或多个套管在它们被经皮引入植入端口后,其本身可以充当ECG电极。在其他特定实施方式中,可以通过以常规方式附接到患者的一个或多个外部电极来测量ECG信号。应理解,可以采用单通道ECG,但是优选地,将采用至少双通道ECG,优选地,三通道ECG、四通道ECG或更大。电极也可以放置在植入的气动执行器上,以在患者心动过缓的情况下提供心脏起搏,或在患者出现室性心动过速、心室颤动或心搏停止的情况下提供心脏除颤。
本发明的方法还包括可选地检测异常心律。异常心律将基于测量的ECG来确定,并且异常心律的存在典型地将导致气动执行器的停止或修改操作。例如,当检测到异常心律时,可以停止驱动气体。替代地,当检测到异常心律时,可以改变驱动气体的输送速率。特别地,在存在快速心跳(心动过速)的情况下,行驶速率可能降低,或在存在慢速心跳(心动过缓)的情况下,行驶速率可能增加。
本发明的方法还包括用于在组织进入部位被感染的情况下治疗患者的方案。在此类情况下,针或其他套管可以从组织管道中抽出,组织管道进行感染治疗,并且套管(消毒后的或新的套管)典型地通过不同的进入路径被重新引入到植入端口。例如,对于隔膜型端口,可以通过未感染组织中的新组织管道将套管引入到所述部分的不同区域。
在第三方面,本发明提供一种与外部驱动单元一起使用的可植入心脏辅助导管,所述可植入心脏辅助导管包括导管主体,所述导管主体具有近侧端部和远侧端部。气动执行器附接到导管主体的远侧端部,并且被配置为植入患者心包囊下方和覆盖患者左心室的心肌表面上方。可植入端口附接在导管主体的近侧端部,并且被配置为接收经皮引入的套管。所述端口被连接以通过导管主体中的气体腔将从套管接收到的驱动气体供应到气动执行器。通过控制驱动气体向可植入端口的供应,气动执行器可由外部驱动单元控制的期望速率驱动。
在特定实施方式中,可植入心脏辅助导管可以包括具有导丝腔的远侧尖端,所述导丝腔具有入口端口和出口端口,其中两个端口都位于气动执行器的远侧。此类“单轨”结构是有利的,因为它允许导管主体的剩余部分仅具有单个流体输送腔,因此减小了导管所需的直径。因此,气体腔和导管主体典型地将是存在于导管主体近侧端部和气动执行器之间的唯一腔。
可选地,可植入心脏辅助导管的远侧尖端还可以包括锚定球囊或其他锚定结构。可以通过将远侧导管尖端向外推进穿过心包来使用此类锚定结构。在气动执行器被正确定位后,典型地在患者的左心室上方,可以部署锚定件(例如,通过球囊充气)以稳定导管位置以供后续使用。
在第四方面,本发明提供一种用于可植入心脏辅助导管(诸如刚刚描述的心脏辅助导管)的外部驱动单元。外部驱动单元包括泵组件和控制电路。控制电路典型地被配置为操作泵组件,以响应于患者感测到的心律来致动可植入心脏辅助导管上的气动执行器。
在特定实施方式中,外部驱动单元还可以包括连接管,所述连接管具有附接到所述泵组件的泵端和经皮端口连接端,所述经皮端口连接端被配置为可移除地附接到可植入端口,所述可植入端口流体连接到所述可植入心脏辅助导管上的气动执行器。在此外其他实施方式中,外部驱动单元可以包含ECG电路,其中ECG电路被配置为从位于前述任何位置的至少一个ECG电极接收信号,其中至少一个ECG电极被植入以检测患者的心律。典型地,连接管将包括至少一个导体,所述导体电耦合到套管并且被配置为将ECG电极连接到外部驱动单元中的ECG电路。
在又一示例性实施方式中,外部驱动单元的控制电路可以被配置为与由ECG电极测量的患者的心律同步地致动气动执行器。如上所描述的,可以通过检测R波峰值的出现来实现致动。控制电路还可以被配置为检测异常心律,并且还进一步以前面描述的任何方式停止或修改气动执行器的致动。泵组件还可以具有先前关于本发明的心脏辅助系统描述的任何配置。
为了更全面地理解本发明的实质和优点,应参考随后的具体实施方式和附图。
附图说明
为了更好地理解本发明并且了解如何在实践中实践本发明,接下来参考附图,仅通过非限制性示例的方式描述一些优选实施方式,在附图中,类似的附图标记始终表示类似实施方式中的对应特征。
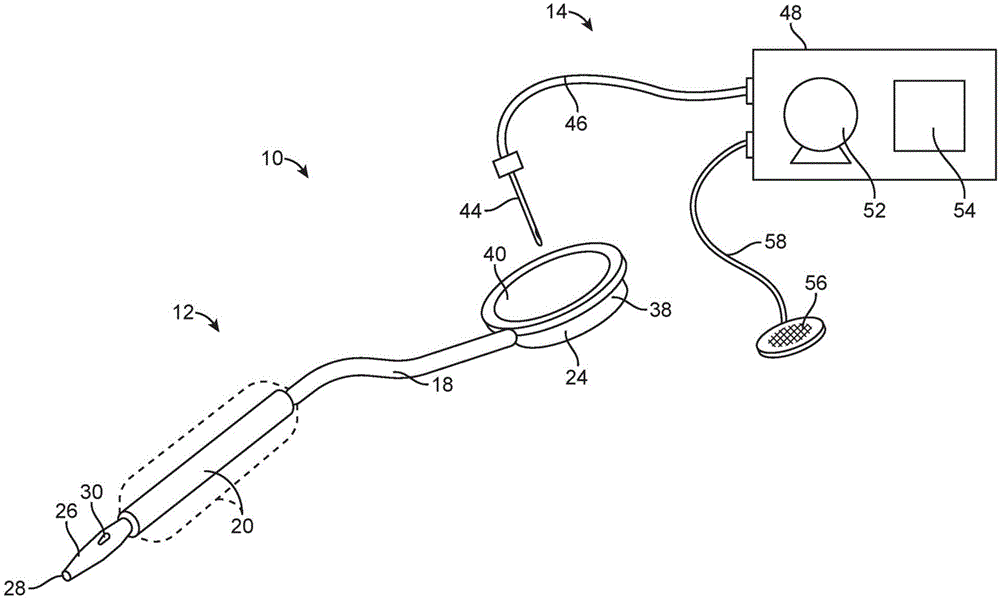
图1是根据本发明的原理配置的心脏辅助系统的透视图。
图2A至图2D绘示了适用于本发明心脏辅助系统的泵组件的不同配置。
图3A至图3B绘示了根据本发明的原理配置的第一可植入端口配置。
图4A至图4B绘示了根据本发明的原理配置的第二可植入端口实施方式。
图5A至图5B绘示了根据本发明的原理配置的第三种可植入端口配置。
图6绘示了针或其他套管如何与嵌入可植入端口的隔膜中的导电网的导线接合的细节。
图7A绘示了沿着其长度具有保持球形物的针套管。
图7B绘示了根据本发明的针或其他套管,其沿着其长度具有保持倒钩。
图8A至图8B绘示了根据本发明的原理配置的并且具有用于将心律信息从可植入端口输送到外部驱动单元的光纤部件的替代进入套管。
图9绘示了适用于图8A和图8B的进入套管的可植入端口。
图10绘示了植入患者内的图1的心脏辅助系统。
图10A绘示了在其远侧尖端具有球囊锚定件的心脏辅助导管的替代实施方式。
图11是说明本发明的心脏辅助系统的外部驱动单元的操作的逻辑流程图。
具体实施方式
在以下描述中,将描述本发明的各种实施方式。出于解释的目的,阐述了具体的配置和细节,以便提供对实施方式的透彻理解。然而,对于本领域技术人员来说容易理解的是,可在没有具体细节的情况下实践本发明。此外,可以省略或简化众所周知的特征以免模糊所描述的实施方式。
现在参考图1,根据本发明的原理配置的心脏辅助系统10可以包括心脏辅助导管12和外部驱动单元14。心脏辅助导管12典型地包含导管主体18,所述导管主体18具有位于其远侧端部的球囊20或其他气动执行器。可植入端口24连接在导管主体18的近侧端部,并且所述主体典型地具有远侧尖端26,所述远侧尖端26具有限定在导丝腔入口端口28和导丝腔出口端口30之间的短“单轨”导丝腔。导丝腔的长度典型地为0.5cm至3cm,典型地为1cm至2cm。
端口24包括端口主体38或在其上表面上具有开口的其他外壳。开口典型地被针可穿透的隔膜40覆盖。
外部驱动单元14包括附接到连接管46的远侧端部的针44或其他套管。连接管附接到控制台48内的泵52,并且控制台还包含用于控制泵和心脏辅助系统10的其他操作的控制电路54。可选地,外部驱动单元14还可以包括通过连接电缆58连接到控制电路54的ECG垫56。典型地,泵、控制电路和全部其他有源部件将由电池操作,并且外部驱动单元14将包含可更换和/或可充电的电池。
现在参考图2A至图2D,泵组件52可以包括多种配置。例如,如图2A中所示,典型地为隔膜型泵的泵单元52A通过一系列阀60a-60d连接到套管44。泵50A将被配置为始终沿着单个方向运行,即入口将始终接收气体而出口将始终输送气体。为了将气体输送到套管44,阀60a将打开,允许环境空气流向泵50A。环境空气从泵的出口输送到打开的阀60b。当向套管输送气体时,阀60c和60d将关闭。气体继续被输送,直到气动执行器20充气,此时阀60a-60d反转。也就是说,气体入口阀60a关闭而回流旁通阀60c打开,从而允许气体通过套管44被抽取,并且由泵52A通过打开的排气阀60d输送。通过反转阀60a-60d的打开/关闭状态,可以使得在无需反转泵52A的操作的情况下的泵首先通过套管输送气体,然后通过套管抽取气体。
同样如图2A中示出的,ECG导线70可以设置在套管44和外部驱动单元14的控制电路54之间。
现在参考图2D,单个泵52B可以与一对套管44a和44b一起使用。阀62a-62d将用于使套管之间的气流反转。特别地,通过打开阀62a和阀62d,环境空气可以被输送到气体输送套管44a。通过随后关闭阀62a和62b,并且打开阀62c和62d,气体可以通过套管44b被抽取并且排出排气阀62d。气体的流入和流出可以通过以类似于图2A的阀的方式反转阀的状态来循环。
在图2B中,每个套管44a和44b具有单独的ECG导线72a和72b,所述单独的ECG导线72a和72b连接到外部驱动单元14的控制电路54。
现在参考图2C,将描述包括两个泵52c1和52c2的泵组件52。控制电路54致动第一泵52c1以通过阀64a然后通过套管44输送环境空气,同时回流阀64b保持关闭。在气动执行器被完全充气或以其他方式致动后,阀64a将被关闭,并且泵典型地停止。如图所绘示,然后,回流阀64b将被打开,并且泵52c2被致动,以通过套管44排出气体,并且通过排气管线排出。两个泵和阀的操作可以周期性地反转,以便以期望的速率循环输送气体到植入端口和从植入端口排出气体。
同样如图2C中示出的,ECG导线74可以设置在套管44和外部驱动单元14的控制电路54之间。
现在参考图2D,将描述第四泵组件配置。此组件包括两个泵52d1和52d2。每个泵又相应地连接到单个套管44a和44b。尽管典型地会设置阀,但是理论上不需要阀来使系统在通过泵52d1和套管44a的气体输送和通过套管44b和泵52d2的气体抽取之间循环,这可以通过在循环期间的交替时间简单地起动和停止泵来实现。
同样如图2D中示出的,每个套管44a和44b相应地通过ECG导线76a和76b连接到控制电路54。
现在参考图3A和图3B,绘示了第一可植入端口实施方式24a。图3A是端口的俯视图,其中在植入后,顶部表面典型地“向前”朝向患者的皮肤取向。环形电极80附接到可植入端口24a的外圆周并且可以可选地充当ECG电极。金属网82的圆周带可以定位在端口的上表面的外周上方,典型地定位在针可穿透的隔膜84上方。第二个较小的内环电极86也可以设置在隔膜的上表面上。外网状电极82通过非导电隔膜材料与内电极86电绝缘。因此,第一金属套管和第二金属套管可以通过内电极和外电极引入,以提供用于双导线EKG信号检测的单独连接。ECG电极本身可以位于端口44a的主体上或可植入系统中的其他地方。将在ECG电极和网状电极82和86之间提供内部导电线路。
现在参考图4A和图4B,绘示了替代的可植入端口24b,其具有形成在针可穿透隔膜92的上表面上的第一弓形网状电极90a和第二弓形网状电极90b。如图4B中所示,第一电极94a可以定位在端口主体的外周上,其中内部连接到两个弓形网状电极中的一个。第二电极(图4B中未示出)位于端口主体的相对面上,并且可以连接到弓形网状电极的另一个,以便为ECG电极中的每个提供单独的套管连接。
图5A和图5B绘示了又一可植入端口组件95。端口组件95包含第一端口24b,所述第一端口24b可以与前面参考图4A和图4B描述的相同。第二端口24c可以具有覆盖下面的针可穿透隔膜的整个表面的单个网状电极。网状电极96可以连接到任何ECG电极,典型地连接到端口主体的导电部分。端口24b和24c通过导管部分18a和18b连接在一起,通过y形连接器100到公共导管主体18,所述公共导管主体18可以连接到气动执行器,如前面参考图1所描述的。
图6绘示了套管14如何与网状电极的丝线形成电连接。特别地,网状电极包括正交布置的导线102a和102b。在丝线102a和102b交叉的地方形成小的方形单元。选择单元的尺寸使得它们小于套管的直径,使得当插入穿过丝网时,套管14的壁将必然接触限定单个单元的全部四根丝线。这样,就保证了良好的电接触。
现在参考图7A,当套管通过可植入端口的隔膜,特别是通过此类隔膜上的丝网电极结构插入时,套管可以被修改以增强保持力。特别地,如图7A中所示,针结构106可以具有一系列球形物108,所述一系列球形物108有助于针防止从网意外抽取。类似地,如图7B中所示,针110可以具有一系列阻止针拔出的倒钩112。
现在参考图8A、图8B和图9,将描述用于将ECG信息从可植入端口输送到外部驱动单元的光学系统。如图8A中所示,针组件120包括针122,所述针122具有轴向嵌入护套128中的多根光纤126。如图8B中所示,光纤126暴露在护套128的远侧表面中。如图9中所示,可植入端口130可以被修改为以将光学信息传输到光纤126的方式接收针组件120。特别地,针组件120可以插入穿过端口的隔膜132。护套128的外表面接合嵌入隔膜132中的壁龛的丝线。护套128的远侧表面接合电路板140的上表面。电路板140包括多个光学发射器(未示出),所述多个光学发射器被配置为将光输送到针组件120的光纤126。针122将穿过电路板中的孔或孔口142,以准许护套的表面接合电路板。提供漏斗144来辅助针与孔正确对准。端口130外部的ECG电极146a和146b连接到电路板140。电路板上的电路从电极抽取ECG信息,将所述信息转换成光能,所述光能由光学发射器输送到光纤126。光通过光纤传输到外部驱动单元,在那里光被转换回适用于控制系统的电子信息,如前所描述的。
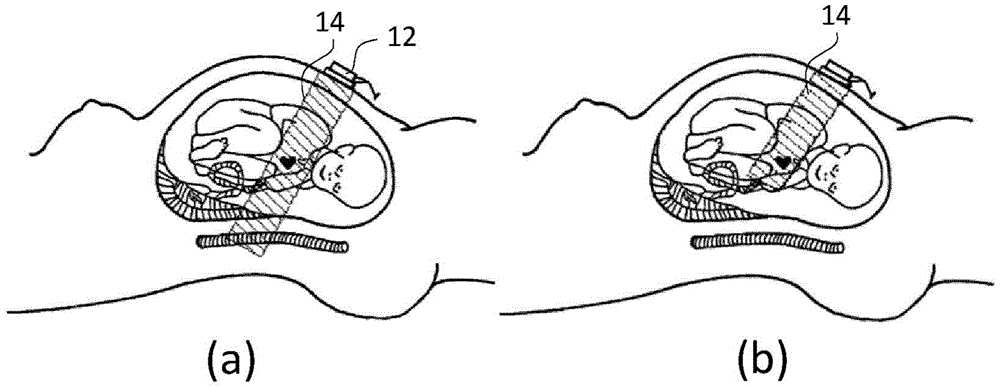
现在参考图10,如所绘示,图1的心脏辅助系统10可以植入患者。特别地,球囊或其他气动执行器20被引入心包P的内表面和心肌M的外表面之间的心包囊中。气动执行器20将优选地大体上位于左心室上方,使得执行器的充气或其他致动压缩左心室,如图10中的虚线所示。端口24通过导管主体18连接到球囊,并且通过套管14经皮进入。外部驱动单元48通过连接管46和套管14将致动气体输送到端口24以便致动(典型地通过给球囊充气和放气)气动执行器。ECG由ECG垫56测量,所述ECG垫56通过电缆58连接到外部驱动单元。可选地,可由可植入端口24上的电极或系统中的其他地方测量其他ECG信号。
现在参考图11,将描述用于操作本发明的气动执行器的示例性协议。使用前面描述的任何ECG电极测量患者的ECG。ECG测量电路典型地集成到外部驱动单元中,并且按照众所周知的ECG测量原理操作。原始ECG原理将经历处理,典型地是用于从信号移除移动伪影的数字处理,然后扫描处理后的信号以来确定(典型地是通过测量R峰值)与患者的心律相关联的信号伪影的出现。
尽管R峰值可以用于直接驱动泵组件和气动执行器,但典型地会对R峰值模式进行评估,以确定它是正常或者异常。例如,可以比较连续单个峰值R值的出现,以确定它们的长度是增加还是减少。如果R-R峰值间隔在前一个间隔的±10%内保持恒定,则心律将被视为正常,并且可能会生成触发。通常,第二次异常测试将在累积的跳动数(例如10次跳动)上应用于R-R间隔。如果R-R间期大于前10次心跳的平均R-R间期的阈值量(例如10%),则认为心律异常。
在检测到异常心律的情况下,系统可以采取多种措施中的任一种。例如,系统可以关闭气动执行器的触发,直到患者的自然心律恢复正常。替代地,在快速心跳的情况下,自然心律和气动执行器的触发之间的1∶1同步可以被改变,例如执行器可在每第二个自然跳动(2∶1的比率)、每第三次跳动(3∶1的比率)等被触发。一旦心律恢复正常,就可以以1:1的比例重新致动气动执行器。
尽管上面已经详细描述了本发明的特定实施方式,但是应理解,所描述的描述仅是为了说明的目的,并且本发明的上述描述不是穷尽的。本发明的特定特征在一些附图中示出,而在其他附图中未示出,这仅是为了方便,根据本发明,任何特征都可以与另一个特征组合。对于本领域的普通技术人员来说,许多变化和替换是容易理解的。此类替代和变化意图包含在权利要求的范围内。从属权利要求中呈现的特定特征可以被组合并且落入本发明的范围内。本发明还涵盖实施方式,就好像从属权利要求是参考其他独立权利要求以多从属权利要求格式替代编写的一样。
除非本文中另有说明或与上下文明显矛盾,否则在描述本发明的上下文中(特别是所附权利要求的上下文中),术语“一”和“一个”和“所述”以及类似的指代物的使用应被解释为涵盖单数和复数两者。除非另有说明,否则术语“包括”、“具有”、“包含”和“含有”应被解释为开放式术语(即,意思是“包含但不限于”)。术语“附接”应被解释为部分或全部含有在内、附接在一起或接合在一起,即使有一些东西介入。除非本文中另有说明,否则本文中数值范围的叙述仅意图用作单独提及落入所述范围内的每个单独数值的简写方法,并且每个单独数值被并入说明书中,就好像其在本文中被单独叙述一样。除非本文另有说明或与上下文明显矛盾,否则本文所描述的全部方法都可以任何合适的顺序执行。除非另有声明,否则本文提供的任何和全部示例或示例性语言(例如,“诸如”)的使用仅意图更好地阐明本发明的实施方式,而不是对本发明的范围构成限制。说明书中的任何语言都不应被解释为指示任何未要求保护的元素对于本发明的实践是必要的。
本文引用的全部参考文献,包含出版物、专利申请和专利,本文引入作为参考,其引用程度如同每个参考文献都被单独且具体地指出引入作为参考,并且本文完整阐述。
本文用于企业家、创业者技术爱好者查询,结果仅供参考。