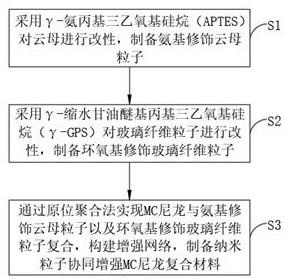
1.本发明属于ldlr基因研究领域,尤其涉及高胆固醇血症相关的新突变基 因及其应用。
背景技术:
2.家族性高胆固醇血症(fh)是最常见的代谢遗传性疾病之一,其特征在于 极高的总胆固醇(tc)和低密度脂蛋白胆固醇(ldl
‑
c)水平,过量胆固醇在 组织中沉淀,导致黄色素瘤,动脉粥样硬化进程的加速和早发性冠状动脉疾 病风险增加。以ldl
‑
c或tc增加为特征的血脂异常是动脉粥样硬化性心血管 疾病的重要危险因素。因此,降低ldl
‑
c水平是防控动脉粥样硬化性心血管 病的首要干预靶点,发现并精准调控ldl
‑
c水平的新型药物对维护人类健康 具有重大意义。如果没有适当的预防工作,大约85%的男性fh患者和50% 的女性fh患者65岁之前发生冠状动脉疾病,而纯合子家族性高胆固醇血症 患者通常在30岁之前死亡。对<50岁的心肌梗死患者的筛查显示,约2%的 患者具有家族性高胆固醇血症。因此,早期cvd(尤其是早期心肌梗死),中 风和总死亡率风险增加是未经治疗的家族性高胆固醇血症的主要特征。年龄 增加,体重指数升高,2型糖尿病,高血压和吸烟史可以增加杂合子家族性高 胆固醇血症患者的心血管疾病风险。
3.目前有三种基因突变被认为是其主要致病突变,(1)低密度脂蛋白受体 基因(ldlr)的突变,导致ldlr分子数量的减少或者ldlr活性的降低,从 而ldl
‑
c的清除减少;(2)载脂蛋白b基因(apob)的突变,ldl上有缺陷 的apob100不能与ldlr结合;(3)前蛋白转化酶枯草杆菌蛋白酶kexin 9 基因(pcsk9)的突变,导致ldlr的快速内化和降解。极少数情况下,参与 脂蛋白代谢的其他基因突变apoe(编码载脂蛋白e)和stap1(编码信号转导 衔接蛋白1)也可导致家族性高胆固醇血症。目前与fh的相关致病位点仍有 待进一步研究。由此,任何一个或一组家族性高胆固醇血症的相关基因的发 现与提出都将是对本领域的重要技术贡献。
技术实现要素:
4.针对上述问题,本发明提供ldlr基因突变体及其应用,主要发现一种新 的ldlr基因突变体,并填补了家族性高胆固醇血症的基因方面的漏缺,发现 了一些新的突变型基因,并为后续疾病的治疗和筛查提供了新的方案。
5.为了解决上述问题,本发明采用如下技术方案:
6.核酸,包括含下列目标片段,
7.所述目标片段与野生型ldlr基因片段相比,所述目标片段具有c.1879g>a 突变。
8.多肽,与野生型ldlr相比,所述多肽具有p.a627t突变。
9.基因突变,与野生型ldlr基因相比,所述基因突变具有c.1879g>a突变。
10.生物模型在制备高胆固醇血症筛选制剂中应用,所述生物模型至少携带 下列之一:
11.a.前述的核酸;
12.b.前述的多肽;
13.c.前述的基因突变。
14.筛选高胆固醇血症生物样品的试剂盒,包含有
15.能检测ldlr基因突变体的试剂,与野生型ldlr基因相比,所述ldlr基 因突变体至少为下述中之一
16.a.前述的核酸;
17.b.前述的多肽;
18.c.前述的基因突变。
19.一些方式中,试剂盒中所述试剂为核酸探针或引物;
20.优选的,所述引物的核苷酸序列包括:
21.序列为tcatcccagtgtttaacgg的正向引物,
22.序列为gtcagggcaggaacgaga的反向引物。
23.构建体,包含有的核酸或的基因突变。
24.抑制剂在制备防治高胆固醇血症药物中的应用,所述抑制剂至少对下述 中任一具有抑制作用:
25.a.ldlr基因的c.1879g>a突变,
26.b.ldlr基因的p.a627t突变。
27.基因片段在制备防治高胆固醇血症药物中的应用,所述基因片段为ldlr 的c.1879位点单核苷酸为g的基因片段。
28.防治高胆固醇血症药物,至少含有下述之一
29.a.ldlr基因的c.1879g>a突变抑制剂,
30.b.ldlr基因的p.a627t突变抑制剂,
31.c.基因片段,所述基因片段为ldlr基因的c.1879位点单核苷酸为g的 基因片段,
32.d.基因载体,所述基因载体含有能将ldlr基因的c.1879位点单核苷酸 a替换为单核苷酸g并表达的基因片段。
33.本发明的有益效果是:
34.(1)发现了ldlr基因的新的突变位点c.1879g>a,对该突变位点的检测 可以用于高胆固醇血症患者的辅助诊断;对高胆固醇血症的诊断治疗具有十 分重要的意义;
35.(2)ldlr突变位点c.1879g>a较为罕见,在诊断试剂盒中收录本发明中的 突变位点,进一步丰富高胆固醇血症诊断试剂盒的诊断位点;
36.(3)在不违背法律等相关规定前提下,通过基因基因工程手段,对突变 位点进行修复,也可实现防治相关疾病;
37.(4)能够以检测人基因组中c.1879g>a位点基因型作为筛查、鉴定高胆 固醇血症的手段;或者将检测人基因组中c.1879g>a突变或基因型的物质用 于制备筛查高胆固醇血症患者产品、检测高胆固醇血症产品、检测、鉴定或 辅助鉴定与高胆固醇血症相关的单核苷酸多态性的产品。其中,上述检测人 基因组中c.1879g>a突变或基因型的物质,包括但不限于扩增包含c.1879g>a 位点在内的基因组dna片段的pcr引物对和成套探针。
附图说明
38.图1为一个高胆固醇血症患者家系图谱;
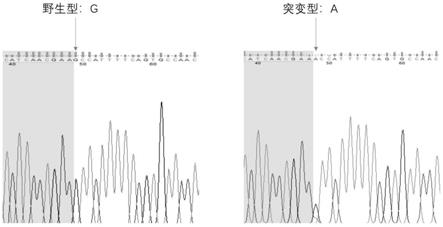
39.图2为高胆固醇血症患者先证者和正常人ldlr基因c.1879g>a突变的 sanger测序验证峰对比图;
40.图3为正常人群中c.1879g>a突变筛查。
具体实施方式
41.下面对本发明做进一步说明:
42.本部分第一方面公开如下技术内容:
43.核酸,包括含下列目标片段,
44.所述目标片段与野生型ldlr基因相比(一种参考序列为seq no:1), 所述核酸具有c.1879g>a突变。另一些现有或后续发现的ldlr基因,只要存 在c.1879g>a突变,并且具有与本发明相同、相近效果的突变体都应当落入 本发明保护范围。并不局限于除c.1879g>a突变外其他序列必须与seq no: 1一致。所述核酸为dna。
45.多肽,与野生型ldlr相比(一种为seq no:2)所述多肽具有p.a627t 突变。同前,并不局限于除p.a627t突变外其他序列必须与seq no:2一致。
46.基因突变,与野生型ldlr基因相比,所述基因突变具有c.1879g>a突变。
47.生物模型在制备筛选制剂中应用,所述生物模型至少携带下列之一:
48.a.前述核酸;
49.b.前述多肽;
50.c.前述基因突变。
51.所述筛选制剂为筛选家族性高胆固醇血症的制剂。
52.筛选家族性高胆固醇血症生物样品的试剂盒,包含有
53.能检测ldlr基因突变体的试剂,与野生型ldlr基因相比,所述ldlr基 因突变体具有c.1879g>a突变。
54.一种实质方式中,所述ldlr基因突变体至少为下述中之一:
55.a.前述核酸;
56.b.前述多肽;
57.c.前述基因突变。
58.所述试剂为核酸探针或引物;一种实施方式中,
59.所述引物的核苷酸序列包括:
60.序列为tcatcccagtgtttaacgg的正向引物
61.序列为gtcagggcaggaacgaga的反向引物。
62.构建体,包含有前述核酸或前述基因突变。
63.重组细胞,所述重组细胞是通过前述构建体转化受体细胞或表达前述多 肽而得。
64.用于制备防治高胆固醇血症药物的重组蛋白,由前述重组细胞表达。
65.抑制剂在制备防治高胆固醇血症药物中的应用,所述抑制剂至少对下述 中任一具有抑制作用:
66.a.ldlr基因的c.1879g>a突变,
67.b.ldlr基因多肽的p.a627t突变。
68.防治高胆固醇血症药物,至少含有下述之一
69.a.ldlr基因的c.1879g>a突变抑制剂,
70.b.ldlr基因多肽的p.a627t突变抑制剂。
71.基因片段在制备防治高胆固醇血症药物中的应用,所述基因片段为ldlr 的c.1879位点单核苷酸为g的基因片段。
72.防治高胆固醇血症药物,至少含有下述之一
73.a.ldlr基因的c.1879g>a突变抑制剂,
74.b.ldlr基因的p.a627t突变抑制剂,
75.c.基因片段,所述基因片段为ldlr的13号外显子c.1879位点单核苷酸 为g的基因片段,
76.d.基因载体,所述基因载体含有能将ldlr基因的13号外显子c.1879位 点单核苷酸a替换为单核苷酸g并表达的基因片段。
77.本部分第二方面介绍部分质粒、药物中间物的制备方法:
78.用于制备防治高胆固醇血症药物的质粒的制备方法,包括下述步骤:
79.(a)以野生型ldlr基因为模版,扩增得突变ldlr cdna片段;
80.(b)酶切dna双链中腺嘌呤n6位甲基化的gatc序列,纯化突变ldlr cdna 片段;
81.(c)突变ldlr cdna片段与表达载体用hindiii酶和kpn1酶进行双酶切、 t4 dna连接酶酶连得表达质粒;
82.(d)将酶连反应所得体系加入大肠杆菌受态细胞中,得质粒菌液;
83.(e)从质粒菌液中提取质粒。
84.上述步骤更具体的说明:
85.步骤(a)中,以野生型ldlr基因为模版,定点突变上游引物f
‑
mut: 5
’‑
tcatcccagtgtttaacgg
‑3’
,下游引物r
‑
mut:5
’‑
gtcagggcaggaacgaga
‑3’ꢀ
以及dna聚合酶primer star通过聚合酶链式反应扩增得到突变ldlr cdna 片段;和/或
86.步骤(b)中,以dpni酶酶切dna双链中腺嘌呤n6位甲基化的gatc序 列,去除模板质粒留下pcr突变产物,使突变ldlr cdna片段得到初步纯化; 和/或
87.步骤(c)中,表达载体为pcmv
‑
3xflag和pegfp
‑
c1,表达质粒为 pcmv
‑
3xflag
‑
ldlr
‑
mut和pegfp
‑
c1
‑
ldlr
‑
mut;和/或
88.步骤(e)中,通过单克隆抗体鉴定和/或测序确定正确的质粒菌液;和/ 或
89.步骤(e)中,通过使用endo
‑
free plasmid dna mini kit ii进行质粒 的抽提。
90.抑制剂在防治家族性高胆固醇血症药物中的应用,所述抑制剂至少对下 述中任一具有抑制作用:
91.a.ldlr基因的c.1879g>a突变,
92.b.ldlr基因多肽的p.a627t突变。
93.基因片段在制备防治高胆固醇血症药物中的应用,所述基因片段为ldlr 的c.1879位点单核苷酸为g的基因片段。
94.防治高胆固醇血症药物,至少含有下述之一
95.a.ldlr基因的c.1879g>a突变抑制剂,
96.b.ldlr基因的p.a627t突变抑制剂,
97.c.基因片段,所述基因片段为ldlr的c.1879位点单核苷酸为g的基因 片段,
98.d.基因载体,所述基因载体含有能将ttn基因的c.1879位点单核苷酸a 替换为单核苷酸g并表达的基因片段
99.用于制备防治高胆固醇血症药物的质粒的一种具体构建步骤如下:
100.野生型ldlr基因的cdna(ccds12254、nm_000527.4)表达质粒购维真生 物科技有限公司。
101.(1)以野生型ldlr cdna为模板,带有hindiii酶切位点的上游引物 ldlr
‑
hindiii
‑
f:tcatcccagtgtttaacgg和带有kpn1酶切位点的下游引物 gtcagggcaggaacgaga;
102.以及高保真dna聚合酶primer star通过聚合酶链式反应(pcr)扩增得 到带有酶切位点的野生型ldlr cdna片段。
103.(2)以上一步中的野生型ldlr cdna为模板,定点突变上游引物 tcatcccagtgtttaacgg,下游引物gtcagggcaggaacgaga以及高保真dna聚合酶 primer star通过聚合酶链式反应(pcr)扩增得到突变ldlr cdna片段。具 体反应体系及扩增步骤如下:
104.反应体系:
[0105][0106]
扩增程序:
[0107][0108]
(3)dpni酶消化突变pcr产物
[0109]
dpni识别并酶切dna双链中腺嘌呤n6位甲基化(n6
‑
methyladenine)的 gatc序列。从大肠杆菌提取的质粒会被甲基化,而pcr产物没有甲基化,所 以dpni酶能够特异型切割模板质粒而不会影响pcr产物,从而去掉模板质粒 留下pcr突变产物。
[0110]
dpni酶消化消化体系及步骤:
[0111][0112]
buffer和水等充分混匀后再加入dpni酶,加入dpni酶后可以用枪吹打 或轻轻涡
旋混匀,37℃孵育1小时或更长时间。
[0113]
(4)目的片段与载体的酶切:将片段与表达载体用hindiii酶和kpn1 酶进行双酶切。
[0114]
目的片段(野生型ldlr cdna和突变ldlr cdna)酶切体系:
[0115][0116]
表达载体(pcmv
‑
3xflag和pegfp
‑
c1)酶切体系:
[0117][0118]
37℃酶切反应6
‑
8小时,分别纯化回收片段跟载体。
[0119]
(5)目的片段与载体酶连
[0120]
双酶切后的片段与载体经过纯化回收后测浓度,按照目的片段(mol): 载体(mol)=3:1,使用t4 dna连接酶4℃酶连过夜。
[0121]
野生型ldlr cdna片段和突变ldlr cdna片段分别与表达载体 pcmv
‑
3xflag酶连,得到表达质粒pcmv
‑
3xflag
‑
ldlr
‑
wt和pcmv
‑
3xflag
‑
ldlr
‑
mut。
[0122]
野生型ldlr cdna片段和突变ldlr cdna片段分别与表达载体 pegfp
‑
c1酶连,得到表达质粒pegfp
‑
c1
‑
ldlr
‑
wt和pegfp
‑
c1
‑
ldlr
‑
mut。
[0123]
具体体系如下:
[0124][0125]
注意设置体系中只有载体,没有目的片段的阴性对照。
[0126]
(6)转化:将酶连反应完成的10l体系和阴性对照体系分别加进100l dh5α大肠杆菌感受态细胞中,冰上放置30分钟,42℃热击90秒,立即放于 冰上再静置3分钟,接着加入500l无抗生素的lb培养基,置于37℃振荡 摇床100转/分钟,复苏活化2小时后,3000
×
rpm,离心5分钟,留取100ul 上清将菌体轻轻悬起,涂布于含有对应抗性的lb固体培养平板上,于37℃培 养箱培养12
‑
16小时。
[0127]
(7)单克隆的鉴定:观察酶连转化与阴性对照转化的平板,正常情况下, 阴性的平
板基本不长克隆或克隆很少。挑取数个单克隆于3ml对应抗性的lb液体培养基中,37℃振荡摇床200转/分钟,培养12小时,先取200ul菌液20%甘油保种,剩余的菌液使用质粒小提试剂盒抽提质粒进行双酶切检测验证。
[0128]
(8)测序:上一步双酶切检测的质粒,如果经过琼脂糖凝胶检测有目的片段和载体片段两条条带,则挑选1
‑
2管质粒进行测序。
[0129]
测序正确的质粒的菌液接种于15ml还有对应抗性的lb液体培养基中,使用endo
‑
freeplasmiddnaminikitii进行质粒的抽提,琼脂糖凝胶检测,测浓度,保存于
‑
20℃。
[0130]
(9)高纯度质粒抽提
[0131]
取测序正确的质粒菌液到含有20ml相应抗生素的lb培养基的50ml离心管中,37℃振捣摇床200转/分钟培养12
‑
16小时。低速离心机3600转,离心20分钟,弃上清,管子倒扣在干净的纸张上5分钟,菌体沉淀在管底待用。使用omega的endo
‑
freeplasmiddnaminikitii试剂盒,提取高质量去内毒素质粒,步骤如下
[0132]
1.在吸附柱中加入500μl平衡缓冲液,放置5分钟,12000g离心2分钟,弃收集管中液体;
[0133]
2.在上述菌体沉淀中加入500μlsolutioni(使用前加入rnasea)溶液,用移液器吹打或者涡旋,将沉淀完全吹散,直至无菌体结块;
[0134]
3.将重悬好的菌液转移到2mlep管中,加入500μlsolutionii,立即轻轻上下颠倒混匀6
‑
8次,菌体完全裂解,菌液变得澄清,放置5分钟;
[0135]
4.立即加入250μl冰浴的n3buffer,轻轻上下颠倒6
‑
8次,直至完全混匀,有白色絮状沉淀产生。12000g转离心15分钟;
[0136]
5.小心吸取上清转移至新的1.5mlep管中,加入0.1倍体积的冰浴etrsolution,上下颠倒混匀,溶液变浑浊。冰上放置10分钟,期间颠倒混匀数次,溶液又变清亮;
[0137]
6.42℃金属恒温器孵育5分钟,溶液变浑浊,12000xg离心5分钟,蓝色etr于管底部;
[0138]
7.小心吸取上清转移至2mlep管中,加入0.5倍体积的无水乙醇,上下颠倒混匀,室温静置5分钟;
[0139]
8.移液器吸取700ul(步骤7)中的溶液到平衡处理过的吸附柱中,放置5分钟,12000
×
g离心2分钟,弃掉收集管中的液体;
[0140]
9.重复步骤8至步骤7中的液体全部经过吸附柱;
[0141]
10.加入500μlhbcbuffer到吸附柱中,室温静置2分钟,12000
×
g离心1分钟,弃掉收集管中的液体;
[0142]
11.加入600μldnawashbuffer到吸附柱中,室温静置2分钟,12000
×
g离心1分钟,弃废液。重复洗涤一次;
[0143]
12.吸附柱空转12000
×
g离心2分钟,完全去除洗涤缓冲液;
[0144]
13.将吸附柱放在新的收集管中,室温静置待无水乙醇挥发;
[0145]
14.小心在吸附柱膜上加入80μl洗脱缓冲液或者超纯水,室温静置10分钟,12000
×
g离心2分钟,即得到质粒溶液;
[0146]
15.利用nanodrop2000c超微量紫外
‑
可见分光光度计测定质粒浓度,保存于
‑
20
℃备用。
[0147]
由于ldlr对于胆同醇代谢至关重要,以致该基因任何部位出现突变均 可致病。以ldlr蛋白合成与功能为基础突变可划分为5型:l型突变为不表 达等位基因,包括启动子序列突变、无义突变、移码突变、剪接突变,这类 突变导致细胞不表达ldlr;2型突变为转运缺陷型等位基因,主要发生在配 体结合域和表皮生长因子前体结构域,虽然能合成受体,但从内质网向高尔 基体的转运障碍,堆积在内质网中最终被降解;3型突变为结合缺陷型等位基 因,本型较常见,特点为突变基因编码的异常受体蛋白可以到达细胞表面, 但丧失了结合ldl的功能,这类突变同样发生在配体结合域和表皮生长因子 前体结构域;4型突变为内移缺陷型等位基因,本型罕见,发生在胞浆区域或 是跨膜域,由于编码npvy序列的密码子发生突变而致,特点为受体能与ldl 结合,但不能将其转运至细胞表面并聚集于被覆陷窝;5型突变为再循环缺陷 型等位基因,受体能够结合ldl,也能内移进人细胞,但在溶酶体内不能与 ldl分离,受体与配体被同时降解,导致ldlr不能够再循环到细胞表面,这 类突变多发生在表皮生长因子前体结构域。
[0148]
需要说明的是,上述给出的突变位点以及序列等,均是以proteon测序 平台内容作为参考,本领域技术人员应该理解的是,由于数据库的更新或者 数据库的不同,所示出的突变位点以及序列可能会稍有不同或者变化,这些 不同或者变化均可以给出的该数据库中的内容为标准找到,这些不同或者变 化也均包含在本发明的保护范围之内。
[0149]
由此,根据本发明实施例的构建体转化受体细胞获得的重组细胞,能够 有效地用作家族性高胆固醇血症,尤其是杂合子型家族性高胆固醇血症的相 关研究的模型。其中,所述受体细胞的种类不受特别限制。
[0150]
在本发明中所使用的术语“构建体”是指这样的一种遗传载体,其包含 特定核酸序列,并且能够将目的核酸序列转入宿主细胞中,以获得重组细胞。 根据本发明的实施例,构建体的形式不受特别限制。根据本发明的实施例, 其可以为质粒、噬菌体、人工染色体、粘粒(cosmid)、病毒的至少一种,优 选质粒。质粒作为遗传载体,具有操作简单,可以携带较大片段的性质,便 于操作和处理。质粒的形式也不受特别限制,既可以是环形质粒,也可以是 线性质粒,即可以是单链的,也可以是双链的。本领域技术人员可以根据需 要进行选择。在本发明中所使用的术语“核酸”可以是任何包含脱氧核糖核 苷酸或者核糖核苷酸的聚合物,包括但不限于经过修饰的或者未经修饰的 dna、rna,其长度不受任何特别限制。对于用于构建重组细胞的构建体,优 选所述核酸为dna,因为dna相对于rna而言,其更稳定,并且易于操作。
[0151]
本部分第三方面结合一些研究实例进行说明:
[0152]
一.样本收集
[0153]
发明人在武汉收集到1个高胆固醇血症的家系,如图1所示,
[0154]
共采集该家系成员共3人,其中患者1人,正常人员2人。
[0155]
□
表示正常男性,
■
表示患病男性,
○
表示正常女性,
●
表示患病女性,
ꢀ↗
表示先证者。参与本发明研究的共3人,所有参与本发明研究的家系成员 均签署了知情同意书。发明人采集获得上述高胆固醇血症患者家系中患者及 家系内正常人的外周血样本。
[0156]
dna提取:应用tianamp血液基因组dna提取试剂盒抽提人外周血白细胞 的dna,利用nanodrop2000分光光度计和和琼脂糖凝胶电泳检测对上述提取 的dna样本进行浓度及
纯度测定。所得的每个标本基因组dna od260/od280 均位于1.8
‑
2.0之间,浓度不少于80ng/ml。
[0157]
二.全外显子测序
[0158]
发明人用proteon测序平台,对高胆固醇血症家系中的先证者进行全外 显子组测序。
[0159]
三.变异检测、注释及数据库比较
[0160]
对测序公司提供的变异检测、注释结果,对非同义突变、编码区插入和 缺失这两类最有可能与病理相关的突变进行研究。结果在这些样本中发现, 先证者有82570个snv突变,15209个indel突变,79个cnv。根据公共数据 库dbsnp数据库、hapmap数据库、千人基因组数据库的过滤,去掉所有已知 的且在数据库中等位基因频率大于0.01的变异。筛选常见的导致家族性高胆 固醇血症的基因ldlr,pcsk9,apob上的突变。由此,发明人发现先证者在 ldlr基因13号外显子上存在一个图2所示的杂合突变,错义突变c.1879g>a, p.a627t:gcc>acc(p.ala627thr)。
[0161]
该突变类型为杂合突变,错义突变,突变频率为0.000004属于罕见变异, 并且在中国人群中没有报道。
[0162]
四.sanger法测序验证
[0163]
1.引物设计
[0164]
应用genetool软件设计突变位点扩增引物:
[0165]
正向引物:5'
‑
tcatcccagtgtttaacgg
‑
3'
[0166]
反向引物:5'
‑
gtcagggcaggaacgaga
‑
3'。
[0167]
2.dna扩增(pcr)
[0168]
pcr反应体系共25ul:1ul样本dna、正反向引物各0.5ul、12.5ul 2
×ꢀ
tsingke master mix和10.5ul ddh2o。
[0169]
pcr扩增程序:样本上机,94℃预热3分钟,循环“94℃变性30s,59℃ 梯度温度退火30s,72℃延伸35s”35次,72℃保持10分钟后,终点温度4℃。
[0170]
pcr产物检测
[0171]
琼脂糖凝胶电泳检测pcr产物。
[0172]
3.测序
[0173]
pcr成功后,进行sanger测序,测序使用abi3730xl型测序仪进行正反 向测序。
[0174]
测序结果分析
[0175]
finch tv version 1.4.0用于读取sanger测序结果。
[0176]
先证者携带ldlr基因突变,该突变位于13号外显子,c.1879g>a,p.a627t: gcc>acc(p.ala627thr),导致第627位的丙氨酸变成了苏氨酸。
[0177]
该突变类型为杂合突变,错义突变,突变频率为0.000004属于罕见变异, 并且在中国人群中没有报道。经有害性预测为:致病性(sift,polyphen2, lrt,mutationtaster,fathmm),改突变区域为保守性。文献检索未发现 本发明发现的突变与家族性高胆固醇血症的关系。
[0178]
五.生物信息学预测
[0179]
(1)突变有害性分析
[0180]
根据有害性预测软件sift、polyphen2_hvar_pred、mutationtaster_pred 分析,发现该位点突变是突变有害性,突变后会致病。经有害性预测为:致 病性(sift,polyphen2,lrt,mutationtaster,fathmm),改突变区域为 保守性。
[0181][0182]
(2)保守性分析
[0183]
该位点位于ldlr蛋白的第627个氨基酸位置,该位点是具有保守性的, 如果位点突变后会导致蛋白功能异常。
[0184]
(3)功能预测
[0185]
该突变exon13:c.1879g>a,p.a627t:gcc>acc(p.ala627thr),导致第 627位的丙氨酸变成了苏氨酸,不能出现正常的终止密码,影响其正常翻译出 ldlr蛋白,进而影响血脂。
[0186]
该位点位于的区域是ldlr蛋白的表皮生长因子前体结构域,此区域负责 调控ldlr的转运与结合,如果其区域发生变化,ldlr的内吞和细胞内转运将 会发生异常,导致血脂升高。
[0187]
六.临床分析
[0188]
(1)acmg标准评级
[0189]
根据acmg遗传变异分类标准与指南该位点可以评为致病性。
[0190]
(2)用药情况
[0191]
先证者最高ldl
‑
c:8.05mmol/l,服用每日剂量阿托伐他汀后先证者的 ldl
‑
c由最高8.05降至5.36mmol/l,后续继续他汀加依泽麦布,和周两周注 射pcsk9抑制剂治疗后ldl
‑
c水平保持在1.2mmol/l,治疗效果较好。pcsk9 抑制剂,能结合pcsk9并抑制循环型pcsk9与低密度脂蛋白受体(ldlr)的 结合,从而阻止pcsk9介导的低密度脂蛋白受体降解,进而控制血脂,该药用 于治疗成人杂合子型家族性高胆甾醇血症,对于纯合型家族性高胆甾醇血症 患者无效。本家系应用pcsk9抑制剂后显著的降低了血脂,说明先证者还保 留了部分ldlr的功能,证实了先证者是杂合突变。
[0192]
(3)健康人群中c.1879g>a突变筛查
[0193]
使用taqman探针法对健康人群进行c.1879g>a突变筛查。
[0194]
taqman探针法进行基因分型实验的具体操作如下:
[0195]
基因组dna样本2ml、2
×
taqman gt master mix 4ml、40
×
taqman snp 探针0.2ul、去离子水1.8ul混合均匀(10ul反应体系)。每孔一人反应体系, 分别加入96孔pcr板,在abi 7300实时荧光定量pcr仪进行反应。95℃变 性30秒,60℃退火1分钟,重复35个循环。反应结束后,使用7500system sdssoftware进行基因型分型,确定以上样本是否属于携带突变。
[0196]
核酸探针为taqman探针,其核酸序列如下所示:
[0197]
正向探针序列:tcatcccagtgtttaacgg,
[0198]
反向探针序列:gtcagggcaggaacgaga。
[0199]
结果显示200例人群中基因型都是cc,未携带突变。
[0200]
基于以上的证据我们发现ldlr基因上一个新的位点突变c.1879g>a会导 致家族性高胆固醇血症。该位点可以用于家族性高胆固醇血症的基因筛查治 疗。
[0201]
本领域的技术人员可以明确,在不脱离本发明的总体精神以及构思的情 形下,可以做出对于以上实施例的各种变型。其均落入本发明的保护范围之 内。本发明的保护方案以本发明所附的权利要求书为准。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。