背景技术
心脏传导系统包含窦房(SA)结、房室(AV)结、希氏束(the bundle of His)、束支和浦肯野纤维(Purkinje fiber)。心跳在SA结中启动,所述SA结充当心脏的自然“起搏器”。由SA结引起的电脉冲使心房心肌收缩。信号通过AV结传导到心室,所述AV结固有地延迟所述传导,以允许心房在心室开始收缩之前停止收缩,从而提供恰当的AV同步性。电脉冲通过希氏束、束支和浦肯野纤维从AV结传导到心室心肌。
患有传导系统异常,例如,AV结传导不良或SA结功能不良的患者可以接受起搏器以恢复更正常的心律和房室同步性。双腔起搏器是可用的,所述双腔起搏器包含承载放置在右心房中的电极的经静脉心房引线和承载经由右心房放置在右心室中的电极的经静脉心室引线。起搏器本身通常植入皮下袋中,其中经静脉引线隧穿到皮下袋。双腔起搏器感测心房电信号和心室电信号,并且可以视需要提供心房起搏和心室起搏,以促进正常心率和右心房腔和右心室腔的电去极化的同步。
心力衰竭患者可能经历心室不同步。多腔起搏器可以通过对心房和/或一个或两个心室进行起搏以改善患有心力衰竭或导致心室腔协调不良的其它异常的患者的心室同步性来递送心脏再同步疗法(CRT)。经静脉引线可以定位在右心房、右心室和左心室的心静脉中,以在至多所有三个心腔中提供感测和起搏。
心脏内起搏器已被引入或被提议用于完全植入患者心脏内,从而消除了对可能成为感染或其它并发症来源的经静脉引线的需求。心脏内起搏器可以在患者心脏的单个腔室内提供感测和起搏。在一些患者中,单腔起搏和感测可以充分满足患者的需求。然而,单腔起搏和感测可能无法完全解决所有患者的心脏传导疾病或异常。可能需要双腔感测和/或起搏功能来恢复更正常的心律。
技术实现要素:
总体而言,本公开涉及一种用于从由运动传感器感测的运动信号中确定同步性量度的医疗装置和方法。所述运动信号包含心脏事件信号。所述医疗装置可以是起搏器,所述起搏器基于所述同步性量度调整起搏间期以改善心腔的机械同步性。所述起搏间期可以是心房事件和心室起搏脉冲之间的AV起搏间期,其在本文中也被称为“AV间期”,以促进所述心腔的最优机械同步性。在其它实例中,所述起搏间期可以是用于改善心室同步性的心室间间期,其在本文中也被称为“V1-V2间期”。所述起搏器可以是无引线起搏器,在一些实例中,所述无引线起搏器可以完全植入右心房中,其能够从心脏电信号或从所述运动信号中感测心房事件和/或能够递送心房起搏脉冲。所述起搏器可以被配置成以所述AV间期将心室起搏脉冲递送到心室组织,所述心室组织与所述心房事件同步。在其它实例中,所述起搏器可以完全植入第一心室腔,并且可以被配置成以心室间起搏间期向相对的第二心室腔提供起搏脉冲,所述第二心室腔与所述第一心室腔同步。根据本文所公开的技术运行的所述起搏器感测包含心房和心室机械事件信号的运动信号、从所述运动信号中确定同步性量度,并基于所述同步性量度调整所述AV起搏间期和/或所述心室间起搏间期,以促进优化的心腔同步性。例如,可以使用调整后的起搏间期通过所述医疗装置来递送心房同步的心室起搏或CRT。
在一个实例中,本公开提供了一种包含运动传感器的医疗装置,所述运动传感器被配置成产生运动信号,所述运动信号包含心房收缩事件信号、对应于心室收缩开始的第一心室收缩事件信号和对应于心室收缩结束的第二心室收缩事件信号。所述医疗装置包含被配置成生成心室起搏脉冲的疗法递送电路。在起搏间期到期时生成每个心室起搏脉冲。所述医疗装置包含控制电路,所述控制电路被配置成基于在至少一个所生成的心室起搏脉冲之后的所述第一心室收缩事件信号和/或所述第二心室收缩事件信号中的至少一个,从所述运动信号中确定同步性量度。所述控制电路可以基于所述同步性量度调整所述起搏间期。
在另一个实例中,本公开提供了一种包含产生运动信号的方法,所述运动信号包含心房收缩事件信号、对应于心室收缩开始的第一心室收缩事件信号和对应于心室收缩结束的第二心室收缩事件信号。所述方法包含:在起搏间期到期时生成心室起搏脉冲;基于在至少一个心室起搏脉冲之后的所述第一心室收缩事件信号和/或所述第二心室收缩事件信号中的至少一个,从所述运动信号中确定同步性量度;以及基于所述同步性量度调整所述起搏间期。
在另一个实例中,本公开提供了一种存储一组指令的非暂时性计算机可读存储介质,当由医疗装置执行时,所述指令使所述医疗装置产生运动信号,所述运动信号包含心房收缩事件信号、对应于心室收缩开始的第一心室收缩事件信号和对应于心室收缩结束的第二心室收缩事件信号。所述指令使所述医疗装置在起搏间期到期时生成心室起搏脉冲。所述指令进一步使所述医疗装置基于在至少一个所生成的心室起搏脉冲之后的所述第一心室收缩事件信号和/或所述第二心室收缩事件信号中的至少一个而从所述运动信号中确定同步性量度,并基于所述同步性量度调整所述起搏间期。
本发明内容旨在提供对本公开中所描述的主题的概述。本发明内容并不旨在提供对在以下附图和描述中详细描述的设备和方法的排他性或详尽解释。在以下附图和描述中阐述了一个或多个实例的另外的细节。
附图说明
图1是植入患者心脏的右心房中的心脏内起搏器的概念图。
图2是图1的心脏内起搏器的放大概念图。
图3是植入患者心脏的右心室中的心脏内起搏器的概念图。
图4是根据一个实例的可以封装在起搏器壳体内以提供心脏起搏和感测功能的电路系统的框图,所述功能伴有基于从运动信号推导出的同步性量度的起搏间期控制。
图5是可以由图1的起搏器产生的心脏信号的图解,包含心房和心室电事件和机械事件。
图6是图5的心脏信号的图解,其描绘了可以由起搏器确定的用于控制AV间期的同步性量度的各种实例。
图7是根据一个实例的用于在心房同步的心室起搏期间通过心脏内起搏器控制AV间期的方法的流程图。
图8是根据另一个实例的用于控制AV间期的方法的流程图。
图9是根据一个实例的用于在双心室起搏期间控制心室间起搏间期的方法的流程图。
图10是根据一些实例的用于在触发的基础上执行起搏间期优化的方法的流程图。
具体实施方式
本文公开了一种心脏起搏器和起搏技术,其用于基于运动传感器信号而控制起搏间期,以优化心腔的机械同步性。在一些实例中,所述心脏起搏器可以是完全植入心腔内的无引线起搏器并且被配置成感测至少两个不同心腔的心脏事件并且可以向一个或两个不同的心腔递送起搏脉冲。例如,所述起搏器可以被配置成递送双腔心房和心室起搏、心房同步的单腔心室起搏或心房同步的双心室起搏。所述起搏器从由包含在所述起搏器中的运动传感器产生的运动信号中确定同步性量度。所述起搏器基于所述同步性量度调整起搏间期,例如,AV起搏间期和/或心室间起搏间期(例如,右心室到左心室的起搏间期或左心室到右心室的起搏间期)。所述AV和/或心室间起搏间期被调整成:当在感测到的或经起搏的心房事件之后以调整后的AV起搏间期递送心室起搏脉冲时和/或当在相对的心室腔中在心室起搏脉冲或感测到的R波之后以调整后的心室间起搏间期递送心室起搏脉冲时,促进心腔的机械同步性。
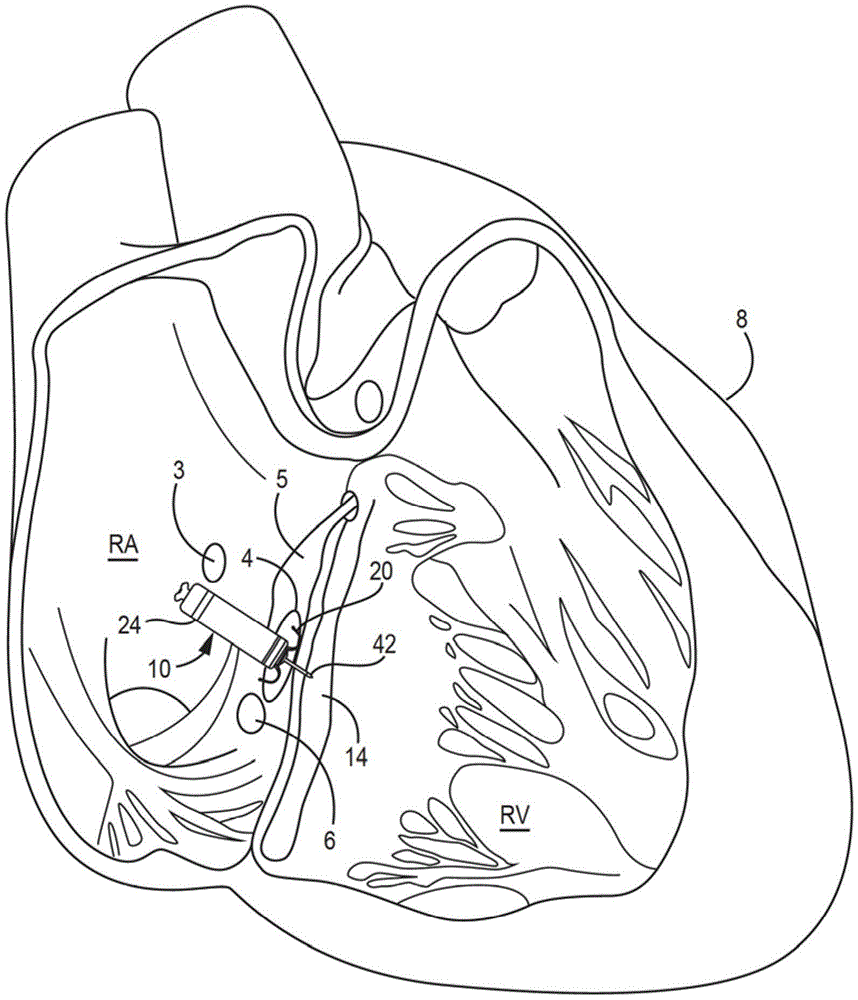
图1是植入患者的心脏8中的双腔心脏内起搏器10的概念图。示出了植入在患者的心脏8的右心房(RA)中的目标植入区域4中的起搏器10。起搏器10可以包含将起搏器10的远端抵靠目标植入区域4中的心房心内膜锚定的固定构件20。目标植入区域4可以位于希氏束5与冠状窦6之间,并且可以与三尖瓣3相邻。在一些实例中,目标植入区域4可以对应于科赫三角(Triangle of Koch)或位于科赫三角内。起搏器10可以是包含远侧心室电极42的无引线起搏器,所述远侧心室电极远离起搏器10的远端延伸。当植入在目标区域4中时,远侧心室电极42可以延伸穿过心房心肌和中心纤维体并且进入到心室心肌14中或沿着心室间隔,而不完全穿透心室心内膜或心外膜表面。远侧心室电极42可以承载在从起搏器远端延伸的轴的远端处,用于将电极42定位在心室组织内,以感测心室信号(例如,伴随心室心肌去极化的R波)并递送心室起搏脉冲。在一些实例中,远侧心室电极42是被提供与基于壳体的阳极电极24一起用在双极起搏和感测电极对中的阴极电极,所述基于壳体的阳极电极沿起搏器壳体定位在近侧。如以下结合图2所描述的,起搏器10可以是包含远侧基于壳体的电极的无引线双腔起搏器,所述远侧基于壳体的电极可以充当心房阴极起搏和感测电极,与基于壳体的近侧阳极电极24配对。以这种方式,起搏器10能够进行DDD起搏和感测或CRT递送。
虽然图1中示出了能够使电极定位在心室心肌中的特定的植入区域4,但应当认识到,被配置成根据本文公开的技术执行心房同步的心室起搏的起搏器可以植入其它位置处,以进行双腔起搏和感测或进行伴有双腔感测的单腔心室起搏,例如,如以下结合图3所描述的。
起搏器10包含产生运动信号的运动传感器,例如产生加速度信号的加速度计,所述加速度信号在起搏器10完全植入心腔内时与通过心脏8和血液的运动直接施加在起搏器10上的运动相关。在其它实例中,起搏器10可以植入在心脏8的心外膜上,并且归因于心脏的运动,所述运动传感器会产生运动信号,从而将运动直接施加在起搏器10上。可以从对应于心室收缩的运动信号中确定同步性量度,作为左心室腔和右心室腔的同步和/或心房腔和心室腔的同步的指征。基于所述同步性量度,AV起搏间期可以被调整成以促进优化的AV同步和/或心室同步性的方式改变从经心房起搏的或感测到的事件到心室起搏脉冲的时延。
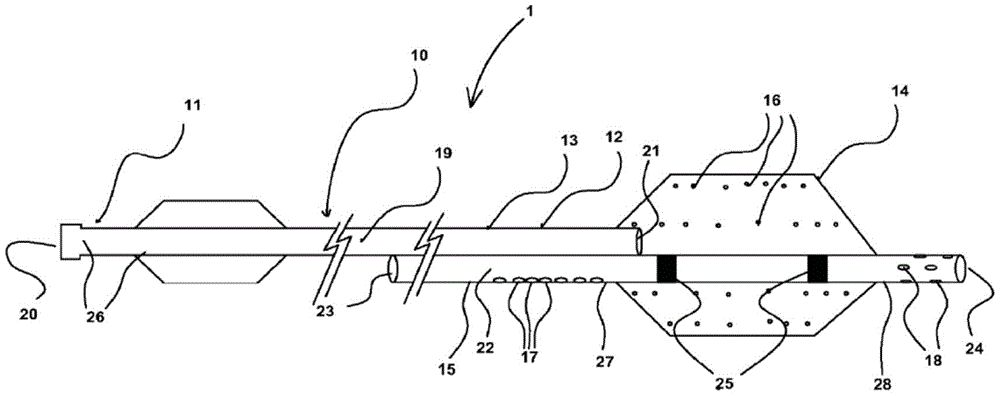
图2是心脏内起搏器10和患者的心脏8的解剖结构的放大概念图。心脏内起搏器10包含壳体30,所述壳体限定起搏器10的内部组件(如以下结合图4总体上描述的感测电路、疗法递送电路、控制电路、存储器、遥测电路、运动传感器以及电源)所驻留的气密密封的内部空腔。壳体30可以由包含钛或钛合金、不锈钢、MP35N(非磁性镍-钴-铬-钼合金)、铂合金或其它生物相容性金属或金属合金的导电材料形成。在其它实例中,壳体30由包含陶瓷、玻璃、蓝宝石、硅酮、聚氨酯、环氧树脂、乙酰基共聚物塑料、聚醚醚酮(PEEK)、液晶聚合物或其它生物相容性聚合物的非导电材料形成。
壳体30包含纵向侧壁38,所述纵向侧壁从起搏器壳体远端32延伸到起搏器壳体近端34并且可以大体上是圆柱形的,其具有纵轴39,以帮助将导管递送到目标区域4。然而,在其它实例中,壳体30可以是棱柱形或其它形状并且不限于本文所示出的大体上圆柱形的实例。壳体30可以包含例如位于近端34处的用于在起搏器10的植入期间与递送工具接合的递送工具接口构件26。
壳体30的一部分可以在起搏和/或感测期间充当阳极电极。在所示出的实例中,基于壳体的电极24被示出为外接纵向侧壁38的近侧部分。当壳体30由如钛合金或上文所列的其它实例等导电材料形成时,可以通过如聚对二甲苯、聚氨酯、硅酮、环氧树脂或其它生物相容性聚合物的涂层等非导电材料对壳体30的部分进行电绝缘,从而使导电材料的一个或多个离散区暴露出来以限定电极,例如,近侧基于壳体的电极24。当壳体30由如陶瓷、玻璃或聚合物材料等非导电材料形成时,可以将如钛、铂、不锈钢或其合金等导电涂层或层施加到壳体30的一个或多个离散区,以形成基于壳体的电极,例如,近侧基于壳体的电极24。在其它实例中,近侧基于壳体的电极24可以是安装或组装到壳体30上的组件,如环形电极。近侧基于壳体的电极24可以例如通过导电壳体30或当壳体30是非导电材料时通过电导体电耦接到起搏器10的内部电路系统。在所示出的实例中,近侧基于壳体的电极24被定位成与壳体远端32相比更靠近壳体近端34,并且因此被称为“近侧基于壳体的电极”24。然而,在其它实例中,基于壳体的电极24可以定位在沿壳体30的其它位置处,例如,比所示出的位置或沿着近端34位置相对更远。
在远端32处,起搏器壳体30可以包含远侧固定和电极组合件36,所述远侧固定和电极组件包含固定构件20和远侧心室电极42,所述远侧心室电极由远离壳体远端32向远侧延伸的轴40承载。远侧心室电极42可以位于轴40的自由远端处或附近。远侧心室电极42可以具有圆锥形或半球形的远侧尖端,所述远侧尖端具有例如小于1mm的相对狭窄的尖端直径,用于穿透进入并穿过组织层,而不需要可能以其它方式产生切削动作的锋利的尖端或具有锋利的或斜切的边缘的针状尖端,所述切削动作可能导致远侧心室电极42的横向位移和不期望的组织创伤。
在一些实例中,轴40可以是正常的笔直的、刚性的构件,其能够被推进穿过组织以定位远侧心室电极42,以起搏心室组织。在其它实例中,轴40相对较硬,在横向方向上的柔韧性有限。轴40可以是非刚性的,以允许随着心脏运动而发生一些横向挠曲。然而,在松弛状态下,当未经受到任何外力时,轴40维持如图所示的笔直位置,以保持远侧心室电极42与壳体远端32间隔开。远侧心室42和轴40被配置成刺穿一个或多个组织层,以将远侧心室电极42定位在期望的组织层(例如,心室心肌)内。因此,轴40可以具有对应于所预期的心室起搏部位深度的高度47,并且可以沿其纵轴具有相对高的压缩强度,以在抵靠植入部位按压时在对远侧心室电极42施加纵轴力时抵抗横向或径向方向上的弯曲,例如,通过将纵向推力施加到壳体30的近端34以将电极42推进到目标植入区域4内的组织中。轴40可以是纵向非压缩的。轴40在经受横向或径向力时可以在横向或径向方向上是可弹性变形的,以允许例如随着组织运动而暂时挠曲,但是当横向力减小时,所述轴返回到其正常笔直位置。
固定构件20可以包含具有正常弯曲位置的一个或多个尖齿。在起搏器10的植入期间,固定构件20的尖齿可以被保持在递送工具内的向远侧延伸的位置中。所述固定构件的尖齿的远侧尖端穿透心脏组织至有限深度,然后其一从递送工具释放,就向近侧弹性地弯曲回到正常弯曲位置(如图所示)。固定构件20的方面可以对应于在美国专利第9,675,798号(Grubac等人)或美国专利第9,119,959号(Rys等人)中大体上公开的固定构件。
在一些实例中,为提供双腔起搏和感测,远侧固定和电极组合件36包含远侧基于壳体的电极22,所述远侧基于壳体的电极可以充当与近侧基于壳体的电极24配对的阴极电极。在使用起搏器10用于双腔起搏和感测或用于CRT应用的情况下,远侧心室电极42可以用作与充当返回阳极电极的近侧基于壳体的电极24配对的阴极电极。可替代地,远侧基于壳体的电极22可以充当与用于感测心室信号并且递送心室起搏脉冲的远侧心室电极42配对的返回阳极电极。在其它实例中,远侧基于壳体的电极22可以是用于感测心房信号并且将起搏脉冲递送到目标植入区域4中的心房心肌的阴极电极。当远侧基于壳体的电极22充当心房阴极电极时,近侧基于壳体的电极24可以充当与用于心室起搏和感测的远侧心室电极42配对的返回阳极,并且充当与用于心房起搏和感测的远侧基于壳体的电极22配对的返回阳极。已示出远侧基于壳体的电极22位于起搏器壳体30的远端32上,并且被耦接到包含在远侧固定和电极组合件36中的引电器,用于将电极22电耦接到壳体30内的起搏和感测电路系统。在其它实例中,远侧基于壳体的电极22可以沿纵向侧壁38的圆周表面进行定位。
如本文所使用的,有关电极的术语“基于壳体的”是指在不使用柔性的细长医疗电引线的情况下,直接承载在壳体30的表面上或直接耦接到所述壳体的表面的电极,所述表面包含包围起搏器10的纵向侧壁38的外部表面以及远端32和近端34的外面。相比之下,“基于引线的”电极由围绕电导体(例如,金属丝或电缆)的柔性引线体承载,所述电导体将所述电极电耦接到由连接器组合件接收的引线的近侧连接器销,所述近侧连接器销有时被称为“接头”,用于与内部起搏器电路系统的电气连接。基于壳体的电极不由细长的柔性引线体承载。电极22、24和42中的每一个电极都是“基于壳体的电极”,因为起搏器10是无引线起搏器,其中每个电极直接位于所述起搏器壳体上或直接耦接到所述起搏器壳体,而无需使用承载手动连接到起搏器连接器组合件的金属丝导体的细长的柔性引线体。
在其它实例中,起搏器10可以被提供有四个电极、一个心房感测和起搏对以及一个心室感测和起搏对。作为实例,一个或多个环形、按钮或球形电极可以承载在远端32上,以充当与相对更近的阳极电极配对的心房阴极电极。可用于从采用本文公开的技术的起搏器的心脏内植入位置递送心房同步的心室起搏的电极配置的各种实例在预授权美国专利公开号2019/0083779(Yang等人)和预授权美国专利公开号2019/0083800(Yang等人)中被大体上公开。在其它实例中,目标起搏部位可以包含希氏束。被配置成用于通过希氏束从所述起搏器的心房腔植入部位起搏心室的示例心房内起搏器在预授权美国专利公开号2019/0134404(Sheldon等人)中被大体上公开。
如图2中所示出的,在一些起搏应用中,目标植入区域4沿心房心内膜18,通常在AV结15和希氏束5下部。轴40和电极42可以被提供有高度47,所述高度穿透目标植入区域4中的心房心内膜18、穿过中心纤维体16并且进入心室心肌14而不穿透心室心内膜表面17。当轴40的整个高度47完全推进到目标植入区域4中时,远侧心室电极42搁置在心室心肌14内,并且远侧基于壳体的电极22被定位成与心房心内膜18紧密接触或极为接近。在各种实例中,轴40的总高度47可以为大约3mm到8mm。轴40的直径可以小于2mm,并且可以为1mm或更小,或甚至0.6mm或更小。在一些实例中,轴40和电极42可以被提供有组织固定特征组件,如钩、螺旋、倒钩或倾向于阻止电极42从起搏部位缩回的其它特征。例如,代替所示出的线性轴40,远侧心室电极42可以是绝缘的螺旋轴的暴露的导电尖端,所述导电尖端从心房心内膜推进穿过心脏组织进入心室心肌组织和/或接近希氏束,以起搏心室。
图3是根据另一个实例的植入在替代位置以递送心房同步的心室起搏的起搏器10的概念图。在一些情况下,起搏器10可以被植入心室腔中并且可以被提供有远侧心室电极42,所述远侧心室电极定位在远离起搏器10的远端延伸以穿透心室间隔7的轴上。在图3所示的实例中,起搏器10被植入右心室(RV)中,其中固定构件20锚定在上间隔壁中。轴40上的远侧心室电极42被推进穿过间隔壁7,而不刺穿左心室心内膜或心外膜表面,以将远侧心室电极42定位在左心室中的目标心室起搏部位。目标心室起搏部位可以在心室心肌中或沿着心室传导系统,例如,沿着束支。在一些情况下,远侧心室电极42可以被推进到间隔壁7中以将远侧心室电极42放置在目标起搏部位处,以从RV内的壳体植入位置例如沿着左束支起搏左心室(LV)。远侧基于壳体的电极22可以充当与右心室心肌可操作地接近的阴极电极,以起搏RV。通过将远侧心室电极42用作与基于壳体的近侧阳极电极24配对的阴极电极(参见图2)来起搏LV并使用与基于壳体的近侧阳极电极24配对的远侧基于壳体的电极22(参见图2)来起搏RV,可以提供双心室起搏。当起搏器10用于双心室起搏时,可以从运动传感器信号中确定同步性量度,以用于优化RV和LV起搏脉冲之间的心室间起搏间期和/或用于优化从心室内运动信号检测到的心房收缩机械事件与心室起搏脉冲之间的AV起搏间期。
如本文所述,起搏器10包含产生心脏机械信号的运动传感器,所述心脏机械信号包含心房收缩事件信号和心室机械事件信号。当置于RV中时,起搏器10可能能够也可能无法从由起搏器10在所述RV内感测到的心脏电信号中感测到心房P波(伴随心房去极化),因为与心室R波相比,P波是相对低幅度的信号。因此,起搏器10可以通过从运动信号中感测心房收缩机械事件信号来感测心房收缩事件,用于开始AV间期以递送心房同步的心室起搏。可以以AV间期起搏RV或LV。如本文所公开的,起搏器10可以从心脏机械信号中确定同步性量度以基于所述同步性量度来优化AV间期,所述同步性量度可以与心室机械同步性相关。在一些患者中,心室腔的机械同步性可能会例如由于心肌病、心力衰竭或传导异常而受损。通过控制用于递送与心房事件同步的LV起搏脉冲的AV间期,可以重新同步RV收缩和LV收缩的定时,或者至少可以减少心室不同步。
图4是根据一个实例的可以封装在起搏器10的壳体30内以提供心脏起搏功能的电路系统的框图,所述功能伴有基于从心脏内运动信号中确定的同步性量度的起搏间期控制。起搏器10可以被配置成用于例如在图1所示的植入位置处进行双腔起搏和感测,或例如在图1或图3的植入位置中的任一位置处进行伴有双腔感测的单腔心室起搏,或例如如图3所示进行伴有双腔感测的双心室起搏。封装在壳体30内的电子电路系统包含软件、固件和硬件,所述软件、固件和硬件协同地监测心房和心室的心脏信号、确定何时需要起搏疗法并且根据编程的起搏模式和起搏脉冲控制参数视需要将起搏电脉冲递送到患者的心脏。如本文所公开的,所述电路系统进一步包含在起搏控制反馈回路中使用的运动感测能力,其用于调整在心房事件和心室起搏脉冲之间调度的AV间期和/或右心室电事件和左心室电事件之间的心室间间期,以促进心腔收缩之间的最优机械同步性。心房和心室之间的同步性以及RV和LV之间的同步性以及每个心室腔区域的经协调的收缩可以通过基于本文公开的一个或多个同步性量度调整AV间期和/或心室间间期来改善。所述电子电路系统包含控制电路80、存储器82、疗法递送电路84、感测电路86、遥测电路88和运动传感器90,用于产生包含与心脏运动相关的心脏机械事件信号的信号。
电源98视需要向包含组件80、82、84、86、88和90中的每一个组件的起搏器10的电路系统提供电力。电源98可以包含一个或多个储能装置,如一个或多个可再充电或不可再充电电池。根据图4的总体框图可以理解电源98与其它组件80、82、84、86、88和90中的每一个组件之间的连接,但为清楚起见未示出所述连接。例如,电源98耦接到包含在疗法递送电路84中的一个或多个充电电路,以便提供为包含在疗法递送电路84中的保持电容器进行充电时所需的电力,所述保持电容器在控制电路80的控制下在适当时候进行放电,以例如根据双腔起搏模式来递送起搏脉冲。电源98还耦接到如感测放大器、模数转换器、开关电路系统等的感测电路86的组件、运动传感器90、遥测电路88和存储器82,以视需要向各种电路提供电力。
图4中所示出的功能框代表起搏器10中包含的功能,并且可以包含实施模拟和/或数字电路的任何离散和/或集成的电子电路组件,所述模拟和/或数字电路能够产生本文中的起搏器10所拥有的功能。各个组件可以包含执行一个或多个软件或固件程序的专用集成电路(ASIC)、电子电路、处理器(共享、专用或组)和存储器、组合逻辑电路、状态机或提供所描述功能的其它合适的组件或组件的组合。用于实施本文所公开的功能的软件、硬件和/或固件的特定形式将主要由起搏器中采用的特定系统架构以及由起搏器采用的特定检测和疗法递送方法来确定。鉴于本文的公开内容,提供软件、硬件和/或固件以在任何现代心脏医疗装置的上下文中实现所描述功能在本领域技术人员的能力范围内。
存储器82可以包含任何易失性、非易失性、磁性或电非暂时性计算机可读存储介质,如随机存取存储器(RAM)、只读存储器(ROM)、非易失性RAM(NVRAM)、电-可擦除可编程ROM(EEPROM)、闪存存储器或任何其它存储器装置。此外,存储器82可以包含存储指令的非暂时性计算机可读介质,所示指令在由一个或多个处理电路执行时会使控制电路80和/或其它电路执行本文中起搏器10所拥有的心房同步的心室起搏功能或其它双腔感测和起搏疗法递送功能。存储指令的非暂时性计算机可读介质可以包含上文所列的介质中的任何一种介质。
控制电路80例如通过数据总线与疗法递送电路84和感测电路86通信,以感测心脏电信号并且响应于感测到的心脏事件(例如,P波和R波,或者其不存在)而控制心脏电刺激疗法的递送。远侧心室电极42、远侧基于壳体的电极22和近侧基于壳体的电极24电耦接到疗法递送电路84以将电刺激脉冲递送到患者心脏,并且电耦接到感测电路86以感测心脏电信号。
感测电路86通过电极22、24和/或42接收心脏电信号并且可以包含多个感测通道,例如,心房(A)感测通道87和心室(V)感测通道89。远侧基于壳体的电极22和近侧基于壳体的电极24可以耦接到心房感测通道87以感测心房电事件信号,例如,伴随心房心肌去极化的P波。远侧心室电极42和近侧基于壳体的电极24(或远侧基于壳体的电极22)可以作为心室感测电极对耦接到心室感测通道89以感测心室电事件信号,例如,伴随心室心肌去极化的R波。在包含由起搏器壳体30和/或轴40承载的另外的电极的实例中,感测电路86可以包含用于选择性地将心房感测电极对耦接到心房感测通道87以及将心室感测电极对耦接到心室感测通道89的开关电路系统。开关电路系统可以包含开关阵列、开关矩阵、多路复用器或适合于将感测电路86的组件选择性地耦接到所选电极的任何其它类型的开关装置。
心房感测通道87和心室感测通道89中的每一个可以包含心脏电事件检测电路系统,用于从由相应感测通道接收的心脏电信号中分别检测P波和R波。包含在每个心房通道87和心室通道89中的心脏电事件检测电路系统分别可以被配置成对从所选电极接收的心脏电信号进行放大、滤波、数字化和整流,以改善用于检测心脏电事件的信号质量。每个通道87和89内的心脏事件检测电路系统可以包含一个或多个感测放大器、滤波器、整流器、阈值检测器、比较器、模数转换器(ADC)、定时器或其它模拟或数字组件。可以例如基于由控制电路80确定的存储在存储器82中和/或由控制电路80和/或感测电路86的硬件、固件和/或软件控制的定时间期和感测阈值,在控制电路80的控制下由每个相应感测通道87和89自动调整心脏事件感测阈值,例如,P波感测阈值和R波感测阈值。感测电路86可以将各种消隐期和不应期应用于所接收的心脏电信号,来以避免心房和心室电事件的错误或过度感测的方式控制心房和心室事件的感测。
每个通道87和89可以被配置成响应于所接收的心脏电信号超过相应的心房P波感测阈值或心室R波感测阈值而产生传递到控制电路80的感测到的事件信号。例如,心房感测通道87可以响应于P波感测阈值交叉而产生P波感测的事件信号。心室感测通道89可以响应于R波感测阈值交叉而产生R波感测的事件信号。控制电路80使用感测到的事件信号来设置对用于调度心脏起搏脉冲的基本时间间期进行控制的起搏逃逸间期定时器。取决于特定的编程起搏模式,感测到的事件信号可以触发或抑制起搏脉冲。例如,从心房感测通道87接收到的P波感测的事件信号可以使控制电路80抑制经调度的心房起搏脉冲(当起搏器10植入RA内时)并以编程的AV起搏间期来调度心室起搏脉冲。如本文所述,可以基于对来自运动传感器90的信号的分析来调整感测到的心房P波和心室起搏脉冲之间的AV起搏间期。如果在AV起搏间期到期之前感测到R波,则抑制心室起搏脉冲。如果AV起搏间期在控制电路80从心室感测通道89接收到R波感测的事件信号之前到期,则控制电路80控制疗法递送电路84以递送与感测到的P波同步的经调度的心室起搏脉冲。
例如,如图1所示,当定位在RA中以进行双腔起搏和感测时,控制电路80可以设置用于控制心房起搏脉冲的递送的较低起搏速率间期,例如,通过设置AA起搏间期。当控制电路80在AA起搏间期到期之前未从心房感测通道87接收到P波感测的事件信号时,控制电路80控制疗法递送电路84以递送心房起搏脉冲并开始AV起搏间期。控制电路80可以设置VV起搏间期以在不存在触发心室起搏脉冲的感测到的心房事件的情况下以最小的较低速率控制心室起搏。
当被配置成用于双腔起搏时,疗法递送电路84可以包含心房起搏电路83和心室起搏电路85。每个起搏电路83和85包含充电电路系统、如一个或多个低电压保持电容器等一个或多个电荷存储装置、输出电容器和开关电路系统,所述开关电路系统控制所述一个或多个保持电容器何时跨输出电容器充电和放电以将起搏脉冲递送到耦接到相应起搏电路83或85的起搏电极矢量。远侧心室电极42和近侧基于壳体的电极24可以作为双极阴极和阳极对耦接到心室起搏电路85,以例如在由控制电路80设置的用于提供心房同步的心室起搏和基本的较低心室起搏速率的AV或VV起搏间期到期时递送心室起搏脉冲。
心房起搏电路83可以耦接到远侧基于壳体的电极22和近侧基于壳体的电极24,以递送心房起搏脉冲。控制电路80可以根据编程的较低起搏速率或根据速率响应性传感器指示的起搏速率进行设置的暂时较低速率来设置心房起搏间期。在一些实例中,心房起搏电路83是任选的。例如,一些患者可能具有正常的SA结和心房电功能,但会出现AV阻滞或其它心室传导异常或不同步,这提供了心室起搏指征但不需要心房起搏。因此,起搏器10可以被配置成用于心房和心室事件的单腔心室起搏和双腔感测。在包含心房起搏电路83时,当在AA起搏间期到期之前未从心房感测通道87接收到P波感测的事件信号时,可以递送心房起搏脉冲。控制电路80响应于递送的心房起搏脉冲而开始AV起搏间期,以提供同步的心室起搏。如本文所述,可以基于对来自运动传感器90的信号的分析来调整心房起搏脉冲和心室起搏脉冲之间的AV起搏间期。
在一些实例中,起搏器10可以被配置成例如在图3的植入位置中递送双心室起搏,在所述情况下不需要心房起搏通道83。然而,可以提供右心室起搏通道和左心室起搏通道。例如,远侧心室电极42和近侧壳体电极24可以耦接到心室通道85以递送左心室起搏脉冲。代替“心房”起搏通道83,第二起搏通道83可以是右心室起搏通道,所述右心室起搏通道耦接到远侧基于壳体的电极22和近侧基于壳体的电极24,以递送右心室起搏脉冲。以这种方式,可以递送双心室起搏以提供CRT,从而改善或恢复心室同步性。可以以心室间(V1-V2)起搏间期递送右心室起搏脉冲和左心室起搏脉冲,所述心室间起搏间期控制右心室和左心室的电激活的相对定时。可以基于从控制电路80从运动传感器90接收的心室内运动信号中确定的同步性量度来调整所述心室间间期。
应当理解,心室间起搏间期可以是用于控制右心室感测到的R波和左心室起搏脉冲之间的时间间期、左心室感测到的R波和右心室起搏脉冲之间的时间间期或右心室起搏脉冲和左心室起搏脉冲之间的时间间期的起搏间期。这些心室间起搏间期中的每一个间期可以单独设置为不同的可编程设置,并且可以由控制电路80基于从心室内运动信号中确定的同步性量度来调整。取决于个体患者的需要,右心室电事件可以引起左心室电事件,反之亦然。在双心室感测和起搏的情况下,心室感测通道89可以包含两个心室感测通道,一个用于感测例如来自电极22和24的右心室R波,而一个用于感测例如来自电极42和24的左心室R波。
疗法递送电路84通过将相应的心房起搏电路83和心室起搏电路85的保持电容器充电至相应的编程的起搏电压幅度来递送起搏脉冲,并根据从控制电路80的定时电路94接收的控制信号,针对相应的起搏脉冲宽度对所述保持电容器放电。例如,定时电路94可以包含由控制电路80的处理器92设置的可编程数字计数器,用于控制与各种起搏模式相关联的基本起搏时间间期。控制电路80还可以设置由疗法递送电路84生成的心脏起搏脉冲的幅度、脉冲宽度、极性或其它特性,所述设置可以基于存储在存储器82中的编程值。
起搏器10包含运动传感器90,所述运动传感器产生包含心脏机械事件信号的信号,所述心脏机械事件信号可以被分析用于控制由疗法递送电路84递送的心室起搏。在一些实例中,运动传感器90可以被实施为封装在壳体30内的加速度计。然而,在其它实例中,运动传感器可以是如压力传感器等另一种类型的机械传感器,所述压力传感器被配置成当起搏器10被植入心腔内或心腔上时,产生与由心脏和血液直接施加在起搏器壳体30上的机械运动相关的电信号。运动传感器90向控制电路80(例如,向处理器92)提供信号,以用于分析检测心脏机械事件并基于一个或多个检测到的心脏机械事件的一个或多个方面确定同步性量度。基于所述同步性量度,控制电路80可以设置或调整起搏间期,例如,用于控制心室起搏脉冲相对于心房事件的定时的AV间期,用于控制右心室电事件和左心室电事件之间的定时的心室间间期,或两者兼而有之。开始AV间期的心房事件可以是电事件,例如,感测到的P波或经递送的心房起搏脉冲,或是从运动传感器90产生的运动信号中被感测为心房收缩事件的机械事件。例如,在图3的实例中,控制电路80可以被配置成从自运动传感器90接收的运动信号中感测机械心房收缩事件并且响应于感测到所述机械心房收缩事件而开始AV间期。
运动传感器90的加速度计可以是一维、二维或三维加速度计。例如,所述加速度计可以包含三个单轴加速度计元件,所述三个单轴加速度计元件彼此正交定位以形成三个轴。包含在运动传感器90中的单维或多维加速度计的每个轴可以由能够响应于施加在起搏器10和随后施加在所述传感器元件上的加速度的改变而产生电信号(例如,通过将所述加速度转换为所述运动传感器元件的力或位移,所述力或位移由所述运动传感器元件转换为电信号)的压电元件、微机电系统(MEMS)装置或其它传感器元件来限定。
每个运动传感器元件产生对应于与所述传感器元件的轴对准的矢量的加速度信号。每个运动传感器元件产生对应于沿相应的运动传感器轴的重力矢量分量的DC分量。每个运动传感器元件沿相应的轴产生与归因于患者运动的加速度相关的AC分量。由所述运动传感器的每个轴产生的AC加速度信号可以包含直接施加在起搏器10的壳体30上的加速度,从而引起归因于RA内(当植入RA中时)或RV内(当植入RV中时)的血液运动的起搏器壳体30的加速度,以及归因于心腔运动(例如,心房腔收缩和舒张以及心室腔收缩和舒张)的加速度。加速度信号可以进一步包含归因于由患者身体运动引起的起搏器壳体30的加速度的信号,例如,归因于患者参与日常生活、锻炼等的活动时的患者身体活动。
在一些实例中,所述加速度计可以具有与起搏器10的纵轴39(参见图2)平行或对准的一个“纵向”轴和相对于所述纵轴39在径向方向上延伸的两个正交轴,例如,径向向外朝向纵向侧壁38。尽管一个轴或多个轴的组合可以提供所关注的心脏机械事件的更大信号强度,但用于感测心脏机械事件信号的最优轴(或多个轴)可以在运动传感器定向、植入后的起搏器定向和其它因素之间变化。因此,本文公开的技术的实践不限于运动传感器在壳体30内或沿所述壳体或相对于心脏8的特定定向。总体而言,运动传感器90从至少一个运动传感器信号轴产生心脏内运动信号,控制电路80被配置成从所述至少一个运动传感器信号轴检测和分析心脏机械事件信号,以用于控制疗法递送电路84在心室起搏期间使用的起搏间期。在图1的实例中,所述心脏内运动信号是包含机械心房收缩事件信号和机械心室收缩事件信号的心房内运动信号。在图3实例中,所述心脏内运动信号是还包含机械心房收缩事件信号和机械心室收缩事件信号的心室内信号。控制电路80分析心脏内运动信号以检测心脏机械事件,确定与心腔同步性相关的同步性量度,并视需要基于所述同步性量度调整AV间期和/或心室间间期以改善心腔同步性。
如本文所使用的,“心腔同步性”可以指心房收缩和随后的心室收缩之间的同步性和/或同时发生的右心室收缩和左心室收缩之间的同步性。心腔同步性可以进一步包含心腔各段之间的同步性,例如前壁、间隔壁和下壁的左心室心尖段、中段和基底段之间的同步性或协调。例如,当AV间期使得心室收缩不早于心房收缩的结束而开始时和/或当与心室收缩力相关的同步性量度相对于其它AV间期为最大化时,所述心房收缩和心室收缩之间的机械同步性可以被认为是“优化的”。当同步性量度指示左右心室收缩和舒张的同时性为最大化时,左右心室收缩或其节段之间的机械同步性可以被认为是“优化的”。以下结合图5描述了可以由控制电路80确定的同步性量度的实例。
在一些实例中,控制电路80可以进一步分析从运动传感器90接收的运动信号,以确定患者身体活动的量度,从而提供速率响应性起搏。从运动传感器信号确定的患者身体活动量度可以与对增加的心输出量或增加的代谢需求的需要相关,其可以由控制电路80使用以确定传感器指示的起搏速率。控制电路80可以根据传感器指示的起搏速率将编程的基本的较低起搏速率调整为临时的、较高的起搏速率。例如,编程的基本的较低起搏速率可以是每分钟40次到60次脉冲。控制电路80可以根据传感器指示的起搏速率来增加起搏速率,所述速率可以使用传递函数来确定,所述传递函数将患者活动量度与支持所指示的患者活动水平所需的目标心率相关联。
起搏器10可以包含遥测电路88,用于与如编程器或家庭监视器等外部装置进行无线通信。遥测电路88可以被配置成使用如Wi-Fi、医疗植入通信服务(MICS)或其它通信带宽等射频(RF)链路来与外部装置建立通信链路。例如,遥测电路88可以被配置成用于与如编程器或患者监视器(两者均可从美国明尼苏达州明尼阿波利斯的美敦力公司(Medtronic,Inc.Minneapolis MN,USA.)购得)等外部编程器或监视器进行通信。由控制电路80所利用的用于感测心脏事件并控制起搏疗法递送的控制参数可以通过遥测电路88编程到存储器82中。遥测电路88包含用于根据经实施的通信协议与外部装置进行通信的收发器和天线。在控制电路80的控制下,遥测电路88可以从外部装置接收下行链路遥测并将上行链路遥测发送到所述外部装置。在一些情况下,遥测电路88可以用于向植入患者中的另一个医疗装置发射通信信号并从所述医疗装置接收通信信号。
图5是可以由起搏器10产生的心脏信号的图解100,所述心脏信号包含可以由控制电路80检测以用于确定同步性量度的心房和心室电事件和机械事件信号。所述同步性量度可以与心腔的机械同步性或收缩力相关。控制电路80可以基于一个或多个经确定的同步性量度来调整AV起搏间期和/或心室间起搏间期,以促进心腔同步和/或改善的收缩力。通过从自运动传感器90接收的运动传感器信号中检测一个或多个机械事件并基于所检测到的机械事件确定量度或特征来确定同步性量度。
图5示出了可以分别由感测电路86和运动传感器90产生的心电图(EGM)信号102和运动信号110。EGM信号102可以从心脏电信号产生,所述心脏电信号由起搏器10例如通过电极42和24接收。在此实例中,运动信号110是当起搏器10完全植入右心房腔内时由运动传感器90产生的加速度信号。运动信号110可以称为心房内运动信号。
EGM信号102包含伴随心房心肌去极化的P波104。感测电路86的心房感测通道87可以被配置成产生心房感测的事件信号120,所述心房感测的事件信号被传递到控制电路80以指示已经感测到P波104。运动信号110中被标记为A4信号116的心房收缩事件在每个P波104之后,并代表心房的机械收缩。A4信号116在本文中也被称为“机械心房收缩事件”。
EGM信号102包含经起搏的R波信号106和固有的R波信号108,每个信号都伴随着心室心肌的去极化。每个R波106和108之后是运动信号110的相应的A1信号112和118。A1信号112和118随着电去极化之后的心室收缩而出现,并且可以对应于心室机械收缩的开始。A1信号112和118各自之后是相应的A2信号114和119,所述信号可以随着主动脉瓣和肺动脉瓣的关闭而发生,从而标志着心室机械收缩的近似偏移或结束(以及心室机械舒张的开始)。A1信号(112和118)和A2信号(114和119)在本文中都被称为“心室收缩事件信号”,因为A1信号标志着机械收缩的开始,而A2信号标志着心室机械收缩的结束。
在一些实例中,EGM信号102的电事件和运动信号110的机械事件之间的时间关系和/或运动信号110的两个机械事件之间的时间关系可以被确定为同步性量度,所述同步性量度用于设置和调整起搏间期,所述起搏间期用于控制由起搏器10递送的心室起搏脉冲的定时。以下描述了可以由控制电路80确定和使用的各种同步性量度的实例。为了确定此类同步性量度,控制电路80检测运动信号事件,例如A1信号、A2信号和/或A4信号。为了从运动信号110检测期望的机械事件,控制电路80可以设置用于检测A1、A2和A4信号的各种时间窗口和/或阈值或其它检测标准。
例如,可以通过在从感测电路86接收的心房感测的事件信号120之后设置A4窗口150来检测A4信号116。可以响应于A4窗口150期间的A4幅度感测阈值交叉而检测A4信号116。A4窗口150可以在预先确定的时间间期后或在接收到心室感测的事件信号124(或心室起搏脉冲122的递送)时到期。在响应于阈值交叉而检测到A4信号116之后,控制电路80可以检测A4信号116的峰值幅度、负峰值斜率、返回基线或A4信号端115或其它特征,以便识别用于将同步性量度确定为时间间期(例如,从所述A4信号端115到紧随其后的A1信号112或118的时间间期)的信号采样时间点。在其它实例中,可以相对于心室事件设置A4窗口150,例如,在心室起搏脉冲122或心室感测的事件信号124之后的心室后心房不应期之后。
在一些实例中,可以在心室起搏脉冲122之后设置A1窗口130,用于在A1窗口130期间基于运动信号110的A1幅度阈值交叉而检测经起搏的A1信号112。类似地,可以在心室感测的事件信号124之后设置A1窗口134,用于检测固有的A1信号118。归因于固有的R波之后的机械收缩的定时与心室起搏脉冲之后的机械收缩的定时之间的任何差异,A1窗口130和134可以具有相同的持续时间或不同的持续时间。如图5所示,在一些情况下,A1信号112和118可以具有双峰。归因于右心室和左心室之间的心室不同步和/或心室段的区域性不同步,心房内或心室间A1信号可以包含两个或更多个峰。心脏内(或心外膜运动信号)可以对区域性或节段性和/或心室间的不同步更加敏感,从而产生多峰A1信号,而非被感测到进一步远离心脏的其它类型的传感器信号,这会提供更全面的心脏电事件和/或机械事件的信号。A1信号的特征(例如,第一峰值、第二峰值、最大峰值、最大斜率或其它特征)的时间可以由控制电路80识别,以用于将同步性量度确定为以A1信号112开始或结束的时间间期。在其它实例中,同步性量度可以被确定为A1信号的特征,例如,最大峰值幅度、信号宽度、最大斜率、峰的数量或可以指示心室同步性或收缩力的其它特征。
控制电路80可以在心室起搏脉冲122之后设置A2窗口132并在心室感测的事件信号124之后设置A2窗口136,以帮助分别检测A2信号114和119。A2窗口132和136可以具有相同或不同的持续时间,因为在固有的R波108之后的A2信号119的定时可以不同于在心室起搏脉冲122之后的A2信号114的定时。在相应的A1窗口130和134到期后或在相应的A1信号112和118已被检测到后,A2信号114和119可以在相应的A2窗口132和136期间被检测到。可以确定响应于运动信号110的阈值幅度交叉而检测A2信号的时间和/或由控制电路80识别的A2信号114或119的特征(例如最大峰值幅度、最大斜率(或导数)、峰数量或信号宽度)的时间,以用于确定同步性量度。
在其它实例中,对A4信号116的端115的检测可以被用于设置A1时间窗口140和/或A2时间窗口142,以帮助检测在A4信号116的端之后的心室机械事件信号112、114、118或119。图5描绘了可以用于帮助从运动信号110检测心脏机械事件的感测窗口的各种实例。应当理解,可以根据个体患者的需要,设置包含感测阈值幅度和感测窗口的机械事件感测控制参数。可以相对于由控制电路80识别的先前的电事件或机械事件来定义用于帮助检测特定的心脏机械事件的各种感测窗口。
图6是图5的EGM信号102和运动信号110的图解180,其示出了可以由控制电路80使用运动信号110确定的同步性量度的各种实例。以从运动信号110或心脏机械事件信号特征检测到的心脏机械事件开始和/或结束的各种时间间期可以由控制电路80确定为同步性量度。可以确定不同的同步性量度以用于设置和调整AV间期,从而根据临床应用控制心房同步的心室起搏和/或设置心室间间期。在一些实例中,A4信号116(具体地说,A4信号116的端115)相对于心室起搏脉冲122或A1信号112的定时可以被确定为同步性量度。心室收缩应在心房收缩完成后开始,以避免心房收缩期间心室充盈不完全,并避免心室收缩对抗仍在收缩的心房腔。因此,控制电路80可以将从A4信号116的基准点到A1信号112的基准点的A4-A1时间间期182确定为同步性量度。A4信号116的基准点可以是基于运动信号超过A4感测阈值幅度170而检测到A4事件的时间、A4信号116的最大峰值幅度、A4信号116的结束时间115、A4信号的最大负斜率或由控制电路80识别为心房机械收缩的参考时间点的其它基准点。A1信号112的基准点可以是基于运动信号超过A1感测阈值幅度172而检测到A1事件的时间、A1信号116的最大峰值幅度、A1信号的最大正斜率或由控制电路80识别为心室机械收缩开始的参考时间点的其它基准点。如果A4-A1时间间期182小于(或大于)阈值间期(或在目标范围之外),则可以调整响应于心房感测的事件信号120而开始的AV起搏间期178,直到所述A4-A1时间间期落入目标范围内或至少长于最小A4-A1时间间期阈值为止。
在一些实例中,可以在非起搏的、固有的心室心跳期间确定目标同步性量度值。例如,在接受心动过缓心室起搏以治疗间歇性AV传导阻滞的患者中,可以确定同步性量度并将所述同步性量度用于设置目标同步性量度值或范围,在不存在固有的R波的情况下递送心室起搏脉冲时,所述目标同步性量度值或范围是所期望的。经历间歇性AV阻滞的患者可以间歇性地具有正常传导,所述正常传导可以导致心房和心室之间以及右心室和左心室之间的正常同步性。可以在跟随有心室感测的事件信号124的A4信号116和随后的A1信号118之间确定固有的A4-A1时间间期188。固有的A4-A1时间间期188可以用作心室起搏期间的目标A4-A1时间间期。当心室起搏期间的A4-A1间期182短于固有的A4-A1时间间期188或其百分比时,控制电路80可以增大AV间期178。当经起搏的A4-A1间期182长于固有的A4-A1间期188或其百分比时,控制电路80可以减小AV间期178。当心室起搏期间的A4-A1间期182在固有的A4-A1间期188的阈值或目标范围内时,控制电路80可以保持AV间期178不变。应认识到,在一些实例中,可以针对多个不同的心房率来确定基于固有的A4-A1间期188的目标A4-A1间期,从而可以根据给定的心率或心率范围的目标A4-A1间期来调整AV间期178。
在其它实例中,患者可能在固有的AV传导期间经历传导延迟或可能经历完全的AV传导阻滞,使得固有的A4-A1时间间期没有用处或无法被确定以用于设置被用作心室起搏期间的同步性量度的所述A4-A1时间间期的目标值。在此类情况下,目标A4-A1间期可以基于经验数据进行设置,或可以在对患者进行的其它AV间期优化研究期间建立,例如,使用超声波心动描记术(echocardiography)或其它血液动力学评估方式或测量方式来确定优化的AV间期178。当基于超声波心动描记术或其它临床血液动力学评估方式而认为AV间期178对于给定患者是最优的时,可以从运动信号110确定经优化的A4-A1间期并将其用作调整AV起搏间期178中的目标A4-A1间期。
可以从运动信号110确定其它同步性量度,所述运动信号可以用作A4-A1时间间期的补充或替代,以用于调整起搏间期。可以由控制电路80确定的其它同步性量度时间间期包含A1宽度间期184和/或A1-A2间期186。A1宽度间期184可以是双峰A1信号的两个单独峰之间的时间间期,如在A1信号112的实例中。A1信号112的两个峰之间的A1宽度间期可以与RV和LV(或其节段)之间的同步性相关,其中一个峰可以对应于右心室收缩而另一个峰可以对应于左心室收缩。在其它实例中,A1宽度可以是例如在预定义的阈值幅度处的单峰A1信号的宽度。相对长的A1宽度间期184可以指示心室不同步增加。可以调整AV间期178,直到所述A1宽度间期184最小化为止或直到A1信号112从两个峰减少到单个峰为止,这表明心室同步性得到改善。心室同步性的改善可以包含左右心室的同时同步收缩的改善和/或左心室或右心室之一的节段的协调收缩的改善。例如,在一些患者中,与心室腔的其它部分或节段相比,一个心室腔(右心室或左心室)的心室壁的一部分的收缩可能延迟。为了说明,与左心室的其它部分相比,左心室侧壁的收缩可能会延迟。对应于心室段之间经改善的心室同步性的同步性量度可以对应于心室腔的区域性或节段性收缩延迟的校正或减少。
另一个示例同步性量度是在A1信号112和A2信号184的基准点之间确定的A1-A2间期186。例如,可以在运动信号110超过A1感测阈值172和运动信号110超过A2感测阈值174之间确定A1-A2间期186。可替代地,A1-A2时间间期186可以被确定为A1信号112的最大峰值和A2信号116的最大峰值之间或定义A1-A2间期的A1信号112的基准点和A2信号116的基准点的另一个组合之间的时间间期。A1-A2间期186可以与心室收缩时间间期或射血期相关,并且可以是心室同步性的指标。可以在心室起搏期间确定A1宽度184和/或A1-A2间期186,并将其与相应的目标宽度和目标A1-A2间期进行比较。所述目标A1宽度和所述目标A1-A2间期可以分别基于在非起搏的心室跳动期间确定的固有的A1宽度和固有的A1-A2间期或在如超声波心动描记术等其它起搏间期优化程序期间确定的A1宽度和A1-A2间期。
在其它实例中,同步性量度可以被确定为固有地感测到的或起搏的心脏电事件与心脏机械事件之间的时间间期。例如,Vpace-A1时间间期190可以被确定为从心室起搏脉冲122到A1信号112的最大峰值幅度或其它基准点的时间间期。Vpace-A2时间间期192可以被确定为从心室起搏脉冲122到A2信号116的最大峰值幅度或其它基准点的时间间期。在一些实例中,当所述Vpace-A1时间间期190或Vpace-A2时间间期192用作同步性量度时,可以基于在非起搏的心室跳动期间确定的相应的固有的Vsense-A1时间间期194或固有的Vsense-A2时间间期196来设置所述同步性量度的目标范围或阈值。
所述同步性量度不限于被确定为时间间期。在其它实例中,所述同步性量度可以被确定为A1和/或A2信号的特征。在一些实例中,控制电路80可以设置A1窗口130和/或A2窗口132(参见图5)并且可以在所述A1窗口130和/或A2窗口132期间识别大于预先确定的阈值幅度的运动信号采样点。可以从经识别的采样点确定同步性量度,这可以包含例如对所述采样点进行积分或求和、对所述采样点进行计数、从所述经识别的采样点确定斜率或从所述经识别的采样点确定最大峰值幅度。所述经识别的采样点可以包含来自A1信号112和A2信号114中的一者或两者的采样点。例如,大于预先确定的基线或阈值幅度的A1信号112的面积可以由包含在控制电路80中的积分器或求和电路确定并且可以是心室同步性的指标。随着A1信号面积的增加,左右心室之间和/或一个心室腔的区域之间可能会出现更大的心室不同步。基于目标A1信号面积,可以对AV间期182进行调整(增大或减小),直到A1信号面积被最小化(达到所有经测试的AV间期的最小值)或落入目标范围内或低于目标阈值为止。
在另一个实例中,可以对A1信号和/或A2信号的采样点的数量进行计数,所述采样点大于预先确定的阈值幅度并且在A1窗口130内、在A1窗口130和A2窗口132两者内或在A2窗口130内但不在A1窗口130内(图5示出了A1窗口130和A2窗口132)。同步性量度可以被确定为大于所述预先确定的阈值的采样点的数量。相对较高的采样点计数可以与较大的心室不同步性相关。采样点计数可以由处理器92的固件或软件或由在控制电路80的硬件中实施的比较器和计数器确定。
在仍其它实例中,A1窗口130内的运动信号110的面积、A2窗口132内的运动信号的面积、A1信号112的最大峰值幅度、A2信号114的最大峰值幅度、A1信号112的最大斜率(正或负)、A2信号114的最大斜率(正或负)或其任何组合可以被确定为用于以促进正常的或改善的心腔同步性的方式控制对AV间期182(或心室间间期)的调整的一个或多个同步性量度。另一个示例同步性量度可以被确定为A1窗口130和/或A2窗口132内的运动信号110的可变性的量度。例如,拐点的数量或阈值交叉的数量可以指示与心室同步性相关的运动信号的变化。在A1和/或A2窗口期间的更大的拐点的数量或更大的阈值交叉的数量可以是心室不同步增加的证据。可以调整控制心室起搏脉冲递送的定时的起搏间期,以减少A1和/或A2窗口期间的拐点的数量或阈值交叉的数量。
在一些患者中,如被诊断患有心力衰竭的患者,心室起搏可以由起搏器10递送以提供CRT以改善心室同步性。因此,可以确定从与心室同步性相关的A1信号112和/或A2信号114确定的同步性量度。可以调整AV间期178直到所述同步性量度指示心室同步性改善为止,取决于正被确定的同步性量度,所述改善可以是同步性量度值的增大或减小。由于固有的AV传导和通过固有的心室传导系统进行的传导(如果存在的话)可能异常或延迟,因此可以基于经验数据确定同步性量度的目标值,或当基于如超声波心动描记术研究等其它临床测量方式或评估方式认为AV间期为最优时,可以从运动信号110确定同步性量度的目标值。当起搏器10被植入RV中时,可以对AV间期和/或心室间间期进行调整,直到同步性量度指示心室同步性改善为止。
在图4和5的实例中,EGM信号102中示出的心房电事件是固有的心房感测的事件,例如,由感测电路86的心房通道87感测到的P波。然而,应当理解,用于设置A4窗口150并触发AV间期178的开始的心房电事件可以是由起搏器10递送的心房起搏脉冲。患者可能是依赖起搏器的,长期需要习心房起搏。在一些情况下,响应于感测到的P波的缺失或以传感器指示的起搏速率递送心房起搏脉冲,以提供速率响应性起搏。在心房起搏脉冲之后的AV间期可以被设置为与在心房感测的事件信号之后设置的AV间期不同的间期。然而,在两种情况下,可以基于同步性量度调整AV间期,以促进优化的心腔同步。在心房感测和心房起搏期间,所述同步性量度的目标值或范围可以是相同的值,因为所述目标值指示了心腔机械功能的同步性的优化和改善。在其它实例中,与用于调整心房起搏期间所使用的AV间期的同步性量度的目标值或范围相比,用于调整心房感测期间所使用的AV间期的同步性量度的目标值和范围可以被不同地定义。心房起搏和心房感测期间心脏的收缩反应可以不同。因此,不同的同步性量度目标值或范围可以指示心房感测和心房起搏期间心腔同步性的优化。此外,与心房起搏期间确定的用于调整起搏-AV间期的同步性量度相比,可以在心房感测期间确定不同的同步性量度以用于调整感测-AV间期。
在一些实例中,开始AV起搏间期的心房事件是感测到的A4信号116。在图3实例中,当起搏器10被植入心室腔中时,控制电路80可以被配置成检测A4信号116并开始AV起搏间期。在这种情况下,与响应于心房感测的事件信号120而开始的AV起搏间期178相比,所述AV起搏间期设置得相对短,因为心室收缩应该在心房收缩完成时或完成之后不久开始。然而,在两种情况下,可以基于在心室起搏脉冲递送之后确定的同步性量度和所述同步性量度的经建立的目标值来调整AV起搏间期。
图7是根据一个实例的由起搏器10执行的用于在心房同步的心室起搏期间控制AV间期的方法的流程图200。在框201处,建立一个或多个同步性量度的目标值。如上所述,所述目标值可以基于在向心室的固有的传导期间确定的同步性量度的值,所述固有的传导可以在心房起搏脉冲或固有的感测到的P波之后。例如,如果同步性量度是A1信号宽度,则可以在未递送心室起搏时测量所述A1信号宽度。所述目标值可以被设置为A1信号宽度的最大阈值,所述最大阈值可以被定义为所述A1信号宽度的百分比或大于所述A1信号宽度的预先确定的间期。在此实例中,假设A1信号宽度的增加超过所述目标值指示了RV和LV收缩的不同步增加的趋势。
在另一个实例中,如果同步性量度是A4-A1间期,则可以在心室感测期间(未递送心室起搏脉冲)确定所述A4-A1间期。可以基于在心室感测期间确定的目标A4-A1间期值来设置目标A4-A1间期范围。最小A4-A1间期可以被定义为心室感测期间确定的A4-A1间期的第一百分比,并且可以代表从心房机械收缩的结束到心室收缩的开始为止的最小时间延迟。最大A4-A1间期可以被定义为心室感测期间确定的A4-A1间期的第二百分比,并且可以代表从心房机械收缩的结束到心室收缩的开始为止的最大时间延迟,以促进心室起搏期间的最优血液动力学功能。
在其它实例中,一个或多个同步性量度的目标阈值或范围可以由用户在框201处例如使用外部编程器编程到存储器82中。当如在超声波心动描记术研究期间基于另一种临床测量方式或评估方式确定AV间期将被优化时,可以在心室起搏期间确定目标同步性量度值。可以在心室起搏期间以优化的AV间期确定同步性量度的目标值,并且基于所确定的同步性量度目标值的目标阈值或范围可以被编程到存储器82中。
在框202处,控制电路80检测心房事件。在一些实例中,所述心房事件是电事件。所述心房电事件可以是由感测电路86感测到的固有的P波或由疗法递送电路84递送的心房起搏脉冲。然而,在一些实例中,在框202处检测到的心房事件可以是从自运动传感器90接收的运动信号中感测到的A4信号。控制电路80响应于检测到心房事件而在框204处开始AV间期。在框204处开始的所述AV间期可以是在感测到的P波之后的感测AV(SAV)间期或是在经递送的心房起搏脉冲之后的经起搏的AV(PAV)间期或是在感测到的A4信号之后的A4-V间期。所述SAV间期、PAV间期和A4-V起搏间期可以各自是不同的间期,以说明心房和心室电事件以及心房和心室机械事件的相对定时的差异。此外,相比于当经感测的P波是异位搏动或房性期前收缩(PAC)时所设置的SAV间期,当所述经感测的P波是由窦房结引起的窦性P波时,SAV间期可以不同地设置。例如,当在先前感测到的P波或心房起搏脉冲之后连续感测到P波而没有心室事件介入时,可以感测到PAC。如果早期感测到PAC,例如在心房不应期期间,则可以忽略所述PAC。然而,如果在心房不应期到期之后感测到PAC,则控制电路80可以响应于在框202处感测到PAC而在框204处开始AV间期。响应于PAC而开始的SAV间期可以被设置为与响应于窦性P波而开始的SAV间期不同的间期。
如果在框208处感测到R波,例如从感测电路86接收到心室感测的事件信号,则在AV间期到期之前(框206的“否”分支),控制电路80会取消经调度的心室起搏脉冲并且返回框202处以等待下一个心房事件开始下一个AV间期。在一些实例中,当感测到固有的R波并且目标同步性量度阈值或范围基于在心室感测期间确定的同步性量度目标值时,控制电路80可以从框208返回到框201。控制电路80可以在心室感测的事件之后确定同步性量度值并且在框201处基于所确定的值而更新目标同步性量度阈值或范围。例如,在固有的、感测到的心室周期期间确定的多个同步性量度值可以在先进先出的基础上进行存储和平均(其中忽略异常值),或者最近存储的同步性量度目标值(其可以是多个值的平均值)和当前测量的同步性量度值的加权组合可以被确定为更新的同步性量度目标值。所述目标值可以用于设置用于控制AV间期调整的同步性量度的目标阈值或范围。
当AV间期在框206处到期而R波未被感测到时,在框210处通过疗法递送电路84递送心室起搏脉冲。控制电路212在心室起搏脉冲之后在框212处确定同步性量度。在一些实例中,可以在每个心室起搏脉冲之后逐心跳地确定同步性量度,以允许像每个心室起搏脉冲递送一样频繁地调整AV间期。在其它实例中,当在框210处递送的心室起搏脉冲是第n个心室起搏脉冲时,在框212处确定同步性量度,其中n是预先确定的心室起搏脉冲的数量。例如,可以按每8th个起搏脉冲、每12th个起搏脉冲、每20th个起搏脉冲或按其它选定的起搏脉冲数来确定同步性量度。在仍其它实例中,可以在框212处根据预先确定的调度来确定同步性量度,例如每天一次、每小时一次、每分钟一次或其它频率。此外,应当认识到,在框212处确定同步性量度可以包含确定多个起搏的心室周期的同步性量度并通过求平均或其它统计方法组合经确定的值以确定当前应用的AV间期的代表性同步性量度,所述AV间期可以是SAV间期、PAV间期、PAC-AV间期或A4-V间期。
在框214处,通过控制电路80将同步性量度与目标同步性量度阈值或范围进行比较。如果在框212处确定的同步性量度满足在框201处建立的目标同步性量度阈值或范围,则控制电路80在不调整AV间期的情况下返回到框202处以等待下一个心房事件。当同步性量度小于在框201处建立的最小阈值或大于在框201处建立的最大阈值时,在框212处确定的同步性量度可能不满足目标阈值或范围。响应于在框212处确定的同步性量度在框214处不满足目标同步性量度需求,控制电路80在框216处调整AV起搏间期。
AV间期的调整可以是增大或减小步进间期(step interval),例如10ms、15ms、20ms、25ms、30ms、50ms或其它选定的间期。取决于在框212处确定的同步性量度值和对应的目标阈值或范围,所述AV间期调整可以是例如当A4-A1间期太短时的增大,或可以是例如当所述A4-A1间期太长时的减小。在一些实例中,基于目标值和在框212处确定的同步性量度值之间的差异,AV间期可以在一个步进中增大或减小。以这种方式,可以在单个调整中校正AV间期,以使同步性量度在目标要求范围内。
在一些情况下,AV间期是否需要增大或减小或增大或减小多少可能并不明显。因此,框216处的调整可以是步进递增或递减,并且框202到框216的过程可以被重复,直到在框212处确定的同步性量度在框214处满足同步性量度需求为止,这可以包含AV间期的多个增大和/或减小的调整。
图8是根据另一个实例的用于通过起搏器10来控制AV间期的方法的流程图300。起搏器10可以被配置成通过调整AV间期直到与改善的心腔同步性相关的同步性量度的变化得以实现为止来学习优化的同步性量度值,而不需要用额外的AV间期调整获得进一步的改善。控制电路80可以在心室起搏期间以多个AV间期设置确定一个或多个同步性量度,并选择产生被认为是最大的改善或被认为比在其它AV间期设置下确定的其它同步性量度值更优化的同步性量度值的AV间期设置,而不是如结合图7所描述的那样基于目标值建立目标同步性量度阈值或范围。
在框302处,控制电路80检测心房事件,例如心房起搏脉冲、感测到的P波或感测到的A4信号。控制电路80响应于检测到心房事件而在框304处开始AV间期。如果在AV间期到期(框306)之前由感测电路感测到R波(框308),例如当在所述AV间期期间从感测电路86接收到R波感测的事件信号时,则控制电路80等待下一个心房事件。经调度的心室起搏脉冲被抑制。
当AV间期在框306处到期而R波未被感测到时,在框310处,通过疗法递送电路84递送经调度的心室起搏脉冲。在框312处,控制电路80从运动信号中确定同步性量度。同步性量度可以是上文结合图5和6给出的任何实例,并且在一些实例中,可以确定多于一个的同步性量度。在一个实例中,除了如A1幅度、A1宽度、A1-A2时间间期或可指示RV和LV同步性的其它量度等心室机械事件的至少一个其它量度之外,还确定了A4-A1间期。在框314处,可以将在框312处确定的每个同步性量度与先前确定的同步性量度进行比较。所述比较可以由控制电路80通过确定所述同步性量度的当前确定值和先前确定值之间的趋势或差异来进行。
如果当前确定的值代表心腔同步性的改善,如在框316处所确定的,则在框320处,控制电路80可以将AV间期调整到另一个测试间期。可以继续调整AV间期,直到基于框316处的确定未实现任何进一步的改善为止。如果量度的值与先前值相比有所增大或减小(这取决于所述量度是什么),则控制电路80可以确定同步性量度已被改善。例如,A1峰值幅度的增加可以指示心室同步性的改善,而A1宽度或面积的增加可以指示值的变差。如Vpace-A1、Vpace-A2或A1-A2时间间期等心室机械事件时间间期的增大可以指示与心室不同步性增加相关联的值的变差,而心室时间间期值的减小可以指示与心室同步性改善相关联的值的改善。
在当前确定的同步性量度值在框316处未被控制电路80确定为经改善的值并且未被确定为比先前值更差的值(例如,保持不变)时,在框320处,在搜索会使得同步性量度改善的AV间期时,控制电路80可以将AV间期调整到另一个测试设置。然而,当同步性量度值被确定为比先前值更差的值时,在框322处,可以将AV间期调整回先前的AV间期设置。所述先前的AV间期设置是对应于改善程度最大的同步性量度的设置(迄今为止),所述改善程度最大的同步性量度是相对于针对所有测试的AV间期所确定的其它同步性量度值而进行确定的。
应当认识到,当在AV间期调整期间监测两个或更多个同步性量度时,一个同步性量度可以充当对可能的AV间期设置以及可以在另一个同步性量度中实现的最大可能变化的约束。例如,举例来说,当A4-A1间期在最小界限处时,所述A4-A1间期可能受到所述最小界限的限制,使得AV间期不能进一步减小以改善A1幅度或A1宽度。在由最小A4-A1间期定义的AV间期界限内,可以优化(例如,最小化或最大化)可指示心室同步性的另一个同步性量度。
图8的过程可以由起搏器10在逐心跳的基础上执行,使得控制电路80可以视需要调整AV间期,以维持被监测的一个或多个同步性量度的改善。在其它实例中,流程图300的过程可以在经调度的、周期性的基础上执行,使得一旦基于实现经改善的同步性量度而找到最优AV间期时,就可以使用所述最优AV间期,直到流程图300的所述过程被调度为再次执行为止。在仍其它实例中,在心室起搏期间确定同步性量度并调整AV间期以达到所述同步性量度的改善或目标阈值或范围的过程可以在触发的基础上执行。
图9是根据一个实例的用于控制心室间起搏间期的方法的流程图350。如图3所示,起搏器10可以定位在右心室中,以使用远侧心室电极42提供LV起搏。可以在来自运动信号的感测到的A4信号之后或在RV和LV之间的心室间起搏间期之后以AV起搏间期递送LV起搏脉冲,以提供心脏再同步疗法。所述心室间起搏间期可以响应于感测到RV中的R波或响应于使用远侧基于壳体的电极22和近侧基于壳体的电极24来递送RV起搏脉冲而开始。在一些实例中,通过响应于从运动信号中感测到A4信号而开始AV间期来递送心房同步的双心室起搏,以将心室起搏脉冲递送到第一心室腔、RV或LV,然后响应于所述第一心室起搏脉冲而开始心室间起搏间期,以对从第二心室起搏脉冲到第二心室腔、LV或RV的递送进行定时。
在框351处,使用如上所述的示例技术中的任何一种技术通过控制电路80来建立目标同步性量度值。所述目标同步性量度值是心室同步性的指征。在框352处检测心房事件。所述心房事件可以是对应于机械心房收缩事件的A4信号。可以在A4信号的早期部分期间(例如,在A4信号峰之前)基于运动信号的A4感测阈值交叉检测所述心房事件,以开始AV起搏间期。可以基于如上所述的同步性量度对AV起搏间期进行调整,例如,基于A4-A1时间间期。所述A4-A1时间间期可以是从A4信号的结束时间到A1信号的开始的时间间期,以避免在所述A4信号结束之前开始心室收缩。作为实例,在返回到基线幅度、预先确定的结束时间阈值幅度的负走向交叉或低于预先确定的结束时间阈值幅度的预定数量的采样点时,可以检测A4信号的结束时间(例如,如图5所示,如结束时间115)。
在AV间期到期时,在框356处,通过疗法递送电路84将V1起搏脉冲递送到第一心室腔(右或左)。在框358处,控制电路80响应于第一V1起搏脉冲的递送而开始心室间起搏间期(V1-V2起搏间期)。在框360处,在V1-V2起搏间期到期时,通过疗法递送电路84将第二V2起搏脉冲递送到其它的、相对的心室腔(左或右)。在递送双心室起搏脉冲之后,在框362处,从运动信号中确定同步性量度。所述同步性量度可以是从A1和/或A2信号中确定的上文描述的实例中的任何一个,作为心室同步性的指标。通过控制电路80将所述同步性量度与目标值(或基于在框351处确定的目标值的阈值或范围)进行比较。如果所述同步性量度不满足同步性要求,则可以在框366处通过控制电路80调整V1-V2起搏间期。如果满足了应用在框364处的所述同步性要求,则控制电路80在框352处等待检测下一个心房事件,而不调整V1-V2起搏间期。图9的过程可以在逐心跳的基础上或更不频繁地进行重复,例如,每第n个心动周期、每分钟一次、每小时一次、每天一次或其它经调度的间期。应当认识到,在一些实例中,图7或图8的过程可以与图9的过程组合,以用于调整AV起搏间期和V1-V2起搏间期。
图10是用于通过起搏器10在触发的基础上执行起搏间期优化的方法的流程图400。在框402处,控制电路80检测触发事件,以基于至少一个同步性量度来优化起搏间期。被优化的起搏间期可以是AV起搏间期和/或心室间起搏间期。所述触发事件可以是心脏电信号的变化或心脏运动信号的变化。在一个实例中,控制电路80被配置成从自感测电路86接收的EGM信号监测R波回转率。R波的所述回转率的变化可以指示心室同步性的变化。例如,回转率的降低可以指示心室不同步性的增加。R波的可以由控制电路80检测为触发事件的其它变化可以包含R波峰值幅度的变化和/或R波宽度的变化。在另一个实例中,控制电路80可以监测A1信号的斜率或峰值幅度的变化。控制电路80可以通过检测R波回转率的变化,例如与先前确定的回转率或平均回转率相比下的降低,在框402处检测触发事件。另外地或可替代地,控制电路80可以通过检测与先前确定的特征值或平均值相比的A1信号斜率或峰值幅度或所述A1信号的其它特征的变化而在框402处检测触发事件。
当在框402处检测到触发事件时,在框404处,控制电路80确定在以当前设置的AV起搏间期和/或V1-V2起搏间期递送的心室起搏之后的一个或多个同步性量度。可以根据上文给出的实例中的任何一个实例来确定所述一个或多个同步性量度。在框406处,控制电路80将所述一个或多个同步性量度与相应的目标阈值或范围进行比较。如果所确定的同步性量度满足目标范围或阈值,则控制电路80返回到框402处以等待下一个触发事件。如果所述同步性量度不满足同步性量度目标范围或阈值,则控制电路80在框408处调整起搏间期,然后在框404处,以调整后的一个或多个起搏间期重新确定在一个或多个后续心室起搏脉冲之后的同步性量度。这一过程可以视需要继续进行多次起搏间期调整,以调整到AV和心室内起搏间期中的一者或两者,直到在框406处满足一个或多个同步性量度的一个或多个同步性量度目标范围或阈值为止。
在其它实例中,可以响应于检测触发事件(而不是调整起搏间期,直到满足先前建立的同步性量度目标阈值或范围为止)而启动图10的过程,控制电路80可以将一个或多个起搏间期调整到多个设置(或AV间期设置和V1-V2间期设置的组合),直到检测到所述同步性量度的改善为止,所述改善可以是所述AV间期设置和/或A4-A1间期的任何预定义的界限内和/或心室间起搏间期的上下界限内的最大改善。取决于所述同步性量度,所述同步性量度可以在AV间期、V1-V2间期和/或另一个同步性量度的任何预定义的界限内被最小化或最大化。
通过以下实施例描述了本公开的示例技术。
实施例1:一种方法,其包括:产生运动信号,所述运动信号包括心房收缩事件信号、对应于心室收缩开始的第一心室收缩事件信号和对应于心室收缩结束的第二心室收缩事件信号;在起搏间期到期时生成心室起搏脉冲;基于在所述心室起搏脉冲之后的所述第一心室收缩事件信号和所述第二心室收缩事件信号中的至少一个,从所述运动信号中确定同步性量度;以及基于所述同步性量度调整所述起搏间期。
实施例2:根据实施例1所述的方法,其进一步包括:将所述同步性量度确定为从所述心房收缩事件信号到所述第一心室收缩事件信号的时间间期;确定所述时间间期小于时间间期阈值;以及响应于所述时间间期小于所述时间间期阈值而增大所述起搏间期。
实施例3:根据实施例1或2所述的方法,其进一步包括:将所述同步性量度确定为结束于所述第一心室收缩事件和所述第二心室收缩事件之一的时间间期;确定所述时间间期大于阈值时间间期;以及响应于所述时间间期大于所述阈值时间间期而调整所述起搏间期,以减小所述同步性量度。
实施例4:根据实施例1到3中任一项所述的方法,其进一步包括:通过确定从所述第一心室收缩事件信号的第一峰到所述第一心室收缩事件信号的第二峰的时间间期来确定所述同步性量度;以及调整所述起搏间期以增大从所述第一峰到所述第二峰的所述时间间期。
实施例5:根据实施例1到4中任一项所述的方法,其进一步包括:感测伴随心室心肌的固有的去极化的固有的R波;从在所述固有的R波之后的所述运动信号中确定所述同步性量度的目标值;基于所述目标值设置所述同步性量度的阈值;确定所述同步性量度不满足所述阈值;以及响应于所述同步性量度不满足所述阈值而调整所述起搏间期。
实施例6:根据实施例1到5中任一项所述的方法,其进一步包括:感测伴随心室心肌的去极化的R波;检测所述R波的变化;以及响应于检测到所述R波的所述变化而从所述运动信号中确定所述同步性量度。
实施例7:根据实施例6所述的方法,其进一步包括通过检测所述R波的回转率的变化来检测所述R波的所述变化。
实施例8:根据实施例1到7中任一项所述的方法,其中:产生所述运动信号包括产生心房内运动信号,所述心房内运动信号包括所述心房收缩事件信号、所述第一心室收缩事件信号和所述第二心室收缩事件信号;以及在所述壳体被植入心房腔中时,通过多个基于壳体的电极递送所生成的心室起搏脉冲。
实施例9:根据实施例1到8中任一项所述的方法,其进一步包括:将所述起搏间期调整到多个设置;通过确定在以所述多个设置中的每一个设置递送的心室起搏脉冲之后的所述同步性量度来确定所述起搏间期的所述多个设置中的每一个设置的所述同步性量度;比较针对所述起搏间期的所述多个设置确定的所述同步性量度,基于所述比较,识别所述同步性量度中对应于所述同步性量度的最大改善的一个同步性量度;识别所述起搏间期的所述多个设置中对应于所述同步性量度的所述最大改善的一个设置;以及将所述起搏间期设置为所述起搏间期的所述多个设置中的一个经识别的设置。
实施例10:根据实施例1到9中任一项所述的方法,其中确定所述同步性量度包括:设置对应于所述第一心室收缩事件和所述第二心室收缩事件中的至少一个的时间窗口;识别在所述时间窗口期间所述运动信号的大于阈值幅度的采样点;以及从所述经识别的采样点的至少一部分中确定所述同步性量度。
实施例11:根据实施例1到10中任一项所述的方法,其中调整所述起搏间期包括调整心房心室起搏间期和心室间起搏间期中的至少一个。
实施例12:根据实施例1到11中任一项所述的方法,其进一步包括:感测伴随心房心肌的固有的去极化的固有的P波,通过设置心房心室起搏间期来设置所述起搏间期;响应于感测到所述固有的P波而从所述运动信号中确定第一同步性量度;通过基于所述第一同步性量度调整第一心房心室起搏间期来调整所述起搏间期;生成心房起搏脉冲;响应于所述所生成的心房起搏脉冲而从所述运动信号中确定第二同步性量度;以及基于所述第二同步性量度调整第二心房心室起搏间期。
实施例13:根据实施例1到12中任一项所述的方法,其进一步包括:生成被递送到第一心室起搏部位的第一心室起搏脉冲;响应于所述第一心室起搏脉冲被生成而开始心室间起搏间期;在所述心室间起搏间期到期时生成第二心室起搏脉冲,所述第二心室起搏脉冲被递送到第二心室起搏部位;在生成所述第二心室起搏脉冲之后从所述运动信号中确定所述同步性量度;以及通过基于所述同步性量度调整所述心室间起搏间期来调整所述起搏间期。
实施例14:根据实施例1到13中任一项所述的方法,其进一步包括:从所述运动信号中感测所述心房收缩事件;响应于感测到所述心房收缩事件而设置心房心室起搏间期;在所述心房心室起搏间期到期时生成第一心室起搏脉冲;响应于所述第一心室起搏脉冲被生成而设置心室间起搏间期;在所述心室间起搏间期到期时生成第二心室起搏脉冲;从所述第二心室起搏脉冲之后的所述运动信号中确定所述同步性量度;以及通过基于所述同步性量度调整所述心室间起搏间期来调整所述起搏间期。
实施例15:一种存储一组指令的非暂时性计算机可读存储介质,当由起搏器执行时,所述指令使所述起搏器:产生运动信号,所述运动信号包括心房收缩事件信号、对应于心室收缩开始的第一心室收缩事件信号和对应于心室收缩结束的第二心室收缩事件信号;在起搏间期到期时生成心室起搏;基于在所述心室起搏脉冲之后的所述第一心室收缩事件信号和所述第二心室收缩事件信号中的至少一个,从所述运动信号中确定同步性量度;以及基于所述同步性量度调整所述起搏间期。
应当理解,根据实例,本文所描述的方法中的任何一种方法的某些动作或事件可以按不同顺序执行,可被添加、合并或完全省略(例如,并非所有所描述的动作或事件对于实践所述方法来说都是必须的)。此外,在某些实例中,动作或事件可以例如通过多线程处理、中断处理或多个处理器同时地执行,而不是按顺序地执行。另外,虽然为了清楚起见,本公开的某些方面被描述为由单个电路或单元执行,但是应当理解,本公开的技术可以由与例如医疗装置相关联的单元、电路或处理器的组合来执行。
在一个或多个实例中,所描述的功能可以以硬件、软件、固件或其任何组合实施。如果以软件或固件实施,则可以将功能以一或多个指令或代码的形式存储在计算机可读介质上并且可以由基于硬件的处理单元执行所述功能。计算机可读介质可以包含非暂时性计算机可读存储介质,其对应于有形介质,如数据存储介质(例如,RAM、ROM、EEPROM、闪速存储器或可以用于存储呈指令或数据结构形式的期望程序代码并且可以由计算机访问的任何其它非暂时性介质)。
指令可以由一个或多个处理器执行,如一个或多个数字信号处理器(DSP)、通用微处理器、专用集成电路(ASIC)、现场可编程逻辑阵列(FPGA)或其它等效的集成或离散逻辑电路系统。因此,如本文所使用的,术语“处理器”可以指代任何前述结构或适于实施本文所描述的技术的任何其它结构。而且,所述技术可以完全实施在一个或多个电路或逻辑元件中。
因此,在前面的描述中已经参考具体实例呈现了起搏器。应当理解,本文公开的各个方面可以按与附图中呈现的具体组合不同的组合形式进行组合。应理解,在不脱离本公开的范围及所附权利要求书的情况下,可对参考实例进行各种修改。
本文用于企业家、创业者技术爱好者查询,结果仅供参考。