用于肺癌诊断的试剂盒、装置及方法
1.本技术为分案申请,其母案申请的申请号为202010391310.6,申请日为2020年05月11日,发明名称为“用于肺癌诊断的试剂盒、装置及方法”。
技术领域
2.本发明涉及医学诊断领域,具体涉及一种用于早期肺癌的诊断试剂盒、装置及方法。
背景技术:
3.肺癌是我国乃至全球主要癌种之一。根据2018年最新全球癌症统计数据,肺癌在所有癌种中发病率及致死率均居于首位。而根据2019年中国肿瘤登记数据,中国2015年新增390.2万癌症病例,癌症的死亡病例约为233.8万,其中肺癌是中国癌症死亡的主要原因。因此,为提升我国肺癌诊疗行为,改善肺癌患者预后,早期诊断成为肺癌诊治的重要问题。
4.随着低剂量螺旋ct的应用,越来越多的影像学表现为肺结节(肺间质内<3cm的单一病变、而且无相关的肺不张或淋巴结病)被发现。然而并非所有的肺结节都是恶性,肺结节良恶性鉴别一直以来是胸外科临床诊疗的难点。目前也有采用血浆循环肿瘤细胞、循环肿瘤游离dna等的无创检测手段,但其在早期肺癌诊断中检测的灵敏度并不高;因此,亟待开发一种高灵敏度的无创肺癌早期检测的方法。
技术实现要素:
5.本发明提供了一种基于外泌体的无创的早期肺癌诊断的试剂、装置和方法。
6.本发明一方面提供一种用于肺癌诊断的试剂盒,包括检测外泌体mirna标志物的引物和探针,所述外泌体mirna标志物包括let
‑
7a
‑
3p、let
‑
7f
‑
2、mir
‑
106b
‑
3p、mir
‑
10a
‑
3p、mir
‑
10a
‑
5p、mir
‑
125a
‑
5p、mir
‑
1294、mir
‑
19a
‑
3p、mir
‑
22
‑
3p、mir
‑
29a
‑
3p、mir
‑
30e
‑
5p、mir
‑
3158
‑
3p、mir
‑
330
‑
5p、mir
‑
3605
‑
3p、mir
‑
3615、mir
‑
378h、mir
‑
425
‑
3p、mir
‑
450b
‑
5p、mir
‑
4746
‑
5p、mir
‑
483
‑
3p、mir
‑
502
‑
3p、mir
‑
550a
‑
5p、mir
‑
651
‑
5p、mir
‑
7706、mir
‑
885
‑
5p中的一种或多种。
7.优选,所述外泌体mirna标志物为mir
‑
3615、mir
‑
502
‑
3p、mir
‑
450b
‑
5p、mir
‑
4746
‑
5p、mir
‑
10a
‑
5p、mir
‑
106b
‑
3p、mir
‑
125a
‑
5p、mir
‑
885
‑
5p中的一个或者多个组合。
8.优选,所述外泌体mirna标志物为mir
‑
106
‑
3p、mir
‑
125a
‑
5p、mir
‑
3615三者的组合。
9.优选,所述外泌体mirna标志物为mir
‑
106b
‑
3p、mir
‑
3615、mir
‑
450b
‑
5p三者的组合。
10.优选,所述外泌体mirna标志物为mir
‑
106b
‑
3p、mir
‑
125a
‑
5p、mir
‑
3615、mir
‑
450b
‑
5p、mir
‑
885
‑
5p五者的组合。
11.优选,所述外泌体mirna标志物为mir
‑
106b
‑
3p、mir
‑
10a
‑
3p、mir
‑
125a
‑
5p、mir
‑
3615、mir
‑
450b
‑
5p五者的组合。
12.优选,外泌体来源包括血液、唾液及痰液的一种或多种。
13.优选,所述引物和探针包括:
14.用于检测let
‑
7a
‑
3p的逆转录引物、pcr引物和探针:所述let
‑
7a
‑
3p的逆转录引物如序列号1所示的核苷酸序列,pcr上游引物如序列号2所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号3所示的核苷酸序列;
15.用于检测let
‑
7f
‑
2的逆转录引物、pcr引物和探针:所述let
‑
7f
‑
2的逆转录引物如序列号4所示的核苷酸序列,pcr上游引物如序列号5所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号6所示的核苷酸序列;
16.用于检测mir
‑
106b
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
106b
‑
3p的逆转录引物如序列号7所示的核苷酸序列,pcr上游引物如序列号8所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号9所示的核苷酸序列;
17.用于检测mir
‑
10a
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
10a
‑
3p的逆转录引物如序列号10所示的核苷酸序列,pcr上游引物如序列号11所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号12所示的核苷酸序列;
18.用于检测mir
‑
10a
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
10a
‑
5p的逆转录引物如序列号13所示的核苷酸序列,pcr上游引物如序列号14所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号15所示的核苷酸序列;
19.用于检测mir
‑
125a
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
125a
‑
5p的逆转录引物如序列号16所示的核苷酸序列,pcr上游引物如序列号17所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号18所示的核苷酸序列;
20.用于检测mir
‑
1294的逆转录引物、pcr引物和探针:所述mir
‑
1294的逆转录引物如序列号19所示的核苷酸序列,pcr上游引物如序列号20所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号21所示的核苷酸序列;
21.用于检测mir
‑
19a
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
19a
‑
3p的逆转录引物如序列号22所示的核苷酸序列,pcr上游引物如序列号23所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号24所示的核苷酸序列;
22.用于检测mir
‑
22
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
22
‑
3p的逆转录引物如序列号25所示的核苷酸序列,pcr上游引物如序列号26所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号27所示的核苷酸序列;
23.用于检测mir
‑
29a
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
29a
‑
3p的逆转录引物如序列号28所示的核苷酸序列,pcr上游引物如序列号29所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号30所示的核苷酸序列;
24.用于检测mir
‑
30e
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
30e
‑
5p的逆转录引物如序列号31所示的核苷酸序列,pcr上游引物如序列号32所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号33所示的核苷酸序列;
25.用于检测mir
‑
3158
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
3158
‑
3p的逆转录引物如序列号34所示的核苷酸序列,pcr上游引物如序列号35所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号36所示的核苷酸序列;
26.用于检测mir
‑
330
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
330
‑
5p的逆转录引
物如序列号37所示的核苷酸序列,pcr上游引物如序列号38所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号39所示的核苷酸序列;
27.用于检测mir
‑
3605
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
3605
‑
3p的逆转录引物如序列号40所示的核苷酸序列,pcr上游引物如序列号41所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号42所示的核苷酸序列;
28.用于检测mir
‑
3615的逆转录引物、pcr引物和探针:所述mir
‑
3615的逆转录引物如序列号43所示的核苷酸序列,pcr上游引物如序列号44所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号45所示的核苷酸序列;
29.用于检测mir
‑
378h的逆转录引物、pcr引物和探针:所述mir
‑
378h的逆转录引物如序列号46所示的核苷酸序列,pcr上游引物如序列号47所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号48所示的核苷酸序列;
30.用于检测mir
‑
425
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
425
‑
3p的逆转录引物如序列号49所示的核苷酸序列,pcr上游引物如序列号50所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号51所示的核苷酸序列;
31.用于检测mir
‑
450b
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
450b
‑
5p的逆转录引物如序列号52所示的核苷酸序列,pcr上游引物如序列号53所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号54所示的核苷酸序列;
32.用于检测mir
‑
4746
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
4746
‑
5p的逆转录引物如序列号55所示的核苷酸序列,pcr上游引物如序列号56所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号57所示的核苷酸序列;
33.用于检测mir
‑
483
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
483
‑
3p的逆转录引物如序列号58所示的核苷酸序列,pcr上游引物如序列号59所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号60所示的核苷酸序列;
34.用于检测mir
‑
502
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
502
‑
3p的逆转录引物如序列号61所示的核苷酸序列,pcr上游引物如序列号62所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号63所示的核苷酸序列;
35.用于检测mir
‑
550a
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
550a
‑
5p的逆转录引物如序列号64所示的核苷酸序列,pcr上游引物如序列号65所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号66所示的核苷酸序列;
36.用于检测mir
‑
651
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
651
‑
5p的逆转录引物如序列号67所示的核苷酸序列,pcr上游引物如序列号68所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号69所示的核苷酸序列;
37.用于检测mir
‑
7706的逆转录引物、pcr引物和探针:所述mir
‑
7706的逆转录引物如序列号70所示的核苷酸序列,pcr上游引物如序列号71所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号72所示的核苷酸序列;
38.用于检测mir
‑
885
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
885
‑
5p的逆转录引物如序列号73所示的核苷酸序列,pcr上游引物如序列号74所示的核苷酸序列,下游引物如序列号80所示的核苷酸序列,探针如序列号75所示的核苷酸序列。
39.本发明另一方面提供一种用于肺癌诊断的装置,包括检测外泌体mirna标志物的
试剂,所述外泌体mirna标志物包括let
‑
7a
‑
3p、let
‑
7f
‑
2、mir
‑
106b
‑
3p、mir
‑
10a
‑
3p、mir
‑
10a
‑
5p、mir
‑
125a
‑
5p、mir
‑
1294、mir
‑
19a
‑
3p、mir
‑
22
‑
3p、mir
‑
29a
‑
3p、mir
‑
30e
‑
5p、mir
‑
3158
‑
3p、mir
‑
330
‑
5p、mir
‑
3605
‑
3p、mir
‑
3615、mir
‑
378h、mir
‑
425
‑
3p、mir
‑
450b
‑
5p、mir
‑
4746
‑
5p、mir
‑
483
‑
3p、mir
‑
502
‑
3p、mir
‑
550a
‑
5p、mir
‑
651
‑
5p、mir
‑
7706、mir
‑
885
‑
5p中的一种或多种。
40.本发明另一方面提供一种用于肺癌诊断的方法,包括检测外泌体mirna标志物的特异性,所述外泌体mirna标志物包括let
‑
7a
‑
3p、let
‑
7f
‑
2、mir
‑
106b
‑
3p、mir
‑
10a
‑
3p、mir
‑
10a
‑
5p、mir
‑
125a
‑
5p、mir
‑
1294、mir
‑
19a
‑
3p、mir
‑
22
‑
3p、mir
‑
29a
‑
3p、mir
‑
30e
‑
5p、mir
‑
3158
‑
3p、mir
‑
330
‑
5p、mir
‑
3605
‑
3p、mir
‑
3615、mir
‑
378h、mir
‑
425
‑
3p、mir
‑
450b
‑
5p、mir
‑
4746
‑
5p、mir
‑
483
‑
3p、mir
‑
502
‑
3p、mir
‑
550a
‑
5p、mir
‑
651
‑
5p、mir
‑
7706、mir
‑
885
‑
5p中的一种或多种。
41.本发明提供了一种基于外泌体的无创的肺癌诊断的方法,在肺癌中具有高灵敏度及高特异性,为肺癌的早期诊断及复发监控提供了重要价值。对我国肺癌的防治有很大的帮助。更进一步,其中5个mirna标志物(联合auc最高可达0.951,其阴性预测值为90.32%、灵敏度为90.00%、特异性为93.33%),具有极其优越的诊断性能。
附图说明
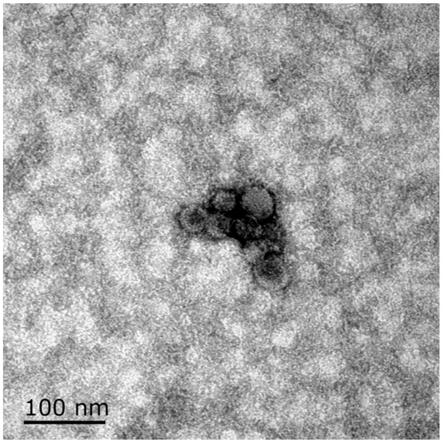
42.图1是外泌体电镜鉴定结果。
43.图2是mir
‑
3615单独检测肺癌的roc曲线。
44.图3是mir
‑
502
‑
3p单独检测肺癌的roc曲线。
45.图4是mir
‑
450b
‑
5p单独检测肺癌的roc曲线。
46.图5是mir
‑
4746
‑
5p单独检测肺癌的roc曲线。
47.图6是mir
‑
10a
‑
5p单独检测肺癌的roc曲线。
48.图7是mir
‑
106
‑
3p mir
‑
125a
‑
5p mir
‑
3615组合检测肺癌的roc曲线。
49.图8是mir
‑
106b
‑
3p mir
‑
3615 mir
‑
450b
‑
5p组合检测肺癌的roc曲线。
50.图9是mir
‑
106b
‑
3p mir
‑
125a
‑
5p mir
‑
3615 mir
‑
450b
‑
5p mir
‑
885
‑
5组合检测肺癌的roc曲线。
51.图10是mir
‑
106b
‑
3p mir
‑
10a
‑
3p mir
‑
125a
‑
5p mir
‑
3615 mir
‑
450b
‑
5p组合检测肺癌的roc曲线。
52.图11是mir
‑
106b
‑
3p mir
‑
10a
‑
5p mir
‑
125a
‑
5p mir
‑
3615 mir
‑
450b
‑
5p组合检测肺癌的roc曲线(以u6为参照)。
具体实施方式
53.细胞外囊泡(extracellular vesicles,evs;以下囊泡均代表细胞外囊泡)是指从细胞膜上脱落或由细胞分泌的具有双层膜结构的囊泡状小体,直径从30
‑
1000nm不等,胞外囊泡主要由微囊泡(microvesicles,mvs)和外泌体(exosomes)组成,微囊泡是细胞激活或损伤后从细胞膜脱落的小囊泡。由于细胞外囊泡独特的生物学特征,其在疾病诊断中有着重要的意义,特别是其中的外泌体。
54.外泌体是一种由细胞内多泡体与细胞膜融合后分泌到细胞外环境中粒径介于30
~150nm的膜性小囊泡,是细胞间信息传递的重要媒介,在抗原呈递、细胞凋亡、炎症反应、肿瘤发生发展及转移过程中发挥了重要作用。其在体液中分布广泛,包括血液、唾液、尿液、乳汁和胸腹水等;包含dna、rna及蛋白质等多种内含物,可以作为肿瘤等多种疾病的无创诊断标志物。而mirna则是外泌体中含量最为丰富的核酸组分,因而外泌体mirna具备作为肺癌早期诊断的潜力。
55.本发明提供的试剂盒、装置和方法,以通过实验研究发现在患有早期肺癌患者的外泌体中呈现显著差异表达的mirna中的一种或多种作为诊断早期肺癌的标志物。
56.显著差异表达的mirna包括:let
‑
7a
‑
3p、let
‑
7f
‑
2、mir
‑
106b
‑
3p、mir
‑
10a
‑
3p、mir
‑
10a
‑
5p、mir
‑
125a
‑
5p、mir
‑
1294、mir
‑
19a
‑
3p、mir
‑
22
‑
3p、mir
‑
29a
‑
3p、mir
‑
30e
‑
5p、mir
‑
3158
‑
3p、mir
‑
330
‑
5p、mir
‑
3605
‑
3p、mir
‑
3615、mir
‑
378h、mir
‑
425
‑
3p、mir
‑
450b
‑
5p、mir
‑
4746
‑
5p、mir
‑
483
‑
3p、mir
‑
502
‑
3p、mir
‑
550a
‑
5p、mir
‑
651
‑
5p、mir
‑
7706、mir
‑
885
‑
5p。
57.在一些优选的实施方案中,显著差异表达的mirna分子标志物联合使用,其中较优的组合是:mir
‑
3615、mir
‑
502
‑
3p、mir
‑
450b
‑
5p、mir
‑
4746
‑
5p、mir
‑
10a
‑
5p、mir
‑
106b
‑
3p、mir
‑
125a
‑
5p、mir
‑
885
‑
5p中的一个或者多个组合。上述组合可为肺癌的早期诊断提供更好的依据,预示疾病风险。
58.另外,本发明的用于肺癌诊断的试剂盒包括检测上述外泌体mirna标志物的引物和探针。检测外泌体mirna标志物的引物和探针包括:
59.用于检测let
‑
7a
‑
3p的逆转录引物、pcr引物和探针:所述let
‑
7a
‑
3p的逆转录引物如序列号1所示的核苷酸序列,pcr上游引物具体如序列号2所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号3所示的核苷酸序列;
60.用于检测let
‑
7f
‑
2的逆转录引物、pcr引物和探针:所述let
‑
7f
‑
2的逆转录引物如序列号4所示的核苷酸序列,pcr上游引物具体如序列号5所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号6所示的核苷酸序列;
61.用于检测mir
‑
106b
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
106b
‑
3p的逆转录引物如序列号7所示的核苷酸序列,pcr上游引物具体如序列号8所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号9所示的核苷酸序列;
62.用于检测mir
‑
10a
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
10a
‑
3p的逆转录引物如序列号10所示的核苷酸序列,pcr上游引物具体如序列号11所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号12所示的核苷酸序列;
63.用于检测mir
‑
10a
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
10a
‑
5p的逆转录引物如序列号13所示的核苷酸序列,pcr上游引物具体如序列号14所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号15所示的核苷酸序列;
64.用于检测mir
‑
125a
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
125a
‑
5p的逆转录引物如序列号16所示的核苷酸序列,pcr上游引物具体如序列号17所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号18所示的核苷酸序列;
65.用于检测mir
‑
1294的逆转录引物、pcr引物和探针:所述mir
‑
1294的逆转录引物如序列号19所示的核苷酸序列,pcr上游引物具体如序列号20所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号21所示的核苷酸序列;
66.用于检测mir
‑
19a
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
19a
‑
3p的逆转录引
物如序列号22所示的核苷酸序列,pcr上游引物具体如序列号23所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号24所示的核苷酸序列;
67.用于检测mir
‑
22
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
22
‑
3p的逆转录引物如序列号25所示的核苷酸序列,pcr上游引物具体如序列号26所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号27所示的核苷酸序列;
68.用于检测mir
‑
29a
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
29a
‑
3p的逆转录引物如序列号28所示的核苷酸序列,pcr上游引物具体如序列号29所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号30所示的核苷酸序列;
69.用于检测mir
‑
30e
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
30e
‑
5p的逆转录引物如序列号31所示的核苷酸序列,pcr上游引物具体如序列号32所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号33所示的核苷酸序列;
70.用于检测mir
‑
3158
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
3158
‑
3p的逆转录引物如序列号34所示的核苷酸序列,pcr上游引物具体如序列号35所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号36所示的核苷酸序列;
71.用于检测mir
‑
330
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
330
‑
5p的逆转录引物如序列号37所示的核苷酸序列,pcr上游引物具体如序列号38所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号39所示的核苷酸序列;
72.用于检测mir
‑
3605
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
3605
‑
3p的逆转录引物如序列号40所示的核苷酸序列,pcr上游引物具体如序列号41所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号42所示的核苷酸序列;
73.用于检测mir
‑
3615的逆转录引物、pcr引物和探针:所述mir
‑
3615的逆转录引物如序列号43所示的核苷酸序列,pcr上游引物具体如序列号44所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号45所示的核苷酸序列;
74.用于检测mir
‑
378h的逆转录引物、pcr引物和探针:所述mir
‑
378h的逆转录引物如序列号46所示的核苷酸序列,pcr上游引物具体如序列号47所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号48所示的核苷酸序列;
75.用于检测mir
‑
425
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
425
‑
3p的逆转录引物如序列号49所示的核苷酸序列,pcr上游引物具体如序列号50所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号51所示的核苷酸序列;
76.用于检测mir
‑
450b
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
450b
‑
5p的逆转录引物如序列号52所示的核苷酸序列,pcr上游引物具体如序列号53所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号54所示的核苷酸序列;
77.用于检测mir
‑
4746
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
4746
‑
5p的逆转录引物如序列号55所示的核苷酸序列,pcr上游引物具体如序列号56所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号57所示的核苷酸序列;
78.用于检测mir
‑
483
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
483
‑
3p的逆转录引物如序列号58所示的核苷酸序列,pcr上游引物具体如序列号59所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号60所示的核苷酸序列;
79.用于检测mir
‑
502
‑
3p的逆转录引物、pcr引物和探针:所述mir
‑
502
‑
3p的逆转录引
物如序列号61所示的核苷酸序列,pcr上游引物具体如序列号62所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号63所示的核苷酸序列;
80.用于检测mir
‑
550a
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
550a
‑
5p的逆转录引物如序列号64所示的核苷酸序列,pcr上游引物具体如序列号65所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号66所示的核苷酸序列;
81.用于检测mir
‑
651
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
651
‑
5p的逆转录引物如序列号67所示的核苷酸序列,pcr上游引物具体如序列号68所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号69所示的核苷酸序列;
82.用于检测mir
‑
7706的逆转录引物、pcr引物和探针:所述mir
‑
7706的逆转录引物如序列号70所示的核苷酸序列,pcr上游引物具体如序列号71所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号72所示的核苷酸序列;
83.用于检测mir
‑
885
‑
5p的逆转录引物、pcr引物和探针:所述mir
‑
885
‑
5p的逆转录引物如序列号73所示的核苷酸序列,pcr上游引物具体如序列号74所示的核苷酸序列,下游引物具体如序列号80所示的核苷酸序列,探针如序列号75所示的核苷酸序列;
84.用于检测内参u6的逆转录引物、pcr引物和探针:所述u6的逆转录引物如序列号78所示的核苷酸序列,pcr上游引物具体如序列号76所示的核苷酸序列,下游引物具体如序列号78所示的核苷酸序列,探针如序列号79所示的核苷酸序列。引物和探针的核苷酸序列如表1所示。
85.表1
86.87.[0088][0089]
进一步地,外泌体来源包括血液、唾液及痰液的一种或多种。
[0090]
本发明的试剂盒、装置和方法适用个体可以为肺癌高危的人群、正常个体及肺癌术后的患者。
[0091]
下面结合实施案例对本发明的技术方案进行完整清晰的描述,所描述的实施例是本发明一部分实施例,而不是全部的实例。基于本发明的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的其他实施例,都属于本发明保护的范围。
[0092]
下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0093]
为了筛选到与结肺癌诊断相关的外泌体标志物,早期肺癌患者50例和对照各72例,取血液不少于10ml并分离血浆,用于经典超速离心方法分离血浆中的外泌体并提取rna,得到的rna分别进行rna建库测序。得到的数据进行生物信息学的分析,比较早期肺癌患者及对照中差异表达的rna。这些来自外泌体的mrna层面标志物可以用于肺癌早期诊断。
[0094]
进一步的针对其中rna标志物进应用分析,其方法所述如下:(1)采集待检测个体的体液样本(包括血液、痰液和唾液);(2)分离体液中的外泌体;(3)spkin外参cel
‑
mir
‑
39提取外泌体rna;(4)利用两步法检测目标rna表达水平;(5)使用外参基因对检测目标rna的
表达水平进行归一化;(6)将归一化后的基因表达水平代入判定模型得到输出值;(7)根据模型的输出值及判定阈值对待测个体是否为肺癌。
[0095]
试剂盒包括检测外泌体rmina标志物的pcr引物、探针、标准品及逆转加pcr的两步法检测体系。
[0096]
包括选用外参cel
‑
mir
‑
39或者内参u6进行目标rna的定量。其中选用参照时目标rna的定量根据检测ct值使用定量公式2δδct计算标志物的表达水平。得到目标rna表达水平后,使用roc特征曲线和auc来评估单个rna或联合多个rna检测肺癌的准确度。
[0097]
实施例1基于高通量测序筛选与早期肺癌相关的外泌体mirna标志物
[0098]
为了筛选到与早期肺癌诊断相关的外泌体标志物,早期肺癌诊断患者72和对照各50例,取血液不少于10ml并分离血浆,用于经典超速离心方法分离血浆中的外泌体并采用qiagen mirneasy mini kit提取rna,得到的rna进行small rna建库测序。得到的数据进行生物信息学的分析,比较早期肺癌患者及对照中差异表达的mirna,得到显著差异的mirna如下表2所示。这些来自外泌体的rna层面标志物可以用于肺癌早期诊断。
[0099]
表2
[0100]
[0101]
[0102][0103]
实施例2基于荧光定量pcr平台mirna检测体系
[0104]
1、mirna逆转录反应体系
[0105]
mirna反转录试剂、酶和oligdt从takara采购,标准品从上海英潍捷基合成,特异性反转的引物由苏州泓迅合成。采用20ul的反转录体系,如下表3所示。
[0106]
表3
[0107]
[0108][0109]
2、pcr反应体系
[0110]
pcr反应混合液从takara采购,上游引物、探针即通用下游引物由苏州泓迅合成、荧光定量pcr仪为abi 7500。pcr反应体系,如下表4所示。
[0111]
表4
[0112][0113]
pcr程序为95℃10min,(95℃15s;55℃30s)15个循环不采集荧光,(95℃15s;55℃30s)35个循环采集荧光。
[0114]
实施例3以外参cel
‑
mir
‑
39为参照单标志物肺癌早期诊断检测效果评估
[0115]
1、样本采集
[0116]
收集经医院确诊的早期(i期和ii期)肺结节肺癌患者,良性肺结节病人、健康人等对照样本的血液10ml,并分离成血浆。
[0117]
2、外泌体rna提取
[0118]
采用超速离心或echobiotech(北京恩泽康泰)的exosupur进行血浆外泌体分离(外泌体电镜鉴定结果如图1),分离后的外泌体用qiagen mireasy mini kit试剂盒提取外泌体中的mirna,并利用agilent 2100检测rna浓度和质量,记录rna浓度。
[0119]
3、rna两步法检测体系
[0120]
采用实施例1中基于pcr平台mirna的两步法检测体系,对早期肺癌病人30例和30例对照样本(健康人和良性结节)的血浆外泌体mirna进行检测,检测目标mirna的ct值,根据ct值和相对定量公式计算相对表达量。
[0121]
4、外泌体mirna诊断早期肺癌性能评估
[0122]
(1)mir
‑
3615单独检测性能评估
[0123]
如图2所示,对早期肺癌病人30例和30例对照样本(健康人和良性病变)的血浆外泌体,检测mir
‑
3615的ct值,以外参cel
‑
mir
‑
39为参照,根据ct值,得出mirna的拷贝数。使用相对定量公式值,计算联合标志物相对表达量的倍数变化,进而得出rna相对表达量。对检测结果采用r语言进行t检测分析pvalue=0.00058<=0.05,说明外泌体mir
‑
3615与早期肺癌显著相关。mir
‑
3615单独诊断早期肺癌的auc为0.785,其阴性预测值为85%、灵敏度为
90%、特异性为56.57%,具有诊断标志物的潜力。
[0124]
(2)mir
‑
502
‑
3p单独检测性能评估
[0125]
如图3所示,对早期肺癌病人30例和30例对照样本(健康人和良性病变)的血浆外泌体,检测mir
‑
502
‑
3p的ct值,以外参cel
‑
mir
‑
39为参照,根据ct值,得出mirna的拷贝数。使用相对定量公式值,计算联合标志物相对表达量的倍数变化,进而得出rna相对表达量。对检测结果采用r语言进行t检测分析pvalue=0.00139<=0.05,说明外泌体mir
‑
502
‑
3p与早期肺癌显著相关。mir
‑
502
‑
3p单独诊断早期肺癌的auc为0.756,其阴性预测值为68.42%、灵敏度为60%、特异性为86.67%,具有诊断标志物的潜力。
[0126]
(3)mir
‑
450b
‑
5p单独检测性能评估
[0127]
如图4所示,对早期肺癌病人30例和30例对照样本(健康人和良性病变)的血浆外泌体,检测mir
‑
450b
‑
5p的ct值,以外参cel
‑
mir
‑
39为参照,根据ct值,得出mirna的拷贝数。使用相对定量公式值,计算联合标志物相对表达量的倍数变化,进而得出rna相对表达量。对检测结果采用r语言进行t检测分析pvalue=0.00199<=0.05,说明外泌体mir
‑
450b
‑
5p与早期肺癌显著相关。mir
‑
450b
‑
5p单独诊断早期肺癌的auc为0.744,其阴性预测值为80%、灵敏度为86.67%、特异性为53.33%,具有诊断标志物的潜力。
[0128]
(4)mir
‑
4746
‑
5p单独检测性能评估
[0129]
如图5所示,对早期肺癌病人30例和30例对照样本(健康人和良性病变)的血浆外泌体,检测mir
‑
4746
‑
5p的ct值,以外参cel
‑
mir
‑
39为参照,根据ct值,得出mirna的拷贝数。使用相对定量公式值,计算联合标志物相对表达量的倍数变化,进而得出rna相对表达量。对检测结果采用r语言进行t检测分析pvalue=0.00183<=0.05,说明外泌体mir
‑
4746
‑
5p与早期肺癌显著相关。mir
‑
4746
‑
5p单独诊断早期肺癌的auc为0.743,其阴性预测值为66.67%、灵敏度为60%、特异性为80%,具有诊断标志物的潜力。
[0130]
(5)mir
‑
10a
‑
5p单独检测性能评估
[0131]
如图6所示,对早期肺癌病人30例和30例对照样本(健康人和良性病变)的血浆外泌体,检测mir
‑
10a
‑
5p的ct值,以外参cel
‑
mir
‑
39为参照,根据ct值,得出mirna的拷贝数。使用相对定量公式值,计算联合标志物相对表达量的倍数变化,进而得出rna相对表达量。对检测结果采用r语言进行t检测分析pvalue=0.00183<=0.05,说明外泌体mir
‑
10a
‑
5p与早期肺癌显著相关。mir
‑
10a
‑
5p单独诊断早期肺癌的auc为0.73,其阴性预测值为77.27%、灵敏度为83.33%、特异性为56.67%,具有诊断标志物的潜力。
[0132]
(6)其他与早期肺癌显著相关的标志物性能评估
[0133]
其他显著相关的mirna性能评估如下表5所示。
[0134]
表5
[0135]
[0136]
[0137][0138]
从表5所示数据可以看出表中所述的mirna均具有诊断标志物的潜力。
[0139]
实施例4以外参cel
‑
mir
‑
39为参照多标志物组合肺癌早期诊断检测效果评估
[0140]
1、三标志物组合性能评估
[0141]
按照实施例3中的方法计算每个mirna的相对表达量,利用逻辑回归对三个标志物组合进行训练,得到的三标志物组合auc在0.85以上的组合如下表6所示。其中mir
‑
106
‑
3p mir
‑
125a
‑
5p mir
‑
3615、mir
‑
106b
‑
3p mir
‑
3615 mir
‑
450b
‑
5p等两个组合性能最优,auc分别为0.887和0.881,其auc曲线分别如图7和图8所示。
[0142]
表6
[0143]
[0144][0145]
2、五标志物组合性能评估
[0146]
按照实施例3中的方法计算每个mirna的相对表达量,利用逻辑回归对五个标志物组合进行训练,得到的五标志物组合auc在0.93以上的组合如下表7所示。其中mir
‑
106b
‑
3p mir
‑
125a
‑
5p mir
‑
3615 mir
‑
450b
‑
5p mir
‑
885
‑
5p、mir
‑
106b
‑
3p mir
‑
10a
‑
3p mir
‑
125a
‑
5p mir
‑
3615 mir
‑
450b
‑
5p等两个组合性能最优,auc分别为0.951和0.948,其auc曲线分别如图9和图10所示。
[0147]
表7
[0148]
[0149][0150]
实施例5以内参u6为参照多标志物组合肺癌早期诊断检测效果评估
[0151]
按照实施例3中的方法计算以u6为参照每个mirna的相对表达量,利用逻辑回归对五个标志物组合进行训练,得到的五标志物组合auc在85以上的组合如下表8所示。其中mmir
‑
106b
‑
3p mir
‑
10a
‑
5p mir
‑
125a
‑
5p mir
‑
3615 mir
‑
450b
‑
5p组合性能最优,auc为0.864,其auc曲线分别如图11所示。
[0152]
表8
[0153][0154][0155]
通过以上数据可以看出,本发明的基于外泌体mirna标志的肺癌检测方法,可以实现肺癌的无创诊断,为肺癌的早期诊断及复发监控提供了重要价值,对我国肺癌的防治有很大的帮助。其中5个mirna标志物(联合auc最高可达0.951,其阴性预测值为90.32%、灵敏度为90.00%、特异性为93.33%),具有极其优越的诊断性能。
[0156]
以上公开的本发明优选实施例只是用于帮助阐述本发明。优选实施例并没有详尽叙述所有的细节,也不限制该发明仅为所述的具体实施方式。显然,根据本说明书的内容,
可作很多的修改和变化。本说明书选取并具体描述这些实施例,是为了更好地解释本发明的原理和实际应用,从而使所属技术领域技术人员能很好地理解和利用本发明。本发明仅受权利要求书及其全部范围和等效物的限制。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。