1.本发明涉及酸法合成多酚类化合物的技术领域,具体涉及一种酸法合成多羟基酚类化合物的方法。
背景技术:
[0002]4‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚和4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚产品均为一种多羟基酚类物质,是重要工业材料,可用于微电子集成电路工业的光致抗蚀剂、医药中间体、紫外线吸收剂、光引发剂、染料等领域;在微电子工业方面主要是用作紫外正性光刻胶的感光剂中间体。该类物质在国内外开发研究相对较少。随着光敏剂、光致抗蚀剂、光引发剂等产品用量的攀升,该类物质合成方法的发现对光敏剂领域的进一步研究有较大意义。
[0003]
日本专利jph037240a阐述了4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚的一种合成方法。该方法使用4
‑
异丙烯基苯酚与邻苯三酚在三氯化铝的催化下合成4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚。该方法在合成过程中使用到了三氯化铝,三氯化铝在潮湿环境中不稳定,易发生水解;在投料过程中粉尘较大,对环境、人员健康都不理想。三氯化铝在后处理过程中需要用水进行淬灭,由此产生了较大的废水,给环保带来较大压力。该专利在合成过程中使用了非质子性溶剂使用量较大,成本压力相对较大。此外,该文献报道的合成方法收率不高,产品竞争优势不大。
[0004]
而4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚的合成方法在国内外报道相对较少,仅在部分文献中将其作为原料,在制备光敏剂的过程中被提及。
[0005]
因此,寻找一种操作简单,对环境污染小,经济实用,且又符合微电子电路产品的制造要求的4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚或4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚的合成方法成为目前噬待解决的新课题。
技术实现要素:
[0006]
基于上述背景技术,本发明的目的在于提供一种酸法合成多羟基酚类化合物的方法,该方法具有制备方法简单、对环境污染小、对设备要求低,合成过程中无金属离子的引入或使用,合成得到的产品符合微电子电路产品的制造要求等特点。
[0007]
本发明采用以下的技术方案:
[0008]
一种酸法合成多羟基酚类化合物的方法,包括以下步骤:
[0009]
将4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚加入与之互溶的溶剂中,所述溶剂为质子性溶剂或非质子性溶剂;
[0010]
使用酸性催化剂进行催化反应;
[0011]
将反应后所得反应液经过萃取、浓缩、析晶等后处理程序即可得到多羟基酚类化合物。
[0012]
作为其中的一个实施例,所述多羟基酚类化合物为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙
基]邻苯三酚或4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚。
[0013]
作为其中的一个实施例,当所述多羟基酚类化合物为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚时,所述4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体以4
‑
异丙烯基苯酚计,与邻苯三酚的摩尔比为1:0.1
‑
0.5;
[0014]
当所述多羟基酚类化合物为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚时,所述4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体以4
‑
异丙烯基苯酚计,与邻苯三酚的摩尔比为1:2
‑
10。(后续出现的4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体均以4
‑
异丙烯基苯酚计)。
[0015]
上述技术方案中,4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚的摩尔比不同可分别得到4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚与4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚。
[0016]
当所述多羟基酚类化合物为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚时,4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚的摩尔比为1:0.1
‑
0.5;优选地,4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚的摩尔比为1:0.3
‑
0.5;进一步优选地,4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚的摩尔比为1:0.4
‑
0.5。
[0017]
当所述多羟基酚类化合物为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚时,4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚的比例为1:2
‑
10;优选地,4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚的比例为1:2
‑
5;进一步优选地,4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚的比例为1:2
‑
2.5。
[0018]
另外,当所述多羟基酚类化合物为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚时,邻苯三酚与4
‑
异丙烯基苯酚及其线性二聚体的摩尔比不可过高,邻苯三酚过多则产生的杂质较多,主要杂质为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚;邻苯三酚过少,则会造成4
‑
异丙烯基苯酚及其线性二聚体的浪费;所以将二者的摩尔比控制在一定范围内,才可得到良好的试验结果。
[0019]
当所述多羟基酚类化合物为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚时,邻苯三酚与4
‑
异丙烯基苯酚及其线性二聚体的摩尔比不可过低,邻苯三酚过少则产生的杂质较多,主要杂质为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚;邻苯三酚过多,则会造成邻苯三酚的浪费;所以将二者的摩尔比控制在一定范围内,才可得到良好的试验结果。
[0020]
作为其中的一个实施例,当所述多羟基酚类化合物为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚时,所述催化反应的反应温度为20
‑
40℃;
[0021]
当所述多羟基酚类化合物为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚时,所述催化反应的反应温度为40
‑
80℃。
[0022]
上述技术方案中,由于摩尔比不同,温度不同,则生成不同产品:4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚或4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚。
[0023]
作为其中的一个实施例,当所述多羟基酚类化合物为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚时,所述催化反应的反应时间为0.5
‑
3h;
[0024]
当所述多羟基酚类化合物为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚时,所述催化反应的反应时间为2
‑
3h。
[0025]
上述技术方案中,强酸催化剂进行催化反应时,反应的速度较快,但为了充分反应,则需适当延长反应时间。
[0026]
作为其中的一个实施例,所述溶剂与4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体的质量比为60
‑
5:1。
[0027]
上述技术方案中,所述溶剂与4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体的质量比为60:1;优选地,所述溶剂与4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体的质量比为30:1;更优选地,所述溶剂与4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体的质量比为5
‑
10:1。
[0028]
作为其中的一个实施例,所述质子性溶剂为醇类溶剂;所述非质子性溶剂为脂类溶剂、芳香性有机溶剂或卤代有机溶剂。
[0029]
上述技术方案中,所述质子性溶剂,包括各种醇类,如甲醇、乙醇、异丙醇、二恶烷等。所述非质子性溶剂包括各种脂类,如乙酸乙酯、乙酸丁酯、甲酸乙酯、乙酸甲酯等;各种芳香性有机溶剂,如甲苯、二甲苯等;各种卤代有机溶剂,如二氯甲烷、二氯乙烷、氯仿等。
[0030]
作为其中的一个实施例,所述酸性催化剂为硫酸、硝酸、盐酸、甲磺酸、三氟乙酸、对甲苯磺酸中的一种或多种。
[0031]
上述技术方案中,强酸催化剂可以为硫酸(浓度10
‑
98%)、硝酸(10
‑
68%)、盐酸(10
‑
36%)、甲磺酸、三氟乙酸、对甲苯磺酸等。
[0032]
作为其中的一个实施例,所述酸性催化剂与邻苯三酚的质量比为1:8
‑
20。
[0033]
作为其中的一个实施例,萃取所用溶剂为与多羟基酚类化合物相溶的有机溶剂。
[0034]
本发明具有的有益效果是:
[0035]
本发明提出了一种酸法合成多羟基酚类化合物的方法,使用4
‑
异丙烯基苯酚和/或4
‑
异丙烯基苯酚线性二聚体与邻苯三酚在酸性催化剂的作用下,调整二者之间的摩尔比,即可制备得到不同的多羟基化合物;所述多羟基酚类化合物为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚或4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚;本发明具有合成方法简单、所用原料少、对设备要求低、环境污染小等特点;制备得到的4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚或4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚符合微电子电路产品的制造的要求,能够广泛应用于符合微电子电路产品的制造要求的原料领域。
附图说明
[0036]
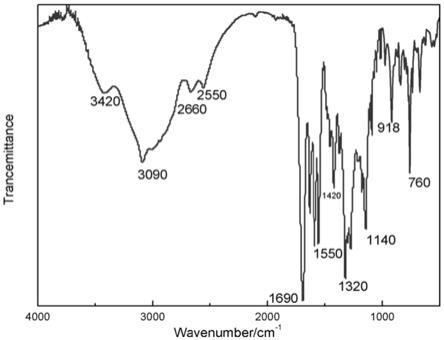
图1为实施例1
‑
7所制得的4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚核磁图谱;
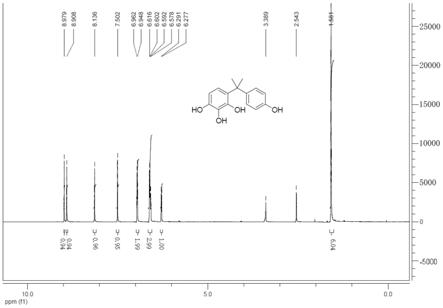
[0037]
图2为实施例8
‑
11所制得的4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚核磁图谱。
具体实施方式
[0038]
需要说明的是本发明4
‑
异丙烯基苯酚线性二聚体可以以双酚a为起始原料,经高温裂解后得到。下面结合具体实施例对本发明进行具体的说明:
[0039]
实施例1
[0040]
取20g 4
‑
异丙烯基苯酚与其二聚体溶解在200g乙酸乙酯中,搅拌20min;加入40g邻苯三酚,20
‑
25℃下加入盐酸5g;25℃保温2h;浓缩乙酸乙酯,加入二氯乙烷200g,过滤,滤
饼用200g乙酸乙酯溶解,用水溶液萃取3次,300ml/次;萃取完毕,50℃
‑
55℃下浓缩乙酸乙酯,得到油状物(或固体),加入200g二氯甲烷,降温至0
‑
5℃搅拌析晶,过滤,60℃下干燥,得产品27.2g,收率67%。液相含量99.5%。其核磁图谱h
‑
nmr(400mhz,dmso)见图1所示。产品为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚。
[0041]
实施例2
[0042]
取20g 4
‑
异丙烯基苯酚与其二聚体溶解在200g乙酸乙酯中,搅拌20min;加入40g邻苯三酚,20
‑
25℃下加入甲磺酸1g;20℃保温2h;所得乙酸乙酯溶液用水萃取3次,300ml/次;萃取完毕,50℃
‑
55℃下浓缩乙酸乙酯,得到油状物(或固体),加入200g二氯甲烷,降温至0
‑
5℃搅拌析晶,过滤,60℃下干燥,得产品24.1g,收率62%。液相含量98.7%。产品为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚。
[0043]
实施例3
[0044]
取20g 4
‑
异丙烯基苯酚与其二聚体溶解在200g甲醇中,搅拌20min;加入40g邻苯三酚,20
‑
25℃下加入浓硫酸0.5g;30℃保温2h;所得甲醇溶液,在50℃下浓缩至干,加入乙酸乙酯200g,用水溶液萃取3次,萃取完毕,50
‑
55℃下浓缩乙酸乙酯,得到油状物(或固体),加入200g二氯甲烷,降温至0
‑
5℃搅拌析晶,过滤,60℃下干燥,得产品22.1g,收率57%。液相含量98.3%。产品为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚。
[0045]
实施例4
[0046]
取20g 4
‑
异丙烯基苯酚与其二聚体溶解在200g乙酸乙酯中,搅拌20min;加入60g邻苯三酚(邻苯三酚比例增大),20
‑
25℃下加入盐酸5g;25℃保温2h;浓缩乙酸乙酯,加入二氯乙烷200g,过滤,滤饼用200g乙酸乙酯溶解,用水溶液萃取3次,300ml/次;萃取完毕,50℃
‑
55℃下浓缩乙酸乙酯,得到油状物(或固体),加入200g二氯甲烷,降温至0
‑
5℃搅拌析晶,过滤,60℃下干燥,得产品26.4g,收率65%。液相含量99.3%。产品为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚。
[0047]
实施例5
[0048]
取20g 4
‑
异丙烯基苯酚与其二聚体溶解在200g乙酸乙酯中,搅拌20min;加入40g邻苯三酚,20
‑
25℃下加入盐酸5g;15℃保温8h(温度降低);浓缩乙酸乙酯,加入二氯乙烷200g,过滤,滤饼用200g乙酸乙酯溶解,用水溶液萃取3次,300ml/次;萃取完毕,50℃
‑
55℃下浓缩乙酸乙酯,得到油状物(或固体),加入200g二氯甲烷,降温至0
‑
5℃搅拌析晶,过滤,60℃下干燥,得产品18.8g,收率46.3%。液相含量78.6%。产品为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚。
[0049]
实施例6
[0050]
取20g 4
‑
异丙烯基苯酚与其二聚体溶解在200g乙酸乙酯中,搅拌20min;加入40g邻苯三酚,20
‑
25℃下加入盐酸5g;65℃保温3h(温度升高);浓缩乙酸乙酯,加入二氯乙烷200g,过滤,滤饼用200g乙酸乙酯溶解,用水溶液萃取3次,300ml/次;萃取完毕,50℃
‑
55℃下浓缩乙酸乙酯,得到油状物(或固体),加入200g二氯甲烷,降温至0
‑
5℃搅拌析晶,过滤,60℃下干燥,得产品17.7g,收率43.6%。液相含量67.8%。产品为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚。
[0051]
实施例7
[0052]
取20g 4
‑
异丙烯基苯酚与其二聚体溶解在1200g乙酸乙酯中(增大溶剂用量),搅
拌20min;加入40g邻苯三酚,20
‑
25℃下加入盐酸5g;65℃保温3h;浓缩乙酸乙酯,加入二氯乙烷200g,过滤,滤饼用200g乙酸乙酯溶解,用水溶液萃取3次,300ml/次;萃取完毕,50℃
‑
55℃下浓缩乙酸乙酯,得到油状物(或固体),加入200g二氯甲烷,降温至0
‑
5℃搅拌析晶,过滤,60℃下干燥,得产品21.5g,收率53%。液相含量98.6%。产品为4
‑
[1
‑
(4
‑
羟苯基)
‑1‑
甲基
‑
乙基]邻苯三酚。
[0053]
实施例8
[0054]
取40g 4
‑
异丙烯基苯酚与其二聚体溶解在400g二氧六环中,搅拌20min;加入17g邻苯三酚,加入盐酸浓3g;45℃保温2h;浓缩,所得油状物加入乙酸乙酯400g,用水溶液萃取3次,萃取完毕,浓缩,得到油状物,加入200g氯仿,降温至0
‑
5℃搅拌析晶过夜;过滤,60℃下干燥,得产品37.63g,收率73%(邻苯三酚计)。其核磁图谱h
‑
nmr(400mhz,dmso)见图2所示。产品为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚。
[0055]
实施例9
[0056]
取40g 4
‑
异丙烯基苯酚与其二聚体溶解在100g乙酸乙酯中,搅拌20min;加入16.5g邻苯三酚,40℃下加入甲磺酸1g;保温2h;所得乙酸乙酯溶液用水萃取3次;萃取完毕,浓缩乙酸乙酯,得到油状物(或固体),加入200g二氯甲烷,降温至0
‑
5℃搅拌析晶过夜;过滤,60℃下干燥,得产品33.54g,收率65%。产品为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚。
[0057]
实施例10
[0058]
取40g 4
‑
异丙烯基苯酚与其二聚体溶解在200g甲醇中,搅拌20min;加入16g邻苯三酚,加入浓硫酸0.5g;50℃保温2h;浓缩,所得油状物加入乙酸乙酯200g,用水溶液萃取3次,萃取完毕,浓缩乙酸乙酯,得到油状物(或固体),加入200g氯仿,降温至0
‑
5℃搅拌析晶过夜;过滤,60℃下干燥,得产品34.4g,收率68.8%。产品为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚。
[0059]
实施例11
[0060]
取40g 4
‑
异丙烯基苯酚与其二聚体溶解在400g二氧六环中,搅拌20min;加入17g邻苯三酚,加入苯乙烯型强酸性离子交换树脂15g;45℃保温2h;降温,过滤,50g二氧六环洗涤,浓缩,得到油状物,加入200g乙酸乙酯,纯化水萃取3次,400ml/次;萃取完毕,浓缩至干,加入二甲苯200g,降温至0
‑
5℃搅拌析晶过夜;过滤,60℃下干燥,得产品37.2g,收率70%(邻苯三酚计)。产品为4,6
‑
双[1
‑
(4
‑
羟苯基)
‑1‑
甲基乙基]
‑
1,2,3
‑
苯三酚。
[0061]
当然,上述说明并非是对本发明的限制,本发明也并不仅限于上述举例,本技术领域的技术人员在本发明的实质范围内所做出的变化、改型、添加或替换,也应属于本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。