通用逆转录引物及mirna的cdna合成方法、合成试剂盒和mirna检测方法
技术领域
1.本发明属于分子生物学技术领域,具体涉及一种通用逆转录引物及mirna的cdna合成方法、合成试剂盒和mirna检测方法,尤其涉及一种同时适用于sda(链置换恒温扩增)和pcr检测mirna体系的用于mirna合成cdna的通用逆转录引物及mirna的cdna合成方法、cdna合成试剂盒和mirna检测方法。
背景技术:
2.mirna是一类由18
‑
24个核苷酸组成的非编码单链rna,广泛参与动物、植物等真核生物基因的调控。多项研究表明,循环mirna是一类与肿瘤发生密切相关的分子标志物,通过定量检测患者血清或血浆中循环mirna的表达水平,能够实现癌症的早期筛查和预后监测(参见例如铁轶等人,循环microrna与肿瘤诊断,中国科学,2009,第39卷第1期:64
‑
68)。
3.目前,rt
‑
qpcr是实时定量检测mirna的常用技术手段之一,通过加尾逆转录合成cdna后,可以实现对mirna分子的检测,参见例如专利文献cn105177132a和cn110804656a等。然而,pcr方法需要连续变温才能实现mirna靶标的有效扩增,这对检测设备的性能提出了较高的要求,并且适用于pcr检测mirna的cdna的合成方法兼容性较差,仅能适用于pcr检测原理。近年来,随着等温扩增技术的快速发展,这种在恒定温度下即可实现核酸分子有效扩增的新技术受到了广泛关注。研究发现,等温扩增技术,如链置换恒温扩增(sda)特别适合mirna这类序列较短、单链rna的检测,能够在30~60分钟内,将mirna靶标放大109倍以上。然而,目前尚未有可以用于sda检测mirna的cdna合成方法的报道,更没有可以同时满足sda等温扩增和pcr变温扩增检测mirna的cdna合成方法,这在一定程度上限制了sda等温扩增技术在mirna检测中的应用。
技术实现要素:
4.针对现有技术中存在的一个或多个问题,本发明一个方面提供一种通用逆转录引物,用于对mirna进行cdna合成,所述通用逆转录引物的核苷酸序列由以下通式(i)表示:
5.r
‑
(dt)
n
‑
vn
ꢀꢀꢀ
(i)
6.其中,r为所述通用逆转录引物的5’端序列,其核苷酸序列如seq id no:1所示;vn为所述通用逆转录引物的3’端序列,其中v表示腺嘌呤残基、鸟嘌呤残基或胞嘧啶残基,n表示腺嘌呤残基、鸟嘌呤残基、胞嘧啶残基或胸腺嘧啶残基;(dt)
n
为所述通用逆转录引物的中间部分,表示n个连续的胸腺嘧啶残基,其中n为8
‑
20内的任意整数。
7.在一个优选的实施方式中,上述通用逆转录引物的核苷酸序列如seq id no:2所示。
8.本发明另一方面提供一种mirna的cdna合成方法,其包括在同一反应体系和同一反应条件下进行的以下反应步骤:
9.s1:mirna加poly(a)尾反应:以mirna为靶标,以atp为反应原料,在poly(a)聚合酶
的催化下,进行加poly(a)尾反应;
10.s2:逆转录合成cdna反应:以步骤s1获得的已加poly(a)尾的mirna为靶标,利用上述的通用逆转录引物,在逆转录酶的催化下,合成cdna。
11.上述cdna合成方法中,所述反应体系包含:10
‑
100mm tris
‑
hcl ph 8.3、20
‑
100mm nacl、10
‑
100mm kcl、1
‑
20mm mgcl2、5
‑
50mm dtt、1
‑
20nm上述的通用逆转录引物、0.1
‑
1mm atp、0.1
‑
5u/μl poly(a)聚合酶、5
‑
50u/μl逆转录酶、0.1
‑
1.0mm dntp;优选为:20
‑
60mm tris
‑
hcl ph 8.3、30
‑
60mm nacl、20
‑
60mm kcl、5
‑
15mm mgcl2、10
‑
30mm dtt、5
‑
10nm上述的通用逆转录引物、0.3
‑
0.7mm atp、0.25
‑
2.5u/μl poly(a)聚合酶、5
‑
20u/μl amv逆转录酶、0.4
‑
0.8mm dntp;所述反应条件为:37℃
‑
42℃保温20
‑
60min,65℃
‑
90℃保温5
‑
20min。
12.本发明另一方面还提供一种mirna的cdna合成试剂盒,其包含上述的通用逆转录引物。
13.上述的cdna合成试剂盒还包含用于进行mirna合成cdna反应的成分:atp、poly(a)聚合酶、逆转录酶、dntp和反应缓冲液,其中所述反应缓冲液包含tris
‑
hcl ph 8.3、nacl、kcl、mgcl2和dtt;优选地,所述cdna合成试剂盒在使用时各成分在cdna合成反应体系中的浓度分别为:10
‑
100mm tris
‑
hcl ph 8.3、20
‑
100mm nacl、10
‑
100mm kcl、1
‑
20mm mgcl2、5
‑
50mm dtt、1
‑
20nm上述的通用逆转录引物、0.1
‑
1mm atp、0.1
‑
5u/μl poly(a)聚合酶、5
‑
50u/μl逆转录酶、0.1
‑
1.0mm dntp。
14.本发明再一方面还提供一种通用扩增反向引物,其核苷酸序列由以下通式(ii)表示:
15.p
‑
r
ꢀꢀꢀ
(ii)
16.其中,p为所述通用扩增反向引物的5’端序列,表示切刻内切酶的酶切位点及其保护性碱基,其中所述切刻内切酶的酶切位点选自seq id no:3、seq id no:4、seq id no:5和seq id no:6中的任一种;r为所述通用扩增反向引物的3’端序列,其核苷酸序列如seq id no:1所示;优选地,所述通用扩增反向引物的核苷酸序列如seq id no:7、seq id no:8、seq id no:9和seq id no:10中的任一种所示。该通用扩增反向引物用于以cdna为模板的sda等温扩增或pcr变温扩增反应体系中进行cdna的扩增,其中所述cdna利用上述的通用逆转录引物由mirna合成获得。
17.本发明再一方面还提供一种多核苷酸,其用于上述的通用逆转录引物或通用扩增反向引物中,所述多核苷酸的核苷酸序列如seq id no:1所示。该多核苷酸的存在使得由通用逆转录引物合成的cdna可以用于sda等温扩增体系和pcr变温扩增体系中作为扩增模板,或使得通用扩增反向引物可以用于sda等温扩增体系和pcr变温扩增体系中作为扩增模板的反向引物,并且适用于利用上述通用逆转录引物由任意mirna合成的cdna的扩增。
18.本发明再一方面还提供一种定量检测mirna的方法,其在上述的cdna合成方法的基础上还包括:
19.s3:以步骤s2逆转录合成的cdna为模板进行rt
‑
sda和/或rt
‑
pcr定量检测;其中用于扩增cdna模板的反向引物为上述的通用扩增反向引物。
20.本发明再一方面还提供一种mirna检测试剂盒,其包含上述的通用逆转录引物和通用扩增反向引物。
21.上述mirna可以是任意类型的mirna,例如选自以下中的一种或多种:真核生物的
循环mirna、组织mirna、总rna和人工合成的mirna分子。
22.基于以上技术方案提供的通用逆转录引物的5’端为适用于sda等温扩增和pcr变温扩增的通用扩增引物结合序列,3’端为识别位点通用碱基序列,两者之间为与mirna的poly(a)尾互补的poly(t)碱基序列,因此基于该通用逆转录引物提供的mirna的cdna合成方法和合成试剂盒合成获得的cdna不仅适用于sda等温检测mirna的体系,还可适用于pcr变温检测mirna的体系,可以实现sda等温和pcr变温同时检测同一mirna的目的,两者的结果可相互验证,有利于mirna的精确定量,进而有效提高mirna定量结果的准确性。另一方面,本发明提供的cdna合成方法可在同一反应体系中和同一反应条件下同步实现mirna加poly(a)尾和逆转录的反应,整个反应时间较短,并且反应体系简单,可以实现快速合成cdna的目的,有利于提高mirna的检测效率。再一方面,本发明提供的mirna检测方法中可以使用一条基于本发明提供的通用逆转录引物设计的通用扩增反向引物,该通用扩增反向引物的使用不以检测的mirna的改变而发生变化,因此在检测不同的mirna时,无需另外合成新的反向引物,可以提高检测效率并节约检测成本。
附图说明
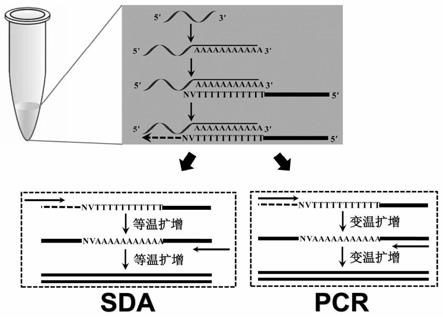
23.图1为本发明的一个实施例中的同时适用于sda和pcr检测mirna的cdna合成方法的反应原理示意图;
24.图2为利用本发明的一个实施例合成的cdna为模板在sda和pcr检测方法中的扩增曲线,其中a幅表示以合成的cdna为模板在sda检测方法中的扩增曲线,b幅表示以合成的cdna为模板在pcr检测方法中的扩增曲线。
具体实施方式
25.针对现有技术中仍缺乏适用于sda(例如rt
‑
sda)检测mirna的cdna合成方法,尤其是缺乏同时适用于sda和pcr(例如rt
‑
pcr)检测mirna的cdna合成方法的技术缺陷,本发明旨在提供一种适用于sda检测mirna的cdna合成方法,尤其提供一种可同时适用于sda和pcr检测mirna的cdna合成方法,并且提供了用于该cdna合成方法中将mirna逆转录成cdna的通用逆转录引物和cdna合成试剂盒,基于提供的cdna合成方法,还提供了可适用于sda检测原理的mirna检测方法,尤其是可同时适用于sda和pcr检测原理的mirna检测方法以及可用于提供的mirna检测方法的通用扩增反向引物和mirna检测试剂盒。
26.具体地,本发明提供一种适用于sda检测mirna的cdna合成方法,尤其提供一种同时适用于sda和pcr检测mirna的cdna合成方法,其技术原理如图1所示,该cdna合成方法包括在同一反应体系和同一反应条件下的两个反应步骤:(1)mirna靶标在poly(a)聚合酶的催化下,以5
’‑
三磷酸腺苷(atp)为反应原料,进行poly(a)加尾反应;和(2)已加poly(a)尾的mirna序列与poly(t)逆转录引物(即通用逆转录引物)结合(通过已加poly(a)尾的mirna序列中的poly(a)序列与通用逆转录引物中的poly(t)序列互补结合),并在逆转录酶的催化下,逆转录合成cdna。其中在以上cdna合成方法中使用的反应体系包括以下成分:poly(t)逆转录引物(即通用逆转录引物)、5
’‑
三磷酸腺苷(atp)、poly(a)聚合酶、逆转录酶(可以为amv逆转录酶、m
‑
mulv逆转录酶、protoscript ii逆转录酶中的一种或多种)、反应缓冲液(包含tris
‑
hcl(ph 8.3)、nacl、kcl、mgcl2、dtt(二硫苏糖醇))和dntp。反应条件为:37
℃
‑
42℃保温20
‑
60min,随后65℃
‑
90℃保温5
‑
20min结束反应。作为靶标的mirna可在以上反应体系和反应条件下同步发生上述的poly(a)加尾反应和逆转录反应,进而合成cdna。其中在逆转录反应中使用的通用逆转录引物的核苷酸序列如以下通式(i)表示:
27.r
‑
(dt)
n
‑
vn
ꢀꢀꢀ
(i)
28.在通式(i)中,r为通用逆转录引物的5’端序列,其核苷酸序列为同时适用于sda等温扩增和pcr变温扩增的通用扩增引物结合序列(cagtcgtcgcaccctcc,seq id no:1);3’端为由vn表示的核苷酸残基组成,作为识别位点通用碱基序列,其中v表示腺嘌呤残基a、鸟嘌呤残基g或胞嘧啶残基c,n表示腺嘌呤残基a、鸟嘌呤残基g、胞嘧啶残基c或胸腺嘧啶残基t;(dt)
n
为通用逆转录引物的中间部分,表示n个连续的胸腺嘧啶残基,其中n可为数值8
‑
20以内的任意整数(包括端点值),优选为12,即上述通用逆转录引物的核苷酸序列优选为cagtcgtcgcaccctccttttttttttttvn(seq id no:2)。
29.由于以上通式(i)表示的通用逆转录引物中包含可同时适用于sda等温扩增和pcr变温扩增的通用扩增引物结合序列(seq id no:1),根据图1所示的技术原理,可知由已加poly(a)尾的mirna序列逆转录获得的第一链cdna(即根据mirna模板第一步得到的单链dna)序列中也含有该通用扩增引物结合序列(seq id no:1),则通过以上方法合成的第一链cdna既可作为sda等温扩增体系中的模板,又可以作为pcr变温扩增体系中的模板,并且该cdna模板在扩增体系中正向引物的引导下扩增的模板互补链中含有与seq id no:1互补的序列片段,因此在sda等温扩增体系和pcr变温扩增体系中可以使用一条通用扩增反向引物,该通用扩增反向引物的3’端序列设计为seq id no:1,可以使得该通用扩增反向引物与扩增体系中由正向引物扩增获得的模板互补链互补结合,进而引导反向扩增。另一方面,为了扩增的延续性(即为了切割形成的双链cdna以获得单链模板),该通用扩增反向引物的5’端设计为包含切刻内切酶的酶切位点及其保护性碱基,其中根据使用的切刻内切酶的不同,可选择的酶切位点包括:gagtc(seq id no:3,nt.bstnbi的酶切位点)、ggatc(seq id no:4,nt.alwi的酶切位点)、gtctc(seq id no:5,nt.bsmai的酶切位点)和gctcttc(seq id no:6,nt.bspqi的酶切位点)。由此,在由以上通式(i)表示的通用逆转录引物合成的cdna作为sda等温扩增体系或pcr变温扩增体系中的模板时,在两者的扩增体系中可以使用由以下通式(ii)表示的核苷酸序列作为通用扩增反向引物来检测任意mirna:
30.p
‑
r
ꢀꢀꢀ
(ii)
31.在通式(ii)中,p为通用扩增反向引物的5’端序列,为切刻内切酶的酶切位点及其保护性碱基,其中切刻内切酶的酶切位点可以选用seq id no:3至seq id no:6中的任一种,酶切位点的保护性碱基可以根据酶切切点的类型而常规选择,这对于本领域普通技术人员是熟知的;r为通用扩增反向引物的3’端序列,其核苷酸序列如seq id no:1所示。优选地,由通式(ii)表示的通用扩增反向引物的核苷酸序列如以下seq id no:7至seq id no:10中任一种所示:
32.33.以上序列seq id no:7至seq id no:10中,单下划线部分表示切刻内切酶的酶切位点,双下划线部分表示seq id no:1,其他部分为酶切位点的保护性碱基。
34.以下结合具体实施例,对本发明进一步阐述。应当理解的是,具体实施例仅用于进一步说明本发明,而不是用于限制本发明的内容。
35.下述实施例中所用方法如无特别说明均为常规方法。具体步骤可参见:《分子克隆实验指南》(《molecular cloning:a laboratory manual》sambrook,j.,russell,david w.,molecular cloning:a laboratory manual,3rd edition,2001,ny,cold spring harbor)。
36.实施例中描述到的各种生物材料的取得途径仅是提供一种实验获取的途径以达到具体公开的目的,不应成为对本发明生物材料来源的限制。事实上,所用到的生物材料的来源是广泛的,任何不违反法律和道德伦理能够获取的生物材料都可以按照实施例中的提示替换使用。下述实施例中所用的实验材料如无特殊说明,均为常规生化试剂,可通过商业途径购买得到。
37.本发明提供的方法适用于任意类型的mirna,包括人类、动物、植物等所有真核生物的天然mirna分子,例如循环mirna、组织mirna、总rna中的一种或多种,还可包括任何人工合成的mirna分子。以下实施例中以人工合成的mir
‑
21分子标准品(uagcuuaucagacugauguuga,seq id no:11)为例来描述本发明的方法。
38.以下实施例中涉及的序列均可使用已有技术合成。
39.实施例1:mirna的cdna合成方法
40.该实施例利用人工合成的mir
‑
21标准品为样品,根据图1所示的技术原理构建其可同时适用于sda和pcr检测mirna的cdna合成方法,具体为按照以下要求配制20μl反应体系:mir
‑
21分子标准品50pm,atp 1.0μl(终浓度为0.5mm),poly(a)聚合酶5u(终浓度为0.25u/μl),反应缓冲液2.0μl(终浓度分别为:50mm tris
‑
hcl(ph 8.3)、50mm nacl、50mm kcl、5mm mgcl2、10mm dtt),amv逆转录酶100u(终浓度为5u/μl),poly(t)逆转录引物(seq id no:2)1.0μl(终浓度为5nm),0.5mm dntp,补充水至20μl。在37℃保温30min,随后85℃保温5min的反应条件下,该20μl反应体系中同步发生以下两个反应:
41.1.1)mir
‑
21加poly(a)尾反应:以mir
‑
21分子为靶标,以atp为反应原料,在poly(a)聚合酶的催化下,进行mir
‑
21加poly(a)尾反应;和
42.1.2)逆转录合成cdna反应:以步骤1.1)获得的已加poly(a)尾的mir
‑
21分子为靶标,以dntp为原料,利用poly(t)逆转录引物在amv逆转录酶的催化下,合成cdna。
43.由于在逆转录合成cdna反应中使用的poly(t)逆转录引物中含有同时适用于sda等温扩增和pcr变温扩增的通用扩增引物结合序列(seq id no:1),根据图1所示的技术原理可知合成获得的第一链cdna中也含有该通用扩增引物结合序列(seq id no:1),因此合成的cdna也可以同时适用于sda等温扩增体系和pcr变温扩增体系中作为扩增模板,进而可以使用sda等温和pcr变温检测方法定量检测mir
‑
21,将通过以下实施例2验证。
44.实施例2:mir
‑
21的rt
‑
sda等温和rt
‑
pcr变温检测
45.该实施例利用上述实施例1合成的mir
‑
21的cdna作为模板,使用sda和pcr方法对其进行实时定量检测,以验证本发明提供的cdna合成方法的有效性和在sda等温和pcr变温检测体系中的兼容性,具体包括以下操作。
46.2.1)按照以下体系配制用于rt
‑
sda等温扩增的20μl反应体系:实施例1合成的mir
‑
21的cdna模板1μl,终浓度为1.25mm的正向引物(cggttggagtccttgttagcttatcagactg(seq id no:12)),终浓度为1.25mm反向引物(seq id no:7),反应缓冲液2.0μl(终浓度分别为:50mm tris
‑
hcl(ph 8.3)、50mm nacl、50mm kcl、5mm mgcl2、10mm dtt),终浓度为0.5mm的dntp,终浓度为0.1u/μl的dna聚合酶,终浓度为0.2u/μl的核酸内切酶(nt.bstnbi),1
×
eva green染料1μl,补充水至20μl,并按照以下扩增程序对实施例1获得的cdna进行扩增:55℃保温40min,每间隔一分钟采集一次荧光信号,共计40次,作为阳性组,同时设置阴性组(扩增体系中未添加cdna模板)。sda等温扩增结果如图2中a幅所示。
47.2.2)按照以下体系配制用于rt
‑
pcr变温扩增的20μl反应体系:实施例1合成的mir
‑
21的cdna模板1μl,终浓度为1.25mm的正向引物(seq id no:12),终浓度为1.25mm反向引物(seq id no:7),反应缓冲液2.0μl(终浓度分别为:50mm tris
‑
hcl(ph 8.3)、50mm nacl、50mm kcl、5mm mgcl2、10mm dtt),终浓度为0.5mm的dntp,终浓度为0.1u/μl的dna聚合酶,终浓度为0.2u/μl的核酸内切酶(nt.bstnbi),1
×
eva green染料1μl,补充水至20μl,并按照以下扩增程序对实施例1获得的cdna进行扩增:95℃加热10s;95℃加热5s,52℃加热20s,72℃加热20s,共计40个循环,每个循环结束后采集一次荧光信号,共计40次,作为阳性组,同时设置阴性组(扩增体系中未添加cdna模板)。pcr变温扩增结果如图2中b幅所示。
48.根据图2中a幅和b幅所示的结果,可见rt
‑
sda等温扩增和rt
‑
pcr变温扩增试验中阳性组均出现有效的扩增曲线,且阴性组均未出现扩增信号,表明本发明提供的cdna合成方法能够实现从mirna到cdna的有效合成,并且合成的cdna可以同时适用于sda等温扩增和pcr变温扩增,表明本发明建立的cdna合成方法的兼容性较高,可以同时为sda等温扩增和pcr变温扩增提供扩增所需的cdna模板。另一方面,由于在本发明提供的cdna合成方法中使用的通用逆转录引物5’端的通用扩增引物结合序列(seq id no:1)的兼容化结构设计,使得包含seq id no:1的引物(seq id no:7至seq id no:10)可以作为以合成的cdna为扩增模板的sda等温扩增和pcr变温扩增体系中的通用扩增反向引物。
49.实施例3:cdna合成试剂盒和mirna检测试剂盒
50.基于以上实施例1和实施例2的结果,本发明还提供可以用于以上实施例1中由mirna合成其cdna的cdna合成试剂盒,以及用于以上实施例2中以合成的cdna作为扩增模板检测mirna的mirna检测试剂盒。
51.提供的cdna合成试剂盒可包含由通式(i)表示的通用逆转录引物,优选为如seq id no:2所示的通用逆转录引物。提供的cdna合成试剂盒还可包含在本发明提供的cdna合成方法中同步进行poly(a)加尾反应和逆转录合成cdna反应的成分:atp、poly(a)聚合酶、逆转录酶、dntp和反应缓冲液,其中所述反应缓冲液包含tris
‑
hcl ph 8.3、nacl、kcl、mgcl2和dtt。这些成分在使用时的浓度分别为:1
‑
20nm poly(t)引物(即通用逆转录引物),0.1
‑
1mm atp,0.1
‑
5u/μl poly(a)聚合酶、5
‑
50u/μl逆转录酶、0.1
‑
1.0mm dntp和反应缓冲液(10
‑
100mm tris
‑
hcl(ph 8.3),20
‑
100mm nacl,10
‑
100mm kcl,1
‑
20mm mgcl2,5
‑
50mm dtt),优选为20
‑
60mm tris
‑
hcl ph 8.3、30
‑
60mm nacl、20
‑
60mm kcl、5
‑
15mm mgcl2、10
‑
30mm dtt、5
‑
10nm poly(t)引物、0.3
‑
0.7mm atp、0.25
‑
2.5u/μl poly(a)聚合酶、5
‑
20u/μl逆转录酶、0.4
‑
0.8mm dntp;其中逆转录酶可为amv、m
‑
mulv、protoscript ii中的一种或多种。使用该cdna合成试剂盒进行mirna的cdna合成时,同步进行poly(a)加尾反应和逆转录
合成cdna反应的反应条件可为:37℃
‑
42℃保温20
‑
60min,随后65℃
‑
90℃保温5
‑
20min。
52.提供的mirna检测试剂盒则可包含由通式(i)表示的通用逆转录引物,优选为如seq id no:2所示的通用逆转录引物;还可包含由通式(ii)表示的用于扩增cdna的通用扩增反向引物,优选为如seq id no:7至seq id no:10中的任一种所示的通用扩增反向引物。
53.最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。