用于产生糖蛋白、鉴定糖基化途径的平台
1.关于联邦资助的研究或开发的声明
2.本发明是在国防威胁减少局授予的hdtra1
‑
15
‑1‑
0052/p00001下在政府支持下完成的。政府对本发明享有一定的权利。
3.相关申请的交叉引用
4.本技术根据35 u.s.c.
§
119(e)要求2019年1月25日提交的美国临时申请号62/796,773的优先权,其内容通过引用整体并入本文。
5.发明背景
6.本发明总体上涉及用于糖蛋白蛋白质合成的组分、系统和方法。特别地,本发明涉及用于产生糖蛋白和鉴定糖基化途径的模块化平台。本文公开的组分、系统和方法可用于在无细胞蛋白质合成(cfps)和经修饰的细胞中合成糖蛋白和重组糖蛋白。
7.糖基化调节蛋白质治疗剂和疫苗的药代动力学和效力。大多数糖蛋白合成的方法使用真核生物体(通常是哺乳动物细胞,例如中国仓鼠卵巢(cho)细胞)内的天然途径。然而,这些方法导致聚糖异质性,限制了生物制造宿主的选择,并对已知严重影响蛋白质特性的糖基化结构提供有限的控制,尤其是对于蛋白质治疗剂。这些限制推动了工程化或合成的糖基化系统的开发,无论是通过真核生物(通常是酵母或cho细胞)、细菌系统的细胞工程化还是体外的。其中,在细菌中或体外构建的合成的糖基化系统提供了最密切控制糖基化模式和更快速地开发更多样化糖基化模式的机会。细菌宿主的使用还可以实现更具成本效益的生物制造。
8.已经开发了几种细菌系统来产生蛋白质疫苗或糖基化治疗剂。然而,这些合成的糖基化系统的开发仍然缓慢,因为它需要在活细胞中构建和测试酶的集合(生物合成途径)。因此,细菌中产生的糖基化结构通常局限于可以通过表达自然界中发现的完整操纵子来合成的那些,这严重限制了可以构建的结构的多样性,从而限制了该技术可以用于的应用的多样性。
9.在此,发明人公开了一种与通过快速体外混合和表达进行糖基化途径组装(glycoprime)的模块化无细胞平台相关的技术。使用该技术,发明人已经发现了几种新的生物合成途径,其可用于在体外或在活细胞中产生糖蛋白治疗剂、疫苗和分析标准品。
技术实现要素:
10.公开了用于在体外和体内的糖蛋白蛋白质合成的组分、系统和方法。特别地,所公开的组分、系统和方法涉及用于产生糖蛋白的模块化平台。本文公开的组分、系统和方法可用于在无细胞蛋白质合成(cfps)和经修饰的细胞中合成糖蛋白和重组糖蛋白。
11.所公开的组分、系统和方法通常包括或利用可溶性或任选不溶性(例如膜结合的)n
‑
连接的糖基转移酶(n
‑
糖基转移酶,或ngt)以将葡萄糖部分转移至存在于肽、多肽或蛋白质中的接受者肽序列。所公开的组分、系统和方法还可以包括或利用额外的可溶性或任选不溶性(例如膜结合的)糖基转移酶以修饰n
‑
连接的葡萄糖部分并提供更复杂的n
‑
连接的聚糖。
12.附图简述
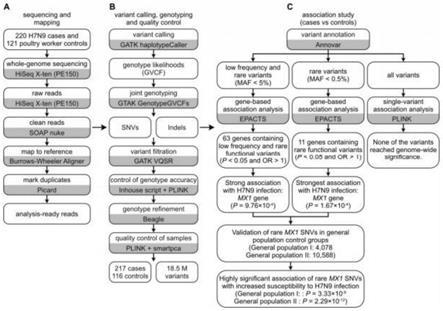
13.图1.提供了通过快速体外混合和表达进行糖基化途径组装(glycoprime)的平台的图。建立glycoprime以构建和筛选产生多种n
‑
连接的聚糖的生物合成途径。通过无细胞蛋白质合成(cfps)将富含靶蛋白质或个体糖基转移酶(gt)的粗制大肠杆菌裂解物以各种组合方式混合,以鉴定用于各种n
‑
连接的聚糖的构建的生物合成途径。模型受体蛋白(im7
‑
6)、来自胸膜肺炎放线杆菌(a.pleuropneumoniae)的n
‑
连接的糖基转移酶(apngt)和24个精心设计的gt在cfps中产生,然后在37条独特的糖基化途径中与活化的糖供体组装。在这37条途径中,我们鉴定了产生独特糖基化结构的23种生物合成gt组合,其中一些具有治疗相关性。体外发现的途径被转移至无细胞或基于细胞的生产平台,以产生治疗相关的糖蛋白。
14.图2:单酶和双酶糖基化途径的体外合成和组装。(a)蛋白质名称、种类、先前表征的活性和对于选择用于聚糖精心制作的im7
‑
6靶蛋白、apngt和gt的优化的可溶性cfps产率。参考图8中先前表征的活性。cfps产率指示来自n=3个cfps反应的平均值和标准偏差(s.d.),其通过[14c]
‑
亮氨酸掺入定量。完整cfps表达数据在图6和图12和13中。(b)用于通过apngt在im7
‑
6上安装n
‑
连接的葡萄糖和通过选择的gt进行精心制作的符号性关键和成功途径。本文中的聚糖结构使用用于聚糖的符号命名法(snfg)和用于键联的oxford system惯例。唾液酸是指n
‑
乙酰神经氨酸。(c)从由有和没有0.4μm apngt以及2.5mm udp
‑
glc的cfps反应产物组装的ivg反应纯化来自im7
‑
6蛋白质的解卷积质谱光谱。在30℃下24小时后观察到完全转化为n
‑
连接的葡萄糖。(d)从含有10μm im7
‑
6、0.4μm apngt和7.8μm nmlgtb、13.9μm nglgtb、3.1μm bfgalnact或9.4μm apα1
‑
6的ivg反应纯化来自im7蛋白质的完整解卷积ms光谱。视情况而定,ivg反应补充有2.5mm udp
‑
glc以及2.5mm udp
‑
gal或5mm udp
‑
galnac,在30℃下反应24小时。观察到的质量位移和ms/ms碎片化光谱(图14)与用β1
‑
4gal、β1
‑
4gal、β1
‑
3galnac或α1
‑
6葡聚糖聚合物对n
‑
连接的葡萄糖的有效修饰一致。图7中发现理论蛋白质质量。hpβ4galt、btβ4galt1和spwchj k不修饰通过apngt安装的n
‑
连接的葡萄糖(图15)。所有光谱均从所有检测的糖基化和非糖基化im7
‑
6种类的完全洗脱峰区域获得,并且代表n=3个独立的ivg。使用bruker compass数据分析最大熵方法将来自m/z 100
‑
2000的光谱解卷积为11,000
‑
14,000da。
[0015]
图3:复杂糖基化途径的体外合成和组装。(a)蛋白质名称、种类、先前表征的特异性(图8)和对于针对n
‑
连接的乳糖的精心制作测试的酶的优化的cfps可溶性产率(图6)。cfps产率指示来自n=3个cfps反应的平均值和s.d.,其通过[14c]
‑
亮氨酸掺入定量。在氧化条件下测量cjcst
‑
i和hssiat1产率(参见图20)。(b)从含有10μm im7
‑
6、0.4μm apngt、2μm nmlgtb和2.5mm合适的核苷酸活化糖供体以及4.0μm btggta、5.3μm nmlgtc、4.9μm hpfuta、2.6μm hpfutc、4.9μm pdst6、5.0μm cjcst
‑
ii、1.3μm cjcst
‑
i、11.5μm nglgta或2.2μm sppvg1的ivg反应纯化来自im7
‑
6蛋白质的完整解卷积ms光谱。完整的im7
‑
6的质量位移、胰蛋白酶化的im7
‑
6糖肽的碎片化光谱(图18)和外切糖苷酶消化(图21和22)与根据btggta、nmlgtc、hpfuta、hpfutc、pdst6、cjcst
‑
ii、cjcst
‑
i、nglgta或sppvg1的已知活性用α1
‑
3gal、α1
‑
4gal、α1
‑
3fuc、α2
‑
6sia、α2
‑
3 sia、α2
‑
8 sia、β1
‑
3 glcnac或丙酮酸化修饰n
‑
连接的乳糖一致。(d)通过四酶和五酶组合产生的岩藻糖基化和唾液酸化lacnac结构的解卷积的完整im7
‑
6光谱。ivg反应包含10μm im7
‑
6、0.4μm apngt、2μm nmlgtb、适当的糖供
体,并且指示分别对于四酶和五酶途径在b中所示浓度的一半或三分之一的gt。根据已知活性,完整质量位移和碎片化光谱(图23)与lacnac核心的岩藻糖基化和唾液酸化一致。来自此处未显示的其他筛选的gt和gt组合的完整蛋白质和糖肽碎片化光谱在图17
‑
19和23
‑
25中。为了提供最大转化率,ivg反应在30℃下孵育24小时,补充了额外的2.5mm糖供体,并在30℃下孵育另外24小时。光谱从所有检测的糖基化和非糖基化im7种类的完全洗脱区域获得,并且代表n=2个ivg。使用bruker compass数据分析最大熵方法将来自m/z 100
‑
2000的光谱解卷积为11,000
‑
14,000da。
[0016]
图4:用于无细胞和细菌生产平台的生物合成途径的设计。(a)用于用αgal聚糖修饰的h1ha10蛋白疫苗的合成的一锅式cfps
‑
gps。编码通过glycoprime筛选发现的靶蛋白和生物合成途径gt的质粒与适当的活化的糖供体在cfps
‑
gps反应中组合。(b)胰蛋白酶化的糖肽ms光谱,(c)糖肽的外切糖苷酶消化,以及(d)来自从包含等摩尔量的每种指定的编码h1ha10、apngt、nmlgtb和btggta的质粒以及2.5mm的udp
‑
glc和udp
‑
gal的ivg反应纯化的h1ha10的ms/ms糖肽碎片化光谱(参见方法)。所有反应均含有10nm总质粒浓度,并在30℃下孵育24小时。糖肽包含位于h1ha10的n末端的一个工程化受体序列。在b
‑
d光谱中观察到的质量和质量位移与通过apngt用n
‑
连接的glc、通过apngt和nmlgtb用乳糖(glcβ1
‑
4gal)或通过apngt、nmlgtb和btggta用αgal表位(glcβ1
‑
4galα1
‑
3gal)修饰h1ha10肽一致。(e)设计细胞质糖基化系统以在大肠杆菌中产生唾液酸化igg fc。三个质粒包含nmneua(cmp
‑
sia合成)、用优化的受体序列(靶蛋白)工程化的igg fc,以及使用glycoprime(gt操纵子)发现的生物合成途径。(f)解卷积的完整糖蛋白ms光谱,(g)完整糖蛋白的外切糖苷酶消化光谱,以及(h)来自从补充有唾液酸、iptg和阿拉伯糖并在25℃孵育过夜的大肠杆菌培养物纯化的fc
‑
6的ms/ms糖肽碎片化光谱(见方法)。指出了所有糖基化途径中的最后一个gt。ms光谱是从所有检测的糖基化和非糖基化蛋白质或肽种类的完全洗脱区域获得的,并代表n=3个cfps
‑
gps或大肠杆菌培养物。通过伪多反应监测(mrm)碎片化以对应于使用30ev碰撞能量检测的完整糖肽或蛋白质ms峰的理论糖肽质量(红色菱形)获得ms/ms光谱。使用compass数据分析最大熵方法将收集来自m/z 100
‑
2000的光谱解卷积为27,000
‑
29,000da。对于理论质量参见图9
‑
11。
[0017]
图5.提供总结此研究1
‑
6中使用的所有菌株和质粒的表格。列出了质粒主链特征,然后是蛋白质编码序列和任何修饰或融合序列的uniprot或ncbi标识符。在此研究中开发的所有质粒的注释的蛋白质编码序列与侧翼质粒序列背景一起显示在图29中。
[0018]
图6.提供显示与im7靶标和糖基化酶的无细胞蛋白质合成的优化相关的概述的表格。通过glycoprime测试的体外糖基化途径的im7
‑
6靶标和酶的cfps产率。cfps产率和误差指示来自通过14c
‑
亮氨酸掺入定量的n=3个cfps反应的平均值和s.d.。所有cfps反应在指定的温度和条件下孵育20小时。溶解度是从以12,000xg离心15分钟后分离的级分的产率的定量计算的。星号(*)指示在氧化条件下进行cfps时的产率。优化条件下的产率也显示在图2和图3中。列出的平均值和s.d.值的源数据在源数据文件中提供(可在kightlinger等人,nature communications,2019中获得,其通过引用整体并入本文)。
[0019]
图7.提供对于在glycoprime生物合成途径工程化期间产生的im7
‑
6糖型的理论糖蛋白和糖肽质量的表格。预测的糖基化结构基于先前建立的gt活性,其显示于图2和3和图8中。显示了预期糖蛋白产物的理论、中性和平均质量,以及糖肽的理论、三电荷、单同位素的
质荷比(m/z)。糖肽质量对应于im7
‑
6中唯一的apngt糖基化位点,其包含在胰蛋白酶肽eattggnwttaggdvldvllehfvk中。实验观察到的质量在解卷积的完整蛋白质ms和糖肽ms/ms光谱中进行了注释。
[0020]
图8.提供显示本研究7
‑
23中使用的糖基转移酶的先前表征的活性的表格。下面列出的gt被选择用于在glycoprime系统中基于它们之前建立的活性进行测试。许多以前也被用于糖脂或游离寡糖的生物合成,为它们在本研究中精心制作通过apngt安装的n
‑
连接的葡萄糖的新背景下进行测试奠定了基础。
[0021]
图9.提供显示在糖肽ms/ms光谱中检测到的糖碎片离子的理论质量的表格。在糖肽的ms/ms碎片化过程中,检测到诊断的糖离子。这些糖离子的理论质荷比示于表中。理论m/z的所有计算均假设单电荷离子。本文中所有提及的唾液酸(sia)均指n
‑
乙酰神经氨酸(neuac)。
[0022]
图10.提供显示体外合成和糖基化的h1ah10的理论糖肽质量的表格。通过一锅式体外反应合成和糖基化的h1ah10中的含有n末端工程化糖基化位点的胰蛋白酶肽的理论、双电荷、单同位素的质荷比(m/z)。预测的糖基化结构基于先前建立的gt活性,其显示于图2和3和图8中。实验观察到的质量在图4和25中的解卷积ms和ms/ms光谱上进行了注释。
[0023]
图11.提供显示在大肠杆菌细胞质中合成和糖基化的fc
‑
6的理论糖蛋白和糖肽质量的表格。预测的糖基化结构基于先前建立的gt活性,其显示于图2和3和图8中。表中显示了预期糖蛋白产物的理论、中性、平均质量和糖肽的理论、三电荷、单同位素的质荷比(m/z)。糖肽质量对应于fc
‑
6中唯一的apngt糖基化位点,其包含在胰蛋白酶肽eeattggnwttaggr中。实验观察到的质量在图4和26中的解卷积ms和ms/ms光谱上进行了注释。
[0024]
图12.考马斯染色的蛋白质凝胶显示glycoprime靶标和酶的cfps表达。在im7
‑
6靶标和指示的glycoprime酶的体外合成后,基于cfps反应的大肠杆菌粗制裂解物的可溶性级分的考马斯染色的蛋白质凝胶。高度富集的蛋白质根据接近预期分子量的增加的条带厚度(箭头)是明显的,其他产物可以在图13中看到。来自cfps反应的产物在通过(*)指示的氧化条件下运行。通过在4℃下以12,000xg离心15分钟来分离可溶性样品。代表n=2个凝胶。将相同的凝胶曝光为放射自显影图以确定含有[14c]
‑
亮氨酸蛋白的条带(图13)。
[0025]
图13.蛋白质凝胶的放射自显影图,显示cfps中glycoprime靶标和酶的cfps表达。在im7
‑
6靶标和指示的glycoprime酶的体外合成后,基于含有[14c]
‑
亮氨酸的cfps反应的大肠杆菌粗制裂解物的可溶级分的蛋白质凝胶的放射自显影图。接近预期分子量的含有[14c]
‑
亮氨酸的条带的存在指示没有大截断的蛋白质的全长表达(箭头指示预期的全长产物)。来自cfps反应的产物在通过(*)指示的氧化条件下运行。通过在4℃下以12,000xg离心15分钟来分离可溶性样品。通过将在mops中运行的4
‑
12%sds
‑
page凝胶曝光于磷屏(phosphoscreen)72小时来生成放射自显影图。放射自显影图代表n=2个凝胶和曝光。相同的凝胶被考马斯染色(补充图1)并与放射自显影图像对齐作为分子量标准参考。
[0026]
图14.来自精心制作n
‑
连接的葡萄糖的两种酶生物合成途径的glycoprime反应产物的糖肽ms/ms光谱。来自含有图2所示的修饰im7
‑
6的两种酶途径的ivg反应的产物经过纯化、胰蛋白酶消化,并通过在对应于检测的蛋白质ms峰的理论糖肽质量(红色菱形)处的伪多反应监测(mrm)ms/ms碎片化使用30ev的碰撞能量进行分析(参见方法)。光谱代表来自n
=1个ivg反应的许多ms/ms采集。源自预期糖基化结构的理论蛋白质、肽和糖离子质量示于图7和9。所有指示的糖离子都是带单电荷的,并且糖肽碎片化产物是带三个电荷的离子,与使用指示的糖结构的im7
‑
6胰蛋白酶肽eattggnwttaggdvldvllehfvk的修饰一致。(a)999.49
±
2m/z的ms/ms光谱对应于通过bfgalnact安装的n连接的glcβ1
‑
3galnac。(b)1418.29
±
2m/z的ms/ms光谱对应于通过apα1
‑
6安装的n
‑
连接的葡聚糖聚合物。(c)985.81
±
2m/z的ms/ms光谱对应于通过nmlgtb安装的n
‑
连接的乳糖。所有ivg反应都含有im7
‑
6、apngt和根据建立的酶活性的合适的糖供体(图8)。
[0027]
图15.显示没有通过apngt安装的n
‑
连接的葡萄糖的修饰的ivg反应产物的解卷积完整蛋白质ms光谱。含有10μm im7
‑
6、0.4μm apngt、2.5mm适当糖供体和一个精心制作性gt的ivg反应的产物通过完整蛋白质ms进行纯化和分析(参见方法)。(a)含有1.3μm hpβ4galt的ivg的解卷积完整蛋白质ms光谱。(b)含有1.4μm btβ4galt1并补充有10μmα
‑
乳清蛋白并在氧化条件下进行的ivg的解卷积完整蛋白质ms光谱(参见方法)。(c)包含1.5μm spwchj和1.0μm spwchk的ivg的解卷积完整蛋白质ms光谱。没有检测到指示im7
‑
6被通过apngt安装的n
‑
连接的葡萄糖修饰的峰(理论质量值如图7所示)。使用bruker compass数据分析最大熵方法将来自m/z 100
‑
2000的光谱解卷积为11,000
‑
14,000da。此处显示的解卷积光谱代表n=2个ivg反应。
[0028]
图16.lgtb同源物和浓度的优化。含有10μm im7
‑
6、0.4μm apngt、2.5mm适当糖供体和指定浓度的nmlgtb或nglgtb的ivg反应的产物通过完整蛋白质ms进行纯化和分析(参见方法)。(a)来自含有指定浓度的nmlgtb的ivg反应的解卷积完整蛋白质ms光谱。(b)来自含有指定浓度的nglgtb的ivg反应的解卷积完整蛋白质ms光谱。代表在30℃下进行24小时的n=2个ivg反应的结果表明,在cfps中产生的nmlgtb具有更高的比活性,并且可以用2μm nmlgtb获得几乎均质的n
‑
连接的乳糖。理论质量值如图7所示。所有光谱从所有检测到的糖基化和非糖基化im7
‑
6种类的完全洗脱峰区域获得,并使用bruker bruker compass数据分析最大熵方法从m/z100
‑
2000解卷积为11,000
‑
14,000da。
[0029]
图17.唾液酸转移酶同源物的优化。代表含有0.4μm apngt、2μm nmlgtb、图3所示的每种唾液酸转移酶和各2.5mm的udp
‑
glc、udp
‑
gal和cmp
‑
sia的n=2个ivg反应的解卷积完整蛋白质ms光谱。将通过cfps富含唾液酸转移酶的裂解物以等体积添加到每个ivg反应,以使得每个32μl
‑
ivg反应包含总共25μl的cfps裂解物。基于图6中所示的cfps产率,这些反应包含12.9μm ppst3;9.8μm vsst3;1.8μm pmst3,6;1.3μm cjcst
‑
i;5.6μm plst6;0.7μm hssiat1;和4.9μm pdst6。cjcst
‑
i和hssiat1在氧化条件下在cfps中合成,因为发现它们在以这种方式产生时更具活性(图20)。在上述条件下,含有pdst6的反应提供最有效的向6
’‑
唾液酸乳糖的转化,而含有cjcst
‑
i的反应提供最有效的向3
’‑
唾液酸乳糖的转化(为了确认键联的外切糖苷酶消化显示在图21中)。尽管ppst6和vsst3中仅出现痕量,但ms/ms检测和鉴定表明这些酶是有功能的(图18)。所有光谱均从所有检测的糖基化和非糖基化im7
‑
6种类的完全洗脱峰区域获得,并使用bruker compass数据分析最大熵方法从m/z 100
‑
2000解卷积为11,000
‑
14,000da。
[0030]
图18.来自精心制作n
‑
连接的乳糖的三种酶生物合成途径的glycoprime反应产物的糖肽ms/ms光谱。来自含有图3所示的修饰im7
‑
6的三种酶途径的ivg反应的产物经过纯化、胰蛋白酶消化,并通过在对应于图3和图17中检测的蛋白质ms峰的理论糖肽质量(由红
色菱形指示)处的伪mrm ms/ms碎片化进行分析(参见方法)。使用30ev的碰撞能量将所有糖肽碎片化,其中使用从靶m/z值的
±
2m/z的窗口(参见方法)。光谱代表了来自n=1个ivg反应的许多ms/ms采集。源自预期糖基化结构的理论蛋白质、肽和糖离子质量示于图7和9。所有指示的糖离子都是带单电荷的,并且糖肽碎片化产物是带三个电荷的离子,与使用指示的糖结构的im7
‑
6胰蛋白酶肽eattggnwttaggdvldvllehfvk的修饰一致。预测的糖键联基于先前建立的gt活性(图8)和外切糖苷酶测序(图21和22)。所有ivg反应都包含根据已建立的gt活性的合适的糖供体、im7
‑
6、apngt、nmlgtb和指示的gt。
[0031]
图19.hdglcnact不修饰通过apngt和nmlgtb安装的n
‑
连接的乳糖底物。包含10μm im7
‑
6、0.4μm apngt、2μm nmlgtb、1.5μm hdglcnact和2.5mm udp
‑
glc、udp
‑
gal和udp
‑
glcnac的ivg反应产物的解卷积完整蛋白质ms光谱。没有检测到指示im7
‑
6被通过apngt和nmlgtb安装的n
‑
连接的乳糖修饰的峰(理论质量值参见图7)。解卷积光谱代表n=2个ivg反应。
[0032]
图20.cjcst
‑
i和hssiat1当在氧化条件下产生时表现出更大的活性。解卷积完整蛋白质ms光谱代表n=2个ivg反应产物,其包含10μm im7
‑
6、0.4μm apngt、2μm nmlgtb、2.5mm udp
‑
glc、udp
‑
gal和cmp
‑
sia以及在氧化条件、补充了大肠杆菌二硫键异构酶(dsbc)的还原条件或标准还原条件下进行的cfps中制备的cjcst
‑
i或hssiat1(参见方法)。已知cfps条件产生有助于二硫键形成的蛋白质合成环境,如前所述24。以等体积加入通过cfps富含唾液酸转移酶的裂解物。因此,还原反应条件包含1.9μm的cjcst
‑
i或3.8μm的hssiat1,而氧化反应条件反应包含1.3μm的cjcst
‑
i和0.7μm的hssiat1(详细的cfps产率信息如图15所示)。除了对于cjcst
‑
i和hssiat1的cfps合成条件外,ivg反应在不确保用于糖基化的氧化环境的情况下相同地进行。im7
‑
6、apngt和nmlgtb是用标准cfps反应条件产生的。相对糖基化效率指示cfps的氧化cfps环境允许每单位cfps反应体积和每μm酶的更高的酶活性。这一观察结果对于hssiat1是有意义的,hssiat1通常在人高尔基体的氧化环境中具有活性,并且已知含有二硫键。有趣的是,氧化合成环境似乎也有利于不含二硫键的cjcst
‑
i的活性。然而,cjcst
‑
i的增加的活性不能通过dsbc的一般分子伴侣活性来解释。
[0033]
图21.通过含有唾液酸的glycoprime生物合成途径修饰的im7
‑
6的外切糖苷酶测序。从glycoprime工作流程完成ivg反应,其中使用ni
‑
nta磁珠进行纯化,在有和没有指定的市售外切糖苷酶的情况下在37℃下孵育至少4小时,胰蛋白酶化过夜,然后通过糖肽lc
‑
ms进行分析。α2
‑
3神经氨酸酶s能够去除通过cjcst
‑
i;pmst3,6安装的唾液酸;以及通过cjcst
‑
ii安装的第一个唾液酸,表明这些酶安装了具有α2
‑
3键联的唾液酸。通过pdst6、hssiat1安装的唾液酸以及通过cjcst
‑
ii安装的第二个和第三个唾液酸对通过α2
‑
3神经氨酸酶s的消化具有抗性,但容易被α2
‑
3,6,8神经氨酸酶裂解,这与pdst6和hssiat1的建立的α2
‑
6活性以及在随后的唾液酸添加中通过cjcst
‑
ii安装的α2,8键联是一致的。对于外切糖苷酶的详细信息,参见方法部分。所有光谱均从含有apngt糖基化受体序列的im7
‑
6胰蛋白酶肽eattggnwttaggdvldvllehfvk的所有检测的糖基化和非糖基化种类的完全洗脱峰区域获得。所有指定的糖肽产物都是带三个电荷的离子,与用指定的糖结构修饰的此im7
‑
6胰蛋白酶肽一致。
[0034]
图22.通过不含唾液酸的glycoprime生物合成途径修饰的im7
‑
6外切糖苷酶测序。从glycoprime工作流程完成ivg反应,其中使用ni
‑
nta磁珠进行纯化,在有和没有指定的市
售外切糖苷酶的情况下在37℃下孵育至少4小时,胰蛋白酶化过夜,然后通过糖肽lc
‑
ms进行分析。通过nmlgtb、btggta、hpfuta和hpfutc安装的糖分别容易被市售的β1
‑
4半乳糖苷酶s;α1
‑
3,6半乳糖苷酶;α1
‑
3,4岩藻糖苷酶;和α1
‑
2岩藻糖苷酶裂解。通过nmlgtc安装的半乳糖对通过β1
‑
4半乳糖苷酶s和α1
‑
3,6半乳糖苷酶的裂解具有抗性,但容易被α1
‑
3,4,6半乳糖苷酶裂解。通过nmlgtb和nglgta的交替活动安装的lacnac聚合物容易被β1
‑
4半乳糖苷酶s和β
‑
n
‑
乙酰葡糖胺苷酶s的混合物裂解。所有光谱均从含有apngt糖基化受体序列的im7
‑
6胰蛋白酶肽eattggnwttaggdvldvllehfvk的所有检测的糖基化和非糖基化种类的完全洗脱峰区域获得。所有指定的糖肽产物都是带三个电荷的离子,与用指定的糖结构修饰的此im7
‑
6胰蛋白酶肽一致。裂解观察结果与先前建立的gt活性(图2
‑
3和8)一致。对于外切糖苷酶的详细信息,参见方法部分。
[0035]
图23.来自精心制作n
‑
连接的乳糖的四种和五种酶生物合成途径的glycoprime反应产物的糖肽ms/ms光谱。来自包含图3d和图25所示的修饰im7
‑
6的四种和五种酶途径的ivg反应的产物经过纯化、胰蛋白酶化并通过在对应于图3d和图25中检测的蛋白质ms峰的理论糖肽质量(由红色菱形指示)处的伪mrm ms/ms碎片化进行分析(参见方法)。使用30ev的碰撞能量将所有糖肽碎片化,其中使用从靶m/z值的
±
2m/z的窗口(参见方法)。光谱代表了来自n=1个ivg反应的许多ms/ms采集。源自预期糖基化结构的理论蛋白质、肽和糖离子质量示于图7和9。所有指示的糖离子都是带单电荷的,并且糖肽碎片化产物是带三个电荷的离子,与使用指示的糖结构的im7
‑
6胰蛋白酶肽eattggnwttaggdvldvllehfvk的修饰一致。预测的糖键联基于先前建立的gt活性(图8)。尽管无法明确定义来自五种酶生物合成途径的产物,但糖和糖肽片段确实暗示了岩藻糖和唾液酸的修饰。所有ivg反应都包含根据已建立的gt活性的合适的糖供体、im7
‑
6、apngt、nmlgtb和指示的酶。
[0036]
图24.ivg反应产物的解卷积完整蛋白质ms光谱,显示未产生岩藻糖基化和唾液酸化的种类。含有10μm im7
‑
6、0.4μm apngt、2μm nmlgtb、指示的酶和2.5mm的适当糖供体(udp
‑
glc、udp
‑
gal、cmp
‑
sia和gdp
‑
fuc)的ivg反应的产物经过纯化并通过完整蛋白质ms进行分析。如所示的,反应包含2.4μm hpfuta和2.4μm pdst6或1.3μm hpfutc和0.65μm cjcst
‑
i。解卷积光谱代表n=2个ivg。没有检测到指示用唾液酸和岩藻糖修饰的im7
‑
6的存在的峰(通过箭头注释的光谱区域[在12000和12200之间]显示了唾液酸化和岩藻糖基化种类的预期范围)(对于理论质量值参见图8)。
[0037]
图25.含有五种酶的生物合成途径glycoprime筛选。含有10μm im7
‑
6、0.4μm apngt、2μm nmlgtb、指示的gt和2.5mm的适当糖供体(udp
‑
glc、udp
‑
gal、cmp
‑
sia和gdp
‑
fuc)的ivg反应的产物经过纯化并通过完整蛋白质ms进行分析。解卷积光谱代表n=2个ivg。(a)含有0.87μm hpfutc、3.83μm nglgta和1.63μm pdst6的ivg反应的解卷积完整蛋白质ms。(b)含有1.63μm hpfuta、3.83μm nglgta和1.63μm pdst6的ivg反应的解卷积完整蛋白质ms(也显示在图3d中)(c)含有1.63μm hpfuta、3.83μm nglgta和0.43μm cjcst
‑
i的ivg反应的解卷积完整蛋白质ms。(d)包含0.87μm hpfutc、3.83μm nglgta和0.43μm cjcst
‑
i的ivg反应的解卷积完整蛋白质ms。a和b中的光谱以及图23中的碎片化光谱分别指示含有唾液酸和岩藻糖的3种和1种种类。预测的糖基化结构基于先前建立的gt活性(图8)和碎片化光谱(图23)。尽管无法明确鉴定结构,但之前观察到的hpfuta和pdst6的不兼容,以及碎片化光谱中1083m/z峰(glcβ4galα6sia)的存在和1034m/z(glc(α3fuc)β4gal)峰的不存在表
明在b中,近端半乳糖被唾液酸修饰,而glcnac被岩藻糖修饰。在c或d中没有检测到指示用唾液酸和岩藻糖修饰的im7
‑
6的存在的峰(对于理论质量值参见图7)。
[0038]
图26.通过cfps
‑
gps反应合成和糖基化的im7
‑
6的完整蛋白质ms光谱。(a)编码基于通过两锅示glycoprime筛选开发的12条成功生物合成途径的im7
‑
6靶蛋白和多至3种gt的集合的质粒与合适的糖供体在一锅式cfps
‑
gps反应中组合并在30℃孵育24小时。(b)来自在有和没有apngt质粒的cfps
‑
gps反应中合成和糖基化的im7
‑
6的解卷积完整蛋白质光谱。(c)来自在具有apngt质粒和指示的gt质粒的cfps
‑
gps反应中合成和糖基化的im7
‑
6的解卷积完整蛋白质光谱。(d)来自在具有apngt、nmlgtb和指示的gt质粒的cfps
‑
gps反应中合成和糖基化的im7
‑
6的解卷积完整蛋白质光谱。所有反应都含有等摩尔量的每种质粒和10nm的总质粒浓度。在完整蛋白质分析之前,使用ni
‑
nta磁珠纯化所有im7
‑
6蛋白质(参见方法)。所有反应都显示出完整的蛋白质质量位移,这与在我们的两锅式系统中观察到的使用相同聚糖对im7
‑
6的修饰一致(图2
‑
3),尽管效率较低。ms光谱是从所有检测的糖基化和非糖基化蛋白质或肽种类的完全洗脱区域获得的,并代表n=2个cfps
‑
gps反应。使用bruker compass数据分析最大熵方法将收集来自m/z 100
‑
2000的光谱解卷积到11,000
‑
14,000da。对于理论质量值参见图16。
[0039]
图27.在大肠杆菌细胞质中产生唾液酸化的im7
‑
6。(a)设计细胞质糖基化系统以在大肠杆菌中产生唾液酸化糖蛋白。三种质粒包含nmneua(cmp
‑
sia合成)、含有apngt糖基化受体序列的靶蛋白和使用glycoprime(gt操纵子)发现的生物合成途径。(b
‑
f)来自从含有cmp
‑
sia合成质粒和im7
‑
6靶蛋白质粒以及无gt操纵子b;含有apngt的gt操纵子c;含有apngt和lgtb的gt操纵子d;含有apngt、nmlgtb和cjcst
‑
i的gt操纵子e;或含有apngt、nmlgtb和pdst6 f的gt操纵子的clm24δnana大肠杆菌菌株纯化的im7
‑
6的解卷积完整蛋白质光谱。指示了所有糖基化途径中的最后一个gt。完整蛋白质光谱中的质量位移与每个gt的已建立的活性以及分别在b、c、d、e和f中的n
‑
连接的glc、乳糖、3
’‑
唾液酸乳糖和6
’‑
唾液酸乳糖在im7
‑
6上的安装一致。所有大肠杆菌培养物都补充有5mm唾液酸,并在37℃下生长至od600=0.6,用1mm iptg和0.2%阿拉伯糖诱导,然后在25℃下孵育过夜。ms光谱从所有检测的糖基化和非糖基化蛋白质种类的完全洗脱区域获得,并使用bruker compass数据分析最大熵方法从m/z 100
‑
2000解卷积为11,000
‑
14,000da。对于理论质量参见图7。光谱代表n=2个细菌培养物。
[0040]
图28.大肠杆菌细胞质中糖基化fc的外切糖苷酶测序。(a)来自从含有cmp
‑
sia合成质粒、fc
‑
6靶蛋白质粒和含有apngt、nmlgtb和pdst6的gt操纵子质粒的clm24δnana大肠杆菌菌株纯化的fc
‑
6的解卷积完整蛋白质光谱。(b
‑
d)将来自a的纯化的fc
‑
6与市售的α2
‑
3神经氨酸酶s b、α2
‑
3,6,8神经氨酸酶c或β1
‑
4半乳糖苷酶s和α2
‑
3,6,8神经氨酸酶d在37℃下孵育至少4小时。末端唾液酸对α2
‑
3神经氨酸酶s的抗性和对α2
‑
3,6,8神经氨酸酶的敏感性表明存在α2
‑
6键联,这与pdst6的先前建立的活性一致(图8)。(e)来自从含有cmp
‑
sia合成质粒、fc
‑
6靶蛋白质粒和含有apngt、nmlgtb和cjcst
‑
i的gt操纵子质粒的clm24δnana大肠杆菌菌株纯化的fc
‑
6的解卷积完整蛋白质光谱。(f
‑
g)将来自e的纯化的fc
‑
6与市售的α2
‑
3神经氨酸酶s b或β1
‑
4半乳糖苷酶s和α2
‑
3神经氨酸酶s在37℃下孵育至少4小时。末端唾液酸对α2
‑
3神经氨酸酶的敏感性证实了cjcst
‑
i的先前建立的活性(图8)。在d和g中去除中间的半乳糖并添加β1
‑
4半乳糖苷酶s证实了nmlgtb的先前建立的活性(图8)。a
‑
c和e
‑
f也
显示在图4中。对于外切糖苷酶的细节参见方法并且对于理论糖蛋白质量参见图11。所有大肠杆菌培养物均补充有5mm唾液酸,并在37℃下生长至od600=0.6,然后用1mm iptg和0.2%阿拉伯糖诱导,然后在25℃下孵育过夜。ms光谱从所有检测的糖基化和非糖基化蛋白质种类的完全洗脱区域获得,并使用bruker compass数据分析最大熵方法从m/z 100
‑
2000解卷积为27,000
‑
29,000da。
[0041]
图29.显示了编码工程化的糖基化靶标、体外表达的糖基转移酶、体内糖基转移酶操纵子和体内cmp
‑
sia产生质粒的dna序列。关键词:翻译区域;工程化的糖基化受体序列;与糖基化受体序列相邻的侧翼区域;启动子;终止子;亲和标签或csl前导序列。
[0042]
图30是显示在活大肠杆菌中使用非标准糖进行糖基化的示意图。
[0043]
图31.解卷积的糖蛋白ms结果,显示模型蛋白im7(attccnwttagg接枝到暴露的环中)用具有α2,3和α2,6键联的叠氮基唾液酸成功修饰。
[0044]
图32.解卷积糖蛋白ms结果,显示模型蛋白人fc(用attggnwttagg替换fc上的天然qynsty糖基化位点)用具有α2,3和α2,6键联的叠氮基唾液酸成功修饰。
[0045]
图33.提供了显示示例性治疗化合物的定点glycopegylation和用于致耐受反应的示例性“点击”型siglec
‑
结合配体的示意图。
[0046]
发明详述
[0047]
介绍
[0048]
糖基化赋予蛋白质治疗剂有益的特性,包括增加的血清半衰期和引发保护性免疫反应的能力。基因编辑、工程化微生物菌株和体外合成系统的发展为糖蛋白疗法提供了新的机会。然而,构建生物合成途径来改造蛋白质糖基化仍然是一个关键的瓶颈。在这里,发明人开发并采用了模块化无细胞平台用于通过快速体外混合和表达进行糖基化途径组装(glycoprime)。在glycoprime中,粗制大肠杆菌裂解物通过无细胞蛋白质合成富含糖基转移酶,然后组装糖基化途径以精心制作由可溶性、n连接的糖基转移酶安装的单个葡萄糖引发手柄。发明人使用glycoprime构建了37条推定的蛋白质糖基化途径,创建了23个独特的聚糖基序。许多这些途径以前没有被描述过,并产生了用于蛋白质治疗剂和疫苗的感兴趣的糖基化结构。然后,发明人使用选择的生物合成途径以在活大肠杆菌中产生具有最少唾液酸聚糖的人抗体的恒定区的糖蛋白和在按需无细胞表达平台中产生具有辅助性聚糖的蛋白质疫苗候选物。glycoprime和此处描述的途径可以加速具有确定特性的糖蛋白的工程化以及替代宿主中糖蛋白的制造。
[0049]
定义和术语
[0050]
所公开的用于糖蛋白和重组糖蛋白蛋白质合成的组分、系统和方法可以使用如下定义和术语进一步描述。本文中使用的定义和术语仅用于描述特定实施方案的目的,并不旨在进行限制。
[0051]
如在本说明书和权利要求中使用的,单数形式“一个”、“一种”和“该”包括复数形式,除非上下文另有明确规定。例如,术语“一个/种寡糖”或“一个/种糖基转移酶”应分别解释为是指“一个或多个/一种或多种寡糖”和“一个或多个/一种或多种糖基转移酶”,除非上下文另有明确规定。如本文所用,术语“多个/多种”是指“两个或更多个/两种或更多种”。
[0052]
如本文所用,“约”、“大约”、“基本上”和“显著”将被本领域普通技术人员理解并且将在它们使用的上下文中在一定程度上变化。如果考虑到使用它的上下文,该术语的使用
对于本领域的普通技术人员来说是不清楚的,则“约”和“大约”将意味着特定术语的多至正负10%和“基本上”和“显著”将意味着超过特定术语的正负10%。
[0053]
如本文所用,术语“包括”和“包括的”与术语“包含”和“包含的”具有相同的含义。术语“包括”和“包含”应被解释为“开放”过渡性术语,其允许进一步包括在权利要求中记载的那些组分之外的附加组分。术语“组成”和“由
……
组成”应被解释为“封闭式”过渡性术语,其不允许包括除权利要求中记载的组分之外的附加组分。术语“基本上由
……
组成”应被解释为部分封闭,其仅允许包含不会根本上改变要求保护的主题的性质的附加组分。
[0054]
短语“诸如”应被解释为“例如,包括”。此外,任何和所有示例性语言的使用,包括但不限于“诸如”,仅意在更好地阐明本发明而不对本发明的范围构成限制,除非另有声明。
[0055]
此外,在其中使用类似于“a、b和c等中的至少一个”的约定的那些情况下,一般而言,这样的造句意在具有本领域普通技术人员将理解该约定的意义(例如,“具有a、b和c中的至少一个的系统”将包括但不限于具有单独的a、单独的b、单独的c、a和b一起、a和c一起、b和c一起和/或a、b和c一起的系统)。本领域技术人员将进一步理解,呈现两个或更多个替代术语的实际上任何分离词和/或短语(无论是在说明书还是附图中)都应该被理解为考虑包括术语中的一个、术语中的任一个或术语中的两者的可能性。例如,短语“a或b”将被理解为包括“a”或“b”或“a和b”的可能性。
[0056]
诸如“多至”、“至少”、“大于”、“小于”等的所有语言包括所列举的数字并且指的是随后可以被分解为范围和子范围的范围。范围包括每个个体成员。因此,例如,具有1
‑
3个成员的组是指具有1、2或3个成员的组。类似地,具有6个成员的组是指具有1、2、3、4或6个成员的组,以此类推。
[0057]
情态动词“可以”是指在几个所描述的实施方案或包含在其中的特征中的一个或多个选项或选择的优选使用或选择。当没有公开关于特定实施方案或其中包含的特征的选项或选择时,情态动词“可以”是指关于如何制作或使用所描述的实施方案或包含在其中的特征的方面的肯定行为,或使用关于所描述的实施方案或包含在其中的特征的特定技能的最终决定。在后一种情况下,情态动词“可以”与助动词“可能”具有相同的含义和内涵。
[0058]
多核苷酸和合成方法
[0059]
如本文所用,术语“核酸”和“寡核苷酸”是指聚脱氧核糖核苷酸(含有2
‑
脱氧
‑
d
‑
核糖)、聚核糖核苷酸(含有d
‑
核糖),以及作为嘌呤或嘧啶碱基的n糖苷的任何其他类型的多核苷酸。术语“核酸”、“寡核苷酸”和“多核苷酸”之间在长度上没有意图的区别,并且这些术语将互换使用。这些术语仅指分子的一级结构。因此,这些术语包括双链和单链dna,以及双链和单链rna。为了在本方法中使用,寡核苷酸还可以包括其中碱基、糖或磷酸主链被修饰的核苷酸类似物以及非嘌呤或非嘧啶核苷酸类似物。
[0060]
寡核苷酸可以通过任何合适的方法制备,包括通过诸如narang等人,1979,meth.enzymol.68:90
‑
99的磷酸三酯方法;brown等人,1979,meth.enzymol.68:109
‑
151的磷酸二酯方法;beaucage等人,1981,tetrahedron letters 22:1859
‑
1862的二乙基亚磷酰胺方法;和美国专利号4,458,066的固体支持方法(每个都通过引用并入本文)的方法直接化学合成。goodchild,1990,bioconjugate chemistry 1(3):165
‑
187中提供了寡核苷酸和修饰的核苷酸的缀合物的合成方法的综述,该文献通过引用并入本文。
[0061]
术语“扩增反应”是指任何化学反应,包括酶促反应,其导致模板核酸序列的增加
的拷贝或导致模板核酸的转录。扩增反应包括逆转录、聚合酶链反应(pcr),包括实时pcr(参见美国专利号4,683,195和4,683,202;pcr protocols:a guide to methods and applications(innis等人,eds,1990)),和连接酶链反应(lcr)(参见barany等人,美国专利号5,494,810)。示例性的“扩增反应条件”或“扩增条件”通常包括两步或三步循环。两步循环具有高温变性步骤,然后是杂交/延伸(或连接)步骤。三步循环包括变性步骤,接着是杂交步骤,接着是单独的延伸步骤。
[0062]
如本文所用,术语“靶标”、“靶序列”、“靶区域”和“靶核酸”是同义词,并且是指待扩增、测序或检测的核酸的区域或序列。
[0063]
如本文所用,术语“杂交”是指由于互补碱基配对由两条单链核酸形成双链体结构。杂交可发生在完全互补的核酸链之间或包含少量错配区域的“基本互补”核酸链之间。其中完全互补的核酸链的杂交是强烈优先的条件称为“严格杂交条件”或“序列特异性杂交条件”。在不太严格的杂交条件下可以获得基本互补序列的稳定双链体;可以通过适当调整杂交条件来控制容许的错配程度。核酸技术领域的技术人员可以根据经验确定双链体稳定性,其中考虑许多变量,包括例如寡核苷酸的长度和碱基对组成、离子强度和错配碱基对的发生率,遵循本领域提供的指导(参见,例如,sambrook等人,1989,molecular cloning
–
a laboratory manual,cold spring harbor laboratory,cold spring harbor,new york;wetmur,1991,critical review in biochem.and mol.biol.26(3/4):227
‑
259;和owczarzy等人,2008,biochemistry,47:5336
‑
5353,其通过引用并入本文)。
[0064]
如本文所用,术语“引物”是指在合适的条件下能够充当dna合成起始点的寡核苷酸。此类条件包括其中在四种不同的三磷酸核苷和用于延伸的试剂(例如,dna聚合酶或逆转录酶)的存在下在适当的缓冲液中并且在合适的温度下诱导与核酸链互补的引物延伸产物的合成的那些条件。
[0065]
引物优选地是单链dna。引物的合适长度取决于引物的预期用途,但通常范围为约6至约225个核苷酸,包括中间范围,例如15至35个核苷酸、18至75个核苷酸和25至150个核苷酸。短引物分子通常需要较低的温度以与模板形成足够稳定的杂交复合物。引物不需要反映模板核酸的确切序列,但必须充分互补以与模板杂交。用于扩增给定靶序列的合适引物的设计是本领域众所周知的并且描述于本文引用的文献中。
[0066]
引物可以包括允许检测或固定引物但不改变引物的基本特性(即作为dna合成起始点)的附加特征。例如,引物可以在5’端包含额外的核酸序列,该序列不与靶核酸杂交,但其有助于扩增产物的克隆或检测,或其使得能够转录rna(例如,通过包含启动子)或翻译蛋白质(例如,通过包含5
’‑
utr,例如内部核糖体进入位点(ires)或3
’‑
utr元件,例如聚(a)n序列,其中n在约20至约200的范围内)。与模板充分互补以杂交的引物区域在本文中称为杂交区域。
[0067]
如本文所用,如果在足够严格的条件下用于扩增反应中时,引物主要与靶核酸杂交,则引物对于靶序列是“特异性的”。通常,如果引物
‑
靶标双链体稳定性大于引物与样品中发现的任何其他序列之间形成的双链体的稳定性,则引物对靶序列具有特异性。本领域技术人员将认识到各种因素(例如盐条件以及引物的碱基组成和错配的位置)将影响引物的特异性,并且引物特异性的常规实验确认将在很多情况下是需要的。可以选择杂交条件,在该条件下引物可以仅与靶序列形成稳定的双链体。因此,在适当严格的扩增条件下使用
靶特异性引物能够选择性扩增含有靶引物结合位点的那些靶序列。
[0068]
如本文所用,“聚合酶”是指催化核苷酸的聚合的酶。“dna聚合酶”催化脱氧核糖核苷酸的聚合。已知的dna聚合酶包括例如激烈火球菌(pyrococcus furiosus)(pfu)dna聚合酶、大肠杆菌dna聚合酶i、t7 dna聚合酶和水生栖热菌(thermus aquaticus)(taq)dna聚合酶等。“rna聚合酶”催化核糖核苷酸的聚合。dna聚合酶的上述实例也称为dna依赖性dna聚合酶。rna依赖性dna聚合酶也属于dna聚合酶的范围。逆转录酶,包括由逆转录病毒编码的病毒聚合酶,是rna依赖性dna聚合酶的一个实例。rna聚合酶(“rnap”)的已知实例包括例如t3 rna聚合酶、t7 rna聚合酶、sp6 rna聚合酶和大肠杆菌rna聚合酶等。rna聚合酶的上述实例也称为dna依赖性rna聚合酶。任何上述酶的聚合酶活性可以通过本领域公知的方法测定。
[0069]
术语“启动子”是指顺式作用dna序列,其指导rna聚合酶和其他反式作用转录因子从包含顺式作用dna序列的dna模板起始rna转录。
[0070]
如本文所用,术语“序列确定的生物聚合物”是指具有特定一级序列的生物聚合物。在基因编码具有特定一级序列的生物聚合物的情况下,序列确定的生物聚合物可以等同于基因编码的确定的生物聚合物。
[0071]
本文考虑的多核苷酸序列可以存在于表达载体中。例如,载体可以包含:(a)编码蛋白质的orf的多核苷酸;(b)表达rna的多核苷酸,该rna指导靶dna序列的rna介导的结合、切口和/或裂解;以及(a)和(b)。载体中存在的多核苷酸可以与原核或真核启动子可操作地连接。“可操作地连接”是指其中将第一核酸序列放置于与第二核酸序列的功能关系中的情况。例如,如果启动子影响编码序列的转录或表达,则启动子与编码序列可操作地连接。可操作地连接的dna序列可以在同一阅读框中非常接近或连续并且在需要时连接两个蛋白质编码区。本文考虑的载体可包含与编码蛋白质的多核苷酸可操作地连接的异源启动子(例如,真核或原核启动子)。“异源启动子”是指不是所表达的蛋白质或rna的天然或内源启动子的启动子。本文公开的载体可包括质粒载体。
[0072]
如本文所用,“表达”是指多核苷酸从dna模板转录的过程(例如转录成mrna或其他rna转录物)和/或转录的mrna随后翻译成肽、多肽或蛋白质的过程。转录物和编码的多肽可以统称为“基因产物”。如果多核苷酸源自基因组dna,则表达可包括在真核细胞中mrna的剪接。
[0073]
如本文所用,“表达模板”是指作为底物用于转录至少一种可以翻译成序列确定的生物聚合物(例如,多肽或蛋白质)的rna的核酸。表达模板包括由dna或rna组成的核酸。将核酸用于表达模板的dna的合适来源包括基因组dna、cdna和可以转化为cdna的rna。基因组dna、cdna和rna可以来自任何生物来源,例如组织样品、活组织检查、拭子、痰、血液样品、粪便样品、尿液样品、刮屑等。基因组dna、cdna和rna可以来自宿主细胞或病毒来源以及来自任何物种,包括现存和灭绝的生物体。如本文所用,“表达模板”和“转录模板”具有相同含义并可互换使用。
[0074]
如本文所用,术语“载体”是指能够运输与其连接的另一种核酸的核酸分子。一种类型的载体是“质粒”,它指的是环状双链dna环,其中可以连接额外的dna区段。此类载体在本文中称为“表达载体”。通常,可用于重组dna技术的表达载体通常是质粒形式。在本说明书中,“质粒”和“载体”可以互换使用。然而,所公开的方法和组合物旨在包括此类其他形式
的表达载体,例如起到等效功能的病毒载体。
[0075]
在某些示例性实施方案中,重组表达载体包含适合在本文所述的一种或多种方法中表达核酸序列的形式的核酸序列,这意味着重组表达载体包括与待表达的核酸序列可操作地连接的一种或多种调节性序列。在重组表达载体内,“可操作地连接”旨在意指编码一种或多种rrna或报告多肽和/或本文所述的蛋白质的核苷酸序列以允许表达核苷酸序列(例如,在体外转录和/或翻译系统中)的方式连接至一种或多种调节序列。术语“调节序列”旨在包括启动子、增强子和其他表达控制元件(例如,聚腺苷酸化信号)。例如,在goeddel;gene expression technology:methods in enzymology 185,academic press,san diego,calif.(1990)中描述了这样的调节序列。
[0076]
寡核苷酸和多核苷酸可以任选地包括一种或多种非标准核苷酸、核苷酸类似物和/或修饰的核苷酸。修饰的核苷酸的实例包括但不限于二氨基嘌呤、s2t、5
‑
氟尿嘧啶、5
‑
溴尿嘧啶、5
‑
氯尿嘧啶、5
‑
碘尿嘧啶、次黄嘌呤、黄嘌呤、4
‑
乙酰胞嘧啶、5
‑
(羧基羟甲基)尿嘧啶、5
‑
羧甲基氨基甲基
‑2‑
硫尿苷、5
‑
羧甲基氨基甲基尿嘧啶、二氢尿嘧啶、β
‑
d
‑
半乳糖基奎苷(galactosylqueosine)、肌苷、n6
‑
异戊烯基腺嘌呤、1
‑
甲基鸟嘌呤、1
‑
甲基肌苷、2,2
‑
二甲基鸟嘌呤、2
‑
甲基腺嘌呤、2
‑
甲基鸟嘌呤、3
‑
甲基胞嘧啶、5
‑
甲基胞嘧啶、n6
‑
腺嘌呤、7
‑
甲基鸟嘌呤、5
‑
甲基氨基甲基尿嘧啶、5
‑
甲氧基氨基甲基
‑2‑
硫尿嘧啶、β
‑
d
‑
甘露糖基奎苷、5
’‑
甲氧基羧甲基尿嘧啶、5
‑
甲氧基尿嘧啶、2
‑
甲硫基
‑
d46
‑
异戊烯基腺嘌呤、尿嘧啶
‑5‑
羟乙酸(v)、wybutoxosine、假尿嘧啶、奎苷(queosine)、2
‑
巯基胞嘧啶、5
‑
甲基
‑2‑
硫尿嘧啶、2
‑
硫尿嘧啶、4
‑
硫尿嘧啶、5
‑
甲基尿嘧啶、尿嘧啶
‑5‑
羟乙酸甲酯、尿嘧啶
‑5‑
羟乙酸(v)、5
‑
甲基
‑2‑
硫尿嘧啶、3
‑
(3
‑
氨基
‑3‑
n
‑2‑
羧丙基)尿嘧啶、(acp3)w、2,6
‑
二氨基嘌呤等。核酸分子也可以在碱基部分(例如,在通常可用于与互补核苷酸形成氢键的一个或多个原子处和/或在通常不能与互补核苷酸形成氢键的一个或多个原子处)、糖部分或磷酸主链处进行修饰。
[0077]
术语“多核苷酸”、“多核苷酸序列”、“核酸”和“核酸序列”是指核苷酸、寡核苷酸、多核苷酸(这些术语可以互换使用)或其任何片段。这些短语也指基因组、天然或合成来源的dna或rna(其可以是单链或双链,并且可以代表有义链或反义链)。
[0078]
关于多核苷酸序列,术语“同一性百分比”和“%同一性”是指使用标准化算法比对的至少两个多核苷酸序列之间的残基匹配的百分比。这样的算法可以以标准化和可重复的方式在被比较的序列中插入缺口以优化两个序列之间的比对,并因此实现两个序列的更有意义的比较。核酸序列的同一性百分比可以如本领域所理解的那样确定。(参见,例如,美国专利号7,396,664,其通过引用整体并入本文)。国家生物技术信息中心(ncbi)基本局部比对搜索工具(blast)提供了一套常用且可免费获得的序列比较算法,其可从多个来源获得,包括ncbi,bethesda,md.,在其网站上获得。blast软件套件包括各种序列分析程序,包括“blastn”,其用于将已知的多核苷酸序列与来自各种数据库的其他多核苷酸序列进行比对。还可用的是称为“blast 2 sequences”的工具,其用于两个核苷酸序列的直接成对比较。“blast 2 sequences”可以在ncbi网站上以交互方式访问和使用。“blast 2 sequences”工具可用于blastn和blastp(如上所讨论的)。
[0079]
关于多核苷酸序列,同一性百分比可以在整个确定的多核苷酸序列(例如,如由特定的seq id号确定的)的长度上测量,或者可以在较短的长度上测量,例如,在取自更大的、
确定的序列的片段的长度(例如至少20、至少30、至少40、至少50、至少70、至少100或至少200个连续核苷酸的片段)上测量。此类长度仅是示例性的,并且应理解,本文、表格、附图或序列表中所示序列支持的任何片段长度可用于描述在其上可测量同一性百分比的长度。
[0080]
关于多核苷酸序列,“变体”、“突变体”或“衍生物”可以定义为使用国家生物技术信息中心网站上提供的blastn和“blast 2 sequences”工具在核酸序列之一的特定长度上与特定核酸序列具有至少50%序列同一性的核酸序列。(参见tatiana a.tatusova,thomas l.madden(1999),"blast 2 sequences
‑
a new tool for comparing protein and nucleotide sequences",fems microbiol lett.174:247
‑
250)。此类核酸对可在某个确定的长度上显示例如至少60%、至少70%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%或更高的序列同一性。
[0081]
由于遗传密码的简并性(其中多个密码子可以编码单一氨基酸),因此不显示高度同一性的核酸序列仍然可以编码相似的氨基酸序列。应当理解,可以使用这种简并性来改变核酸序列以产生全部编码基本相同蛋白质的多个核酸序列。例如,本文考虑的多核苷酸序列可以编码蛋白质并且可以针对在特定宿主中的表达进行密码子优化。在本领域中,已经为包括人、小鼠、大鼠、猪、大肠杆菌、植物和其他宿主细胞在内的许多宿主生物制备了密码子使用频率表。
[0082]“重组核酸”是非天然存在的序列或具有通过人工组合序列的两个或更多个另外分离的区段而制成的序列。这种人工组合通常通过化学合成来实现,或者更常见的通过人工操作核酸的分离的区段(例如通过本领域已知的基因工程技术)来实现。术语重组体包括仅通过添加、取代或缺失一部分核酸而改变的核酸。通常,重组核酸可包括与启动子序列可操作地连接的核酸序列。这样的重组核酸可以是用于例如转化细胞的载体的一部分。
[0083]
本文公开的核酸可以是“基本上分离的或纯化的”。术语“基本上分离或纯化”是指从其天然环境中去除的核酸,并且至少60%不含,优选至少75%不含,以及更优选至少90%不含,甚至更优选至少95%不含与它天然相关的其他组分。
[0084]
肽、多肽、蛋白质和合成方法
[0085]
如本文所用,术语“肽”、“多肽”和“蛋白质”是指包含通过酰胺键连接的氨基酸残基的聚合物链的分子。术语“氨基酸残基”包括但不限于包含在由丙氨酸(ala或a)、半胱氨酸(cys或c)、天冬氨酸(asp或d)、谷氨酸(glu或e)、苯丙氨酸(phe或f)、甘氨酸(gly或g)、组氨酸(his或h)、异亮氨酸(ile或i)、赖氨酸(lys或k)、亮氨酸(leu或l)、甲硫氨酸(met或m)、天冬酰胺(asn或n)、脯氨酸(pro或p)、谷氨酰胺(gln或q)、精氨酸(arg或r)、丝氨酸(ser或s)、苏氨酸(thr或t)、缬氨酸(val或v)、色氨酸(trp或w)和酪氨酸(tyr或y)残基组成的组中的氨基酸残基。术语“氨基酸残基”还可包括非标准或非天然氨基酸。术语“氨基酸残基”可包括α
‑
、β
‑
、γ
‑
和δ
‑
氨基酸。
[0086]
在一些实施方案中,术语“氨基酸残基”可包括包含在由同型半胱氨酸、2
‑
氨基己二酸、n
‑
乙基天冬酰胺、3
‑
氨基己二酸、羟赖氨酸、β
‑
丙氨酸、β
‑
氨基丙酸、别羟赖氨酸、2
‑
氨基丁酸、3
‑
羟脯氨酸、4
‑
氨基丁酸、4
‑
羟脯氨酸、哌啶酸、6
‑
氨基己酸、异锁链素、2
‑
氨基庚酸、别异亮氨酸、2
‑
氨基异丁酸、n
‑
甲基甘氨酸、肌氨酸、3
‑
氨基异丁酸、n
‑
甲基异亮氨酸、2
‑
氨基庚二酸、6
‑
n
‑
甲基赖氨酸、2,4
‑
二氨基丁酸、n
‑
甲基缬氨酸、锁链素、正缬氨酸、2,2
’‑
二
氨基庚二酸、正亮氨酸、2,3
‑
二氨基丙酸、鸟氨酸和n
‑
乙基甘氨酸组成的组中的非标准或非天然氨基酸残基。术语“氨基酸残基”可包括任何上述氨基酸的l异构体或d异构体。
[0087]
非标准或非天然氨基酸的其他实例包括但不限于对
‑
乙酰基
‑
l
‑
苯丙氨酸、对
‑
碘
‑
l
‑
苯丙氨酸、o
‑
甲基
‑
l
‑
酪氨酸、对炔丙氧基苯丙氨酸、对
‑
炔丙基
‑
苯丙氨酸、l
‑3‑
(2
‑
萘基)丙氨酸、3
‑
甲基
‑
苯丙氨酸、o
‑4‑
烯丙基
‑
l
‑
酪氨酸、4
‑
丙基
‑
l
‑
酪氨酸、三
‑
o
‑
乙酰基
‑
glcnacpβ
‑
丝氨酸、l
‑
多巴、氟化苯丙氨酸、异丙基
‑
l
‑
苯丙氨酸、对
‑
叠氮基
‑
l
‑
苯丙氨酸、对
‑
酰基
‑
l
‑
苯丙氨酸、对
‑
苯甲酰基
‑
l
‑
苯丙氨酸、l
‑
磷酸丝氨酸、磷酸丝氨酸、磷酸酪氨酸、对溴苯丙氨酸、对
‑
氨基
‑
l
‑
苯丙氨酸、异丙基
‑
l
‑
苯丙氨酸、酪氨酸氨基酸的非天然类似物;谷氨酰胺氨基酸的非天然类似物;苯丙氨酸氨基酸的非天然类似物;丝氨酸氨基酸的非天然类似物;苏氨酸氨基酸的非天然类似物;甲硫氨酸氨基酸的非天然类似物;亮氨酸氨基酸的非天然类似物;异亮氨酸氨基酸的非天然类似物;烷基、芳基、酰基、叠氮基、氰基、卤素、肼、酰肼、羟基、烯基、炔基、醚、硫醇、磺酰基、硒基、酯、硫代酸、硼酸盐、硼酸酯、28ufa28hor、膦酰基、膦、杂环、烯酮、亚胺、醛、羟胺、酮或氨基取代的氨基酸,或其组合;具有可光活化交联剂的氨基酸;自旋标记的氨基酸;荧光氨基酸;金属结合氨基酸;含金属的氨基酸;放射性氨基酸;光笼罩的和/或光致异构化氨基酸;含生物素或生物素类似物的氨基酸;含酮的氨基酸;包含聚乙二醇或聚醚的氨基酸;重原子取代的氨基酸;可化学裂解或可光裂解的氨基酸;具有延长侧链的氨基酸;含有毒性基团的氨基酸;糖取代的氨基酸;碳连接的含糖氨基酸;具有氧化还原活性的氨基酸;含α
‑
羟基的酸;麦角氨酸(amino thio acid);α,α双取代氨基酸;β
‑
氨基酸;γ
‑
氨基酸,脯氨酸或组氨酸以外的环状氨基酸,苯丙氨酸、酪氨酸或色氨酸以外的芳香族氨基酸。
[0088]
如本文所用,“肽”被定义为氨基酸的短聚合物,其长度通常为20个或更少个氨基酸,更通常长度为12个或更少个氨基酸(garrett&grisham,biochemistry,第2版,1999,brooks/cole,110)。在一些实施方案中,如本文所考虑的肽可包括不超过约2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20个氨基酸。多肽,也称为蛋白质,通常具有>100个氨基酸的长度(garrett&grisham,biochemistry,第2版,1999,brooks/cole,110)。如本文所考虑的多肽可包含但不限于100、101、102、103、104、105、约110、约120、约130、约140、约150、约160、约170、约180、约190、约200、约210、约220、约230、约240、约250、约275、约300、约325、约350、约375、约400、约425、约450、约475、约500、约525、约550、约575、约600、约625、约650、约675、约700、约725、约750、约775、约800、约825、约850、约875、约900、约925、约950、约975、约1000、约1100、约1200、约1300、约1400、约1500、约1750、约2000、约2250、约2500个或更多个氨基酸残基。
[0089]
如本文所考虑的肽或多肽可以被进一步修饰以包括非氨基酸部分。修饰可以包括但不限于酰化(例如,o
‑
酰化(酯)、n
‑
酰化(酰胺)、s
‑
酰化(硫酯))、乙酰化(例如,在蛋白质的n
‑
末端或在赖氨酸残基处添加乙酰基)、甲酰化脂酰化(例如,硫辛酸酯、c8官能团的附接)、肉豆蔻酰化(例如,肉豆蔻酸酯、c14饱和酸的附接)、棕榈酰化(例如,棕榈酸酯、c16饱和酸的附接)、烷基化(例如,烷基的添加,例如在赖氨酸或精氨酸残基处添加甲基)、异戊二烯化或戊二烯化(例如,添加类异戊二烯基团,例如法呢醇或香叶基香叶醇)、在c
‑
末端的酰胺化、糖基化(例如,在天冬酰胺、羟赖氨酸、丝氨酸或苏氨酸上添加糖基,产生糖蛋白)、糖化(被认为是糖的非酶促附接)、聚唾液酸化(例如,添加聚唾液酸)、糖基磷脂酰肌醇化
(glypiation)(例如,糖基磷脂酰肌醇(gpi)锚形成、羟基化、碘化(例如甲状腺激素的)和磷酸化(例如,添加磷酸基团,通常添加到丝氨酸、酪氨酸、苏氨酸或组氨酸)。
[0090]
本文公开的修饰的氨基酸序列可以包括一个或多个氨基酸的缺失。如本文所用,“缺失”是指相对于天然氨基酸序列去除一个或多个氨基酸。本文公开的修饰的氨基酸序列可以包括一个或多个氨基酸的插入。如本文所用,“插入”是指向天然氨基酸序列添加一个或多个氨基酸。本文公开的修饰的氨基酸序列可以包括一个或多个氨基酸的取代。如本文所用,“取代”意指用对氨基酸序列而言非天然的氨基酸替换天然氨基酸序列的氨基酸。例如,本文公开的修饰的氨基序列可以包括一个或多个缺失、插入和/或取代,以便修饰靶蛋白的天然氨基酸序列以包括被n
‑
糖基转移酶糖基化的一个或多个异源氨基酸基序。
[0091]
关于蛋白质,“缺失”是指导致一个或多个氨基酸残基的不存在的氨基酸序列的变化。缺失可以去除至少1、2、3、4、5、10、20、50、100、200或更多个氨基酸残基。缺失可包括内部缺失和/或末端缺失(例如,参考多肽的n
‑
末端截短、c
‑
末端截短或两者)。参考多肽序列的“变体”、“突变体”或“衍生物”可以包括相对于参考多肽序列的缺失。
[0092]
关于蛋白质,“片段”是与参考序列在序列上相同但长度比参考序列短的氨基酸序列的一部分。片段可以包含多至参考序列的整个长度,减去至少一个氨基酸残基。例如,片段可分别包含参考多肽的5至1000个连续氨基酸残基。在一些实施方案中,片段可包含参考多肽的至少5、10、15、20、25、30、40、50、60、70、80、90、100、150、250或500个连续氨基酸残基。片段可以优先选自分子的某些区域。术语“至少一个片段”包括全长多肽。相对于全长蛋白质,片段可以包括n
‑
末端截短、c
‑
末端截短或这两种截短。参考多肽序列的“变体”、“突变体”或“衍生物”可以包括参考多肽序列的片段。
[0093]
关于蛋白质,词语“插入”和“添加”是指导致一个或多个氨基酸残基的添加的氨基酸序列的变化。插入或添加可指1、2、3、4、5、10、20、30、40、50、60、70、80、90、100、150、200或更多个氨基酸残基。参考多肽序列的“变体”、“突变体”或“衍生物”可以包括相对于参考多肽序列的插入或添加。蛋白质的变体可具有n
‑
末端插入、c
‑
末端插入、内部插入或n
‑
末端插入、c
‑
末端插入和内部插入的任意组合。
[0094]
关于蛋白质,短语“同一性百分比”和“%同一性”是指使用标准化算法比对的至少两个氨基酸序列之间的残基匹配的百分比。氨基酸序列比对的方法是众所周知的。一些比对方法考虑了保守的氨基酸取代。下文更详细解释的此类保守取代通常保留取代位点处的电荷和疏水性,从而保留多肽的结构(并因此保留功能)。氨基酸序列的同一性百分比可以如本领域所理解的那样确定。(参见,例如,美国专利号7,396,664,其通过引用整体并入本文)。国家生物技术信息中心(ncbi)基本局部比对搜索工具(blast)提供了一套常用且可免费获得的序列比较算法,其可从多个来源获得,包括ncbi,bethesda,md.,在其网站上获得。blast软件套件包括各种序列分析程序,包括“blastp”,其用于将已知氨基酸序列与来自各种数据库的其他氨基酸序列进行比对。
[0095]
关于蛋白质,同一性百分比可以在整个确定的多肽序列(例如,如由特定的seq id号确定的)的长度上测量,或可以在较短的长度上测量,例如,在取自更大的、确定的多肽序列的片段的长度(例如至少15、至少20、至少30、至少40、至少50、至少70或至少150个连续残基的片段)上测量。此类长度仅是示例性的,并且应理解,本文、表格、附图或序列表中所示序列支持的任何片段长度可用于描述在其上可测量同一性百分比的长度。
[0096]
本文包含的肽、多肽和蛋白质可以包括或可以被修饰以包括糖基转移酶的氨基酸受体基序。例如,本文包含的肽、多肽和蛋白质可以包括或可以被修饰以包括包含n
‑
x
‑
s/t的氨基酸受体基序,其是本文讨论的n
‑
连接的糖基转移酶(ngt)的氨基酸受体基序(例如,apngt)。
[0097]
关于蛋白质,如本文所考虑的变体、突变体或衍生物的氨基酸序列可以包括相对于参考氨基酸序列的保守氨基酸取代。例如,变体、突变体或衍生物蛋白质可以包括相对于参考分子的保守氨基酸取代。“保守氨基酸取代”是将氨基酸取代为不同氨基酸的那些取代,其中预测该取代对参考多肽的特性干扰最少。换言之,保守氨基酸取代基本上保留了参考多肽的结构和功能。下表提供了本文考虑的示例性保守氨基酸取代的列表:
[0098][0099]
保守氨基酸取代通常保持(a)取代区域中的多肽主链的结构,例如作为β折叠或α螺旋构象,(b)在取代位点处分子的电荷或疏水性,和/或(c)大部分侧链。非保守氨基酸通常破坏(a)取代区域中的多肽主链的结构,例如,作为β折叠或α螺旋构象,(b)在取代位点处分子的电荷或疏水性,和/或(c)大部分侧链。
[0100]
本文所述或公开的蛋白质、突变体、变体可以具有由参考多肽展示的一种或多种功能或生物活性(例如,由野生型蛋白质展示的一种或多种功能或生物活性)。
[0101]
所公开的蛋白质可以是基本上分离的或纯化的。术语“基本上分离或纯化”是指从其天然环境中去除的蛋白质,并且至少60%不含,优选至少75%不含,以及更优选至少90%不含,甚至更优选至少95%不含与它天然相关的其他组分。
[0102]
无细胞蛋白质合成(cfps)
[0103]
本文公开的组分、系统和方法可以应用于本领域已知的无细胞蛋白质合成方法。参见,例如,美国专利号5,478,730;5,556,769;5,665,563;6,168,931;6,548,276;6,869,774;6,994,986;7,118,883;7,186,525;7,189,528;7,235,382;7,338,789;7,387,884;7,399,610;7,776,535;7,817,794;8,703,471;8,298,759;8,715,958;8,734,856;8,999,668;和9,005,920。还参见美国公开申请号2018/0016614,2018/0016612,2016/0060301,
2015
‑
0259757,2014/0349353,2014
‑
0295492,2014
‑
0255987,2014
‑
0045267,2012
‑
0171720,2008
‑
0138857,2007
‑
0154983,2005
‑
0054044,和2004
‑
0209321。还参见美国公开申请号2005
‑
0170452;2006
‑
0211085;2006
‑
0234345;2006
‑
0252672;2006
‑
0257399;2006
‑
0286637;2007
‑
0026485;2007
‑
0178551。还参见公开的pct国际申请号2003/056914;2004/013151;2004/035605;2006/102652;2006/119987;和2007/120932。还参见jewett,m.c.,hong,s.h.,kwon,y.c.,martin,r.w.,和des soye,b.j.2014,“methods for improved in vitro protein synthesis with proteins containing non standard amino acids,”美国专利申请系列号:62/044,221;jewett,m.c.,hodgman,c.e.,和gan,r.2013,“methods for yeast cell
‑
free protein synthesis,”美国专利申请系列号:61/792,290;jewett,m.c.,j.a.schoborg,和c.e.hodgman.2014,“substrate replenishment and byproduct removal improve yeast cell
‑
free protein synthesis,”美国专利申请系列号:61/953,275;和jewett,m.c.,anderson,m.j.,stark,j.c.,hodgman,c.e.2015,“methods for activating natural energy metabolism for improved yeast cell
‑
free protein synthesis,”美国专利申请系列号:62/098,578。还参见guarino,c.,&delisa,m.p.(2012).a prokaryote
‑
based cell
‑
free translation system that efficiently synthesizes glycoproteins.glycobiology,22(5),596
‑
601。所有这些参考文献的内容通过引用整体并入本技术。
[0104]
在一些实施方案中,“cfps反应混合物”通常可包含粗制或部分纯化的细胞提取物、rna翻译模板和用于促进从rna翻译模板的无细胞蛋白质合成的合适的反应缓冲液中的一种或多种。在一些方面,cfps反应混合物可以包括外源rna翻译模板。在其他方面,cfps反应混合物可以包括编码与dna依赖性rna聚合酶的启动子元件可操作地连接的开放阅读框的dna表达模板。在这些其他方面,cfps反应混合物还可包括dna依赖性rna聚合酶以指导编码开放阅读框的rna翻译模板的转录。在这些其他方面,cfps反应混合物中可以包含额外的ntp和二价阳离子辅因子。如果反应混合物包含实现反应所需的所有试剂,则称其为完全反应混合物,如果其仅包含一部分必需试剂,则称其为不完全反应混合物。本领域普通技术人员将理解,反应组分通常作为单独的溶液储存,每个溶液包含总组分的一个子集,这是出于方便、储存稳定性的原因,或以允许组分浓度的应用依赖性调整,并且在反应之前将反应组分合并以产生完全反应混合物。此外,本领域普通技术人员将理解,为了商业化,反应组分被分开包装,并且有用的商业试剂盒可以包含本发明的反应组分的任何子集。
[0105]
所公开的无细胞蛋白质合成系统可以利用粗制的和/或至少部分分离和/或纯化的组分。如本文所用,术语“粗制”可以指通过破碎和裂解细胞获得的组分,并且至多最低限度地纯化来自破碎和裂解的细胞的粗制组分,例如通过离心破碎和裂解的细胞并从离心后的上清液和/或沉淀收集粗制组分。术语“分离的或纯化的”是指从其天然环境中去除的组分,并且至少60%不含,优选至少75%不含,以及更优选至少90%不含,甚至更优选至少95%不含与它天然相关的其他组分。
[0106]
如本文所用,多肽的“翻译模板”是指来自表达模板的转录的rna产物,其可被核糖体用于合成多肽或蛋白质。
[0107]
如本文所用,术语“反应混合物”是指含有进行给定反应所需的试剂的溶液。如果反应混合物包含进行反应所需的所有试剂,则该反应混合物被称为完全反应混合物。反应
混合物的组分可以分别储存在单独的容器中,每个容器包含全部组分中的一种或多种。组分可以单独包装用于商业化,并且有用的商业试剂盒可以包含反应混合物的反应组分中的一种或多种。
[0108]
反应混合物可以包括表达模板、翻译模板或表达模板和翻译模板两者。表达模板用作用于转录至少一种rna的底物,该rna可以翻译成序列确定的生物聚合物(例如,多肽或蛋白质)。翻译模板是一种rna产物,其可以被核糖体用来合成序列确定的生物聚合物。在某些实施方案中,平台包括表达模板和翻译模板。在某些特定实施方案中,反应混合物可包含偶联的转录/翻译(“tx/tl”)系统,其中从相同细胞提取物合成翻译模板和序列确定的生物聚合物。
[0109]
反应混合物可以包含能够从表达模板产生翻译模板的一种或多种聚合酶。聚合酶可以外源提供或可以从用于制备提取物的生物体提供。在某些特定实施方案中,聚合酶由存在于用于制备提取物的生物体中的质粒和/或用于制备提取物的生物体的基因组中的整合位点表达。
[0110]
改变cfps反应的物理化学环境以更好地模拟细胞质可以改善蛋白质合成活性。以下参数可以单独考虑或与一种或多种其他组分结合考虑以改善基于粗制细胞提取物(例如,s12、s30和s60提取物)的稳健cfps反应平台。
[0111]
温度可以是适合于cfps的任何温度。温度可在约10℃至约40℃的一般范围内,包括该一般范围内的中间特定范围,包括约15℃至约35℃、约15℃至约30℃,约15℃至约25℃。在某些方面,反应温度可以是约15℃、约16℃、约17℃、约18℃、约19℃、约20℃、约21℃、约22℃、约23℃、约24℃、约25℃。
[0112]
反应混合物可以包括适用于cfps的任何有机阴离子。在某些方面,有机阴离子可以是谷氨酸根、乙酸根等。在某些方面,有机阴离子的浓度独立地在约0mm至约200mm的一般范围内,包括该一般范围内的中间特定值,例如约0mm、约10mm、约20mm、约30mm、约40mm、约50mm、约60mm、约70mm、约80mm、约90mm、约100mm、约110mm、约120mm、约130mm、约140mm、约150mm、约160mm、约170mm、约180mm、约190mm和约200mm,等等。
[0113]
反应混合物可以包括适用于cfps的任何卤化物阴离子。在某些方面,卤化物阴离子可以是氯化物、溴化物、碘化物等。优选的卤化物阴离子是氯化物。通常,卤化物阴离子(如果存在于反应中)的浓度在约0mm至约200mm的一般范围内,包括该一般范围内的中间特定值,例如本文一般公开的用于有机阴离子的那些。
[0114]
反应混合物可以包括适用于cfps的任何有机阳离子。在某些方面,有机阳离子可以是多胺,例如亚精胺或腐胺等。优选多胺存在于cfps反应中。在某些方面,反应中有机阳离子的浓度通常可为约0mm至约3mm、约0.5mm至约2.5mm、约1mm至约2mm。在某些方面,可以存在多于一种有机阳离子。
[0115]
反应混合物可以包括适用于cfps的任何无机阳离子。例如,合适的无机阳离子可包括一价阳离子,例如钠、钾、锂等;和二价阳离子,例如镁、钙、锰等。在某些方面,无机阳离子是镁。在这样的方面,镁浓度可以在约1mm至约50mm的一般范围内,包括在这个一般范围内的中间特定值,例如约1mm、约2mm、约3mm、约5mm、约6mm、约7mm、约8mm、约9mm、约10mm等。在优选的方面,无机阳离子的浓度可在约4mm至约9mm的特定范围内,更优选在约5mm至约7mm的范围内。
[0116]
反应混合物可以包括内源性ntp(即,存在于细胞提取物中的ntp)和/或外源性ntp(即,添加到反应混合物中的ntp)。在某些方面,反应使用atp、gtp、ctp和utp。在某些方面,个体ntp的浓度在约0.1mm至约2mm的范围内。
[0117]
反应混合物可以包括适用于cfps的任何醇。在某些方面,醇可以是多元醇,更具体地是甘油。在某些方面,醇在约0%(v/v)至约25%(v/v)的一般范围内,包括约5%(v/v)、约10%(v/v)和约15%(v/v)和约20%(v/v)等的特定中间值。
[0118]
在某些示例性实施方案中,本文所述的一种或多种方法在容器例如单个容器中进行。如本文所用,术语“容器”是指适合容纳本文所述的一种或多种反应物(例如,用于一个或多个转录、翻译和/或糖基化步骤)的任何容器。容器的实例包括但不限于微量滴定板、试管、微量离心管、烧杯、烧瓶、多孔板、比色皿、流动系统、微纤维、显微镜载玻片等。
[0119]
蛋白质的糖基化
[0120]
本文公开的组分、系统和方法可以应用于重组细胞系统和无细胞蛋白质合成方法以制备糖基化蛋白质。可以使用所公开的组分、系统和方法制备的糖基化蛋白质可以包括具有n
‑
连接的糖基化(即,附接至天冬酰胺的氮的聚糖)的蛋白质。本文公开的糖基化蛋白质可以包括由本领域已知的单糖(例如葡萄糖(例如,β
‑
d
‑
葡萄糖)、半乳糖(例如,β
‑
d
‑
半乳糖)、甘露糖(例如,β
‑
d
‑
甘露糖)、岩藻糖(例如,α
‑
l
‑
岩藻糖)、n
‑
乙酰基
‑
葡糖胺(glcnac)、n
‑
乙酰基
‑
半乳糖胺(galnac)、n
‑
乙酰基
‑
葡糖胺、丙酮酸、神经氨酸、n
‑
乙酰神经氨酸(即唾液酸)和木糖,它们可以通过各自的糖基转移酶附接至糖基化的蛋白质、生长的聚糖链或供体分子(例如,糖供体核苷酸))组成的无支链和/或支链糖链。用于糖基化蛋白质的其他单糖可以包括阿洛糖、阿卓糖、古洛糖、艾杜糖、塔罗糖、核糖、阿拉伯糖、来苏糖。用于糖基化蛋白质的其他单糖可包括脱氧单糖,例如脱氧核糖。此外,由于非天然糖独特的生物物理特性(包括表面电荷和氢键合)、与内源性受体(包括凝集素和siglec)的独特结合特征、通过双正交或半双正交缀合方法(包括点击化学和迈克尔加成)进一步修饰的潜力以及它们被物理降解或酶促降解或去除(包括通过糖苷酶)的能力的差异,非天然糖也可用于糖基化蛋白质。这些非天然糖包括但不限于具有叠氮基、炔烃或应变炔烃/烯烃官能团糖(包括叠氮基唾液酸,(叠氮基
‑
sia))的糖;具有硫醇或马来酰亚胺基团的糖;脱氧糖;聚乙二醇化的糖;氨基糖;含有天然和/或非天然单体的预组装的寡糖或多糖;氟化糖;和其它的。
[0121]
原核生物中的糖基化
[0122]
原核生物中的糖基化是本领域已知的。(参见,例如,美国专利号8,703,471;和8,999,668;和美国公开申请号2005/0170452;2006/0211085;2006/0234345;2006/0252672;2006/0257399;2006/0286637;2007/0026485;2007/0178551;和国际公开申请wo2003/056914a1;wo2004/035605a2;wo2006/102652a2;wo2006/119987a2;和wo2007/120932a2;其全部内容通过引用整体并入本文)。
[0123]
用于产生糖蛋白和鉴定糖基化途径的模块化平台
[0124]
发明人已经公开了用于在体外和体内的糖蛋白蛋白质合成的组分、系统和方法。特别地,发明人已经公开了与用于产生糖蛋白的模块化平台相关的组分、系统和方法。发明人公开的组分、系统和方法可用于在无细胞蛋白质合成(cfps)和经修饰的细胞中合成糖蛋白和重组糖蛋白。
[0125]
在一个实施方案中,发明人公开了一种用于在体外对肽或多肽序列进行糖基化的
无细胞系统。肽或多肽序列可以存在于肽(即相对较短的氨基酸序列)或多肽(即相对较长的氨基酸序列)中,肽或多肽序列通常包含天冬酰胺残基,其可通过n
‑
连接的糖基转移酶糖基化。例如,肽或多肽序列可以包含氨基酸基序n
‑
x
‑
s/t。所公开的系统可包含以下组分:(i)糖基转移酶,其是可溶的n
‑
连接的糖基转移酶(如本文所用的术语“n
‑
连接的糖基转移酶”和“n
‑
糖基转移酶”和“ngt”可互换使用),其催化将单糖(任选地,其中单糖是葡萄糖(glc))转移至天冬酰胺残基的氨基以提供n
‑
连接的聚糖,或在无细胞蛋白质合成(cfps)反应混合物中表达ngt的表达载体;(ii)包含单糖供体(任选地,glc供体;任选地,单糖;如本文所用的术语“单糖供体”包括但不限于单糖和多糖)的糖基化混合物;其中所述肽或多肽序列在体外在所述糖基化混合物中被糖基化以提供包含n
‑
连接的聚糖(任选地n
‑
连接的glc)的肽或多肽序列。在一些实施方案中,ngt是膜结合的。
[0126]
在所公开系统的进一步实施方案中,该系统还可以包含以下组分:(iii)第二糖基转移酶,其是可溶性的并且催化将单糖转移至n
‑
连接的聚糖(任选地,其中单糖是glc、半乳糖(gal)、n
‑
乙酰半乳糖胺(galnac)、n
‑
乙酰葡糖胺(glcnac)、丙酮酸、岩藻糖(fuc)、唾液酸(sia)),或在无细胞蛋白质合成(cfps)反应混合物中表达第二糖基转移酶的表达载体;其中糖基化混合物包含glc供体、gal供体、galnac供体、glcnac供体、丙酮酸供体、岩藻糖供体、唾液酸供体或其混合物,并且其中n
‑
连接的聚糖被选自glc、gal、galnac、glcnac、丙酮酸、fuc和sia的一种或多种部分糖基化(任选地提供n
‑
连接的右旋糖、n
‑
连接的乳糖或n
‑
连接的glc
‑
galnac)。在一些实施方案中,第二糖基转移酶是膜结合的。
[0127]
在所公开系统的更进一步的实施方案中,该系统还可以包含以下组分:(iv)第三糖基转移酶,其是可溶性的并且催化将单糖转移至n
‑
连接的聚糖(任选地,其中单糖是glc、gal、galnac、glcnac、丙酮酸、fuc、sia或其组合),或在无细胞蛋白质合成(cfps)反应混合物中表达第三糖基转移酶的表达载体;其中糖基化混合物包含glc供体、gal供体、galnac供体、glcnac供体、丙酮酸供体、岩藻糖供体、唾液酸供体或其混合物,并且其中n
‑
连接的聚糖进一步被选自glc、gal、galnac、glcnac、丙酮酸、fuc和sia的一种或多种部分糖基化(任选地以提供包含选自唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac以及αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)的一种或多种部分的n
‑
连接的聚糖)。如本文所用,lacnac与乳糖
‑
(聚)lacnac可互换使用。在一些实施方案中,第三糖基转移酶是膜结合的。
[0128]
所公开的系统可以包括或利用无细胞蛋白质合成(cfps)和/或用于执行cfps的组分。在所公开系统的一些实施方案中,系统包含或利用无细胞蛋白质合成(cfps)反应混合物,并且在cfps反应混合物中存在或表达第一糖基转移酶、第二糖基转移酶和第三糖基转移酶中的一种或多种。在所公开系统的进一步实施方案中,该系统包含或利用一种或多种无细胞蛋白质合成(cfps)反应混合物,并且在cfps反应混合物中存在或表达第一糖基转移酶、第二糖基转移酶和第三糖基转移酶中的一种或多种。任选地,可以组合一种或多种cfps
反应混合物以提供公开的系统和/或公开的系统的组分。在一些实施方案中,可组合一种或多种cfps反应混合物以产生糖基化途径。
[0129]
所公开的系统可用于对肽或多肽序列进行糖基化。在所公开系统的一些实施方案中,系统包含肽或多肽序列,或表达肽或多肽序列的表达载体。任选地,可以在无细胞蛋白质合成(cfps)反应混合物中提供和/或表达肽或多肽序列。
[0130]
合适的cfps反应混合物可包含获自原核细胞的一种或多种组分。例如,用于cfps反应混合物的组分可包括原核细胞裂解物。任选地,细胞裂解物可以富含一种或多种如本文公开的糖基转移酶。在一些实施方案中,cfps反应混合物可包含或利用由大肠杆菌制备的裂解物,任选地其中大肠杆菌已被修饰以表达所公开的系统的一种或多种组分,例如本文所公开的糖基转移酶。
[0131]
所公开的系统通常包含和/或利用第一糖基转移酶。任选地,第一糖基转移酶可以是细菌n
‑
连接的糖基转移酶(ngt)或相对于野生型ngt具有一个或多个突变的修饰的ngt。任选地,细菌ngt是选自以下的细菌ngt:胸膜肺炎放线杆菌(actinobacillus pleuropneumoniae)(apngt)(seq id no:1)、大肠杆菌(escherichia coli)ngt(ecngt)(seq id no:3)、流感嗜血杆菌(haemophilus influenza)ngt(hingt)(seq id no:5)、溶血曼海姆菌(mannheimia haemolytica)ngt(mhngt)(seq id no:7)、杜雷嗜血杆菌(haemophilus dureyi)ngt(hdngt)(seq id no:9)、海藻百伯史坦菌(bibersteinia trehalosi)ngt(btngt)(seq id no:11)、嗜沫聚合杆菌(aggregatibacter aphrophilus)ngt(aangt)(seq id no:13)、小肠结肠炎耶尔森菌(yersinia enterocolitica)(yengt)ngt(seq id no:15)、鼠疫耶尔森菌(yersinia pestis)(ypngt)ngt(seq id no:17)和金格金氏杆菌(kingella kingae)(kkngt)ngt(seq id no:19)。在一些实施方案中,ngt是可溶的。在一些实施方案中,ngt是膜结合的。可用于本发明的组合物和方法的其他ngt可以在pct/us2018/000185中找到,例如具有q469a突变的胸膜肺炎放线杆菌(apngt)糖基转移酶(ngt)。
[0132]
在一些实施方案中,所公开的系统可以包含和/或可以表达用于所公开的方法的糖基转移酶,例如包含一个或多个突变(例如,改变肽受体特异性和/或增加酶促周转率的突变)的经修饰的细菌ngt。(参见song等人,“production of homogeneous glycoprotein with multisite modifications by an engineered n
‑
glycosyltransferase mutant,”j.biol.chem.,april 5,2017,292,8856
‑
8863,其内容通过引用整体并入本文)。在一些实施方案中,经修饰的细菌ngt是在q469处具有取代的修饰的apngt,例如其中q469被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q469a的seq id no:2)。在一些实施方案中,经修饰的细菌ngt是在f482处具有取代的修饰的ecngt,其中f482被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有f482a的seq id no:4)。在一些实施方案中,经修饰的细菌ngt是在q495处具有取代的修饰的hingt,其中q495被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q495a的seq id no:6)。在一些实施方案中,经修饰的细菌ngt是在q469处具有取代的修饰的mhngt,其中q469被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q469a的seq id no:8)。在一些实施方案中,经修饰的细菌ngt是在q468处具有取代的修饰的hdngt,其中q468被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q468a的seq id no:10)。在一些实施方案中,
经修饰的细菌ngt是在q471处具有取代的修饰的btngt,其中q471被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q471a的seq id no:12)。在一些实施方案中,经修饰的细菌ngt是在q468处具有取代的修饰的aangt,其中q468被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q468a的seq id no:14)。在一些实施方案中,经修饰的细菌ngt是在f466处具有取代的修饰的yengt,其中f466被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有f466a的seq id no:16)。在一些实施方案中,经修饰的细菌ngt是在f466处具有取代的修饰的ypngt,其中f466被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有f466a的seq id no:18)。在一些实施方案中,经修饰的细菌ngt是在q474处具有取代的修饰的kkngt,其中q474被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q474a的seq id no:20)。
[0133]
在一些实施方案中,所公开的系统可包括和/或可表达具有seq id no:1、3、5、7、9、11、13、15、17或19中任一个的氨基酸序列或与seq id no:1、3、5、7、9、11、13、15、17或19中的任一个具有至少50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性的糖基转移酶,或第一糖基转移酶是经修饰的细菌n
‑
连接的糖基转移酶(ngt),其具有seq id no:2、4、6、8、10、12、14、16、18或20中任一个的氨基酸序列,或与seq id no:2、4、6、8、10、12、14、16、18或20中的任一个具有至少50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性。
[0134]
所公开的系统可以包括和/或利用第二糖基转移酶。任选地,第二糖基转移酶是细菌糖基转移酶。任选地,第二糖基转移酶是α1
‑
6葡萄糖基转移酶、β1
‑
4半乳糖基转移酶或β1
‑
3n
‑
乙酰半乳糖胺转移酶。任选地,第二糖基转移酶选自胸膜肺炎放线杆菌α1
‑
6葡萄糖基转移酶(apα1
‑
6)、淋病奈瑟菌(neisseria gonorrhoeae)β1
‑
4半乳糖基转移酶lgtb(nglgtb)、脑膜炎奈瑟菌(neisseria meningitidis)β1
‑
4半乳糖基转移酶lgtb(nmlgtb)和脆弱拟杆菌(bacteriodes fragilis)β1
‑
3n
‑
乙酰半乳糖胺转移酶(bfgalnact)。
[0135]
所公开的系统可以包括和/或利用第三糖基转移酶。任选地,第三糖基转移酶是细菌糖基转移酶。任选地,第三糖基转移酶是β1
‑
3n
‑
乙酰葡糖胺转移酶、丙酮酸转移酶、α1
‑
3岩藻糖基转移酶、α1
‑
2岩藻糖基转移酶、α1
‑
4半乳糖基转移酶、α1
‑
3半乳糖基转移酶、α2
‑
6唾液酸转移酶、α2
‑
3,6唾液酸转移酶、α2
‑
3唾液酸转移酶或α2
‑
3,8唾液酸转移酶。任选地,第三糖基转移酶选自淋病奈瑟菌β1
‑
3n
‑
乙酰葡糖胺转移酶(nglgta)、粟酒裂殖酵母(schizosaccharomyces pombe)丙酮酸转移酶(sppvg1)、幽门螺杆菌(helicobacter pylori)α1
‑
3岩藻糖基转移酶(hpfuta)、幽门螺杆菌α1
‑
2岩藻糖基转移酶(hpfutc)、脑膜炎奈瑟菌α1
‑
4半乳糖基转移酶(nmlgtc)、牛(bos taurus)α1
‑
3半乳糖基转移酶(btggta)、智人(homo sapiens)α2
‑
6唾液酸转移酶(hssiat1)、美人鱼发光杆菌(photobacterium damselae)α2
‑
6唾液酸转移酶(pdst6)、鳆发光杆菌(photobacterium leiognathid)α2
‑
6唾液酸转移酶(plst6)、多杀巴斯德氏菌(pasteurella multocida)α2
‑
3,6唾液酸转移酶(pmst3,6)、弧菌属(vibrio sp)jt
‑
faj
‑
16α2
‑
3唾液酸转移酶(vsst3)、明亮发光杆菌(photobacterium phosphoreum)α2
‑
3唾液酸转移酶(ppst3)、空肠弯曲杆菌(campylobacter jejuni)α2
‑
3唾液酸转移酶(cjcst
‑
i)和空肠弯曲杆菌α2
‑
3,8唾液酸转移酶(cjcst
‑
ii)。
[0136]
所公开的系统的一个或多个组分可以是保存的形式。在一些实施方案中,所公开
的系统的一种或多种组分是冷冻干燥的。
[0137]
还公开了包含n
‑
连接的聚糖的肽或多肽序列。任选地,公开的肽或多肽序列使用本文公开的任何系统或使用本文公开的系统的任何组分制备。在一些实施方案中,肽或多肽序列包含n
‑
连接的聚糖,其中该n
‑
连接的聚糖包含选自唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac以及αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)的部分。在一些实施方案中,公开了包含在α1,2或α1,3键联中添加了一个或多个岩藻糖和/或在α2,3或α2,6键联中添加了一个或多个唾液酸的形式的乳糖或乳糖
‑
(聚)lacnac的肽或多肽。在一些实施方案中,所公开的肽或多肽可被利用或配制以用作治疗性蛋白质或疫苗。如本文所用,术语lacnac与乳糖
‑
(聚)lacnac可互换使用。
[0138]
本文还公开了经修饰的细胞。所公开的经修饰的细菌细胞可以包括经修饰的细菌细胞,例如基因修饰的细菌细胞。基因修饰的细菌细胞可包括其中细胞的基因组已被修饰以表达异源蛋白质(例如,异源糖基转移酶或用于糖基化的肽或多肽序列)的细胞和已被表达异源蛋白质(例如,用于糖基化的异源糖基转移酶或肽或多肽序列)的表观遗传载体转化的细胞。所公开的经修饰的细胞可以包含和/或表达本文公开的系统的一种或多种组分。所公开的经修饰的细胞可用于制备本文公开的系统的一种或多种组分。所公开的经修饰的细胞可过表达特定蛋白质或可缺乏特定蛋白质的表达。例如但不作为限制,在一些实施方案中,经修饰的细胞或细胞裂解物可能缺乏nana(唾液酸醛缩酶),产生减少量的nana(唾液酸醛缩酶),或表达无功能或功能降低的nana(唾液酸醛缩酶)。
[0139]
在一些实施方案中,经修饰的细胞和/或经修饰的细胞的组分可用于本文公开的方法中以对肽或多肽序列进行糖基化。在公开的用于体内制备糖基化肽或多肽序列的方法的一些实施方案中,所述方法包括培养经修饰的细菌细胞,其中所述经修饰的细菌细胞包含或表达用于糖基化的肽或多肽序列、n
‑
连接的糖基转移酶和/或一种或多种额外的糖基转移酶,并且肽或多肽序列在经修饰的细菌细胞中或在糖基化反应混合物中被糖基化。在一些实施方案中,体内糖基化包括非天然糖(例如,叠氮基修饰的糖,包括叠氮基唾液酸)。
[0140]
在一些实施方案中,经修饰的细胞的组分可用于无细胞蛋白质合成cfps方法和/或糖基化反应方法。从经修饰的细胞制备的组分可包括但不限于细胞裂解物,任选其中裂解物单独地或与从其他经修饰的细胞制备的细胞裂解物组合地适用于cfps反应方法和/或糖基化反应方法。
[0141]
本文还公开了体外制备糖基化肽或多肽序列的方法。所述方法可包括使包含天冬酰胺残基的肽或多肽序列(例如包含氨基酸基序n
‑
x
‑
s/t的肽或多肽序列)在包含单糖供体(任选其中单糖供体是葡萄糖(glc)供体,或其中单糖供体是单糖)的糖基化混合物中与糖基转移酶反应,所述糖基转移酶是可溶性n
‑
连接的糖基转移酶(如本文所用,术语“n
‑
连接的糖基转移酶”、“n
‑
糖基转移酶”和“ngt”可互换使用),其催化将来自单糖供体的单糖(任选地来自glc供体的glc或其中单糖供体是单糖)转移至天冬酰胺残基的氨基,以提供n
‑
连
接的聚糖(任选地,n
‑
连接的glc)。在公开的方法中,所述肽或多肽序列在体外在所述糖基化混合物中被糖基化以提供包含n
‑
连接的聚糖(任选地n
‑
连接的glc)的肽或多肽序列。任选地,在公开的体外方法中,肽或多肽序列、ngt或两者可以在进行糖基化反应之前在一种或多种无细胞蛋白质合成(cfps)反应混合物中表达。任选地,肽或多肽序列可以在第一cfps反应混合物中表达,和/或ngt可以在第二cfps反应混合物中表达,并且该方法可以包括组合第一cfps反应混合物和第二cfps反应混合物以对肽或多肽序列进行糖基化。
[0142]
在公开的体外方法的一些实施方案中,该方法进一步包括使包含n
‑
连接的glc聚糖的肽与第二糖基转移酶反应,所述第二糖基转移酶是可溶性的并且催化将单糖转移至n
‑
连接的聚糖(任选地,其中单糖是glc、半乳糖(gal)、n
‑
乙酰半乳糖胺(galnac)、n
‑
乙酰葡糖胺(glcnac)、丙酮酸、岩藻糖(fuc)、唾液酸(sia)、非标准糖例如包含在c5或c9用叠氮基位置官能化的唾液酸的叠氮基糖、具有炔烃的糖或应变炔烃/烯烃官能团糖(包括叠氮基唾液酸);具有硫醇或马来酰亚胺基团的糖;脱氧糖;聚乙二醇化的糖;氨基糖;含有天然和/或非天然单体的预组装的寡糖或多糖;氟化糖;及其组合,其中糖基化混合物包含glc供体、gal供体、galnac供体、glcnac供体、丙酮酸供体、岩藻糖供体、唾液酸供体、叠氮基唾液酸供体或其混合物。然后将n
‑
连接的聚糖糖基化以提供包含选自glc、gal、galnac、glcnac、丙酮酸、fuc和sia的一个或多个部分的n
‑
连接的聚糖(任选地提供n
‑
连接的右旋糖、n
‑
连接的乳糖或n
‑
连接的glc
‑
galnac),任选地其中第二寡核苷酸转移酶在进行糖基化之前在无细胞蛋白质合成(cfps)反应混合物中表达。任选地,肽或多肽序列可以在第一cfps反应混合物中表达,ngt可以在第二cfps反应混合物中表达,和/或第二糖基转移酶可以在第三cfps反应混合物中表达,并且该方法可以包括组合第一cfps反应混合物、第二cfps反应混合物和/或第三反应混合物中的两种或更多种以对肽或多肽序列进行糖基化。
[0143]
在公开的体外方法的一些实施方案中,该方法进一步包括使包含聚糖的肽与第三糖基转移酶反应,该第三糖基转移酶是可溶性的并且催化将单糖转移至n
‑
连接的聚糖(任选地,其中单糖是glc、gal、galnac、glcnac、丙酮酸、fuc、sia或非标准糖例如叠氮基糖,其中糖基化混合物包含glc供体、gal供体、galnac供体、glcnac供体、丙酮酸供体、岩藻糖供体、唾液酸供体、叠氮基唾液酸供体、非天然糖供体例如叠氮基糖供体,包括在c5或c9用叠氮基位置官能化的唾液酸的供体,或其混合物,并且其中n
‑
连接的聚糖进一步被选自glc、gal、galnac、glcnac、丙酮酸、fuc、sia和非标准糖的一个或多个部分糖基化,非标准糖是例如具有叠氮基、炔烃或应变炔烃/烯烃官能团糖(包括叠氮基唾液酸)的糖;具有硫醇或马来酰亚胺基团的糖;脱氧糖;聚乙二醇化的糖;氨基糖;含有天然和/或非天然单体的预组装的寡糖或多糖;氟化糖;和其他的。然后将n
‑
连接的聚糖进一步糖基化以提供包含选自唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac以及αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)的一种或多种部分的n
‑
连接的聚糖。任选地,肽或多肽序列可以在第一cfps反应混合物中表达,ngt可以在第二cfps反应混合物中表达,第二糖基
转移酶可以在第三cfps反应混合物中表达,和/或第三糖基转移酶可以在第四cfps反应混合物中表达,并且该方法可以包括将第一cfps反应混合物、第二cfps反应混合物、第三反应混合物和/或第四反应混合物中的两个或更多个组合以对肽或多肽序列进行糖基化。
[0144]
用于所公开方法的合适的cfps反应混合物可以包括原核cfps反应混合物。在一些实施方案中,合适的cfps反应混合物可包括原核cfps反应混合物,所述原核cfps反应混合物包含由大肠杆菌制备的裂解物。
[0145]
在一些实施方案中,用于所公开方法的cfps反应混合物可以包含和/或可以表达所公开的方法中用于糖基化的肽或多肽序列(例如,包含氨基酸基序n
‑
x
‑
s/t的肽或多肽序列或经工程化以包含氨基酸基序n
‑
x
‑
s/t的肽或多肽序列,其中氨基酸基序n
‑
x
‑
s/t并非天然存在于肽或多肽序列中。
[0146]
在一些实施方案中,所公开的方法可包括和/或可利用细菌ngt,其任选地选自胸膜肺炎放线杆菌(apngt)(seq id no:1)或其具有以下取代q469a的衍生物、大肠杆菌ngt(ecngt)(seq id no:3)、流感嗜血杆菌ngt(hingt)(seq id no:5)、溶血曼海姆菌ngt(mhngt)(seq id no:7)、杜雷嗜血杆菌ngt(hdngt)(seq id no:9)、海藻百伯史坦菌ngt(btngt)(seq id no:11)、嗜沫聚合杆菌ngt(aangt)(seq id no:13)、小肠结肠炎耶尔森菌ngt(yengt)(seq id no:15)、鼠疫耶尔森菌ngt(ypngt)(seq id no:17)和金格金氏杆菌ngt(kkngt)(seq id no:19)。任选地,细菌ngt可以是相对于野生型细菌ngt具有一个或多个突变的经修饰的细菌ngt。
[0147]
在一些实施方案中,所公开的方法可以包括或利用修饰的ngt,例如包含一个或多个突变(例如改变肽受体特异性和/或增加酶周转率的突变)的经修饰的细菌ngt。(参见song等人,“production of homogeneous glycoprotein with multisite modifications by an engineered n
‑
glycosyltransferase mutant,”j.biol.chem.,april 5,2017,292,8856
‑
8863,其内容通过引用整体并入全文)。在一些实施方案中,经修饰的细菌ngt是在q469处具有取代的修饰的apngt,例如其中q469被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q469a的seq id no:2)。在一些实施方案中,经修饰的细菌ngt是在f482处具有取代的修饰的ecngt,其中f482被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有f482a的seq id no:4)。在一些实施方案中,经修饰的细菌ngt是在q495处具有取代的修饰的hingt,其中q495被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q495a的seq id no:6)。在一些实施方案中,经修饰的细菌ngt是在q469处具有取代的修饰的mhngt,其中q469被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q469a的seq id no:8)。在一些实施方案中,经修饰的细菌ngt是在q468处具有取代的修饰的hdngt,其中q468被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q468a的seq id no:10)。在一些实施方案中,经修饰的细菌ngt是在q471处具有取代的修饰的btngt,其中q471被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q471a的seq id no:12)。在一些实施方案中,经修饰的细菌ngt是在q468处具有取代的修饰的aangt,其中q468被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q468a的seq id no:14)。在一些实施方案中,经修饰的细菌ngt是在f466处具有取代的修饰的yengt,其中f466被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有f466a的seq id no:16)。在一些实施方案中,经修饰的细菌ngt是在f466处具有取代的修
饰的ypngt,其中f466被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有f466a的seq id no:18)。在一些实施方案中,经修饰的细菌ngt是在q474处具有取代的修饰的kkngt,其中q474被氨基酸x取代,其中x选自s、t、n、c、g、p、a、i、l、m、v(参见,例如具有q474a的seq id no:20)。
[0148]
在一些实施方案中,所公开的方法可包括和/或可利用具有seq id no:1、3、5、7、9、11、13、15、17或19中任一个的氨基酸序列或与seq id no:1、3、5、7、9、11、13、15、17或19中的任一个具有至少50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性的糖基转移酶,或第一糖基转移酶是经修饰的细菌n
‑
连接的糖基转移酶(ngt),其具有seq id no:2、4、6、8、10、12、14、16、18或20中任一个的氨基酸序列,或与seq id no:2、4、6、8、10、12、14、16、18或20中的任一个具有至少50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性。
[0149]
在一些实施方案中,用于所公开的方法的cfps反应混合物可以包括和/或可以表达用于所公开的方法的糖基转移酶,例如α1
‑
6葡萄糖基转移酶、β1
‑
4半乳糖基转移酶或β1
‑
3n
‑
乙酰半乳糖胺转移酶,任选地选自胸膜肺炎放线杆菌α1
‑
6葡萄糖基转移酶(apα1
‑
6)、淋病奈瑟菌β1
‑
4半乳糖基转移酶lgtb(nglgtb)、脑膜炎奈瑟菌β1
‑
4半乳糖基转移酶lgtb(nmlgtb)和脆弱拟杆菌β1
‑
3n
‑
乙酰半乳糖胺转移酶(bfgalnact)。
[0150]
在一些实施方案中,用于所公开的方法的cfps反应混合物可以包括和/或可以表达,cfps反应混合物可以包括和/或可以表达β1
‑
3n
‑
乙酰葡糖胺转移酶、丙酮酸转移酶、α1
‑
3岩藻糖基转移酶、α1
‑
2岩藻糖基转移酶、α1
‑
4半乳糖基转移酶、α1
‑
3半乳糖基转移酶、α2
‑
6唾液酸转移酶、α2
‑
3,6唾液酸转移酶、α2
‑
3唾液酸转移酶或α2
‑
3,8唾液酸转移酶,任选地选自淋病奈瑟菌β1
‑
3n
‑
乙酰葡糖胺转移酶(nglgta)、粟酒裂殖酵母丙酮酸转移酶(sppvg1)、幽门螺杆菌α1
‑
3岩藻糖基转移酶(hpfuta)、幽门螺杆菌α1
‑
2岩藻糖基转移酶(hpfutc)、脑膜炎奈瑟菌α1
‑
4半乳糖基转移酶(nmlgtc)、牛α1
‑
3半乳糖基转移酶(btggta)、智人α2
‑
6唾液酸转移酶(hssiat1)、美人鱼发光杆菌α2
‑
6唾液酸转移酶(pdst6)、鳆发光杆菌α2
‑
6唾液酸转移酶(plst6)、多杀巴斯德氏菌α2
‑
3,6唾液酸转移酶(pmst3,6)、弧菌属jt
‑
faj
‑
16α2
‑
3唾液酸转移酶(vsst3)、明亮发光杆菌α2
‑
3唾液酸转移酶(ppst3)、空肠弯曲杆菌α2
‑
3唾液酸转移酶(cjcst
‑
i)和空肠弯曲杆菌α2
‑
3,8唾液酸转移酶(cjcst
‑
ii)。
[0151]
还公开了包含n
‑
连接的聚糖并通过任何公开的方法制备的肽、多肽或蛋白质。在一些实施方案中,n
‑
连接的聚糖包含选自唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac以及αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)的部分,任选地其中肽、多肽或蛋白质被用作或配制为治疗剂或疫苗。
[0152]
应用
[0153]
所公开的技术的应用包括但不限于:(i)糖基转移酶特异性和活性的高通量测试,以选择用于在活细胞中的合成或按需制造的最佳酶变体和组合;(ii)本文所述的经发现的
生物合成途径用于糖蛋白的按需合成,其中糖基化酶和靶蛋白均在一锅中合成并且使用糖供体进行补充;(iii)本文所述的经发现的生物合成途径用于在体外或在活大肠杆菌中产生糖蛋白治疗剂、疫苗、诊断剂或分析标准品;(iv)使用本文所述的经发现的生物合成途径在体外或在活大肠杆菌中产生更均质的糖蛋白治疗剂、疫苗、诊断剂或分析标准品;(v)使用在用于体外按需生物制造或用于在活细胞中产生糖蛋白的本工作中描述的体外途径合成用免疫刺激性糖基化结构修饰的疫苗蛋白;(vi)在体外或活细胞中合成具有免疫调节性最小唾液酸基序的过敏疫苗;(vii)使用在用于体外按需生物制造或用于在活细胞中产生糖蛋白的本工作中描述的途径合成用含有唾液酸的聚糖修饰的治疗性蛋白质(包括抗体);(viii)具有半乳糖
‑
α1,3
‑
半乳糖(α
‑
半乳糖或α
‑
gal)的疫苗的无细胞生物合成;(ix)通过点击已知与t调节细胞上的siglec受体相互作用的亲脂性基团来简化致耐受性过敏疫苗的产生;和(x)简化从细菌产生聚乙二醇化蛋白质(无纯化的酶以及与所有ots策略和标准氨基酸化学正交)。
[0154]
优点
[0155]
所公开的技术的优点可以包括但不限于以下方面中的一个或多个。本文所述的糖基化途径提供了针对来自通过n
‑
连接的糖基转移酶(ngt)安装的asn连接的葡萄糖残基的治疗相关的聚糖的几种新的途径。以单糖在细胞质中的ngt安装开始的糖基化途径与现有的化学缀合或寡糖基转移酶糖基化方法相比具有几个优点,因为它们允许在没有真核宿主的情况下对多肽的有效糖基化、跨细胞膜转运、复杂的化学合成或脂质结合的底物和酶。ngt的肽受体特异性也是被充分理解的。最终,这些途径可用于在体外或在活细胞中产生治疗相关的糖蛋白。
[0156]
目前对可以使用的疫苗蛋白或糖缀合物载体蛋白的多样性有严格的限制,因为大多数蛋白不会引发实质性的免疫反应。通过使用本工作中描述的方法用佐剂聚糖修饰疫苗蛋白,有可能改进现有疫苗或使得能够使用更广泛的疫苗蛋白或糖缀合物载体蛋白。
[0157]
许多糖蛋白产生系统导致异质性或不想要的糖型。通过定义在不包含内源性糖基化系统的细菌中的糖基化系统或通过定义体外反应条件,这里描述的方法和途径可以实现产生或更均质的糖蛋白治疗剂。
[0158]
糖蛋白的合理设计和工程改造仍然受限于用于糖蛋白生物合成途径构建的当前方法的通量,这些方法需要对来自活细胞的糖蛋白进行基因操作、表达和分析。发明人的用于蛋白质糖基化途径的合成和原型设计的无细胞平台允许快速测试新的蛋白质糖基化途径。该平台适用于糖基化途径的大规模平行合成和组装、反应条件的轻松操作和自动液体处理。经原型设计后,这些途径可以应用于糖蛋白的体外或体内产生。
[0159]
尽管无细胞生物合成途径原型设计已经被应用于小分子的合成并且一些单酶糖基化过程已经在体外重现,但这是无细胞生物合成原型设计对多酶蛋白糖基化系统的首次应用。
技术领域
[0160]
技术领域涉及使用无细胞蛋白质合成开发新型多酶蛋白质糖基化途径。
[0161]
通过该技术解决的技术问题
[0162]
用于糖蛋白合成的大多数方法使用真核生物(通常是cho细胞)体内的天然途径。
然而,这些方法导致聚糖异质性,限制生物制造宿主的选择,并对已知严重影响蛋白质特性的糖基化结构提供有限的控制,尤其是对于蛋白质治疗剂。这些限制推动了工程化或合成的糖基化系统的开发,无论是通过真核生物(酵母或cho细胞)、细菌系统的细胞工程化还是体外的。其中,在细菌中或体外构建的合成的糖基化系统提供了最密切控制糖基化模式和更快速地开发更多样化糖基化模式的机会。细菌宿主的使用还可以实现更具成本效益的生物制造。
[0163]
已经开发了几种细菌系统来产生蛋白质疫苗或糖基化治疗剂。然而,这些合成的糖基化系统的开发仍然缓慢,因为它需要在活细胞中构建和测试酶的集合(生物合成途径)。因此,细菌中产生的糖基化结构通常局限于可以通过表达自然界中发现的完整操纵子来合成的那些,这严重限制了可以构建的结构的多样性,从而限制了该技术可以用于的应用的多样性。发明人的无细胞糖基化原型设计技术提供了一种快速合成和测试合成糖基化系统的方法。使用该技术,发明人已经发现了几种新的生物合成途径,其可用于在体外或在活细胞中产生糖蛋白治疗剂、疫苗和分析标准品。
[0164]
与现有工作相比,发明人开发的生物合成途径的一个关键区别因素是他们使用可溶性、高活性的n
‑
连接的糖基转移酶(ngt)来将单个糖安装到蛋白质上,然后将该单个糖精心制作成广泛的治疗相关聚糖。这与大多数现有工作形成对比,这些工作使用寡糖基转移酶(ost)将脂质连接的糖供体整体缀合到蛋白质上。ngt的高活性和可溶性性质为在活细胞或体外合成糖蛋白提供了主要的技术优势。然而,用于修饰异源蛋白质的ngt的使用受到限制,这可能是由于缺乏已知的生物合成途径来精心制作安装到治疗相关的糖基化结构的单个糖。到目前为止,只有一项工作(keyes等人,metabolic engineering,2017)证明了ngt的完全生物合成使用来产生治疗相关的聚糖(聚唾液酸)。发明人的工作提供了多种具有更广泛适用性的新糖基化结构,例如具有免疫刺激性糖基化结构的蛋白质疫苗的产生。
[0165]
除了在生命系统中产生蛋白质之外,其他人已经使用全化学合成来通过固相肽合成(spps)构建确定的糖蛋白。虽然可用于小糖肽,但这种方法对于较大的蛋白质变得更加困难,并且不太可能在商业上可用于产生完整糖蛋白蛋白质。还有一些人使用化学合成来产生确定的聚糖,然后将这些聚糖转移至在细胞中产生的完整蛋白质。事实上,这也已经与用ngt修饰蛋白质结合使用(lomino等人,bioorg med chem.,2013)。虽然对于商业应用比全化学合成更有前景,但这种方法仍然需要费力且昂贵的化学步骤来产生聚糖。发明人的技术使用酶来直接在蛋白质上构建聚糖,并且适合在活细胞或一锅式无细胞系统中进行总生物合成产生,从而提供了一种更便宜、更具商业可行性的方法。
[0166]
虽然其他方法已将叠氮基糖掺入细菌中,但其仅将此用于可视化和研究,而非治疗剂的工程化修饰。
[0167]
商业化
[0168]
所公开的技术可以以包括但不限于以下的方式商业化。发明人的无细胞平台允许在体外对多酶糖基化系统进行原型设计,从而允许更快速地开发用于蛋白质糖基化的生物合成途径。在发明人的工作中发现的几种途径可以解决关于哺乳动物细胞中糖蛋白的合成的现有问题,因为它们将允许在细菌中产生治疗相关的糖蛋白以用于大规模产生或在体外产生治疗相关的糖蛋白以用于研究或按需合成应用。具体应用领域包括具有抗原性或免疫调节性聚糖的蛋白质疫苗以及具有延长的半衰期或增加的稳定性的蛋白质治疗剂。
[0169]
价值
[0170]
所公开的技术的价值包括但不限于以下内容。发明人已经描述了使用无细胞系统来原型设计和发现新的糖基化生物合成途径。生物制药公司可能会授权这项技术来针对他们选择的某些糖蛋白进行无细胞原型设计项目,或者直接使用在这项工作中发现的生物合成途径来在体外或在活细胞中产生具有增强的特性的蛋白质治疗剂和疫苗(特别是在蛋白质治疗剂或疫苗上唾液酸的安装和在蛋白质疫苗上α
‑
半乳糖免疫刺激基序的安装)。在这项工作中发现的生物合成途径的脂质非依赖性性质使它们对于体外或细菌细胞质中糖蛋白治疗剂的合成特别有吸引力。这些高滴度、快速表达系统可以允许糖蛋白治疗剂的开发和更快地和以更低的成本产生。
[0171]
其它
[0172]
除非本文另有说明或与上下文明显矛盾,否则本文描述的方法的步骤可以以任何合适的顺序执行。除非本文另有说明或与上下文明显矛盾,否则这些步骤可以重复或反复任意次数以实现期望的目标。
[0173]
本文描述了本发明的优选方面,包括发明人已知的用于实施本发明的最佳模式。在阅读上述描述后,那些优选方面的变化对于本领域普通技术人员来说将变得明显。发明人期望本领域的普通技术人员适当地采用这种变化,并且发明人打算以不同于本文具体描述的方式来实践本发明。因此,本发明包括在适用法律允许的情况下在所附权利要求中记载的主题的所有修改和等效物。此外,除非本文另有说明或与上下文明显矛盾,否则本发明涵盖其所有可能变化形式的上述要素的任何组合。
[0174]
实施方案
[0175]
1.生物合成途径(酶的集合)以及所附手稿中描述的所有糖型的合成模式。
[0176]
2.通过实施方案1的生物合成途径制备的糖型。
[0177]
3.实施方案1中的酶途径在活细胞中的表达,特别是以α
‑
gal和唾液酸终止的聚糖的所证明的实施方案。在一些实施方案中,提供了n
‑
连接的葡萄糖和/或n
‑
连接的乳糖。
[0178]
4.实施方案1中的多肽序列和/或酶作为体外糖基化的手段的用途。
[0179]
5.使用在任何前述实施方案中描述的生物合成途径的糖蛋白的无细胞生物合成。
[0180]
6.使用在任何前述实施方案中描述的生物合成途径的以冻干形式的糖蛋白的无细胞生物合成。
[0181]
7.用于蛋白质糖基化途径的快速原型设计以设计体内生物合成途径的无细胞方法。该方法包括以下步骤中的一个或多个:(i)使用ngt来将引发葡萄糖安装到蛋白质上;(ii)通过混合和匹配富含途径酶的细胞裂解物进行途径在无细胞系统中的组合性组装;(iii)快速体外糖基化途径组装;和(iv)鉴定的用于在体外和体内生产平台中制造糖蛋白的途径的转移。
[0182]
8.权利要求7的实施方案,其中通过无细胞蛋白质合成在裂解物中富集酶。
[0183]
9.权利要求7的实施方案,其中通过在裂解物来源菌株中的过表达富集酶。
[0184]
美国公开申请和专利
[0185]
us2004/0171826;us2004/0018590;us2004/0230042;us2005/0260729;us2005/0170452;us2005/0208617;us2005/0170452;us2006/0148035;us2006/040353;us2006/0286637;us2006/0177898;us2006/0211085;us2006/0024292;us2006/0024304;us2006/
cell
‑
free transcription
‑
translation system enriched with glycosylation machinery.nature communications 9,2686(2018).
[0199]
schoborg,j.a.等人,a cell
‑
free platform for rapid synthesis and testing of active oligosaccharyltransferases.biotechnology and bioengineering(2017).
[0200]
guarino,c.,&delisa,m.p.(2012).a prokaryote
‑
based cell
‑
free translation system that efficiently synthesizes glycoproteins.glycobiology,22(5),596
‑
601.
[0201]
lizak,c.,fan,y.
‑
y.,weber,t.c.&aebi,m.n
‑
linked glycosylation of antibody fragments in escherichia coli.bioconjugate chemistry 22,488
‑
496(2011).
[0202]
karim,a.s.&jewett,m.c.a cell
‑
free framework for rapid biosynthetic pathway prototyping and enzyme discovery.metabolic engineering 36,116
‑
126(2016).
[0203]
huai,g.,qi,p.,yang,h.&wang,y.i.characteristics of a
‑
gal epitope,anti
‑
gal antibody,a1,3galactosyltransferase and its clinical exploitation(review).international journal of molecular medicine 37,11
‑
20(2016).
[0204]
abdel
‑
motal,u.m.等人,increased immunogenicity of hiv
‑
1 p24 and gp120 following immunization with gp120/p24 fusion protein vaccine expressing alpha
‑
gal epitopes.vaccine 28,1758
‑
1765(2010).
[0205]
meuris,l.等人,glycodelete engineering of mammalian cells simplifies n
‑
glycosylation of recombinant proteins.nat biotech 32,485
‑
489(2014).
[0206]
前述非专利参考文献的内容通过引用整体并入本文。
[0207]
图5、6和20中引用的参考文献。
[0208]
1.martin,r.w.等人,cell
‑
free protein synthesis from genomically recoded bacteria enables multisite incorporation of noncanonical amino acids.nature communications 9,1203(2018).
[0209]
2.bundy,b.c.&swartz,j.r.site
‑
specific incorporation of p
‑
propargyloxyphenylalanine in a cell
‑
free environment for direct protein
‑
protein click conjugation.bioconjugate chemistry 21,255
‑
263(2010).
[0210]
3.kightlinger,w.等人,design of glycosylation sites by rapid synthesis and analysis of glycosyltransferases.nature chemical biology 14,627
‑
635(2018).
[0211]
4.ollis,a.a.,zhang,s.,fisher,a.c.&delisa,m.p.engineered oligosaccharyltransferases with greatly relaxed acceptor
‑
site specificity.nature chemical biology 10,816
‑
822(2014).
[0212]
5.glasscock,c.j.等人,a flow cytometric approach to engineering escherichia coli for improved eukaryotic protein glycosylation.metabolic engineering 47,488
‑
495(2018).
[0213]
6.valentine,jenny l.等人,immunization with outer membrane vesicles displaying designer glycotopes yields class
‑
switched,glycan
‑
specific antibodies.cell chemical biology 23,655
‑
665(2016).
[0214]
7.naegeli,a.等人,substrate specificity of cytoplasmic n
‑
glycosyltransferase.journal of biological chemistry 289,24521
‑
24532(2014).
[0215]
8.schwarz,f.,fan,y.
‑
y.,schubert,m.&aebi,m.cytoplasmic n
‑
glycosyltransferase of actinobacillus pleuropneumoniae is an inverting enzyme and recognizes the nx(s/t)consensus sequence.journal of biological chemistry 286,35267
‑
35274(2011).
[0216]
9.park,j.e.,lee,k.y.,do,s.i.&lee,s.s.expression and characterization of beta
‑
1,4
‑
galactosyltransferase from neisseria meningitidis and neisseria gonorrhoeae.journal of biochemistry and molecular biology 35,330
‑
336(2002).
[0217]
10.peng,w.等人,helicobacter pylori β1,3
‑
n
‑
acetylglucosaminyltransferase for versatile synthesis of type 1 and type 2 poly
‑
lacnacs on n
‑
linked,o
‑
linked and i
‑
antigen glycans.glycobiology 22,1453
‑
1464(2012).
[0218]
11.ramakrishnan,b.&qasba,p.k.crystal structure of lactose synthase reveals a large conformational change in its catalytic component,the beta1,4
‑
galactosyltransferase
‑
i.journal of molecular biology 310,205
‑
218(2001).
[0219]
12.aanensen,d.m.,mavroidi,a.,bentley,s.d.,reeves,p.r.&spratt,b.g.predicted functions and linkage specificities of the products of the streptococcus pneumoniae capsular biosynthetic loci.journal of bacteriology 189,7856
‑
7876(2007).
[0220]
13.ban,l.等人,discovery of glycosyltransferases using carbohydrate arrays and mass spectrometry.nature chemical biology 8,769
‑
773(2012).
[0221]
14.blixt,o.,van die,i.,norberg,t.&van den eijnden,d.h.high
‑
level expression of the neisseria meningitidis lgta gene in escherichia coli and characterization of the encoded n
‑
acetylglucosaminyltransferase as a useful catalyst in the synthesis of glcnacβ1
→
3gal and galnacβ1
→
3gal linkages.glycobiology 9,1061
‑
1071(1999).
[0222]
15.higuchi,y.等人,a rationally engineered yeast pyruvyltransferase pvg1p introduces sialylation
‑
like properties in neo
‑
human
‑
type complex oligosaccharide.scientific reports 6,26349(2016).
[0223]
16.sun,s.,scheffler,n.k.,gibson,b.w.,wang,j.&munson jr.,r.s.identification and characterization of the n
‑
acetylglucosamine glycosyltransferase gene of haemophilus ducreyi.infection and immunity 70,5887
‑
5892(2002).
[0224]
17.wang,g.,ge,z.,rasko,d.a.&taylor,d.e.lewis antigens in helicobacter pylori:biosynthesis and phase variation.molecular microbiology 36,1187
‑
1196
(2000).
[0225]
18.persson,k.等人,crystal structure of the retaining galactosyltransferase lgtc from neisseria meningitidis in complex with donor and acceptor sugar analogs.nature structural biology 8,166(2001).
[0226]
19.fang,j.等人,highly efficient chemoenzymatic synthesis of α
‑
galactosyl epitopes with a recombinant α(1
→
3)
‑
galactosyltransferase.journal of the american chemical society 120,6635
‑
6638(1998).
[0227]
20.hidari,k.i.等人,purification and characterization of a soluble recombinant human st6gal i functionally expressed in escherichia coli.glycoconjugate journal 22,1
‑
11(2005).
[0228]
21.yamamoto,t.marine bacterial sialyltransferases.marine drugs 8,2781(2010).
[0229]
22.chiu,c.p.c.等人,structural analysis of the α
‑
2,3
‑
sialyltransferase cst
‑
i from campylobacter jejuni in apo and substrate
‑
analogue bound forms.biochemistry 46,7196
‑
7204(2007).
[0230]
23.keys,t.g.等人,a biosynthetic route for polysialylating proteins in escherichia coli.metabolic engineering 44,293
‑
301(2017).
[0231]
24.kim,d.m.&swartz,j.r.efficient production of a bioactive,multiple disulfide
‑
bonded protein using modified extracts of escherichia coli.biotechnology and bioengineering 85,122
‑
129(2004).
[0232]
前述非专利参考文献的内容通过引用整体并入本文。
[0233]
举例说明性实施方案
[0234]
以下实施方案是举例说明性的,并且不应被解释为限制所要求保护的主题的范围。
[0235]
实施方案1.一种用于在体外对肽或多肽序列进行糖基化的无细胞系统,所述肽或多肽序列包含天冬酰胺残基,并且所述系统包含以下组分:(i)糖基转移酶,其为可溶性n
‑
连接的糖基转移酶(ngt),其催化将单糖(任选地,其中单糖是葡萄糖(glc))转移至天冬酰胺残基的氨基以提供n
‑
连接的聚糖,或在无细胞蛋白质合成(cfps)反应混合物中表达ngt的表达载体;(ii)包含单糖供体(任选地,glc供体)的糖基化混合物;其中所述肽或多肽序列在体外在所述糖基化混合物中被糖基化以提供包含n
‑
连接的聚糖(任选地n
‑
连接的glc)的肽或多肽序列。
[0236]
2.权利要求1的系统,其进一步包含以下组分:(iii)第二糖基转移酶,其是可溶性的并且催化将单糖转移至n
‑
连接的聚糖(任选地,其中单糖是glc、半乳糖(gal)、n
‑
乙酰半乳糖胺(galnac)、n
‑
乙酰葡糖胺(glcnac)、丙酮酸、岩藻糖(fuc)、唾液酸(sia)),或在无细胞蛋白质合成(cfps)反应混合物中表达第二糖基转移酶的表达载体;其中糖基化混合物包含glc供体、gal供体、galnac供体、glcnac供体、丙酮酸供体、岩藻糖供体、唾液酸供体或其混合物,并且其中n
‑
连接的聚糖被选自glc、gal、galnac、glcnac、丙酮酸、fuc、sia和叠氮基
‑
sia的一种或多种部分糖基化(任选地提供n
‑
连接的右旋糖、n
‑
连接的乳糖或n
‑
连接的glc
‑
galnac)。
[0237]
3.权利要求2的系统,其进一步包含以下组分:(iv)第三糖基转移酶,其是可溶性的并且催化将单糖转移至n
‑
连接的聚糖(任选地,其中单糖是glc、gal、galnac、glcnac、丙酮酸、fuc、sia或其组合),或在无细胞蛋白质合成(cfps)反应混合物中表达第三糖基转移酶的表达载体;其中糖基化混合物包含glc供体、gal供体、galnac供体、glcnac供体、丙酮酸供体、岩藻糖供体、唾液酸供体或其混合物,并且其中n
‑
连接的聚糖进一步被选自glc、gal、galnac、glcnac、丙酮酸、fuc、sia和叠氮基
‑
sia的一种或多种部分糖基化(任选地以提供包含选自唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac以及αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)的一种或多种部分的n
‑
连接的聚糖)。
[0238]
4.前述权利要求中任一项的系统,其中所述系统包含无细胞蛋白质合成(cfps)反应混合物并且在cfps反应混合物中存在或表达第一糖基转移酶、第二糖基转移酶和第三糖基转移酶中的一种或多种。
[0239]
5.前述权利要求中任一项的系统,其中所述系统包含一种或多种无细胞蛋白质合成(cfps)反应混合物并且在cfps反应混合物中存在或表达第一糖基转移酶、第二糖基转移酶和第三糖基转移酶中的一种或多种,并且将一种或多种cfps反应混合物组合以提供系统。
[0240]
6.前述权利要求中任一项的系统,其进一步包含所述肽或多肽序列或表达所述肽或多肽序列的表达载体,任选地其中在无细胞蛋白质合成(cfps)反应混合物中提供或表达所述肽或多肽序列。
[0241]
7.前述权利要求中任一项的系统,其中所述cfps反应混合物是原核cfps反应混合物。
[0242]
8.前述权利要求中任一项的系统,其中所述cfps反应混合物是原核cfps反应混合物,所述原核cfps反应混合物包含由大肠杆菌制备的裂解物。
[0243]
9.前述权利要求中任一项的系统,其中任选地第一糖基转移酶是细菌n
‑
连接的糖基转移酶(ngt),任选地其中细菌ngt是选自以下的细菌ngt:胸膜肺炎放线杆菌(apngt)、大肠杆菌ngt(ecngt)、流感嗜血杆菌ngt(hingt)、溶血曼海姆菌ngt(mhngt)、杜雷嗜血杆菌ngt(hdngt)、海藻百伯史坦菌ngt(btngt)、嗜沫聚合杆菌ngt(aangt)、小肠结肠炎耶尔森菌ngt(yengt)、鼠疫耶尔森菌ngt(ypngt)和金格金氏杆菌ngt(kkngt)或其经修饰的形式。
[0244]
10.前述权利要求中任一项的系统,其中第一糖基转移酶是具有seq id no:1、3、5、7、9、11、13、15、17或19中任一项的氨基酸序列或与seq id no:1、3、5、7、9、11、13、15、17或19中任一项的氨基酸序列具有至少50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性的细菌n
‑
连接的糖基转移酶(ngt),或第一糖基转移酶是具有seq id no:2、4、6、8、10、12、14、16、18或20中任一项的氨基酸序列或与seq id no:2、4、6、8、10、12、14、16、18或20中任一项的氨基酸序列具有至少50%、60%、70%、80%、90%、95%、96%、
97%、98%或99%的序列同一性的修饰的细菌n
‑
连接的糖基转移酶(ngt)。
[0245]
11.前述权利要求中任一项的系统,其中任选地第二糖基转移酶是α1
‑
6葡萄糖基转移酶、β1
‑
4半乳糖基转移酶或β1
‑
3n
‑
乙酰半乳糖胺转移酶,并且任选地其中第二糖基转移酶选自胸膜肺炎放线杆菌α1
‑
6葡萄糖基转移酶(apα1
‑
6)、淋病奈瑟菌β1
‑
4半乳糖基转移酶lgtb(nglgtb)、脑膜炎奈瑟菌β1
‑
4半乳糖基转移酶lgtb(nmlgtb)和脆弱拟杆菌β1
‑
3n
‑
乙酰半乳糖胺转移酶(bfgalnact)。
[0246]
12.前述权利要求中任一项的系统,其中任选地第三糖基转移酶是β1
‑
3n
‑
乙酰葡糖胺转移酶、丙酮酸转移酶、α1
‑
3岩藻糖基转移酶、α1
‑
2岩藻糖基转移酶、α1
‑
4半乳糖基转移酶、α1
‑
3半乳糖基转移酶、α2
‑
6唾液酸转移酶、α2
‑
3,6唾液酸转移酶、α2
‑
3唾液酸转移酶或α2
‑
3,8唾液酸转移酶,任选地其中第三糖基转移酶选自淋病奈瑟菌β1
‑
3n
‑
乙酰葡糖胺转移酶(nglgta)、粟酒裂殖酵母丙酮酸转移酶(sppvg1)、幽门螺杆菌α1
‑
3岩藻糖基转移酶(hpfuta)、幽门螺杆菌α1
‑
2岩藻糖基转移酶(hpfutc)、脑膜炎奈瑟菌α1
‑
4半乳糖基转移酶(nmlgtc)、牛α1
‑
3半乳糖基转移酶(btggta)、智人α2
‑
6唾液酸转移酶(hssiat1)、美人鱼发光杆菌α2
‑
6唾液酸转移酶(pdst6)、鳆发光杆菌α2
‑
6唾液酸转移酶(plst6)、多杀巴斯德氏菌α2
‑
3,6唾液酸转移酶(pmst3,6)、弧菌属jt
‑
faj
‑
16α2
‑
3唾液酸转移酶(vsst3)、明亮发光杆菌α2
‑
3唾液酸转移酶(ppst3)、空肠弯曲杆菌α2
‑
3唾液酸转移酶(cjcst
‑
i)和空肠弯曲杆菌α2
‑
3,8唾液酸转移酶(cjcst
‑
ii)。
[0247]
13.前述权利要求中任一项的系统,其中所述系统的一个或多个组分处于保存的形式,任选地其中所述系统的一个或多个组分被冷冻干燥。
[0248]
14.一种包含n
‑
连接的聚糖的肽或多肽序列(任选地使用前述权利要求的任何系统或前述权利要求的系统的组分制备),所述n
‑
连接的聚糖包含选自以下的部分:唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac、αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)和glc
‑
gal
‑
叠氮基
‑
sia,任选地其中肽或多肽序列被用作或配制为治疗剂或疫苗。
[0249]
15.一种经修饰的细胞,其包含或表达权利要求1
‑
13的系统的一种或多种组分,任选地其中所述经修饰的细胞是经修饰的细菌细胞。
[0250]
16.一种用于制备糖基化肽或多肽序列的方法,该方法包括培养权利要求15的经修饰的细胞,其中所述经修饰的细胞包含或表达肽或多肽序列、n
‑
连接的糖基转移酶和任选地一种或多种额外的糖基转移酶,并且肽或多肽序列在经修饰的细菌细胞中被糖基化。
[0251]
17.一种包含n
‑
连接的聚糖的肽或多肽序列(任选地使用权利要求16的方法制备),所述n
‑
连接的聚糖包含选自以下的部分:唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式
的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac、αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)和glc
‑
gal
‑
叠氮基
‑
sia,任选地其中肽或多肽序列被用作或配制为治疗性蛋白或疫苗。
[0252]
18.由权利要求15的经修饰的细胞制备的裂解物,任选地其中所述裂解物适用于无细胞蛋白质合成(cfps)反应。
[0253]
19.一种用于体外制备糖基化肽或多肽序列的方法,所述方法包括使在包含单糖供体(任选其中单糖供体是葡萄糖(glc)供体,或者是单糖)的糖基化混合物中的包含天冬酰胺残基的肽或多肽序列与糖基转移酶反应,所述糖基转移酶是催化将单糖(任选地,来自glc供体的glc)从单糖供体转移至天冬酰胺残基的氨基以提供n
‑
连接的聚糖(任选地n
‑
连接的glc)的可溶性n
‑
连接的糖基转移酶(“n
‑
糖基转移酶”,“ngt”),其中所述肽或多肽序列在体外在所述糖基化混合物中被糖基化以提供包含n
‑
连接的聚糖(任选地n
‑
连接的glc)的肽或多肽序列,任选地,其中在进行糖基化之前,所述肽或多肽序列、ngt或两者在一种或多种无细胞蛋白质合成(cfps)反应混合物中表达。
[0254]
20.权利要求19的方法,其中肽或多肽序列在第一cfps反应混合物中表达,ngt在第二cfps反应混合物中表达,并且所述方法包括将第一cfps反应混合物和第二cfps反应混合物组合。
[0255]
21.权利要求19或20的方法,其进一步包括使包含聚糖的肽与第二糖基转移酶反应,所述第二糖基转移酶是可溶性的并且催化将单糖转移至n
‑
连接的聚糖(任选地,其中单糖是glc、半乳糖(gal)、n
‑
乙酰半乳糖胺(galnac)、n
‑
乙酰葡糖胺(glcnac)、丙酮酸、岩藻糖(fuc)、唾液酸(sia)或其组合),其中糖基化混合物包含glc供体、gal供体、galnac供体、glcnac供体、丙酮酸供体、岩藻糖供体、唾液酸供体或其混合物,并且其中n
‑
连接的聚糖被选自glc、gal、galnac、glcnac、丙酮酸、fuc、sia和叠氮基
‑
sia的一个或多个部分糖基化(任选地提供n
‑
连接的右旋糖、n
‑
连接的乳糖或n
‑
连接的glc
‑
galnac),任选地其中第二寡核苷酸转移酶在进行糖基化之前在无细胞蛋白质合成(cfps)反应混合物中表达。
[0256]
22.权利要求21的方法,其中所述肽或多肽序列在第一cfps反应混合物中表达,所述ngt在第二cfps反应混合物中表达,并且所述第二糖基转移酶在第三cfps反应混合物中表达,并且所述方法包括将第一cfps反应混合物、第二cfps反应混合物和第三反应混合物中的两种或更多种组合。
[0257]
23.权利要求21或22的方法,其还包括使包含聚糖的肽与第三糖基转移酶反应,所述第三糖基转移酶是可溶性的并且催化将单糖转移至n
‑
连接的聚糖(任选地,其中单糖是glc、gal、galnac、glcnac、丙酮酸、fuc或sia),其中糖基化混合物包含glc供体、gal供体、galnac供体、glcnac供体、丙酮酸供体、岩藻糖供体、唾液酸供体或其混合物,并且其中n
‑
连接的聚糖进一步被选自glc、gal、galnac、glcnac、丙酮酸、fuc、sia、叠氮基
‑
sia的一个或多个部分糖基化(任选地提供包含选自以下的一个或多个部分的n
‑
连接的聚糖:唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式
的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac以及αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal),并且任选地其中在进行糖基化之前第二寡核苷酸转移酶在无细胞蛋白质合成(cfps)反应混合物中表达。
[0258]
24.权利要求23的方法,其中所述肽或多肽序列在第一cfps反应混合物中表达,所述ngt在第二cfps反应混合物中表达,所述第二糖基转移酶在第三cfps反应混合物中表达,所述第三糖基转移酶在第四cfps反应混合物中表达,并且所述方法包括组合第一cfps反应混合物、第二cfps反应混合物、第三反应混合物和第四反应混合物中的两种或更多种。
[0259]
25.权利要求19
‑
24中任一项的方法,其中所述cfps反应混合物是原核cfps反应混合物。
[0260]
26.权利要求19
‑
25中任一项的方法,其中所述cfps反应混合物是原核cfps反应混合物,所述原核cfps反应混合物包含由大肠杆菌制备的裂解物。
[0261]
27.权利要求19
‑
26中任一项的方法,其中任选地第一糖基转移酶是细菌n
‑
连接的糖基转移酶(ngt),并且任选地细菌n
‑
连接的糖基转移酶(ngt)是选自以下的细菌ngt:胸膜肺炎放线杆菌(apngt)、大肠杆菌ngt(ecngt)、流感嗜血杆菌ngt(hingt)、溶血曼海姆菌ngt(mhngt)、杜雷嗜血杆菌ngt(hdngt)、海藻百伯史坦菌ngt(btngt)、嗜沫聚合杆菌ngt(aangt)、小肠结肠炎耶尔森菌ngt(yengt)、鼠疫耶尔森菌ngt(ypngt)和金格金氏杆菌ngt(kkngt)或其经修饰的形式。
[0262]
28.权利要求19
‑
27中任一项的方法,其中第一糖基转移酶是具有seq id no:1、3、5、7、9、11、13、15、17或19中任一项的氨基酸序列或与seq id no:1、3、5、7、9、11、13、15、17或19中任一项的氨基酸序列具有至少50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性的细菌n
‑
连接的糖基转移酶(ngt),或第一糖基转移酶是具有seq id no:2、4、6、8、10、12、14、16、18或20中任一项的氨基酸序列或与seq id no:2、4、6、8、10、12、14、16、18或20中任一项的氨基酸序列具有至少50%、60%、70%、80%、90%、95%、96%、97%、98%或99%的序列同一性的经修饰的细菌n
‑
连接的糖基转移酶(ngt)。
[0263]
29.权利要求19
‑
28中任一项的方法,其中任选地第二糖基转移酶是α1
‑
6葡萄糖基转移酶、β1
‑
4半乳糖基转移酶或β1
‑
3n
‑
乙酰半乳糖胺转移酶,并且任选地其中第二糖基转移酶选自胸膜肺炎放线杆菌α1
‑
6葡萄糖基转移酶(apα1
‑
6)、淋病奈瑟菌β1
‑
4半乳糖基转移酶lgtb(nglgtb)、脑膜炎奈瑟菌β1
‑
4半乳糖基转移酶lgtb(nmlgtb)和脆弱拟杆菌β1
‑
3n
‑
乙酰半乳糖胺转移酶(bfgalnact)。
[0264]
30.权利要求19
‑
29中任一项的方法,其中任选地第三糖基转移酶是β1
‑
3n
‑
乙酰葡糖胺转移酶、丙酮酸转移酶、α1
‑
3岩藻糖基转移酶、α1
‑
2岩藻糖基转移酶、α1
‑
4半乳糖基转移酶、α1
‑
3半乳糖基转移酶、α2
‑
6唾液酸转移酶、α2
‑
3,6唾液酸转移酶、α2
‑
3唾液酸转移酶或α2
‑
3,8唾液酸转移酶,任选地其中第三糖基转移酶选自淋病奈瑟菌β1
‑
3n
‑
乙酰葡糖胺转移酶(nglgta)、粟酒裂殖酵母丙酮酸转移酶(sppvg1)、幽门螺杆菌α1
‑
3岩藻糖基转移酶(hpfuta)、幽门螺杆菌α1
‑
2岩藻糖基转移酶(hpfutc)、脑膜炎奈瑟菌α1
‑
4半乳糖基转移酶(nmlgtc)、牛α1
‑
3半乳糖基转移酶(btggta)、智人α2
‑
6唾液酸转移酶(hssiat1)、美人鱼发光杆菌α2
‑
6唾液酸转移酶(pdst6)、鳆发光杆菌α2
‑
6唾液酸转移酶(plst6)、多杀巴斯德氏菌α2
‑
3,6唾液酸转移酶(pmst3,6)、弧菌属jt
‑
faj
‑
16α2
‑
3唾液酸转移酶(vsst3)、明亮发光
杆菌α2
‑
3唾液酸转移酶(ppst3)、空肠弯曲杆菌α2
‑
3唾液酸转移酶(cjcst
‑
i)和空肠弯曲杆菌α2
‑
3,8唾液酸转移酶(cjcst
‑
ii)。
[0265]
31.一种包含通过权利要求19
‑
30中任一项的方法制备的n
‑
连接的聚糖的肽或多肽序列,任选地其中所述n
‑
连接的聚糖包含选自以下的部分:唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac、αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)和glc
‑
gal
‑
叠氮基
‑
sia,任选地其中肽或多肽序列被用作或配制为治疗剂或疫苗。
[0266]
32.一种通过权利要求19
‑
30中任一项的方法合成并用作或配制为治疗剂或疫苗的蛋白质,任选地其中所述蛋白质包含n
‑
连接的聚糖并且所述n
‑
连接的聚糖包含选自以下的部分:唾液酸化形式的乳糖(例如,单唾液酸化形式的乳糖,例如3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖和二唾液酸化形式的乳糖)、岩藻糖基化形式的乳糖(例如,单岩藻糖基化形式的乳糖,例如2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)和3
’‑
岩藻糖基乳糖(即(glcβ1
‑
4galα1
‑
23fuc)和双岩藻糖基化形式的乳糖)、唾液酸化形式的lacnac(例如单唾液酸化形式的lacnac和二唾液酸化形式的lacnac)、岩藻糖基化形式的lacnac(例如,单岩藻糖基化形式的lacnac和双岩藻糖基化形式的lacnac)、丙酮酸化的乳糖或丙酮酸化的lacnac、αgal表位(例如glcβ1
‑
4galα1
‑
3gal或glcnacβ1
‑
4galα1
‑
3gal)和glc
‑
gal
‑
叠氮基
‑
sia。
实施例
[0267]
以下实施例是举例说明性的,并不旨在限制要求保护的主题的范围。
[0268]
实施例1
‑
用于产生糖蛋白和鉴定糖基化途径的模块化无细胞平台
[0269]
摘要
[0270]
糖基化在细胞功能中起重要作用并且赋予蛋白质治疗剂有益的特性。然而,构建生物合成途径来研究和设计蛋白质上的精确聚糖结构仍然是一个瓶颈。在这里,我们报告了通过快速体外混合和表达进行糖基化途径组装(glycoprime)的模块化、多功能无细胞平台。在glycoprime中,通过混合和匹配无细胞合成的糖基转移酶(其可以通过n
‑
糖基转移酶精心设计安装在蛋白质靶标上的葡萄糖引物)来组装糖基化途径。我们通过以下来证明glycoprime:构建了37条推定的蛋白质糖基化途径,创建了23个独特的聚糖基序,其中18个尚未在蛋白质上合成。我们使用选择的途径以在一锅式无细胞系统中合成具有α
‑
半乳糖佐剂基序的蛋白质疫苗候选物,并在糖工程化的大肠杆菌中合成具有最少唾液酸基序的人抗体恒定区。我们预计这些方法和途径将促进糖科学并使新的糖工程化应用成为可能。
[0271]
a.引言
[0272]
蛋白质糖基化,即将寡糖附接到氨基酸侧链的酶促过程,是自然界中最丰富和最复杂的翻译后修饰之一
1,2
,并且在人健康中起着关键作用1。糖基化存在于超过70%的蛋白质治疗剂中3,并深刻影响蛋白质稳定性
4,5
、免疫原性
6,7
和活性8。糖基化在生物学中的重要
性以及蛋白质上的聚糖结构的有意操纵可以改善治疗特性的证据
4,6,8
促使许多努力以研究和工程化蛋白质糖基化结构9‑
11
。
[0273]
不幸的是,糖蛋白工程化受到可以在蛋白质以及可用于糖蛋白产生的平台上构建的聚糖结构的数量和多样性的限制
9,12
。一个关键的挑战是聚糖在自然界中是由跨多个亚细胞区室的许多糖基转移酶(gt)合成的1,从而使工程化工作复杂化并导致结构异质性
3,12
。此外,真核生物中的基本生物合成途径限制了可以在这些系统中进行工程化的聚糖结构的多样性
9,13
。细菌糖工程化通过在缺乏内源性糖基化酶的实验室大肠杆菌菌株中表达异源糖基化途径来解决这些限制
13,14
。已在细菌细胞
13
‑
17
和无细胞系统
18
‑
21
中成功重建了几种天冬酰胺(n连接)糖基化途径。特别地,在粗制细胞裂解物中合成蛋白质和代谢物的无细胞系统可以加速酶和生物合成途径的表征和工程化
22
‑
25
。基于大肠杆菌的无细胞蛋白质合成(cfps)系统可以在数小时内产生克/升滴度的复杂蛋白质
26
,使得能够快速发现、原型设计和优化代谢途径而无需针对每个途径迭代重新工程化生物体
23
‑
25
。
[0274]
然而,现有的无细胞糖蛋白合成平台尚未充分利用该范例,因为它们依赖寡糖基转移酶(ost)来将预构建的糖从脂质连接的寡糖(llo)转移至蛋白质。ost很难表达,因为它们是完整的膜蛋白,其通常包含多个亚基1。此外,ost的llo底物特异性限制了可转移至蛋白质的聚糖结构的模块化和多样性
27
。最后,能够通过ost进行转移的llo难以在体外合成
12
。事实上,尚未表明llo生物合成和糖基化可以在体外共同激活,或者llo可以在细菌cfps系统中转移和扩展。相反,llo必须通过活细胞中llo生物合成途径的表达从细胞裂解物中衍生或预先富集
18
‑
20
。在细胞中表达llo生物合成途径需要耗时的多顺反子操纵子的克隆和调整、细胞转化以及用于每个聚糖结构的新的裂解物的产生。总之,膜相关ost和llo的复杂性以及ost底物特异性阻碍了糖工程化和多酶糖基化途径的简便构建和筛选
12
。
[0275]
n
‑
糖基转移酶(ngt)可以通过构建简化的、与ost和llo无关的蛋白质糖基化途径来克服这些限制
9,16,28
。ngt是细胞质细菌酶,其将葡萄糖残基从尿嘧啶二磷酸葡萄糖(udp
‑
glc)糖供体转移到天冬酰胺侧链上
29
。重要的是,ngt是可溶性酶,其可以将葡萄糖引物安装到大肠杆菌细胞质中的蛋白质上
16,17,22
。然后可以通过共表达的gt依次精心制作该引物
16,28
。基于合成ngt的糖基化系统不受ost底物特异性的限制,并且不需要跨膜蛋白质转运或脂质相关组分9。这些系统作为合成糖蛋白(包括治疗剂和疫苗)的补充方法引起了极大的兴趣,使用基于ost的系统很难或不可能产生这些糖蛋白
9,16,22,28,30
‑
32
。最近的几项进展为实现这一愿景奠定了基础。首先,使用糖蛋白组学和glycoscores技术
17,22,31
对ngt的受体特异性进行严格表征揭示ngt修饰了n
‑
x
‑
s/t氨基酸基序。其次,胸膜肺炎放线杆菌(apngt)的ngt已被证明可以在体外和在大肠杆菌中修饰真核蛋白质中天然和合理设计的糖基化位点
16,17,22,28
。第三,aebi小组和其他人最近报道了apngt将葡萄糖安装到大肠杆菌细胞中的聚唾液酸乳糖
28
或葡聚糖
16
基序上,以及将预构建的噁唑啉官能化的寡糖转移至该葡萄糖残基上的化学酶促方法
30,32
。然而,尚未探索使用ngt构建聚糖的其他生物合成途径9,可能是由于与在活细胞中建立和测试合成糖基化途径相关的缓慢时间线。基于apngt的无细胞合成平台将通过实现合成糖基化途径的高通量和完全体外构建、组装和筛选来加速糖工程化努力。
[0276]
在此,我们描述了通过快速体外混合和表达进行糖基化途径组装(glycoprime)的模块化、无细胞方法。在这种两锅式方法中,粗制大肠杆菌裂解物通过cfps表达选择性地富
集个体gt,然后以混合和匹配的方式组合以构建多酶糖基化途径。glycoprime的目标是设计、建立、测试和分析多种酶组合,而无需为每种组合制造新的基因构建体、菌株、细胞裂解物或纯化的酶,以发现感兴趣的糖蛋白结构的新生物合成途径(包括许多在自然界中未发现的途径)。然后可以将这些酶组合转移至生物制造系统,例如活细胞,并用于产生和测试糖蛋白。glycoprime的一个关键特征是使用apngt将单个n连接的葡萄糖引物位点特异性地安装到蛋白质上,其可以被精心制作为聚糖的多样库。使用apngt作为起始糖基化酶移除了针对llo的ost特异性对聚糖结构的限制,并通过避免在活细胞中的llo前体上合成聚糖的需要,实现了第一个完全体外的糖基化途径合成和筛选工作流程。
[0277]
为了验证glycoprime,我们优化了24种细菌和真核生物gt的体外表达,并将它们组合以创建37条推定的生物合成途径,以精心制作通过apngt在模型糖蛋白底物上安装的葡萄糖。我们生成了23种独特的聚糖结构,其由1至5个核心糖和更长的重复结构组成。这些途径产生了18种尚未报道的在蛋白质上的聚糖结构,并为治疗相关基序(包括α1
‑
3连接的半乳糖(αgal)表位以及岩藻糖基化和唾液酸化的乳糖或聚n
‑
乙酰乳糖胺(lacnac))提供了新的生物合成途径。然后,我们证明使用glycoprime鉴定的途径可以通过(i)在一锅式无细胞蛋白质合成驱动的糖蛋白合成(cfps
‑
gps)平台中产生具有佐剂αgal聚糖6,7,33的蛋白质疫苗候选物和(ii)在大肠杆菌细胞质中产生具有已知改善体内药代动力学的最小唾液酸聚糖人免疫球蛋白(igg1)抗体的恒定区(fc)
5,34
来转移至无细胞和细胞生物合成系统。glycoprime方法代表了一种加速多酶糖基化途径的构建和筛选的强大的新方法。通过鉴定可行的合成糖基化途径,我们预计glycoprime将使未来努力能够产生和工程化糖蛋白以用于引人注目的应用,包括基础研究和改进的治疗学。
[0278]
b.建立体外糖工程化平台
[0279]
我们将glycoprime建立为模块化的体外蛋白质合成和糖基化平台,以开发生物合成途径,其将通过apngt安装的n
‑
连接的葡萄糖引发残基精心制作为多样的糖基化基序,包括唾液酸化和岩藻糖基化形式的乳糖和lacnac以及αgal表位(图1)。
[0280]
为了证明概念,我们的目的是在使得能够在我们的glycoprime工作流程中进一步精心制作聚糖的设置中用apngt糖基化模型蛋白质。具体来说,我们确定了提供高gt表达滴度的cfps条件,以便可以将完全糖蛋白转化所需的最小体积的富含gt的裂解物添加到每个体外糖基化(ivg)反应中,从而留下足够的反应体积并产生底物用于通过混合无细胞裂解物的进一步精心制作。基于我们之前对apngt受体序列特异性的表征
22
,我们选择了一个工程化形式的在内部环处具有一个单一的、优化的糖基化序列ggnwtt的大肠杆菌免疫蛋白im7(im7
‑
6)作为我们的模型靶蛋白(图5和图29)。我们使用[14c]
‑
亮氨酸掺入来测量和优化我们的工程化的im7
‑
6靶标和apngt的cfps反应温度(图6和图2a),并通过sds
‑
page放射自显影图确认它们的全长表达(图12和13)。我们发现23℃提供了这些蛋白质的最易溶解的产物,平衡了较高温度下更大的整体蛋白质产率和较低温度下更大的溶解度。我们通过cfps合成了im7
‑
6和apngt,然后在32μl ivg反应中将这些反应产物与udp
‑
glc混合在一起。然后我们使用ni
‑
nta官能化磁珠纯化im7
‑
6底物并进行完整的糖蛋白液相色谱质谱(lc
‑
ms)(参见方法)。我们观察到10μm im7
‑
6底物(11μl)的几乎完全转化,只有0.4μm apngt(1μl)(图2c),如通过解卷积的蛋白质质谱中162da(葡萄糖残基的质量)的质量位移所示(理论质量如图7所示)。这表明cfps产物可以直接组装到ivg反应中以产生糖蛋白,剩余的反应体
积用于添加精心设计的gt。
[0281]
接下来,我们鉴定了具有先前表征的特异性的7个gt,其可用于将apngt安装的葡萄糖引物精心制作为相关聚糖(图2和图8)。先前的工作表明,在胸膜肺炎放线杆菌中,通过聚合apα1
‑
6葡萄糖基转移酶修饰apngt安装的葡萄糖以形成n
‑
连接的葡聚糖29,并且这种结构可能是一种有用的疫苗抗原16,35。最近的工作还表明来自脑膜炎奈瑟菌的β1
‑
4半乳糖基转移酶lgtb(nmlgtb)可以修饰大肠杆菌中apngt安装的葡萄糖,形成n连接的乳糖(asn
‑
glcβ1
‑
4gal)28。在这里,我们试图在体外重现这些途径,并选择了另外5种具有潜在有用活性的酶(图2a)。我们选择了来自脆弱拟杆菌的n
‑
乙酰半乳糖胺(galnac)转移酶(bfgalnact),因为它安装的galnac残基36可以作为o
‑
连接聚糖表位的精心制作点。我们还选择了来自肺炎链球菌(spwchk)、淋病奈瑟菌(nglgtb)、幽门螺杆菌(hpβ4galt)和牛(btβ4galt1)的几种β1
‑
4半乳糖基转移酶,以确定n
‑
连接的乳糖的最佳生物合成途径。这很重要,因为乳糖是修饰牛奶寡糖和人n连接的聚糖的末端的许多gt的已知底物1,37
‑
40,使其成为进一步聚糖多样化的关键反应节点。
[0282]
鉴定后,我们优化了cfps条件并确认了这7个gt(图2、图6和图12和13)以及来自肺炎链球菌(s.pneumoniae)的spwchj(其已知增强spwchk的活性41)的可溶性全长表达。然后,我们根据先前表征的活性,通过将包含这些gt的cfps产物与im7
‑
6和apngt cfps产物以及udp
‑
glc和其他合适的糖供体混合来组装ivg反应(图2)。我们观察到与nmlgtb和nglgtb(β1
‑
4半乳糖基转移酶)、bfgalnact(β1
‑
3n
‑
乙酰半乳糖基转移酶)和apα1
‑
6(聚合α1
‑
6葡萄糖基转移酶)的已知活性一致的胰蛋白酶化糖肽的im7
‑
6完整质量位移和串联ms(ms/ms)碎片化光谱(图2、图14和图9)。我们没有观察到通过hpβ4galt、spwchk(甚至使用spwchj)或btβ4galt1(即使使用α
‑
乳清蛋白和有助于二硫键形成的条件)的修饰(图15)。通过测试具有递减量的nmlgtb和nglgtb的ivg,我们发现2μm的nmlgtb提供几乎完全转化为n
‑
连接的乳糖,而相同量的nglgtb效率较低(图16)。这些结果表明可以在体外快速合成、组合组装和评估多酶糖基化途径。使用这种方法,我们发现apngt和nmlgtb提供了针对n
‑
连接的乳糖的有效的体外途径,并发现apngt和bfgalnact可以位点特异性地安装galnac封端的聚糖。
[0283]
c.多样糖基化途径的模块化构建
[0284]
为了证明glycoprime用于模块化途径构建和筛选的能力,我们接下来选择了15个具有已知特异性的gt,这些gt提示它们有能力将通过apngt和nmlgtb安装的n
‑
连接的乳糖精心制作成3至5个糖基序的多样库和更长的重复结构(图3和图8)。具体来说,我们试图发现将n
‑
连接的乳糖精心制成9种包含唾液酸(sia)、半乳糖(gal)、丙酮酸、岩藻糖(fuc)和lacnac的低聚糖的生物合成途径。从那里,我们可以通过以各种方式重新组合这些gt来获得更大的多样性。我们首先描述我们选择这些途径类别的基本原理,包括它们对各种应用的潜在价值,然后展示我们的实验结果。
[0285]
我们的第一个目标是构建末端为唾液酸的聚糖,因为它们提供了许多有用的特性以用于蛋白质治疗应用
5,8,28,34,42
(例如改进的运输、稳定性和药效学);功能生物材料
43
;与细菌受体
44,45
、人半乳凝集素
46
和siglecs
47
的结合相互作用;以及用于疫苗的佐剂
48
和肿瘤相关碳水化合物抗原(taca)
49,50
。由于末端唾液酸的连接对这些应用很重要,我们选择酶来使用α2
‑
3、α2
‑
6和α2
‑
8键联将sia安装到n
‑
连接的乳糖上。我们首先构建了3
’‑
唾液酸乳糖(glcβ1
‑
4galα2
‑
6sia)结构,该结构可以提供多种有用的特性,包括与粘附在人体细胞上的
病原体受体的特异性结合
44
、将疫苗递送至巨噬细胞以增加抗原呈递
48
以及模拟用于癌症疫苗的人gm3神经节苷脂(神经酰胺
‑
glcβ1
‑
4galα2
‑
3sia)
50
。3
’‑
唾液酸乳糖结构也可以模拟最近报道的glycodelete结构(glcnacβ1
‑
4galα2
‑
3sia),这是一种已知保留糖蛋白治疗活性和药代动力学的简化的n
‑
聚糖
51
。为了构建3
’‑
唾液酸乳糖,我们选择了来自多杀巴斯德氏菌(pmst3,6)、弧菌属物种jt
‑
faj
‑
16(vsst3)、明亮发光杆菌(ppst3)和空肠弯曲杆菌(cjcst
‑
i)的四种α2
‑
3唾液酸转移酶。接下来,我们的目标是发现针对6
’‑
唾液酸乳糖(glcβ1
‑
4galα2
‑
6sia)的生物合成途径,因为具有末端α2
‑
6sia的n
‑
聚糖在分泌的人蛋白质中很常见5,表现出抗炎特性8,使得能够靶向b细胞用于治疗淋巴瘤
52
,并提供一组独特的siglec、凝集素和受体结合特征谱
5,44,47
。为了产生6
’‑
唾液酸乳糖,我们选择了来自人(hssiat1)、美人鱼发光杆菌(pdst6)和鳆发光杆菌(plst6)的三种α2
‑
6唾液酸转移酶。最后,我们研究了用于产生具有α2
‑
8sia的聚糖的途径,这些聚糖可以模拟gd3神经节苷脂(神经酰胺
‑
glcβ1
‑
4galα2
‑
3siaα2
‑
8sia),一种taca和可能的针对黑色素瘤的疫苗表位
49,53
。基于先前的工作
28,42
,我们选择来自空肠弯曲杆菌的cst
‑
ii双功能唾液酸转移酶来安装末端α2
‑
8sia。除了含有sia的聚糖外,我们还探索了丙酮酸半乳糖的合成,因为这种结构显示出与sia相似的凝集素结合特性
54
。为了构建末端的丙酮酸化乳糖,我们选择了来自粟酒裂殖酵母(sppvg1)的丙酮酸转移酶
54
。
[0286]
除了末端为sia的结构之外,我们探索了用gal、fuc和lacnac修饰n
‑
连接的乳糖的途径。例如,我们的目标是工程化一种首创的细菌系统用于用αgal(glcβ1
‑
4galα1
‑
3gal)表位修饰的蛋白质的完全生物合成。αgal是在人中的一种有效的自身:非自身鉴别表位,并且与估计1%的人igg库结合
6,7,33
。因此,当与各种肽、蛋白质、全细胞和基于纳米颗粒的免疫原缔合时,αgal赋予佐剂性质6,7,33,55。为了构建αgal,我们选择了来自牛的α1,3半乳糖基转移酶(btggta)。此外,我们试图合成球二糖(globobiose)结构(glcβ1
‑
4galα1
‑
4gal),因为它可以模拟gb3神经节苷脂(神经酰胺
‑
glcβ1
‑
4galα1
‑
4gal),其可以结合并中和由病原菌分泌的志贺样毒素
56
。我们选择了来自脑膜炎奈瑟菌的半乳糖基转移酶lgtc(nmlgtc)来合成球二糖。我们还旨在构建lacnac,因为它为生物材料提供了有用的特性
57
以及提供了半乳凝集素的抑制和调节以控制癌症、炎症和纤维化
58
。我们选择了来自淋病奈瑟菌(nglgta)和杜克雷嗜血杆菌(hdglcnact)的两种β1
‑
3n
‑
乙酰氨基葡糖(glcnac)转移酶来制造这种结构。最后,我们的目标是构建岩藻糖基化乳糖结构,其可应用于用于神经元组织的生物材料
59
以及靶向或防止细菌粘附
60
。为了合成岩藻糖基化乳糖,我们筛选了来自幽门螺杆菌的α1,3和α1,2岩藻糖基转移酶(分别为hpfuta和hpfutc)。
[0287]
在设计途径和选择gt之后,我们使用glycoprime来合成和组装包含apngt、nmlgtb和上述15个gt中的每一个的三酶生物合成途径。我们首先优化并证明了每个gt的全长、可溶性表达(图3a和图6以及图12和13)。然后,我们使用glycoprime工作流来合成im7
‑
6、apngt、nmlgtb和gt以用于在单独的cfps反应中进行聚糖延伸,然后将这些cfps产物和适当的糖供体混合以形成ivg反应。值得注意的是,当ivg产物通过ni
‑
nta纯化并通过lc
‑
ms(/ms)分析时,我们观察到完整的im7
‑
6质量位移(图3和图17)和胰蛋白酶化糖肽的碎片化光谱(图18),根据选择用于精心制作该结构的所有15个gt(除了hdglcnact)的假设活性,这与由apngt和nmlgtb安装的n
‑
连接的乳糖的修饰一致(图19)。虽然我们确实通过完整蛋白质和/或糖肽分析检测到来自所有八种唾液酸转移酶的一些活性,但我们发现cjcst
‑
i和
pdst6分别提供了所有α2
‑
3和α2
‑
6唾液酸转移酶的最高转化率(图17)。这种优化证明了glycoprime快速比较几种生物合成途径以确定产生所需产物的酶组合的能力。我们还发现,通过在氧化条件下对那些gt进行cfps,我们可以显著提高包含cjcst
‑
i和hssiat1的反应的转化率(图20)。该结果证明了cfps反应的开放反应环境为改善酶合成(包括具有二硫键的人酶(hssiat1)的合成)提供的优势。值得注意的是,我们发现nglgta不仅安装了glcnac,而且还进而与nmlgtb一起用于形成具有多达6个重复单元的lacnac聚合物(图3)。除了完整的蛋白质和糖肽lc
‑
ms(/ms),我们还使用市售外切糖苷酶对通过apngt、nmlgtb和pdst6、hssiat1、cjcst
‑
i、hpfuta、hpfutc、nglgta和btggta修饰的im7
‑
6进行了消化(图21和22)。我们的发现支持这些酶的先前建立的连接特异性(图2、3和图8)。在这些条件下,我们发现pmst3,6主要表现出α2
‑
3活性,这与之前的报道一致
61
。
[0288]
使用三酶途径证明了多种gt的活性后,我们进一步推动glycoprime系统来评估包含四种和五种酶的生物合成途径。具体而言,我们的目标是使用hpfuta、hpfutc、cjcst
‑
i、pdst6和nglgta的组合合成唾液酸化和岩藻糖基化的乳糖和lacnac结构。与上述构建的较小聚糖相比,这些结构可以在各种应用(包括靶向和抑制人和病原细胞上的半乳凝集素、siglecs和凝集素
44,46,57,58
以及通过在树突细胞上安装与dc
‑
sign受体结合的lewis
‑
x聚糖结构辅助疫苗
62
)中提供更大的特异性。虽然这些gt的一些组合已被用于产生游离寡糖或糖脂
37
‑
40,63
‑
65
,但尚未在蛋白质底物的背景下系统地研究由它们的特异性之间的相互作用产生的产物。我们使用glycoprime来测试这五个gt的所有成对组合,在单独的cfps反应中表达它们中的每一个,然后将这些粗制裂解物中的两种以等体积与含有10μm im7
‑
6、0.4μm apngt和2μm nmlgtb的cfps反应混合。在我们对这些ivg产物的分析中,我们观察到完整的蛋白质(图3d)和糖肽碎片化产物(图23),表明几种有趣结构(包括双岩藻糖基化乳糖、二唾液酸化乳糖、具有唾液酸化和岩藻糖基化键联的组合的乳糖变体、具有分支或仅末端sia的唾液酸化lacnac结构和岩藻糖基化的lacnac结构)的合成。我们的分析还揭示了酶之间的一些可能的特异性冲突。例如,cjcst
‑
i与hpfuta和pdst6与hpfutc的组合产生被唾液酸化和岩藻糖基化的产物,但pdst6与hpfutc和cjcst
‑
i与hpfutc则没有(图24)。此外,我们观察到,当hpfutc和nglgta一起使用时,无论其长度如何,仅将一种岩藻糖添加到lacnac主链中(图3d和图23)。相反,当hpfuta和nglgta结合时,我们的观察表明两种可用的glc(nac)残基都可被修饰;然而,较短的聚合物长度表明,使用hpfuta的岩藻糖基化可能阻止lacnac链通过nglgta的持续生长(图3)。虽然我们在这里重点测试所有途径酶同时作用的反应,但使用类似工作流程的体外连续糖基化反应可用于进一步表征这些特异性冲突并严格确定酶动力学。为了测试glycoprime可以支持的生物合成节点的数量,我们使用nglgta、一种岩藻糖基转移酶(hpfuta或hpfutc)和一种唾液酸转移酶(cjcst
‑
i或pdst6)构建了几个五酶糖基化途径。虽然这些聚糖的复杂性不允许我们明确指定它们的结构,但来自包含nglgta、pdst6和hpfuta或hpfutc的途径的完整蛋白质质量位移(图24)和碎片化光谱(图23)指明了被岩藻糖基化和唾液酸化的lacnac结构聚糖的构建(图3d和图23和25)。由这些四酶和五酶组合合成的许多聚糖先前没有被描述过,并将需要进一步研究以了解它们提供的功能特性。
[0289]
d.glycoprime途径在细菌产生系统中起作用
[0290]
使用glycoprime构建和筛选了许多新的生物合成途径后,我们试图证明我们发现
的合成糖基化途径可以在体外和体内生物生产平台内转化为新的背景,以合成治疗相关的糖蛋白(图4)。
[0291]
首先,我们的目标是将使用我们的两锅式glycoprime系统发现的糖基化途径转化为一锅式、协调的无细胞蛋白质合成驱动的糖蛋白合成(cfps
‑
gps)平台。在cfps
‑
gps中,靶蛋白在糖供体的存在下与gt共表达,以同时合成和糖基化感兴趣的糖蛋白。通过使得能够在细胞裂解前在体外而不是在底盘菌株内体内表达糖基化途径酶,该策略为我们之前报道的一锅式无细胞糖蛋白合成(cfgps)平台18提供了一种替代和互补的方法。我们通过混合im7
‑
6靶蛋白质粒、基于在我们的两锅式glycoprime筛选中开发的12条成功生物合成途径的多达三种gt质粒的组以及在一锅式cfps
‑
gps反应中的适当糖供体来验证我们的一锅式cfps
‑
gps方法。在所有反应中,我们观察到与用在我们的两锅式系统中观察到的相同聚糖对im7
‑
6的修饰一致的完整蛋白质质量位移,尽管效率较低(图26)。这些结果表明,在一锅式体外反应中,靶蛋白和gt合成与蛋白质糖基化的共同激活是可能的,与两锅式glycoprime形式相比,进一步简化和缩短了产生糖蛋白所需的时间。总体而言,cfps
‑
gps仅使用质粒、市售小分子和未富集的粗制大肠杆菌裂解物来产生糖蛋白,使得能够根据需要或所需的应用,通过简单地添加不同的质粒到单一的粗制裂解物来源来进行不同糖蛋白靶标和/或聚糖结构的通用产生。
[0292]
在开发了cfps
‑
gps方法之后,我们的目标是使用我们使用glycoprime发现的生物合成途径(图4)合成和糖基化具有αgal聚糖基序的流感疫苗候选物h1ha10
66
。我们选择在h1ha10模型蛋白上展示αgal途径,因为h1ha10是一种有效的免疫原,其可以在大肠杆菌中表达,并且αgal的化学酶促安装已被显示可用作其他流感疫苗候选物的有效分子内佐剂
7,67
。当我们在一锅式cfps
‑
gps反应中组合udp
‑
glc、udp
‑
gal和编码h1ha10蛋白apngt、nmlgtb和btggta的质粒时,我们观察到αgal在h1ha10的n末端处安装在含有工程化受体序列的胰蛋白酶肽上(图4b)。我们通过外切糖苷酶消化和lc
‑
ms/ms进一步证实了这种αgal聚糖的连接(图4c
‑
d和图10)。
[0293]
为了证明使用glycoprime发现的途径向活细胞的转移,我们设计了合成糖基化系统以将n
‑
连接的3
’‑
唾液酸乳糖和6
’‑
唾液酸乳糖安装到大肠杆菌中人igg1的fc区(图4)。虽然已经在工程化大肠杆菌中产生了具有α2,8连接的多唾液酸的糖蛋白
28
,但这些具有不同末端唾液酸连接和简化、更均质的结构的聚糖可以为糖蛋白治疗的一些应用提供独特和理想的特性
5,8,34,51
。为此,我们构建了一个三质粒系统,其由编码脑膜炎奈瑟菌cmp
‑
sia合酶(conneua)的组成型表达的胞苷
‑5’‑
单磷酸
‑
n
‑
乙酰神经氨酸(cmp
‑
sia)合成质粒;异丙基β
‑
d
‑1‑
硫代吡喃半乳糖苷(iptg)诱导型靶蛋白质粒;以及编码apngt、nmlgtb和cjcst
‑
i或pdst6的gt操纵子质粒组成。cmp
‑
sia合成质粒是必需的,因为实验室大肠杆菌菌株不会内源性产生cmp
‑
sia。根据之前的报道
28,40
,我们选择了一种携带nant唾液酸转运蛋白基因的k
‑
12大肠杆菌菌株用于摄取补充到培养基中的sia并敲除cmp
‑
sia醛缩酶基因(nana)以防止细胞内sia的消化,从而产生clm24δnana。与cfps
‑
gps一样,我们使用im7
‑
6模型蛋白验证了我们的靶聚糖的体内合成。当我们在clm24δnana中转化和诱导我们的三质粒系统时,我们观察到分别与通过apngt用n
‑
连接的glc修饰im7
‑
6、通过nmlgtb精心制作成乳糖以及通过cjcst
‑
i或pdst6精心制作成3
’‑
唾液酸乳糖或6
’‑
唾液酸乳糖一致的完整的蛋白质光谱(图27)。为了合成用这些聚糖修饰的fc,我们将im7
‑
6靶质粒替换为编码fc的质粒,其
在asn297(fc
‑
6)的保守人igg1糖基化位点处具有工程化受体序列22。在该系统中,我们观察到完整的蛋白质ms、ms/ms肽碎片化和外切糖苷酶消化,这与根据提供的gt操纵子的glc、乳糖和3
’‑
唾液酸乳糖或6
’‑
唾液酸乳糖在fc
‑
6上的预期安装一致(图4f
‑
h、图28和图11)。将需要进一步研究以评估αgal表位作为用于h1ha10的佐剂的功效以及fc上最小唾液酸基序的治疗效果。然而,我们的研究结果清楚地表明,在glycoprime工作流程中鉴定的有用糖基化途径可以快速且轻松地转化为细菌无细胞和基于细胞的表达平台以用于产生治疗相关的糖蛋白。
[0294]
e.讨论
[0295]
这项工作建立并证明了glycoprime平台(这是一种用于多酶糖基化途径的模块化合成、组装和发现的无细胞工作流程)的效用。glycoprime有几个关键特性。首先,通过消除活细胞中llo产生的需要,glycoprime是第一个能够完全在体外生物合成糖基化靶标、gt和糖蛋白的系统。这种方法将设计
‑
构建测试单元从活细胞系转移至无细胞裂解物。我们通过快速探索37条推定的蛋白质糖基化途径证明了glycoprime的效用,其中23条产生了独特的糖基化基序。
[0296]
其次,使用apngt(一种可溶性细菌酶)有效地将引发n
‑
连接葡萄糖安装到糖蛋白上是促进途径组装的关键。通过精心制作这种葡萄糖残基,我们在体外自下而上生成了治疗相关糖基化基序的多样化文库。在这项工作中对于其发现生物合成途径的23个独特糖基化基序中,有几个已合成为游离
37
‑
40,63,64
或脂质连接
37,38
的寡糖或通过重塑现有的糖蛋白
6,30,42
合成;然而,据我们所知,之前只有葡萄糖
16,22,28
、葡聚糖
16
、乳糖
28
、lacnac
65
和聚唾液酸乳糖28已在细菌系统中产生为糖蛋白缀合物。在这项工作中发现的导致蛋白质上的新聚糖基序的18条合成糖基化途径代表了迄今为止通过任何单一细菌糖工程化研究完成的最大的增加。具体来说,我们开发了产生携带n
‑
连接的3
’‑
唾液酸乳糖、6
’‑
唾液酸乳糖、αgal表位、丙酮酸化乳糖、2
’‑
岩藻糖基乳糖(glcβ1
‑
4galα1
‑
2fuc)、3
‑
岩藻糖基乳糖(glcβ1
‑
4[α1
‑
3fuc]gal),以及许多其他单或双岩藻糖基化和唾液酸化形式的乳糖或lacnac的蛋白质的第一条细菌生物合成途径。
[0297]
第三,在glycoprime中鉴定的生物合成途径可以在新的背景中和在用于体外和大肠杆菌细胞质中糖蛋白产生的新蛋白质上实施。具体而言,我们展示了在一锅式cfps
‑
gps反应中用αgal佐剂基序修饰的候选疫苗蛋白h1ha10的合成,以及在大肠杆菌中用3
’‑
唾液酸乳糖和6
’‑
唾液酸乳糖修饰的igg1 fc的产生(图4)。虽然没有研究大规模产生和纯化方法,但我们的工作显示了将通过glycoprime发现的途径转化为相关生物制造表达系统的可行性。此外,使用apngt而不是ost使这些途径具有吸引力,因为它们不需要跨细胞膜的运输或膜相关组分。这些发现证明了glycoprime用于加速糖工程化工作的潜力并与在分布式生物制造系统
21,68,69
和具有降低的内毒素水平的大肠杆菌菌株
21,70,71
中的最新发展组合实现了在生物技术中的新应用,包括糖蛋白疗法的按需产生。
[0298]
虽然在这项工作中产生的糖基化结构没有天然人聚糖复杂,但它们仍然提供了许多有前途的应用。潜在应用包括开发用于碳水化合物结合蛋白的基础研究
44
;基于聚糖的细菌靶向
60
、毒素中和
56
和粘附预防
44,45,60
;糖蛋白治疗特性和运输的改善
5,8,28,34,42,52
;功能生物材料的新机遇
43,57,59
;人半乳凝集素46和siglecs
46,47
的调节和抑制;以及新抗原的开发
49,50,53
和用于免疫的佐剂
6,7,33,48,55,62
的其他研究试剂和成像。尽管游离寡糖或小分子可
以实现一些上述功能,但在这项工作中证明的在糖蛋白上位点特异性地构建聚糖的能力将实现广泛的附加功能,包括靶向、抗原呈递、检测、成像和破坏
6,62
。值得注意的是,将需要进一步研究以评估通过apngt产生的asn
‑
βglc连接的免疫原性,其存在仅在哺乳动物系统中报道过一次
72
。如果这种连接是免疫原性的,这里描述的糖蛋白结构仍然可能在研究、急性治疗应用或免疫中产生重大影响。此外,最近的工作旨在发现或工程化具有放松的糖供体特异性的ngt(例如glcnac)
32,73
,或将这些ngt变体与乙酰转移酶组合以产生n连接的glcnac
32
。我们预计这些方法和未来的进步将与这里描述的大多数生物合成途径兼容,因为nmlgtb可以修改glc或glcnac受体
39
。
[0299]
展望未来,glycoprime提供了一种发现、研究和优化糖基化途径的新方法。例如,未来的应用可以利用glycoprime的开放和灵活的反应环境来优化酶化学计量以用于更均匀的生物合成,并更好地理解gt特异性和动力学。通过使得能够合成和快速组装产生所需糖蛋白的酶,glycoprime还准备好针对按需和按设计产生糖蛋白进一步扩展糖工程化工具包。例如,将脂质相关聚糖补充到无细胞合成反应中
18
‑
20
或在体外产生galnact
22
和ost
19
的最近报道的方法提供了新的机会来在对glycoprime工作流程进行小修饰的情况下发现产生多样的聚糖(n
‑
和o
‑
连接的)的生物合成途径。最后,通过glycoprime途径可访问的多样但简单的聚糖组可有助于阐明提供所需糖蛋白特性的最小基序。总而言之,我们预计这项工作中描述的glycoprime和生物合成途径将加速细菌系统中糖蛋白的工程化,有助于融合糖科学和合成生物学团体。
[0300]
f.方法
[0301]
质粒构建和分子克隆。本研究中使用的质粒的细节和来源以适用的数据库登录号示于图5。在质粒背景下的完整编码序列区显示在图29中。编码cfps中糖基化靶标和gt的密码子优化dna序列由twist bioscience、integrated dna technologies或life technologies合成为基因片段或完整质粒。根据标准分子生物学技术,使用聚合酶链反应(pcr)扩增和gibson组装将基因片段插入卡那霉素抗性pjl1
22
体外表达载体中的ndei和sali限制位点之间
74
。一些gt是用n末端cat
‑
strep
‑
linker(csl)融合序列产生的,该序列已显示增加体外表达
22
(见图29)。用于在clm24δnana大肠杆菌菌株中表达im7
‑
6和fc
‑
6糖基化靶标的质粒是通过来自pjl1.im7
‑
6和pjl1.fc
‑
6的携带优化的apngt糖基化受体序列和his标签的工程化形式的im7(im7
‑
6)和fc(fc
‑
6)的聚合酶链反应(pcr)扩增产生的
22
。然后使用gibson组装将这些基因片段置于具有在ncoi和hindiii限制性位点之间的iptg诱导性表达和羧苄青霉素抗性的pbr322(ptrc99)主链75中。用于在大肠杆菌中表达gt操纵子的质粒是通过从它们的pjl1质粒形式pcr扩增apngt、nmlgtb和cjcst
‑
i或pdst6,然后gibson组装成具有ncoi和hindiii限制性位点之间的阿拉伯糖诱导性表达、pbbr1复制起点和甲氧苄氨嘧啶抗性的pmaf10主链
22
构建的。将使用rbs calculator v2.076设计以用于最大翻译起始率的strep
‑
ii标签、flag标签和核糖体结合位点插入到这些质粒中,如图5和29所示。用于在大肠杆菌中产生cmp
‑
sia的pcon.neua质粒是通过从ptf77 pcr扩增neua随后gibson组装成具有卡那霉素抗性并用p32100启动子修饰以用于在nsii和sali限制位点之间的组成性表达的pconycg主链产生的。
[0302]
用于cfps的细胞提取物的制备。糖基化酶和靶蛋白的cfps使用来自使用成熟的方法制备的最近描述的高产率mg1655衍生大肠杆菌菌株c321.δa.75926的粗制大肠杆菌裂
解物进行
22,26
。简而言之,大肠杆菌细胞的1升培养物在2xytpg培养基(酵母提取物10g/l、胰蛋白胨16g/l、nacl 5g/l、k2hpo
4 7g/l、kh2po
4 3g/l和葡萄糖18g/l,ph7.2)中在2.5升tunair烧瓶中在34℃下在以250r.p.m振荡的情况下从od
600
=0.08开始生长。在od
600
=3.0时在冰上收获细胞,并将其通过在5,000xg在4℃下离心15分钟沉淀。细胞沉淀用冷s30缓冲液(10mm tris
‑
乙酸盐ph 8.2、14mm乙酸镁、60mm乙酸钾、2mm二硫苏糖醇[dtt])洗涤3次,然后在液氮上冷冻,然后储存在
‑
80℃。细胞沉淀在冰上解冻并重新悬浮于每克湿细胞重量0.8ml的s30缓冲液中,并使用q125 sonicator(qsonica)使用三个脉冲(50%振幅,45秒开启和59秒关闭)在冰上裂解在1.4ml等分试样中。超声处理后,向每个等分试样加入4μl的1m dtt。每个等分试样在12,000xg和4℃下离心10分钟。上清液以250r.p.m在37℃下孵育1小时,并以10,000xg在4℃离心10分钟。然后将澄清的s12裂解上清液在液氮上冷冻并储存在
‑
80℃。
[0303]
无细胞蛋白质合成。糖基化靶标和gt的cfps是使用良好建立的panox
‑
sp粗制裂解液系统26进行的。简而言之,cfps反应包含各0.85mm的gtp、utp和ctp;1.2mm atp;170μg/ml的大肠杆菌trna混合物;34μg/ml亚叶酸;16μg/ml纯化的t7 rna聚合酶;2mm的20种标准氨基酸中的每一种;0.27mm辅酶a(coa);0.33mm烟酰胺腺嘌呤二核苷酸(nad);1.5mm亚精胺;1mm腐胺;4mm草酸钠;130mm谷氨酸钾;12mm谷氨酸镁;10mm谷氨酸铵;57mm hepes,ph=7.2;33mm磷酸烯醇丙酮酸(pep);在pjl1载体中编码所需蛋白质的13.3μg/ml dna质粒模板;和27%v/v的大肠杆菌粗制裂解物。大肠杆菌总trna混合物(来自mre600菌株)和磷酸烯醇丙酮酸购自roche applied science。atp、gtp、ctp、utp、20种氨基酸和其他材料购自sigma
‑
aldrich。使用zymopure midi试剂盒(zymo research)从dh5
‑
α大肠杆菌菌株(neb)纯化用于cfps的质粒dna。在有助于二硫键形成的氧化条件下的cfps反应与标准cfps反应类似地进行,不同之处在于使用裂解物与14.3μm iam的30分钟预孵育并添加4mm氧化的l
‑
谷胱甘肽gssg、1mm还原的l
‑
谷胱甘肽和3μm纯化的大肠杆菌dsbc到cfps反应78。所有蛋白质均在2.0ml离心管中的15μl批次cfps反应中表达。对于glycoprime,cfps反应在每种蛋白质的优化温度下孵育20小时(图6)。
[0304]
无细胞蛋白质合成驱动的糖蛋白合成。一锅式cfps
‑
gps与cfps类似地进行,不同之处在于cfps
‑
gps反应具有50μl的总体积,并补充有2.5mm的每个合适的活化的糖供体以及来自所需靶蛋白的多个质粒模板和最多三个gt。cfps
‑
gps反应包含10nm的总质粒浓度,其在反应中的每个独特质粒之间均分。cfps
‑
gps反应在23℃下孵育24h,然后通过ni
‑
nta磁珠针对糖肽进行纯化,或通过lc
‑
ms进行完整蛋白质分析。
[0305]
cfps产率的定量。glycoprime的糖基化靶标和gt的cfps产率是通过使用已建立的方案在标准cfps反应中补充10μm[
14
c]
‑
亮氨酸来确定的
22,26
。简而言之,沉淀cfps中产生的蛋白质和使用5%三氯乙酸(tca)洗涤3次然后通过microbeta2液体闪烁计数器对掺入的放射性进行定量。从在4℃下以12,000xg离心15分钟后分离的级分确定可溶性产率。在不含质粒模板的cfps反应中测量低水平的背景放射性,并将其在计算蛋白质产率之前减去。
[0306]
cfps反应产物的放射自显影图。根据已建立的方法
22
,在glycoprime中使用酶和im7
‑
6靶标的可溶部分的放射自显影图。简而言之,使用mops缓冲液、使用4
‑
12%bolt bis
‑
tris plus sds
‑
page凝胶(invitrogen)分离cfps反应前补充10μm[14c]
‑
亮氨酸并在cfps反应后在4℃以12,000xg离心15分钟的2μl cfps反应。凝胶使用instantblue(expedeon)染
色、成像,然后在玻璃纸膜之间干燥过夜,然后暴露于storage phosphor screen(ge healthcare)72小时。phosphor screen使用typhoon fla7000成像仪(ge healthcare)成像,并且干燥的凝胶使用geldoc xr imager(bio
‑
rad)成像,以帮助与分子量标准阶梯对齐。sds
‑
page和放射自显影凝胶图像分别使用image lab软件6.0.0版和typhoon fla7000控制软件1.2版build 1.2.1.93获得。
[0307]
体外糖基化反应。glycoprime的ivg反应从含有im7
‑
6靶蛋白的已完成的cfps反应的上清液在标准的0.2ml管中组装,并且指示的gt在4℃下以12,000xg离心10分钟。通过[
14
c]
‑
亮氨酸掺入对靶标和酶产率进行定量和优化(图6)。标准ivg反应包含10μm im7
‑
6靶标、指示的量的形成推定的生物合成途径的多达5个gt、10mm mncl2(以提供用于nmlgtb和其他gt的首选金属辅因子)、23mm hepes缓冲液(ph=7.5)和2.5mm的每种所需的核苷酸活化糖供体(根据图8中显示的先前表征的活性)。每个反应包含32μl的总体积,其中有25μl的已完成的cfps反应(必要时,剩余的cfps反应体积由已合成sfgfp的已完成的cfps反应填充)。组装后,包含多达两个gt的ivg反应在30℃下孵育24小时。为了提高转化率,将含有超过两个gt的ivg反应在30℃下孵育24小时,补充额外2.5mm的每种活化的糖供体,然后孵育另外24小时。当需要时,cfps反应和ivg都可以在它们各自的孵育步骤后快速冷冻。孵育后,使用磁性his
‑
标签dynabeads(thermo fisher scientific)从ivg反应纯化im7
‑
6。ivg反应在90μl缓冲液1(50mm nah2po4和300mm nacl,ph8.0)中稀释,并在4℃下以12,000xg离心10分钟。将此上清液在滚筒上在室温下与已用120μl缓冲液1平衡的20μl珠子孵育10分钟。然后用120μl缓冲液1将珠子洗涤3次,然后使用具有500mm咪唑的70μl缓冲液1洗脱。使用3.5kda mwco微透析盒(pierce)将样品针对缓冲液2(12.5mm nah2po4和75mm nacl,ph7.5)透析过夜。一锅式cfps
‑
gps反应的纯化与ivg反应类似地完成。
[0308]
从活大肠杆菌产生糖蛋白。构建大肠杆菌菌株clm24δnana(基因型w3110 δweca δnana δwaal::kan)以实现细胞质中唾液酸的摄取和存活以用于在体内产生唾液酸化糖蛋白。clm24δnana是使用来源于keio集合
79
的weca::kan、nana::kan和waal::kan等位基因以该顺序的p1转导从w3110中产生的。在连续转导之间,使用pe
‑
flp去除卡那霉素标记
80
。如所示的,clm24δnana依次用cmp
‑
sia产生质粒pcon.neua;靶蛋白质粒pbr322.im7
‑
6或pbr322.fc
‑
6;和gt操纵子质粒pmaf10.ngt、pmaf10.apngt.nmlgtb、pmaf10.cjcst
‑
i.nmlgtb.apngt或pmaf10.pdst6.nmlgtb.apngt通过在每个步骤中用适当的抗生素分离个体克隆进行转化。然后将完整的菌株用于接种含有适当抗生素的lb培养基中的5ml过夜培养物,然后将其以od
600
=0.08继代培养到5ml新鲜的lb培养基中,该培养基补充有5mm购自carbosynth的n
‑
乙酰神经氨酸(唾液酸)并使用naoh和hcl调节至ph=6.0。然后将该培养物在37℃下在以250r.p.m.的振荡的情况下生长。通过在od
600
=0.4下用0.2%阿拉伯糖补充培养物来诱导gt操纵子表达,然后在od600=1.0下用1mm iptg诱导靶蛋白表达。iptg诱导后,培养物在28℃和250r.p.m下生长过夜。通过在4℃下以4,000xg离心10分钟使细胞沉淀,在液氮中冷冻,并在
‑
80℃下储存。将细胞沉淀解冻并重新悬浮于630μl含有5mm咪唑并补充有70μl的10mg/ml溶菌酶(sigma)、1μl(250u)benzonase(millipore)和7μl 100x halt蛋白酶抑制剂(thermo fisher scientific)的缓冲液1中。解冻和重新悬浮15分钟后,将细胞在冰上孵育15
‑
60分钟,以50%振幅超声处理45秒,然后以12,000xg离心15分钟。然后将上清液与已用缓冲液1中的5mm咪唑预平衡的50μl his
‑
标签dynabeads一起在室温下在滚筒上
孵育10分钟。然后将珠子用1ml的含有5mm咪唑的缓冲液1洗涤3次,然后用70μl的含有500mm咪唑的缓冲液1通过在滚筒上在室温孵育10分钟进行洗脱。然后在用于lc
‑
ms的糖肽或糖蛋白处理和分析之前,用3.5kda mwco微透析盒针对缓冲液2透析样品过夜。
[0309]
糖蛋白修饰的lc
‑
ms分析。通过将5μl(或约5pmol)his
‑
标签纯化、透析的糖蛋白注射到配备有具有与impact
‑
ii uhr tof质谱仪(bruker daltonics,inc.)偶联的相同填料的10mm保护柱(186004495 waters corp.)的acquity uplc peptide beh c4柱,1.7μm,2.1mm x 50mm(186004495 waters corp.)的bruker elute uplc中通过lc
‑
ms确定完整糖蛋白靶标的修饰。注射前,fc样品用50mm dtt还原。液相色谱使用100%h2o和0.1%甲酸作为溶剂a和100%乙腈和0.1%甲酸作为溶剂b以0.5ml/min的流速和50℃的柱温进行。在从20%到50%b的4分钟梯度期间洗脱感兴趣的蛋白质之前,将20%b的初始条件保持1分钟。通过在71.4%b下0.5分钟、0.1分钟梯度至100%b、在100%b下洗涤2分钟、0.1分钟梯度至20%b和然后在20%b下保持2.2分钟来洗涤和平衡柱子,总共运行10分钟。使用100
‑
3000m/z的ms扫描范围和2hz的光谱速率。在数据收集之前进行外部校准。
[0310]
糖肽修饰的lc
‑
ms分析。用于lc
‑
ms(/ms)分析的糖肽是通过用0.0044μg/μl ms级胰蛋白酶(thermo fisher scientific)在37℃下将his标签纯化的经透析的糖基化靶标消化过夜制备的。注射前,通过与10mm dtt孵育2小时来减少h1ha10样品。lc
‑
ms(/ms)通过将2μl(或约2pmol)的经消化的糖肽注射到配备有具有与impact
‑
ii uhr tof质谱仪偶联的相同填料的10mm保护柱(186004629 waters corp.)的acquity uplc peptide beh c18柱,1.7μm,2.1mm x 100mm(186003686 waters corp.)的bruker elute uplc中来进行lc
‑
ms(/ms)。液相色谱使用100%h2o和0.1%甲酸作为溶剂a和100%乙腈和0.1%甲酸作为溶剂b以0.5ml/min的流速和40℃的柱温进行。将0%b的初始条件保持1分钟,然后在4分钟梯度至50%b的过程中洗脱感兴趣的肽。通过0.1分钟梯度至100%b、在100%b下洗涤2分钟、0.1分钟梯度至0%b和然后在0%b下保持1.8分钟来洗涤和平衡柱子,总共运行9分钟。进行糖肽的lc
‑
ms/ms以确认gt修饰符合先前表征的特异性。伪多反应监测(mrm)ms/ms碎片化被靶向至对应于检测到的完整蛋白质ms峰的理论糖肽质量。使用30ev的碰撞能量将所有糖肽碎片化,其中使用从靶m/z值的
±
2m/z的窗口。源自预期糖基化结构的理论蛋白质、肽和糖离子质量显示于图7和9
‑
11。对于糖肽的lc
‑
ms和lc
‑
ms/ms,使用具有8hz的光谱速率的100
‑
3000m/z的扫描范围。在数据收集之前进行外部校准。
[0311]
外切糖苷酶消化。在可能的情况下,使用来自new england biolabs的具有充分表征的活性的市售酶通过外切糖苷酶消化确认由各种gt和生物合成途径安装的糖键联。如图和图例所示,使用制造商建议的缓冲液和消化条件,将糖蛋白或糖肽与外切糖苷酶在37℃下孵育至少4小时。本研究中使用的外切糖苷酶和相关产品编号为:β1
‑
4半乳糖苷酶s(p0745s);α1
‑
3,6半乳糖苷酶(p0731s);α1
‑
3,4岩藻糖苷酶(p0769s);和α1
‑
2岩藻糖苷酶(p0724s);α1
‑
3,4,6半乳糖苷酶(p0747s);β
‑
n
‑
乙酰葡糖胺苷酶s(p0744s);α2
‑
3神经氨酸酶s(p0743s);和α2
‑
3,6,8神经氨酸酶(p0720s)。
[0312]
lc
‑
ms(/ms)数据分析。lc
‑
ms(/ms)数据使用bruker compass hystar v4.1收集并使用bruker compass data analysis v4.1(bruker daltonics,inc.)进行分析。糖肽ms和完整糖蛋白ms光谱在糖基化和非糖基化糖型的整个洗脱时间进行平均(通过理论糖肽和糖
蛋白电荷状态的提取的离子光谱图确定)。然后通过从100
‑
2,000的完整m/z扫描范围到对于im7
‑
6样品的10,000
‑
14,000da或对于fc
‑
6样品的27,000
‑
29,000da的质量范围的数据分析最大熵解卷积分析完整糖蛋白的ms光谱。选择来自mrm碎片化的代表性lc
‑
ms/ms光谱并手动注释。观察到的糖肽m/z和完整蛋白质解卷积质量在图中注释,理论值显示在图7和9
‑
11中。lc
‑
ms(/ms)数据从bruker compass data analysis导出并在microsoft excel 365中绘制。
[0313]
统计信息。图例指示每个实验的平均值、标准偏差(误差条)和代表性数据的确切样品数。本研究中未使用统计显著性的测试或动物受试者。
[0314]
数据可用性。本研究期间生成或分析的所有数据均包括在内,或可应合理要求从发明人处获得。作为图6中报告的平均值的基础的源数据作为源数据文件提供,可在kightlinger等人,nature communications,10,article no.5404(nov.27,2019)获得,其通过引用整体并入本文。
[0315]
g.实施例1中引用的参考文献
[0316]
1.helenius,a.&aebi,m.intracellular functions of n
‑
linked glycans.science(new york,n.y.)291,2364
‑
2369(2001).
[0317]
2.khoury,g.a.,baliban,r.c.&floudas,c.a.proteome
‑
wide post
‑
translational modification statistics:frequency analysis and curation of the swiss
‑
prot database.scientific reports 1,90(2011).
[0318]
3.sethuraman,n.&stadheim,t.a.challenges in therapeutic glycoprotein production.current opinions in biotechnology 17,341
‑
346(2006).
[0319]
4.elliott,s.等人,enhancement of therapeutic protein in vivo activities through glycoengineering.nature biotechnology 21,414
‑
421(2003).
[0320]
5.varki,a.sialic acids in human health and disease.trends in molecular medicine 14,351
‑
360(2008).
[0321]
6.abdel
‑
motal,u.m.等人,increased immunogenicity of hiv
‑
1 p24 and gp120 following immunization with gp120/p24 fusion protein vaccine expressing alpha
‑
gal epitopes.vaccine 28,1758
‑
1765(2010).
[0322]
7.abdel
‑
motal,u.m.,guay,h.m.,wigglesworth,k.,welsh,r.m.&galili,u.immunogenicity of influenza virus vaccine is increased by anti
‑
gal
‑
mediated targeting to antigen
‑
presenting cells.journal of virology 81,9131
‑
9141(2007).
[0323]
8.lin,c.
‑
w.等人,a common glycan structure on immunoglobulin g for enhancement of effector functions.proceedings of the national academy of sciences usa 112,10611
‑
10616(2015).
[0324]
9.keys,t.g.&aebi,m.engineering protein glycosylation in prokaryotes.current opinion in systems biology 5,23
‑
31(2017).
[0325]
10.li,h.等人,optimization of humanized iggs in glycoengineered pichia pastoris.nature biotechnology 24,210
‑
215(2006).
[0326]
11.yang,z.等人,engineered cho cells for production of diverse,homogeneous glycoproteins.nature biotechnology 33,842
‑
844(2015).
[0327]
12.wang,l.
‑
x.&amin,m.n.chemical and chemoenzymatic synthesis of glycoproteins for deciphering functions.chemistry&biology 21,51
‑
66(2014).
[0328]
13.valderrama
‑
rincon,j.d.等人,an engineered eukaryotic protein glycosylation pathway in escherichia coli.nature chemical biology 8,434
‑
436(2012).
[0329]
14.wacker,m.等人,n
‑
linked glycosylation in campylobacter jejuni and its functional transfer into e.coli.science(new york,n.y.)298,1790
‑
1793(2002).
[0330]
15.feldman,m.f.等人,engineering n
‑
linked protein glycosylation with diverse o antigen lipopolysaccharide structures in escherichia coli.proceedings of the national academy of sciences of the united states of america 102,3016
‑
3021(2005).
[0331]
16.cuccui,j.等人,the n
‑
linking glycosylation system from actinobacillus pleuropneumoniae is required for adhesion and has potential use in glycoengineering.open biology 7(2017).
[0332]
17.naegeli,a.等人,molecular analysis of an alternative n
‑
glycosylation machinery by functional transfer from actinobacillus pleuropneumoniae to escherichia coli.journal of biological chemistry 289,2170
‑
2179(2014).
[0333]
18.jaroentomeechai,t.等人,single
‑
pot glycoprotein biosynthesis using a cell
‑
free transcription
‑
translation system enriched with glycosylation machinery.nature communications 9,2686(2018).
[0334]
19.schoborg,j.a.等人,a cell
‑
free platform for rapid synthesis and testing of active oligosaccharyltransferases.biotechnology and bioengineering(2017).
[0335]
20.guarino,c.&delisa,m.p.a prokaryote
‑
based cell
‑
free translation system that efficiently synthesizes glycoproteins.glycobiology 22,596
‑
601(2012).
[0336]
21.stark,j.c.等人,on
‑
demand,cell
‑
free biomanufacturing of conjugate vaccines at the point
‑
of
‑
care.preprint at https://www.biorxiv.org/content/biorxiv/early/2019/2006/2024/681841.full.pdf(2019).
[0337]
22.kightlinger,w.等人,design of glycosylation sites by rapid synthesis and analysis of glycosyltransferases.nature chemical biology 14,627
‑
635(2018).
[0338]
23.karim,a.s.&jewett,m.c.a cell
‑
free framework for rapid biosynthetic pathway prototyping and enzyme discovery.metabolic engineering 36,116
‑
126(2016).
[0339]
24.dudley,q.m.,anderson,k.c.&jewett,m.c.cell
‑
free mixing of escherichia coli crude extracts to prototype and rationally engineer high
‑
production of 2
′‑
fucosyllactose and 3
‑
fucosyllactose through modular pathway enhancement.metabolic engineering 41,23
‑
38(2017).
[0354]
39.li,y.等人,donor substrate promiscuity of bacterial beta1
‑3‑
n
‑
acetylglucosaminyltransferases and acceptor substrate flexibility of beta1
‑4‑
galactosyltransferases.bioorganic and medicinal chemistry 24,1696
‑
1705(2016).
[0355]
40.priem,b.,gilbert,m.,wakarchuk,w.w.,heyraud,a.&samain,e.a new fermentation process allows large
‑
scale production of human milk oligosaccharides by metabolically engineered bacteria.glycobiology 12,235
‑
240(2002).
[0356]
41.aanensen,d.m.,mavroidi,a.,bentley,s.d.,reeves,p.r.&spratt,b.g.predicted functions and linkage specificities of the products of the streptococcus pneumoniae capsular biosynthetic loci.journal of bacteriology 189,7856
‑
7876(2007).
[0357]
42.lindhout,t.等人,site
‑
specific enzymatic polysialylation of therapeutic proteins using bacterial enzymes.proceedings of the national academy of sciences 108,7397
‑
7402(2011).
[0358]
43.sgambato,a.等人,different sialoside epitopes on collagen film surfaces direct mesenchymal stem cell fate.acs applied materials&interfaces 8,14952
‑
14957(2016).
[0359]
44.imberty,a.&varrot,a.microbial recognition of human cell surface glycoconjugates.curr opin struct biol 18,567
‑
576(2008).
[0360]
45.barthelson,r.,mobasseri,a.,zopf,d.&simon,p.adherence of streptococcus pneumoniae to respiratory epithelial cells is inhibited by sialylated oligosaccharides.infection and immunity 66,1439
‑
1444(1998).
[0361]
46.rabinovich,g.a.&toscano,m.a.turning"sweet"on immunity:galectin
–
glycan interactions in immune tolerance and inflammation.nature reviews immunology 9,338(2009).
[0362]
47.o’reilly,m.k.&paulson,j.c.siglecs as targets for therapy in immune
‑
cell
‑
mediated disease.trends in pharmacological sciences30,240
‑
248(2009).
[0363]
48.chen,w.c.等人,antigen delivery to macrophages using liposomal nanoparticles targeting sialoadhesin/cd169.plos one 7,e39039(2012).
[0364]
49.ragupathi,g.等人,induction of antibodies against gd3 ganglioside in melanoma patients by vaccination with gd3
‑
lactone
‑
klh conjugate plus immunological adjuvant qs
‑
21.international journal of cancer 85,659
‑
666(2000).
[0365]
50.pan,y.,chefalo,p.,nagy,n.,harding,c.&guo,z.synthesis and immunological properties of n
‑
modified gm3 antigens as therapeutic cancer vaccines.journal of medicinal chemistry 48,875
‑
883(2005).
[0366]
51.meuris,l.等人,glycodelete engineering of mammalian cells simplifies n
‑
glycosylation of recombinant proteins.nature biotechnology 32,485
‑
489(2014).
[0367]
52.chen,w.c.等人,in vivo targeting of b
‑
cell lymphoma with glycan ligands of cd22.blood 115,4778
‑
4786(2010).
[0368]
53.zou,w.等人,bioengineering of surface gd3 ganglioside for immunotargeting human melanoma cells.journal of biological chemistry(2004).
[0369]
54.higuchi,y.等人,a rationally engineered yeast pyruvyltransferase pvg1p introduces sialylation
‑
like properties in neo
‑
human
‑
type complex oligosaccharide.scientific reports 6,26349(2016).
[0370]
55.deguchi,t.等人,increased immunogenicity of tumor
‑
associated antigen,mucin 1,engineered to expressα
‑
gal epitopes:a novel approach to immunotherapy in pancreatic cancer.cancer research 70,5259
‑
5269(2010).
[0371]
56.kitov,p.i.等人,shiga
‑
like toxins are neutralized by tailored multivalent carbohydrate ligands.nature 403,669(2000).
[0372]
57.beer,m.v.等人,the next step in biomimetic material design:poly
‑
lacnac
‑
mediated reversible exposure of extra cellular matrix components.advanced healthcare materials 2,306
‑
311(2013).
[0373]
58.laaf,d.,bojarov
á
,p.,pelantov
á
,h.,v.&elling,l.tailored multivalent neo
‑
glycoproteins:synthesis,evaluation,and application of a library of galectin
‑3‑
binding glycan ligands.bioconjugate chemistry 28,2832
‑
2840(2017).
[0374]
59.kalovidouris,s.a.,gama,c.i.,lee,l.w.&hsieh
‑
wilson,l.c.a role for fucoseα(1
‑
2)galactose carbohydrates in neuronal growth.journal of the american chemical society 127,1340
‑
1341(2005).
[0375]
60.yu,y.等人,human milk contains novel glycans that are potential decoy receptors for neonatal rotaviruses.molecular&cellular proteomics 13,2944
‑
2960(2014).
[0376]
61.yu,h.等人,a multifunctional pasteurella multocida sialyltransferase: a powerful tool for the synthesis of sialoside libraries.journal of the american chemical society 127,17618
‑
17619(2005).
[0377]
62.wang,j.等人,lewis x oligosaccharides targeting to dc
‑
sign enhanced antigen
‑
specific immune response.immunology 121,174
‑
182(2007).
[0378]
63.yavuz,e.,maffioli,c.,ilg,k.,aebi,m.&priem,b.glycomimicry:display of fucosylation on the lipo
‑
oligosaccharide of recombinant escherichia coli k12.glycoconjugate journal 28,39
‑
47(2011).
[0379]
64.ilg,k.,yavuz,e.,maffioli,c.,priem,b.&aebi,m.glycomimicry:display of the gm3 sugar epitope on escherichia coli and salmonella enterica sv typhimurium.glycobiology 20,1289
‑
1297(2010).
disulfide
‑
bonded protein using modified extracts of escherichia coli.biotechnology and bioengineering 85,122
‑
129(2004).
[0394]
79.baba,t.等人,construction of escherichia coli k
‑
12in
‑
frame,single
‑
gene knockout mutants:the keio collection.molecular systems biology 2,2006.0008
‑
2006.0008(2006).
[0395]
80.st
‑
pierre,f.等人,one
‑
step cloning and chromosomal integration of dna.acs synthetic biology 2,537
‑
541(2013).
[0396]
前述非专利参考文献的内容通过引用整体并入本文。
[0397]
实施例2.用于将非标准糖掺入活大肠杆菌细胞的方法。
[0398]
概述
[0399]
我们使用上文针对glycoprime方法描述的途径在活大肠杆菌中将唾液酸的非标准(叠氮基)变体在n
‑
连接的三糖(asn
‑
glc
‑
gal
‑
sia)的末端掺入。这种方法可用于提供小治疗剂的一般修饰策略(聚乙二醇化等),以及通过掺入已知与siglecs和半乳凝集素产生耐受性反应的特定唾液酸来产生过敏原疫苗的方法。与现有技术相比这很有趣,因为这提供了在活大肠杆菌中掺入非标准(或可点击)聚糖用于蛋白质治疗的第一个实例。因此,在哺乳动物细胞中或酶促体外方法中可比目前的方法更容易安装非标准唾液酸。如下所述,我们已将使用glycoprime开发的最小唾液酸聚糖途径应用于在大肠杆菌中产生具有可点击唾液酸的重组蛋白。我们的数据表明这些叠氮基唾液酸掺入到im7
‑
6模型蛋白和fc
‑
6中。
[0400]
与经典的免疫原性疫苗相比,致耐受性疫苗被设计成诱导长期的、抗原特异性的、抑制性记忆,其防止对良性物质(例如过敏原或自身免疫性病症的靶标)的炎症免疫反应1。最近有证据表明,siglecs与细胞和抗原上的唾液酸的结合可能在免疫细胞(特别是树突状细胞和调节性t细胞)介导的致耐受反应中发挥重要作用
2,3
。还有进一步的证据表明,siglec
‑
唾液酸相互作用可以使用化学修饰的唾液酸放大和调整4‑9。因此,唾液酸并且尤其是化学修饰的唾液酸与自身免疫所靶向的过敏原或蛋白质的缔合提供了一种很有前景的治疗策略以治疗过敏或自身免疫性病症
7,10
‑
12
。还显示了使用代谢标记将具有炔烃部分的唾液酸掺入到细胞表面蛋白质中以用于使用点击化学
13
进行进一步的化学修饰以调节siglec相互作用7。使用在glycoprime中开发的途径在细菌中安装叠氮基唾液酸的方法可以为这些致耐受性疫苗提供新的途径。
[0401]
一旦在我们的系统中产生,这些可点击的唾液酸可以用针对siglecs的多种高亲和力和选择性配体进一步功能化以产生致耐受性疫苗。由于它发生在具有较低产生成本并且能够更容易工程化的细菌中,因此该系统将与其他基于哺乳动物的代谢标记系统互补。从理论上讲,用于收集该初步数据以实现这一目标的系统的唯一需要的修改是用编码耐受诱导所需要的与apngt靶向的glyctag的重复区域融合的蛋白质的质粒替换靶蛋白质质粒,类似于先前研究中描述的构建体
14
。
[0402]
除了允许调节siglec结合之外,叠氮基唾液酸聚糖还可以用作将聚乙二醇(peg)附接至小治疗剂(例如gm
‑
csf)以增加它们的循环半衰期或将化疗“弹头”附接至短链抗体片段或纳米抗体以实现对癌细胞的精确靶向和破坏的通用化学柄。虽然还有其他方法将化学柄安装到细菌中的蛋白质上,例如掺入非标准氨基酸或先前报道的glycopegylation策略
15,16
,但这种方法确实具有不需要使用正交翻译系统或昂贵的非天然活化糖供体或纯化
的酶的优点(如glycopegylation那样)。
[0403]
方法
[0404]
在本实施例中使用了在上述实施例1中描述的体内方法中实施并在图4中举例说明的相同的三酶途径(apngt、lgtb和cst
‑
1或pd2st6)。简而言之,在大肠杆菌培养物中,细菌用携带三种糖基转移酶、cmp
‑
sia合酶和具有针对ngt的优化的肽受体序列的靶蛋白的三种质粒转化,并补充有叠氮基唾液酸(脱氧c
‑
9;c
‑
5也可以被取代)合成糖(在9位取代,购自carbosynth)。参见图30。如图31和32所示,非标准糖被掺入糖蛋白中;细菌吸收叠氮基糖并使用所实施的途径以非常高的效率(接近100%,参见图31和32中的ms光谱)将其作为三糖asn
‑
glc
‑
gal
‑
azido
‑
sia掺入糖蛋白中。在图中,完整的蛋白质ms数据和糖肽ms/ms数据最终通过将叠氮基唾液酸补充到具有含有与上述对glycoprime所述的相同的三个质粒系统的大肠杆菌的培养基中显示叠氮基唾液酸(与标准唾液酸的区别是24da的质量差)的有效地掺入。因此,nant唾液酸转运蛋白、cmp
‑
sia合酶和pdst6以及cst
‑
i sia t都接受非标准糖。因为系统中没有天然唾液酸,非特异性掺入不是一个严重的问题,在光谱中没有观察到。因此,c9
‑
叠氮基唾液酸可以使用2,6和2,3键联附接。细菌吸收叠氮基糖并使用所实施的途径以非常高的效率将其作为三糖asn
‑
glc
‑
gal
‑
azido
‑
sia掺入糖蛋白中。这是使用重组表达的蛋白质糖基化途径将叠氮基糖单体掺入细菌宿主中重组表达的糖蛋白的第一个实例。
[0405]
下表提供了使用本文公开的组合物和方法进行过敏原基因设计的示例性、非限制性靶标。
[0406]
[0407]
[0408][0409]
在一些实施方案中,选择先前已在大肠杆菌中表达且未二硫键键合的过敏原或自身免疫靶标。另外或可选择地,在一些实施方案中,采用具有例如1、5或10个重复受体序列的“糖模块”。在一些实施方案中,这些多个序列紧密堆积,同时仍确保良好的修饰(例如,coka或hmw1蛋白或glycoscores上的天然受体)。
[0410]
在一些实施方案中,仅添加非天然糖。举例来说,但不作为限制,仅将葡萄糖添加到无细胞裂解物(其可以被精确的糖供体合酶取代)并且可以将单糖加载到糖供体上。
[0411]
实施例2的参考文献:
[0412]
1.mannie,m.d.&curtis,a.d.,2nd tolerogenic vaccines for multiple sclerosis.human vaccines&immunotherapeutics 9,1032
‑
1038(2013).
[0413]
2.u.&p.induction of tolerogenic dendritic cells by endogenous biomolecules:an update.frontiers in immunology 9,2482
‑
2482(2018).
[0414]
3.l
ü
bbers,j.,rodr
í
guez,e.&van kooyk,y.modulation of immune tolerance via siglec
‑
sialic acid interactions.frontiers in immunology 9,2807
‑
2807(2018).
[0415]
4.rillahan,c.d.,schwartz,e.,mcbride,r.,fokin,v.v.&paulson,j.c.click and pick:identification of sialoside analogues for siglec
‑
based cell targeting.angewandte chemie international edition 51,11014
‑
11018(2012).
[0416]
5.spence,s.等人,targeting siglecs with a sialic acid
–
decorated nanoparticle abrogates inflammation.science translational medicine 7,303ra140
‑
303ra140(2015).
[0417]
6.prescher,h.,schweizer,a.,kuhfeldt,e.,nitschke,l.&brossmer,r.discovery of multifold modified sialosides as human cd22/siglec
‑
2 ligands with nanomolar activity on b
‑
cells.acs chemical biology 9,1444
‑
1450(2014).
structure of a hypoallergenic isoform of the major birch pollen allergen bet v 1 and its likely biological function as a plant steroid carrier.journal of molecular biology 325,123
‑
133(2003).
[0431]
在前述描述中,本领域技术人员将容易明白,在不脱离本发明的范围和精神的情况下,可以对本文公开的发明进行各种替换和修改。此处举例说明性描述的本发明可以适当地在不存在此处未具体公开的任何一个或多个元素、一个或多个限制或限制的情况下实施。已使用的术语和表达被用作描述而非限制,并且在使用这些术语和表达时无意排除所示和描述的特征或其部分的任何等效物,但认识到各种修改在本发明的范围内是可能的。因此,应当理解,虽然本发明已经通过特定实施方案和可选特征进行了举例说明,但是本领域技术人员可以对这里公开的概念进行修改和/或变化,并且考虑这样的修改和变化在本发明的范围内。
[0432]
除非本文另有说明或与上下文明显矛盾,否则本文描述的所有方法都可以以任何合适的顺序进行。除非另外声明,否则本文提供的任何和所有实例的使用仅旨在更好地阐明本发明并且不对本发明的范围构成限制。说明书中的任何语言都不应被解释为表明任何未要求保护的元素对于本发明的实践是必不可少的。
[0433]
本文引用了大量专利和非专利参考文献。引用的参考文献通过引用整体并入本文。如果说明书中的术语定义与引用的参考文献中的术语定义不一致,则应根据说明书中的定义来解释该术语。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
![一种5-卤代-2[(烷氧基羰基)氨基]-3-甲基苯甲酸的制备方法与流程](/upload/img/202111/alq13fxki5y.jpg)