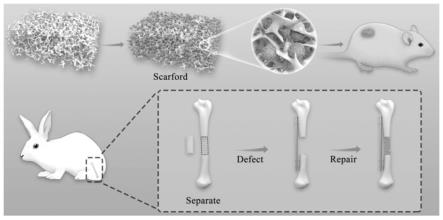
1.本发明涉及生物医学组织工程领域,尤其涉及一种基于多孔水凝胶材料构建的血管化组织工程骨及其应用。
背景技术:
2.当前,组织工程骨作为新一代的骨修复材料,在骨缺损修复与再生领域有着重要的应用前景。通常来讲,组织工程骨是通过生物相容性支架材料负载细胞并进行组织培养来实现的。在众多支架材料中,水凝胶材料以其高度含水、合适的力学强度,是组织工程与再生医学领域常用的支架材料。但是,基于水凝胶材料构建的组织工程骨仍然存在一些不足:1)作为三维培养方式的水凝胶材料在培养过程中存在营养物质交换问题;2)当前构建的组织工程骨大多缺乏血管化,使得植入后难以与周围骨组织整合。因此,如何构建血管化组织工程骨,并解决组织培养过程中的营养物质交换,一直是该领域的技术难题。
3.目前,多孔水凝胶材料的出现为构建血管化组织工程骨提供了一种有效的技术手段。简而言之,多孔水凝胶材料就是通过一定的构建方式,在水凝胶内部制备合适孔径的孔洞。常规的多孔水凝胶的构建方式,包括冷冻干燥法、发泡法、制孔剂法、模板法、相分离法等。然而如何将多孔水凝胶材料用于血管化组织工程骨中仍存在技术难题。
技术实现要素:
4.本发明的目的在于提供一种基于多孔水凝胶材料构建的血管化组织工程骨及其应用。
5.本发明的目的可以通过以下技术方案来实现:
6.本发明的第一个目的是提供一种多孔水凝胶材料的制备方法。
7.本发明中,所述多孔水凝胶材料的制备方法:将水溶性高分子溶于生物相容性介质,通过一定的制备技术,经一定的交联方式,制备多孔水凝胶材料。
8.在本发明的一个实施方式中,所述水溶性高分子选自天然高分子材料或合成高分子材料。
9.在本发明的一个实施方式中,所述天然高分子材料包括天然多糖类物质及其修饰物或降解物,蛋白及其修饰物或降解物。
10.在本发明的一个实施方式中,所述天然多糖类物质包括透明质酸、羧甲基纤维素、甲基纤维素、羟乙基纤维素、羟丙基纤维素、海藻酸、葡聚糖、琼脂糖、肝素、硫酸软骨素、乙二醇壳聚糖、丙二醇壳聚糖、壳聚糖乳酸盐、羧甲基壳聚糖或壳聚糖季铵盐。
11.在本发明的一个实施方式中,所述蛋白包括各种亲水或水溶性动植物蛋白、胶原蛋白、血清蛋白、丝素蛋白、弹性蛋白。
12.在本发明的一个实施方式中,所述蛋白降解物包括明胶或多肽。
13.在本发明的一个实施方式中,所述合成高分子材料包括两臂或多臂聚乙二醇、聚乙烯亚胺、树枝体、合成多肽、聚赖氨酸、聚谷氨酸、聚丙烯酸、聚甲基丙烯酸、聚丙烯酸酯、
聚甲基丙烯酸酯、聚丙烯酰胺、聚甲基丙烯酰胺、聚乙烯醇、聚乙烯吡咯烷酮。
14.在本发明的一个实施方式中,所述水凝胶材料优选为天然多糖类或蛋白类高分子,进一步优选为透明质酸、明胶。
15.本发明中,所述多孔水凝胶的制备技术包括冷冻干燥法、发泡法、制孔法、模板法、相分离法等。优选为冷冻干燥法、制孔法、相分离法。
16.在本发明的一个实施方式中,所述冷冻干燥法是利用深度冷却的溶剂经真空升华而产生孔结构的原理制备多孔水凝胶。首先将无孔水凝胶进行吸水溶胀,然后进行低温冷冻,再经真空干燥,使冷冻固化的水分直接气化,从而在原来的位置留下孔洞。
17.在本发明的一个实施方式中,所述发泡法是利用某些化学物质与酸作用或高温下分解产生气体的特性,从而在交联过程中形成气泡,气泡膨胀后在水凝胶内留下孔洞,获得具备多孔结构的水凝胶材料。
18.在本发明的一个实施方式中,所述制孔剂法是在制孔剂存在下制备水凝胶,再用水或酸将制孔剂浸泡、冲洗或溶解掉,从而在原来的位置留下孔洞,获得具备多孔结构的水凝胶材料。所述制孔剂包括蔗糖、聚乙二醇、氯化钠、碳酸钙、硅胶微粒等。
19.在本发明的一个实施方式中,所述模板法是通过制备中间相液滴模板,在交联过程中,模板液滴均匀分散在水溶性高分子的连续相中,待交联完成后,去除模板,水凝胶内便会留下与模板结构相同或相似的孔洞。
20.在本发明的一个实施方式中,所述相分离法是利用上述水溶性高分子溶液在某些外加物质影响下产生固-液或液-液相分离特点,待交联完成后,再以合适的方式脱除外加物质,从而得到开孔的多孔水凝胶材料。
21.本发明中,所述水凝胶材料的交联方式包括物理交联或化学交联或光交联中的一种或多种交联方式,或单一交联方式的多种材料组合交联形成。
22.在本发明的一个实施方式中,所述物理交联是通过高分子链间的缠结或非共价键交联(参考文献xiangyu liang,pingguo duan,jingming gao,et al.acs biomater.sci.eng.2018,4,3506.)。
23.在本发明的一个实施方式中,所述化学交联是通过高分子链间的共价键交联(参考文献luping cao,bin cao,chengjiao lu,et al.j.mater.chem.b 2015,3,1268.)。
24.在本发明的一个实施方式中,所述光交联是通过发生光化学反应形成共价键交联(参考文献huitang xia,dandan zhao,hailin zhu,et al.acs appl.mater.interfaces2018,10,31704.)。
25.在本发明的一个实施方式中,物理交联构建的水凝胶材料涉及的物理交联反应包括热缩合(温敏性):聚异丙基丙烯酰胺(pnipaam)、嵌段共聚物(peo-ppo-peo、plga-peg-plga、peg-plla-peg、pcl-peg-pcl等);自组装作用:亲疏水作用、氢键作用、主客体相互作用;离子交联:海藻酸与钙离子;静电相互作用:壳聚糖与磷酸类物质。
26.在本发明的一个实施方式中,物理交联水凝胶采用海藻酸与钙离子的交联,即海藻酸与钙离子通过络合作用交联制备水凝胶,即海藻酸水凝胶。所述海藻酸水凝胶可实现的实施方式:将海藻酸高分子溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,加入一定量的钙离子溶液搅拌均匀后,即可获得物理交联的海藻酸水凝胶。
27.在本发明的一个实施方式中,所述化学交联构建的水凝胶材料涉及的化学交联反
应包括巯基-迈克尔加成反应、酰胺缩合反应、席夫碱反应等。
28.在本发明的一个实施方式中,所述化学交联水凝胶采用席夫碱反应制备,即含醛基的高分子衍生物与含胺基的高分子衍生物通过席夫碱反应交联制备水凝胶。所述席夫碱水凝胶可实现的实施方式:将含醛基的高分子衍生物和含氨基的高分子衍生物分别溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,混合均匀后,即可获得化学交联的席夫碱水凝胶。
29.所述含醛基的高分子衍生物的制备方法为邻二醇氧化法,即利用高碘酸钠氧化含邻二醇结构的高分子衍生物得到醛基官能团(参考文献brendan p.purcell,david lobb,jason a.burdick,et al.nat.mater.2014,13,653.)。所述含醛基的高分子衍生物可实现的实施方式:将含有邻二醇结构的水溶性高分子衍生物于蒸馏水中溶解,加入一定量的高碘酸钠,室温下搅拌反应5-12h,加入乙二醇淬灭反应。然后将反应液倒入透析袋中透析2-3d,然后冷冻干燥,即可得到所述的含醛基的高分子衍生物。反应中,水溶性高分子中的邻二醇结构与高碘酸钠的摩尔比优选为1:0.1-2;高分子溶液的质量浓度优选为1.0%-10%w/v。
30.所述含醛基的高分子衍生物的制备方法中,含有邻二醇结构的水溶性高分子衍生物可以为多糖类(如葡聚糖、透明质酸、羧甲基纤维素、海藻酸、硫酸软骨素等),优选为透明质酸、硫酸软骨素。
31.所述含胺基的高分子衍生物可以是天然含胺基多糖类亲水或水溶性高分子及其修饰物或降解物(如乙二醇壳聚糖、丙二醇壳聚糖、壳聚糖乳酸盐、羧甲基壳聚糖、壳寡糖等);也可以是生物或经微生物表达后提取的蛋白及其改性物或降解物(如胶原,血清蛋白及明胶等)。优选为明胶、羧甲基壳聚糖。
32.在本发明的一个实施方式中,所述光交联构建的水凝胶材料是通过光引发聚合交联反应制备,即光引发剂在光源照射下生成的自由基,引发含甲基丙烯酸酯基的高分子衍生物上双键官能团的聚合反应,从而制备光交联水凝胶。
33.在本发明的一个实施方式中,所述光交联水凝胶可实现的实施方式:将含甲基丙烯酸酯基的高分子衍生物和光引发剂溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,在254nm-450nm(优选为365nm或405nm)波长的光源照射下,即可获得光交联水凝胶。
34.所述含甲基丙烯酸酯基的高分子衍生物的制备方法:将含羟基或胺基的水溶性高分子溶于去离子水,冷却至0-4℃,加入甲基丙烯酸酐,再缓慢滴加5m naoh,反应24h,然后将反应液倒入透析袋中,用去离子水透析2-3d,然后冷冻干燥,即可得到所述的含甲基丙烯酸酯基的高分子衍生物。
35.上述含羟基或胺基的多糖类(如:透明质酸、海藻酸、羧甲基纤维素、羧甲基壳聚糖、葡聚糖、硫酸软骨素等)、含羟基或胺基的蛋白或多肽类(如:明胶等),优选为透明质酸、明胶、海藻酸、羧甲基纤维素、硫酸软骨素,进一步优选为透明质酸、明胶。
36.上述光交联水凝胶可实现的实施方式中,用于构建光交联水凝胶材料的光引发剂可以选用i 2959(2-羟基-4'-(2-羟乙氧基)-2-甲基苯丙酮)或lap(苯基-2,4,6-三甲基苯甲酰基膦酸锂)。
37.本发明中,所述水凝胶材料除了通过单一交联方式构建,还可以由水溶性高分子通过物理交联或化学交联或光交联的一种或多种交联方式,或单一交联方式的多种材料组
合交联形成。
38.在本发明的一个实施方式中,所述水凝胶材料可以是由单一交联方式形成的水凝胶材料,称为单网络水凝胶;或者是由两种或两种以上交联方式形成的水凝胶材料,称为互穿网络水凝胶,或双网络水凝胶;或者是由同一交联方式的多种材料复合交联而成,称为复合交联水凝胶。
39.在本发明的一个实施方式中,所述由多种交联方式构建的水凝胶可实现的实施方式:利用物理交联和光交联构建互穿网络水凝胶,将海藻酸、含甲基丙烯酸酯基的高分子和光引发剂溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,在254nm-450nm(优选为365nm或405nm)波长的光源照射下实现光交联。然后将制备的水凝胶浸泡于含钙离子的溶液中交联海藻酸高分子,即可获得互穿网络水凝胶。所述含甲基丙烯酸酯基的高分子优选为甲基丙烯酸酯化明胶(gelma)。
40.在本发明的一个实施方式中,所述由单一交联方式的多种材料组合交联构建的水凝胶可实现的实施方式:将多种含甲基丙烯酸酯基的高分子和光引发剂溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,在254nm-450nm(优选为365nm或405nm)波长的光源照射下实现光交联,即可获得复合交联水凝胶。所述多种含甲基丙烯酸酯基的高分子优选为甲基丙烯酸酯化明胶(gelma)和甲基丙烯酸酯化透明质酸(hama)的复合水凝胶材料。
41.在本发明的一个实施方式中,所述生物相容性介质选自蒸馏水、生理盐水、缓冲液或细胞培养基溶液。根据不同的应用,可选取不同的生物相容性介质。
42.在本发明的一个实施方式中,所述一定浓度的水凝胶前体溶液可以为0.1%w/v-60%w/v,优选为1%w/v-20%w/v。
43.在本发明的一个实施方式中,所述水凝胶材料优选为光交联水凝胶材料,进一步优选为复合光交联水凝胶材料。
44.本发明中,所述多孔水凝胶材料可以添加或不添加成骨活性成分。
45.在本发明的一个实施方式中,所述多孔水凝胶材料添加有成骨活性成分。
46.所述成骨活性成分能够有效促进水凝胶负载的成骨细胞或干细胞的成骨分化,或者刺激内源性干细胞的成骨分化,进一步提高再生骨组织的成熟度。
47.在本发明的一个实施方式中,所述成骨活性成分包括生物活性的无机材料或生物活性因子。
48.在本发明的一个实施方式中,所述成骨活性成分的无机材料包括羟基磷灰石、磷酸钙、碳酸钙、生物玻璃、脱钙骨基质等。在本发明的一个实施方式中,所述生物活性因子包括bmp-2~bmp-9(骨形态发生蛋白)等。
49.在本发明的一个实施方式中,所述成骨活性成分优选为羟基磷灰石、脱钙骨基质、bmp-2。
50.本发明中,所述多孔水凝胶材料可以添加或不添加血管化活性成分。
51.在本发明的一个实施方式中,所述多孔水凝胶材料中添加有血管化活性成分。所述血管化活性成分能够有效促进水凝胶负载的细胞血管化,或者刺激内源性血管化长入,进一步提高组织工程骨的血管化。
52.在本发明的一个实施方式中,所述血管化活性成分优选为富集血小板血浆(prp)、生长因子vegf、tgfβ。
53.在本发明的一个实施方式中,所述多孔水凝胶材料制备可实现的实施方式:将壳聚糖和磷酸盐溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,混合后交联形成水凝胶,然后通过冷冻干燥的方式,即可获得多孔水凝胶材料。
54.在本发明的一个实施方式中,所述多孔水凝胶材料制备可实现的实施方式:将羟基磷灰石、富集血小板血浆(prp)、氧化透明质酸、壳聚糖溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,并加入一定量的碳酸钙作为制孔剂,等比例混合后交联形成水凝胶,再浸泡于酸性溶液除去制孔剂,即可获得负载羟基磷灰石/prp的多孔水凝胶材料。
55.在本发明的一个实施方式中,所述多孔水凝胶材料可实现的实施方式:将生长因子(bmp-2)、生长因子tgfβ、海藻酸、甲基丙烯酸酯化明胶(gelma)和光引发剂(lap)溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,并加入一定量的聚环氧乙烷(peo)作为相分离剂,在254nm-450nm(优选为365nm或405nm)波长的光源照射下实现光交联,并于一定浓度的钙离子溶液浸泡进一步交联,再浸泡于pbs溶液除去相分离剂,即可获得负载bmp-2/tgfβ的多孔水凝胶材料。
56.在本发明的一个实施方式中,所述多孔水凝胶材料可实现的实施方式:将脱钙骨基质粉末、生长因子vegf、甲基丙烯酸酯化明胶(gelma)、甲基丙烯酸酯化透明质酸(hama)的高分子和光引发剂(lap)溶于生物相容性介质,配成一定浓度的水凝胶前体溶液,并加入一定量的聚环氧乙烷(peo)作为相分离剂,在254nm-450nm(优选为365nm或405nm)波长的光源照射下实现光交联,再浸泡于pbs溶液除去相分离剂,即可获得负载脱钙骨基质/vegf的多孔水凝胶材料。
57.在本发明的一个实施方式中,所述生物相容性介质选自蒸馏水、生理盐水、缓冲液或细胞培养基溶液。根据不同的应用,可选取不同的生物相容性介质。
58.在本发明的一个实施方式中,所述一定浓度的水凝胶前体溶液可以为0.1%w/v-60%w/v,优选为1%w/v-20%w/v。
59.本发明还提供基于上述方法得到的多孔水凝胶材料。
60.本发明的第二个目的是提供一种基于多孔水凝胶材料构建血管化组织工程骨的方法。
61.基于多孔水凝胶材料构建血管化组织工程骨的方法包括:将成骨分化潜力的细胞包裹于本发明第一个目的提供的多孔水凝胶材料,并通过一定的培养方式培养一段时间,即可获得成熟的基于多孔水凝胶材料构建的血管化组织工程骨。
62.在本发明的一个实施方式中,所述成骨分化潜力的细胞选自成骨细胞、间充质干细胞、脂肪干细胞或胚胎干细胞等,优选为成骨细胞或间充质干细胞。
63.在本发明的一个实施方式中,所述培养方式包括:体外诱导分化、培养;或体内皮下植入培养,或体外/体内联合培养方式。
64.在本发明的一个实施方式中,所述体外诱导分化、培养方式可以为静态培养或动态培养,静态培养方式即将包裹细胞的多孔水凝胶放置于培养皿中培养,动态培养方式即将包裹细胞的多孔水凝胶放置于生物反应器中搅拌或加压培养,以促进水凝胶中的营养物质交换。经过所述体外诱导分化、培养后得到基于多孔水凝胶材料构建的血管化组织工程骨。
65.在本发明的一个实施方式中,所述体内皮下植入培养是将经过所述体外诱导分
化、培养后获得的组织工程骨植入动物体的皮下培养。所述动物体可以为裸鼠、sd大鼠、兔子、羊、狗、猪,优选为裸鼠、羊。
66.在本发明的一个实施方式中,所述体外/体内联合培养方式是首先在体外诱导培养成相对成熟的血管化组织工程骨(相对成熟的血管化组织工程骨是指:成骨相关基因(alp,runx2,col1)达到正常骨组织基因水平的10%-30%,成血管基因(vegf)达到正常骨组织基因水平的10%-30%),然后植入皮下进一步培养为成熟的血管化组织工程骨(成熟的血管化组织工程骨是指:成骨相关基因(alp,runx2,col1)达到正常骨组织基因水平的80%-100%,成血管基因(vegf)基因达到正常骨组织基因水平的80%-100%)。
67.在本发明的一个实施方式中,所述培养时间为1周-24周,优选为4周-8周。
68.在本发明的一个实施方式中,所述成熟的血管化组织工程骨包括以下生物学与组织学特征:1)dna、胶原、钙盐含量基本达到正常组织水平(基本达到正常组织水平是指:dna含量约50-100ng/mg,胶原含量约占总质量的25%-35%,钙盐含量约占总质量的65%-75%);2)生物力学强度基本达到骨组织的正常水平(基本达到骨组织的正常水平是指:弹性模量大于5mpa);3)组织学上具有清晰的骨小梁结构,以及masson和lap的成骨特异性表达;4)组织学上具有清晰的血管结构,以及cd31的成血管特异性表达。
69.本发明基于多孔水凝胶材料构建血管化组织工程骨的原理:1)多孔水凝胶材料给细胞提供三维的培养环境,并且水凝胶拥有合适的孔隙结构,有利于水凝胶内的营养物质交换,为组织构建提供合适的三维培养体系;2)水凝胶内负载的成骨活性成分能够诱导细胞向成骨方向分化、增殖,负载的血管化活性成分能够促进再生骨组织的血管化。经过一段时间培养,成骨分化潜力的细胞逐渐分化为成熟的成骨细胞,并且分泌出丰富的细胞外基质,最终形成成熟的骨组织;3)水凝胶内预留的孔隙结构,有利于再生血管的长入,从而成功构建血管化组织工程骨。因此,运用本发明提供的方法基本可以通过多孔水凝胶材料包裹成骨分化潜力的细胞构建血管化组织工程骨。
70.本发明的第三个目的是提供基于多孔水凝胶材料构建血管化组织工程骨的方法获得的基于多孔水凝胶材料构建的血管化组织工程骨。
71.本发明的第四个目的是提供基于多孔水凝胶材料构建血管化组织工程骨的应用。
72.本发明提供了基于多孔水凝胶材料构建的血管化组织工程骨在骨缺损修复与再生领域的应用。
73.其中,骨缺损包括粉碎性骨折、骨不连、骨肿瘤、颅骨、下颌骨损伤。
74.与现有技术相比,本发明具有以下优点及有益效果:
75.(1)合适的孔隙结构,促进了水凝胶材料用于组织培养过程中的营养渗透,有利于三维培养模式;
76.(2)水凝胶内部的孔隙结构,为血管的再生预留了生长空间,有利于组织工程骨的血管化再生;
77.(3)负载生物活性物质的多孔水凝胶能够有效促进骨组织再生,以及促进血管化生成。
78.因此,本发明提供的基于多孔水凝胶构建的血管化组织工程骨,可以应用于骨缺损的修复与再生领域。
附图说明
79.图1为明胶多孔水凝胶材料的扫描电镜直观图。
80.图2为明胶多孔水凝胶材料负载细胞的活死细胞染色图。
81.图3为负载细胞的明胶多孔水凝胶材料埋植裸鼠皮下的效果直观图。
82.图4为血管化组织工程骨培养4周后的组织学图。
83.图5为血管化组织工程骨培养4周后的pcr图。
具体实施方式
84.下面结合附图和具体实施例对本发明进行详细说明。
85.实施例一:基于多孔壳聚糖水凝胶材料构建血管化组织工程骨
86.多孔壳聚糖水凝胶材料构建:称取0.05g壳聚糖(cs)溶于1ml pbs溶液(ph=7.4)中,并加入10mg磷酸盐,混合后交联形成水凝胶,然后通过冷冻干燥的方式,即可获得多孔壳聚糖水凝胶材料。
87.血管化组织工程骨构建:从兔子骨髓分离骨髓干细胞,常规分离培养扩增,传代培养至第二代或第三代,收集并调节细胞悬液终浓度为10
×
106/ml,并包裹于上述多孔壳聚糖水凝胶材料,并通过静态培养的方式,于成骨诱导培养基中,放入培养皿中培养8周,即可获得成熟的血管化组织工程骨。
88.实施例二:基于负载hap/prp的多孔水凝胶材料构建血管化组织工程骨
89.氧化透明质酸的合成:将透明质酸(2g,340kda)溶于100ml蒸馏水中至完全溶解,将高碘酸钠(naio4,1g)溶于5ml蒸馏水中,然后缓慢滴加上述溶液,于室温下搅拌反应12h。反应结束后,滴加1ml乙二醇继续搅拌30min,然后将反应液倒入透析袋(mwco 7000)中,用去离子水透析2-3d,冷冻干燥即可得到hao(1.82g)。根据盐酸羟胺滴定法,可以计算出醛基的含量大约为35%。
[0090][0091]
负载hap/prp的多孔水凝胶(hap/prp/hao/cs)材料构建:称取0.02g羟基磷灰石(hap),2mg富集血小板血浆prp,0.05g氧化透明质酸(hao),0.05g壳聚糖(cs)分别溶于1ml pbs溶液(ph=7.4)中,并加入0.01g碳酸钙(caco3)作为制孔剂,于37℃下配成hap/prp/hao/cs的水凝胶前体溶液,等比例混合后交联形成水凝胶,再浸泡于0.01m hcl溶液除去相分离剂,即可获得hap/prp/hao/cs多孔水凝胶材料。
[0092]
血管化组织工程骨构建:从兔子骨髓分离骨髓干细胞,常规分离培养扩增,传代培养至第二代或第三代,收集并调节细胞悬液终浓度为10
×
106/ml,包裹于上述hap/prp/hao/cs多孔水凝胶材料,并通过生物反应器加压培养8周,即可获得成熟的血管化组织工程骨。
[0093]
实施例三:基于负载bmp-2/tgfβ的多孔水凝胶材料构建血管化组织工程骨
[0094]
甲基丙烯酸酯化明胶(gelma)的合成:将明胶(1g)溶于10ml pbs(ph=7.4)中,加热至50℃搅拌至完全溶解,加入0.5ml甲基丙烯酸酐,反应2-3h,反应后用40ml pbs稀释反应液,然后倒入透析袋(mwco 7000)中,用去离子水透析2-3d,冷冻干燥即可得到甲基丙烯
酸酯化明胶(0.9g)。根据核磁氢谱图,可计算出双键的含量大约为75%。
[0095][0096]
负载bmp-2/tgfβ的多孔水凝胶(bmp-2/tgfβ/alg/gelma)材料构建:称取2ng bmp-2,2ng tgfβ,0.02g海藻酸(alg),0.05g gelma,和2mg lap溶于1ml pbs溶液(ph=7.4)中,并加入0.01g聚环氧乙烷(peo)作为相分散剂,于37℃下配成bmp-2/tgfβ/alg/gelma的水凝胶前体溶液,灌注于预制的模具中,在365nm波长的光源照射下实现光交联,并于1m cacl2溶液浸泡进一步交联,再浸泡于pbs溶液除去相分离剂,即可获得bmp-2/tgfβ/alg/gelma多孔水凝胶材料。
[0097]
血管化组织工程骨构建:从兔子骨髓分离骨髓干细胞,常规分离培养扩增,传代培养至第二代或第三代,收集并调节细胞悬液终浓度为10
×
106/ml,包裹于上述bmp-2/tgfβ/alg/gelma多孔水凝胶材料,并通过植入裸鼠皮下进行体内培养8周,即可获得成熟的血管化组织工程骨。
[0098]
实施例四:基于负载脱钙骨基质/vegf的多孔水凝胶材料构建血管化组织工程骨
[0099]
按实施例三的方法制备甲基丙烯酸酯化明胶(gelma)。
[0100]
甲基丙烯酸酯化透明质酸(hama)的合成:将透明质酸(1g,340kda)溶于100ml去离子水,冷却至0-4℃,加入5ml甲基丙烯酸酐,再缓慢滴加5ml 5m naoh,反应24h,然后将反应液倒入透析袋(mwco 7000)中,用去离子水透析2-3d,冷冻干燥即可得到甲基丙烯酸酯化透明质酸(0.9g)。根据核磁氢谱图,可计算出双键的含量大约为60%。
[0101][0102]
负载脱钙骨基质/vegf的多孔水凝胶(dbm/vegf/gelma/hama)材料构建:称取0.05g dbm,2ng vegf,0.05g gelma,0.02g hama和2mg lap溶于1ml pbs溶液(ph=7.4)中,并加入0.01g聚环氧乙烷(peo)作为相分散剂,于37℃下配成dbm/vegf/gelma/hama的水凝胶前体溶液,灌注于预制的模具中,在365nm波长的光源照射下实现光交联,再浸泡于pbs溶液除去相分离剂,即可获得dbm/vegf/gelma/hama多孔水凝胶材料(图1所示)。
[0103]
血管化组织工程骨构建:从兔子骨髓分离骨髓干细胞,常规分离培养扩增,传代培养至第二代或第三代,收集并调节细胞悬液终浓度为10
×
106/ml,包裹于上述dbm/vegf/gelma/hama多孔水凝胶材料(图2所示),并通过植入裸鼠皮下进行体内培养8周,即可获得成熟的血管化组织工程骨(图3所示)。
[0104]
实施例五:血管化组织工程骨的生物学评价
[0105]
体外培养4周后,取材,进行大体观、组织学、q-pcr定量等骨再生和血管再生指标体外检测。实验结果表明,血管化组织工程骨经培养后呈现淡红色的外观,逐渐表现为血管化的骨样组织。组织学上可以观察到成骨细胞在支架材料上聚集,并分泌出细胞外基质,再生骨组织周围有明显的血管化迹象。组织学上,固绿、masson、alp和cd31组织学呈现特异性染色,说明再生骨组织已经逐渐成熟,并有新生血管生成(图4所示)。q-pcr的基因定量数据
表明col1,runx2、ocn和vegf的表达达到正常软骨组织的60%(图5所示)。
[0106]
实施例六:血管化组织工程骨应用于兔子颅骨缺损修复
[0107]
采用新西兰雄性大白兔,每只兔子均在颅骨处制造直径为10mm的骨缺损。实验前按体重随机分组(每组4只):1.血管化组织工程骨修复组;2.不做处理的空白组。手术过程中,首先按实施例四构建成熟的血管化组织工程骨,然后将其填充至缺损部位。在手术3月后,通过静脉注射空气的方法处死实验中的兔子,并取样对实验修复效果进行评价。实验结果表明,使用血管化组织工程骨处理的缺损部位取得了完全的骨修复,而对照组中骨缺损部位没有得到任何修复。因此,该类可血管化组织工程骨对骨缺损有很好的骨修复效果,并且能够与周围骨组织实现很好的整合。
[0108]
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。