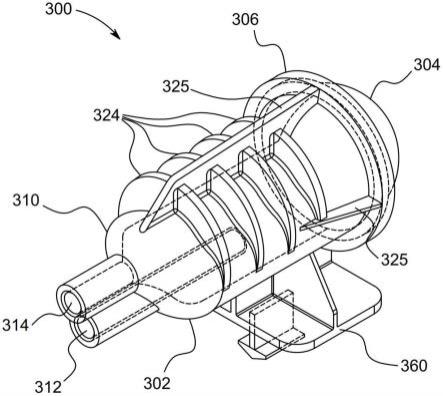
1.本发明属于医学美容技术领域,具体涉及一种刺激弹性蛋白形成的组合物,更具体地涉及包括透明质酸,肌肽和氨基酸等的组合物,其可以用于促进弹性蛋白形成,治疗、减轻和/或改善皮肤或粘膜的症状、紊乱或疾病,抗衰老等用途,属于抗衰老制剂领域。
背景技术:
2.人的皮肤是一种覆盖整个身体的器官,其中,真皮主要由成纤维细胞组成,也存在肥大细胞或组织巨噬细胞(真皮还包含血管和神经纤维)。真皮的无细胞部分(即细胞之间的区域)称为细胞外基质,细胞外基质由多种细胞外组分组成,包括蛋白,如胶原蛋白纤维和弹性蛋白,还包括糖胺聚糖,如透明质酸,硫酸软骨素等,还包括蛋白聚糖和多种糖蛋白,如纤连蛋白等。这些细胞外组分由真皮成纤维细胞合成,故细胞外基质组分的机能障碍和变化可能干扰细胞表现和组织完整性。人皮肤、粘膜细胞外基质组分的功能障碍和变化可能导致皮肤衰老、萎缩、受损或其他与细胞外基质组分的变化相关的皮肤和粘膜的紊乱和/或疾病。
3.此外,随着年龄和/或环境的变化,人体的皮肤等器官或组织会发生衰老。皮肤自然老化,会使皮肤内的胶原蛋白和透明质酸钠含量减少,弹性纤维及胶原纤维变性、皮肤变薄等,这种损伤会出现在全身所有部位的皮肤;皮肤老化可表现出皮肤干燥、粗糙、毛细血管扩张、弹性降低、不规则色素沉着、脂溢性角化等现象或状态。
4.因此,在皮下补充胶原蛋白和/或透明质酸钠,或者刺激胶原蛋白、弹性蛋白形成等维持或增加细胞外基质组分的水平的方法,是治疗、减轻和/或改善与细胞外基质组分变化相关的皮肤或粘膜的症状、紊乱或疾病,改善皮肤老化状态的有效方式或方案。
5.透明质酸是一种天然多糖,由下列重复单元连接而成:n-乙酰-d-葡糖胺和d-葡糖醛酸。透明质酸能够结合和保持水分,在皮肤水合作用中起到支持作用,具有优异的粘弹性。为了避免外源性的透明质酸在皮肤等器官/组织中的快速降解,往往将交联剂与透明质酸交联并且用于产品中,但交联剂(如1,4-丁二醇二缩水甘油醚(bdde))为非人体组织中组分,容易存在未交联情况或解交联情况,这些交联剂作为外来组分,大大提升了安全风险,也导致相关产品的组分确定及其生产工艺、质量控制的难度大大提高。
6.临床上用于人体的胶原蛋白注射填充剂有人源胶原蛋白和非人源胶原蛋白,人源胶原蛋白虽无免疫风险,但获得费时费力,价格昂贵;非人源胶原蛋白有一定的免疫风险,使用存在较多不确定因素;并且胶原蛋白较为昂贵;因此直接注射胶原蛋白填充剂并不是最优方案。
7.弹性蛋白是人体内重要的承重组织,也对皮肤弹性起着重要作用(弹性蛋白在动脉,肺、弹性韧带,弹性软骨等中也具有重要作用),主要负责使被拉伸的组织恢复原来的形状,对保持皮肤弹性、紧实度、光滑性非常重要,如果体内弹性蛋白发生功能障碍或变化,将导致人体发生紊乱、疾病或老化等变化。
8.目前,市场上的部分产品宣称可以补充胶原蛋白或刺激胶原蛋白增加,具有抗衰
老作用,但这些作用未见验证数据,不能确定是否可以促进胶原蛋白增加,更不能确定是否可以促进弹性蛋白形成、增加。
9.氨基酸是蛋白质的结构单元,补充某些氨基酸能为胶原蛋白的合成提供原料,从而为改善皮肤老化状态提供了可能,并且氨基酸无安全风险,获得也较为方便容易。然而,如何合理高效地配比透明质酸类、氨基酸类及其他物质,以得到安全高效易得的抗衰老的制剂,目前还无法获知。
10.因此,提供一种有助于维持或增加细胞外基质组分水平的组合物,对于治疗、减轻和/或改善与细胞外基质组分变化相关的皮肤或粘膜的症状、紊乱或疾病,包括改善皮肤老化状态,是非常有用的和必要的。
技术实现要素:
11.基于目前存在的问题和需求,本发明提供了一种可以用于治疗、减轻和/或改善与细胞外基质组分变化相关的皮肤或粘膜的症状、紊乱或疾病,包括改善皮肤老化状态的组合物。本发明提供的组合物,不仅具有填充材料具备的补充胞外基质的功能,还能刺激、促进成纤维细胞增殖,胶原蛋白和弹性蛋白形成,治疗、减轻和/或改善皮肤或粘膜的症状、紊乱或疾病,改善、解决皮肤的衰老老化现象,如缺水、干燥,色素沉着,皱纹等现象。
12.由此,本发明提供一种组合物,其基本上由以下组分组成:透明质酸和/或其药学上可接受的盐,肌肽,氨基酸或其药学上可接受的盐和缓冲剂;其中,氨基酸包括甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸和亮氨酸。
13.在一些实施方式中,本发明提供的一种组合物,其基本上由以下组分组成:透明质酸和/或其药学上可接受的盐,肌肽,氨基酸或其药学上可接受的盐和缓冲剂;其中,所述氨基酸为甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸和亮氨酸。
14.所述透明质酸药学上可接受的盐可以为透明质酸钠,透明质酸锌,透明质酸钙或其组合;所述缓冲剂为基本上不含有钾元素如钾离子,如所述的缓冲剂不为钾盐如磷酸氢钾或磷酸二氢钾等。
15.所述透明质酸或其药学上可接受的盐的分子量不宜过高,也不宜过低,过高则难以溶解和难以注射,过低,则容易被酶水解或作用较弱或不能达到期望的作用;本发明中,透明质酸或其药学上可接受的盐的分子量可以为约110万道尔顿—约180万道尔顿。在一些实施方式中,所述透明质酸或其药学上可接受的盐的分子量优选为约120万道尔顿—约170万道尔顿。在一些实施方式中,所述透明质酸或其药学上可接受的盐的分子量优选为约130万道尔顿-约160万道尔顿。在一些实施方式中,所述透明质酸或其药学上可接受的盐的分子量优选为约140万道尔顿-约160万道尔顿。在一些实施方式中,所述透明质酸或其药学上可接受的盐的分子量优选为约145万道尔顿-约155万道尔顿。在一些实施方式中,所述透明质酸或其药学上可接受的盐的分子量优选为约148万、约150万或约152万道尔顿。
16.在一些实施方式中,所述透明质酸或其药学上可接受的盐为透明质酸或其钠盐。
17.基于组合物的体积,所述透明质酸或其药学上可接受的盐的含量可以为约2.5mg/ml-约10mg/ml(例如:约3mg/ml、约4mg/ml、约5mg/ml、约6mg/ml、约7mg/ml、约8mg/ml、约9mg/ml或约10mg/ml)。在一些实施方式中,基于组合物的体积,所述透明质酸或其药学上可接受的盐的含量优选为约3mg/ml-约8mg/ml,或优选约3mg/ml-约7.5mg/ml,或优选约4mg/
ml-约6mg/ml,或进一步优选约4.5mg/ml,约5mg/ml,或约5.5mg/ml。
18.所述肌肽可以为l-肌肽(化学名:(s)-2-(3-氨基丙酰胺)-3-(1h-咪唑-4-基)丙酸),或l-肌肽的衍生物。
19.基于组合物的体积,所述肌肽的含量可以为0.1mg/ml-5.0mg/ml(如0.5mg/ml,1.0mg/ml,1.5mg/ml,3.0mg/ml),优选为0.5mg/ml-2.0mg/ml。在一些实施方式中,基于组合物的体积,所述肌肽的含量为1.5mg/ml,更有利于组合物刺激、促进胶原蛋白和弹性蛋白的形成及抗衰老作用。
20.所述氨基酸药学上可接受的盐可以为氨基酸的盐酸盐,硫酸盐,乙酸盐,柠檬酸盐,钠盐,镁盐或钙盐。在一些实施方式中,氨基酸药学上可接受的盐为所述氨基酸的盐酸盐或钠盐。
21.在组合物中包含本发明所述的氨基酸,有利于为皮肤提供营养成分,有助于刺激、促进胶原蛋白和弹性蛋白的形成,使组合物具有更好的改善疾病症状、抗衰老作用。
22.根据本发明的实施例,发明人发现,相对单一成分或其他组合,将透明质酸和/或其药学上可接受的盐、肌肽及氨基酸或其药学上可接受的盐按照本发明的方案组合,对促进皮肤、软组织等的胶原蛋白和弹性蛋白的形成及抗衰老作用有协同作用,本发明的组合物,更有利于刺激、促进胶原蛋白和弹性蛋白的形成,能够更好的改善皮肤等的疾病症状、衰老现象。
23.基于组合物的体积,所述氨基酸或其药学上可接受的盐的含量独立地可以为0.01mg/ml-2.0mg/ml,优选0.05mg/ml-1.5mg/ml或0.05mg/ml-1.0mg/ml。在一些实施方式中,基于组合物的体积,所述氨基酸或其药学上可接受的盐的含量独立地为0.1mg/ml或1.0mg/ml,有利于刺激、促进弹性蛋白和/或胶原蛋白形成。
24.根据本发明的实施例,所述组合物的ph可以为6.5-8.0,优选6.8-7.6。在一些实施方式中,所述组合物的ph优选为6.9,7.0,7.1,7.2,7.3,7.4或7.5。所述ph范围有助于使组合物适宜使用于皮肤和/或适宜的渗透压。
25.根据本发明的实施例,基于组合物的体积计算,本发明提供的组合物,钾离子含量不超过0.008mg/ml,优选不超过0.007mg/ml或优选不超过0.005mg/ml。在一些实施方式中,除所使用的物料引入的杂质钾离子外,所述组合物不含钾离子。发明人发现,控制组合物中钾离子的含量在本发明所述的范围内,有利于所述组合物促进皮肤、软组织等的胶原蛋白和弹性蛋白的形成及抗衰老作用。如果组合物中钾离子的含量超出本发明所述的范围,根据本发明所述得到的组合物,其促进皮肤、软组织等的胶原蛋白和弹性蛋白的形成及抗衰老作用将降低减弱。
26.所述缓冲剂可以调节组合物的ph和/或渗透压,可以为任意适宜的量,可以为任意适宜浓度的含水溶液,以有助于使组合物具有适宜皮肤使用的渗透压、流动性和/或稳定性,使组合物可以用于注射于人体皮肤或软组织等部位,或使组合物可以以外用如涂抹,贴敷等方式用于人体皮肤等部位。所述缓冲剂可以包括氯化钠,盐酸,氢氧化钠,磷酸二氢钠或其水合物,磷酸氢二钠或其水合物中的一种或多种;或者所述缓冲剂是由氯化钠,盐酸,磷酸二氢钠或其水合物,磷酸氢二钠或其水合物和氢氧化钠中的一种或多种配制成的水溶液。在一些实施方式中,所述缓冲剂包括磷酸氢二钠或其水合物。在一些实施方式中,所述缓冲剂包括磷酸二氢钠或其水合物。在一些实施方式中,所述缓冲剂包括磷酸氢二钠或其
水合物,还包括磷酸二氢钠或其水合物。在一些实施方式中,所述缓冲剂包括或为磷酸二氢钠和氢氧化钠。在一些实施方式中,所述缓冲剂为磷酸氢二钠(na2hpo4)或其水合物和磷酸二氢钠(nah2po4)或其水合物配制成的水溶液。在一些实施方式中,所述缓冲剂ph为6.8-7.6。在一些实施方式中,所述缓冲剂ph为7.0,7.2,或7.4。
27.在一些实施方式中,前述的组合物基本上由以下组分组成:透明质酸和/或透明质酸钠,l-肌肽,甘氨酸或其盐,脯氨酸或其盐,赖氨酸或其盐,缬氨酸或其盐,丙氨酸或其盐,亮氨酸或其盐和缓冲剂;所述缓冲剂包括氯化钠,盐酸,氢氧化钠,磷酸二氢钠或其水合物,磷酸氢二钠或其水合物中的一种或多种;所述组合物的ph为6.8-7.6。在一些实施方式中,前述的组合物基本上由以下组分组成:透明质酸和/或透明质酸钠,l-肌肽,甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸,亮氨酸和缓冲剂;所述缓冲剂包括氯化钠,盐酸,氢氧化钠,磷酸二氢钠或其水合物,磷酸氢二钠或其水合物中的一种或多种;所述组合物的ph为6.8-7.6;能够较好地刺激、促进弹性蛋白和胶原蛋白形成和细胞新生。
28.在一些实施方式中,前述的组合物基本上由以下组分组成:透明质酸和/或透明质酸钠,l-肌肽,甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸,亮氨酸和缓冲剂;其中,所述缓冲剂包括氯化钠,盐酸,氢氧化钠,磷酸二氢钠或其水合物,磷酸氢二钠或其水合物中的一种或多种;所述组合物的ph为6.8-7.6;所述透明质酸或透明质酸钠的分子量为130万道尔顿-160万道尔顿;能够较好地刺激、促进弹性蛋白和胶原蛋白形成和细胞新生。
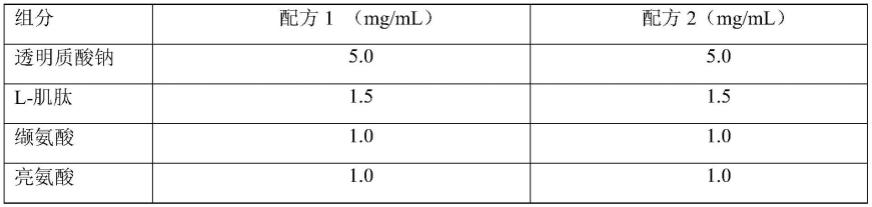
29.在一些实施方式中,前述的组合物为配方1或配方2,分别基本上由以下含量的组分组成,含量基于组合物的体积计算:
[0030][0031][0032]
;其中,透明质酸钠的分子量为130万-160万道尔顿;钾离子含量低于0.008mg/ml。
[0033]
本发明提供的组合物,可以为注射剂,用于注射于人体皮肤或软组织等部位,也可以为外用制剂,用于外用涂抹或贴敷于人体皮肤等。
[0034]
本发明还提供制备所述组合物的方法。所述方法能够简便地获得本发明的组合物,使所述组合物中的成分不会发生降解等不符合质量要求的现象。
[0035]
一种制备前述组合物的方法,包括:将透明质酸和/或其药学上可接受的盐,肌肽,氨基酸或其药学上可接受的盐和缓冲剂混合,任选加水至足量,然后除菌,得到组合物。
[0036]
在一些实施方式中,一种制备前述组合物的方法,包括:将透明质酸和/或其药学上可接受的盐,肌肽,氨基酸或其药学上可接受的盐与水混合,然后与缓冲剂混合,任选地加水至足量,然后除菌,得到组合物。
[0037]
在一些实施方式中,一种制备前述组合物的方法,包括:或者包括:将缓冲剂,肌肽和氨基酸或其药学上可接受的盐混合,任选除菌,再与透明质酸或其药学上可接受的盐混合,然后除菌,得到组合物。
[0038]
在一些实施方式中,一种制备前述组合物的方法,包括:以缓冲剂水液为溶剂,搅拌条件下,加入透明质酸或其药学上可接受的盐,肌肽,氨基酸或其药学上可接受的盐,充分混合,任选地调节ph或加水至足量,然后除菌,得到所述组合物。
[0039]
在一些实施方式中,一种制备前述组合物的方法,包括:将透明质酸钠,l-肌肽,甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸和亮氨酸与水混合,加入缓冲剂,调节ph至6.8-7.6,任选地加水至足量,然后除菌,得到组合物。
[0040]
在一些实施方式中,一种制备前述组合物的方法,包括:将透明质酸钠,l-肌肽,甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸和亮氨酸与缓冲剂溶液混合,控制ph为6.8-7.6,任选地加水至足量,然后除菌,得到组合物。
[0041]
在一些实施方式中,一种制备前述组合物的方法,包括:将l-肌肽,甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸和亮氨酸与缓冲剂溶液混合,控制ph为6.8-7.6,然后与透明质酸钠混合,任选地加水至足量,然后除菌,得到组合物。
[0042]
所述除菌可以使用微孔滤膜过滤除菌,也可以使用其他方式,如终端灭菌法,辐照灭菌法等。在一些实施方式中,采用0.22μm滤膜过滤除菌。
[0043]
为了获得可以用于注射的所述组合物,达到中国药典注射剂要求的无菌质量标准,前述的组合物还可以在无菌环境下或采用无菌操作等无菌生产工艺制备。
[0044]
在一些实施方式中,一种制备前述组合物的方法,包括:以ph为6.8-7.6的缓冲剂水溶液为溶剂,搅拌条件下,加入l-肌肽,甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸和亮氨酸,充分混合,然后加入透明质酸钠,充分混合,配制成含透明质酸钠5mg/ml,l-肌肽1.5mg/ml,甘氨酸0.1mg/ml,脯氨酸0.1mg/ml,赖氨酸0.1mg/ml,缬氨酸1mg/ml,丙氨酸1mg/ml和亮氨酸1mg/ml的溶液,然后0.22μm滤膜过滤除菌,得到所述组合物。
[0045]
在一些实施方式中,一种制备前述组合物的方法,包括:以ph为6.8-7.6的缓冲剂水溶液为溶剂,搅拌条件下加入l-肌肽,甘氨酸,脯氨酸,赖氨酸,缬氨酸,丙氨酸和亮氨酸,充分混合,然后加入透明质酸钠,充分混合,配制成含透明质酸钠5mg/ml,l-肌肽1.5mg/ml,甘氨酸0.3mg/ml,脯氨酸0.1mg/ml,赖氨酸0.1mg/ml,缬氨酸1mg/ml,丙氨酸0.5mg/ml和亮氨酸1mg/ml的溶液,然后0.22μm滤膜过滤除菌,得到所述组合物。
[0046]
本发明提供的制备组合物的方法,可以将组合物制备成注射剂,也可以制备成外用制剂。
[0047]
所述制备组合物的方法,简便、可控,易于操作,可以简便地获得组合物,并且使组合物中的成分不会发生降解、变性等不符合质量要求的现象。
附图说明
[0048]
图1示c系列样品对弹性蛋白分泌的定量分析,其中*表示p<0.05;
[0049]
图2示ha系列样品的浸提液对hff-1细胞弹性蛋白分泌的影响(24h),*表示p<0.05;
[0050]
图3示组合物样品(浸提液)对hff-1细胞增殖的影响(24h、48h、72h);
[0051]
图4示组合物样品(浸提液)对hff-1细胞增殖的影响(24h、48h、72h,形态);
[0052]
图5示组合物样品(浸提液)对hff-1细胞迁移的影响(0h、12h、24h);
[0053]
图6示组合物样品(浸提液)对hff-1细胞胶原蛋白分泌的影响(24h);
[0054]
图7示组合物样品(浸提液)对hff-1细胞弹性蛋白分泌的影响(48h),*表示p<0.05;
[0055]
图8示组合物样品(浸提液)对氧化损伤模型细胞sod活力的影响,其中,a表示与对照组比较,p《0.05,b表示与模型组比较,p《0.05;
[0056]
图9示组合物样品(浸提液)对氧化损伤模型细胞mda水平的影响,其中,a表示与对照组比较,p《0.05,b表示与模型组比较,p《0.05。
具体实施方式
[0057]
术语“包含”或“包括”为开放式表达,即包括本发明所指明的内容,但并不排除其他方面的内容。
[0058]
本发明中,“基本上由以下组分组成”表示所述组合物还可以含有不可避免的杂质和水。
[0059]
本发明中,ppm表示百万分之一。
[0060]
本发明中,任选表示可以有也可以没有。
[0061]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“一些实施方式”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0062]
本发明中,室温为环境温度,在20℃-30℃,或者22℃-28℃,或者25℃。
[0063]
本发明中,透明质酸或其药学上可接受的盐的分子量以重均分子量计。
[0064]
本发明中,组分的含量计算方法为:组合物中组分的重量/组合物的体积,如透明质酸钠含量为5mg/ml,表示每1ml组合物含有透明质酸钠5mg。
[0065]
组合物中,透明质酸浓度基于透明质酸或透明质酸钠总质量计算,如样品中是含透明质酸则以透明质酸计算,如样品中是含透明质酸钠,则以透明质酸钠计算,如样品中是含有透明质酸和透明质酸钠,则以二者总量计算。
[0066]
本发明中,待测样品的各种测试实验的实验方法参见如下描述:
[0067]
对hff-1细胞增殖的影响:hff-1细胞以dmem高糖培养基(含15%胎牛血清)制备细胞悬液后,接种至96孔板,每孔接种细胞量为2
×
104个,细胞贴壁后,弃去原培养基;根据分组设计,加入各待测样品,每组设3个平行孔;37℃、5% co2条件下培养24h、48h或72h后,以cck-8法检测细胞增殖率,倒置显微镜观察细胞形态。
[0068]
cck-8法用于细胞增殖检测的原理:cck-8化学名为2-(2-甲氧基-4-硝基苯基)-3-(4-硝基苯基)-5-(2,4-二磺酸苯)-2h-四唑单钠盐,在电子载体pms的存在下可被细胞线粒体中的脱氢酶还原为水溶性的橙黄色甲瓒产物。对于平行培养的同种细胞,活细胞的数量与甲瓒生成量成正比,细胞增殖越快、状态越好,甲瓒转化量越多、颜色越深,测定450nm下的吸光值,生成的甲臜的量与活细胞数量成正比,利用这一特性可进行细胞增殖和毒性检测分析。
[0069]
对hff-1细胞胶原蛋白分泌的影响:参考gb/t 16886.5-2017标准,采用酶联免疫吸附(elisa)方法评价样品对hff-1细胞胶原蛋白分泌的影响。hff-1细胞接种于6孔板上,待细胞贴壁后,弃去原培养基,根据分组设计,加入各待测样品,每组设3个平行孔;37℃、5% co2条件下培养24h或48h,胰酶消化收集细胞并超声破碎,3000转/分钟离心20分钟,收集上清,根据i型胶原蛋白elisa检测试剂盒的说明书进行后续操作,以对照组的胶原水平为基数计算各组的i型胶原蛋白水平。
[0070]
对hff-1细胞弹性蛋白分泌的影响:参考gb/t 16886.5-2017标准,采用酶联免疫吸附(elisa)方法评价样品对hff-1细胞弹性蛋白分泌的影响。hff-1细胞接种于6孔板上,待细胞贴壁后,弃去原培养基,根据分组设计,加入各待测样品,每组设3个平行孔;37℃、5% co2条件下培养24h或48h;胰酶消化收集细胞并超声破碎,3000转/分钟离心20分钟,收集上清;采用弹性蛋白elisa检测试剂盒测定各组的弹性蛋白浓度,以对照组数值为基数计算各组弹性蛋白水平。
[0071]
对hff-1细胞拮抗氧化损伤功能的影响:参考gb/t 16886.5-2017标准,采用sod(超氧化物歧化酶)和mda(丙二醛)两种常用氧化损伤生化指标评价样品拮抗氧化损伤的功能活性。根据经典方法建立过氧化氢(h2o2)氧化损伤模型,使用800μmmol/l的h2o2造模。将hff-1细胞接种于6孔板,细胞密度为5
×
105个/孔,待细胞贴壁后,弃去原培养基,根据分组设计,加入各待测样品,37℃、5% co2条件下培养24h;胰酶消化收集细胞并超声破碎,2500转/分钟离心10分钟,收集上清;分别按照sod试剂盒、mda试剂盒操作要求检测各组sod和mda水平。
[0072]
对hff-1细胞迁移的影响:参考gb/t 16886.5-2017标准,采用细胞划痕实验评价样品对hff-1细胞迁移的影响。取对数生长期的hff-1细胞,按2
×
105个/孔细胞数接种于6孔板中,37℃、5% co2条件下培养24h,以200μl移液器吸头在培养板孔内划线,pbs洗涤3次;根据分组设计,加入各待测样品,每组设3个平行孔;37℃、5% co2条件下培养12h或24h,然后显微镜观察细胞迁移情况。
[0073]
为了使本领域的技术人员更好地理解本发明的技术方案,下面进一步披露一些非限制实施例,对本发明作进一步的详细说明。
[0074]
以下实施例中,涉及的部分试剂/材料的配制方法参见以下说明。
[0075]
完全培养基配制方法:dmem高糖培养基 15% fbs(胎牛血清) 1% ps(青霉素100u/ml和链霉素100μg/ml)。
[0076]
pbs:磷酸盐缓冲液(使用nah2po4和na2hpo4配制),0.01mol/l,ph为7.0。
[0077]
h2o2(过氧化氢)溶液配制方法:将30%过氧化氢用pbs(ph 7.2-7.4)稀释为3% h2o2溶液,并过滤除菌分装,4℃保存;800μmol/l h2o2:取10μl 3% h2o2溶液稀释至100μl,从中取16.5μl加2ml完全培养基,即得;400μmol/l h2o2:取1ml 800μmol/l h2o2,以完全培
养基等比例稀释,即得;200μmol/l h2o2:取1ml 400μmol/l h2o2,以完全培养基等比例稀释,即得。
[0078]
样品的浸提液制备方法:参考“gb/t 16886.12-2017医疗器械生物学评价样品制备与参照材料”中样品制备方法进行浸提液制备:取0.1g样品,加1ml完全培养基,振荡混匀,37℃培养箱孵育24h,现用现配。
[0079]
第一部分:分别测试各类组分对hff-1细胞的多种功能/特性的影响,涉及的样品分组、编号、组分、浓度及配制方法参见以下说明。
[0080]
各样品分组如下表。
[0081]
各样品分组
[0082]
样品样品信息对照组完全培养基a系列l-肌肽b系列甘氨酸、脯氨酸和赖氨酸组合,质量比1:1:1c系列缬氨酸、丙氨酸和亮氨酸组合,质量比1:1:1ha系列高、中、低分子量透明质酸钠
[0083]
a-c系列各样品配制及其浓度参见如下各表。
[0084]
a系列样品编号a1.0a1.5a2.0a系列母液体积(45mg/ml,μl)33.35067dmem高糖培养基 15%fbs体积(ml)1.471.451.43总体积(ml)1.51.51.5a系列样品浓度(mg/ml)1.01.52.0
[0085]
b系列样品编号b0.1b0.5b1.0b2.0b3.0b系列母液体积(15mg/ml,μl)1050100200300dmem高糖培养基 15%fbs体积(ml)1.491.451.41.31.2总体积(ml)1.51.51.51.51.5b系列样品浓度(mg/ml)0.10.51.02.03.0
[0086]
c系列样品编号c0.1c0.5c1.0c2.0c3.0c系列母液体积(15mg/ml,μl)1050100200300dmem高糖培养基 15%fbs体积(ml)1.491.451.41.31.2总体积(ml)1.51.51.51.51.5c系列样品浓度(mg/ml)0.10.51.02.03.0
[0087]
其中,a系列母液配制方法:以l-肌肽78.6mg与dmem高糖培养基1.75ml混合,配制成45mg/ml的溶液;b系列母液配制方法:甘氨酸、脯氨酸和赖氨酸各15mg与1ml dmem高糖培养基合,配制成15mg/ml的溶液;c系列母液配制方法:缬氨酸、丙氨酸和亮氨酸各15mg与1ml dmem高糖培养基混合,配制成15mg/ml的溶液。
[0088]
ha(透明质酸钠)系列样品配制方法:以0.01mol/l ph=7.0的磷酸盐缓冲液(na2hpo4/nah2po4)溶解透明质酸钠,制备得到一系列样品,其中,高分子量组(h)透明质酸钠分子量为150万道尔顿,中分子量组(m)分子量为80-100万道尔顿,低分子量组(l)分子量
为30-50万道尔顿,具体参见下表。
[0089][0090]
实施例1:测试a系列、b系列、c系列样品和ha系列样品(浸提液)对hff-1细胞增殖的影响
[0091]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,a系列-c系列各浓度组,ha系列样品的浸提液。
[0092]
实验结果:
[0093]
1)b系列、c系列高浓度样品(3mg/ml)在不同时间点均对hff-1有不同程度抑制作用;b系列中低浓度样品(≤0.5mg/ml)对hff-1细胞增殖基本无抑制作用,其中,b0.1样品在48h、72h均可显著促进细胞增殖,b0.5样品在72h时可显著促进细胞增殖,但在24h、48h时则表现为轻微抑制作用;c系列中低浓度样品(≤2mg/ml)对hff-1细胞增殖抑制较低,细胞毒性均为0/i级,满足注射植入的要求;
[0094]
2)a系列样品(l-肌肽)在不同浓度、不同时间点时细胞毒性均为0级,其中,相比对照组、a1.0和a2.0样品,a1.5样品在72h可显著促进hff-1细胞增殖。
[0095]
3)ha样品(透明质酸钠)中的中分子量组(m)的对hff-1细胞增殖的抑制作用高于高分子量(h)和低分子量组(l),h0.5、h0.8样品在72h时可促进细胞增殖。
[0096]
根据结果可知,不同浓度氨基酸对hff-1细胞增殖有不同影响。不同分子量的透明质酸钠对hff-1细胞增殖作用不同。
[0097]
实施例2:测试b系列样品和ha系列样品(浸提液)对hff-1细胞胶原蛋白分泌的影响
[0098]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,b系列各浓度组,ha系列样品的浸提液。
[0099]
实验结果:
[0100]
1)b系列在中低浓度时可促进成纤维细胞的胶原蛋白分泌,较高浓度时(如3.0mg/ml)则抑制胶原蛋白分泌;
[0101]
2)24h时,b系列对胶原蛋白分泌的影响作用不显著;48h时,表现出显著的刺激胶原蛋白分泌活性:b系列的0.1mg/ml-2.0mg/ml浓度样品均可显著刺激细胞胶原蛋白分泌,0.1mg/ml浓度样品效果最佳,0.5mg/ml浓度样品效果略次之,而3.0mg/ml的高浓度样品对胶原蛋白分泌略有抑制,但影响不显著。
[0102]
3)ha样品(透明质酸钠)中,高分子量组(h)促进胶原蛋白分泌作用最强,低分子量组(l)略优于中分子量组(m);同分子量、不同浓度样品对胶原蛋白分泌的影响作用基本无差异。
[0103]
实施例3:测试c系列样品和ha系列样品(浸提液)对hff-1细胞弹性蛋白分泌的影响
[0104]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,c系列各浓度组,ha系列样品的浸提液。
[0105]
实验结果:
[0106]
1)培养24h,c系列在不同浓度对hff-1细胞形态均无明显影响,高浓度组也未见细胞肿胀、死亡等现象;
[0107]
2)c系列在不同浓度均可显著促进弹性蛋白分泌,在0.1-1.0mg/ml中低浓度梯度范围内,c系列浓度对弹性蛋白分泌的促进作用与浓度呈正相关,1.0mg/ml浓度促进弹性蛋白分泌最为显著(参见图1)。
[0108]
3)24h时,ha样品(透明质酸钠)总体上有刺激弹性蛋白分泌的趋势,其中,高分子量组中的h0.5样品对弹性蛋白分泌的促进作用极为显著,其他样品也可显著刺激、促进弹性蛋白分泌,刺激促进作用依次为m0.6>l0.5>h0.8,m0.3样品对弹性蛋白分泌略有抑制作用,但不显著(参见图2)。
[0109]
实施例4:测试a系列样品和ha系列样品(浸提液)对hff-1细胞拮抗氧化损伤功能的影响
[0110]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,a系列各浓度组,ha系列样品的浸提液。
[0111]
实验结果:
[0112]
1)a系列在不同浓度梯度、不同时间点对过氧化氢导致的氧化损伤均有显著拮抗作用,可增加内源性抗氧化酶sod(超氧化物歧化酶)活力、降低过氧化产物mda(丙二醛)含量;其中,1.5mg/ml浓度a组合提升sod活力效果最为显著;
[0113]
2)在各浓度梯度中,a1.5样品氧化拮抗活性最为突出,提示l-肌肽在1.5mg/ml浓度时拮抗氧化胁迫效果最优。
[0114]
根据第一部分的实验结果可知,氨基酸组合及其浓度/含量,透明质酸钠的分子量及其浓度/含量,都对细胞的各项性能/特性有一定的影响。
[0115]
根据第一部分的实验结果,发明人设计了不同组合的样品,以期获得有利于抗衰老的组合物,并且进行了第二部分实验。
[0116]
第二部分:分别测试不同组合的样品对hff-1细胞的多种功能/特性的影响,涉及的样品分组、编号、组分、浓度及配制方法参见以下说明;其中对照组(空白组)为完全培养基。
[0117][0118]
[0119]
对照组1-对照组4样品制备方法:以nah2po4和na2hpo4混合物的水溶液(0.01mol/l,ph为7.0,分别称取各0.1mol,定容至1l,稀释至0.01mol/l,即得)为溶剂,先加入各氨基酸和l-肌肽,混合均匀,使各组分浓度达到设计值,再经0.22μm滤膜过滤除菌;然后加入透明质酸钠,持续搅拌至完全溶解,4℃静置12小时,0.22μm滤膜过滤除菌,分别得到各对照组样品。
[0120]
预实验例1:对照组样品(浸提液)对hff-1细胞增殖的影响
[0121]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,对照组1-对照组4的浸提液。
[0122]
实验结果:
[0123]
各组样品对hff-1细胞的增殖几乎无抑制作用,对细胞形态也无影响作用,证明适于注射。
[0124]
预实验例2:对照组样品(浸提液)对hff-1细胞胶原蛋白分泌的影响
[0125]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,对照组1-对照组4的浸提液。
[0126]
实验结果:对照组1-对照组4的胶原蛋白水平都高于对照组,各组的胶原蛋白水平高低顺序为:对照组《对照组2《对照组4《对照组3《对照组1。
[0127]
组合物1和组合物2样品配方:
[0128]
组合物样品编号组合物1组合物2组分配方1(mg/ml)配方2(mg/ml)透明质酸钠5.05.0l-肌肽1.51.5缬氨酸1.01.0亮氨酸1.01.0丙氨酸1.00.5甘氨酸0.10.3赖氨酸0.10.1脯氨酸0.10.1缓冲剂nah2po4和na2hpo4的水溶液nah2po4和na2hpo4的水溶液ph6.8-7.66.8-7.6
[0129]
组合物1和组合物2制备方法:分别按照配方1和配方2,以nah2po4和na2hpo4混合物的水溶液(0.01mol/l,ph为7.0,分别称取各0.1mol,定容至1l,稀释至0.01mol/l,即得)为溶剂,先加入各氨基酸和l-肌肽,混合均匀,使各组分浓度达到配方要求值,再经0.22μm滤膜过滤除菌;然后加入透明质酸钠,持续搅拌至完全溶解,4℃静置12小时,0.22μm滤膜过滤除菌,分别得到组合物1和组合物2。
[0130]
组合物3的制备方法:按照组合物1的配方和制备方法,在所得组合物中加入少量经0.22μm滤膜过滤除菌的磷酸二氢钾水溶液,使组合物中钾离子含量为0.008mg/ml,得到组合物3。
[0131]
实施例5:组合物样品(浸提液)对hff-1细胞增殖的影响
[0132]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,组合物1的浸
提液,组合物2的浸提液。
[0133]
实验结果:
[0134]
组合物1、组合物2对hff-1细胞的增殖几乎无抑制作用,对细胞形态也无影响作用(参见图3、图4),证明本发明提供的组合物1、组合物2有良好的细胞相容性,适于注射。
[0135]
实施例6:组合物样品(浸提液)对hff-1细胞迁移的影响
[0136]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,组合物1的浸提液,组合物2的浸提液。
[0137]
实验结果:与对照组相比,组合物1、组合物2均可显著促进hff-1向划痕区域迁移(参见图5),说明本发明提供的组合物1、组合物2可显著提高皮肤成纤维细胞的迁移能力,促进皮肤组织的再生修复。
[0138]
实施例7:组合物样品(浸提液)对hff-1细胞胶原蛋白分泌的影响
[0139]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,组合物1的浸提液,组合物2的浸提液。
[0140]
实验结果:组合物1、组合物2组的胶原蛋白水平均显著高于对照组(参见图6),说明组合物1、组合物2可显著促进皮肤成纤维细胞的胶原蛋白分泌。
[0141]
实施例8:组合物样品(浸提液)对hff-1细胞弹性蛋白分泌的影响
[0142]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,对照组1的浸提液,组合物1的浸提液,组合物2的浸提液,组合物3的浸提液。
[0143]
实验结果:组合物1、组合物2、组合物3组的弹性蛋白水平均显著高于对照组和对照组1,说明组合物1、组合物2和组合物3可显著促进皮肤成纤维细胞的弹性蛋白分泌,其中组合物3相对组合物1或组合物2减弱(参见图7)。
[0144]
实施例9:组合物样品(浸提液)对hff-1细胞拮抗氧化损伤功能的影响
[0145]
按照前述的实验方法和样品配制方法进行,其中实验分组:对照组,模型组(含800μmmol/l h2o2的完全培养基),含800μmmol/l h2o2的组合物1的浸提液,含800μmmol/l h2o2的组合物2的浸提液。
[0146]
实验结果:模型组的sod活力被显著抑制、mda水平显著升高,表明在h2o2胁迫下hff-1细胞的氧化损伤风险显著升高;组合物1、组合物2均可显著降低sod抑制率和mda水平,抗氧化损伤的能力显著增强(参见图8、图9),说明组合物1、组合物2可显著提高细胞拮抗氧化损伤的能力,降低氧化应激损伤风险。
[0147]
根据实施例的结果可知,采用本发明所述的分子量的透明质酸钠,配以本发明所述含量范围的氨基酸等组分,能够得到具有较好的抗衰老作用和稳定的透明质酸钠组合物溶液。
[0148]
本发明的方法已经通过较佳实施例进行了描述,相关人员明显能在本发明内容和范围内对本文所述的方案或应用进行改动或适当变更与组合,来实现和应用本发明技术。本领域技术人员可以借鉴本文内容,适当改进条件/参数来实现和/或应用本发明技术。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。