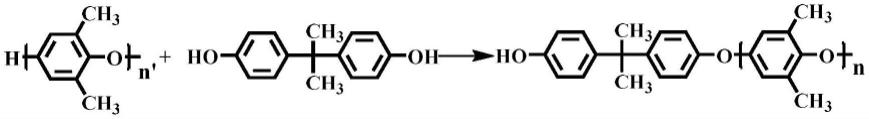
1.发明属于免疫化学技术领域,具体涉及一种新型三聚氰胺半抗原、完全抗原、抗体及制备方法。
背景技术:
2.三聚氰胺,俗称“密胺”、“蛋白精”,其是一种三嗪类含氮杂环有机化合物,常被用作化工原料。它是白色单斜晶体,几乎无味,微溶于水,可溶于甲醛、乙酸、热乙二醇、甘油、吡啶等,不溶于丙酮、醚类。三聚氰胺是一种以尿素为原料的重要的氮杂环有机化工中间体,由于其所具有的环保性能和用途广泛而越来越受到人们的青睐,广泛用于木材加工、塑料、涂料、减水剂、造纸、粘合剂、纺织、皮革、电器、医药、阻燃剂等行业。三聚氰胺对身体有害,不可用于食品加工或食品添加物。
3.目前,三聚氰胺检测常用的方法有气相色谱、高效液相色谱以及气质联用等理化分析方法,虽然这些方法特异性强、灵敏度高,但是样品前处理操作步骤繁琐,成本较高,也不适用于大批量样品的筛选检测,免疫化学分析鉴于在抗原抗体的定性定量方面独特的优势和操作简便快速、成本低、灵敏度较高、分析样本量大的优点弥补了理化分析的不足,在奶制品中三聚氰胺的残留检测起着越来越重要的作用。
4.因此,本发明提出了一种新型三聚氰胺半抗原、完全抗原、抗体及制备方法,由此半抗原制备的单克隆抗体,可以特异性识别三聚氰胺和环丙氨嗪,该半抗原最大限度保留了三聚氰胺的化学结构,提高了半抗原的特异性,又为抗原制备加入了反应位点。经过柱净化浓缩,以该半抗原为基础,与载体蛋白偶联,用于免疫小鼠制备抗体,并以抗原抗体为基础开发了胶体金产品,为三聚氰胺和环丙氨嗪在食品中的残留检测提供了高效和可靠的检测方法。
技术实现要素:
5.发明的目的在于提供一种新型三聚氰胺半抗原、完全抗原、抗体及制备方法,以解决上述背景技术中提出现有的技术问题。
6.本发明设计合成了小分子目标分析物三聚氰胺半抗原,并与载体蛋白质偶联,制备有效新型三聚氰胺完全抗原,免疫动物制备对小分子分析物特异性抗体,利用抗原抗体的特异性免疫学反应和易被检测识别的标记物的放大作用,从而定性定量的检测样本中超微量小分子目标物,可用于样本测定。该技术研究的关键是半抗原的分子设计、合成和全抗原及抗体的制备。
7.一种新型三聚氰胺半抗原的化学式为式ⅰ:
[0008][0009]
式ⅰ所示的化合物的制备方法,包括如下步骤:
[0010]
(1)取2-氯-4,6-二氨基均三嗪0.73g、水合肼(80%)10.0ml投入反应瓶,搅拌加热,回流反应4~6h;
[0011]
(2)反应完毕,降温至室温,再冷冻降温至3~5℃,抽滤,少量冷冻甲醇淋洗,在45~50℃干燥至恒重,得第一步产物;
[0012]
(3)取第一步产物0.42g,乙醛酸0.24g,加入20ml甲醇,常温搅拌反应30min,再分批加入氰基硼氢化钠0.28g,常温搅拌反应过夜;
[0013]
(4)反应完毕,减压蒸除甲醇,通过盐酸调ph=5~6,搅拌析晶1.0h。过滤,固体用少量甲醇重结晶,得0.20g白色固体,即为所述三聚氰胺半抗原。
[0014]
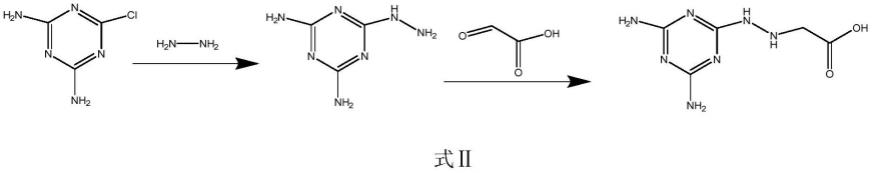
一种新型三聚氰胺半抗原的合成路径为式ⅱ所示:
[0015][0016]
一种新型三聚氰胺完全抗原化学式为式ⅲ所示:
[0017][0018]
式ⅲ所示的新型三聚氰胺完全抗原分为免疫原和包被原,
[0019]
免疫原的获取包括以下步骤:
[0020]
(1)取半抗原活化酯4mg,加入到溶有10mg血蓝蛋白的pbs(0.01mol/l,ph=7.4)溶液中,与4度条件下反应过夜;
[0021]
(2)将反应液装入透析袋,用0.01mol/l pbs溶液充分透析,得到所述免疫原;
[0022]
所述包被原的获取包括以下步骤:
[0023]
(1)取半抗原活化酯25mg,加入到溶有100mgbsa的pbs(0.01mol/l,ph=7.4)溶液中,与4度条件下反应过夜;
[0024]
(2)然后将反应液装入透析袋,用0.01mol/l pbs溶液充分透析,得到所述包被原。
[0025]
4.根据权利要求3所述的一种新型三聚氰胺完全抗原,其特征在于,所述半抗原活化酯的合成包括以下步骤:
[0026]
(1)在5ml的玻璃瓶中,取半抗原20mg,用1ml的n,n-二甲基甲酰胺溶解配制成a液;
[0027]
(2)分别称取1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐20mg,n-羟基丁二酰亚胺12mg,两者混合一起用0.5ml的n,n-二甲基甲酰胺溶解配制成b液;
[0028]
(3)常温条件下b液逐滴加入a液中,然后室温搅拌过夜,终止反应后即得半抗原活化酯。
[0029]
三聚氰胺完全抗原为所述半抗原中羧基与载体蛋白中氨基发生化学反应形成酰胺键连接的偶联物。
[0030]
优选的,载体蛋白选自牛血清白蛋白、人血清白蛋白、血蓝蛋白和卵清白蛋白中的至少一种。
[0031]
三聚氰胺抗体的制备方法包括以下步骤:
[0032]
(1)选取8周龄左右雌性balb/c小鼠进行免疫,分别编号为1号、2号、3号、4号,免疫采取颈背部皮下多点注射法,第4次免疫和第5次免疫后测定抗血清的效价和抑制率,在细胞融合前3天加强免疫;
[0033]
(2)从第2次加强免疫开始,每次免疫7天后对动物试采血进行血清效价测定和特异性测定。
[0034]
(3)选取加强免疫后效价高且特异性强的小鼠脾细胞和骨髓瘤细胞进行融合,7天后对培养的细胞进行筛选,筛选出能分泌特异性抗体的杂交瘤细胞,找到达到要求的细胞孔,对其进行亚克隆,最终获得单一的细胞株,扩大培养;
[0035]
(4)将扩大培养的杂交瘤细胞注入已提前注射石蜡的小鼠体内,7天左右,抽取小鼠腹腔积液,对其进行蛋白提纯既可获得所述三聚氰胺单克隆抗体。
[0036]
免疫程序包括初次免疫和加强免疫,具体如下:
[0037]
初次免疫:为提高抗原的免疫性,采用由弗氏完全佐剂乳化的免疫原,相同体积的免疫原和弗氏完全佐剂混合进行乳化,剂量为0.1mg。
[0038]
加强免疫:初次免疫后第14天和35天进行加强免疫,剂量为0.1mg,乳化方法相同,以后每隔21天加强免疫一次,共免疫6次。
[0039]
血清效价检测方法包含以下步骤:
[0040]
(1)将制备好的三聚氰胺包被原溶于ph 9.6na2co3-nahco3的缓冲液中,将三聚氰胺包被原稀释为1.0μg/ml作为包被液,96孔微孔板每孔各加入100μl,4℃放置过夜或者37℃恒温温育2~3小时,用pbst即磷酸盐缓冲液0.05%(v/v),tween20洗液洗涤1次;
[0041]
(2)每孔加入200μl 3%脱脂奶粉的pbs封闭液,封闭2小时,用洗液洗涤1次;
[0042]
(3)加抗血清及标准品:将抗血清梯度稀释;将甲萘威标准品溶于适量dmf配制成1.0mg/ml的标准品溶液,4℃保存备用。效价列:每孔加50ul的空白稀释液、50ul梯度稀释的抗血清和50ul的羊抗鼠酶标二抗;抑制列:每孔加50ul的标准品溶液、50ul梯度稀释的抗血清和50ul的羊抗鼠酶标二抗,37℃温育30分钟;
[0043]
(4)用洗液洗微孔板3次,将孔内液体甩掉,微孔板脱水仪甩干,加入50ul底物a和50ul底物b,室温下反应15分钟;
[0044]
(5)读数测定:450nm和630nm双波长下测吸光值;选择吸光度值在1.5~2.0区间内的抗血清稀释倍数为抗血清效价,抗血清的效果由其抑制率得出。
[0045]
与现有技术相比,发明的有益效果是:
[0046]
克服现有技术的不足,针对三聚氰胺,从头合成了一种保留三聚氰胺完全结构同时又带有羧基的半抗原,进一步偶联不同载体蛋白分别作为人工免疫原和包被原,进而制备三聚氰胺检测抗体,其具有灵敏度高,特异性好,对三聚氰胺和环丙氨嗪能同时识别等显著优势,可用于快速检测动物食品中残留的三聚氰胺和环丙氨嗪。
附图说明
[0047]
图1为三聚氰胺半抗原的化学式分子图;
[0048]
图2为三聚氰胺半抗原的化学式合成路径图;
[0049]
图3为三聚氰胺完全抗原的化学式分子图;
具体实施方式
[0050]
下面将结合图1-图3和表1说明本发明实施例,对发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是发明一部分实施例,而不是全部的实施例,基于发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于发明保护的范围。
[0051]
实施例1:三聚氰胺半抗原合成
[0052]
三聚氰胺半抗原的化学式为式ⅰ:
[0053][0054]
三聚氰胺半抗原合成以多菌灵为起始原料,合成路径如式ⅱ所示,
[0055][0056]
三聚氰胺半抗原制备方法,包括如下步骤:
[0057]
(1)取2-氯-4,6-二氨基均三嗪0.73g、水合肼(80%)10.0ml投入反应瓶,搅拌加热,回流反应4~6h;
[0058]
(2)反应完毕,降温至室温,再冷冻降温至3~5℃,抽滤,少量冷冻甲醇淋洗,在45~50℃干燥至恒重,得第一步产物;
[0059]
(3)取第一步产物0.42g,乙醛酸0.24g,加入20ml甲醇,常温搅拌反应30min,再分
批加入氰基硼氢化钠0.28g,常温搅拌反应过夜;
[0060]
(4)反应完毕,减压蒸除甲醇,通过盐酸调ph=5~6,搅拌析晶1.0h。过滤,固体用少量甲醇重结晶,得0.20g白色固体,即为所述三聚氰胺半抗原。
[0061]
实施例2:三聚氰胺完全抗原制备
[0062]
所述三聚氰胺完全抗原化学式为式ⅲ所示:
[0063][0064]
式ⅲ所示的新型三聚氰胺完全抗原分为免疫原和包被原,免疫原的获取包括以下步骤:
[0065]
(1)取半抗原活化酯4mg,加入到溶有10mg血蓝蛋白的pbs(0.01mol/l,ph=7.4)溶液中,与4度条件下反应过夜;
[0066]
(2)将反应液装入透析袋,用0.01mol/l pbs溶液充分透析,得到免疫原;
[0067]
包被原的获取包括以下步骤:
[0068]
(3)取半抗原活化酯25mg,加入到溶有100mgbsa的pbs(0.01mol/l,ph=7.4)溶液中,与4度条件下反应过夜;
[0069]
(4)然后将反应液装入透析袋,用0.01mol/l pbs溶液充分透析,得到包被原。
[0070]
实施例3:半抗原活化酯的合成
[0071]
(1)在5ml的玻璃瓶中,取半抗原20mg,用1ml的n,n-二甲基甲酰胺溶解配制成a液;
[0072]
(2)分别称取1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐20mg,n-羟基丁二酰亚胺12mg,两者混合一起用0.5ml的n,n-二甲基甲酰胺溶解配制成b液;
[0073]
(3)常温条件下b液逐滴加入a液中,然后室温搅拌过夜,终止反应后即得半抗原活化酯。
[0074]
实施例4:单克隆抗体的制备
[0075]
(1)选取8周龄左右雌性balb/c小鼠进行免疫,分别编号为1号、2号、3号、4号,免疫采取颈背部皮下多点注射法,第4次免疫和第5次免疫后测定抗血清的效价和抑制率,在细胞融合前3天加强免疫;
[0076]
(2)从第2次加强免疫开始,每次免疫7天后对动物试采血进行血清效价测定和特异性测定。
[0077]
(3)选取加强免疫后效价高且特异性强的小鼠脾细胞和骨髓瘤细胞进行融合,7天后对培养的细胞进行筛选,筛选出能分泌特异性抗体的杂交瘤细胞,找到达到要求的细胞孔,对其进行亚克隆,最终获得单一的细胞株,扩大培养;
[0078]
(4)将扩大培养的杂交瘤细胞注入已提前注射石蜡的小鼠体内,7天左右,抽取小鼠腹腔积液,对其进行蛋白提纯既可获得所述三聚氰胺单克隆抗体。
[0079]
免疫程序包括初次免疫和加强免疫,具体如下:
[0080]
初次免疫:为提高抗原的免疫性,采用由弗氏完全佐剂乳化的免疫原,相同体积的免疫原和弗氏完全佐剂混合进行乳化,剂量为0.1mg。
[0081]
加强免疫:初次免疫后第14天和35天进行加强免疫,剂量为0.1mg,乳化方法相同,以后每隔21天加强免疫一次,共免疫6次。
[0082]
实施例5:间接酶联免疫法测定抗血清的效价和特异性分析
[0083]
(1)从第3次加强免疫开始,每次免疫后的第8天,小鼠尾部采血30ul,离心取抗血清,-20℃保存备用;
[0084]
(2)包被:将5mg/ml的包被抗原用包被缓冲液稀释5000倍,并做空白对照组,100ul/孔加入到酶标板中,置于4℃冰箱孵育过夜,然后用pbst即磷酸盐缓冲液0.05%(v/v),tween20洗液洗涤1次;
[0085]
(3)封闭:倾去孔内液体,洗板1次,每孔加洗涤液200μl,甩干每孔加入200μl封闭液,37℃封闭2h,甩干,置于4℃冰箱中备用;
[0086]
(4)对照孔每孔加入50ul标品稀释液、稀释好的酶标二抗和稀释好的血清;样品孔每孔加入50ul稀释好的标品、稀释好的酶标二抗和稀释好的血清;震荡混匀,37℃反应30min后,洗板机洗板3次,每孔加入洗涤液200μl,甩干;
[0087]
(5)显色:每孔加入显色液a和b各50μl,置于37℃烘箱中显色15min后,每孔加入50μl终止液(1mol/l的h2so4);
[0088]
(6)测定:用酶联免疫检测仪测定各孔a450nm的吸光值。选择吸光度值在1.5~2.0区间内的抗血清稀释倍数为抗血清效价,抗血清的效果由其抑制率得出,相同的药物浓度下,抑制率越高,则抗体对此药物的灵敏度越高。
[0089]
实施例6:细胞融合和阳性杂交瘤的筛选
[0090]
(1)复苏骨髓瘤细胞:将骨髓瘤细胞从液氮中取出,迅速放入37℃水浴中解冻,融化后1000r/min离心5min,在超净工作台中倒掉上清液,并在细胞沉淀中加入完全培养液约1ml,吹散细胞,用移液枪取出和完全培养基混均后放入25cm2培养瓶中,并扩大至4~6瓶,其间需多次换液,当每个培养瓶的细胞铺满底部时,可用于细胞融合;
[0091]
(2)饲养细胞制备:在细胞融合前1天对balb/c小鼠脱颈椎处死,经75%酒精浸泡5min后移入超净工作台进行解剖。剪开腹部,剥离腹部皮肤,剪开腹膜,取出脾脏,移入9cm培养皿,加入dmem基础培养基,用注射器反复抽吸冲洗,冲洗液转入50ml离心管,1200r/min离心5min,弃上清液,底部细胞沉淀用完全培养基重悬后加入96孔细胞培养板,每孔100ul;
[0092]
(3)脾细胞制备:将已多次免疫并检血合格的balb/c小鼠眼眶放血,收集血清,然后在75%酒精浸泡5min消毒,移入超净工作台进行解剖,无菌取出脾脏,用dmem基础培养基冲洗后置于培养皿中待用,用一次性注射器吸取培养基,左手用镊子夹住取下的脾脏,右手将注射器插入脾脏,缓慢注入培养基,以将脾脏里的细胞洗出。反复进行直至脾脏由深红色转为无色透明状,弃脾脏。将混合的培养基收集到50ml离心管中,封口后离心,转速1200r/min共6min,离心后弃去上清液,待用;
[0093]
(4)细胞融合:将离心去上清液的骨髓瘤细胞和免疫脾细胞按1:6左右混合于离心管内,加入25ml的基础培养基,封口后离心,转速1500r/min共8min,离心后弃上清待用,将经离心混合的骨髓瘤细胞和免疫脾细胞弃上清,离心管口朝下用枪吸掉的多余的培养基,
将沉淀的细胞用手指弹松,把离心管置于37℃温水中,用枪头吸取预热至37℃的peg1ml,在1min内将peg缓慢加入到沉淀的细胞中,每加一滴peg就用枪头轻柔搅拌一下以混均,静置1min,预热好完全培养基,在2min内加入10ml,伴随轻轻搅拌,沿壁加入,使peg分开,离心管封口1000r/min离心10min,倒掉上清,加入hat完全培养基,用弯头吸管轻轻吸液放液,轻柔搅拌,均匀加入到前一天准备的10块含有饲养细胞的96孔培养板里,保持每孔中添加饲养细胞的hat培养基和含有融合细胞的hat培养基体积相同;
[0094]
(5)阳性杂交瘤的筛选:融合后3~4天内使用hat培养基换液一次,7天后抽取多孔培养板中里的上清,用间接elisa检测培养液中的特异性抗体,选择效价高和对药物抑制强的阳性杂交瘤细胞,筛选出融合效果最好的阳性孔,做好标记。无菌条件下,用显微镜挑取阳性孔中团簇生长的细胞,移至预先以饲养细胞铺板的96孔培养板中,每个原始孔克隆成96孔,待细胞贴壁长满1/4孔底后,取上清液,icelisa检测,同样以效价和抑制率做为衡量指标,取呈阳性强者利用有限稀释法进行亚克隆,如此反复3~4轮,注意每轮挑出的阳性孔细胞需扩大培养,后冻存备用,直至每板每个孔都为阳性且经检测效价和抑制相近,至此杂交瘤细胞系建立成功,得到能稳定分泌均一抗体的杂交瘤细胞系。挑取单细胞克隆,检测为全阳性者转移至24孔细胞培养板或细胞培养皿中扩大培养,及时冻存。
[0095]
实施例7:单克隆抗体的大量制备
[0096]
在获得分泌特异性单克隆抗体的杂交瘤细胞克隆后,通常以体外培养法和动物体内诱生单克隆抗体法大量制备单克隆抗体,包含以下步骤:
[0097]
(1)提前在十多只8周龄以上的balb/c小鼠的腹腔内注射液体石碏,剂量为0.5ml/只,1~2两周后在小鼠的腹腔注射杂交瘤细胞;
[0098]
(2)接种细胞后每天观察小鼠状态,特别是从第7天开始,小鼠的腹腔会胀大,在小鼠死亡前用一次性注射器无菌采取腹水;
[0099]
(3)将采集的腹水12000r/min离心10min,去除上层脂肪和下层纤维蛋白,收集中间层,用icelisa法测定其效价和抑制率,纯化后在-20℃保存备用。
[0100]
实施例8:单克隆抗体的大量制备
[0101]
在获得分泌特异性单克隆抗体的杂交瘤细胞克隆后,通常以体外培养法和动物体内诱生单克隆抗体法大量制备单克隆抗体,包含以下步骤:
[0102]
(1)提前在十多只8周龄以上的balb/c小鼠的腹腔内注射液体石碏,剂量为0.5ml/只,1~2两周后在小鼠的腹腔注射杂交瘤细胞;
[0103]
(2)接种细胞后每天观察小鼠状态,特别是从第7天开始,小鼠的腹腔会胀大,在小鼠死亡前用一次性注射器无菌采取腹水;
[0104]
(3)将采集的腹水12000r/min离心10min,去除上层脂肪和下层纤维蛋白,收集中间层,用icelisa法测定其效价和抑制率,纯化后在-20℃保存备用。
[0105]
实施例9:间接竞争酶联免疫测定三聚氰胺方法的建立
[0106]
间接竞争酶联免疫(icelisa)反应具体包括以下步骤:
[0107]
(1)包被:将5mg/ml的包被抗原用包被缓冲液稀释5000倍,并做空白对照组,100ul/孔加入到酶标板中,置于4℃冰箱孵育过夜。然后用pbst即磷酸盐缓冲液0.05%(v/v),tween20洗液洗涤1次;
[0108]
(2)封闭:倾去孔内液体,洗板1次,每孔加洗涤液200μl,甩干每孔加入200μl封闭
液,37℃封闭2h,甩干,置于4℃冰箱中备用;
[0109]
(3)加样:对照孔每孔加入50ul标品稀释液、稀释好的酶标二抗和稀释好的血清;样品孔每孔加入50ul稀释好的标品、稀释好的酶标二抗和稀释好的血清;震荡混匀,37℃反应30min后,洗板机洗板3次,每孔加入洗涤液200μl,甩干;
[0110]
(4)显色:每孔加入显色液a和b各50μl,置于37℃烘箱中显色15min后,每孔加入50μl终止液(1mol/l的h2so4);
[0111]
(5)测定:用酶联免疫检测仪测定各孔a450nm的吸光值。
[0112]
(6)计算:用graphpad prism7.0拟合模块计算抑制曲线的ic50值;
[0113]
(7)配制24.3ng/ml、8.1ng/ml、2.7ng/ml、0.9ng/ml、0.3ng/ml、0.1ng/ml的三聚氰胺标准品溶液,建立间接酶联免疫检测方法的标准曲线,条件优化后该方法针对三聚氰胺ic50=0.98ng/ml,线性检测范围为0.1~24.3ng/ml。
[0114]
实施例10:抗体交叉反应率的测定
[0115]
按实施例9中所得最佳包被抗原浓度和最佳抗血清稀释倍数,以三聚氰胺和环丙氨嗪等为竞争标准品,进行间接竞争elisa实验,检测三聚氰胺单克隆抗体的特异性,其半数抑制浓度(ic50)和交叉反应率(cr)数值在表1中列出。
[0116]
表1
[0117][0118]
实验结果表明,三聚氰胺单克隆抗体可同时识别三聚氰胺和环丙氨嗪,对其它药物无交叉反应,说明本发明的三聚氰胺单克隆抗体特异性好,可用于三聚氰胺和环丙氨嗪在食品中残留的检测。
[0119]
尽管已经示出和描述了发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,发明的范围由所附权利要求及其等同物限。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。