1.本发明涉及皮克林(pickering)乳液制备技术领域,特指一种以莲藕淀粉和黄原胶为原料,采用聚能式超声波技术制备莲藕淀粉-黄原胶pickering乳液,并用其负载鱼油制备功能食品的方法。
背景技术:
2.皮克林(pickering)乳液通常是指由固体颗粒充当乳化剂稳定的乳液,或者由胶体颗粒稳定的乳液。而传统的表面活性剂是在油水界面处亲水性部分伸入水相,亲油性部分伸入油相,从而产生空间排斥来稳定乳液。在pickering乳液中,是通过固体颗粒在油-水界面的不可逆吸附,形成立体屏障来稳定乳液。与传统乳液相比,pickering乳液的乳化剂用量少、成本低、对人体的毒副作用小,相关环境问题少;乳液稳定性好,不易受体系的ph、盐离子、温度等环境因素的影响。在过去的二十几年中,合成高分子和无机颗粒乳化剂因其形状、尺寸、表面性质的可调控性而成为人们的研究热点。但是合成高分子和无机颗粒的生物相容性、生物可降解性和可持续性较差而在食品、生物医药、化妆品等领域的应用受到了限制。近五年来,人们逐渐倾向于采用天然来源的生物材料来制备可以稳定pickering乳液的颗粒乳化剂。到目前为止,已经有不少关于以纤维素、淀粉、蛋白质、果胶、等作为天然来源的固体颗粒制备出pickering乳液的研究报告。采用天然来源的生物材料来制备新型的固体颗粒,用于稳定pickering乳液及制备相关功能性材料对防止环境污染、节约资源具有促进作用。
3.在天然来源的原材料中,淀粉因来源广泛、价格低廉等优点而受到了广泛的关注。我国是农业大国,淀粉种类丰富,主要包括谷物类淀粉、豆类淀粉、薯类淀粉等其它多种来源淀粉。目前,高纯度淀粉及其衍生物已经实现工业化生产并被广泛应用于食品、生物医药、化工、造纸、农业等不同领域。因此,以淀粉为基质的颗粒乳化剂具有潜在的应用前景。
4.莲藕(nelumbo nucifera gaertn),又称荷藕,简称藕,为睡莲科多年生植物,在我国主要分布在长江、黄河及珠江三大流域,尤以江苏、浙江、湖南、湖北等省栽培的莲藕为优。莲藕中含有丰富的淀粉、蛋白质、维生素、铁、钙、生物碱等多种对人体健康有益的物质,具有较高的食用和药用价值,是一种用途十分广泛的水生经济作物。据《本草纲目》记载:藕,生者甘寒,能凉血止血,除热清胃,故主消散淤血,止热渴、霍乱、烦闷、解酒等功效。熟者甘温,能健脾开胃,益血补心,故主补五脏。
5.莲藕淀粉(lotus root starch)是莲藕经去皮、切块、护色、匀浆、过滤、烘干、粉碎等加工工艺而制成的初级粉状产品,其保留了莲藕肉质的颜色及香味,保存了天然莲藕去除皮质之外的其他成分,如淀粉、黄酮类、维生素、矿物质、天门冬素等。它的特点是含有新鲜的莲藕的风味和营养价值。莲藕的淀粉中直链淀粉含量占总淀粉的25%~30%左右,支链淀粉含量占总淀粉的65%左右,支链淀粉在淀粉颗粒中起支架的作用,呈放射状,并从淀粉颗粒的中部有规律地往外延伸,形成微晶纤维束,在支链淀粉之间,直链淀粉以双螺旋结构的晶体形式有规律的分布在其中。
6.黄原胶是由野油菜黄单胞杆菌(xanthomnas campestris)发酵产生的一种胞外多糖。由葡萄糖主链和三糖侧链组成,为阴离子亲水性胶体。溶于水时,其侧链能够反向缠绕于纤维主链形成黄原胶的一级结构;分子间通过氢键作用形成双螺旋结构,为黄原胶的二级结构;进一步,双螺旋结构之间相互缠绕而形成网状的立体三级构象。这种独特的分子构象决定了它具有良好的乳化性、增稠性、触变性、假塑性等性能,且能够与其他多糖(如淀粉)相互作用,同时又是安全、无毒、绿色的物质,在国内外成为食品工业上最优越的亲水性胶体之一。
7.目前,淀粉颗粒作为皮克林乳液稳定剂的应用,主要源于对淀粉颗粒的修饰和改性,从而降低淀粉颗粒的粒径、提高其疏水性。常见淀粉纳米颗粒制备方法有机械研磨法,反溶剂沉淀法,辛烯基琥珀酸酐(osa)改性法,酸水解法,酶解回生法。这些方法或多或少都存在能耗高、操作繁琐、使用化学试剂等问题。亟待开发一种操作简便、产物稳定、无化学试剂的绿色制备方法。而对于乳状液的制备技术,主要采用高压均质、高压微射流、先高速剪切后高压均质等高能乳化技术,使得蛋白质分子紧密排列在油-水界面,促使两相界面张力降低,制备得到乳状液。但是上述乳化技术设备造价昂贵、维护成本高、样品处理量小,复杂的操作,以及对操作人员的高要求限制了其在食品领域中的应用。
8.在乳液的加工和贮藏中,油脂氧化所导致的腐败变质会影响食品的外观和口感。然而,目前关于pickering乳液应用的研究多集中于对活性物质的包埋和递送,对油脂抗氧化性和负载不饱和脂肪酸的研究相对较少。乳液中油脂的氧化主要发生在油水界面,而纳米淀粉基pickering乳液的油水界面具有微淀粉颗粒排列组成的高强度物理屏障,阻隔氧气侵入,且黄原胶还具有螯合金属离子和清除自由基的功效,能极大的增强油脂的抗氧化性。
9.为了解决上述问题,本发明采用压热回生法制备淀粉纳米颗粒,采用聚能式超声波技术制备莲藕淀粉-黄原胶pickering乳液,操作简便、无化学试剂的使用、绿色安全,以期获得粒径更小、稳定性更好的莲藕淀粉-黄原胶pickering乳液。并用其负载鲱鱼油,探究该pickering乳液的氧化稳定性和对二十二碳六烯酸(dha)、二十碳五烯酸(epa)的保护作用。
技术实现要素:
10.为解决上述问题,本发明采用压热回生法制备莲藕淀粉纳米颗粒,并使用聚能式超声波技术对莲藕淀粉-黄原胶pickering乳液进行处理,探究纳米颗粒的理化特性、结构特性的变化,以及对pickering乳液稳定性的影响。并替换油相为鱼油,制备一种负载鱼油的抗氧化乳液。
11.通过压热回升法制备莲藕淀粉纳米颗粒,高温高压能够破坏淀粉的颗粒结构,促进直链淀粉溶出,更有利于重结晶产生淀粉纳米颗粒。然后与黄原胶充分水合,制备复合纳米颗粒。再采用双频聚能式超声波设备辅助乳化制备pickering乳液。双频聚能式超声波能够克服单一频率的超声波可能产生的驻波,充分发挥超声波的乳化效果。此外,乳液中油脂的氧化一直是不可避免的问题,选用易被氧化的鱼油制备乳液,构建一种负载鱼油的抗氧化乳液。
12.本发明中莲藕淀粉-黄原胶复合纳米颗粒,是由以下质量份的原料制备而成:
13.莲藕淀粉1-20份,
14.黄原胶1-20份,
15.水600-1000份。
16.优选的莲藕淀粉-黄原胶复合纳米颗粒,由以下重量份的原料制备而成:
17.莲藕淀粉8份,
18.黄原胶2.4份
19.水800份。
20.本发明中莲藕淀粉-黄原胶pickering乳液,由以下重量份的原料制备而成:
21.莲藕淀粉1-20份,
22.黄原胶1-20份,
23.大豆油100-300份,
24.水600-1000份。
25.优选的莲藕淀粉-黄原胶pickering乳液,由以下重量份的原料制备而成:
26.莲藕淀粉8份,
27.黄原胶2.4份
28.大豆油200份
29.水800份。
30.本发明中负载鱼油的莲藕淀粉-黄原胶pickering乳液,由以下重量份的原料制备而成:
31.莲藕淀粉1-20份,
32.黄原胶1-20份,
33.鲱鱼油150-200份,
34.橘精油10-50份,
35.水600-1000份。
36.优选的负载鱼油的莲藕淀粉-黄原胶pickering乳液,由以下重量份的原料制备而成:
37.莲藕淀粉8份,
38.黄原胶2.4份,
39.鲱鱼油160份,
40.橘精油40份,
41.水800份。
42.莲藕淀粉-黄原胶复合纳米颗粒的制备方法,按照下述步骤进行:
43.(1)莲藕淀粉分散在蒸馏水中,分散液的浓度为1~5wt%;
44.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
45.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理;
46.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶;
47.(5)将黄原胶溶于蒸馏水,浓度为0.2wt%~1wt%,置于磁力搅拌器上搅拌过夜,使其完全溶解;
48.(6)将步骤(4)中制备的淀粉纳米颗粒分散液和步骤(5)中的黄原胶溶液混合,获得复合纳米颗粒。
49.其中步骤(1)中所述优选的分散液浓度为2wt%;
50.其中步骤(3)中所述的压热处理条件为121℃,20分钟;
51.其中步骤(4)中所述的重结晶的时间为8~12h,优选的重结晶时间为9h;
52.其中步骤(5)中所述优选的黄原胶溶液浓度为0.6wt%;
53.其中步骤(6)中所述复合纳米颗粒中莲藕淀粉和黄原胶的质量比为10:1~10:5,优选的比例为10:3。
54.莲藕淀粉-黄原胶pickering乳液的制备方法,按照下述步骤进行:
55.(1)莲藕淀粉分散在蒸馏水中,浓度为2wt%;
56.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
57.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20分钟;
58.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶9h;
59.(5)将黄原胶溶于蒸馏水,浓度为0.6wt%,置于磁力搅拌器上搅拌过夜,使其完全溶解;
60.(6)将步骤(4)中制备的淀粉纳米颗粒分散液和步骤(5)中黄原胶溶液混合,其中莲藕淀粉和黄原胶的质量比为10:3,获得复合纳米颗粒溶液;
61.(7)制备粗乳液:按大豆油与莲藕淀粉的质量比为25:1将大豆油加入步骤(6)中复合纳米颗粒溶液,用高速剪切分散机分散,转速为12000rpm,分散2min形成粗乳液;
62.(8)超声波乳化:将步骤(7)中粗乳液置于双频聚能式超声波装置中进行乳化处理,超声波处理条件为:超声波频率为20khz、40khz或者20/40khz,超声波功率为400w/l-2000w/l,超声波处理时间为2min-10min;得到最终的成品莲藕淀粉-黄原胶pickering乳液。
63.其中步骤(8)中优选超声波处理条件为超声波频率为20/40khz,超声波功率为1200w/l,超声波处理时间为4min。
64.负载鱼油的莲藕淀粉-黄原胶pickering乳液的制备方法,按照下述步骤进行:
65.(1)莲藕淀粉分散在蒸馏水中,浓度为2wt%;
66.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
67.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理条件为121℃,20分钟;
68.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,回生时间为9h;
69.(5)将黄原胶溶于蒸馏水,浓度为0.6wt%,置于磁力搅拌器上搅拌过夜,使其完全溶解;
70.(6)将步骤(4)中制备的淀粉纳米颗粒分散液和步骤(5)中黄原胶溶液混合,莲藕淀粉和黄原胶的质量比为10:3,获得复合纳米颗粒溶液;
71.(7)制备粗乳液:将鲱鱼油和橘精油加入步骤(6)中复合纳米颗粒溶液,用高速剪
切分散机分散,转速为12000rpm,分散2min形成粗乳液;其中鲱鱼油与莲藕淀粉的质量比为22.5:1-12.5:1,橘精油与莲藕淀粉的质量比为2.5:1-12.5:1;
72.(8)超声波乳化:将步骤(7)中粗乳液置于双频聚能式超声波装置中进行超声波处理,超声波处理条件为:超声波频率为20khz、40khz或者20/40khz,超声波功率为400w/l-2000w/l,超声波处理时间为2min-10min;得到最终的成品莲藕淀粉-黄原胶pickering乳液。
73.其中步骤(7)中优选鲱鱼油与莲藕淀粉的比例为20:1;
74.其中步骤(7)中优选橘精油与莲藕淀粉的比例为5:1;
75.其中步骤(9)中优选超声波处理条件为超声波频率为20/40khz,超声波功率为1200w/l,超声波处理时间为4min。
76.莲藕淀粉-黄原胶pickering乳液的应用,可以用于制备食品、功能性食品、特医食品、保健品、药品及化妆品。
77.负载鱼油的莲藕淀粉-黄原胶pickering乳液的应用,可以用于制备食品、功能性食品、特医食品、保健品、药品及化妆品。
78.本发明的有益效果在于:
79.(1)本发明通过压热回生法制备莲藕淀粉纳米颗粒,这是一种操作简便、产物稳定、不使用化学试剂的绿色制备方法。
80.(2)本发明将黄原胶添加至淀粉纳米颗粒中作为一种pickering乳液稳定剂,能够显著提高pickering乳液稳定性,且二者都是天然来源的多糖,安全可靠,可用于食用。
81.(3)超声波乳化法相较于昂贵的高压均质法和微射流法,工艺操作简单、维护成本低,适宜工业化生产,且原料、设备价格便宜。
82.(4)本发明中的莲藕淀粉纳米颗粒粒径约为243nm,莲藕淀粉-黄原胶复合纳米颗粒粒径约为486nm,电位为-35mv。具有粒径小、粒径分布均匀、稳定性好、生物相容相好等优点。
83.(5)本发明的莲藕淀粉-黄原胶pickering乳液储藏稳定性好,受温度、ph、离子强度等环境条件影响小,储存非常稳定,可应用于食品、保健品、药品及化妆品等多个领域。
附图说明
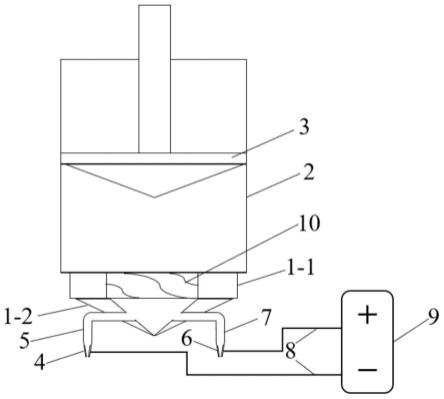
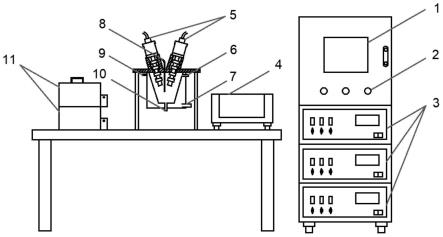
84.图1为本发明的双频聚能式超声波处理设备结构图,其中1为控制器、2为指示灯、3为超声波发生器、4为温控器、5为聚能式超声波探头、6为料液出口、7为恒温水入口、8为温度计、9为恒温水出口、10为料液进口、11为蠕动泵。
85.图2-3分别为本发明中莲藕淀粉的粒径和多分散指数随浓度和时间的变化图,注:图中同一指标中不同小写英文字母表示同组数据之间具有显著性差异(p《0.05)。
86.图4为本发明中莲藕淀粉-黄原胶复合纳米颗粒的粒径、多分散指数和ζ电位随二者比例的变化图,注:图中同一指标中不同小写英文字母表示同组数据之间具有显著性差异(p《0.05)。
87.图5为本发明中各原料的扫描电镜和透射电镜图。
88.图6为本发明中各原料的红外光谱图。
89.图7为本发明中各原料的x射线衍射图。
90.图8-10为本发明中不同超声波频率、功率和时间下的pickering乳液的粒径和电位图。
91.注:图中同一指标中不同小写英文字母表示同组数据之间具有显著性差异(p《0.05);a为乳液粒径图,b为乳液电位图。
92.图11为本发明中不同pickering乳液的光学显微镜图。
93.图12为本发明中不同pickering乳液的激光共聚焦显微镜图。
94.图13-14为本发明中不同条件下pickering乳液的光学显微镜图和外观图。
95.图15为本发明中不同精油添加量下的鱼油pickering乳液的粒径和电位图,注:图中同一指标中不同小写英文字母表示同组数据之间具有显著性差异(p《0.05);a为乳液粒径图,b为乳液电位图。
96.图16为本发明中不同鱼油pickering乳液加速氧化后次级氧化产物含量图,注:t80-emulsion代表对比例2中吐温80稳定的乳液;ho-emulsion代表对比例3中莲藕淀粉-黄原胶稳定的鱼油pickering乳液;ho/mo-emulsion代表实施例11中莲藕淀粉-黄原胶稳定的鱼油/橘精油pickering乳液。
具体实施方式
97.在本发明中所使用的术语,除非有另外说明,一般都能被本领域普通技术人员理解。下面结合具体的实施例,并参照数据进一步详细地描述本发明。特此说明,这些实施例只是为了举例说明本发明,而非以任何方式限制本发明的范围。
98.图1为本发明的双频聚能式超声波处理设备,该设备可通过控制器1设定超声波工作参数(超声波功率密度、频率、脉冲工作时间、间歇时间和处理总时间),工作时可选择不同超声波频率的探头(20khz、28khz、35khz、40khz、50khz),连接不同的超声波发生器3,可实现单一频率/两个频率超声波处理。在超声波处理之前,开启温控器,将恒温水通过蠕动泵11从恒温水入口泵入,恒温水出口9泵出。处理时,将需要处理的料液通过蠕动泵11从料液进口10泵入处理槽,并从料液出口6泵出,实现循环均匀处理。可通过温度计实时监测处理槽内的温度。
99.本发明中所使用的莲藕淀粉可以用莲藕自行提取,也可购买市售成品莲藕淀粉。
100.莲藕淀粉的提取方法如下:
101.(1)莲藕的前处理:将新鲜的莲藕进行迅速的清洗、去沙、削皮、称重、切块、放入用1%nacl和0.2%nahso3的混合溶液浸泡。
102.(2)打浆(料液比为1:6)、过滤,将滤渣置于0.05%的naoh溶液中浸泡40min后进行过滤,取其滤液;再将滤渣加水洗两次,取滤液。
103.(3)得到的所有滤液4500r/min下离心10min,得到离心杯底部白色固体,刮去表面深色杂质。重复清洗三次得到湿淀粉,将湿淀粉放在50℃烘箱中干燥12小时,再用粉碎机磨粉得到莲藕淀粉。
104.实施例1:
105.莲藕淀粉纳米颗粒的制备方法,按照下述步骤进行:
106.(1)莲藕淀粉分散在蒸馏水中,浓度分别为1wt%、2wt%、3wt%、4wt%和5wt%;
107.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
108.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅灭菌处理,条件为121℃,20min;
109.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中重结晶10h。
110.测定方法:使用litesizer 500型纳米粒度分析仪测定莲藕淀粉纳米颗粒的粒径和多分散指数。待测样品用蒸馏水稀释50倍,混匀后采用抛弃型样品池在25℃下测量样品的粒径大小,样品折射率为1.53,溶剂折射率为1.33,每个样品连续测量三次。
111.以粒径和多分散性指数对莲藕淀粉纳米颗粒分散液浓度进行优化,结果见图2,随着莲藕淀粉浓度的增加,淀粉纳米颗粒的粒度呈现先减小后增大的趋势,且多分散指数均小于30%,表明测试时分散良好。淀粉浓度为2wt%时,粒径最小,多分散指数也最小,因此选择淀粉浓度为2wt%制备莲藕淀粉纳米颗粒。
112.实施例2:
113.莲藕淀粉纳米颗粒的制备方法,按照下述步骤进行:
114.(1)莲藕淀粉分散在蒸馏水中,浓度为2wt%;
115.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
116.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅灭菌处理,条件为121℃,20min;
117.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,时间分别为8h、9h、10h、11h、12h。
118.测定方法:同实施例1。
119.以粒径和多分散性指数对莲藕淀粉纳米颗粒制备回生时间进行优化,结果见图3,随着回生时间的增加,淀粉纳米颗粒的粒度呈现先减小后增大的趋势,且多分散指数均小于30%,表明测试时分散良好。回生时间为9h时,纳米颗粒的粒径最小,因此选择回生时间为9h制备莲藕淀粉纳米颗粒。
120.实施例3:
121.莲藕淀粉-黄原胶复合纳米颗粒的制备方法,按照下述步骤进行:
122.(1)莲藕淀粉1g分散在300ml蒸馏水中;
123.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
124.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
125.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,时间为9h。
126.(5)将黄原胶1g溶于300ml蒸馏水,置于磁力搅拌器上搅拌过夜,使其完全溶解;
127.(6)将步骤(4)中制备的300ml淀粉纳米颗粒分散液和(5)中的300ml黄原胶混合,获得复合纳米颗粒溶液。
128.实施例4:
129.莲藕淀粉-黄原胶复合纳米颗粒的制备方法,按照下述步骤进行:
130.(1)莲藕淀粉20g分散在500ml蒸馏水中;
131.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
132.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
133.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,时间为9h。
134.(5)将黄原胶20g溶于500ml蒸馏水,置于磁力搅拌器上搅拌过夜,使其完全溶解;
135.(6)将步骤(4)中制备的500ml淀粉纳米颗粒分散液和(5)中的500ml黄原胶溶液混合,获得复合纳米颗粒溶液。
136.实施例5:
137.莲藕淀粉-黄原胶复合纳米颗粒的制备方法,按照下述步骤进行:
138.(1)莲藕淀粉8g分散在400ml蒸馏水中;
139.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
140.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
141.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,时间为9h。
142.(5)将黄原胶2.4g溶于400ml蒸馏水,置于磁力搅拌器上搅拌过夜,使其完全溶解;
143.(6)将步骤(4)中制备的400ml淀粉纳米颗粒分散液和(5)中的400ml黄原胶溶液混合,获得复合纳米颗粒。
144.测定方法:莲藕淀粉纳米颗粒粒径测定:使用litesizer 500型纳米粒度分析仪测定莲藕淀粉-黄原胶复合纳米颗粒的粒径、多分散指数和ζ电位。待测样品用蒸馏水稀释50倍,混匀后采用抛弃型样品池在25℃下测量样品的粒径大小,样品折射率为1.53,溶剂折射率为1.33,每个样品连续测量三次。ζ电位测量采用omegaⅱ型样品池,溶剂折射率为1.33,每个样品连续测量三次。
145.以粒径、多分散性指数和ζ电位对莲藕淀粉-黄原胶的比例进行优化,结果见图4。随着黄原胶的增加,复合纳米颗粒的粒径呈现一直增加的趋势,这可能是因为黄原胶附着在淀粉纳米颗粒外侧,形成了包覆层;多分散指数均低于30%,表明测试时颗粒分散良好;所有样品的ζ电位绝对值均大于30mv,在颗粒之间有足够大的斥力存在,表明制备的复合纳米颗粒稳定性较好。随着黄原胶的增加,复合纳米颗粒的ζ电位绝对值呈现先增大后减小的趋势,当莲藕淀粉和黄原胶比例为10:3时,ζ电位的绝对值达到最大,此时复合纳米颗粒最稳定。因此选择莲藕淀粉和黄原胶比例为10:3制备莲藕淀粉-黄原胶复合纳米颗粒。
146.实验例1:纳米颗粒的表征
147.莲藕淀粉、莲藕淀粉纳米颗粒和莲藕淀粉-黄原胶复合纳米颗粒的结构分析和表征:
148.本实验例的莲藕淀粉纳米颗粒和莲藕淀粉-黄原胶复合纳米颗粒的制备方法,分别按照实施例2和实施例5的步骤进行。
149.(1)扫描电镜和透射电镜分析
150.用镊子夹取硅晶片置于粘有导电胶的样品台上,将新鲜制备的样品滴在硅晶片上,风干后喷金5min,分别采用5kv和15kv的加速电压对莲藕淀粉、莲藕淀粉纳米颗粒和莲藕淀粉-黄原胶复合纳米颗粒进行扫描电镜观察;取稀释后样品分散液,滴在涂有超薄碳支
撑膜的铜网上,用滤纸吸去多余液体,烘干后在100kv的加速电压下对莲藕淀粉纳米颗粒和莲藕淀粉-黄原胶复合纳米颗粒进行透射电镜观察。
151.由图5可知,原莲藕淀粉形状为柱状,粒径较大,在35μm左右;莲藕淀粉纳米颗粒的电镜图表明,压热处理成功获得了粒径为250nm的淀粉纳米颗粒,这也证明了粒度仪的测试结果;莲藕淀粉-黄原胶复合纳米颗粒的扫描电镜图和透射电镜图同时证明了黄原胶在颗粒之间形成了较为紧密的网络结构。
152.(2)傅里叶变换红外光谱分析
153.在4000~500cm-1
的波数范围内进行样品的红外光谱分析,分辨率为4cm-1
,扫描次数32次。试验结果使用omnic离线软件进行处理与分析。
154.由图6可知,在原莲藕淀粉ft-ir图谱中,3420cm-1
处的吸收峰主要是-oh的伸缩振动所引起的,2931cm-1
处的吸收峰可以归因于-ch2的伸缩振动,而1648cm-1
处的吸收峰是由结合水的弯曲振动引起,1367cm-1
处的吸收峰是由c-h的弯曲振动引起的。在莲藕淀粉纳米颗粒的ft-ir图谱中,吸收峰基本与原莲藕淀粉保持一致,但是,-oh伸缩振动所形成的吸收峰从3420cm-1
移动到了3412cm-1
且峰强增强,另外指纹区的吸收峰也明显往短波方向移动,这表明莲藕淀粉纳米颗粒中可能形成了更加稳定的氢键相互作用。对于黄原胶的ft-ir图谱,其特征峰出现在1732cm-1
,为糖醛酸的特征吸收峰。相比较于莲藕淀粉纳米颗粒和黄原胶各自的ft-ir图谱,莲藕淀粉-黄原胶复合纳米颗粒的ft-ir图谱显示没有新的吸收峰出现,表明通过物理方法制备的复合纳米颗粒没有产生新的基团。此外,在复合纳米颗粒的ft-ir谱图中-oh的伸缩振动所引起的吸收峰(3408)比莲藕淀粉纳米颗粒(3412)和黄原胶(3446)往更短的波长方向移动且峰强变强,表明氢键相互作用是复合纳米颗粒中莲藕淀粉和黄原胶之间的主要作用力。
155.(3)x-射线衍射分析
156.样品置于样品台中央,压平后进行x射线衍射(xrd)测试,测试条件为:5-45
°
,5
°
/min。
157.由图7可知,原莲藕淀粉在15
°
、17
°
、18
°
、23
°
出现结晶峰,为a型淀粉;压热处理之后,淀粉转变为b型,且峰强降低,说明压热处理能够使淀粉颗粒结构崩塌,使得内部结晶结构被破坏,形成纳米级的颗粒,这支持了扫描电镜的观察结果。此外,黄原胶在12
°
左右有一个强峰出现,但是,莲藕淀粉-黄原胶复合纳米颗粒的衍射图谱的对应位置并未出现此峰,该现象可能证明了莲藕淀粉和黄原胶之间的相互作用,证明了复合纳米颗粒的形成。
158.实施例6:
159.莲藕淀粉-黄原胶pickering乳液的制备方法,按照下述步骤进行:
160.(1)莲藕淀粉8g分散在蒸馏水400ml中;
161.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
162.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
163.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,回生时间为9h;
164.(5)将黄原胶2.4g溶于蒸馏水400ml,置于磁力搅拌器上搅拌过夜,使其完全溶解;
165.(6)将步骤(4)中制备的400ml淀粉纳米颗粒分散液和步骤(5)中的400ml黄原胶溶
液混合,获得复合纳米颗粒溶液。
166.(7)制备粗乳液:大豆油200g加入步骤(6)得到的800ml复合纳米颗粒溶液,用高速分散机分散,转速为12000rpm,分散2min形成粗乳液;
167.(8)超声波乳化:将步骤(7)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉-黄原胶pickering乳液。超声波功率为800w/l,超声波处理时间为6min。对超声波频率为20khz、40khz和20/40khz的参数进行优化。
168.测定方法:采用mastersizer 3000粒度分布仪测定乳液滴的粒径大小。以水为分散剂,采用通用分析模式,部分参数如下:颗粒折射率1.47,颗粒吸收率0.001,分散剂折射率1.330,搅拌器的转速3000r/min。每个样品连续测量三次。乳液ζ电位使用litesizer 500型ζ电位分析仪测定,选用omegaⅱ型样品池,溶剂折射率为1.33,每个样品连续测量三次。
169.由图8可知,未经超声波处理的空白乳液平均粒径最大,为19.83
±
0.55μm,超声波处理后的乳液粒径都有显著降低,其中,经双频超声波处理的乳液粒径达到最小值10.50
±
0.56μm,这可能是因为双频超声波能够克服单一频率超声波所造成的驻波现象,从而充分发挥超声波的作用。从乳液的粒径分布图可以看出,经过超声波处理后的乳液在3μm左右出现一个小峰,说明乳液中出现更多较小的油滴,其中20/40khz的双频超声波处理的乳液在3μm处的小峰最大,说明双频超声波处理的乳液中的小液滴最多,处理效果最好。
170.乳液的ζ-电位能够表征乳液的稳定性,乳液的绝对电位越大,液滴间的斥力越大,空间位阻越大,乳液就越稳定。由图8可知,所有乳液的测试结果表明乳液都带负电,超声波处理能显著提高乳液的绝对电位,其中经双频超声波处理的乳液绝对电位最大,达到了29.90
±
0.59mv,此时乳液中存在的斥力最大,乳液最稳定。
171.实施例7:
172.莲藕淀粉-黄原胶pickering乳液的制备方法,按照下述步骤进行:
173.(1)莲藕淀粉8g分散在蒸馏水400ml中;
174.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
175.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
176.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,回生时间为9h;
177.(5)将黄原胶2.4g溶于蒸馏水400ml,置于磁力搅拌器上搅拌过夜,使其完全溶解;
178.(6)将步骤(4)中制备的400ml淀粉纳米颗粒分散液和步骤(5)中的400ml黄原胶溶液混合,获得复合纳米颗粒溶液。
179.(7)制备粗乳液:大豆油200g加入步骤(6)得到的800ml复合纳米颗粒溶液,用高速分散机分散,转速为12000rpm,分散2min形成粗乳液;
180.(8)超声波乳化:将步骤(7)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉-黄原胶pickering乳液。超声波频率为20/40khz,超声波处理时间为6min,对超声波功率为400w/l、800w/l、1200w/l、1600w/l、2000w/l的参数进行优化。
181.测定方法同实施例6。
182.由图9可知,未经超声波处理的空白乳液平均粒径最大,为18.53
±
1.52μm,超声波处理后的乳液粒径都有显著降低,乳液的粒径大小随超声波功率的增加而降低,这可能是
因为随着超声波功率的增加,在处理槽中传播的能量就越大,能够使更多的液滴破碎,从而降低乳液粒径。此外,从乳液的粒径分布图可以看出,经过超声波处理后的乳液在3μm左右出现一个小峰,说明乳液中出现更多较小的油滴,其中经1600w/l和2000w/l处理后的乳液分布在3μm处的小峰最大,此时乳液中的小液滴最多,这与乳液平均粒径测试结果吻合。
183.乳液的ζ-电位测试结果表明,所有乳液的测试结果表明乳液都带负电,乳液的绝对电位随超声波功率的增加先增大后减小,当超声波功率为1200w/l时,乳液的绝对电位最大,达到了32.58
±
0.33mv,此时乳液中存在的斥力最大,乳液最稳定。研究表明,当乳液的绝对电位大于30mv时,就能够长时间稳定。
184.实施例8:
185.莲藕淀粉-黄原胶pickering乳液的制备方法,按照下述步骤进行:
186.(1)莲藕淀粉8g分散在蒸馏水400ml中;
187.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
188.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
189.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,回生时间为9h;
190.(5)将黄原胶2.4g溶于蒸馏水400ml,置于磁力搅拌器上搅拌过夜,使其完全溶解;
191.(6)将步骤(4)中制备的400ml淀粉纳米颗粒分散液和步骤(5)中的400ml黄原胶溶液混合,获得复合纳米颗粒溶液。
192.(7)制备粗乳液:大豆油200g加入步骤(6)得到的800ml复合纳米颗粒溶液,用高速分散机分散,转速为12000rpm,分散2min形成粗乳液;
193.(8)超声波乳化:将步骤(7)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉-黄原胶pickering乳液。超声波频率为20/40khz,超声波功率为1200w/l,对超声波处理时间为2min、4min、6min、8min、10min的参数进行优化。
194.测定方法同实施例6。
195.由图10可知,未经超声波处理的空白乳液平均粒径最大,为19.20
±
0.66μm,超声波处理后的乳液粒径都有显著降低,乳液的粒径大小随超声波处理时间的增加而降低,这可能是因为随着超声波时间的增加,能够使更多的液滴破碎,从而降低乳液粒径。此外,从乳液的粒径分布图可以看出,经过超声波处理后的乳液在3μm左右出现一个小峰,说明乳液中出现更多较小的油滴,其中处理8min和10min的乳液分布在3μm处的小峰最大,此时乳液中的小液滴最多,这与乳液平均粒径测试结果吻合。
196.乳液的ζ-电位测试结果表明,所有乳液的测试结果表明乳液都带负电,乳液的绝对电位随超声波处理时间的延长先增大后减小,当超声波处理时间为4min时,乳液的绝对电位最大,达到了35.38
±
0.62mv此时乳液中存在的斥力最大,乳液最稳定。这可能是因为过长时间的超声波处理可能会破坏颗粒间的凝胶网络结构,使得乳液的绝对电位减小,稳定性降低。因此,综上所述,优选的超声波条件为20/40khz、1200w/l、4min。
197.对比例1:
198.莲藕淀粉pickering乳液的制备方法,按照下述步骤进行:
199.(1)莲藕淀粉8g分散在400ml蒸馏水中;
200.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
201.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min。
202.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,回生时间为9h。
203.(5)制备粗乳液:100g大豆油加入步骤(4)的400ml淀粉纳米颗粒分散液中,用高速剪切分散机分散,转速为12000rpm,分散2min形成粗乳液;
204.(6)超声波乳化:将步骤(5)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉pickering乳液。超声波频率为20/40khz,超声波功率为1200w/l,超声波处理时间为4min。
205.实验例2:光学显微镜观察
206.莲藕淀粉pickering乳液的制备方法同对比例1。
207.莲藕淀粉-黄原胶pickering乳液的制备方法同实施例8。
208.取20μl新鲜制备的乳液滴于载玻片上,盖上盖玻片,放在bm2000型光学显微镜上,通过dc6000型摄像头拍摄乳液微观照片。
209.作为热力学不稳定体系,乳液通常会在不同时间出现不稳定现象。一般来讲,乳液失稳的物理原因有:乳析、絮凝、聚结和奥斯特熟化。乳析指的是由重力作用引起的乳滴沉降,这和乳液体系的抗沉降性能有关。由斯托克斯沉降定律可知,可以通过减小分散相的粒径或者增大连续相的粘度来减缓这种重力分离。絮凝指的是多个乳滴聚集在一起形成絮凝体,但是这些乳滴仍然能够保持自己的完整性并没有合并,因此,这种现象是可逆的。絮凝现象发生在乳滴之间的吸引力大于排斥力,在乳液体系中,主要为静电力。聚结指的是乳滴界面膜破裂,由多个小液滴变为一个大液滴的现象,这种现象是不可逆的。在o/w体系中,大规模的乳滴聚结现象最终会形成一个分离的油层出现在乳液的顶部。奥斯瓦尔德熟化现象是由于不同粒径乳滴之间的内压差而引起的小液滴与大液滴聚结现象。在乳液失稳现象中,奥斯瓦尔德熟化是容易被忽视的原因之一。
210.在图11中,样品a为莲藕淀粉纳米颗粒稳定的粗乳液,由图可知,乳滴粒径较大,另外一个非常明显的特征是乳滴絮凝。可以看到小液滴和小液滴之间的絮凝以及多个小液滴絮凝在大液滴周围。这些絮凝会增加乳滴平均粒径,从而增强重力分离,最终导致乳液的分层。样品b为超声波处理后的莲藕淀粉纳米颗粒稳定的乳液,由图可知,乳滴的粒径明显减小,这可以归因于双频超声波出色的空化破碎效果。但是乳液的絮凝现象仍然存在,这依然会导致乳液的较快分层。样品c是由莲藕淀粉-黄原胶复合纳米颗粒稳定的粗乳液,由图可知,乳滴粒径仍然较大,但是絮凝现象得到明显的改善,小液滴之间更加分散,且小液滴与大液滴也能够较好的分散。这种现象出现的原因可能是,黄原胶的加入在乳液体系中形成了致密的三维网络结构,能够很好的限制乳滴之间的团聚,从而改善乳液的絮凝现象,提高乳液的稳定性。样品d是超声波处理后的莲藕淀粉-黄原胶pickering乳液,由图可知,相比样品c,乳滴粒径得到了明显的降低,而在乳滴絮凝方面,同样品c一样,乳滴絮凝现象得到了明显的改善。综上所述,莲藕淀粉-黄原胶复合纳米颗粒能够提高乳液粘度,抑制重力作用带来的乳析现象;黄原胶还能在体系中形成三维网络结构,显著改善乳滴的絮凝现象;最后,结合超声波的空化破碎效果,形成更小粒径的乳滴,最终大大提高pickering乳液的稳
定性。
211.实验例3:激光共聚焦显微镜观察
212.莲藕淀粉pickering乳液的制备方法同对比例1。
213.莲藕淀粉-黄原胶pickering乳液的制备方法同实施例8。
214.试验方法:采用leica tcs sp5型激光共聚焦系统观察乳液的微观形态和界面结构。准确称取5mg尼罗红和尼罗蓝溶于5ml丙二醇,配置成1mg/ml的染色剂溶液。取50μl染色剂与1ml新鲜制备的乳液混合,染色30min。取10μl乳液样品滴在载玻片上,盖上盖玻片,送入激光共聚焦系统观察。所有图像的扫描频率为200khz,分辨率为1024
×
1024。尼罗红的激发波长为488nm,尼罗蓝的激发波长为633nm。
215.在图12中,样品a为莲藕淀粉纳米颗粒稳定的粗乳液,由图可知,乳滴粒径较大,与光学显微镜观察结果一致。在激光共聚焦显微镜下,在乳滴为绿色,莲藕淀粉纳米颗粒和莲藕淀粉-黄原胶复合纳米颗粒为红色。可以明显的看到,样品a中绿色乳滴周围的红色比较暗,说明乳滴吸附的淀粉纳米颗粒较少。样品b为超声波处理后的莲藕淀粉纳米颗粒稳定的乳液,与光学显微镜的观察结果一致,乳滴的粒径明显降低,值得注意的是绿色乳滴周围的红色变得明亮,说明乳滴吸附的淀粉纳米颗粒变多。样品c是由莲藕淀粉-黄原胶复合纳米颗粒稳定的粗乳液,而样品d是超声波处理后的莲藕淀粉-黄原胶pickering乳液,同样的现象在样品c和样品d中再次出现。综上所述,激光共聚焦的观察结果证明了采用的双频超声波不仅能够有效的降低乳滴粒径,此外非常重要的一点是超声波还能够增强颗粒在乳滴界面的吸附,使得更多的颗粒被聚集在界面上,形成更加致密的界面膜,避免了因聚结而导致的乳液不稳定现象。
216.实验例4:ph稳定性分析
217.莲藕淀粉-黄原胶pickering乳液的制备方法同实施例8。
218.测定方法:取20ml新鲜制备的乳液,用0.5m的hcl和naoh调节乳液的ph 2-8,在室温下储存30天,并在1天、7天和30天时进行宏观和微观监测。光学显微镜观察方法同实施例8,宏观监测通过手机拍照记录。
219.由图13可知,莲藕淀粉-黄原胶pickering乳液在整个储藏的30天内稳定性良好,在所有ph值条件下都没有出现分层现象。新鲜制备的乳液ph在5-6之间,从乳液的光学显微镜观察结果可知,莲藕淀粉-黄原胶pickering乳液对酸性条件下的粒径相差不大,但在ph=8的碱性条件下,乳滴粒径明显上升,这说明碱性条件可能会导致乳液相对酸性条件的不稳定。此外,观察结果表明,所有样品在1天、7天和30天时,乳滴粒径没有明显增加,说明乳液非常稳定,这归因于莲藕淀粉-黄原胶复合纳米颗粒的界面吸附和体系中的三维网络结构,从而有效克服了乳液的乳析、絮凝和聚结,提高了乳液的稳定性;此外,双频超声波处理能够降低乳滴的粒径,使乳液更加均匀,有效克服了重力造成的乳析和奥斯瓦尔德熟化现象。
220.实验例5:离子强度稳定性分析
221.莲藕淀粉-黄原胶pickering乳液的制备方法同实施例8。
222.测定方法:向新鲜制备的乳液中加入nacl粉末,使乳液离子浓度为50mm,100mm,200mm和300mm,在室温下储存30天,并在1天、7天和30天时进行宏观和微观监测。光学显微镜观察方法同实施例8,宏观监测通过手机拍照记录。
223.由图14可知,由图14可知,莲藕淀粉-黄原胶pickering乳液在整个储藏的30天内稳定性良好,在所有离子强度条件下都没有出现分层现象。从乳液的光学显微镜观察结果可知,莲藕淀粉-黄原胶pickering乳液对离子强度稳定性较高,且随着nacl浓度的上升,乳滴粒径减小,说明nacl能够改善乳液的稳定性,这与目前其他人的研究结果一致。此外,观察结果表明,所有样品在1天、7天和30天时,乳滴粒径没有明显增加,说明乳液非常稳定,这归因于莲藕淀粉-黄原胶复合纳米颗粒的界面吸附和体系中的三维网络结构,从而有效克服了乳液的乳析、絮凝和聚结,提高了乳液的稳定性;此外,双频超声波处理能够降低乳滴的粒径,使乳液更加均匀,有效克服了重力造成的乳析和奥斯瓦尔德熟化现象。
224.实施例9:
225.负载鱼油的莲藕淀粉-黄原胶pickering乳液的制备方法,按照下述步骤进行:
226.(1)莲藕淀粉1g分散在蒸馏水300ml中;
227.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
228.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
229.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,回生时间为9h;
230.(5)将黄原胶1g溶于蒸馏水300ml,置于磁力搅拌器上搅拌过夜,使其完全溶解;
231.(6)将步骤(4)中制备的300ml淀粉纳米颗粒分散液和步骤(5)中的300ml黄原胶溶液混合,获得复合纳米颗粒溶液。
232.(7)制备粗乳液:加入150g鲱鱼油和10g橘精油到步骤(6)的600ml复合纳米颗粒溶液中,用高速剪切分散机分散,转速为12000rpm,分散2min形成粗乳液;
233.(8)超声波乳化:将步骤(7)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉-黄原胶pickering乳液。超声波频率为20/40khz,超声波功率为1200w/l,超声波处理时间为4min。
234.实施例10:
235.负载鱼油的莲藕淀粉-黄原胶pickering乳液的制备方法,按照下述步骤进行:
236.(1)莲藕淀粉20g分散在蒸馏水500ml中;
237.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
238.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
239.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,回生时间为9h;
240.(5)将黄原胶20g溶于蒸馏水500ml,置于磁力搅拌器上搅拌过夜,使其完全溶解;
241.(6)将步骤(4)中制备的500ml淀粉纳米颗粒分散液和步骤(5)中的500ml黄原胶溶液混合,获得复合纳米颗粒溶液。
242.(7)制备粗乳液:加入200g鲱鱼油和50g橘精油到步骤(6)的1000ml复合纳米颗粒溶液中,用高速剪切分散机分散,转速为12000rpm,分散2min形成粗乳液;
243.(8)超声波乳化:将步骤(7)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉-黄原胶pickering乳液。超声波频率为20/40khz,超声波功率
为1200w/l,超声波处理时间为4min。
244.实施例11:
245.负载鱼油的莲藕淀粉-黄原胶pickering乳液的制备方法,按照下述步骤进行:
246.(1)莲藕淀粉8g分散在蒸馏水400ml中;
247.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
248.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min;
249.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中进行重结晶,回生时间为9h;
250.(5)将黄原胶2.4g溶于蒸馏水400ml,置于磁力搅拌器上搅拌过夜,使其完全溶解;
251.(6)将步骤(4)中制备的400ml淀粉纳米颗粒分散液和步骤(5)中的400ml黄原胶溶液混合,获得复合纳米颗粒溶液。
252.(7)制备粗乳液:加入160g鲱鱼油和40g橘精油到步骤(6)的800ml复合纳米颗粒溶液中,用高速剪切分散机分散,转速为12000rpm,分散2min形成粗乳液;
253.(8)超声波乳化:将步骤(7)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉-黄原胶pickering乳液。超声波频率为20/40khz,超声波功率为1200w/l,超声波处理时间为4min。
254.测定方法同实施例6。
255.由图15可知,随着精油添加量的增加,pickering乳液的平均粒径不断增大。但乳液的绝对电位随精油添加量呈现增加先增大后减小的趋势,当精油添加量为总油相的20%时,乳液的绝对电位最大,达到了39.53
±
1.31mv,此时乳液中存在的斥力最大,乳液最稳定。这表明精油可以调节乳液界面的物理化学特性,提高乳液的稳定性。因此选择精油与鱼油的比例为8:2制备pickering乳液。
256.对比例2:
257.一种作为对照的使用吐温80稳定的乳液制备方法如下:
258.(1)8g吐温80分散在400ml蒸馏水中;
259.(2)制备粗乳液:100g大豆油加入步骤(1)的400ml吐温80溶液中,用高速分散机分散,转速为12000rpm,分散2min形成粗乳液;
260.(3)超声波乳化:将步骤(2)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉pickering乳液。超声波频率为20/40khz,超声波功率为1200w/l,超声波处理时间为4min。
261.对比例3:
262.一种作为对照不添加精油的鱼油莲藕淀粉-黄原胶pickering乳液的制备方法如下:
263.(1)莲藕淀粉8g分散在400ml蒸馏水中;
264.(2)将淀粉分散液置于沸水中预糊化5min,并不断搅拌,保证其分散均匀;
265.(3)将步骤(2)中预糊化好的淀粉分散液立即转移至灭菌锅,进行压热处理,条件为121℃,20min。
266.(4)将步骤(3)中压热处理好的分散液,取出自然冷却至室温后,再转入4℃冰箱中
进行重结晶,回生时间为9h。
267.(5)将黄原胶2.4g溶于蒸馏水,置于磁力搅拌器上搅拌过夜,使其完全溶解;
268.(6)将步骤(4)中制备的400ml淀粉纳米颗粒分散液和步骤(5)中的400ml黄原胶溶液混合,获得复合纳米颗粒溶液。
269.(7)制备粗乳液:加入200g鲱鱼油到步骤(6)的800ml复合纳米颗粒溶液中,用高速剪切分散机分散,转速为12000rpm,分散2min形成粗乳液;
270.(8)超声波乳化:将步骤(8)中粗乳液置于双频聚能式超声波装置中进行乳化处理,得到最终的成品莲藕淀粉-黄原胶pickering乳液。超声波频率为20/40khz,超声波功率为1200w/l,超声波处理时间为4min。
271.实验例6:氧化稳定性测定
272.吐温80稳定的乳液的制备方法同对比例2。
273.不添加精油的负载鱼油的莲藕淀粉-黄原胶pickering乳液的制备方法同对比例3。
274.负载鱼油的莲藕淀粉-黄原胶pickering乳液的制备方法同实施例11。
275.采用史卡尔烘箱法,将不同乳液样品放置在65℃烘箱中加速氧化24h,考察乳液中油脂的温度稳定性;将不同乳液样品放置在紫外灯下照射24h,考察乳液中油脂的光稳定性;将不同乳液样品在常温下静置30天,考察乳液中油脂的储藏稳定性。
276.测定方法:
277.氧化产物的测定:氧化产物通过丙二醛(mda)含量来表征。取1.0ml乳液与2.0ml硫代巴比妥酸溶液(tba)混合,沸水浴加热20min,冷却后在1000g下离心10min,取上清液在532nm处测定吸光值。标准曲线使用1,1,3,3-四乙氧基丙烷绘制,以计算样品的tbars值。
278.由图16可知,由传统的表面活性剂吐温80稳定的乳液在热、光和储存等条件下,鱼油的氧化程度最高,且比莲藕淀粉-黄原胶复合纳米颗粒稳定的pickering乳液中鱼油的氧化程度高出一个数量级,这说明莲藕淀粉-黄原胶复合纳米颗粒在油滴表面形成了致密的防护层,能够有效阻隔油滴与氧气接触,大大降低了油脂的氧化。有研究还表明黄原胶具有螯合金属离子的作用,这也是该复合纳米颗粒保护鱼油免受氧化的另外一个重要原因。此外,采用在鱼油中添加精油的方案,能够进一步降低乳液的氧化产物,保护鱼油免受氧化,这可以归因于橘精油的抗氧化功效。
279.实验例7:dha和epa的保留率测定
280.吐温80稳定的乳液的制备方法同对比例2。
281.不添加精油的负载鱼油的莲藕淀粉-黄原胶pickering乳液的制备方法同对比例3。
282.负载鱼油的莲藕淀粉-黄原胶pickering乳液的制备方法同实施例11。
283.采用gc-ms测定乳液中dha和epa的保留率。
284.乳液中脂肪酸提取:用移液枪取1ml乳液置于抽脂瓶中,加入10ml65
±
1℃的水,振荡溶解样品,并使样品分散均匀。然后加入2ml体积分数为25%的氨水,65℃水浴15min,取出微微振荡,冷却至室温。然后向抽脂瓶中加入10ml乙醇,摇匀后,再加入25ml乙醚,盖盖振荡。最后再加入25ml石油醚(30℃~60℃),盖盖振荡。静置分层,将上层有机层转入磨口烧瓶中,通过旋转蒸发仪浓缩至干。
285.甲酯化(碱催化法):向旋蒸后的烧瓶中加入30ml正己烷,充分振荡后转移至50ml容量瓶,正己烷定容,获得总油储备液。取2ml储备液于具塞试管,加入0.2ml koh-甲醇溶液(2mol/l),充分振荡后于5000rpm离心5min,取上层有机相。最后,过0.22μm滤膜,将样品加入气质样品瓶中,用gc-ms检测分析。
286.gc条件:进样口温度为250℃;升温程序为50℃保温2min,开始升温,以7℃/min升至320℃,保温5min。采用恒速模式,流量为1ml/min,分流比为1:10;进样量为1μl,载气为he,色谱柱名称为db-5ms。
287.ms条件:离子源温度230℃;接口温度为250℃。质量扫描范围50~700m/z;溶剂延迟时间设置为6min。
288.成分分析:定性分析通过nist数据库检索,对标准谱图进行比较来确认样品中的dha和epa甲酯成分。定量分析时用面积归一化法来确定dha和epa的百分含量。
289.表1加速氧化处理(65℃、5h)乳液中的dha和epa保留率
[0290][0291]
(表中t80-emulsion代表对比例2中吐温80稳定的乳液;ho-emulsion代表对比例3中莲藕淀
[0292]
粉-黄原胶稳定的鲱鱼油pickering乳液;ho/mo-emulsion代表实施例7中莲藕淀粉-黄原胶稳定
[0293]
的鲱鱼油/橘精油pickering乳液。)
[0294]
由表1可知,由传统的表面活性剂t80稳定的鱼油乳液由于对dha和epa没有任何保护,因此dha和epa的保留率最低。由莲藕淀粉-黄原胶复合纳米颗粒稳定的鱼油pickering乳液对dha和epa的保留率得到了显著的提升,这可以归因于复合纳米颗粒在油滴表面形成了致密的壳层,减少其与氧气的接触,尽管在较高的温度下,乳液中dha和epa的保留率也能够保持较高的水平。当在鱼油中添加橘精油时,制备的由莲藕淀粉-黄原胶复合纳米颗粒稳定的pickering乳液中dha和epa的保留率进一步提高,这可能是因为橘精油作为一种抗氧化剂分散在油相中,能够进一步保护乳液中的dha和epa。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。