1.本发明涉及生物医药材料领域,特别涉及一种可载药单分散碳酸钙-明胶复合栓塞微球及载药栓塞微球。
背景技术:
2.肝细胞癌(hcc)是一种发病率和死亡率都极高的恶性肿瘤,具有发病隐匿、恶性程度高且进展迅速等特征,70%以上的患者在临床确诊时已处于中晚期,进而失去根治性手术切除的最佳时机。经导管肝动脉化疗栓塞术(tace)已逐渐成为临床上不可切除性肝癌的首选治疗方案,其主要通过阻断肿瘤供血动脉并联合局部化学治疗,使肿瘤在短时间内坏死、萎缩,从而达到治疗的目的。
3.在肝癌栓塞治疗中,栓塞剂在阻断肿瘤组织的血供的同时也会抑制乳酸从肿瘤部位排除,而肿瘤微环境中高表达的乳酸会使肿瘤细胞在缺乏营养供给时进入休眠状态,保护肿瘤细胞免受葡萄糖匮乏带来的影响,同时也会显著降低肿瘤细胞对化疗药物的敏感性,进而提高肝癌的复发率和转移率。有研究显示在供血动脉栓塞之前往肿瘤部位注射碳酸氢钠溶液来中和乳酸的治疗方案能够显著提高肝癌的栓塞治疗效果。但是,碳酸氢钠是一种水溶性小分子,很容易从肿瘤部位流失,难以长时间使肿瘤部位保持偏碱性环境。
4.载药栓塞微球是目前临床常用的栓塞剂,与传统的碘油/化疗药物栓塞剂相比,其能更长时间地维持肿瘤部位的化疗药物浓度,在提高化疗疗效的同时还能降低药物的全身毒副作用。但是,现有栓塞微球存在着粒径不均一、尺寸不可控的问题,严重影响肝癌的栓塞治疗效果,在临床上主要表现为:尺寸过大的微球难以对肝癌供血动脉末梢进行有效栓塞,造成栓塞效果不够彻底;尺寸太小的微球可能会通过静脉吻合支而进入静脉,从而导致肺部及其他组织的栓塞,造成非靶器官的缺血坏死,出现严重并发症。
5.明胶是一种天然的天然高分子材料,具有生物相容性好、价格便宜、生物可降解等优点,已被广泛应用于栓塞治疗中。此外,明胶微球制备方法简单,经过交联制得的明胶微球外观光滑呈球形,可以更好的适配血管,且吸水后有良好的弹性,能够达到较好的栓塞效果。但是,传统的明胶微球对化疗药物的负载能力有限,且难以实现对肿瘤酸性微环境的有效调控。
6.专利cn202111363386.9公开了一种含纳米碳酸钙的明胶复合栓塞微球、其制备方法及载药栓塞微球,其采用明胶和碳酸钙成功制备得到了一种可载药的栓塞微球,具备制备方法简单、成本较低、重现性好等优点,但其还存在以下不足:其制备的栓塞微球的粒径均一性不够,且粒径难以控制。
7.因此,现在有必要对现有技术进行改进,以提供一种更可靠的方案。
技术实现要素:
8.本发明所要解决的技术问题在于针对上述现有技术中的不足,提供一种具有肿瘤酸性微环境调控功能的可载药单分散碳酸钙-明胶复合栓塞微球及基于该微球的载药栓塞
微球。
9.为解决上述技术问题,本发明采用的技术方案是:一种可载药单分散碳酸钙-明胶复合栓塞微球,该微球的成分包括碳酸钙纳米粒和明胶,该微球具有肿瘤酸性微环境调控功能,其采用基于微流控的方法制备得到,具体制备方法包括以下步骤:
10.s1、搭建微通道反应器,该微通道反应器包括液滴生成管、与所述液滴生产管的输入端连通的流动相输入管和分散相输入管、与所述液滴生产管的输出端连通的样品接收管;
11.s2、制备到含碳酸钙纳米粒的明胶水溶液,作为分散相;
12.s3、制备流动相;
13.s4、将制得的分散相和流动相分别注入分散相输入管、流动相输入管,使分散相在液滴生成管中被流动相剪切,不断生成w/o型碳酸钙-明胶液滴;
14.s5、利用收集的碳酸钙-明胶液滴制备得到碳酸钙-明胶复合栓塞微球。
15.优选的是,所述碳酸钙-明胶复合栓塞微球的成分按质量百分数计包括:3-30%的碳酸钙纳米粒和70-90%的明胶;
16.所述碳酸钙-明胶复合栓塞微球的平均粒径大小为50-300μm,变异系数为5%以下。
17.优选的是,所述步骤s1具体包括:
18.s1-1、提供一根玻璃点样毛细管和两根透明硅胶软管,将玻璃点样毛细管的两端分别插入两根透明硅胶软管中,玻璃点样毛细管作为液滴生成管,玻璃点样毛细管前端和后端连接的透明硅胶软管分别作为流动相输入管和样品接收管;进一步优选的是,玻璃点样毛细管长约7cm,透明硅胶软管长约20cm,玻璃点样毛细管插入透明硅胶软管的深度约为10mm;
19.s1-2、将一根注射针头穿过透明硅胶软管并插入至玻璃点样毛细管中,将注射针头作为分散相输入管;进一步优选的是,注射针头插入玻璃点样毛细管的深度约为10mm;
20.s1-3、将注射针头、玻璃点样毛细管以及两根透明硅胶软管上与玻璃点样毛细管连接的部分放置在载玻片上,并用ab胶密封连接处进行固定,搭建得到微通道反应器。
21.优选的是,所述步骤s2具体包括:
22.s2-1、制备碳酸钙纳米悬浮液:
23.s2-1-1、将聚丙烯酸和氯化钙溶解于去离子水中,常温下搅拌,得到混合液;
24.s2-1-2、将碳酸钠溶解于去离子水中,然后将得到的碳酸钠溶液加入到步骤s2-1-1得到的混合液中,常温下搅拌;
25.s2-1-3、反应结束后,离心,收集沉淀物并用去离子水洗涤,然后将沉淀物重新分散于去离子水中,得到碳酸钙纳米混悬液;
26.s2-2、将明胶加入到步骤s2-1-3所制得的碳酸钙纳米混悬液中,热至并搅拌,使明胶完全溶解,制备得到含碳酸钙纳米粒的明胶水溶液,即分散相。
27.优选的是,所述步骤s3具体为:取液体石蜡,向其中加入乳化剂,室温搅拌均匀,得到流动相。
28.优选的是,所述步骤s4具体包括:
29.s4-1、将步骤s2制备的分散相和步骤s3制备的流动相分别装入注射器中,将装有
分散相的注射器与分散相输入管连接,将装有流动相的注射器加热后与流动相输入管连接,控制分散相以5-50μl/min的流速、流动相以100-700μl/min的流速注入液滴生成管,使分散相在液滴生成管中被流动相剪切,不断生成w/o型碳酸钙-明胶液滴。
30.优选的是,所述步骤s5具体包括:
31.s5-1、通过含有流动相的玻璃瓶收集样品接收管排出的经步骤s4制得的碳酸钙-明胶液滴,在收集过程中使玻璃瓶处于冰浴条件下,并对碳酸钙-明胶液滴施加搅拌作用;
32.s5-2、向步骤s5-1得到的混合物中加入交联剂,继续搅拌反应,即得碳酸钙-明胶复合栓塞微球粗品;
33.s5-3、将步骤s5-2得到的碳酸钙-明胶复合栓塞微球粗品离心,取沉淀,用体积分数分别为50%、70%和100%的异丙醇依次洗涤沉淀,以除去残留的流动相和交联剂;
34.s5-4、将步骤s5-3得到的产物自然风干,即得碳酸钙-明胶复合栓塞微球。
35.优选的是,所述玻璃点样毛细管的内径为0.4-1.1mm,所述的注射针头为34g、32g、30g、27g针头中的任意一种。
36.优选的是,所述乳化剂为span 20,span 40,span60和span 80中的一种或多种的混合物,所述交联剂为质量分数6%的甲醛溶液、质量分数25%的戊二醛溶液或质量分数5%的京尼平溶液中的一种或多种的混合物。
37.优选的是,步骤s2-1中的聚丙烯酸的平均分子量为2kda,3kda,5kda或10kda。
38.优选的是,步骤s2-2中,碳酸钙纳米粒的浓度为5-30mg/ml,明胶的浓度为95-200mg/ml。
39.优选的是,s5-2中交联时间为2-24h。
40.本发明还提供一种载药栓塞微球,其包括如上所述的可载药单分散碳酸钙-明胶复合栓塞微球以及负载于该微球上的药物,所述药物包括阿霉素、表柔比星、顺铂和吉西他滨中的一种或几种。
41.本发明的有益效果是:
42.一、本发明基于微流控技术制备得到了一种粒径均一且尺寸可控的可载药单分散碳酸钙-明胶复合栓塞微球,不仅能显著提高对不同大小肿瘤供血动脉的栓塞效果,还能有效避免异位栓塞的发生;
43.二、本发明中,将带负电的碳酸钙纳米粒引入至明胶微球所制备的碳酸钙-明胶复合栓塞微球,相比于普通的明胶微球具有更高的载药量,且能延长药物的释放时间,进而可发挥更长效的抗肝癌作用;
44.三、本发明中,载药后的碳酸钙-明胶复合栓塞微球相比于传统载药栓塞微球能有效中和栓塞后肿瘤部位堆积的乳酸,可实现肿瘤微环境调控、栓塞治疗和局部化疗的有效协同,进而显著降低肿瘤的复发和转移率。
附图说明
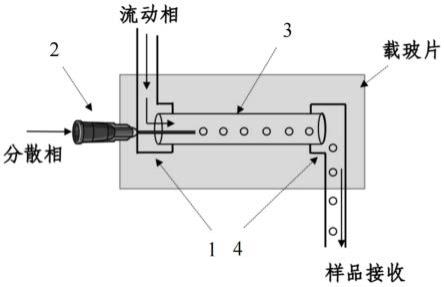
45.图1:微通道反应器的结构示意图。
46.图2:流动相流速对单分散碳酸钙-明胶复合栓塞微球制备的影响。(a)不同流动相流速下制备的单分散碳酸钙-明胶复合栓塞微球的光学显微镜照片;(b)不同流动相流速下制备的单分散碳酸钙-明胶复合栓塞微球的平均粒径大小和变异系数(cv)值。
47.图3:分散相流速对单分散碳酸钙-明胶复合栓塞微球制备的影响。(a)不同分散相流速下制备的单分散碳酸钙-明胶复合栓塞微球的光学显微镜照片;(b)不同分散相流速下制备的单分散碳酸钙-明胶复合栓塞微球的平均粒径大小和变异系数(cv)值。
48.图4:单分散碳酸钙-明胶复合栓塞微球的体内栓塞效果。(a)单分散碳酸钙-明胶复合栓塞微球在栓塞兔左肾前的dsa照片;(b)单分散碳酸钙-明胶复合栓塞微球在栓塞兔左肾后的dsa照片;(c)栓塞后第14天的兔肾脏的ct血管造影图;(e)栓塞后第14天的兔的左右肾脏的照片图;(e)栓塞后第14天的兔左肾的h&e染色图;(f)栓塞后第14天的兔右肾的h&e染色图。
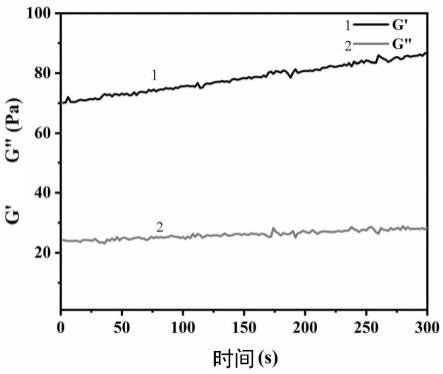
49.图5:单分散碳酸钙-明胶复合栓塞微球和单分散普通明胶栓塞微球对化疗药物阿霉素载药效能的测定结果。
50.图6:单分散碳酸钙-明胶复合栓塞微球调节肿瘤微酸环境、提高肿瘤细胞化疗敏感性的测定结果。
51.附图标记说明:
52.1—流动相输入管;2—分散相输入管;3—液滴生成管;4—样品接收管。
具体实施方式
53.下面结合实施例对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
54.应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不排除一个或多个其它元件或其组合的存在或添加。
55.下列实施例中所使用的试验方法如无特殊说明,均为常规方法。下列实施例中所用的材料试剂等,如无特殊说明,均可从商业途径得到。下列实施例中未注明具体条件者,按照常规条件或者制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
56.实施例1
57.一种可载药单分散碳酸钙-明胶复合栓塞微球,该微球的的成分按质量百分数计包括:3-30%的碳酸钙纳米粒和70-90%的明胶,该微球采用基于微流控的方法制备得到,具体制备方法包括以下步骤:
58.s1、搭建微通道反应器,该微通道反应器包括液滴生成管3、与所述液滴生产管3的输入端连通的流动相输入管1和分散相输入管2、与所述液滴生产管3的输出端连通的样品接收管4;具体包括:
59.s1-1、提供一根约7cm长的内径为0.5mm的玻璃点样毛细管和两根约20cm长的透明硅胶软管,将玻璃点样毛细管的两端分别插入两根透明硅胶软管中,插入的深度约为10mm,玻璃点样毛细管作为液滴生成管,玻璃点样毛细管前端和后端连接的透明硅胶软管分别作为流动相输入管和样品接收管;
60.s1-2、将一根32g注射针头穿过透明硅胶软管并插入至玻璃点样毛细管中,注射针头插入玻璃点样毛细管的深度约为10mm(即注射针头末端距离玻璃点样毛细管左端口约10mm),将注射针头作为分散相输入管;
61.s1-3、将注射针头、玻璃点样毛细管以及两根透明硅胶软管上与玻璃点样毛细管
连接的部分放置在载玻片上,并用ab胶密封连接处进行固定,搭建得到微通道反应器,其结构如图1所示。
62.s2、制备到含碳酸钙纳米粒的明胶水溶液,作为分散相;
63.s2-1、制备碳酸钙纳米悬浮液:
64.s2-1-1、将分子量为2kda的聚丙烯酸和(0.5m)和氯化钙(0.5m)溶解于50ml的去离子水中,常温下搅拌1h,得到混合液;
65.s2-1-2、将碳酸钠(0.5m)溶解于50ml的去离子水中,然后将得到的碳酸钠溶液加入到步骤s2-1-1得到的混合液中,常温下搅拌1h;
66.s2-1-3、反应结束后,12000rpm下高速离心10min,收集沉淀物并用去离子水洗涤3次,然后将沉淀物重新分散于去离子水中,得到浓度为5mg/ml的碳酸钙纳米混悬液;
67.s2-2、将300mg明胶加入到3ml步骤s2-1-3所制得的碳酸钙纳米混悬液中,热至至55℃并搅拌,使明胶完全溶解,制备得到含碳酸钙纳米粒的明胶水溶液,即分散相。
68.s3、制备流动相:
69.取50ml液体石蜡,向其中加入5g乳化剂span 80,室温搅拌均匀使乳化剂溶解,得到流动相。
70.s4、制备碳酸钙-明胶液滴;
71.s4-1、将步骤s2制备的分散相和步骤s3制备的流动相分别装入注射器中,将装有分散相的注射器与分散相输入管连接,将装有流动相的注射器加热至55℃后与流动相输入管连接,控制分散相以5-50μl/min的流速、流动相以100-700μl/min的流速注入液滴生成管,使分散相在液滴生成管中被流动相剪切,不断生成w/o型碳酸钙-明胶液滴。
72.该步骤中共进行四组实验,各组实验中均控制分散相的流量均为10μl/min,第一~第四组实验分别控制流动相的流量为100,200,300和400μl/min。
73.s5、利用收集的碳酸钙-明胶液滴制备得到碳酸钙-明胶复合栓塞微球。
74.s5-1、通过含有20ml流动相的玻璃瓶收集样品接收管排出的经步骤s4制得的碳酸钙-明胶液滴,连续收集30min,在收集过程中使玻璃瓶处于冰浴条件下,并对碳酸钙-明胶液滴施加低速搅拌,使其冷凝成胶以及防止凝胶微球相互之间产生粘连;
75.s5-2、向步骤s5-1得到的混合物中加入0.5ml浓度为25%的戊二醛使明胶发生反应交联,搅拌反应6h,即得碳酸钙-明胶复合栓塞微球粗品;
76.s5-3、将步骤s5-2得到的碳酸钙-明胶复合栓塞微球粗品在1000rpm下离心10min,取沉淀,用体积分数分别为50%、70%和100%的异丙醇依次洗涤沉淀,以除去残留的流动相和交联剂;
77.s5-4、将步骤s5-3得到的产物自然风干,即得碳酸钙-明胶复合栓塞微球。
78.采用光学显微镜对本实施例制备的的第一~第四组碳酸钙-明胶复合栓塞微球的形态进行表征。结果显示,采用微流控技术制备的碳酸钙-明胶复合栓塞微球形态完整、粒径均一,平均粒径随着流动相流速的增加有下降的趋势(图2a)。
79.采用image j软件对对本实施例制备的的第一~第四组碳酸钙-明胶复合栓塞微球进行粒径统计,并进一步计算微球的变异系数(cv),其中cv值是通过如下公式计算得到:cv=(标准偏差/平均值)
×
100%。结果显示,当流动相流速从100,200,300增加到400μl/min,碳酸钙-明胶复合栓塞微球的平均粒径从133.7
±
6.5,116.7
±
4.6,95.9
±
3.5减少到
76.3
±
3.7μm,但cv值均不超过5%,进一步说明本实例制备的微球尺寸均一,单分散性良好(图2b)。
80.实施例2
81.一种可载药单分散碳酸钙-明胶复合栓塞微球,其制备方法包括以下步骤:
82.s1、搭建微通道反应器,具体包括:
83.s1-1、提供一根约7cm长的内径为0.5mm的玻璃点样毛细管和两根约20cm长的透明硅胶软管,将玻璃点样毛细管的两端分别插入两根透明硅胶软管中,插入的深度约为10mm,玻璃点样毛细管作为液滴生成管,玻璃点样毛细管前端和后端连接的透明硅胶软管分别作为流动相输入管和样品接收管;
84.s1-2、将一根32g注射针头穿过透明硅胶软管并插入至玻璃点样毛细管中,注射针头插入玻璃点样毛细管的深度约为10mm(即注射针头末端距离玻璃点样毛细管左端口约10mm),将注射针头作为分散相输入管;
85.s1-3、将注射针头、玻璃点样毛细管以及两根透明硅胶软管上与玻璃点样毛细管连接的部分放置在载玻片上,并用ab胶密封连接处进行固定,搭建得到微通道反应器,其结构如图1所示。
86.s2、制备到含碳酸钙纳米粒的明胶水溶液,作为分散相;
87.s2-1、制备碳酸钙纳米悬浮液:
88.s2-1-1、将分子量为2kda的聚丙烯酸和(0.5m)和氯化钙(0.5m)溶解于50ml的去离子水中,常温下搅拌1h,得到混合液;
89.s2-1-2、将碳酸钠(0.5m)溶解于50ml的去离子水中,然后将得到的碳酸钠溶液加入到步骤s2-1-1得到的混合液中,常温下搅拌1h;
90.s2-1-3、反应结束后,12000rpm下高速离心10min,收集沉淀物并用去离子水洗涤3次,然后将沉淀物重新分散于去离子水中,得到浓度为5mg/ml的碳酸钙纳米混悬液;
91.s2-2、将300mg明胶加入到3ml步骤s2-1-3所制得的碳酸钙纳米混悬液中,热至至55℃并搅拌,使明胶完全溶解,制备得到含碳酸钙纳米粒的明胶水溶液,即分散相。
92.s3、制备流动相:
93.取50ml液体石蜡,向其中加入5g乳化剂span 80,室温搅拌均匀使乳化剂溶解,得到流动相。
94.s4、制备碳酸钙-明胶液滴;
95.s4-1、将步骤s2制备的分散相和步骤s3制备的流动相分别装入注射器中,将装有分散相的注射器与分散相输入管连接,将装有流动相的注射器加热至55℃后与流动相输入管连接,控制分散相以5-50μl/min的流速、流动相以100-700μl/min的流速注入液滴生成管,使分散相在液滴生成管中被流动相剪切,不断生成w/o型碳酸钙-明胶液滴。
96.该步骤中共进行四组实验,各组实验中均控制分散相的流量均为30μl/min,第一~第四组实验分别控制流动相的流量为5,15,20和30μl/min。
97.s5、利用收集的碳酸钙-明胶液滴制备得到碳酸钙-明胶复合栓塞微球。
98.s5-1、通过含有20ml流动相的玻璃瓶收集样品接收管排出的经步骤s4制得的碳酸钙-明胶液滴,连续收集30min,在收集过程中使玻璃瓶处于冰浴条件下,并对碳酸钙-明胶液滴施加低速搅拌,使其冷凝成胶以及防止凝胶微球相互之间产生粘连;
99.s5-2、向步骤s5-1得到的混合物中加入0.5ml浓度为25%的戊二醛使明胶发生反应交联,搅拌反应6h,即得碳酸钙-明胶复合栓塞微球粗品;
100.s5-3、将步骤s5-2得到的碳酸钙-明胶复合栓塞微球粗品在1000rpm下离心10min,取沉淀,用体积分数分别为50%、70%和100%的异丙醇依次洗涤沉淀,以除去残留的流动相和交联剂;
101.s5-4、将步骤s5-3得到的产物自然风干,即得碳酸钙-明胶复合栓塞微球。
102.采用光学显微镜对本实施例制备的的第一~第四组碳酸钙-明胶复合栓塞微球的形态进行表征。结果显示,采用微流控技术制备的碳酸钙-明胶复合栓塞微球形态完整、粒径均一,平均粒径随着分散相流速的增加有上升的趋势(图3a)。
103.采用image j软件对对本实施例制备的的第一~第四组碳酸钙-明胶复合栓塞微球进行粒径统计,并进一步计算微球的变异系数(cv)。结果显示,当分散相流速从5,15,20增加到30μl/min,碳酸钙-明胶复合栓塞微球的平均粒径从88.2
±
3.7,105.7
±
3.2,112.7
±
4.4增加到132.3
±
5.0μm,但cv值均不超过5%,进一步说明本实例制备的微球尺寸均一,单分散性良好(图3b)。
104.实施例3单分散碳酸钙-明胶复合栓塞微球的栓塞效果测试
105.按照实施例1第三组实验组的方法(分散相的流量为10μl/min、流动相的流量为300μl/min)制备单分散碳酸钙-明胶复合栓塞微球,采用新西兰大白兔肾栓塞模型考察微球的体内栓塞效果。取新西兰大耳白兔,术前禁食12h。首先通过耳缘静脉注射戊巴比妥钠溶液使兔子麻醉,清理兔右侧腹股沟毛发并消毒,然后按照无菌手术的原则切开腹股沟皮肤,在右股动脉处切开小口。接着,在数字减影血管造影仪(dsa)帮助下,将微导管经切开的小口进入到肾动脉入口处,通过注射碘海醇溶液对微球栓塞前的肾动脉进行血管造影。随后,将分散于生理盐水中的单分散碳酸钙-明胶复合栓塞微球经微导管注入微球至左肾,同时灌注碘海醇溶液进行栓塞造影,栓塞终点为造影时未见明显血管。由图4a和4b可知,栓塞前注射碘海醇可以清晰的看到左肾血管,但是微球栓塞后再次注射碘海醇,左肾血管消失,说明左肾的肾动脉被单分散碳酸钙-明胶复合栓塞微球完全栓塞。栓塞后第14天,采用ct血管造影技术观察碳酸钙-明胶复合栓塞微球的长期栓塞效果。如图4c所示,未栓塞的右肾清晰可见,而栓塞的左肾消失不见,说明单分散碳酸钙-明胶复合栓塞微球对肾动脉具有良好的长期栓塞效果。同时,将栓塞后14天的肾脏取出拍照,发现栓塞后的左肾呈白色,说明左肾发生严重缺血性梗死(如图4d所示)。进一步将收集的肾脏组织做h&e染色,结果(图4e和4f)可见复合单分散碳酸钙-明胶复合栓塞微球栓塞后的左肾有明显凝固性坏死表现,而未栓塞的右肾无明显变化,进一步说明单分散碳酸钙-明胶复合栓塞微球具有良好的栓塞效果。
106.实施例4
107.一种载药栓塞微球,包括实施例1或实施例2的可载药单分散碳酸钙-明胶复合栓塞微球以及负载于该微球上的药物,所述药物包括阿霉素、表柔比星、顺铂和吉西他滨中的一种或几种。
108.实施例5单分散碳酸钙-明胶复合栓塞微球对阿霉素的载药效能测试
109.按照实施例1第三组实验组的方法(分散相的流量为10μl/min、流动相的流量为300μl/min)制备单分散碳酸钙-明胶复合栓塞微球。
110.以同法制备单分散普通明胶微球(不含碳酸钙纳米粒)为对照,单分散普通明胶微球的制备方法为:
111.s1、搭建微通道反应器,与实施例1相同。
112.s2、制备单分散普通明胶复合栓塞微球,具体包括如下步骤:
113.s2-1、将300mg明胶加入到3ml去离子水中,加热至55℃并搅拌,使明胶完全溶解,制备得到明胶水溶液,即分散相;
114.s2-2、量取50ml液体石蜡,加入5g span 80,室温搅拌使其溶解,即形成流动相;
115.s2-3、将步骤s2-1所制备的分散相和步骤s2-2所制备的流动相分别装入注射器中,将装有分散相的注射器与分散相输入管连接,将装有流动相的注射器加热至55℃后与流动相输入管连接,控制分散相和流动相的流速分别为10μl/min和300μl/min,使分散相经微通道反应器中被流动相剪切,不断生成尺寸均一的w/o型明胶液滴;
116.s2-4:通过含有20ml流动相的玻璃瓶收集样品接收管排出的经步骤s2-3制得的碳酸钙-明胶液滴,连续收集30min,在收集过程中使玻璃瓶处于冰浴条件下,并对碳酸钙-明胶液滴施加低速搅拌,使其冷凝成胶以及防止凝胶微球相互之间产生粘连;
117.s2-5:在步骤s2-4得到的混合物体系中加入0.5ml浓度为25%的戊二醛使明胶发生反应交联,搅拌反应6h,即得普通明胶栓塞微球粗品;
118.s026:将步骤s2-5所得的明胶栓塞微球粗品1000rpm下离心10min,取沉淀,将所获的的沉淀物用体积分数为50%、70%和100%的异丙醇依次洗涤3次,以除去残留的流动相和交联剂
119.s027:将步骤s026获得的产物自然风干,得到单分散普通明胶栓塞微球。
120.经测定,按照本实施例方法制备得到的单分散普通明胶栓塞微球的平均粒径是131.7
±
4.1μm,cv值为3.1%。
121.然后采用紫外分光光度法检测单分散碳酸钙-明胶复合栓塞微球和单分散普通明胶微球对阿霉素的载药效能。
122.具体步骤为:精密称取20mg的微球样品,置于1.5ml离心管,每管分别加入0.4ml浓度为2.5,5,7.5和10mg/ml的阿霉素水溶液;随后,将上述离心管置于超声波清洗器,水浴超声10min使微球充分分散于阿霉素水溶液中,1500rpm低速离心10min后收集上清液,用ph7.4 pbs溶液洗涤微球3次以除去未包载的阿霉素,离心,合并上清液,采用紫外分光光度法测定上清液在480nm处的吸光度,将吸光度值代入标准曲线方程式计算上清液中阿霉素的含量,并进一步计算微球对阿霉素的载药量:载药量=(载药前阿霉素的投入量-上清液中阿霉素的含量)/载药微球的重量
×
100%。
123.经测定,当阿霉素溶液的浓度为2.5,5,7.5和10mg/ml时,单分散碳酸钙-明胶复合栓塞微球对阿霉素的载药量分别为4.46
±
0.17%,8.39
±
0.15%,12.18
±
0.11%和15.8
±
0.19%,明显高于单分散普通明胶微球的1.71
±
0.23%,3.16
±
0.40%,4.49
±
0.36,和6.06
±
0.57%(图5)。这一结果也证实将碳酸钙纳米粒引入到单分散明胶微球体系中能有效解决现有明胶栓塞微球载药量过低的问题。
124.实施例6单分散碳酸钙-明胶复合栓塞微球对调节肿瘤微酸环境、提高体外抗肿瘤效能的测定
125.按照实施例1第三组实验组的方法制备单分散碳酸钙-明胶复合栓塞微球,采用
mtt法考察单分散碳酸钙-明胶复合栓塞微球是否能逆转乳酸引起的化疗抵抗。具体步骤如下:精密称取微球样品200mg,置于4ml含有20mm乳酸的dmem培养基中,37℃静置24h,离心取上清液,并将所得的上清液过滤除菌,备用;将lm3肝癌细胞常规消化,以1
×
104个/孔的密度接种于96孔细胞板,每孔体积约0.2ml;孵育24h待细胞完全贴壁后,将细胞板中培养基更换成等体积的新鲜培养基、含20mm乳酸的新鲜培养基或上述微球处理过的培养基;待细胞赋予1h后,将5μl不同浓度的游离阿霉素溶液加入到上述3组实验细胞中(药物最终浓度分别为0.5,1,2,4,8和16μg/ml),每组设3个平行孔;孵育24h后,每孔加mtt溶液200μl(5mg/ml),继续培养4h,弃上清液,每孔加dmso 200μl,采用酶标仪测定570nm处各孔吸光度a,计算细胞存活率。
126.如图6所示,可以看出,乳酸的存在可以显著降低阿霉素对肿瘤细胞的杀伤能力,表明乳肿瘤酸性微环境可以导致化疗抵抗。当含乳酸培养基经单分散碳酸钙-明胶复合栓塞微球处理后,阿霉素对肿瘤细胞的杀伤作用明显提高,细胞的死亡率与正常培养基组相当。这一结果也表明,单分散碳酸钙-明胶复合栓塞微球能有效清除乳酸,从而逆转诊疗酸性微环境下的化疗抵抗,进而能为实现更为高效的肝癌tace治疗提供可能。
127.尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。