一种clusterin在肝硬化不同进展阶段的应用
技术领域
1.本发明属于生物医药化学技术领域,尤其涉及一种载脂蛋白clusterin在肝硬化不同进展阶段的应用。
背景技术:
2.目前,肝脏纤维化是一种由嗜肝病毒(如hbv,hcv)、酒精、药物、自身免疫性疾病以及遗传性代谢缺陷等因素引起的慢性肝脏疾病,脂肪肝、肝癌等多种肝脏疾病都伴有纤维化的发生。肝纤维化的主要病理特征为炎症反应,肝脏中多种细胞发生病变,细胞外基质(extracellular matrix,ecm)大量沉积。这些胞外基质主要包括纤连蛋白(fibronectin)、层粘连蛋白(laminins)、透明质酸(hyaluronan)以及多种胶原蛋白等。ecm蛋白持续积累形成纤维性瘢痕,再生的肝细胞结节形成假小叶结构,最终发展为肝硬化。肝硬化引起肝细胞功能障碍,并增加肝内血流阻力,分别导致肝功能不全和门静脉高压症,严重危害人类健康。目前,临床上治疗肝纤维化的方法主要有:针对原发病因去除致病因素,如抗病毒药物、戒酒等;针对肝脏损伤,常用抗炎药物或者辅助肝脏代谢治疗。尽管目前已经有大量的关于肝纤维化的病理及机制研究成果,并在动物模型的临床前试验取得了一些成功,像欧洲,美国等正在进行一些抗纤维化药物的临床i及ii期实验,但至今为止还没有一个明确的药理化合物可用于临床实践。
3.因此,有效的抗纤维化药物治疗将是慢性肝病患者的福音,即使在慢性肝病晚期,一定程度上缓解纤维化进程也可帮助患者达到更好临床治疗效果,带来巨大的经济利益和社会效益。
4.目前,特异缓解肝纤维化本身的药物较少,重要原因就是对人肝纤维化发生发展的细胞分子机制认识不够。另一方面,准确的检测肝纤维化程度和监测纤维化发展动态有助于治疗肝脏纤维化。组织活检技术是诊断肝脏纤维化的金标准,但是该方法会导致机体创伤、不能准确反应整个组织纤维化程度等明显缺陷。更重要的是,早期轻度肝纤维化的病人一般不会去做组织活检,错过了最佳治疗时机。影像学检测(包括核磁共振、增强ct等)是无创诊断的代表方法,但是不能精确对纤维化程度进行分级以及不能动态监测治疗程度。从20世纪90年代证实肝纤维化是可逆的以来,研究人员一直在努力寻找抗纤维化治疗方法。然而,迄今为止治疗肝纤维化的最有效疗法仍然是去除致病因子,而这还不足以有效地改善所有肝纤维化/肝硬化患者的临床表征。因此,迫切需要在建立去除致病因子的条件下再开发特异性抗纤维化药物。
5.通过上述分析,现有技术存在的问题及缺陷为:
6.(1)组织活检技术会导致机体创伤、不能准确反应整个组织纤维化程度。
7.(2)影像学检测不能精确对纤维化程度进行分级且不能动态监测治疗程度。
8.(3)去除致病因子方法不能有效改善所有肝纤维化/肝硬化患者的临床表征。
技术实现要素:
9.针对现有技术存在的问题,本发明提供了一种载脂蛋白clusterin在肝硬化不同进展阶段的应用。
10.本发明是这样实现的,一种载脂蛋白clusterin在制备肝硬化不同进程的生物学诊断试剂盒中的应用。
11.本发明的另一目的在于提供一种载脂蛋白clusterin在制备用于慢性肝病抗纤维化药物中的应用。
12.本发明的另一目的在于提供一种血清中clusterin蛋白含量在作为判断肝纤维化进程的潜在血清诊断标志物中的应用。
13.本发明的另一目的在于提供一种鉴定载脂蛋白clusterin在肝硬化不同进展阶段应用的方法,所述鉴定载脂蛋白clusterin在肝硬化不同进展阶段应用的方法包括以下步骤:
14.步骤一,对肝纤维化发生过程中clusterin蛋白的表达变化特征进行分析;
15.步骤二,确定clu-/-基因敲除小鼠中肝纤维化发生各个时间段的特征变化;
16.步骤三,分析人clusterin重组蛋白在clu-/-肝纤维小鼠中的作用;
17.步骤四,分析人clusterin重组蛋白在野生型肝纤维小鼠中的作用;
18.步骤五,aav8-clusterin过表达小鼠中评价clusterin蛋白对肝纤维化的作用。
19.进一步,所述步骤一中的分析肝纤维化发生过程中clusterin蛋白的表达变化特征包括:
20.(1)建立小鼠肝纤维化模型
21.腹腔注射ccl4试剂,每只小鼠注射2μl/g的ccl4试剂,每周注射2次,分别于造模2、4、6、8周收集小鼠肝脏组合和血清进行检测;通过he、天狼星红染色、masson染色和血清羟脯氨酸含量判断不同时间点肝脏纤维化程度;通过westernblot检测col-1、α-sma蛋白表达水平确定不同肝纤维化程度下胞外蛋白基质沉淀情况。
22.(2)clusterin蛋白在不同肝纤维化阶段的表达变化
23.取纤维化造模2、4、6、8周的小鼠肝脏组织,通过clusterin蛋白的抗体染色,分析clusterin蛋白表达水平与肝纤维化进展的相关性;通过肝细胞、胆管细胞特异性标志物如ck19、hnf4a与clu蛋白抗体的共染色,判断在纤维化发生过程中clusterin蛋白由哪些细胞产生以及产生的区域。
24.(3)clusterin蛋白在人肝硬化肝脏中的表达变化
25.取正常人和肝纤维化患者肝脏组织标本,进行原位clusterin蛋白的抗体染色和天狼猩红染色,比较clusterin蛋白的表达变化。
26.进一步,所述步骤(1)中的ccl4试剂中的ccl4和橄榄油的比例为1:4。
27.进一步,所述步骤二中的确定clu-/-基因敲除小鼠中肝纤维化发生各个时间段的特征变化包括:
28.与野生型小鼠一样,建立clu-/-小鼠肝纤维化模型,分别于造模2、4、6、8周收集小鼠肝脏组合和血清进行检测;采用肝纤维化相关标志物检测分析clu-/-小鼠肝纤维化的发展进程。
29.进一步,所述步骤三中的分析人clusterin重组蛋白在clu-/-肝纤维小鼠中的作
用包括:
30.(1)clu-/-小鼠肝纤维化建模2周,随机分成两组;
31.(2)从肝纤维化建模开始,尾静脉分别注射100μl生理盐水和浓度为10μg/100μl的人重组clusterin蛋白,一周2次,共注射4次;
32.(3)建模2周后,收集肝脏组织和小鼠血清;通过he、天狼星红、masson染色和血清羟脯氨酸含量分析人重组clusterin蛋白对肝纤维化逆转的作用。
33.进一步,所述步骤四中的分析人clusterin重组蛋白在野生型肝纤维小鼠中的作用包括:
34.(1)野生型小鼠肝纤维化建模2周后,随机分成两组;
35.(2)在四氯化碳造模2周后,从第3周起尾静脉分别注射100μl生理盐水和浓度为30μg/100μl的人重组clusterin蛋白,一周2次,共注射4次;
36.(3)继续造模2周后,收集肝脏组织和小鼠血清;通过he、天狼星红、masson染色和血清羟脯氨酸含量分析人重组clusterin蛋白是否可延缓肝纤维化发生进程。
37.进一步,所述步骤五中的aav8-clusterin过表达小鼠中评价clusterin蛋白对肝纤维化的作用包括:
38.构建clusterin腺相关病毒,病毒滴度按1
×
10
11
gc/只鼠,稀释成100μl体积进行尾静脉注射野生型小鼠,尾静脉注射3周后开始进行肝纤维化造模;建模4周后,收集肝脏组织和小鼠血清;通过he、天狼星红、masson染色和血清羟脯氨酸含量分析clusterin蛋白对肝纤维化的作用。
39.结合上述的技术方案和解决的技术问题,请从以下几方面分析本发明所要保护的技术方案所具备的优点及积极效果为:
40.第一、针对上述现有技术存在的技术问题以及解决该问题的难度,紧密结合本发明的所要保护的技术方案以及研发过程中结果和数据等,详细、深刻地分析本发明技术方案如何解决的技术问题,解决问题之后带来的一些具备创造性的技术效果。具体描述如下:
41.本发明通过对clusterin蛋白在肝纤维化形成和逆转中的表达变化和作用的分析,1)确定clusterin蛋白在肝纤维化发生过程中的表达变化规律,可以通过血清clusterin蛋白的含量来判断肝组织纤维化的程度,可以解决目前临床肝纤维化疾病早期难诊断的难题;而且更为重要的是将clusterin蛋白作为潜在的血清诊断标志物,使肝纤维化疾病的无创性诊断成为可能。2)对于肝纤维化发展到纤维肝纤维化期甚至肝硬化时期的患者,可以通过静脉注射临床级人重组clusterin蛋白而进行抗纤维化治疗,从而逆转或者延缓肝纤维的发展。
42.本发明将血清中clusterin蛋白含量作为判断肝纤维化进程的潜在血清诊断标志物,通过提高肝脏组织或者血清clusterin蛋白含量可以作为治疗肝纤维化的有效方案。
43.第二,把技术方案看做一个整体或者从产品的角度,本发明所要保护的技术方案具备的技术效果和优点,具体描述如下:
44.本发明的技术方案明确了载脂蛋白clusterin(clu)在肝脏纤维化发生中的变化规律,阐明了其在逆转肝纤维化中的作用,并建立了肝硬化不同进程的生物学诊断试剂盒以及肝纤维治疗的救治方案。
附图说明
45.为了更清楚地说明本发明实施例的技术方案,下面将对本发明实施例中所需要使用的附图做简单的介绍,显而易见地,下面所描述的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下还可以根据这些附图获得其他的附图。
46.图1是本发明实施例提供的clusterin蛋白随着小鼠慢性肝纤维化的发生而表达增加的示意图;
47.图1a~d是本发明实施例提供的造模0周、1周、2周、4周肝组织切片天狼星红染色示意图;
48.图1e~h是本发明实施例提供的造模0周、1周、2周、4周肝组织切片clu免疫组化染色示意图;
49.图2是本发明实施例提供的肝脏组织和血清学检测进一步明确clusterin蛋白的表达随着肝纤维化的发生而增加的示意图;
50.图2a是本发明实施例提供的western blot显示正常对照组及造模1周、2周、4周组肝组织clu蛋白表达情况示意图;
51.图2b是本发明实施例提供的elisa显示正常对照小鼠及造模造模1周、2周、4周组血清中clu蛋白浓度示意图;**p《0.01,***p《0.001;
52.图3是本发明实施例提供的clusterin蛋白在正常和纤维化肝脏组织中的表达定位,肝纤维化发生后损伤肝细胞表达clu蛋白示意图;
53.图3a~f是本发明实施例提供的clu蛋白与肝细胞标志物(hnf4a、gs)和胆管细胞标志物ck19的共染结果示意图;
54.图3g~l是clu蛋白与肝细胞标志物(fah)、胆管细胞标志物ck19和肝星状细胞a-sma的共染结果示意图;
55.图4是本发明实施例提供的clusterin蛋白在肝硬化组织高表达示意图;
56.图4a~b是本发明实施例提供的正常和肝硬化肝组织中天狼星红染色示意图;
57.图4c~d是本发明实施例提供的正常和肝硬化肝组织中clusterin蛋白免疫硬化染色示意图,标尺:200μm;
58.图5是本发明实施例提供的clusterin基因敲除后加速四氯化碳诱导的肝脏纤维化示意图;
59.图5a~b是本发明实施例提供的正常小鼠(a)和clu-/-小鼠(b)在四氯化碳造模0、2、4、6周后肝组织切片天狼星红染色示意图;
60.图6是本发明实施例提供的肝纤维化相关蛋白的表达水平检测进一步证明clusterin基因敲除后加速肝脏纤维化进程的示意图;
61.图6a是本发明实施例提供的western blot检测对照组与clu-/-小鼠在损伤后有关纤维化的α-sma和col-1蛋白表达示意图;
62.图6b是本发明实施例提供的α-sma和col-1蛋白表达水平的分析示意图;*p《0.05,**p《0.01;
63.图7是本发明实施例提供的野生型小鼠过表达clusterin基因可以缓解肝纤维化程度的示意图;
64.图7a~b是本发明实施例提供的aav-gfp和aav-clu组肝组织切片天狼星红染色示意图;
65.图7c~d是本发明实施例提供的aav-gfp和aav-clu组肝组织切片α-sma免疫组化染色示意图;
66.图7e是本发明实施例提供的a和b阳性染色区域统计结果示意图;
67.图7f是本发明实施例提供的c和d阳性染色区域统计结果示意图;**p《0.01,***p《0.001;
68.图8是本发明实施例提供的人重组clusterin(hrapoj)静脉给药可缓解肝纤维化疾病示意图;
69.图8a是本发明实施例提供的clu-/-小鼠肝纤维化造模和给予hrapoj蛋白的方式计划图;
70.图8b是本发明实施例提供的在clu-/-小鼠发生肝纤维化过程中给予不用剂量人重组clusterin蛋白后血清羟脯氨酸的浓度示意图;
71.图8c是本发明实施例提供的在clu-/-小鼠发生肝纤维化过程中给予不用剂量人重组clusterin蛋白的肝组织切片天狼星红染色及其统计图;
72.图8d是本发明实施例提供的野生型小鼠肝纤维化造模和给予hrapoj蛋白的方式计划图,小鼠先进行肝纤维化造模再进行人源重组蛋白注射;
73.图8e是本发明实施例提供的野生型小鼠发生肝纤维化过程中给予不用剂量人重组clusterin蛋白后血清羟脯氨酸的浓度示意图;
74.图8f是野生型小鼠发生肝纤维化过程中给予不用剂量人重组clusterin蛋白的肝组织切片天狼星红染色及其统计图;
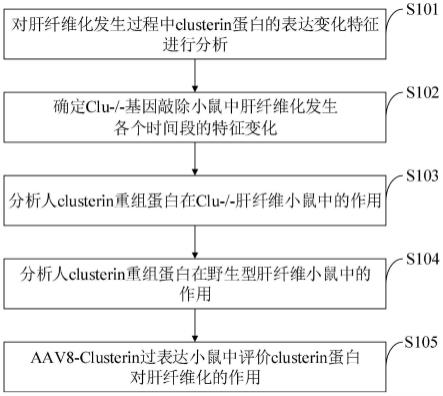
75.图9是本发明实施例提供的鉴定载脂蛋白clusterin在肝硬化不同进展阶段应用的方法流程图。
具体实施方式
76.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
77.针对现有技术存在的问题,本发明提供了一种clusterin在肝硬化不同进展阶段的应用,下面结合附图对本发明作详细的描述。
78.一、解释说明实施例。为了使本领域技术人员充分了解本发明如何具体实现,该部分是对权利要求技术方案进行展开说明的解释说明实施例。
79.如图9所示,本发明实施例提供的鉴定载脂蛋白clusterin在肝硬化不同进展阶段应用的方法包括以下步骤:
80.s101,对肝纤维化发生过程中clusterin蛋白的表达变化特征进行分析;
81.s102,确定clu-/-基因敲除小鼠中肝纤维化发生各个时间段的特征变化;
82.s103,分析人clusterin重组蛋白在clu-/-肝纤维小鼠中的作用;
83.s104,分析人clusterin重组蛋白在野生型肝纤维小鼠中的作用;
84.s105,aav8-clusterin过表达小鼠中评价clusterin蛋白对肝纤维化的作用。
85.一、肝纤维化发生过程中clusterin蛋白的表达变化特征
86.1)建立小鼠肝纤维化模型
87.腹腔注射ccl4试剂(ccl4:橄榄油比例为1:4),每只小鼠注射2μl/g的ccl4试剂,每周注射2次,分别于造模2、4、6、8周收集小鼠肝脏组合和血清进行检测;通过he、天狼星红染色、masson染色和血清羟脯氨酸含量来判断不同时间点肝脏纤维化程度;通过western blot检测col-1、α-sma蛋白表达水平确定不同肝纤维化程度下胞外蛋白基质沉淀情况。
88.2)clusterin蛋白在不同肝纤维化阶段的表达变化
89.取纤维化造模2、4、6、8周的小鼠肝脏组织,通过clusterin蛋白的抗体染色,分析clusterin蛋白表达水平与肝纤维化进展的相关性。其次,通过肝细胞、胆管细胞特异性标志物如ck19、hnf4a与clu蛋白抗体的共染色,判断在纤维化发生过程中clusterin蛋白由哪些细胞产生以及产生的区域。
90.3)clusterin蛋白在人肝硬化肝脏中的表达变化
91.取正常人和肝纤维化患者肝脏组织标本,进行原位clusterin蛋白的抗体染色和天狼猩红染色,比较clusterin蛋白的表达变化。
92.二、clu-/-基因敲除小鼠中肝纤维化发生各个时间段的特征变化
93.与野生型小鼠一样,建立clu-/-小鼠肝纤维化模型,分别于造模2、4、6、8周收集小鼠肝脏组合和血清进行检测;采用肝纤维化相关标志物检测分析clu-/-小鼠肝纤维化的发展进程。
94.三、人clusterin重组蛋白在clu-/-肝纤维小鼠中的作用
95.1、clu-/-小鼠肝纤维化建模2周,随机分成两组;
96.2、从肝纤维化建模开始,尾静脉分别注射100μl生理盐水和人重组clusterin蛋白(10μg/100μl),一周2次,共注射4次;
97.3、建模2周后,收集肝脏组织和小鼠血清。通过he、天狼星红、masson染色和血清羟脯氨酸含量分析人重组clusterin蛋白对肝纤维化逆转的作用。
98.四、人clusterin重组蛋白在野生型肝纤维小鼠中的作用
99.1、野生型小鼠肝纤维化建模2周后,随机分成两组;
100.2、在四氯化碳造模2周后,从第3周起尾静脉分别注射100μl生理盐水和人重组clusterin蛋白(30μg/100μl),一周2次,共注射4次;
101.3、继续造模2周后,收集肝脏组织和小鼠血清。通过he、天狼星红、masson染色和血清羟脯氨酸含量分析人重组clusterin蛋白是否可延缓肝纤维化发生进程。
102.五、aav8-clusterin过表达小鼠中评价clusterin蛋白对肝纤维化的作用
103.构建clusterin腺相关病毒,病毒滴度按1
×
10
11
gc/只鼠,稀释成100μl体积进行尾静脉注射野生型小鼠,尾静脉注射3周以后,开始进行肝纤维化造模。建模4周后,收集肝脏组织和小鼠血清。通过he、天狼星红、masson染色和血清羟脯氨酸含量分析clusterin蛋白对肝纤维化的作用。
104.本发明通过对clusterin蛋白在肝纤维化形成和逆转中的表达变化和作用研究,1)确定clusterin蛋白在肝纤维化发生过程中的表达变化规律,可以通过血清clusterin蛋白的含量来判断肝组织纤维化的程度,可以解决目前临床肝纤维化疾病早期难诊断的难题;而且更为重要的是将clusterin蛋白作为潜在的血清诊断标志物,使肝纤维化疾病的无
创性诊断成为可能。2)对于肝纤维化发展到纤维肝纤维化期甚至肝硬化时期的患者,可以通过静脉注射临床级人重组clusterin蛋白而进行抗纤维化治疗,从而逆转或者延缓肝纤维的发展。
105.图1是clusterin蛋白随着小鼠慢性肝纤维化的发生而表达增加。图1a~d是造模0周、1周、2周、4周肝组织切片天狼星红染色。图1e~h是造模0周、1周、2周、4周肝组织切片clu免疫组化染色。
106.图2是肝脏组织和血清学检测进一步明确clusterin蛋白的表达随着肝纤维化的发生而增加。图2a是western blot显示正常对照组及造模1周、2周、4周组肝组织clu蛋白表达情况。图2b是elisa显示正常对照小鼠及造模造模1周、2周、4周组血清中clu蛋白浓度。**p《0.01,***p《0.001。
107.图3是clusterin蛋白在正常和纤维化肝脏组织中的表达定位,肝纤维化发生后损伤肝细胞表达clu蛋白。图3a~f是clu蛋白与肝细胞标志物(hnf4a、gs)和胆管细胞标志物ck19的共染,结果表明在正常肝脏中,clu蛋白只有在胆管细胞中有表达。图3g~l是clu蛋白与肝细胞标志物(fah)、胆管细胞标志物ck19和肝星状细胞a-sma的共染,结果表明肝纤维化发生过程中,由中央静脉区的肝细胞表达clu蛋白。
108.图4是clusterin蛋白在肝硬化组织高表达。图4a~b是正常和肝硬化肝组织中天狼星红染色。图4c~d是正常和肝硬化肝组织中clusterin蛋白免疫硬化染色。绿色显示clusterin蛋白表达阳性。标尺:200μm。
109.图5是clusterin基因敲除后加速四氯化碳诱导的肝脏纤维化。图5a~b是正常小鼠(a)和clu-/-小鼠(b)在四氯化碳造模0、2、4、6周后肝组织切片天狼星红染色。
110.图6是肝纤维化相关蛋白的表达水平检测进一步证明clusterin基因敲除后加速肝脏纤维化进程。图6a是western blot检测对照组与clu-/-小鼠在损伤后有关纤维化的α-sma和col-1蛋白表达。图6b是α-sma和col-1蛋白表达水平的分析。*p《0.05,**p《0.01。
111.图7是野生型小鼠过表达clusterin基因可以缓解肝纤维化程度。图7a~b是aav-gfp和aav-clu组肝组织切片天狼星红染色。图7c~d是aav-gfp和aav-clu组肝组织切片α-sma免疫组化染色。图7e是a和b阳性染色区域统计结果。图7f是c和d阳性染色区域统计结果。**p《0.01,***p《0.001。
112.图8是人重组clusterin(hrapoj)静脉给药可缓解肝纤维化疾病。图8a是clu-/-小鼠肝纤维化造模和给予hrapoj蛋白的方式计划图。图8b是在clu-/-小鼠发生肝纤维化过程中给予不用剂量人重组clusterin蛋白后血清羟脯氨酸的浓度。图8c是在clu-/-小鼠发生肝纤维化过程中给予不用剂量人重组clusterin蛋白的肝组织切片天狼星红染色及其统计图,结果显示静脉注射15μg/只小鼠hrapoj即可缓解肝纤维化。图8d是野生型小鼠肝纤维化造模和给予hrapoj蛋白的方式计划图,小鼠先进行肝纤维化造模再进行人源重组蛋白注射。图8e是野生型小鼠发生肝纤维化过程中给予不用剂量人重组clusterin蛋白后血清羟脯氨酸的浓度。图8f是野生型小鼠发生肝纤维化过程中给予不用剂量人重组clusterin蛋白的肝组织切片天狼星红染色及其统计图,结果显示即使已经发生肝纤维化,再静脉给予25μg/只小鼠hrapoj也可缓解肝纤维化。
113.二、应用实施例。为了证明本发明的技术方案的创造性和技术价值,该部分是对权利要求技术方案进行具体产品上或相关技术上的应用实施例。
114.本发明的应用实施例提供了一种载脂蛋白clusterin在制备肝硬化不同进程的生物学诊断试剂盒中的应用。
115.本发明的应用实施例提供了一种载脂蛋白clusterin在制备用于慢性肝病抗纤维化药物中的应用。
116.本发明的应用实施例提供了一种血清中clusterin蛋白含量在作为判断肝纤维化进程的潜在血清诊断标志物中的应用。
117.本发明通过对clusterin蛋白在肝纤维化形成和逆转中的表达变化和作用的分析,确定clusterin蛋白在肝纤维化发生过程中的表达变化规律,可以通过血清clusterin蛋白的含量来判断肝组织纤维化的程度,可以解决目前临床肝纤维化疾病早期难诊断的难题;而且更为重要的是将clusterin蛋白作为潜在的血清诊断标志物,使肝纤维化疾病的无创性诊断成为可能。对于肝纤维化发展到纤维肝纤维化期甚至肝硬化时期的患者,可以通过静脉注射临床级人重组clusterin蛋白而进行抗纤维化治疗,从而逆转或者延缓肝纤维的发展。
118.本发明将血清中clusterin蛋白含量作为判断肝纤维化进程的潜在血清诊断标志物,通过提高肝脏组织或者血清clusterin蛋白含量可以作为治疗肝纤维化的有效方案。本发明的技术方案明确了载脂蛋白clusterin(clu)在肝脏纤维化发生中的变化规律,阐明了其在逆转肝纤维化中的作用,并建立了肝硬化不同进程的生物学诊断试剂盒以及肝纤维治疗的救治方案。
119.以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,都应涵盖在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
