用于诊断病毒感染的方法、试剂盒和系统中的诊断肽
发明领域
1.本发明涉及用于体外诊断病毒感染的方法、体外诊断对象病毒感染的方法、用于检测对象存在感染的试剂盒,以及用于检测对象存在感染的系统中的诊断肽,其中所述方法包括提供体液样品。
背景技术:
2.对患者中病毒感染的改进诊断方法的临床需求日益增加。快速检测和鉴定病毒病原体对于限制病毒性疾病的转移和传播以及监测治疗方法至关重要。围绕2019/2020年全球大流行sars相关冠状病毒的事件可以说明对此类方法的需求。
3.sars是由sars相关冠状病毒(sars-cov)引起的病毒性呼吸系统疾病。sars于2003年2月在亚洲被首次报道。2019/20年,sars-cov-19大流行在全球造成》600,000人死亡。
4.sars冠状病毒属于与引起普通感冒的病毒相似的一组病毒。sars病毒通过人与人之间的密切接触传播,且被认为最容易通过感染者咳嗽或打喷嚏时产生的呼吸道飞沫传播。当来自感染者的飞沫在空气中被推动一小段距离(通常多达3英尺)并沉积在附近人的黏膜上时,就会发生飞沫传播。当一个人触摸被传染性飞沫污染的表面,然后触摸他或她的嘴、鼻子或眼睛时,病毒也会传播。
5.实时逆转录酶-pcr(rt-pcr)检测由于其作为特异性和简单的定量测定的优势,目前被青睐用于检测冠状病毒。此外,实时rt-pcr比常规的rt-pcr测定更敏感,这对早期感染的诊断有很大帮助。因此,实时rt-pcr测定仍然是用于检测包括sars-cov-2在内的各种冠状病毒的主要方法[14]。
[0006]
即便如此,仍需要改进实时rt-pcr测定。由于rt-pcr方法容易受到污染并且需要耗时的样品处理和pcr后分析,因此改进的测定是基于taqman的实时rt-pcr,它可以很容易地在常规诊断环境中实施以进行hcov的检测。此外,为了进一步提高灵敏度,可以使用2种taqman探针而不是1种探针进行sars-cov的实时定量rt-pcr测定。这种使用双taqman探针进行定量的简单修改在非常需要超灵敏性的领域具有广泛的应用,其中sars-cov检测限为每个反应1个拷贝rna。
[0007]
lamp是一种新型的高效等温核酸扩增方法。然而,结果分析通常是通过耗时的凝胶电泳进行的。如果这些方法依赖于非特异性信号转导方案,如荧光染料嵌入到任何双链dna扩增子中,或由于聚合过程中焦磷酸盐的释放导致溶液混浊,则不能排除来源于引物二聚体或非引物反应的非预期信号的可能性,
[0008]
在临床检测中,缺乏安全且稳定的外部阳性对照(epc)可能成为pcr/lamp方法诊断冠状病毒的严重问题。
[0009]
同时,冠状病毒的快速突变特性凸显了准确检测遗传多样化冠状病毒的必要性。
[0010]
需要一种能够识别体液样品中是否存在病毒感染并且可以在护理点进行的快速诊断方法。
[0011]
发明概述
[0012]
本发明提供了用于体外诊断病毒感染的方法中的用途的诊断肽,所述肽由式(i)表示:
[0013]
[a]-[b]-[c]
ꢀꢀ(i)[0014]
其中:
[0015]
[a]是具有650-900nm发射波长的荧光剂,
[0016]
[b]是包含氨基酸序列x
aa1
,x
aa2
,x
aa3
的肽
[0017]
其中x
aa1
是疏水性或碱性氨基酸,
[0018]
其中x
aa2
是极性、中性或碱性氨基酸,
[0019]
其中x
aa3
是极性、中性或碱性氨基酸,
[0020]
[c]是具有650-900nm吸收波长的非荧光剂,以用于淬灭所述荧光剂的所述发射,
[0021]
其中x
aa1
,x
aa2
,x
aa3
代表病毒编码的蛋白酶的切割位点,其中所述切割位点的切割导致从所述肽释放所述非荧光剂,其中所述非荧光剂的释放指示病毒的存在,优选地其中[b]代表基于[a]-[b]-[c]的总质量,按重量计诊断肽总质量的最多30%。
[0022]
在一些司法管辖权内,本发明可以被限定为使用式(i)所示的诊断肽进行体外诊断病毒感染的方法:
[0023]
[a]-[b]-[c]
ꢀꢀ(i)[0024]
其中:
[0025]
[a]是具有650-900nm发射波长的荧光剂,
[0026]
[b]是包含氨基酸序列x
aa1
,x
aa2
,x
aa3
的肽,
[0027]
其中x
aa1
是疏水性或碱性氨基酸,
[0028]
其中x
aa2
是极性、中性或碱性氨基酸,
[0029]
其中x
aa3
是极性、中性或碱性氨基酸,
[0030]
[c]是具有650-900nm吸收波长的非荧光剂,以用于淬灭所述荧光剂的所述发射,
[0031]
其中x
aa1
,x
aa2
,x
aa3
代表病毒编码的蛋白酶的切割位点,其中所述切割位点的切割导致从所述肽释放所述非荧光剂,其中所述非荧光剂的释放指示病毒的存在,优选地其中[b]代表基于[a]-[b]-[c]的总质量,按重量计诊断肽的总质量的最多50%。
[0032]
同样,在一些司法管辖权内,本发明可以被限定为诊断肽在体外诊断病毒感染中的用途,其中所述肽由式(i)表示:
[0033]
[a]-[b]-[c]
ꢀꢀ(i)[0034]
其中:
[0035]
[a]是具有650-900nm发射波长的荧光剂,
[0036]
[b]是包含氨基酸序列x
aa1
,x
aa2
,x
aa3
的肽,
[0037]
其中x
aa1
是疏水性或碱性氨基酸,
[0038]
其中x
aa2
是极性、中性或碱性氨基酸,
[0039]
其中x
aa3
是极性、中性或碱性氨基酸,
[0040]
[c]是具有650-900nm吸收波长的非荧光剂,以用于淬灭所述荧光剂的所述发射,
[0041]
其中x
aa1
,x
aa2
,x
aa3
代表病毒编码的蛋白酶的切割位点,其中所述切割位点的切割导致从所述肽释放所述非荧光剂,其中所述非荧光剂的释放指示病毒的存在,优选地其中[b]代表基于[a]-[b]-[c]的总质量,按重量计诊断肽的总质量的最多50%。
[0042]
本发明还涉及用于诊断对象的病毒感染的体外方法,所述方法包括以下步骤:
[0043]
i)使体液/组织样品与肽接触,所述肽包含具有650-900nm发射波长的荧光剂和用于淬灭所述荧光剂的所述发射的具有650-900nm吸收波长的非荧光剂,以及位于所述荧光剂和第一非荧光剂之间的切割位点,所述切割位点特异性针对病毒蛋白酶,
[0044]
ii)监测来自步骤ii)中所述肽的650-900nm范围内的荧光,
[0045]
其中650-900nm范围内荧光的增加指示样品中病毒蛋白酶的存在。
[0046]
根据本发明,本文所限定的方法能够通过分析体液/组织样本来快速且特异性地检测对象的感染。在识别和切割所述切割位点的病毒蛋白酶存在的情况下,所述第一非荧光剂从试剂中释放出来,结果发出荧光信号,所述信号可以被合适的检测器检测到。令人惊讶地发现,与现有技术方法相比,通过监测650-900nm的波长来检测病毒蛋白酶提供了改进的检测限。所述方法执行简单并且适合于护理点使用。
[0047]
本方法的优点是它可以在体液样品中进行,而不需要通过例如富集步骤来富集细胞计数。结果,本方法能够快速检测病毒感染,例如,在试剂与样品接触的几分钟内。
[0048]
所述方法克服了pcr/lamp方法缺乏安全且稳定的外部阳性对照(epc)的问题。
[0049]
在其它方面,提供了用于诊断对象的病毒感染的试剂盒,其包含:
[0050]
a)包含式(i)的诊断肽的容器,
[0051]
b)用于执行本文所限定的诊断方法的一套说明书。
[0052]
在其它方面,提供了用于诊断对象的病毒感染的系统,其包含:
[0053]
a)用于接收样品的容器,
[0054]
b)包含式(i)的诊断肽的容器,
[0055]
c)适于接收所述容器并监测所述在肽与所述体液样品接触时从所述肽发射的荧光信号的装置。
[0056]
本发明还涉及由式(ib)表示的诊断肽:
[0057]
[a]-[连接子1]-[b]-[-连接子2]-[c](ib)
[0058]
其中:
[0059]
[a]是具有650-900nm发射波长的荧光剂,
[0060]
[b]是包含3-10个氨基酸且具有氨基酸序列x
aa1
,x
aa2
,x
aa3
的肽,
[0061]
其中x
aa1
是组氨酸、精氨酸或赖氨酸,
[0062]
其中x
aa2
是谷氨酰胺,
[0063]
其中x
aa3
是极性、中性或碱性氨基酸,
[0064]
[c]是具有650-900nm吸收波长的非荧光剂,以用于淬灭所述荧光剂的所述发射,
[0065]
[连接子1]和[连接子2]独立地选自任选取代的烃基和非蛋白水解烃基,
[0066]
其中x
aa1
,x
aa2
,x
aa3
代表病毒编码的蛋白酶的切割位点,
[0067]
其中所述切割位点的切割导致从所述肽释放事实是非荧光剂,其中所述非荧光剂的释放指示属于冠状病毒科的病毒的存在,优选地其中所述病毒是sars-cov-2(sars-cov-19)。
[0068]
本发明还涉及使用如本文所限定的诊断肽的方法、用途、试剂盒和系统。
[0069]
实施方案的描述
[0070]
如本文所用的,术语“对象”意指处于感染风险或疑似感染的动物或人类个体。术
语“患者”、“对象”、“个体”等在本文中可互换使用,并且是指适合本文所述方法的任何动物或人。在某些非限制性实施方案中,患者、对象或个体是人。
[0071]
如本文所用的,术语“体液样品”意指从对象分离的生物材料。获得样品的步骤不是本发明的一部分。
[0072]
如本文所用的,术语“病毒蛋白酶”意指由病毒rna编码的肽酶。
[0073]
如本文所用的,术语“蛋白酶”和“肽酶”意指病毒rna编码的多肽,其能够在蛋白质中的切割位点(氨基酸基序)处切割肽键(c(o)nh)。
[0074]
如本文所用的,术语“肽”意指包含至少3个氨基酸的寡聚体。优选地,肽包含不超过20个氨基酸。优选地,肽包含4至20个氨基酸,更优选6至15个氨基酸。在一实施方案中,肽优选包含3至10个氨基酸。所使用的氨基酸可以是任何氨基酸,优选地选自天然存在的氨基酸或合成氨基酸,特别是天然氨基酸的衍生物。优选地,肽包括“非天然氨基酸基序”,其包含病毒蛋白酶的切割位点。如本文所用的,“非天然氨基酸基序”是指非天然存在的序列,即遗传工程化的序列和源自分子建模的序列。
[0075]
如本文所用的,术语“监测(monitoring)”、“测量(measuring/measurement)”、“检测(detecting/detection)”或“诊断(diagnostic)”意指评估临床或来源于对象的样品中的给定物质的存在、不存在、数量或量(其可以是有效量),包括此类物质的定性或定量浓度水平的推导,或以其他方式评估对象临床参数的值或分类。
[0076]
术语“病毒编码的蛋白酶”意指从病毒基因组的遗传信息(rna)翻译而来的蛋白酶。
[0077]
如本文所用的,术语“感染”意指临床相关的病毒载量。感染在对象中可能是有症状的或无症状的。临床相关的病毒载量可能导致有症状或无症状的个体。
[0078]
在第一方面,提供了用于体外诊断病毒感染的方法中用途的诊断肽,所述肽由式(i)表示:
[0079]
[a]-[b]-[c]
ꢀꢀ(i)[0080]
其中:
[0081]
[a]是具有650-900nm发射波长的荧光剂,
[0082]
[b]是包含氨基酸序列x
aa1
,x
aa2
,x
aa3
的肽
[0083]
其中x
aa1
是疏水性或碱性氨基酸,
[0084]
其中x
aa2
是极性、中性或碱性氨基酸,
[0085]
其中x
aa3
是极性、中性或碱性氨基酸,
[0086]
[c]是具有650-900nm吸收波长的非荧光剂,以用于淬灭所述荧光剂的所述发射,
[0087]
其中x
aa1
,x
aa2
,x
aa3
代表病毒编码的蛋白酶的切割位点,其中切割位点的切割导致从肽释放非荧光剂,其中非荧光剂的释放指示病毒的存在,优选地其中[b]代表基于[a]-[b]-[c]的总质量,按重量计诊断肽的总质量的最多50%。
[0088]
术语“疏水性氨基酸”意指主要具有赋予在水性环境中缔合倾向的侧链的氨基酸。术语“疏水的(hydrophobic)”和“疏水性(hydrophobicity)”为本领域技术人员所熟知,如从手册
‘
iupac gold book’iupac.compendium of chemical terminology,第2版.(the"gold book"),由a.d.mcnaught和a.wilkinson编译,blackwell scientific publications,oxford(1997)已知的,https://doi.org/10.1351/goldbook.ht06964。疏水
性氨基酸的实例是丙氨酸、亮氨酸、缬氨酸、正亮氨酸、正缬氨酸、异亮氨酸、异缬氨酸、别异亮氨酸、苯丙氨酸、脯氨酸、甲硫氨酸和色氨酸。
[0089]
术语“极性、中性氨基酸”意指能够形成一个或多个氢键的氨基酸"。极性、中性氨基酸的实例是丝氨酸、苏氨酸、半胱氨酸、天冬酰胺、谷氨酰胺和酪氨酸。
[0090]
术语“碱性氨基酸”意指在中性ph下具有碱性侧链的氨基酸。碱性氨基酸的实例是精氨酸、赖氨酸和组氨酸。
[0091]
xaa1是疏水性或碱性氨基酸。优选地xaa1选自:丙氨酸、亮氨酸、缬氨酸、正亮氨酸、正缬氨酸、异亮氨酸、异缬氨酸、别异亮氨酸、苯丙氨酸、组氨酸、精氨酸和赖氨酸,更优选地选自:组氨酸、赖氨酸和精氨酸。优选地,xaa1是组氨酸。xaa2是极性、中性或碱性氨基酸。优选地,xaa2选自:组氨酸、天冬酰胺和谷氨酰胺,更优选地xaa2选自组氨酸和谷氨酰胺。优选地,xaa2是谷氨酰胺。
[0092]
xaa3是极性、中性或碱性氨基酸。优选地,xaa3选自:丝氨酸、苏氨酸和甘氨酸。更优选地xaa3选自丝氨酸和苏氨酸,甚至更优选地xaa3是丝氨酸。
[0093]
优选地,氨基酸序列x
aa1
,x
aa2
,x
aa3
具有选自以下的序列:lqs、hqs、fht、nleqs、nvaqs、vlqs、(seq id no:1)、vlns(seq id no:2)、rqs或kqs。
[0094]
肽优选地包含4至10个氨基酸,更优选地5至9个氨基酸。
[0095]
优选地,切割位点由3至8个氨基酸,优选地4至7个氨基酸组成。切割位点优选地由多个氨基酸,例如至少2个,优选地至少3个氨基酸,更优选地至少4个氨基酸,甚至更优选地至少5个氨基酸组成。
[0096]
优选地基于[a]-[b]-[c]的总质量,[b]代表按重量计诊断肽的总质量的最多50%。更优选地,[b]代表基于[a]-[b]-[c]的总质量,按重量计诊断肽总质量的最多45%,甚至更优选地按重量计诊断肽总质量的最多40%,更优选地按重量计诊断肽总质量的最多35%,甚至更优选地按重量计诊断肽总质量的最多30%,更优选地按重量计诊断肽总质量的最多25%。
[0097]
优选地,[b]代表基于[a]-[b]-[c]的总质量,诊断肽总质量的按重量计诊断肽总质量的5%至50%,更优选地按重量计7%至45%,甚至更优选地按重量计10%至40%,甚至更优选地按重量计15%至35%。
[0098]
优选地,荧光的增加被确定为相对增加,由此从不存在样品(f2)的诊断肽的荧光中减去在存在诊断肽和样品(f1)的情况下所测量的荧光。优选地,根据以下等式,相对增加表示为在样品(f2)的不存在情况下诊断肽的荧光的比例:
[0099]
相对荧光百分比=[(f1-f2)/f2]*100
[0100]
优选地,氨基酸序列x
aa1
,x
aa2
,x
aa3
侧接有其他氨基酸、烃基部分和/或非蛋白水解烃基连接子。
[0101]
在优选的实施方案中,烃基连接子选自:β-丙氨酸基、4-氨基丁酰基、2-(氨基乙氧基)乙酰基、3-(2-氨基乙氧基)丙基、5-氨基戊酰基、6-氨基己基、8-氨基-3,6-二氧杂辛基和12-氨基-4,7,10-三氧杂十二烷基,优选地为6-氨基己基。
[0102]
根据一实施方案,诊断肽由式(ia)表示:
[0103]
[a]-[连接子1]-[b]-[-连接子2]-[c]
ꢀꢀꢀ
(ia)
[0104]
其中连接子独立地选自任选取代的烃基和非蛋白水解烃基。
[0105]
在本发明的一方面,诊断肽由式(ib)表示:
[0106]
[a]-[连接子1]-[b]-[-连接子2]-[c]
ꢀꢀ
(ib)
[0107]
其中:
[0108]
[a]是具有650-900nm发射波长的荧光剂,
[0109]
[b]是包含3-10个氨基酸且具有氨基酸序列x
aa1
,x
aa2
,x
aa3
的肽,
[0110]
其中xaa1是组氨酸、精氨酸或赖氨酸,
[0111]
其中xaa2是谷氨酰胺,
[0112]
其中xaa3是极性、中性或碱性氨基酸,
[0113]
[c]是具有650-900nm吸收波长的非荧光剂,以用于淬灭所述荧光剂的所述发射,
[0114]
[连接子1]和[连接子2]独立地选自任选取代的烃基和非蛋白水解烃基,
[0115]
其中x
aa1
,x
aa2
,x
aa3
代表病毒编码的蛋白酶的切割位点,其中切割位点的切割导致从肽释放非荧光剂,其中非荧光剂的释放指示病毒(优选地属于冠状病毒科的病毒)的存在。更优选地,病毒是sars-cov-2(sars-cov-19)。
[0116]
式(ib)的肽还可以通过其在用于诊断sars-cov-2(sars-cov-19)感染的体外方法中的用途来限定。
[0117]
具有650-900nm发射波长的荧光剂优选地是花氰部分(染料)。优选地,具有650-900nm发射波长的非荧光剂是花氰部分(染料)。
[0118]
优选地,荧光剂是具有650-900nm发射波长的花氰染料,且非荧光剂是具有650-900nm吸收波长的花氰染料。
[0119][0120]
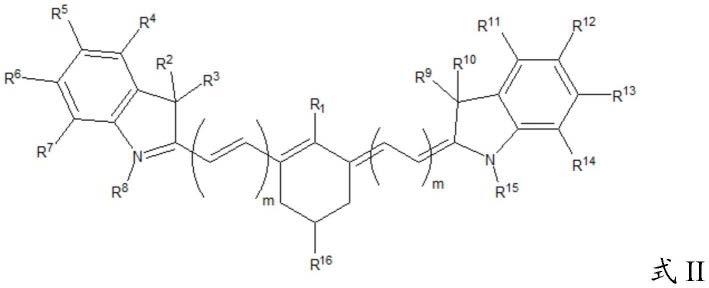
在实施方案中,第一荧光剂是具有式ii中所示通式的花氰染料,其中r1选自h、卤代和其中r
17
选自:羧基、氨基和磺基(sulfanato);x选自:o、s、nh和n-烃基;r2、r3、r9、r
10
各自独立地选自h和烃基;r4、r5、r
11
、r
12
各自独立地选自:h、烃基和磺基或与它们接合的原子一起形成芳环;r6、r7、r
13
、r
14
各自独立地选自h和烃基,r8和r
15
各自独立地选自烃基、(ch2)qfg或(ch2)
p
ln,其中r8和r
15
中的至少一个是(ch2)qfg,其中q是1至20的整数,且fg是不与羧基、羟基、氨基或硫醇基直接反应的官能团,其中p是1至20的整数,且ln是与羧基、羟基、氨基或硫醇基反应的连接子基团;r
16
是h或烃基。
[0121]
优选地,荧光剂是试剂,其中r1是其中x是o,且r
17
是so3na;r2、r3、r9、r
10
是烃基,优选地甲基;r4和r
11
是h,且r5和r
12
是h或磺基;r6、r7、r
13
、r
14
是h;r8是(ch2)qfg,其中q是4,且fg是磺基;r
15
是(ch2)
p
ln,其中p是5且ln是羧基,r
16
是h。
[0122]
甚至更优选地,荧光剂是试剂,其中r1是其中x是o且r
17
是so3na;r2、r3、r9、r
10
是甲基;r4和r
11
是h,且r5和r
12
是磺基;r6、r7、r
13
、r
14
是h;r8是(ch2)qfg,其中q是4,且fg是磺基;r
15
是(ch2)
p
ln,其中p是5且ln是羧基,r
16
是h。优选地,荧光剂是对应于式iii的试剂。
[0123][0124]
具有650-900nm的吸收波长的非荧光剂是具有很少或没有本征荧光并且可以有效地猝灭来自具有很少背景的邻近荧光团的荧光的化合物。在实施方案中,非荧光剂是花氰分子。花氰分子,也称为花氰染料,包括具有通过聚甲炔链连接的两个取代或未取代的含氮杂环的化合物。
[0125]
在优选实施方案中,非荧光剂是试剂,其中r1是氯代,r2、r3、r9、r
10
是甲基;r4是h且r5是n-烃基,优选地是n[(ch2)3so3na]2;r
11
和r
12
形成以磺基单取代的芳环;r6、r7、r
13
、r
14
是h;r8是(ch2)qfg,其中q是3且fg是磺基;r
15
是(ch2)
p
ln,其中p是5,且ln是羧基;r
16
是h。
[0126]
在另一实施方案中,荧光剂和非荧光是相同的试剂,优选地其中r1是其中x是o且r
17
是so3na、r2、r3、r9、r
10
是烃基,优选地是甲基,r4、r5、r
11
、r
12
是h,r6、r7、r
13
、r
14
是h,r8是(ch2)qfg,其中q是4且fg是磺基,r
15
是(ch2)pln,其中p是5且ln是羧基,r
16
是h。
[0127]
非荧光剂还可以是淬灭部分例如bhq3、(biosearch)qc-1(li-cor.com)、tf7qws、tf8qws(aat bio)或包含此类化合物的颗粒(例如金纳米颗粒和铁纳米颗粒)。在实施方案中,肽底物是包含如本文所限定的肽的纳米颗粒。在优选实施方案中,非荧光剂是qc-1(li-cor.com)。
[0128]
可与本发明一起使用的荧光剂的实例包括但不限于alexa660、alexa680、alexa700、alexa750 atto 680、atto 700、dy-647、dy-650、dy-673、dy-675、dy-676、dy-680、dy-681、dy-682、dy-690、dy-700、dy-701、dy-730、dy-731、dy-732、dy-734、dy-750、dy-751、dy-752、dy-776、dy-781、dy-782、dy-831、la jolla蓝、cy5、cy5.5、cy7、ir800cw、ir38、ir800rs、ir700dx、ir680和tf7ws(aatbio)等。“alexa fluor”染料可从molecular peptides inc.,
eugene,or,u.s.a.(www.peptides.com)获得。“atto”染料可从atto-tec gmbh,siegen,德国,(www.atto-tec.com)获得。“dy”染料可从dyomics gmbh,jena,德国,(www.dyomics.com)获得。la jolla蓝可从hyperion inc获得。“cy”染料可从amersham biosciences,piscataway,nj,u.s.a.(www.amersham.com)获得。“红外染料”可从bioscience,inc.lincoln,n e,u.s.a(www.licor.com)获得。
[0129]
在优选实施方案中,荧光剂是ir染料800cw、cy7或tf7ws,优选地是cy7。优选地,cy7具有根据式iv的结构:
[0130][0131]
其中r
18
是与羧基、羟基、氨基或硫醇基反应的连接子基团。cy7例如可从clickchemistrytools;[https://clickchemistrytools.com/product/cy7-nhs-ester/]获得。
[0132]
优选地,肽具有结构([a]-[b]-[c])
m,p
,其中m是1至8的整数并且p是 (正的)或
–
(负的)。优选地,肽具有结构([a]-[b]-[c])
m,p
,其中m为1至8的整数且p为负,更优选地,m为2至7的整数且p为负,甚至更优选m为3至6的整数且p为负,最优选地m为3至6的整数且p为负。
[0133]
优选地,肽具有结构([a]-[b]-[c])
m,p
,其中m为1至8的整数且p为正,更优选地,m为2至7的整数且p为正,甚至更优选地,m为3至6的整数并且p为正,最优选地,m为3至6的整数并且p为正。
[0134]
优选地,切割位点由3至8个氨基酸,优选4至7个氨基酸组成。切割位点优选包含多个氨基酸,例如至少两个,优选至少三个氨基酸,更优选至少四个氨基酸,甚至更优选至少五个氨基酸。优选地,切割位点具有xyz结构,其中x为至少一个氨基酸,y为由至少两个氨基酸组成的分子结构的一部分,且z为至少一个氨基酸。x和z可以是任何氨基酸。优选地,y包含由脂肪族疏水性氨基酸和芳香族或环状氨基酸或碱性氨基酸和亲水性氨基酸组成的二肽。脂肪族疏水性氨基酸优选选自:甘氨酸、丙氨酸、亮氨酸、缬氨酸及它们的衍生物。芳香族或环状氨基酸优选选自:苯丙氨酸、酪氨酸、色氨酸、脯氨酸及它们的衍生物。碱性氨基酸优选为赖氨酸,且亲水性氨基酸优选为苏氨酸或丝氨酸。优选地,切割位点包含非天然氨基酸。非天然氨基酸是技术人员已知的。
[0135]
优选地,肽包含细胞穿透部分。细胞穿透部分包含由x1、x2x3x4x5x6x7x8、x9组成的氨基酸序列,其中x1是a、l或g或r,x2是w、a、l或g或r,x3是r或k,x4是r、k、l或s,x5是r、k、
l,x6是r、k、l,x7是r、k、l,x8是a、v、r、k、l、s或q,且x9是a、v、r、k、l、s、q、w、f或y。优选地,细胞穿透部分是九个精氨酸肽,其中对于所有x1、x2x3x4x5x6x7x8、x9,x是r。
[0136]
如本文所用的,“细胞穿膜肽(cell-penetrating peptide)”是分子,其核心是肽。然而,其他化学基团可以与所述肽核心共价结合,以提高分子的整体稳定性,和/或为其提供另外的性质(如靶向能力)。例如,根据本发明的细胞穿膜肽还可以包含共价连接至c-末端的一个或几个选自以下的基团:半胱酰胺、半胱氨酸、硫醇、酰胺、羧基、任选取代的直链或分支c1-c6烷基、伯胺或仲胺、糖苷(osidic)衍生物、脂质、磷脂、脂肪酸、胆固醇、聚乙二醇、核定位信号(nls)和/或靶向分子。可选地或另外地,细胞穿膜肽还包含共价连接至n-末端的一个或几个选自以下的化学实体:乙酰基、脂肪酸、胆固醇、聚乙二醇、核定位信号和/或靶向分子。如有必要,例如在n-末端添加胆固醇的情况下,肽桥可以被用于结合非肽分子。
[0137]
优选地,[a]是具有700-850nm发射波长的花氰部分,[b]是包含选自的序列的肽:lqs、hqs、rqs、kqs、fht、nleqs、nvaqs、vlqs、(seq id no:1)、vlns(seq id no:2),更优选地选自hqs、rqs或kqs,[连接子1]和[连接子2]都是3-(2-氨基乙氧基)丙基,[c]是具有700-850nm吸收波长的花氰部分。
[0138]
优选地对象是人或动物。优选地,对象是人。
[0139]
优选地,对象是动物。优选地,对象是动物并且属于选自以下的物种:家猪(sus scrofa domesticus)、家鸡(gallus gallus domesticus)、家猫(felis catus)、家犬(canis lupus familiaris)、牛(bos taurus)、绵羊(ovis aries)、山羊((capra)和家畜山羊(aegagurus hircus),优选地选自以下物种:家猪、家鸡、家猫、家犬、牛,更优选地选自以下物种:家猪、家鸡、家猫,甚至更优选地选自家猪和家鸡的物种,最优选地为物种家猪。
[0140]
优选地,病毒感染由属于小核糖核酸病毒科(picornaviridae)、冠状病毒科、腺病毒科(adenoviridae)、冠状病毒科的病毒引起。优选地,病毒是选自以下的小核糖核酸病毒科:鼻病毒,甲型肝炎、乙型肝炎、丙型肝炎、丁型肝炎或戊型肝炎病毒。
[0141]
优选地,鼻病毒是肠病毒属(enterovirus)病毒。
[0142]
优选地,病毒是选自以下的腺病毒科病毒:腺胸腺病毒(atadenovirus)、禽腺病毒(aviadenovirus)、肌腺病毒(ichtadenovirus)、哺乳动物腺病毒(mastadenovirus)、唾液腺病毒(siadenovirus)和以上的组合。
[0143]
优选地,病毒是选自以下属的冠状病毒科:α冠状病毒、β冠状病毒、γ冠状病毒、δ冠状病毒属。优选地,冠状病毒科是α冠状病毒或β冠状病毒。
[0144]
优选地,病毒属于冠状病毒属,并且是选自以下的物种:α冠状病毒1(tgev、猫冠状病毒、犬冠状病毒)、人冠状病毒229e、人冠状病毒nl63、长翼蝠属冠状病毒1、长翼蝠属冠状病毒hku8、猪流行性腹泻病毒、菊头蝠属冠状病毒hku2和黄蝠属冠状病毒512。优选地,病毒是猪流行性腹泻病毒。优选地,病毒是猪流行性腹泻病毒且对象属于家猪。
[0145]
优选地,病毒属于β冠状病毒属,并且是选自以下的物种:β冠状病毒1(牛冠状病毒、人冠状病毒oc43)、刺猬冠状病毒1、人冠状病毒hku1、中东呼吸综合征相关冠状病毒、鼠冠状病毒、伏翼属蝙蝠冠状病毒hku5、果蝠属蝙蝠冠状病毒hku9、严重急性呼吸系统综合征相关冠状病毒(sars-cov、sars-cov-2)和扁颅蝠冠状病毒hku4。优选地,病毒是严重急性呼吸系统综合征相关冠状病毒(sars-cov、sars-cov-2),更优选地病毒是严重急性呼吸系统
综合征相关冠状病毒(sars-cov-2)。优选地,病毒是严重急性呼吸系统综合征相关冠状病毒(sars cov、sars-cov-2),并且对象是人。
[0146]
优选地,病毒属于γ冠状病毒属,并且是选自禽冠状病毒和白鲸冠状病毒sw1的物种。优选地,病毒是禽冠状病毒。优选地,病毒是禽冠状病毒并且对象属于家鸡。
[0147]
优选地,病毒属于δ冠状病毒属,并且是选自夜莺冠状病毒hku11和猪冠状病毒hku15的物种。优选地,病毒是猪冠状病毒hku15。优选地,病毒是猪冠状病毒hku15且对象属于家猪
[0148]
优选地,病毒蛋白酶由病毒rna编码。病毒蛋白酶优选地选自肝炎编码的丝氨酸蛋白酶或金属-蛋白酶(ns2和ns3)、鼻病毒基因组编码的半胱氨酸蛋白酶(3c和2a)、3c蛋白酶、冠状病毒基因组编码的半胱氨酸蛋白酶(3cl)、腺病毒基因组编码的以丝氨酸为中心的中性蛋白酶、逆转录病毒编码的天冬氨酰基蛋白酶。优选地病毒蛋白酶是3c样(3cl)蛋白酶。优选地其中冠状病毒蛋白酶是hsars冠状病毒基因组编码的半胱氨酸蛋白酶、sars冠状病毒19主蛋白酶(ec编号3.4.22.69,brenda数据库发布2021.1(2021年1月))。
[0149]
优选地蛋白酶是sars基因组编码的半胱氨酸蛋白酶,其中sars蛋白酶是sars冠状病毒19主蛋白酶(ec编号3.4.22.69,brenda数据库发布2021.1(2021年1月))。主蛋白酶在大的多聚蛋白质1ab(复制酶1ab,~790kda)上的不少于11个切割位点处操作;切割位点是leu-gln=ser-ala-gl(其中=是易切断的肽键)。
[0150]
优选地,病毒编码的蛋白酶是与3c样蛋白酶[严重急性呼吸系统综合征冠状病毒2]的氨基酸序列具有至少50%同源性,优选地至少55%,更优选地至少60%,甚至更优选地70%,更优选地至少75%,甚至更优选地80%,甚至超过85%,甚至更优选地至少90%,甚至更优选地至少95%,优选地至少97%,最优选地至少98%的蛋白酶,所述3c样蛋白酶具有登陆号yp_009725301,版本号yp_009725301.1,18-jul-2020ncbi蛋白质数据库genpept[2021-03-26];可从https://www.ncbi.nlm.nih.gov/protein/1802476809获得。
[0151]
优选地,病毒编码的蛋白酶是在位置3241-3546处与3c样蛋白酶(3cl pro;r1a_sars)的氨基酸序列具有至少50%同源性,优选地至少55%,更优选地至少60%,甚至更优选地70%,更优选地至少75%,甚至更优选地80%,甚至超过85%,甚至更优选地至少90%,甚至更优选地至少95%,优选地至少97%,最优选地至少98%的蛋白酶,所述3c样蛋白酶具有登陆号p0c6u8(uniprot),整合到uniprotkb/swiss-prot中:序列更新:2008年6月10日,最后修改:2021年2月10日,版本104[2021-03-26];可从https://www.uniprot.org/uniprot/p0c6u8获得。
[0152]
优选地,病毒编码的蛋白酶是与3c蛋白酶[人鼻病毒a1]的氨基酸序列具有至少50%同源性,优选地至少55%,更优选地至少60%,甚至更优选地70%,更优选地至少75%,甚至更优选地80%,甚至超过85%,甚至更优选地至少90%,甚至更优选地至少95%,优选地至少97%,最优选地至少98%的蛋白酶,所述3c蛋白酶具有登陆号yp_009508983.1,版本号yp_009508983.1,24-aug-2018 ncbi蛋白质数据库genpept[2021-03-26];https://www.ncbi.nlm.nih.gov/protein/yp_009508983。
[0153]
优选地,病毒编码的蛋白酶是与pedv主蛋白酶[猪流行性腹泻病毒]的氨基酸序列具有至少50%同源性,优选地至少55%,更优选地至少60%,甚至更优选地70%,更优选地至少75%,甚至更优选地80%,甚至超过85%,甚至更优选地至少90%,甚至更优选地至少
95%,优选地至少97%,最优选地至少98%的蛋白酶,所述pedv主蛋白酶具有登陆号4xfq_a,pdb数据库,存储于28-12-2014,版本1.0 2016-1-20[2021-03-26];https://www.rcsb.org/structure/4xfq。
[0154]
通常使用序列分析软件测量同源性,例如遗传学计算机组,威斯康星大学生物技术中心,1710大学大道,麦迪逊,威斯康星州53705(genetics computer group,university of wisconsin biotechnology center,1710 university avenue,madison,wisconsin 53705)的序列分析软件包、megalign(dnastar,inc.,1228 s.park st.,麦迪逊,威斯康星州53715),以及macvector(牛津大学分子组(oxford molecular group),2105 s.bascom大街,200号,campbell,加利福尼亚州,95008)、blast,其可经由国家生物技术信息中心(ncbi)[互联网](national center for biotechnology information(ncbi)[internet]).bethesda(md):国家生物技术信息中心国家医学图书馆(national library of medicine(us),national center for biotechnology information);[2021]
–
https://www.ncbi.nlm.nih.gov/(madden,t.l.,tatusov,r.l.&zhang,j.(1996)"applications of network blast server"meth.enzymol.266:131-141)获得。此类软件通过将同源度分配给各种替换、缺失和其他修饰来匹配相似的序列。保守性取代通常包括以下组内的取代:甘氨酸和丙氨酸;缬氨酸、异亮氨酸和亮氨酸;天冬氨酸、谷氨酸、天冬酰胺和谷氨酰胺;丝氨酸和苏氨酸;赖氨酸和精氨酸;以及苯丙氨酸和酪氨酸。也可以基于保守的疏水性或亲水性(kyte和doolittle,j.mol.biol 157:105-132,1982),或基于呈现相似多肽二级结构的能力(chou和fasman,adv.enzymol.47:45-148,1978)进行取代。
[0155]
优选地,病毒编码的蛋白酶是与3c样蛋白酶[急性急性呼吸系统综合征冠状病毒2]的氨基酸序列具有至少50%序列相似性,优选地至少55%,更优选地至少60%,甚至更优选地70%,更优选地至少75%,甚至更优选地80%,甚至超过85%,甚至更优选地至少90%,甚至更优选地至少95%,优选地至少97%,最优选地至少98%的蛋白酶,所述3c样蛋白酶具有登陆号yp_009725301,版本号yp_009725301.1,18-jul-2020 ncbi蛋白质数据库genpept[2021-03-26];可从https://www.ncbi.nlm.nih.gov/protein/1802476809获得。
[0156]
优选地,病毒编码的蛋白酶是在位置3241-3546处与3c样蛋白酶(3cl pro;r1a_sars)的氨基酸序列具有至少50%序列相似性,优选地至少55%,更优选地至少60%,甚至更优选地70%,更优选地至少75%,甚至更优选地80%,甚至超过85%,甚至更优选地至少90%,甚至更优选地至少95%,优选地至少97%,最优选地至少98%的蛋白酶,所述3c样蛋白酶具有登陆号p0c6u8(uniprot),其整合到uniprotkb/swiss-prot中:序列更新:2008年6月10日,最后修改:2021年2月10日,版本104[2021-03-26];可从https://www.uniprot.org/uniprot/p0c6u8获得。
[0157]
优选地,病毒编码的蛋白酶是与3c蛋白酶[人鼻病毒a1]的氨基酸序列具有至少50%序列相似性,优选地至少55%,更优选地至少60%,甚至更优选地70%,更优选地至少75%,甚至更优选地80%,甚至超过85%,甚至更优选地至少90%,甚至更优选地至少95%,优选地至少97%,最优选地至少98%的蛋白酶,所述3c蛋白酶具有登陆号yp_009508983.1,版本号yp_009508983.1,24-aug-2018ncbi蛋白质数据库genpept[2021-03-26];https://www.ncbi.nlm.nih.gov/protein/yp_009508983。
[0158]
优选地,病毒编码的蛋白酶是与pedv主蛋白酶[猪流行性腹泻病毒]的氨基酸序列
具有至少50%序列相似性,优选地至少55%,更优选地至少60%,甚至更优选地70%,更优选地至少75%,甚至更优选地80%,甚至超过85%,甚至更优选地至少90%,甚至更优选地至少95%,优选地至少97%,最优选地至少98%的蛋白酶,所述pedv主蛋白酶具有登陆号4xfq_a,pdb数据库,存储于28-12-2014,版本1.0 2016-1-20[2021-03-26];https://www.rcsb.org/structure/4xfq。
[0159]
术语“%序列相似性”意指在两个氨基酸序列之间的给定比对中,允许在所限定的比对长度上对具有相似物理化学性质的氨基酸残基进行保守性取代。相似性百分比容易由技术人员确定,例如根据众所周知的方法,例如curr protoc bioinformatics.2013;43:3.5.1
–
3.5.9。
[0160]
优选地,该方法对病毒感染的特异性优于对宿主炎症反应的特异性。优选地,该方法对特定病毒或病毒家族具有选择性。
[0161]
优选地,病毒感染选自:脑膜炎、胃肠道感染、夏季流感、手足口病、脊髓灰质炎病毒3c脊髓灰质炎、普通感冒、过敏性哮喘恶化、脑炎、甲型肝炎(慢性黄疸)、马脑炎、天花、风疹(德国麻疹)、呼吸道感染、小儿毛细支气管炎、病毒性肺炎、急性呼吸系统综合征、猪疾病、黄热病、丙型肝炎,猪、牛和羊疾病,急性上呼吸道、眼睛和肠道感染、疱疹(全身和局部)感染、兔出血疾病、马铃薯病害和植物病害。
[0162]
优选地,病毒蛋白酶是3c蛋白酶并且感染选自脑膜炎、胃肠道感染、夏季流感、手足口病、脊髓灰质炎病毒3c脊髓灰质炎、普通感冒、过敏性哮喘发作和脑炎。
[0163]
优选地,病毒蛋白酶是3c样蛋白酶并且感染选自小儿毛细支气管炎、病毒性肺炎和急性呼吸系统综合征(sars)、covid-19、猪流行性腹泻病毒、猫传染性腹膜炎、犬冠状病毒感染、犊牛肠炎。
[0164]
优选地,病毒蛋白酶是丝氨酸蛋白酶并且感染选自以下:天花、马脑炎、呼吸道感染、黄热病、丙型肝炎,猪、牛和羊疾病。
[0165]
病毒蛋白酶优选地是参与病毒多肽的蛋白质水解中的蛋白酶。
[0166]
优选地,该方法检测感染,其中病毒(病原体)选自:小核糖核酸病毒科、冠状病毒科、腺病毒科、冠状病毒科和以上的组合,最优选地该方法检测感染,其中病毒(病原体)是冠状病毒科。甚至更优选地,该方法检测感染,其中病毒(病原体)是sars,优选地sars-cov和/或sars-cov-2,甚至更优选地sars-cov-2(2019ncov)。本文所限定的肽具有能够快速检测患者样品中病毒编码的蛋白酶的优点。
[0167]
针对诊断肽所描述的实施方案,经适当修改后适用于本发明涉及肽的方法/用途以及包含所述肽的试剂盒/系统的方面。
[0168]
在本发明的另一方面,描述了用于体外诊断对象的病毒感染的方法,所述方法包括以下步骤:
[0169]
i)使体液样品/组织样品与肽接触,所述肽包含具有650-900nm发射波长的荧光剂,和用于淬灭所述荧光剂的所述发射的具有650-900nm吸收波长的非荧光剂,以及位于所述荧光剂和第一非荧光剂之间的切割位点,所述切割位点特异性针对病毒蛋白酶,
[0170]
ii)监测来自步骤i)中的所述肽的650-900nm范围内的荧光,
[0171]
其中650-900nm范围内荧光的增加指示样品中病毒的存在。
[0172]
优选地,体液样品是血液、唾液、痰、支气管肺泡液、组织活检切片和/或泪液。优选
地,体液样品是唾液。
[0173]
样本可能存在于拭子或其他收集装置上。优选地,体液/组织样本存在于收集装置上。收集装置优选为拭子。
[0174]
优选地,该方法包括使包含体液/组织样品的收集装置与容器中的缓冲液接触的步骤。
[0175]
可选地,收集装置是容器,优选地,其中容器是用于接收唾液或痰的小瓶或瓶。
[0176]
任选地,该方法包括离心样品以从上清液中分离固体物质和/或沉淀的生物材料的步骤。优选地,离心力可以在1,000g至25,000g的范围内,优选地在3,000g至20,000g的范围内,更优选地在3,700g至18,000g的范围内。离心时间优选在1分钟至30分钟的范围内、在2至20分钟的范围内,更优选在3至10分钟的范围内。由离心产生的上清液或聚集物优选与试剂接触。在优选实施方案中,来自离心的上清液优选与试剂接触。在另一优选实施方案中,离心产生的聚集物优选与试剂接触。
[0177]
任选地,在将试剂添加到样品中之后,搅拌混合物。优选通过用移液管抽吸、涡旋或摇动来搅拌混合物。
[0178]
在特别优选的实施方案中,在样品与试剂接触之前,不对样品进行细胞富集步骤。通过“未进行细胞富集步骤”意指没有将样品在37℃下孵育数小时以增加样品的病毒载量的步骤。换言之,样本可以直接从收集装置转移到其中添加试剂的容器中。
[0179]
优选地在测定缓冲液中稀释样品,优选地其中所述样品的稀释倍数范围为1:10至1:10000,更优选地1:100至1:1000。
[0180]
优选地,测定缓冲液能够维持5-9,优选地约6至约8,更优选地约6.5至约7.5的ph范围。优选地缓冲液包括hepes、pipes、tris-盐酸盐(tris-hcl)或mops。
[0181]
优选地,样品与裂解剂接触。更优选地,缓冲液含有能够裂解体液样品中的细胞物质的去污剂。优选地,缓冲液包含选自以下的一种或多种非离子去污剂:n-辛基
‑‑
d-吡喃葡萄糖苷、n-辛基
‑‑
d-麦芽糖苷、zwittergent 3.14、脱氧胆酸盐;正十二烷酰蔗糖;正十二烷基
‑‑
d-吡喃葡萄糖苷;正十二烷基
‑‑
d-麦芽糖苷;正辛基
‑‑
d-吡喃葡萄糖苷;正辛基-对d-吡喃麦芽糖苷;正辛基-对d-硫代吡喃葡萄糖苷;正癸酰蔗糖;正癸基-对d-吡喃麦芽糖苷;正癸基-对d-硫代麦芽糖苷;正庚基
‑‑
d-吡喃葡萄糖苷;正庚基-对d-硫代吡喃葡萄糖苷;正己基
‑‑
d-吡喃葡萄糖苷;正壬基-对d-吡喃葡萄糖苷;正辛酰蔗糖;正辛基
‑‑
d-吡喃葡萄糖苷;正十一烷基
‑‑
d-麦芽糖苷;apo-10;apo-12;big chap;big chap,脱氧;35;d2e5;d2e6;ci2e8;ci2e9;环己基-正乙基-对d-麦芽糖苷;环己基-正己基-对d-麦芽糖苷;环己基-正甲基
‑‑
d-麦芽糖苷;洋地黄皂苷;elugent
tm
;c-100;x-080;x-100;hecameg;mega-10;mega-8;mega-9;noga;np-40;f-127;x-100;x-l 14;14;20;或80及以上的混合物。
[0182]
缓冲液优选包含选自以下的离子型去污剂:batc、十六烷基三甲基溴化铵、鹅去氧胆酸、胆酸、脱氧胆酸、甘胆酸、甘氨脱氧胆酸、甘氨石胆酸、月桂酰肌氨酸、牛磺鹅去氧胆酸、牛磺胆酸、牛磺去氢胆酸、牛磺石胆酸、牛磺熊去氧胆酸、toppa及以上的混合物。
[0183]
优选地,缓冲液包含选自以下的两性离子去污剂:氨基磺基甜菜碱、chaps、
chapso、羧基甜菜碱和甲基甜菜碱。
[0184]
优选地,缓冲液包含选自以下的阴离子去污剂:sds、n-月桂基肌氨酸、脱氧胆酸钠、烷基-芳基磺酸盐、长链(脂肪)醇硫酸盐、烯烃硫酸盐和磺酸盐、α烯烃硫酸盐和磺酸盐、硫酸化甘油单酯、硫酸化醚、磺基琥珀酸盐、烷烃磺酸盐、磷酸酯、烷基羟乙基磺酸盐、蔗糖酯及以上的混合物。
[0185]
步骤iii)中监测荧光增加的步骤优选在适于接收包含样品和试剂的容器的检测器中进行。检测器优选地以相对荧光单位(rfu)提供读数。用户可以将读数与对照进行比较,并且对照和样品之间rfu的相对增加指示病毒感染。
[0186]
优选地,病毒是如上所述的病毒。优选地,病毒属于小核糖核酸病毒科或冠状病毒科。
[0187]
病毒蛋白酶优选地选自:肝炎编码的丝氨酸蛋白酶或金属-蛋白酶(ns2和ns3)、鼻病毒基因组编码的半胱氨酸蛋白酶(3c和2a)、冠状病毒基因组编码的半胱氨酸蛋白酶(3cl)、腺病毒基因组编码的以丝氨酸为中心的中性蛋白酶、逆转录病毒编码的天冬氨酰基蛋白酶,优选地其中所述冠状病毒蛋白酶是hsars冠状病毒基因组编码的半胱氨酸蛋白酶、sars冠状病毒19主蛋白酶(ec编号3.4.22.69),更优选地病毒蛋白酶是3c样(3cl)蛋白酶。
[0188]
优选地,本文中描述了用于体外诊断对象的病毒感染的方法,所述方法包括以下步骤:
[0189]
i)使唾液样品的样品与肽接触,所述肽包含具有650-900nm发射波长的荧光剂,和用于淬灭所述荧光剂的所述发射的具有650-900nm吸收波长非荧光剂,以及位于所述荧光剂和第一非荧光剂之间的切割位点,所述切割位点特异性针对3c样蛋白酶,
[0190]
ii)监测来自步骤i)中肽的650-900nm范围内的荧光,
[0191]
其中650-900nm范围内荧光的增加指示选自以下的病毒感染:小儿毛细支气管炎、病毒性肺炎和急性呼吸系统综合征(sars)、covid-19、猪流行性腹泻病毒、猫传染性腹膜炎、犬冠状病毒感染、犊牛肠炎,优选地病毒感染是急性呼吸系统综合征(sars)、covid-19,更优选地为covid-19。
[0192]
在其他方面,提供了用于诊断对象的病毒感染的试剂盒,其包含:
[0193]
a)包含式(i)的诊断肽的容器,
[0194]
b)用于执行本文所限定的诊断方法的一套说明书。
[0195]
在其他一方面,提供了用于诊断对象的病毒感染的系统,其包括:
[0196]
a)用于接收样品的容器,
[0197]
b)包含式(i)的诊断肽的容器,
[0198]
c)适于接收容器并监测在肽与体液样品接触时从肽发射的荧光信号的装置。
[0199]
本文所述的用于诊断病毒感染的体外方法的优选实施方案经适当修改适用于本文所述的试剂盒。
[0200]
另一方面,提供了用于诊断对象的病毒感染的系统,其包括:
[0201]
a)用于接收样品的容器,
[0202]
b)包含式(i)的诊断肽的容器,
[0203]
c)适于接收容器并监测在肽与体液样品接触时从肽发射的荧光信号的装置。
[0204]
本文所述的用于检测病毒感染的方法的优选实施方案经适当修改适用于本文所
述的系统。
[0205]
优选地,装置是近红外分光光度计。优选地,该装置是护理点装置。
[0206]
上面已经参考多项示例性实施方案描述了本发明。一些部分或元素的修改和替代实施方式是可能的,并且包括在所附权利要求中所限定的保护范围内。
实施例
[0207]
实施例1-sars-cov-19的检测
[0208]
将包含sars-cov-19病毒的样品与荧光淬灭肽(tvrlqsgf)接触,所述荧光淬灭肽包含具有650-900nm发射波长的荧光剂和具有650-900nm吸收波长的非荧光剂,以及特异性针对冠状病毒的切割位点(ex 1.1)。阴性对照(打乱的)肽是fqvlrs(ex 1.2)。
[0209]
在接触试剂后0、1、2和4小时,使用手持式荧光计(deniro nir fluorimeter,detactdiagnostics bv,荷兰)进行测量。从每次测量中减去对照样品(缓冲液)的rfu。
[0210]
检测到rfu或样品的增加,但阴性对照未检测到。
[0211]
实施例2
[0212]
合成肽购自crb(billingham,uk)。荧光剂是10cy 7(cy7 dbco,来自click chemistry tools,亚利桑那州,usa),且非荧光剂是qc-1(qc-1nhsester,licor,内布拉斯加州,usa)。
[0213]
将于超纯水中的肽储备液添加至重组sars-cov-2主蛋白酶(mysourcebio,加利福尼亚州,usa),以给出5um肽的最终浓度。sars-cov-2主蛋白酶的浓度在0.2-2um之间变化。使用的缓冲液30是20mm tris、100mm nacl、1mm edta、1mm dtt、ph 7.3。添加肽溶液后0、5、15、30和45分钟监测荧光。使用deniro nir探测器(detactdiagnostics,格罗宁根,荷兰)监测荧光。
[0214]
作为对照,使用枯草杆菌蛋白酶(merck,荷兰)和弹性蛋白酶(sigma aldrich,荷兰)。对照蛋白酶的浓度和缓冲液与sars-cov-2主蛋白酶的实验相同。
[0215]
根据以下计算公式计算相对活性:
[0216][0217]
结果显示在下表1中:
[0218]
表1
mecn,ph 6.2,和b)10mm甲酸铵/90%v/v mecn,ph 6.2。
[0226]
所用梯度为0.2ml-min,25分钟。
[0227]
将0.1mg/ml的表3中的每种肽溶液与sars-cov-2主蛋白酶(10μm)一起孵育。
[0228]
表3
[0229][0230][0231]
肽1的切割发生在q-s之间。肽2的切割发生在q-s之间。未观察到肽3的切割。
[0232]
将0.1mg/ml的表4中的每种肽溶液与弹性蛋白酶(2μm)一起孵育。结果显示在表4中。
[0233]
表4
[0234][0235]
实施例4
–
临床数据
[0236]
使用了已经通过pcr表征为sars-cov-2阳性或阴性的临床样品(corman等人,detection of 2019 novel coronavirus(2019-ncov)by real-time rt-pcr.euro surveill.2020;25(3):pii=2000045)(streeklab,haarlem,the netherlands)。缓冲液a是pbs,ph 7.2
[0237]
通过加入1ml的缓冲液a至终浓度为0.1mg/ml=26um)来制备底物储备液。
[0238]
空白(仅肽溶液)
[0239]
将50μl肽储备液加入200μl缓冲液a中,并涡旋。
[0240]
‘
空白’在deniro上进行测量。
[0241]
样品测量
[0242]
将100μl缓冲液a添加到500μl eppendorf中,涡旋样品瓶,取出100μl样品并添加到eppendorf。加入50μl肽储备液(终浓度20um)。将eppendorf涡旋2
×
5秒,并立即在deniro上测量荧光。然后将eppendorf置于室温并在5、10、15、30、60分钟时重新测量。结果如表5所示。》10%的相对活性表示存在sars-cov-2( ),相对活性《10%表示不存在sars-cov-2(-)。
[0243]
表5
[0244][0245]
实施例5
–
sars-cov-2测试
[0246]
如实施例2中所述的肽1和肽2以及肽4(cy7-ahx-[peg1]-fht-[peg1]k[(qc1)-conh2)在疑似感染sars-cov-2对象的的鼻咽(np)样品中进行了测试。样本以前用于运行pcr测试以检测感染的存在。样品是m4病毒转运培养基中的np拭子。所有样品在分析前都在4℃下储存了最多48小时。
[0247]
使用根据corman等人,detection of 2019 novel coronavirus(2019-ncov)by real-time rt-pcr.euro surveill.2020;25(3):pii=2000045.https://doi.org/10.2807/1560-7917.es.2020.25.3.2000045的方法对所有样品进行确认性pcr。阳性样品的ct值范围为16至33.8。一个具有ct》35的样品未被包括在内。
[0248]
通过将肽1、2和4分别溶解在缓冲液a(pbs,ph 7.2)中至终浓度为61.86μm来制备肽储备溶液。
[0249]
使用deniro近红外荧光计(detactdiagnostics 5 bv,荷兰)监测样品。
[0250]
阴性对照:仅肽溶液
[0251]
1.将81μl肽储备液(1、2或4)添加到169μl缓冲液a中,涡旋,并在deniro中测量“空白”。
[0252]
样品测量[eppendorf中样品 缓冲液 底物的总体积=250μl)
[0253]
1.将69μl缓冲液a加入至0.5ml eppendorf
[0254]
2.将copan拭子瓶短暂涡旋,移除100μl样品液并加入eppendorf
[0255]
3.将81μl的covitact肽储备液加入eppendorf(终浓度为20μm肽)
[0256]
4.涡旋2
×
5秒
[0257]
5.马上[0分钟]和在5分钟时测量。
[0258]
结果呈现于表6中。
[0259]
表6
[0260][0261]
表7显示了阳性和阴性预测值,其按以下公式计算:
[0262]
阳性预测值=100*tp/(tp fp)
[0263]
阴性预测值=100*tn/(tn fn)
[0264]
总一致百分比=100*(tp tn)/总数
[0265]
表7
[0266][0267][0268]
根据本发明的肽2显示与确认的感染存在/不存在的高(约90%)相关性。
[0269]
在表8中比较了根据本发明肽和现有技术的那些的肽含量。
[0270]
表8
[0271][0272]-未观察到; 观察到。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。