1.本发明涉及关节炎治疗药物技术领域,尤其是一种高异黄酮类化合物在制备类风湿性关节炎治疗药物中的应用。
背景技术:
2.类风湿性关节炎(rheumatoid arthritis,ra)是一种慢性进行性的自身免疫性疾病,以关节滑膜炎及对称性、破坏性的关节病变为主要特征。其典型的临床表现为反复发作的对称的多发性小关节炎,以手、腕、足、膝等关节最常受累。早期可有红、肿、热、痛和关节功能障碍。晚期关节可出现不同程度的强直和畸形,并有骨腐蚀和骨骼肌的萎缩,是一种致残率较高的疾病。
3.目前抗ra药物主要有三种:非甾体抗炎药(nsaids)、慢作用抗风湿药和糖皮质激素。前者如安吡昔康,美洛昔康,氯诺昔康,塞来昔布;甲氨蝶呤、金制剂、青霉胺、雷公藤多苷、硫唑嘌呤、环磷酰胺、环孢素(csa);后者如可的松、氢化可的松、泼尼松、泼尼松龙、地塞米松等。
4.高异黄酮类化合物(homoisoflavonoids)是黄酮化合物中特殊的一类,母体结构比异黄酮多一个碳原子,自然界中高异黄酮类化合物的分布较少,但具有独特的生物活性,是新药候选化合物的重要来源。
技术实现要素:
5.本发明的目的在于提供高异黄酮类化合物在制备类风湿性关节炎治疗药物中的应用,探索了高异黄酮类化合物的一种新用途。
6.为实现上述目的,本发明技术方案如下:
7.本发明提供一种高异黄酮化合物在制备类风湿性关节炎疾病治疗药物中的应用。
8.本发明所述的高异黄酮化合物在制备类风湿性关节炎疾病治疗药物中的应用,其中,所述高异黄酮化合物具有如下结构通式,
[0009][0010]
其中:r1为氢或羟基或甲氧基或乙氧基或正丙氧基;r2为氢或羟基或甲氧基或氟或氯或二甲基氨基;r3为氢或羟基或甲氧基。
[0011]
本发明所述的高异黄酮化合物具体举例如表1所示:
[0012]
表1
[0013]
[0014]
[0015][0016]
胶原性关节炎(cia)大鼠是兼有体液免疫和细胞免疫变化的慢性系统性免疫性炎症模型,是筛选和研究治疗类风湿性关节炎(ra)药物的较理想动物模型之一,在临床表现、病理学和免疫学改变及发病机制方面与ra非常相似。
[0017]
对于类风湿性关节炎,il-17不仅导致炎症,还能造成骨破坏。il-17诱导滑膜细胞、软骨和骨细胞分泌的促炎症细胞因子,通过炎症级联反应不断放大,形成慢性、不断进展的关节炎症。此外,il-17通过刺激多种趋化因子的产生,诱导降解基质金属蛋白酶,加重关节炎症反应,导致滑膜增生侵蚀软骨与骨组织,导致不可逆转的关节骨组织损伤。总之,il-17可增强关节炎症、滑膜增生和迁移,关节骨组织损伤,在类风湿性关节炎的发生和发展中起到关节作用。
[0018]
经细胞体外和动物体内实验证明:本发明所述的高异黄酮化合物具有抗类风湿性关节炎作用;在体外,发明所述化合物能抑制胶原性关节炎(cia)大鼠滑膜细胞的迁移,以及对il-17的分泌;在体内,发明所述化合物能够抑制cia大鼠的关节炎症状、减少滑膜细胞迁移、侵蚀关节软骨,降低系统性il-17水平;在抑制关节炎症状上与上市药物甲氨喋呤(mtx)相当。
附图说明
[0019]
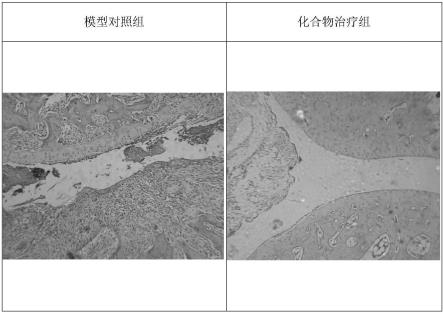
图1为化合物对cia大鼠关节滑膜细胞迁移侵蚀骨组织的抑制作用。
具体实施方式
[0020]
本发明在以下的实施例中进一步说明。这些实施例只是为了说明的目的,而不是用来限制本发明的范围。
[0021]
本发明提供的化合物可以通过多种制备方法来获得,这里仅提供获得这类化合物
的代表性合成方法。
[0022]
反应通式:
[0023][0024]
反应条件:将式a底物加入β-氯丙酸和三氯甲烷磺酸,在80℃条件下反应生成式b中间产物;式b中间产物在2.0m naoh条件下,碱催化环化生成式c中间产物;式c中间产物加入相应的芳香醛,在乙酸溶液反应体系中通入干燥的氯化氢气体,酸催化缩合生成式d终产物。
[0025]
采用上述方法合成的化合物中,具有代表性的化合物及其理化性质如下所述,合成所使用的初始原料、反应试剂等若无特殊说明均为市售产品。
[0026]
下述实施例1-20中合成的化合物分别对应于表1中的化合物1-20。
[0027]
实施例1化合物11合成
[0028][0029]
第一步:将底物间苯二酚加入β-氯丙酸和三氯甲烷磺酸(1:1.2:3),在80℃条件下,反应1小时后冷至室温,先后加入二氯甲烷和水(1:1),经二氯甲烷萃取多次,分离合并有机层,无水硫酸钠干燥过滤,减压蒸除溶剂,得到中间产物1。
[0030]
第二步:将2m氢氧化钠溶液降至5℃,在搅拌条件下加入上一步合成的中间产物1
[0031]
(27.2g/l),室温反应2小时,再次降至5℃,用6m硫酸调节反应液ph至2,黄色沉淀析出,过滤、水洗,真空干燥,得到中间产物2。
[0032]
第三步:将上步合成中间产物2与3,4-二羟基苯甲醛(1:1.2),在适量的冰醋酸中溶解,通入干燥的氯化氢气体5分钟,之后在室温条件下搅拌反应24小时,过滤沉淀、干燥,乙醇中重结晶,得终产物化合物11。
[0033]
黄色粉末。ms(ei)m/z:284[m] 。1h-nmr(dmso-d6,400mhz)δ:10.56(brs,1h),9.55(brs,1h),9.19(brs,1h),7.72(1h,d),7.51(1h,brs),6.86
–
6.81(2h,m),6.76(1h,dd),6.54(1h,dd),6.31(1h,d),5.34(2h,d)。
[0034]
除了使用相应的原料外,以实施例1相同的方法制备化合物1-20,化合物1-20的结构式以及1h-nmr和ms数据如下。
[0035]
实施例2化合物1合成
[0036]
除了使用相应的原料外,以实施例1相同的方法制备化合物,化合物1的结构式以及1h-nmr和ms数据如下。
[0037]
化合物1:
[0038][0039]
白色粉末。ms(ei)m/z:236[m] 。1h-nmr(cdcl3,400mhz)δ:8.03(1h,dd),7.88(1h,brs),7.49(1h,ddd),7.46
–
7.40(3h,m),7.34
–
7.30(2h,m),7.07(1h,ddd),6.97(1h,dd),5.36(2h,d)。
[0040]
实施例3化合物2合成
[0041]
除了使用相应的原料外,以实施例1相同的方法制备化合物2,化合物的结构式以及1h-nmr和ms数据如下。
[0042]
化合物2:
[0043][0044]
黄色粉末。ms(ei)m/z:252[m] 。1h-nmr(dmso-d6,400mhz)δ:10.13(1h,s),7.85(1h,dd),7.66(1h,brs),7.56(1h,ddd),7.33(2h,d),7.10(1h,ddd),7.03(1h,dd),6.87(2h,d),5.41(2h,d)。
[0045]
实施例4化合物3合成
[0046]
除了使用相应的原料外,以实施例1相同的方法制备化合物3,化合物的结构式以及1h-nmr和ms数据如下。
[0047]
化合物3:
[0048][0049]
黄色粉末。ms(ei)m/z:268[m] 。1h-nmr(dmso-d6,400mhz)δ:7.84(1h,dd),7.58(1h,brs),7.56(2h,ddd),7.10(1h,ddd),7.03(1h,dd),6.85
–
6.76(3h,m),5.40(2h,d)。
[0050]
实施例5化合物4合成
[0051]
除了使用相应的原料外,以实施例1相同的方法制备化合物4,化合物的结构式以及1h-nmr和ms数据如下。
[0052]
化合物4:
[0053][0054]
黄色粉末。ms(ei)m/z:266[m] 。1h-nmr(cdcl3,400mhz)δ:8.02(1h,dd),7.84(1h,brs),7.48(1h,ddd),7.29(2h,d),7.07(1h),6.98(2h,d),6.97(1h,dd),5.38(2h,d),3.87(3h,s)。
[0055]
实施例6化合物5合成
[0056]
除了使用相应的原料外,以实施例1相同的方法制备化合物5,化合物的结构式以及1h-nmr和ms数据如下。
[0057]
化合物5:
[0058][0059]
黄色粉末。ms(ei)m/z:296[m] 。1h-nmr(cdcl3,400mhz)δ:8.02(1h,dd),7.83(1h,brs),7.48(1h,ddd),7.08(1h,ddd),6.97(1h,dd),6.94(1h,d),6.90(1h,dd),6.87(1h,d),5.40(2h,d),3.94(3h,s),3.92(3h,s)。
[0060]
实施例7化合物6合成
[0061]
除了使用相应的原料外,以实施例1相同的方法制备化合物6,化合物的结构式以及1h-nmr和ms数据如下。
[0062]
化合物6:
[0063][0064]
黄色粉末。ms(ei)m/z:279[m] 。1h-nmr(cdcl3,400mhz)δ:8.02(1h,dd),7.83(1h,brs),7.46(1h,ddd),7.27(2h,d),7.05(1h,ddd),6.95(1h,dd),6.73(2h,d),5.44(2h,d),3.05(6h,s)。
[0065]
实施例8化合物7合成
[0066]
除了使用相应的原料外,以实施例1相同的方法制备化合物7,化合物的结构式以及1h-nmr和ms数据如下。
[0067]
化合物7:
[0068][0069]
白色粉末。ms(ei)m/z:254[m] 。1h-nmr(cdcl3,400mhz)δ:8.03(1h,dd),7.83(1h,brs),7.50(1h,ddd),7.33
–
7.29(2h,m),7.17
–
7.12(2h,m),7.09(1h,ddd),6.98(1h,dd),5.33(2h,d)。
[0070]
实施例9化合物8合成
[0071]
除了使用相应的原料外,以实施例1相同的方法制备化合物8,化合物的结构式以及1h-nmr和ms数据如下。
[0072]
化合物8:
[0073][0074]
白色粉末。ms(ei)m/z:270[m] 。1h-nmr(cdcl3,400mhz)δ:8.02(1h,dd),7.81(1h,brs),7.50(1h,ddd),7.43(2h,d),7.25(2h,d),7.09(1h,ddd),6.98(1h,dd),5.32(2h,d)。
[0075]
实施例10化合物9合成
[0076]
除了使用相应的原料外,以实施例1相同的方法制备化合物9,化合物的结构式以及1h-nmr和ms数据如下。
[0077]
化合物9:
[0078][0079]
白色粉末。ms(ei)m/z:252[m] 。1h-nmr(dmso-d6,400mhz)δ:7.90(1h,d),7.83(1h,brs),7.66
–
7.55(5h,m),6.70(1h,dd),6.46(1h,d),5.49(2h,d)。
[0080]
实施例11化合物10合成
[0081]
除了使用相应的原料外,以实施例1相同的方法制备化合物10,化合物的结构式以及1h-nmr和ms数据如下。
[0082]
化合物10:
[0083]
[0084]
黄色粉末。ms(ei)m/z:268[m] 。1h-nmr(dmso-d6,400mhz)δ:7.73(1h,d),7.60(1h,brs),7.30(2h,d),6.87(2h,d),6.54(1h,dd),6.31(1h,d),5.35(2h,d)。
[0085]
实施例12化合物12合成
[0086]
除了使用相应的原料外,以实施例1相同的方法制备化合物12,化合物的结构式以及1h-nmr和ms数据如下。
[0087]
化合物12:
[0088][0089]
黄色粉末。ms(ei)m/z:282[m] 。1h-nmr(dmso-d6,400mhz)δ:7.72(1h,d),7.64(1h,brs),7.40(2h,d),7.05(2h,d),6.54(1h,dd),6.30(1h,d),5.35(2h,d),3.82(3h,s)。
[0090]
实施例13化合物13合成
[0091]
除了使用相应的原料外,以实施例1相同的方法制备化合物13,化合物的结构式以及1h-nmr和ms数据如下。
[0092]
化合物13:
[0093][0094]
黄色粉末。ms(ei)m/z:295[m] 。1h-nmr(dmso-d6,400mhz)δ:7.72(1h,d),7.59(1h,brs),7.30(2h,d),6.78(2h,d),6.53(1h,dd),6.31(1h,d),5.38(2h,d),3.00(6h,s)。
[0095]
实施例14化合物14合成
[0096]
除了使用相应的原料外,以实施例1相同的方法制备化合物14,化合物的结构式以及1h-nmr和ms数据如下。
[0097]
化合物14:
[0098][0099]
黄色粉末。ms(ei)m/z:266[m] 。1h-nmr(cdcl3,400mhz)δ:7.97(1h,d),7.85(1h,brs),7.45
–
7.38(3h,m),7.31
–
7.27(2h,m),6.63(1h,dd),6.40(1h,d),5.33(2h,d),3.84(3h,s)。
[0100]
实施例15化合物15合成
[0101]
除了使用相应的原料外,以实施例1相同的方法制备化合物15,化合物的结构式以及1h-nmr和ms数据如下。
[0102]
化合物15:
[0103][0104]
黄色粉末。ms(ei)m/z:282[m] .1h-nmr(dmso-d6,400mhz)δ:7.80(1h,d),7.63(1h,brs),7.32(2h,d),6.87(2h,d),6.69(1h,dd),6.56(1h,d),5.41(2h,dd),3.83(3h,s)。
[0105]
实施例16化合物16合成
[0106]
除了使用相应的原料外,以实施例1相同的方法制备化合物16,化合物的结构式以及1h-nmr和ms数据如下。
[0107]
化合物16:
[0108][0109]
黄色粉末。ms(ei)m/z:(m ):298。1h-nmr(dmso-d6,400mhz)δ:9.75(1h,brs),9.34(1h,brs),8.86(1h,d),7.61(1h,brs),6.91
–
6.80(3h,m),6.75(1h,dd),6.62(1h,d),5.46(2h,d2),3.89(3h,s)。
[0110]
实施例17化合物17合成
[0111]
除了使用相应的原料外,以实施例1相同的方法制备化合物17,化合物的结构式以及1h-nmr和ms数据如下。
[0112]
化合物17:
[0113][0114]
黄色粉末。ms(ei)m/z:296[m] 。1h-nmr(cdcl3,400mhz)δ:7.96(1h,d),7.81(1h,brs),7.28(2h,d),6.97(2h,d),6.63(1h,dd),6.40(1h,d),5.37(2h,d),3.86(3h,s),3.85(3h,s)。
[0115]
实施例18化合物18合成
[0116]
除了使用相应的原料外,以实施例1相同的方法制备化合物18,化合物的结构式以及1h-nmr和ms数据如下。
[0117]
化合物18:
[0118][0119]
黄色粉末。ms(ei)m/z:309[m] 。1h-nmr(cdcl3,400mhz)δ:7.96(1h,d),7.80(1h,brs),7.25(2h,d),6.72(2h,d),6.63(1h,dd),6.40(1h,d),5.42(2h,d),3.84(3h,s),3.04(6h,s)。
[0120]
实施例19化合物19合成
[0121]
除了使用相应的原料外,以实施例1相同的方法制备化合物19,化合物的结构式以及1h-nmr和ms数据如下。
[0122]
化合物19:
[0123][0124]
褐色粉末。1h-nmr(cdcl3,400mhz)δ:7.84(d,1h),7.62(t,1h),7.42(brs,2h),6.92
–
6.66(m,3h),6.58(dd,1h),6.38(d,1h),5.36(d,2h),4.07(q,2h),1.41(t,3h)。
[0125]
实施例20化合物20合成
[0126]
除了使用相应的原料外,以实施例1相同的方法制备化合物20,化合物的结构式以及1h-nmr和ms数据如下。
[0127]
化合物20:
[0128][0129]
褐色粉末。1h-nmr(cdcl,400mhz)δ:7.87(d,1h),7.67(t,1h),7.57(s,1h),7.09(brs,1h),7.03
–
6.67(m,3h),6.59(dd,1h),6.39(d,1h),5.37(d,2h),3.97(t,2h),1.82(sextet,
[0130]
实施例21细胞体外试验
[0131]
实验方法:
[0132]
大鼠cia模型:wistar大鼠采用ⅱ型胶原诱导大鼠cia,将牛二型胶原蛋白(cii)与等体积的弗氏不完全佐剂混合制备乳剂,首次免疫采用尾根部背面皮内注射0.2ml。一周后后,再次于大鼠尾根部腹面注射0.1ml,完成二次免疫。
[0133]
细胞原代培养:首次免疫30天后将具有明显关节炎症状的cia模型大鼠处死,无菌条件下取大鼠膝关节滑膜组织。大鼠膝关节滑膜组织用pbs冲洗后,加入胰蛋白酶10ml/g,37℃培养箱中消化30min,加入10%dmem终止消化,pbs冲洗,加入胶原酶,37℃培养箱中消
化4h,过滤收集悬液,离心,弃上清液,重悬,收集细胞。细胞悬液稀释后,接种于培养瓶中,5%co2培养箱中培养,48h后更换培养液去除未贴壁细胞,每2天更换培养液。
[0134]
细胞毒性试验:适当细胞密度的cia滑膜细胞悬液接种于96孔培养板,于37℃,5%二氧化碳条件下培养24h后去掉上清液,试验组分别加入200μl含有化合物(终浓度1—100μm)的细胞培养液,对照组加200μl空白培养液,继续培养24h后去掉上清液,每孔加入200μl mtt(0.5mg/ml)溶液,放入培养箱中继续孵育4h后,每孔加150μl甲臜裂解液dmso终止反应,振荡30s,使细胞内的蓝紫色结晶物完全溶解。酶标仪上读取od492,计算细胞生长抑制率。
[0135]
细胞迁移试验:滑膜细胞以12
×
104个/孔接种到24孔板中,37℃孵育,直到80%的细胞贴壁生长融合。每孔平行划三条直线,pbs清洗3次。给药组加入化合物(终浓度10μm)的细胞培养液,对照组加空白培养液,采用倒置显微镜观察给药0h和24h时划线处细胞情况并拍照记录。给药24h时,镜下随机取5个视野对越线细胞进行细胞计数,计算各化合物给药对细胞迁移能力的影响。
[0136]
细胞液il-17水平检测:滑膜细胞以2
×
105个/孔接种到12孔板中,于37℃,5%二氧化碳条件下培养24h后去掉上清液,给药组加入200μl含有化合物(终浓度10μm)的细胞培养液,对照组加200μl空白培养液,不含血清以减少对后续实验的影响。继续培养24h后,收集上清液,4℃,1000r/min离心5min。
[0137]
使用96孔酶标板,每孔加入100μl上清液,4℃过夜孵育,每组设3个重复孔。预冷pbst洗涤3次(pbs加入0.1%tween-20),封闭液(含1%bsa和5%蔗糖的pbst溶液)37℃封闭1h。预冷pbst再次洗涤后分别加入il-17(1:1000)一抗,4℃过夜孵育。洗涤后加入二抗(1:2000),37℃孵育3h。每孔加入100μl tmb底物显色液,37℃避光反应25~30min。每孔50μl 0.5mol/l h2so4溶液终止反应,利用酶标仪,在450nm处测各孔吸光度(od)值。
[0138]
实验结果:化合物在10μm以内均无显著细胞毒性,在1μm化合物与空白对照相比,对关节炎滑膜细胞的迁移和对il-17分泌具有显著抑制作用(抑制率>50%)的化合物如表2所示。抑制率=[(模型对照组平均od值一化合物治疗组平均od值)/(模型对照组平均od值一空白对照组平均od值)]
×
100%。
[0139]
表2体外抗关节炎活性
[0140]
[0141][0142]
实施例22动物体内药效试验
[0143]
实验方法:
[0144]
药物准备:化合物-11、16和3为实验室合成制备,阳性对照药化合物为甲氨蝶呤为市售原料药。
[0145]
表3药物治疗化合物及来源
[0146][0147]
模型建立:wistar大鼠采用ⅱ型胶原诱导大鼠cia,将牛二型胶原蛋白(cii)与等体积的弗氏不完全佐剂混合制备乳剂,首次免疫采用尾根部背面皮内注射0.2ml。一周后后,再次于大鼠尾根部腹面注射0.1ml,完成二次免疫。
[0148]
分组治疗:将具有显著cia症状的模型大鼠(关节(炎指数大于2)随机分成五组(每组7只),分别为模型对照组(0.2%乙醇生理盐水)、化合物-11给药组(5mg/kg、10mg/kg、20mg/kg)、化合物-16给药组(20mg/kg)、化合物-3给药组(20mg/kg),阳性药物对照组(mtx5mg/kg),灌胃给药(1次/天),连续四周。
[0149]
关节炎指数评价:给药期间对大鼠的关节炎指数进行评估,关节炎的严重程度分为如下0-4级:0,足爪无肿胀及红斑;1,足爪趾或指关节肿胀;2,足爪踝关节或腕关节轻度肿胀;3,整个足爪严重的炎性症状;4,足爪畸形和关节僵直。大鼠四只爪的总分被记作关节炎指数,最大得分为16分。
[0150]
血清il-17水平检测:连续给药28天之后,腹腔注射水合氯醛(0.3ml/100g)麻醉,心脏穿刺取血,室温20min自然凝固,3000r/min离心15min,收集血清。使用96孔酶标板,每孔加入100μl上清液,4℃过夜孵育,每组设3个重复孔。预冷pbst洗涤3次(pbs加入0.1%tween-20),封闭液(含1%bsa和5%蔗糖的pbst溶液)37℃封闭1h。预冷pbst再次洗涤后分别加入il-17(1:1000)一抗,4℃过夜孵育。洗涤后加入二抗(1:2000),37℃孵育3h。每孔加入100μl tmb底物显色液,37℃避光反应25~30min。每孔50μl 0.5mol/l h2so4溶液终止反应,利用酶标仪,在450nm处测各孔吸光度(od)值。
[0151]
踝关节病理组织观察:处死大鼠后,取双侧后足置于中性甲醛固定液中固定48小时,10%edta 4℃脱钙30天,石蜡包埋,切片(5mm),常规he染色。显微镜观察关节滑膜迁移和关节软骨侵蚀程度。
[0152]
实验结果:
[0153]
关节炎指数评分结果:给药期间(0-28天)监测大鼠的体重和关节炎指数评分结果表明,本发明化合物口服治疗能抑制胶原诱导的大鼠关节炎指数(如表4所示,数据表示为mean
±
s.e.m.,n=7)。而且化合物与阳性对照药甲氨喋呤(mtx)在相当的剂量下,对关节炎指数具有更强的抑制作用。试验期间,给药各剂量组大鼠均未出现死亡,与对照组相比体重变化无明显影响,试验后解剖,肉眼检查组织器官未见明显病变。
[0154]
表4关节炎指数评分结果
[0155][0156][0157]
血清il-17水平检测结果:
[0158]
化合物-11、化合物-16和化合物-3(20mg/kg)能够显著抑制cia大鼠的血清中il-17水平,抑制剂率如下表5所示。抑制率=[(模型对照组平均od值一化合物治疗组平均od值)/(模型对照组平均od值一空白对照组平均od值)]
×
100%。
[0159]
表5化合物对血清il-17水平的抑制率
[0160]
治疗组抑制率化合物-11(20mg/kg)>50%化合物-16(20mg/kg)>50%化合物-3(20mg/kg)>50%
[0161]
踝关节病理组织观察结果:
[0162]
化合物-11、化合物-16和化合物-3(20mg/kg),能够明细抑制大鼠的踝关节滑膜细胞的迁移,以及对骨组织的侵蚀,代表性病理图片如图1所示。
[0163]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
