1.本发明涉及药物技术领域,涉及取代的达玛烷型三萜类化合物及其制备方法,本发明还涉及取代的达玛烷型三萜类化合物在抗凝血生物活性方面的用途。
背景技术:
2.心血管疾病是发达国家的主要死亡原因,每年在全世界影响数百万人。该疾病通常是由动脉壁的动脉粥样硬化引起的,动脉粥样硬化发展多年并且其特征是内皮发炎、内皮下脂质沉积、巨噬细胞浸润和斑块发育。在疾病的急性期,动脉粥样硬化斑块变得不稳定并破裂,引发血栓形成。阻塞血管并由此剥夺组织的氧气的血栓(血凝块)的发展构成导致发病和死亡的主要沉淀事件。血凝块形成是由血小板的活化和聚集引发的。血小板栓塞通过凝血的激活和纤维蛋白网络的形成而巩固。由血栓导致的动脉闭塞导致下游组织死亡,并且取决于其发生位置而与心肌梗塞、中风或跛行的发展有关。
3.血栓形成的原因有三:即血管受损、血液改变和血流淤滞;是由许多不同疾病、不同原因引起的一组并发症。由于各种基础疾病的差异,以及血栓栓塞部位的不同,血栓病的临床上可能表现为心肌梗死、中风、深度静脉血栓(deep vein thrombosis,dvt)、肺栓塞、心房颤动和脑梗死等,尤其是以栓塞和梗塞为主要诱因的心梗、脑梗和肺梗,居各种死亡原因之首,全球每年夺走近1200万人生命,接近世界总死亡人数的四分之一。
4.人体血液凝固过程由内源性途径(intrinsic pathway)、外源性途径(extrinsic pathway)和共同途径(common pathway)组成,是通过系列凝血因子相继被激活而后加强放大,最终形成纤维蛋白的一种凝血级联反应。内源性途径(又称接触激活途径)和外源性途径(又称组织因子途径)启动生成凝血因子xa(factor xa,简称fxa),再经共同途径生成凝血酶iia(factor iia,简称fiia),最终形成纤维蛋白。促凝血(止血)与抗凝血(抗栓)在人体血液系统中互相对立并保持相对平衡。当体内抗凝纤溶系统功能降低,血液中凝血与抗凝血功能失去平衡时则出现凝血,从而引起血栓或栓塞。
5.抗血栓药物(即抗凝剂)是防治血栓性疾病的重要手段,其中中药及其制剂对于抗血栓有着独到的疗效,且副作用小,因而从中药及其制剂中发现具有抗血栓活性的天然化合物一直是抗血栓药物研究领域的热点。宋其玲等发现,部分藜芦生物碱具有明显的抗血栓作用,具体与藜芦生物碱的化学结构有关,药效存在明显的构效关系(藜芦生物碱抗血栓作用及构效关系研究,中药材,第37卷第11期2014年11月)。万彦军等发现,芒柄花素磺酸钠高、中剂量组均能抑制大鼠血栓形成、血小板聚集,延长小鼠出血时间(bt)及活化部分凝血酶时间(aptt),具有抑制血栓形成的作用,其作用机制可能与其具有抑制adp、凝血酶诱导血小板聚集,降低内源凝血途径的功能有关(芒柄花素磺酸钠抗血栓作用及机制研究,中国新药杂志2016年第25卷第12期)。万晓晨等发现,蓬子菜中香叶木苷高、中、低剂量组均能明显抑制大鼠下腔静脉血栓形成,保护血管内皮细胞,且中剂量组与阿司匹林组作用相当,表明香叶木苷具有抗凝血和抗静脉血栓形成的作用(蓬子菜中香叶木苷抗血栓形成作用的实验研究,中医药信息,2014年11月第31卷第6期)。
6.绞股蓝(gynostemma pentaphyllum makino.)又名七叶胆、福音草等,是葫芦科绞股蓝属植物。其中,绞股蓝皂苷是绞股蓝中的主要活性成分。药理实验和临床应用表明,具有降血脂、抗肿瘤、抗衰老、保护肝脏及增强肌体免疫功能等作用,主要用于治疗肝癌、肺癌、子宫癌、皮肤癌等癌细胞的增殖,另外对人体有滋补、镇静、催眠、抗紧张、促食欲、降胆固醇、降转氨酶、延缓衰老等作用。
7.随着研究的深入,对绞股蓝次级皂苷和绞股蓝次级皂苷抗凝血作用的构效关系研究发现,一类具有新的化学结构的达玛烷型三萜类化合物在抗外源性凝血方面的效果与华法林相当,在抗内源性凝血方面的效果优于华法林。
技术实现要素:
8.本发明的目的是旨在从绞股蓝中寻找新的具更强活性的抗凝血药物,采用了酸水解法对绞股蓝水提物进行水解,得到一类具有新的化学结构的达玛烷型三萜类化合物,并且研究它们的抗凝血生物活性和医药用途。
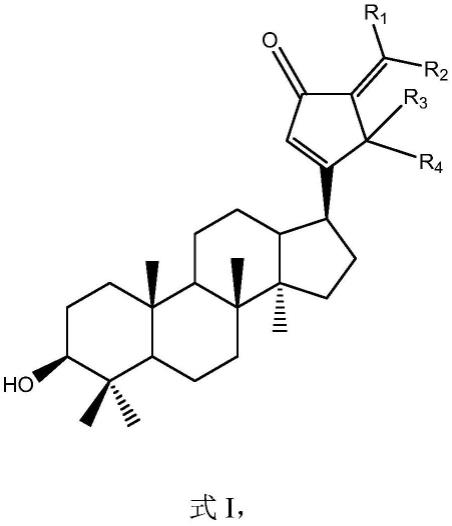
9.为了实现上述目的,根据本发明的一个方面,提供了一种具有式i的达玛烷型三萜类化合物或其立体异构体、互变异构体、氘代物、溶剂化物、代谢产物或前药,
[0010][0011]
其中r1至r4各自独立地选自氢、氟、氯、溴、碘、c1至c8烷基基团、c1至c8烯基基团、c1至c8炔基基团、c1至c8氟代烷基基团、c1至c8氟代烯基基团、c1至c8氟代炔基基团、c1至c8氯代烷基基团、c1至c8氯代烯基基团、c1至c8氯代炔基基团、c1至c8溴代烷基基团、c1至c8溴代烯基基团、c1至c8溴代炔基基团、c1至c8碘代烷基基团、c1至c8碘代烯基基团或c1至c8碘代炔基基团。
[0012]
进一步地,r1至r5各自独立地选自氢、氟、c1至c3烷基基团、c1至c3烯基基团、c1至c3炔基基团、c1至c3氟代烷基基团、c1至c3氟代烯基基团或c1至c3氟代炔基基团。
[0013]
进一步地,该达玛烷型三萜类化合物为绞股蓝次级皂苷z,其中该绞股蓝次级皂苷z具有以下结构式:
[0014][0015]
进一步地,该达玛烷型三萜类化合物是通过酸水解法对绞股蓝水提取物进行水解得到的。
[0016]
根据本发明的另一方面,提供了一种药物组合物,包含上述达玛烷型三萜类化合物和药学上可接受的赋形剂。
[0017]
根据本发明的另一方面,提供了一种制备上述达玛烷型三萜类化合物的方法,其中该方法包括如下步骤:
[0018]
(1)取适量的绞股蓝干燥全草作为原料,用水超声或回流提取1至3次,每次1至3小时,合并提取液,减压浓缩得到水提取物;
[0019]
(2)添加一定体积比的0.5%-3%酸溶液至该水提取物,超声或回流提取0.5至3小时,过滤,水洗得到中性的沉淀;
[0020]
(3)该沉淀经硅胶柱层析得到式i的达玛烷型三萜类化合物。
[0021]
进一步地,步骤(1)中提取所用的水用量按质量计,分别为绞股蓝干燥全草质量的15-25倍。
[0022]
进一步地,步骤(2)中的该酸选自盐酸、硫酸、硝酸、氢溴酸、乙酸、丙酸、丙二酸和丁酸中的一种或多种。
[0023]
进一步地,步骤(3)中的该柱层析是采用粒度为100-400目的硅胶。
[0024]
进一步地,该柱层析的洗脱流动相为正己烷-乙酸乙酯体积比为3∶1至4∶1的混合溶剂。
[0025]
进一步地,该酸溶液与该水提取物的体积比为1∶3至1∶10。
[0026]
根据本发明的另一方面,提供了一种上述达玛烷型三萜类化合物或上述药物组合物在制备用于治疗与血液增稠、凝血或血凝块形成有关的疾病的药物中的用途。
[0027]
根据本发明的另一方面,提供了一种上述达玛烷型三萜类化合物或上述药物组合物在制备用于避免或减轻以下抗凝剂的禁忌症的药物中的用途,其中该抗凝剂选自达比加群、利伐沙班、阿哌沙班、华法林、依度沙班和贝曲沙班中一种或多种。
[0028]
本发明的有益效果:
[0029]
绞股蓝为葫芦科(cucurbitaceae)绞股蓝属植物绞股蓝[gynostemmapentaphyllum(thunb.)makino]的干燥全草,为多年生攀缘草本,主要分布于中国、日本、朝鲜等国。现代药学研究表明,其主要药效成分是绞股蓝皂苷(gypenoside,gyp),与人参皂苷的结构一样或十分接近。我们研究发现,从绞股蓝干燥全草中提取分离得到的一类具有新的化学结构的达玛烷型三萜类化合物在抗外源性凝血方面的效果与华法林相当,在抗内源性凝血方面的效果优于华法林,将其开发为抗凝剂可以扩大绞股蓝的应用范围,提高绞股蓝植物资源的利用价值。
附图说明
[0030]
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,还可以根据这些附图获得其他的附图,而并不超出本发明要求保护的范围。
[0031]
图1为化合物ggypensapogenin z的1h-nmr图谱。
[0032]
图2为化合物ggypensapogenin z的
13
c-nmr图谱。
[0033]
图3为化合物ggypensapogenin c的1h-nmr图谱。
[0034]
图4为化合物ggypensapogenin c的
13
c-nmr图谱。
具体实施方式
[0035]
下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0036]
正如背景技术部分所描述的,中药及其制剂对于抗血栓有着独到的疗效,且副作用小,因而从中药及其制剂中发现具有抗血栓活性的天然化合物一直是抗血栓药物研究领域的热点。随着对于中药绞股蓝的深入研究,本发明提供了一种具有式i的达玛烷型三萜类化合物或其立体异构体、互变异构体、氘代物、溶剂化物、代谢产物或前药,
[0037][0038]
其中r1至r4各自独立地选自氢、氟、氯、溴、碘、c1至c8烷基基团、c1至c8烯基基团、c1至c8炔基基团、c1至c8氟代烷基基团、c1至c8氟代烯基基团、c1至c8氟代炔基基团、c1至c8氯代烷基基团、c1至c8氯代烯基基团、c1至c8氯代炔基基团、c1至c8溴代烷基基团、c1至c8溴代烯基基团、c1至c8溴代炔基基团、c1至c8碘代烷基基团、c1至c8碘代烯基基团或c1至c8碘代炔基基团。
[0039]
在一种优选的实施方式中,r1至r5各自独立地选自氢、氟、c1至c3烷基基团、c1至c3烯基基团、c1至c3炔基基团、c1至c3氟代烷基基团、c1至c3氟代烯基基团或c1至c3氟代炔基基团。
[0040]
在一种优选的实施方式中,该达玛烷型三萜类化合物为绞股蓝次级皂苷z,其中该绞股蓝次级皂苷z具有以下结构式:
[0041][0042]
在一种优选的实施方式中,该达玛烷型三萜类化合物是通过酸水解法对绞股蓝水
提取物进行水解得到的。
[0043]
根据本发明的另一方面,提供了一种药物组合物,包含上述达玛烷型三萜类化合物和药学上可接受的赋形剂。
[0044]
根据本发明的另一方面,提供了一种制备上述达玛烷型三萜类化合物的方法,其中该方法包括如下步骤:
[0045]
(1)取适量的绞股蓝干燥全草作为原料,用水超声或回流提取1至3次,每次1至3小时,合并提取液,减压浓缩得到水提取物;
[0046]
(2)添加一定体积比的0.5%-3%酸溶液至该水提取物,超声或回流提取0.5至3小时,过滤,水洗得到中性的沉淀;
[0047]
(3)该沉淀经硅胶柱层析得到式i的达玛烷型三萜类化合物。
[0048]
在一种优选的实施方式中,步骤(1)中提取所用的水用量按质量计,分别为绞股蓝干燥全草质量的15-25倍。
[0049]
在一种优选的实施方式中,步骤(2)中的该酸选自盐酸、硫酸、硝酸、氢溴酸、乙酸、丙酸、丙二酸和丁酸中的一种或多种。
[0050]
在一种优选的实施方式中,步骤(3)中的该柱层析是采用粒度为100-400目的硅胶。
[0051]
在一种优选的实施方式中,该柱层析的洗脱流动相为正己烷-乙酸乙酯体积比为3∶1至4∶1的混合溶剂。
[0052]
在一种优选的实施方式中,该酸溶液与该水提取物的体积比为1∶3至1∶10。
[0053]
根据本发明的另一方面,提供了一种上述达玛烷型三萜类化合物或上述药物组合物在制备用于治疗与血液增稠、凝血或血凝块形成有关的疾病的药物中的用途。
[0054]
在一种优选的实施方式中,该疾病可以是血栓形成。
[0055]
在一种优选的实施方式中,提供上述化合物或上述药物组合物用于预防和/或治疗或者作为联合疗法治疗与高出血风险、低出血风险或血栓栓塞性病症相关的疾病的用途。
[0056]
在一种优选的实施方式中,提供上述化合物或上述药物组合物用于预防和/或治疗或者作为联合疗法治疗与高出血风险有关的疾病的用途。
[0057]
在一种优选的实施方式中,提供上述化合物或上述药物组合物用于预防和/或治疗或者作为联合疗法治疗与低出血风险有关的疾病的用途。
[0058]
在一种优选的实施方式中,,提供上述化合物或上述药物组合物用于预防和/或治疗或者作为联合疗法治疗与血栓栓塞性病症有关的疾病的用途。
[0059]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用作与高出血风险有关疾病的预防和/或治疗的一部分,其中治疗选自复杂的左侧消融(肺静脉隔离;vt消融)、脊髓或硬膜外麻醉、腰椎诊断穿刺、胸外科手术、腹部外科手术、大型骨科手术、肝活检、肝病、经尿道前列腺切除术、肾脏活检、或肾功能不全。
[0060]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用作与低出血风险有关疾病的预防和/或治疗的一部分,其中治疗选自内窥镜活检、前列腺或膀胱活检、用于室上性心动过速的电生理研究或射频导管消融(包括经由单次经中隔穿刺术进行左侧消融)、血管造影、起搏器或植入式心脏复律除颤器(icd)植入(除非复杂的解剖学背景,例
如先天性心脏病)、机械瓣膜植入或假体瓣膜植入。
[0061]
根据本发明的另一方面,提供了一种上述达玛烷型三萜类化合物或上述药物组合物在制备用于避免或减轻以下抗凝剂的禁忌症的药物中的用途,其中该抗凝剂选自达比加群、利伐沙班、阿哌沙班、华法林、依度沙班和贝曲沙班中一种或多种。
[0062]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用于减轻使用达比加群的疗法的禁忌症;其中禁忌症包括:心房颤动预防中风(预防与非瓣膜性心房颤动相关的中风和全身性栓塞),肾损害crcl《15ml/min或透析,dvt或pe治疗(适用于已接受肠胃外抗凝剂治疗5-10天的患者中的深静脉血栓形成(dvt)和肺栓塞(pe))crcl≤30ml/min或透析,dvt或pe预防(适用于髋关节置换术后预防深静脉血栓形成(dvt)和肺栓塞(pe)),达比加群禁忌去纤核苷酸、米非司酮和人类凝血酶原复合物浓缩物,达比加群不得与以下物质一起使用:抗凝血酶α、抗凝血酶iii、阿哌沙班、卡马西平、达肝素、地塞米松、阿霉素、阿霉素脂质体、决奈达隆、依度沙班、依诺肝素、磺达肝素、磷苯妥英钠、肝素、酮康唑、来普鲁丁、奈法唑酮、苯巴比妥、苯妥英、普里米酮、利福平、圣约翰草、替诺福韦、替拉那韦、长春碱和华法林。
[0063]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用于减轻使用利伐沙班的疗法的禁忌症;其中禁忌症可包括:估计肾小球滤过率(egfr)小于15ml/分钟/1.73m2,活动性出血,来自以下的重大出血风险:当前或最近的胃肠道溃疡,食管静脉曲张,最近的脑或脊髓损伤,最近的脑、脊髓或眼科手术,最近颅内出血,恶性肿瘤,血管动脉瘤,假体心脏瓣膜,与凝血病相关的肝病和临床相关的出血风险,以及患有肝硬化的人或者服用其它抗凝剂的人,除了转为华法林治疗或从华法林治疗转为其它治疗;和正服用细胞色素p3a4酶和p-糖蛋白的强抑制剂(诸如酮康唑)或hiv蛋白酶抑制剂(诸如利托那韦)的人。
[0064]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用于减轻使用阿哌沙班的疗法的禁忌症;其中禁忌症可包括:肌酐清除率(crcl)小于15ml/min或egfr《15ml/分钟/1.73m2,活动性出血,重大出血的重大风险诸如:当前或最近的胃肠道溃疡,食管静脉曲张,最近的脑或脊髓损伤,最近的脑、脊髓或眼科手术,最近颅内出血,恶性肿瘤,血管动脉瘤,与凝血病相关的肝病和临床相关的出血风险,假体心脏瓣膜,服用任何其它抗凝剂的人(除了转为华法林治疗或从华法林治疗转为其它治疗)或正服用细胞色素p3a4酶和p-糖蛋白的强抑制剂(诸如酮康唑)或hiv蛋白酶抑制剂(诸如利托那韦)的人。
[0065]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用于减轻使用华法林的疗法的禁忌症;其中禁忌症可包括:有出血倾向、血友病、血小板减少性紫癜、严重肝肾疾患、活动性消化性溃疡、脑、脊髓及眼科手术患者;恶病质、衰弱、发热、慢性酒精中毒、活动性肺结核、充血性心力衰竭、重度高血压、亚急性细菌性心内膜炎、月经过多、先兆流产的人。
[0066]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用于减轻使用依度沙班的疗法的禁忌症;其中禁忌症包括:与华法林相比,因缺血性中风的风险增加而未在crcl》95ml/分钟的nvaf患者中使用依度沙班。
[0067]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用于减轻使用贝曲沙班的疗法的禁忌症;其中禁忌症包括:服用p-gp抑制剂的患者,严重肾损伤的患者,肝损伤患者,内在凝血异常的患者,假体心脏瓣膜患者,与影响止血的药物共同给药(从而
增加出血风险),与阿司匹林共同给药,与其它抗血小板药共同给药,与其它抗凝剂共同给药,与肝素共同给药,与溶栓剂共同给药,与选择性血清素再摄取抑制剂(ssri)共同给药,与血清素-去甲肾上腺素再摄取抑制剂(snri)共同给药,和与非甾体类抗炎药(nsaid)共同给药。
[0068]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物可用作抗凝剂,用于预防和/或治疗血栓栓塞性病症;其中病症是下列之一:心肌梗塞,心绞痛(包括不稳定型心绞痛),血管成形术或主动脉冠状动脉分流术后的再闭塞和再狭窄,中风,心房颤动以降低其中风风险的患者,患有心房颤动和慢性肾脏疾病的患者,短暂性脑缺血发作,周围动脉阻塞性病症,再灌注损伤(也称为缺血再灌注损伤),经导管主动脉瓣置换(tavr)(也称为经导管主动脉瓣植入(tavi)),肺栓塞,深静脉微血管疾病或需要体外膜氧合(ecmo)的患者。
[0069]
在一种优选的实施方式中,根据本发明的上述化合物或上述药物组合物可以适合于预防和/或治疗弥散性血管内凝血(dic)。
[0070]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物适用于预防和/或治疗动脉粥样硬化和关节炎,并且另外地还适用于预防和/或治疗癌症患者中的血栓形成。
[0071]
在一种优选的实施方式中,本发明的上述化合物或上述药物组合物用于在预防和/或治疗血栓形成的方法中使用。
[0072]
本发明的各方面的目的是至少部分地减轻与现有技术有关的问题。
[0073]
本发明某些实施方式的目的是提供具有与口服生物利用度的潜力一致的理化性质和药代动力学性质的化合物。
[0074]
本发明某些实施方式的目的是提供相对于现有技术化合物和现有疗法表现出降低的细胞毒性或增加的溶解性的化合物。
[0075]
本发明某些实施方式的另一目的是提供在剂量给药后具有方便的药代动力学特征和合适的作用持续时间的化合物。本发明某些实施方式进一步的目的是提供化合物,其中吸收后药物的一个或多个代谢片段是gras(通常被认为是安全的)。
[0076]
本发明的某些实施方式满足了上述目的中的一些或全部。
[0077]
定义和一般术语
[0078]
现在详细描述本发明的某些实施方案,其实例由随附的结构式和化学式说明。本发明意图涵盖所有的替代、修改和等同技术方案,它们均包括在如权利要求定义的本发明范围内。本领域技术人员应认识到,许多与本发明所述类似或等同的方法和材料能够用于实践本发明。本发明绝不限于本发明所述的方法和材料。在所结合的文献、专利和类似材料的一篇或多篇与本技术不同或相矛盾的情况下(包括但不限于所定义的术语、术语应用、所描述的技术,等等),以本技术为准。
[0079]
应进一步认识到,本发明的某些特征,为清楚可见,在多个独立的实施方案中进行了描述,但也可以在单个实施例中以组合形式提供。反之,本发明的各种特征,为简洁起见,在单个实施方案中进行了描述,但也可以单独或以任意适合的子组合提供。
[0080]
除非另外说明,应当应用本发明所使用的下列定义。出于本发明的目的,化学元素与元素周期表cas版以及《化学和物理手册》第75版,1994一致,其全部内容通过引用并入本
发明。
[0081]
除非另有说明或者上下文中有明显的冲突,本发明所使用的冠词“一”、“一个(种)”和“所述”旨在包括“至少一个”或“一个或多个”。因此,本发明所使用的这些冠词是指一个或多于一个(即至少一个)宾语的冠词。
[0082]
术语“立体异构体”是指具有相同化学构造,但原子或基团在空间上排列方式不同的化合物。立体异构体包括对映异构体、非对映异构体、构象异构体(旋转异构体)、几何(顺/反)异构体、阻转异构体,等等。
[0083]
术语“互变异构体”或“互变异构形式”是指具有不同能量的可通过低能垒(lowenergybarrier)互相转化的结构异构体。若互变异构是可能的(如在溶液中),则可以达到互变异构体的化学平衡。例如,质子互变异构体(protontautomer)(也称为质子转移互变异构体(prototropic tautomer))包括通过质子迁移来进行的互相转化,如酮-烯醇异构化和亚胺-烯胺异构化。
[0084]
当本发明化合物或其前药的互变异构(例如,酮-烯醇互变异构)现象存在时,既要求保护它们分别的单个形式(例如,酮或烯醇形式),也要求保护其任意比例的混合物。这同样适用于它们的立体异构体,例如,对映异构体、非对映异构体、构象异构体(旋转异构体)、几何(顺/反)异构体、阻转异构体等。
[0085]
如有需要,可根据本领域已知的方法(例如液相色谱法)对互变异构体进行分离。这同样适用于它们的对映异构体,例如,采用手性固定相分离。此外,对映异构体可通过转化为非对映异构体进行分离,即与对映异构纯的辅助化合物偶连,随后分离所得的非对映异构体并裂解辅助残基。或者,本发明化合物的任何对映异构体可用光学纯原料由立体选择性合成获得。
[0086]
本发明所使用的术语“氘代物”是指式i化合物基团中的一个或多个氢被氘所取代所生成的含氘化合物。
[0087]
本发明所使用的术语“溶剂化物”是指一个或多个溶剂分子与本发明的化合物所形成的缔合物。形成溶剂化物的溶剂包括,但并不限于,水,异丙醇,乙醇,甲醇,二甲亚砜,乙酸乙酯,乙酸、乙醇胺或其混合物。术语“水合物”是指溶剂分子是水所形成的缔合物。当所述溶剂为水时,可以使用术语“水合物”。在一实施方案中,一个本发明化合物分子可以与一个水分子相结合,比如一水合物;在另一实施方案中,一个本发明化合物分子可以与多于一个的水分子相结合,比如二水合物;在又一实施方案中,一个本发明化合物分子可以与少于一个的水分子相结合,比如半水合物。应注意,本发明所述的水合物保留有非水合形式的所述化合物的生物有效性。
[0088]
本发明所使用的术语“代谢产物”是指具体的化合物或其盐在体内通过代谢作用所得到的产物。一个化合物的代谢产物可以通过所属领域公知的技术来进行鉴定,其活性可以通过如本发明所描述的那样采用试验的方法进行表征。这样的产物可以是通过给药化合物经过氧化,还原,水解,酰氨化,脱酰氨作用,酯化,脱脂作用,酶裂解等等方法得到。相应地,本发明包括化合物的代谢产物,包括将本发明的化合物与哺乳动物充分接触一段时间所产生的代谢产物。
[0089]
本发明所使用的术语“前药”,代表一个化合物在体内转化为式i所示的化合物。这样的转化受前体药物在血液中水解或在血液或组织中经酶转化为母体结构的影响。本发明
前体药物类化合物可以是酯,在现有的发明中酯可以作为前体药物的有苯酯类,脂肪族(c
1-24
)酯类,酰氧基甲基酯类,碳酸酯,氨基甲酸酯类和氨基酸酯类。例如本发明里的一个化合物包含羟基,即可以将其酰化得到前体药物形式的化合物。其他的前体药物形式包括磷酸酯,如这些磷酸酯类化合物是经母体上的羟基磷酸化得到的。
[0090]
除非另作说明,本发明的化合物所有合适的立体异构体、互变异构体、氘代物、溶剂化物、代谢产物和前药都包含在本发明范围内。
[0091]
在本说明书的各部分,本发明公开化合物的取代基按照基团种类或范围公开。特别指出,本发明包括这些基团种类和范围的各个成员的每一个独立的次级组合。例如,术语“c1至c8烷基基团”特别指独立公开的甲基、乙基、c3烷基、c4烷基、c5烷基、c6烷基、c7烷基和c8烷基。
[0092]
本发明使用的术语“烷基”或“烷基基团”,表示含有1-20个碳原子、饱和的直链或支链一价烃基基团,其中,所述烷基基团可以任选地被一个或多个本发明描述的取代基所取代。在一些实施方案中,烷基基团含有1-6个碳原子;在另一些实施方案中,烷基基团含有1-4个碳原子;还在一些实施方案中,烷基基团含有1-3个碳原子。烷基基团的实例包含,但并不限于,甲基(me、-ch3),乙基(et、-ch2ch3),正丙基(n-pr、-ch2ch2ch3),异丙基(i-pr、-ch(ch3)2),正丁基(n-bu、-ch2ch2ch2ch3),异丁基(i-bu、-ch2ch(ch3)2(2-甲基丙基)),仲丁基(s-bu、-ch(ch3)ch2ch3(1-甲基丙基)),叔丁基(t-bu、-c(ch3)3),等等。
[0093]
本发明使用的术语“烯基”或“烯基基团”表示含有2-12个碳原子的直链或支链一价烃基,其中至少有一个不饱和位点,即有一个碳-碳sp2双键,其中,所述烯基基团可以任选地被一个或多个本发明所描述的取代基所取代,其包括“顺”和“反”的定位,或者“e”和“z”的定位。在一实施方案中,烯基基团包含2-8个碳原子;在另一实施方案中,烯基基团包含2-6个碳原子;在又一实施方案中,烯基基团包含2-4个碳原子。烯基基团的实例包括,但并不限于,乙烯基(-ch=ch2)、烯丙基(-ch2ch=ch2)、1-丙烯基(即,丙烯基,-ch=ch-ch3),等等。
[0094]
本发明使用的术语“炔基”或“炔基基团”表示含有2-12个碳原子的直链或支链一价烃基,其中至少有一个不饱和位点,即有一个碳-碳sp三键,其中,所述炔基基团可以任选地被一个或多个本发明所描述的取代基所取代。在一实施方案中,炔基基团包含2-8个碳原子;在另一实施方案中,炔基基团包含2-6个碳原子;在又一实施方案中,炔基基团包含2-4个碳原子。炔基基团的实例包括,但并不限于,乙炔基(-c≡ch)、炔丙基(-ch2c≡ch)、1-丙炔基(即,丙炔基,-c≡c-ch3),等等。
[0095]
本发明使用的术语“药学上可接受的赋形剂”意指与给药剂型或药物组合物一致性相关的药学上可接受的材料、混合物或溶媒。每种赋形剂在混合时必须与药物组合物的其它成分相容,以避免对患者给药时会大大降低本发明化合物的功效的相互作用和会导致不是药学上可接受的药物组合物的相互作用。此外,每种赋形剂必须是药学上可接受的,例如,具有足够高的纯度。
[0096]
合适的药学上可接受的赋形剂会依所选具体剂型而不同。此外,可根据它们在组合物中的特定功能来选择药学上可接受的赋形剂。例如,可选择能有助于生产均一剂型的某些药学上可接受的赋形剂。可选择能有助于生产稳定剂型的某些药学上可接受的赋形剂。可选择对患者给药时有助于携带或运输本发明化合物从身体的一个器官或部分到身体
的另一个器官或部分的某些药学上可接受的赋形剂。可选择增强患者依从性的某些药学上可接受的赋形剂。
[0097]
合适的药学上可接受的赋形剂包括以下类型的赋形剂:稀释剂、填充剂、粘合剂、崩解剂、润滑剂、助流剂、造粒剂、包衣剂、润湿剂、溶剂、共溶剂、助悬剂、乳化剂、甜味剂、矫味剂、掩味剂、着色剂、防结块剂、保湿剂、螯合剂、塑化剂、增粘剂、抗氧化剂、防腐剂、稳定剂、表面活性剂和缓冲剂。技术人员可认识到,某些药学上可接受的赋形剂可提供不止一种功能,并提供可供选择的功能,这取决于制剂中存在多少该赋形剂和制剂中存在哪些其他赋形剂。
[0098]
本发明公开的药物组合物使用本领域技术人员已知的技术和方法来制备。本领域一些常用方法的描述可参见remington's pharmaceutical sciences(mack publishing company)。
[0099]
因此,另一方面,本发明涉及制备药物组合物的工艺,所述药物组合物包含本发明公开化合物和药学上可接受的赋形剂,载体,辅剂,溶媒或它们的组合,该工艺包括混合各种成分。包含本发明公开化合物的药物组合物,可以在例如环境温度和大气压下混合来制备。
[0100]
本发明公开的化合物通常被配制成适合于通过所需途径对患者给药的剂型。例如,剂型包括那些适合于以下给药途径的剂型:(1)口服给药,例如片剂、胶囊剂、囊片剂、丸剂、含片剂、粉剂、糖浆剂、酏剂、混悬剂、溶液剂、乳剂、香包剂和扁囊剂;(2)胃肠外给药,例如无菌溶液剂、混悬剂和复溶粉末;(3)透皮给药,例如透皮贴片剂;(4)直肠给药,例如栓剂;(5)吸入,例如气雾剂、溶液剂和干粉剂;和(6)局部给药,例如乳膏剂、油膏剂、洗剂、溶液剂、糊剂、喷雾剂、泡沫剂和凝胶剂。本发明化合物优选口服给药。
[0101]
在一些实施方案中,本发明公开的化合物可以配制成口服剂型。在另一些实施方案中,本发明公开的化合物可以配制成吸入剂型。在另一些实施方案中,本发明公开的化合物可以配制成经鼻给药剂型。在又一些实施方案中,本发明公开的化合物可以配制成透皮给药剂型。还在一些实施方案中,本发明公开的化合物可以配制成局部给药剂型。
[0102]
在实际应用中,根据常规药物配制技术,本发明化合物作为活性成分可以与药用载体结合为紧密混合物。所述载体可根据施用(例如,经口或胃肠外(包括静脉内的))所需的制剂形式而采用多种形式。在制备口服剂型组合物时,可使用任何常规药用介质,例如,水、乙二醇、醇类、油类、防腐剂、矫味剂、着色剂等。在口服液体制剂的情况中,可使用任何常规药用介质,例如,酏剂、溶液剂和混悬剂;或载体例如糖、淀粉、稀释剂、崩解剂、润滑剂、成粒剂、粘合剂、微晶纤维素等。在口服固体制剂情况下,组合物可作为例如粉剂、硬和软胶囊以及片剂形式存在。相对液体剂型来说,优选固体口服剂型。
[0103]
本发明提供的药物组合物可以以压制片、研制片、可咀嚼锭剂、速溶片、复压片、肠溶片、糖衣或薄膜衣片来提供。
[0104]
本发明提供的药物组合物可以以软胶囊或硬胶囊来提供,其可以由明胶、甲基纤维素、淀粉或海藻酸钙来制备。
[0105]
本发明提供的药物组合物可以通过注射、输注或植入肠胃外给药,用于局部或全身给药。如本发明使用的肠胃外给药包括静脉内、动脉内、腹膜内、鞘内、心室内、尿道内、胸骨内、颅内、肌内、滑膜内和皮下给药。
[0106]
本发明提供的药物组合物可以配制成适于肠胃外给药的任何剂型,包括溶液、混悬剂、乳剂、胶束、脂质体、微球、纳米体系和适于在注射前在液体中制成溶液或混悬液的固体形式。这样的剂型可以根据药物科学领域的技术人员已知的常规方法来制备(参见remington's pharmaceutical sciences(mack publishing company))。
[0107]
另一方面,本发明所公开的药物组合物可以配制成适于对患者吸入给药的任何剂型,例如干粉剂、气雾剂、混悬剂或溶液组合物。
[0108]
适合于透皮给药的药物组合物可制备成不连续的贴片剂,意在与患者的表皮保持紧密接触一段延长的时间。例如,可通过离子渗透从贴片剂中递送活性成分,如pharmaceutical research,3(6),318(1986)中的一般描述。
[0109]
适合于局部给药的药物组合物可以被配制成油膏剂、乳膏剂、混悬剂、洗剂、粉剂、溶液剂、糊剂、凝胶剂、喷雾剂、气雾剂或油剂。
[0110]
在一种优选的实施方式中,本发明的上述化合物或包含本发明的上述化合物的药物组合物可以一次性给药,或者根据给药方案,在指定时间段内,在不同的时间间隔给药若干次。例如,每天给药一次、两次、三次或四次。在一种优选的实施方式中,每天给药一次。在又一种优选的实施方式中,每天给药两次。可以给药直至达到想要的治疗效果或无限期地维持想要的治疗效果。本发明化合物或包含本发明化合物的药物组合物的合适给药方案取决于该化合物的药代动力学性质,例如吸收、分布和半衰期,这些可以由技术人员测定。此外,本发明化合物或包含本发明化合物的药物组合物的合适给药方案,包括实施该方案的持续时间,取决于被治疗的疾病,被治疗疾病的严重程度、被治疗患者的年龄和身体状况、被治疗患者的医疗史、同时疗法的性质、想要的治疗效果等在技术人员知识和经验范围内的因素。这样的技术人员还应该理解,对于个体患者对给药方案的反应,或随着时间推移个体患者需要变化时,可要求调整适宜的给药方案。
[0111]
本发明化合物可以与一种或多种其他附加治疗剂同时,或在其之前或之后给药。本发明化合物可以与其他附加治疗剂通过相同或不同给药途径分别给药,或与之以同一药物组合物形式给药。
[0112]
在本发明中,术语“治疗”也包括“预防”,除非存在与此相反的具体说明。术语“治疗(的)”和“治疗(地)”应该作相应的理解。
[0113]
本发明所使用的术语“治疗”任何疾病或病症,在其中一些实施方案中指改善疾病或病症(即减缓或阻止或减轻疾病或其至少一种临床症状的发展)。在另一些实施方案中,“治疗”指缓和或改善至少一种身体参数,包括可能不为患者所察觉的身体参数。在另一些实施方案中,“治疗”指从身体上(例如稳定可察觉的症状)或生理学上(例如稳定身体的参数)或上述两方面调节疾病或病症。在另一些实施方案中,“治疗”指预防或延迟疾病或病症的发作、发生或恶化。
[0114]
本发明使用的术语“预防”指疾病或障碍的风险的减少(即:使疾病的至少一种临床症状在主体内停止发展,该主体可能面对或预先倾向面对这种疾病,但还没有经历或表现出疾病的症状)。
[0115]
本发明还提供了一种预防凝血的方法,该方法包括给予所述患者治疗有效量的上述达玛烷型三萜类化合物或上述药物组合物。
[0116]
本发明还提供了一种预防和/或治疗血栓形成的方法,该方法包括给予所述患者
治疗有效量的上述达玛烷型三萜类化合物或上述药物组合物。
[0117]
本发明所使用的术语“治疗有效量”是指足以显示出有意义的患者益处的各活性组分的总量。当使用单独的活性成分单独给药时,该术语仅指该成分。当组合应用时,该术语则是指不论组合、依次或同时给药时,都引起治疗效果的活性成分的组合量。由此意味着在适当的给予时,任何量的化合物足以在它给予的患者中达到所希望的预防或者治疗效果。通常,取决于待预防或者治疗的病症以及给予的途径。在给予日剂量为约0.01mg到约100mg/kg动物体重时即可以获得大致满意的结果,优选给予单一日剂量。对于大型哺乳动物而言,总的日剂量为约0.1mg到约1000mg,优选为约0.2mg到约50mg。在70kg的成年人情况中,总的日剂量大致为约0.2mg到200mg。所述剂量方案可以调整从而能提供最佳治疗响应。给予的量,给予的途径和进一步的治疗方案可能由治疗的临床医师决定,取决于例如:年龄、性别、患者的一般病症以及待治疗的疾病/症状的性质和严重性等因素。
[0118]
本发明所使用的术语“患者”是指人(包括成人和儿童)或者其他动物。在一些实施方案中,“患者”是指人。
[0119]
需要说明的是,在不冲突的情况下,本技术中的实施例及实施例中的特征可以相互组合。下面将结合实施例来详细说明本发明。
[0120]
以下结合具体实施例对本发明作进一步详细描述,这些实施例不能理解为限制本技术所要求保护的范围。
[0121]
实施例一
[0122]
制备gypensapogenin z
[0123]
制备步骤如下:
[0124]
取绞股蓝干燥全草药材5kg,加水75l回流提取3小时,提取2次,合并提取液,减压浓缩至5l,加0.5%盐酸水溶液1l,回流0.5小时,过滤,收集沉淀,经硅胶柱层析,以正己烷-乙酸乙酯(3.5∶1)洗脱,经氯仿-甲醇重结晶得到白色粉末gypensapogenin z 48mg。
[0125]
实施例二
[0126]
制备gypensapogenin z
[0127]
制备步骤如下:
[0128]
取绞股蓝干燥全草药材5kg,加水125l回流提取1小时,提取3次,减压浓缩至5l,加1.5%盐酸水溶液1l,回流0.5小时,过滤,收集沉淀,经硅胶柱层析,以正己烷-乙酸乙酯(3∶1)洗脱,经氯仿-甲醇重结晶得到白色粉末gypensapogenin z 45mg。
[0129]
实施例三
[0130]
制备gypensapogenin z
[0131]
制备步骤如下:
[0132]
取绞股蓝干燥全草药材5kg,加水100l回流提取2小时,提取1次,减压浓缩至5l,加1%盐酸水溶液1l,回流1小时,过滤,收集沉淀,经硅胶柱层析,以正己烷-乙酸乙酯(4∶1)洗脱,经氯仿-甲醇重结晶得到白色粉末gypensapogenin z 50mg。
[0133]
采用核磁共振等光谱法对所得gypensapogenin z进行结构鉴定。
[0134][0135]1h-nmr(cdcl3,400m):6.01,3.20,3.03,2.49,2.25,2.10,1.85,0.95,0.89,0.82,0.75;
[0136]
13
c-nmr(cdcl3,100m):197.5,175.6,144.5,132.1,129.3,78.8,55.6,50.6,50.0,46.8,44.1,40.4,39.0,38.9,37.1,35.4,35.2,31.5,28.5,27.8,27.3,25.0,24.0,21.1,19.6,18.2,16.2,15.8,15.5,15.3;
[0137]
hr-esi-ms:439.3555(c
30h46
o2 h,计算值:439.3569)。
[0138]
实施例四
[0139]
制备gypensapogenin c
[0140]
制备步骤如下:
[0141]
取绞股蓝干燥全草药材5kg,加水100l回流提取2小时,提取1次,减压浓缩至5l,加1%盐酸水溶液1l,回流1小时,过滤,收集沉淀,经硅胶柱层析,以正己烷-乙酸乙酯(5∶1)洗脱,经氯仿-甲醇重结晶得到白色粉末gypensapogenin c 60mg。
[0142]
采用核磁共振等光谱法对所得gypensapogenin c进行结构鉴定。
[0143][0144]1h-nmr(cdcl3,400m):6.96,3.20,3.02,2.50,2.29,2.08,1.86,0.97,0.95,0.89,0.82,0.75;
[0145]
13
c-nmr(cdcl3,100m):197.1,153.1,145.9,144.7,129.3,78.9,55.7,50.7,50.0,46.5,40.3,39.0,38.9,37.5,37.1,35.4,32.2,31.5,28.5,27.8,27.3,25.0,24.0,21.3,19.6,18.2,16.2,15.6,15.5,15.3;
[0146]
esi-ms:439(c
30h46
o2 h)。
[0147]
其中,gypensapogenin c的22位氢谱核磁位移约在7.0左右,而gypensapogenin z
的22位氢谱核磁位移约在6.0左右;gypensapogenin c的22位碳谱核磁位移约在146.0左右,而gypensapogeninz的22位碳谱核磁位移约在132.0左右。
[0148]
实施例五
[0149]
抗凝血活性-凝血酶原时间(pt)的测定
[0150]
取正常家兔,麻醉后,通过耳缘静脉取血,以1∶9(v/v)的比例加入用3.2%枸橼酸钠抗凝剂,混匀后,以3000转/分钟,4℃离心10min,收集血浆。将乏血小板血浆(ppp)及氯化钙组织凝血活酶溶液置37℃水浴中5分钟。另取适量的gypensapogenin c和gypensapogenin z,以dmso溶解后,加蒸馏水稀释至1μg/μl,作为供试品溶液。华法林作为阳性对照药。取适量的华法林,以dmso溶解后,加蒸馏水稀释至0.3μg/μl,作为阳性对照药溶液。以蒸馏水作为空白组溶液。按照凝血分析仪pt测定的操作要求,取空白组溶液50μl、阳性对照药溶液50μl和供试品溶液50μl加至测试杯中,自动测定血浆凝固终点时间,并记录供试品pt值。
[0151]
表1各样品凝血酶原时间(pt)
[0152][0153]
由表1数据可知,gypensapogenin z具有较强的抗外源性凝血作用,效果与阳性对照药华法林相当,而gypensapogenin c的抗外源性凝血作用不明显。针对凝血酶原时间(pt)而言,gypensapogenin z的抑制率是gypensapogenin c的抑制率约14.2倍,差异显著。
[0154]
实施例六
[0155]
抗凝血活性-活化部分凝血活酶时间(aptt)的测定
[0156]
如1.1凝血酶原时间(pt)的测定,同样方法制备乏血小板血浆,及空白组溶液、阳性对照药溶液和供试品溶液,将乏血小板血浆及aptt试剂,至37℃水浴中5分钟。按照凝血分析仪aptt测定操作要求,取空白组溶液50μl、阳性对照药溶液50μl和供试品溶液50μl加至测试杯中,自动测定血浆凝固终点时间,并记录供试品aptt值。
[0157]
表2各样品活化部分凝血活酶时间(aptt)
[0158][0159][0160]
由表2数据可知,gypensapogenin z具有较强的抗内源性凝血作用,效果与阳性对照药华法林相当,而gypensapogenin c的抗内源性凝血作用不明显。针对活化部分凝血活
酶时间(aptt)而言,gypensapogeninz的抑制率是gypensapogenin c的抑制率约20.52倍,差异显著。
[0161]
以上所述的仅是本发明的实施例,方案中公知的具体技术及特性等常识在此未作过多描述。应当指出,对于本领域的技术人员来说,在不脱离本发明的前提下,还可以作出若干变形和改进,这些也应该视为本发明的保护范围,这些都不会影响本发明实施的效果和专利的实用性。本技术要求的保护范围应当以其权利要求的内容为准,说明书中的具体实施方式等记载可以用于解释权利要求的内容。
[0162]
以上对本发明实施例进行了详细介绍,本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明仅用于帮助理解本发明的方法及其核心思想。同时,本领域技术人员依据本发明的思想,基于本发明的具体实施方式及应用范围上做出的改变或变形之处,都属于本发明保护的范围。综上所述,本说明书内容不应理解为对本发明的限制。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
