用于生产生物活性植物代谢物的重组细胞、提取物、可消费产品和方法
相关申请的交叉引用
1.本专利申请要求2019年10月25日提交的美国临时申请第62/925,941号的优先权。上述申请出于所有目的通过引用以其整体完全并入本文中。背景
2.n-羟基肉桂酸酰胺(hcaa)是通过羟基肉桂酰-coa硫酯和芳香胺的缩合合成的。羟基肉桂酰-coa硫酯包括肉桂酰-coa、对香豆酰-coa、咖啡酰-coa、阿魏酰-coa和芥子酰-coa,并且通过一系列酶(包括肉桂酸-4-羟化酶、香豆酸-3-羟化酶、咖啡酸o-甲基转移酶、阿魏酸-5-羟化酶和羟基肉桂酸:coa连接酶)从肉桂酸合成(douglas(1996)trends plant sci l:171-178)。
3.酪胺衍生的hcaa通常与病原体感染区域或伤口愈合区域附近的组织的细胞壁相关。此外,阿魏酰酪胺和阿魏酰奥克巴胺(feruloyloctapamine)是马铃薯(solanum tuberosum)块茎的天然和创伤周皮的共价细胞壁成分,并且是木栓质的芳香结构域的推定组分。hcaa的沉积被认为通过降低细胞壁的可消化性而产生对抗病原体的屏障。hcaa是通过羟基肉桂酰-coa硫酯与苯乙胺如酪胺或多胺如腐胺的缩合形成的。酪胺衍生的hcaa生物合成的最终步骤由羟基肉桂酰-coa:酪胺n-(羟基肉桂酰)转移酶催化。
4.通过编码分别从拟南芥(arabidopsis thaliana)和胡椒克隆的对香豆酸:辅酶a连接酶和酪胺n-羟基肉桂酰转移酶的两个生物合成基因的异源表达,在大肠杆菌中已经产生了植物特异性的阿魏酰酪胺、对香豆酰酪胺和咖啡酰酪胺(kang等人,(2009)biotechnol.lett.31(9):1469-75)。另外,已经描述了从单一自加工多肽表达酪胺n-羟基肉桂酰转移酶和酪氨酸脱羧酶的转基因水稻种子(park等人,(2009)biotechnol.lett.31(6):911-5)。此外,通过在大肠杆菌中表达几个基因,包括4-香豆酸-coa连接酶、酪胺n-羟基肉桂酰转移酶或苯乙胺n-羟基肉桂酰转移酶、苯丙氨酸脱羧酶或酪氨酸脱羧酶和酪氨酸解氨酶,并工程化莽草酸代谢途径以增加大肠杆菌中的内源性酪氨酸浓度来重建用于合成n-羟基肉桂酰苯乙胺和酪胺的代谢途径(sim等人,(2015)microbial cell fact.14:162)。公开内容的概述
5.本公开内容提供了能够产生含酪胺的羟基肉桂酸酰胺的重组真核宿主细胞,其中所述重组宿主过量产生l-酪氨酸或l-苯丙氨酸;并且具有编码用于制备羟基肉桂酰-coa酯的苯丙素coa途径的一种或多种酶的一种或多种核酸分子;编码酪氨酸脱羧酶(e.c.4.1.1.25)的核酸分子;以及编码酪胺n-羟基肉桂酰转移酶(e.c.2.3.1.110)的核酸分子。在一些实施方案中,含酪胺的羟基肉桂酸酰胺是n-咖啡酰酪胺、n-阿魏酰酪胺、5-羟基阿魏酰酪胺、对香豆酰酪胺、肉桂酰酪胺或芥子酰酪胺。在其它实施方案中,编码用于制备羟基肉桂酰-coa酯的苯丙素coa途径的一种或多种酶的一种或多种核酸分子包括苯丙氨酸解氨酶、4-香豆酸-coa连接酶、肉桂酸-4-羟化酶、香豆酸-3-羟化酶、咖啡酰-coa o-甲基转移酶、阿魏酸-5-羟化酶、咖啡酸/5-羟基阿魏酸o-甲基转移酶、酪氨酸解氨酶或以上的组合。在其它实施方案中,宿主细胞过量产生s-腺苷甲硫氨酸。还提供了使用重组真核宿主细
胞产生含酪胺的羟基肉桂酸酰胺的方法,以及含有含酪胺的羟基肉桂酸酰胺的提取物和可消费产品。附图简述
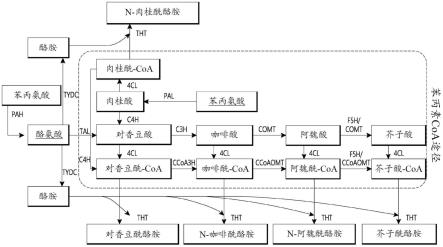
6.图1描述了从羟基肉桂酰-coa酯和酪胺生物合成含酪胺的羟基肉桂酸酰胺的示意性途径。然而,为了清楚起见,没有示出辅因子和辅底物。苯丙素途径的酶是苯丙氨酸解氨酶(pal,e.c.4.3.1.24);肉桂酸-4-羟化酶(c4h,e.c.1.14.14.91);对香豆酰-coa连接酶(4cl,e.c.6.2.1.12);香豆酸-3-羟化酶(c3h,e.c.1.14.13.-);香豆酰-coa 3-羟化酶(ccoa3h,或5-o-(4-香豆酰)-d-奎尼酸3
’‑
单加氧酶,e.c.1.14.14.96);咖啡酰-coa o-甲基转移酶(ccoaomt,e.c.2.1.1.104);阿魏酸-5-羟化酶(f5h,e.c.1.14.-.-);和咖啡酸/5-羟基阿魏酸o-甲基转移酶(comt,e.c.2.1.1.68)。在含酪胺的羟基肉桂酸酰胺的生物合成中的另外的酶包括羟基肉桂酰coa:酪胺羟基肉桂酰转移酶(tht,e.c.2.3.1.110)、酪氨酸解氨酶(tal,e.c.4.3.1.23)、苯丙氨酸羟化酶(pah,e.c.1.14.16.1)和酪氨酸脱羧酶(tydc,e.c.4.1.1.25)。
7.图2显示了在酿酒酵母(saccharomyces cerevisiae)和大肠杆菌中用于过量产生苯丙氨酸和/或酪氨酸的工程化途径的示意图。赤藓糖4-磷酸(e4p)、磷酸烯醇丙酮酸(pep)、3-脱氧-d-阿拉伯-庚糖酮酸7-磷酸(dahp)、3-脱氢奎尼酸(dhq)、3-脱氢-莽草酸酯(dhs)、莽草酸酯(shik)、莽草酸-3-磷酸酯(shp)、5-烯醇丙酮酰莽草酸-3-磷酸(ep3p)、预苯酸(ppa)、苯丙酮酸盐(ppy)、对羟基-苯丙酮酸(hpp)、苯乙醛(pac)、对羟基-乙醛(p-pac)、l-苯丙氨酸(l-phe)、l-酪氨酸(l-tyr)、对香豆酸(p-ca)。“*”表示过表达的酶;框中的aro10和pdc5是敲除的,”fbr“表示抗反馈。公开内容详述
8.目前已经表明一类含酪胺的羟基肉桂酸酰胺对hnf4α(肝细胞核因子4α)表现出激动活性,hnf4α是一种调节参与维持平衡代谢(体内平衡)的基因表达的全局核转录因子。通过激动hnf4α活性,植物特异性酪胺衍生物可用于减轻游离脂肪酸的副作用,调节代谢,改善消化健康和解决代谢病症(如非酒精性脂肪肝病、非酒精性脂肪性肝炎和ii型糖尿病)的潜在发病机理。因此,本公开内容提供了用于重组生产这些生物活性植物代谢物的重组宿主细胞、提取物、食品和方法。
9.如本文所用,本公开内容的生物活性植物代谢物是具有式(i)的结构的含酪胺的羟基肉桂酸酰胺:
10.在一些实施方案中,r1、r2、r3、r4、r5、r6、r7、r8和r9各自独立地选自氢、氘、羟基、卤素、氰基、硝基、任选取代的氨基、任选取代的c-酰氨基、任选取代的n-酰氨基、任选取代的酯、任选取代的-(o)c
1-6
烷基、任选取代的-(o)c
1-6
烯基、任选取代的-(o)c
1-6
炔基、任选取代的-(o)c
4-12
环烷基、任选取代的-(o)c
1-6
烷基c
4-12
环烷基、任选取代的-(o)c
4-12
杂环基、任选取代的-(o)c
1-6
烷基c
4-12
杂环基、任选取代的-(o)c
4-12
芳基、任选取代的-(o)c
1-6
烷基c
5-12
芳基、任选取代的-(o)c
1-12
杂芳基和任选取代的-(o)c
1-6
烷基c
1-12
杂芳基。
11.在一些实施方案中,r1、r2、r3和r8各自独立地选自氢、氘、羟基、卤素、氰基、硝基、任选取代的氨基、任选取代的c-酰氨基、任选取代的n-酰氨基、任选取代的酯、任选取代的-(o)c
1-6
烷基、任选取代的-(o)c
1-6
烯基、任选取代的-(o)c
1-6
炔基、任选取代的-(o)c
4-12
环烷基、任选取代的-(o)c
1-6
烷基c
4-12
环烷基、任选取代的-(o)c
4-12
杂环基、任选取代的-(o)c
1-6
烷基c
4-12
杂环基、任选取代的-(o)c
4-12
芳基、任选取代的-(o)c
1-6
烷基c
5-12
芳基、任选取代的-(o)c
1-12
杂芳基和任选取代的-(o)c
1-6
烷基c
1-12
杂芳基,并且r4、r5、r6、r7和r9各自独立地是氢、氘、羟基或卤素;
12.在一些实施方案中,r1、r2和r8各自独立地选自氢、氘、羟基、卤素、氰基、硝基、任选取代的氨基、任选取代的c-酰氨基、任选取代的n-酰氨基、任选取代的酯、任选取代的-(o)c
1-6
烷基、任选取代的-(o)c
1-6
烯基、任选取代的-(o)c
1-6
炔基、任选取代的-(o)c
4-12
环烷基、任选取代的-(o)c
1-6
烷基c
4-12
环烷基、任选取代的-(o)c
4-12
杂环基、任选取代的-(o)c
1-6
烷基c
4-12
杂环基、任选取代的-(o)c
4-12
芳基、任选取代的-(o)c
1-6
烷基c
5-12
芳基、任选取代的-(o)c
1-12
杂芳基和任选取代的-(o)c
1-6
烷基c
1-12
杂芳基,并且r3、r4、r5、r6、r7和r9各自独立地是氢、氘、羟基或卤素。
13.在一些实施方案中,虚线键是存在或不存在的。
14.在一些实施方案中,x为ch2或o。
15.在一些实施方案中,z为chra、nra或o。
16.在一些实施方案中,ra选自氢、氘、羟基、卤素、氰基、硝基、任选取代的氨基、任选取代的c-酰氨基、任选取代的n-酰氨基、任选取代的酯、任选取代的-(o)c
1-6
烷基、任选取代的-(o)c
1-6
烯基、任选取代的-(o)c
1-6
炔基、任选取代的-(o)c
4-12
环烷基、任选取代的-(o)c
1-6
烷基c
4-12
环烷基、任选取代的-(o)c
4-12
杂环基、任选取代的-(o)c
1-6
烷基c
4-12
杂环基、任选取代的-(o)c
4-12
芳基、任选取代的-(o)c
1-6
烷基c
5-12
芳基、任选取代的-(o)c
1-12
杂芳基和任选取代的-(o)c
1-6
烷基c
1-12
杂芳基。
17.在一些实施方案中,式(i)化合物选自(e)-3-(3,4-二羟基苯基)-n-(4-乙氧基苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(2-甲氧基乙氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(2-(甲基磺酰基)乙氧基)苯乙基)丙烯酰胺、(e)-2-(4-(2-(3-(3,4-二羟基苯基)丙烯酰胺基)乙基)苯氧基)乙酸、(e)-2-(4-(2-(3-(3,4-二羟基苯基)丙烯酰胺基)乙基)苯氧基)乙酸乙酯、(e)-n-(4-(环丙基甲氧基)苯乙基)-3-(3,4-二羟基苯基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(3,3,3-三氟丙氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-((四氢-2h-吡喃-4-基)甲氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-((4-氟苄基)氧基)苯乙基)丙烯酰胺、(e)-n-(4-(氰基甲氧基)苯乙基)-3-(3,4-二羟基苯基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(吡啶-3-基甲氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(吡啶-2-基甲氧基)苯乙基)
丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(2-(二甲基氨基)乙氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-异丁氧基苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(吡啶-4-基甲氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-((4-甲氧基苄基)氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(氧杂环丁烷-3-基甲氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-((四氢-2h-吡喃-2-基)甲氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-((四氢呋喃-2-基)甲氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(噻吩-2-基氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(3,3-二甲基丁氧基)苯乙基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-(2-羟基乙氧基)苯乙基)丙烯酰胺、(e)-n-(4-((1h-四唑-5-基)甲氧基)苯乙基)-3-(3,4-二羟基苯基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-((1-甲基吡咯烷-2-基)甲氧基)苯乙基)丙烯酰胺、(e)-2-羟基-5-(3-((4-羟基苯乙基)氨基)-3-氧代丙-1-烯-1-基)苯基碳酸氢盐、(e)-3-(4-羟基-3-(吡啶-4-基氧基)苯基)-n-(4-羟基苯乙基)丙烯酰胺、(e)-3-(4-羟基-3-异丁氧基苯基)-n-(4-羟基苯乙基)丙烯酰胺、(e)-3-(3-(4-氟苯氧基)-4-羟基苯基)-n-(4-羟基苯乙基)丙烯酰胺、(e)-3-(3-(氰基甲氧基)-4-羟基苯基)-n-(4-羟基苯乙基)丙烯酰胺、(e)-2-(2-羟基-4-(3-((4-羟基苯乙基)氨基)-3-氧代丙-1-烯-1-基)苯氧基)乙酸、(e)-3-(3-羟基-4-(吡啶-4-yl甲氧基)苯基)-n-(4-羟基苯乙基)丙烯酰胺、(e)-3-(4-((4-氟苄基)氧基)-3-羟基苯基)-n-(4-羟基苯乙基)丙烯酰胺、(e)-3-(3-羟基-4-异丁氧基苯基)-n-(4-羟基苯乙基)丙烯酰胺、(e)-3-(4-(氰基甲氧基)-3-羟基苯基)-n-(4-羟基苯乙基)丙烯酰胺、(e)-n-(3-(3,4-二羟基苯基)丙烯酰基)-n-(4-羟基苯乙基)甘氨酸、(e)-3-(3,4-二羟基苯基)-n-(4-羟基苯乙基)-n-(吡啶-4-基甲基)丙烯酰胺、(e)-3-(3,4-二羟基苯基)-n-(4-羟基苯乙基)-n-异丁基丙烯酰胺、(e)-n-(氰基甲基)-3-(3,4-二羟基苯基)-n-(4-羟基苯乙基)丙烯酰胺或3-(3,4-二羟基苯基)-n-(4-羟基苯乙基)丙酰胺、3-(3,4-二羟基苯基)-n-(4-(甲基磺酰胺基)苯乙基)丙酰胺。
18.在一些实施方案中,本公开内容的生物活性植物代谢物是制备的含酪胺的羟基肉桂酸,其具有式(ii)的结构:
19.在一些实施方案中,r1、r2、r3和r4各自独立地选自氢、氘、羟基、卤素、氰基、硝基、任选取代的氨基、任选取代的c-酰氨基、任选取代的n-酰氨基、任选取代的酯、任选取代的-(o)c
1-6
烷基、任选取代的-(o)c
1-6
烯基、任选取代的-(o)c
1-6
炔基、任选取代的-(o)c
4-12
环烷基、任选取代的-(o)c
1-6
烷基c
4-12
环烷基、任选取代的-(o)c
4-12
杂环基、任选取代的-(o)c
1-6
烷基c
4-12
杂环基、任选取代的-(o)c
4-12
芳基、任选取代的-(o)c
1-6
烷基c
5-12
芳基、任选取代
(3,4-二羟基苯基)-n-(4-羟基苯乙基)-n-异丁基丙烯酰胺、(e)-n-(氰基甲基)-3-(3,4-二羟基苯基)-n-(4-羟基苯乙基)丙烯酰胺、3-(3,4-二羟基苯基)-n-(4-羟基苯乙基)丙酰胺或3-(3,4-二羟基苯基)-n-(4-(甲基磺酰胺基)苯乙基)丙酰胺。
24.在一些实施方案中,本公开内容的生物活性植物代谢物包括具有式(iii)的结构的含酪胺的羟基肉桂酸酰胺:其中每次出现的x可以独立地是c或n;z可以是-cr
6-或-so
2-。r1可以选自-oh、-och2ch2r7或-nhr8基团,或者r1与r5一起形成6元取代的杂环烷基环,r2和r3独立地选自氢或-ch2ch2r7基团,或者r2和r3一起形成5元或6元杂环烷基环;r4可以是氢或-ch2ch2r7基团;r5可以是存在或不存在的,并且当存在时是在一个或多个环原子上的取代基,并且每次出现时独立地是卤代、羟基、烷基、取代的烷基、烷氧基、取代的磺酰基、羧基酯、氨基、取代的氨基、氰基、芳基、取代的芳基、环烷基、杂芳基、取代的杂芳基;r6可以是h2、氧代、取代的烷基、螺环烷基或螺杂环烷基;r7是氢、羟基、烷基、取代的烷基、烷氧基、取代的磺酰基、羧基酯、氨基、取代的氨基、氰基、芳基、取代的芳基、环烷基、杂芳基、取代的杂芳基;r8可以是取代的磺酰基、取代的烷基、羧基酯或氨基羰基;并且虚线键可以是存在或不存在的。
25.在一些实施方案中,本公开内容的生物活性植物代谢物包括具有式(iv)的结构的含酪胺的羟基肉桂酸酰胺:其中r1是存在或不存在的,并且当存在时是在一个或多个环原子(例如,2、3和/或4位)上的取代基,并且对于每个环原子独立地是羟基基团、卤代基团、取代的或未取代的低级烷基或者取代或未取代的低级烷氧基;以及虚线键是存在或不存在的。根据本公开内容,含酪胺的羟基肉桂酸酰胺包括顺式
和反式异构体。
26.对于本文中的基团,以下括号内的下标进一步如下定义基团:“(cn)”定义基团中碳原子的确切数目(n)。例如,“c
1-c
6-烷基”表示具有1至6个碳原子(例如1、2、3、4、5或6个,或其中可衍生的任何范围(例如3-6个碳原子))的那些烷基。
27.术语“低级烷基”旨在意指含有1至6个碳原子的分支的或未分支的饱和单价烃基(即,c
1-c
6-烷基),如甲基、乙基、丙基、异丙基、叔丁基、丁基、正己基等。
28.类似地,低级烷氧基是具有结构-or的c
1-c6烷氧基,其中r是如上进一步定义的“烷基”。特定的烷氧基包括例如甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、叔丁氧基、异丁氧基、仲丁氧基、正戊氧基、1,2-二甲基丁氧基等。
29.本文所用的术语“卤代”是指氯代(cl)、氟代(f)、溴代(br)和碘代(i)基团。在特定的实施方案中,卤代基团是氟代基团。
30.在本文所述的任何基团中,取代的基团(例如,取代的低级烷基或取代的低级烷氧基)是指可用的氢被烷基、烯基、炔基、芳基、杂芳基、芳烷基、烷基芳基、杂芳烷基、杂芳基烯基、杂芳基炔基、烷基杂芳基、羟基、羟基烷基、烷氧基、芳氧基、芳烷氧基、烷氧基烷氧基、酰基、卤代、硝基、氰基、羧基、芳烷氧基羰基、杂芳基磺酰基、烷氧基羰基、烷基磺酰基、烷硫基、芳硫基、芳氧基羰基、芳基磺酰基、杂芳硫基、芳烷硫基、杂芳烷硫基、环烷基、杂环基或糖基替代。
31.本技术中所示结构的原子上的任何未定义的化合价都隐含地表示与该原子键合的氢原子。
32.在一些实施方案中,含酪胺的羟基肉桂酸酰胺具有式(v)的结构:其中,r2是存在或不存在的,并且当存在时是羟基或甲氧基;r3是存在或不存在的,并且当存在时是羟基;以及r4是存在或不存在的,并且当存在时是羟基或甲氧基。
[0033]“异构体”尤其是指旋光异构体(例如基本上纯的对映异构体、基本上纯的非对映异构体及其混合物)以及构象异构体(即,仅在其至少一个化学键的角度上不同的异构体)、位置异构体(特别是互变异构体)和几何异构体(例如,顺式-反式异构体)。
[0034]
在某些实施方案中,式(i)-(v)的含有酪胺的羟基肉桂酰胺选自:
[0035]
本公开内容的含酪胺的羟基肉桂酸酰胺已经在许多植物属中发现,包括茄属(solanum sp.)(例如,番茄、马铃薯、荨麻、辣椒和茄子),葱属(allium sp.)(例如,大蒜、洋葱和韭菜),蒺藜属(tribulus sp.)(例如,蒺藜)和番荔枝属(annona sp.)(例如,番荔枝(cherimoya)、番荔枝(custard apple)和番荔枝(sweetsop))。通常,本公开内容的生物合成方法可以如方案1中所述进行。
方案1
[0036]
更具体地,本公开内容的含酪胺的羟基肉桂酸酰胺的生物合成途径呈现在图1中。如图1所示,提供了能够产生含酪胺的羟基肉桂酸酰胺的重组宿主细胞,其中所述宿主细胞过量产生l-酪氨酸和/或l-苯丙氨酸,并且包括编码用于制备羟基肉桂酰-coa酯的苯丙素coa途径的一种或多种酶的一种或多种核酸分子;编码酪氨酸脱羧酶(e.c.4.1.1.25)的核酸分子;以及编码酪胺n-羟基肉桂酰转移酶(e.c.2.3.1.110)的外源性核酸分子。酪氨酸和苯丙氨酸过量产生
[0037]
表现出“l-酪氨酸或l-苯丙氨酸的过量产生”的宿主细胞是指与野生型细胞相比已经被遗传修饰以产生增加量的l-酪氨酸、l-苯丙氨酸或l-酪氨酸和l-苯丙氨酸两者的细胞。如本文所用,术语“苯丙氨酸”、“l-苯丙氨酸”、“phe”和“l-phe”可互换使用。同样,术语“酪氨酸”、“l-酪氨酸”、“tyr”和“l-tyr”可互换使用。
[0038]
许多细菌是经由莽草酸途径的芳香族化合物的天然生产者(bongaerts等人,(2001)metab.eng.3:289-300;ikeda等人,(2006)appl.microbial.biotechnol.69:615-626;sprenger等人,(2007)appl.microbial.biotechnol.75:739-749)。在该途径中,从葡萄糖通过中心代谢途径转化的磷酸烯醇丙酮酸(pep)和赤藓糖4-磷酸(e4p)最初组合以形成3-脱氧-d-阿拉伯-庚糖酮酸7-磷酸(dahp),然后将其转化为分支酸(chorismate)。从分支酸开始,该途径分支形成多种芳香族终产物,包括苯丙氨酸(phe)、酪氨酸(tyr)和色氨酸(trp)(图2)。为了提高芳香族化合物的生产率,已经产生了遗传修饰的菌株。例如,在phe生产中,最重要的步骤是莽草酸途径的第一步和最后一步。然而,这些步骤包括的酶,dahp合酶(由arog编码)和分支酸变位酶/预苯酸(prephenate)脱水酶(由phea编码)被phe强烈抑制。因此,已经研究和利用了抗反馈突变体(fbr)用于phe产生(kikuchi等人,(1997)appl.environ.microbiol.63:761-762;nelms等人,(1992)appl.environ.microbiol.58:
2592-2598)。另外,arog和phea两者的表达水平由转录阻抑物tyrr控制,使得tyrr的缺失对于phe产生也是有效的(berry(1996)trends biotechnol.14:250-256)。为了增强dahp前体pep和e4p的可用性,已经过表达转酮醇酶(tkta)和pep合酶(pps)基因(patnaik&liao(1994)appl.environ.microbiol.60:3903-3908),已经缺失pep羧化酶基因(ppc)(miller等人,(1987)j.ind.microbiol.2:143-149),已经过表达或缺失碳储存调节基因(csra或csrb)(tatarko&romeo(2001)curr.microbiol.43:26-32;yakandawala等人,(2008)appl.microbiol.biotechnol.78:283-291),并且葡萄糖转运系统已经从pep-依赖性糖磷酸转移酶系统(pts)交换到半乳糖通透酶(galp)-葡糖激酶(glk)系统(baez-viveros等人,(2004)biotechnol.bioeng.87:516-524;yi等人,(2003)biotechnol.prog.19:1450-1459)或运动发酵单胞菌(zymomonas mobilis)葡萄糖促进剂(glf)-glk系统(patnaik&liao(1994)appl.environ.microbiol.60:3903-3908)。这些修饰已经以合适的组合使用以增强芳香族化合物的产生。为了重定向合成l-酪氨酸,已经缺失了编码分支酸变位酶/预苯酸脱水酶的phea基因,并且已经插入了编码分支酸变位酶/预苯酸脱氢酶的tyra以及强的trc启动子,以在48小时内实现55g/l的l-tyr滴度(olsen等人,(2007)appl.microbiol.biotechnol.74(5):1031-40)。
[0039]
用于过量产生酪氨酸和/或苯丙氨酸的示例性细菌菌株包括但不限于表1中列出的菌株。表1
[0040]
在酿酒酵母中,经由芳香族氨基酸生物合成途径(aap)合成芳香族化合物(braus(1991)microbiol rev.55:349-70)。这种高度调节的途径是酵母代谢的中心节点并供给几种其它途径(例如醌、叶酸和埃利希(ehrlich)途径;图2)。使用通量平衡分析,已经显示赤藓糖-4-磷酸(e4p)的可用性可以通过缺失zwf1并过表达编码转酮醇酶的tkl1以逆转从糖酵解中间体果糖-6-磷酸(f6p)和甘油醛-3-磷酸(g3p)至e4p和木酮糖-5-磷酸(x5p)的通量来实现。这导致进入芳香族氨基酸途径的通量增加了7倍(app;deaner&alper(2017)metab.eng.40:14-22)。改善朝向aap的通量的另一种方法是转醛醇酶(tall)和烯醇酶2(eno2)的过表达(mao等人,(2017)biotechnol.lett.39(7):977-982)。tall有利于景天庚酮糖-7-磷酸(s7p)和g3p向e4p和f6p的转化,而eno2将2-磷酸甘油酸转化为磷酸烯醇丙酮酸(pep)。
[0041]
莽草酸途径的第一个酶促步骤由dahp合酶催化,其将e4p和pep缩合成3-脱氧-d-阿拉伯庚酮糖酸7-磷酸酯(dahp;图2)。ar03和ar04编码酵母中的两种dahp合酶同种型。ar03以及aro4
k229l
和ar07
fbr
过表达的联合缺失(以避免反馈抑制)增加了通过芳香族氨基酸途径的通量(luttik等人,(2008)metab.eng.10:141-153)。此外,酪氨酸不敏感突变体aro4
g226s
改善了酪氨酸衍生的柚皮素的产生(koopman等人,(2012)microb.cell fact.11:155)并且已经被用于产生酪氨酸衍生的阿片样物质(galanie等人,(2015)science 349:1095-100)。已经显示莽草酸途径的最后一步,即通过分支酸合酶(aro2)将epsp转化为分支酸(chorismite),是aap中的瓶颈。因此,已经显示aro2的过表达在来自酪氨酸的对香豆酸的水平方面提供了2倍的改善(mao等人,(2017)biotechnol.lett.39(7):977-982)。
[0042]
此外,在下游,从分支酸向酪氨酸和苯丙氨酸分支,由aro7催化的常见酶促步骤将分支酸转化为预苯酸(图2)。aro7是芳香族氨基酸生物合成途径的第三反馈调节酶。与过表达aro7的野生型同种型的同等工程化的菌株相比,aro7的突变(例如,aro7
g141s
或aro7
t226i
)
hydroxycinnamic acid)、4-羟基肉桂酸(4-hydroxycinnamic acid)或4-羟基肉桂酸(4-hydroxycinnamate))。香豆酰coa连接酶(4cl;e.c.6.2.1.12)将对香豆酸(和其它取代的肉桂酸)转化为相应的coa硫酯(即对香豆酰coa),其用于类黄酮、异类黄酮、木质素、软木脂和香豆素的生物合成(ehlting等人,(1999)plant j.19(1):9-20)。
[0047]
苯丙氨酸解氨酶广泛分布在植物(koukol等人,(1961)j.biol.chem.236:2692-2698)、真菌(bandoni等人,(1968)phytochemistry 7:205-207)、酵母(ogata等人,(1967)agric.biol.chem.31:200-206)和链霉菌(emes等人,(1970)can.j.biochem.48:613-622)中,但未在大肠杆菌或哺乳动物细胞中发现(hanson&havir,in:the enzymes(3
rd ed.)boyer ed.,academic:new york,1967;pp 75-167)。pal酶将苯丙氨酸转化为肉桂酸,其可以通过肉桂酸-4-羟化酶(c4h,e.c.1.14.14.91)进一步转化为对香豆酸。此外,由于c4h是细胞色素p450酶,因此也可以共表达细胞色素p450还原酶(cpr)。因此,在一些实施方案中,本公开内容的宿主细胞表达与c4h酶组合的pal酶。在另一个实施方案中,本公开内容的宿主细胞表达与c4h和cpr酶组合的pal酶。
[0048]
苯丙氨酸解氨酶在某种程度上也接受酪氨酸作为底物,将酪氨酸直接转化为对香豆酸。例如,分离自欧芹(appert等人,(1994)eur.j.biochem.225:491)或玉米(havir等人,(1971)plant physiol.48:130)的pal酶证明了使用酪氨酸作为底物的能力。类似地,分离自红冬孢酵母的pal酶(hodgins(1971)j.biol.chem.246:2977)也可以使用l-酪氨酸作为底物。此类酶在本文中被称为“pal/tal”酶(e.c.4.3.1.25;rosier等人,(1997)plant physiol.113:175-179)。因此,也可以由本公开内容的宿主细胞表达pal酶(尤其是pal/tal活性比为至少0.1的那些)。当需要产生表达编码pal/tal活性的野生型基因的重组有机体时,基因分离自玉米、小麦、欧芹、立枯丝核菌(rhizoctonia solani)、红冬孢酵母、近玫色锁掷孢酵母(sporobolomyces pararoseus)、红冬孢酵母和黄孢原毛平革菌(phanerochaete chrysosporium)(参见hanson&havir(1981)biochem.plants7:577-625)。作为说明,使用恶臭假单胞菌s12的芳香族氨基酸过量产生菌株,编码来自圆红冬孢酵母(rhodosporidium toruloides)的双功能pal/tal酶的pal基因已经显示出增加肉桂酸(nijkamp等人,(2005)appl.microbiol.biotechnol.69:170-77)和对香豆酸(nijkamp等人,(2007)appl.microbiol.biotechnol.74:617-624)的产生。类似地,来自拟南芥(atpa11或atpa12)的pal已经在酿酒酵母中用于将苯丙氨酸转化为肉桂酸(koopman等人,(2012)microb.cell fact.11:155)。
[0049]
导致产生对香豆酸的另一种生物合成途径是基于使用具有tal活性的酶(e.c.4.3.1.23)。代替用于将苯丙氨酸转化为对香豆酸的两个酶反应,tal将l-酪氨酸直接转化为对香豆酸。因此,在一些实施方案中,本公开内容的宿主细胞表达tal酶。
[0050]
pal和tal酶的分类主要由酶对每种底物的活性决定,其中分类是基于优选的底物来指定的。tal酶被定义为优先使用l-酪氨酸作为底物的那些,而pal酶被定义为优先使用l-苯丙氨酸作为底物的那些。然而,这些酶通常接受l-酪氨酸和l-苯丙氨酸作为底物,尽管程度不同。因此,在一些实施方案中,pal和tal酶通常被称为“pal/tal酶”。
[0051]
在一些实施方案中,可以通过例如将天然存在的pal基因突变成编码优先使用l-酪氨酸作为底物的酶的pal基因来实现对一种底物优于另一种底物的特异性(参见us 6,368,837或us 6,521,748)。可以使用多种方法对pal/tal酶进行诱变。用于诱变的合适方法
包括易错pcr(leung等人,(1989)techniques 1:11-15;zhou等人,(1991)nucleic acids res.19:6052-6052;spee等人,(1993)nucl.acids res.21:777-778)、体外诱变和体内诱变。蛋白质工程可以通过通常称为“基因改组”的方法(us5,605,793;us 5,811,238;us 5,830,721;和us 5,837,458),或通过基于三维结构和经典蛋白质化学的基本设计来实现。
[0052]
本公开内容中的pal、tal或pal/tal酶以及c4h酶的来源可以获自或来源于任何天然存在的来源。本公开内容中使用的合适的pal、tal、pal/tal和c4h酶的实例列在表3中。表3表3登录号获自genbank或uniprotkb/swiss-prot。
[0053]
在另一方面,使用具有苯丙氨酸羟化酶(pah,e.c.1.14.16.1)活性的酶将l-苯丙氨酸转化为l-酪氨酸。然后使用具有tal活性的酶将使用苯丙氨酸羟化酶产生的l-酪氨酸转化为对香豆酸。因此,在一些实施方案中,本公开内容的宿主细胞表达与tal酶组合的pah酶。pah活性可以是内源性的或被引入宿主细胞以增加酪氨酸的产生。pah酶是本领域众所周知的,并已经在变形菌中报道(zhao等人,(1994)proc.natl.acad.sci.usa.91:1366)。例如,铜绿假单胞菌(pseudomonas aeruginosa)具有包括苯丙氨酸羟化酶的多基因操纵子(zhao等人,(1994)proc.natl.acad.sci.usa.91:1366)。l-苯丙氨酸向l-酪氨酸的酶促转化在真核生物中也是已知的。人苯丙氨酸羟化酶在肝脏中特异性表达以将l-苯丙氨酸转化为l-酪氨酸(wang等人,(1994)j.biol.chem.269(12):9137-46)。本公开内容中pah酶的来源可以获自或来源于任何天然存在的来源。本公开内容中使用的合适的pah酶的实例列在表4中。表4来源有机体登录号紫色色杆菌(chromobacterium violaceum)aaa23115铜绿假单胞菌aaa25938geodia cydoniumcaa76184地毯草黄单胞菌(xanthomonas axonopodis)aam35066野油菜黄单胞菌(xanthomonas campestris)aam39475鼻疽诺卡菌(nocardia farcinica)bad55786原鸡属(gallus)np_001001298登录号获自genbank或uniprotkb/swiss-prot。
[0054]
根据一些实施方案,通过重组表达编码苯丙素途径的(i)pal和c4h,(ii)pal、c4h和cpr,(iii)pal/tal和c4h,(iv)pal/tal、c4h和cpr,(v)tal和/或(vi)pah和tal的核酸,宿主细胞经工程化以重组表达编码将由宿主细胞过量产生的一部分芳香族氨基酸转化为对香豆酸所需的酶的核酸。
[0055]
通过表达具有香豆酰-coa连接酶活性的酶,将重组宿主细胞产生的对香豆酸转化为对香豆酰-coa。香豆酰-coa连接酶(4cl,e.c.6.2.1.12)在本公开内容的上下文中用于催化对香豆酸和其它取代的肉桂酸(例如,肉桂酸、咖啡酸、阿魏酸和芥子酸)转化为相应的coa硫酯(即,对香豆酰基-coa、肉桂酰-coa、咖啡酰-coa,阿魏酰-coa和芥子酰-coa)。香豆酰-coa连接酶是本领域众所周知的。香豆酰-coa连接酶可以是宿主细胞内源性的或外源性的。在某些实施方案中,香豆酰-coa连接酶在宿主细胞内过表达以增加对香豆酰基-coa的产生。本公开内容中使用的可公开获得的香豆酰-coa连接酶的非限制性列表提供在表5中。表5
登录号获自genbank或uniprotkb/swiss-prot。
[0056]
在一个方面,基于将对香豆酸转化为对香豆酰-coa的能力选择香豆酰-coa连接酶。在另一方面,共表达多种香豆酰-coa连接酶以增加含酪胺的羟基肉桂酸酰胺的产生。
[0057]
为了分别从对香豆酸或对香豆酰-coa生产咖啡酸或咖啡酰-coa,重组宿主细胞还可以包括和表达编码香豆酸-3-羟化酶(c3h,e.c.1.14.13.-)或香豆酰-coa 3-羟化酶(ccoa3h,e.c.1.14.14.96)的核酸。类似地,对于分别从对香豆酸或对香豆酰-coa生产阿魏酸或阿魏酰-coa,重组宿主细胞还可以包括和表达编码香豆酸-3-羟化酶(c3h,e.c.1.14.13.-)或香豆酰-coa 3-羟化酶(ccoa3h,e.c.1.14.14.96)和咖啡酸/5-羟基阿魏酸o-甲基转移酶(comt,e.c.2.1.1.68)或咖啡酰-coa o-甲基转移酶(ccoaomt,e.c.2.1.1.104)的核酸。为了加速咖啡酰-coa向阿魏酰-coa的转化,从而增加最终产物的生产速率,可以向宿主细胞补充s-腺苷-甲硫氨酸(adomet),可以选择宿主细胞用于adomet的过量产生(choi等人,(2009)korean j.chem.eng.26(1):156-9)或任选地被工程化以过量产生adomet。作为说明,发现表达由酵母met13p n-末端催化结构域和拟南芥mthfr(atmthfr-1)c-末端调节结构域组成的嵌合蛋白的酵母菌株比野生型积累超过100倍的adomet(roje等人,(2002)j.biol.chem.277:4056-4061)。因此,在某些实施方案中,重组宿主细胞过量产生adomet。此外,为了合成芥子酰-coa,重组宿主细胞可以表达编码香豆酸-3-羟化酶(c3h,e.c.1.14.13.-)或香豆酰-coa 3-羟化酶(ccoa3h,e.c.1.14.14.96)、咖啡酸/5-羟基阿魏酸o-甲基转移酶(comt,e.c.2.1.1.68)或咖啡酰-coa o-甲基转移酶(ccoaomt,e.c.2.1.1.104)和阿魏酸-5-羟化酶(f5h,e.c.1.14.-.-)的核酸。用于产生这些羟基肉桂酰-coa酯的可公开获得的酶的非限制性列表提供在表6中。表6
登录号获自genbank或uniprotkb/swiss-prot。含酪胺的羟基肉桂酸酰胺的产生
[0058]
为了将羟基肉桂酰-coa酯(即,对香豆酰基-coa、肉桂酰-coa、咖啡酰-coa、阿魏酰-coa和芥子酰-coa)转化为相应的含酪胺的羟基肉桂酸酰胺,宿主细胞还具有并表达编码酪胺n-羟肉桂酰转移酶(tht,e.c.2.3.1.110)的核酸分子。酪胺n-羟基肉桂酰转移酶在本公开内容的上下文中用于将羟基肉桂酰-coa酯缀合至酪胺以产生含酪胺的羟基肉桂酸酰胺(即,n-咖啡酰酪胺、n-阿魏酰酪胺、对香豆酰酪胺、肉桂酰酪胺或芥子酰酪胺)。tht是本领域众所周知的,并且可以是宿主细胞内源性的或外源性的。在某些实施方案中,tht在宿主细胞内过表达。在本公开内容中使用的可公开获得的tht酶的非限制性列表提供在表7中。表7来源有机体登录号烟草p80969风铃辣椒(capsicum baccatum)pht30257墨西哥辣椒(capsicum annuum)pht64088np 001311493马铃薯np 001305481
番茄(solanum lycopersicum)np 001234022野生烟草(nicotiana attenuate)xp 019254384登录号获自genbank或uniprotkb/swiss-prot。
[0059]
为了提供酪胺的来源,本技术的宿主细胞还包含编码酪氨酸脱羧酶(tydc,e.c.4.1.1.25)的核酸分子。在本公开内容的上下文中使用的酪氨酸脱羧酶将酪氨酸转化为酪胺。tydc可以是宿主细胞内源性的或外源性的,并且优选在宿主细胞内过表达。在本公开内容中使用的可公开获得的tydc酶的非限制性列表提供在表8中。表8来源有机体登录号海氏肠球菌(enterococcus hirae)aaq73505短乳杆菌(lactobacillus brevis)afp73381中华猕猴桃(actinidia chinesis)pss05769酿酒葡萄(vitis vinifera)xp_003631850登录号获自genbank或uniprotkb/swiss-prot。
[0060]
如本文所用,术语“重组宿主”、“重组宿主细胞”或“宿主细胞”旨在指这样的宿主,其基因组已经被至少一个掺入的dna序列增强(augmented)。这样的dna序列包括但不限于不是天然存在的基因,通常不转录成rna或翻译成蛋白质(“表达的”)的dna序列,以及希望引入到非重组宿主中的其它基因或dna序列。应理解,通常通过稳定引入一种或多种重组基因来增强本文所述的重组宿主细胞的基因组。然而,自主的或复制的质粒或载体也可以在本公开内容的范围内使用。此外,本公开内容可以使用低拷贝数(例如单拷贝)或高拷贝数(如本文所例示的)质粒或载体来实践。
[0061]
通常,引入的dna最初不存在于作为dna受体的宿主中,而是在本公开内容的范围内以从给定的宿主中分离dna区段,并随后将该dna的一个或多个另外拷贝引入到相同的宿主中,例如,以增强基因产物的产生或改变基因的表达模式。在一些情况下,引入的dna将通过例如同源重组或定点诱变修饰或甚至替代内源性基因或dna序列。
[0062]
术语“重组基因”或“重组核酸分子”是指被引入受体宿主的基因或dna序列,无论相同或相似的基因或dna序列是否已经存在于这样的宿主中。在此上下文中的“引入的”或“增强的”在本领域中是已知意指经人之手引入或增强。因此,重组基因可以是来自另一种物种的dna序列,或者可以是源自或存在于同一种物种中的dna序列,但已经通过重组方法掺入宿主以形成重组宿主。应理解,引入到宿主中的重组基因可以与通常存在于被转化的宿主中的dna序列相同,并被引入以提供dna的一个或多个另外拷贝,从而允许该dna的基因产物的过表达或修饰表达。
[0063]
编码本文所述多肽的重组基因包括该多肽的编码序列,其在有义方向上与一个或多个适于表达该多肽的调控区可操作地连接。因为许多微生物能够表达来自多顺反子mrna的多种基因产物,如果需要,多种多肽可以在那些微生物的单一调控区的控制下表达。当调控区和编码序列被定位使得调控区有效调节序列的转录或翻译时,认为编码序列和调控区可操作地连接。通常,编码序列的翻译阅读框的翻译起始位点定位在单顺反子基因调控区下游1个至约50个核苷酸之间。
[0064]
在许多情况下,本文所述多肽的编码序列在重组宿主以外的物种中被鉴定,即是
异源核酸。本文所用的术语“异源核酸”是指引入重组宿主中的核酸,其中所述核酸并非天然存在于所述宿主中。因此,如果重组宿主是微生物,则编码序列可以来自其它原核或真核微生物,来自植物或来自动物。然而,在一些情况下,编码序列是宿主天然的序列,并被重新引入到该有机体中。天然序列通常可以通过存在与外源性核酸连接的非天然序列,例如,重组核酸构建体中天然序列侧翼的非天然调控序列而与天然存在的序列区分开。另外,稳定转化的外源性核酸通常整合在除了发现天然序列的位置之外的位置。
[0065]“调控区”或“调控序列”是指影响转录或翻译起始和速率以及转录或翻译产物的稳定性和/或迁移率的核苷酸序列。调控区包括但不限于启动子序列、增强子序列、应答元件、蛋白质识别位点、诱导元件、蛋白质结合序列、5’和3’非翻译区(utr)、转录起始位点、终止序列、聚腺苷酸化序列、内含子及其组合。调控区通常包括至少一个核心(基础)启动子。调控区还可以包括至少一个控制元件,如增强子序列、上游元件或上游激活区(uar)。通过定位调控区和编码序列,调控区可操作地连接到编码序列,使得调控区有效地调节序列的转录或翻译。例如,为了可操作地连接编码序列和启动子序列,编码序列的翻译阅读框的翻译起始位点通常定位在启动子下游一个至约五十个核苷酸之间。然而,调控区可以定位在翻译起始位点上游多达约5,000个核苷酸,或定位在转录起始位点上游约2,000个核苷酸。
[0066]
所包括的调控区的选择取决于几个因素,包括但不限于效率、选择性、可诱导性、所需的表达水平和在某些培养阶段期间的优先表达。对于本领域技术人员来说,通过适当地选择和定位相对于编码序列的调控区来调节编码序列的表达是常规问题。应当理解,可以存在一个以上的调控区,例如反式(intrans)、增强子、上游激活区、转录终止子和诱导元件。
[0067]
用于驱动相关基因在所需宿主细胞中表达的启动子是多种的,并且是本领域技术人员所熟悉的。宿主细胞中的表达可以以瞬时或稳定的方式完成。瞬时表达可以通过诱导与目的基因可操作连接的可调节启动子的活性来实现。稳定的表达可以通过使用与目的基因可操作连接的组成型启动子来实现。事实上,能够驱动这些基因的任何启动子都适用于本公开内容,包括但不限于fbain、fbainm、exp、fba1、gpat、cyc1、his3、gall、gal10、adh1、pgk、pros、gapdh、adci、trp1、ura3、leu2、eno、tpi;aoxi(特别可用于在毕赤酵母中表达);以及lac、trp、ipl、iprr、t7、tac和trc(特别可用于在大肠杆菌中表达)。
[0068]
当宿主细胞是酵母时,提供了在酵母细胞中起作用的转录和翻译区,特别是来自宿主物种(参见,例如,wo2004/101757)。启动子可以获自例如糖酵解途径中的基因,如醇脱氢酶,甘油醛-3-磷酸-脱氢酶,甘油醛-3-磷酸o-酰基转移酶,磷酸甘油酸变位酶、果糖二磷酸醛缩酶、磷酸葡萄糖异构酶、磷酸甘油酸激酶等;或可调节基因,如酸性磷酸酶、乳糖酶、金属硫蛋白、葡糖淀粉酶、翻译延伸因子ef1-cx(tef)蛋白(us6,265,185)、核糖体蛋白s7(us 6,265,185)等。可以使用多种调控序列中的任一种,这取决于是否需要组成型或诱导型转录、启动子在表达目的开放阅读框中的效率、构建的容易性等。
[0069]
已经发现翻译起始密码子“atg”周围的核苷酸序列影响酵母细胞中的表达。如果所需多肽在酵母中的表达较差,则基因可以是外源性的经修饰的核苷酸序列,以包括有效的酵母。
[0070]
翻译起始序列以获得最佳的基因表达。对于在酵母中的表达,这可以通过将低效率表达的基因与内源性酵母基因(优选高表达的基因)框内融合而进行定点诱变来完成。
[0071]
终止控制区也可以来源于优选宿主的各种天然基因。任选地,终止位点可能是不必要的,然而,如果包括的话是最优选的。终止区可以来源于获得起始区的基因的3’区或来源于不同的基因。大量的终止区是已知的,并且在各种宿主中发挥令人满意的功能(当在其来源的相同或不同属和种中使用时)。终止区的选择通常更多是为了方便而不是因为任何特定的特性。优选地,终止区来源于酵母基因,特别是酵母属、裂殖酵母属、假丝酵母属、耶氏酵母属或克鲁维酵母属。编码y-干扰素和α-2干扰素的哺乳动物基因的3’区也已知在酵母中起作用。终止控制区也可以来源于优选宿主天然的各种基因。任选地,终止位点可能是不必要的;然而,如果包括的话是最优选的。在一个实施方案中,终止子是选自lip2、pex20和xpr2的终止子。
[0072]
对于异源核酸,一个或多个基因可以例如在重组核酸构建体中在可用于含酪胺的羟基肉桂酸酰胺产生的“模块”中组合或更多。将多个基因或异源核酸组合在模块中促进模块在多种物种中的使用。例如,涉及l-酪氨酸和/或l-苯丙氨酸、羟基肉桂酰-coa酯、酪胺和含酪胺的羟基肉桂酸酰胺的生物合成的基因可以被组合,使得每个编码序列可操作地连接到单独的调控区,以形成含酪胺的羟基肉桂酸酰胺模块,用于在真核有机体中生产。可选地,该模块可以表达多顺反子信息,用于在原核宿主如rodobacter、大肠杆菌、芽孢杆菌或乳杆菌物种中生产含酪胺的羟基肉桂酸酰胺。除了可用于含酪胺的羟基肉桂酸酰胺生产的基因之外,重组构建体通常还含有复制起点以及用于在适当物种中维持构建体的一种或多种可选择标志物。
[0073]
应当理解,由于遗传密码的简并性,许多核酸可以编码特定的多肽;即,对于用作氨基酸密码子的许多三联体氨基,存在一个以上的核苷酸。因此,可以对给定多肽的编码序列中的密码子进行修饰,以便使用用于特定宿主(例如微生物)的适当密码子偏向表,获得在该宿主中的最佳表达。作为分离的核酸,这些修饰的序列可以作为纯化的分子存在,并且可以掺入到构建模块构建体中。
[0074]
标准重组dna和分子克隆技术可以用于制备本公开内容的构建体和重组宿主细胞。参见,例如,sambrook等人,(1989)molecular cloning:a laboratory manual,2nd ed.,cold spring harbor laboratory,cold spring harbor,ny;silhavy等人,(1984)experiments with gene fusions,cold spring harbor laboratory,cold spring harbor,ny;以及ausubel等人,(1987)in current protocols in molecular biology,wiley-interscience。
[0075]
本公开内容提供了产生含酪胺的羟基肉桂酸酰胺的重组宿主细胞,其具有编码用于过量产生l-酪氨酸和/或l-苯丙氨酸,生物合成羟基肉桂酰-coa酯和酪胺前体的酶的核酸,以及用于产生含酪胺的真核羟基肉桂酸宿主细胞的酪胺n-羟基肉桂酰转移酶是酰胺。原核生物和真核生物两者都预期用于根据本公开内容的用途,正如单细胞和细胞培养物中的细胞(例如细胞系)一样。合适细胞的实例包括细菌宿主细胞,如大肠杆菌或芽孢杆菌;酵母宿主细胞,如酿酒酵母;昆虫宿主细胞,如草地贪夜蛾(spodoptera frugiperda);或人宿主细胞,如hela和jurkat细胞。优选的真核宿主细胞是如来自假丝酵母、毕赤酵母和酵母的单倍体细胞。尽管可以使用细菌宿主细胞,但优选的是本公开内容使用真核宿主细胞,特别是来自酵母属、克鲁维酵母属、毕赤酵母属、汉逊酵母属、裂殖酵母属、克鲁维酵母属、耶氏酵母属和假丝酵母属的酵母宿主细胞的用途。作为用于生产本公开内容的化合物的代谢工
程平台,酿酒酵母具有若干吸引人的特点。除了其对分子和合成生物学技术的极好可及性之外,其真核生物性质促进植物来源的生物合成基因的功能性表达。例如,酿酒酵母可以功能性地表达含有细胞色素p450的酶,并且其亚细胞区室化与植物细胞的亚细胞区室化相当。最后,其gras(通常被认为是安全的)状态促进了随后用于生产用于哺乳动物的化合物的应用。因此,在某些实施方案中,宿主细胞优选是真核宿主细胞,最优选是酿酒酵母。
[0076]
含有指导外源性蛋白高水平表达的调控序列的微生物表达系统和表达载体是本领域技术人员众所周知的。这些中的任一种都可用于构建嵌合基因以在宿主细胞中生产含酪胺的羟基肉桂酸酰胺。然后可以经由转化将这些嵌合基因引入到适当的微生物中以允许高水平的酶的表达。
[0077]
一旦制备了用于在宿主细胞中表达的适当的表达构建体,将其置于能够在宿主细胞中自主复制的质粒载体中,或者将其直接整合到宿主细胞的基因组中。表达盒的整合可以在宿主基因组内随机发生,或者可以通过使用含有与宿主基因组同源的足以靶向与宿主基因座重组的区域的构建体来靶向。当构建体靶向内源性基因座时,所有或一些转录和翻译调控区可以由内源性基因座提供。
[0078]
当两个或更多个基因从单独的复制载体表达时,希望每种载体具有不同的选择手段,并且应缺乏与其它构建体的同源性,以维持稳定的表达并防止构建体之间的元件重配。可以通过实验确定引入构建体的调控区、选择手段和繁殖方法的明智选择,使得所有引入的基因都以必需的水平表达,以提供所需产物的合成。
[0079]
具有目的编码区的构建体可以通过任何标准技术引入到宿主细胞中。这些技术包括转化(例如,乙酸锂转化[guthrie,c.,methods in enzymology,194:186-187(1991)])、原生质体融合、生物射弹冲击(biolistic impact)、电穿孔、显微注射或将目的基因引入宿主细胞的任何其它方法。
[0080]
为方便起见,通过任何方法操作以摄取dna序列(例如表达盒)的宿主细胞在本文中将被称为“转化的”或“重组的”。转化的宿主将具有表达构建体的至少一个拷贝,并且可以具有两个或更多个拷贝,这取决于基因是整合到基因组中,扩增的还是存在于具有多个拷贝数的染色体外元件上。转化的宿主细胞可以通过选择在引入的构建体上包含的标志物来鉴定。
[0081]
可选地,可以将单独的标志物构建体与所需构建体共转化,因为许多转化技术将许多dna分子引入宿主细胞。通常,选择转化的宿主在选择性培养基上生长的能力。选择性培养基可以掺入抗生素或缺乏未转化的宿主生长所必需的因子,如营养物或生长因子。引入的标志物基因可以赋予抗生素抗性或编码必需的生长因子或酶,从而当在转化的宿主中表达时允许在选择性培养基上生长。当可以直接或间接检测表达的标志物蛋白时,也可以发生转化宿主的选择。标志物蛋白可以单独表达或作为与另一种蛋白的融合物表达。标志物蛋白可以通过其酶活性检测(例如,β-半乳糖苷酶可以将底物x-gal[5-溴-4-氯-3-吲哚基-β-d-吡喃半乳糖苷]转化为有色产物,并且荧光素酶可以将荧光素转化为发光产物);或其发光或修饰特点(例如,当用维多利亚多管发光水母(aequorea victoria)照射时绿色荧光蛋白发蓝光)。可选地,抗体可以用于检测例如目的蛋白上的标志物蛋白或分子标签。可以例如通过视觉,或通过技术如facs或使用抗体淘选来选择表达标志物蛋白或标签的细胞。为了选择酵母转化体,可以使用在酵母中起作用的任何标记物。优选用于本文的是对卡
那霉素、潮霉素和氨基糖苷g418的抗性,以及在缺乏尿嘧啶或亮氨酸的培养基上生长的能力。
[0082]
除了重组宿主细胞之外,本公开内容还包括使用重组宿主细胞生产含酪胺的羟基肉桂酸酰胺的方法。根据本公开内容的方法,提供了能够产生含酪胺的羟基肉桂酸酰胺的重组真核宿主细胞,并培养足以使所述重组真核宿主细胞产生含酪胺的羟基肉桂酸酰胺的时间。一旦产生,从重组真核宿主细胞或从培养上清液中分离含酪胺的羟基肉桂酸酰胺。通常,可针对特定目的编码区的高水平表达而优化的培养基条件包括碳源的类型和量、氮源的类型和量、碳/氮比、氧水平、生长温度、ph、生物质生产阶段的长度和细胞收获时间。目的微生物,如酵母,在复合培养基(例如酵母提取物-蛋白胨-葡聚糖肉汤(ypd))或限定的基本培养基中生长,所述基本培养基缺乏生长所必需的组分,从而迫使选择所需的表达盒(例如酵母氮源(difco laboratories,detroit,mi))。
[0083]
本公开内容中的发酵或培养基必须含有用于生产含酪胺的羟基肉桂酸酰胺的合适碳源。合适的碳源可以包括但不限于:单糖(例如葡萄糖、果糖),二糖(例如乳糖、蔗糖),寡糖,多糖(例如淀粉、纤维素或其混合物),糖醇(例如甘油)或来自可再生原料(例如干酪乳清渗透物、玉米浆、甜菜糖蜜、大麦芽)的混合物。另外,碳源可以包括烷烃、脂肪酸、脂肪酸的酯、甘油单酯、甘油二酯、甘油三酯、磷脂和脂肪酸的各种商业来源,包括植物油(例如大豆油)和动物脂肪。另外,碳源可以包括一碳源(例如,二氧化碳、甲醇、甲醛、甲酸盐、含碳的胺),已经证明其代谢转化为关键的生化中间体。因此,预期本公开内容中使用的碳源可以涵盖多种含碳源,并且将仅受宿主有机体的选择的限制。尽管预期所有上述碳源及其混合物都适用于本公开内容,但优选的碳源是糖和/或脂肪酸。最优选的是含有10-22个碳的葡萄糖和/或脂肪酸。
[0084]
氮可以由无机(例如(nh4)2so4)或有机源(例如尿素或谷氨酸)提供。除了适当的碳源和氮源之外,发酵培养基还必须含有合适的矿物质、盐、辅因子、缓冲液、维生素和本领域技术人员已知的适于微生物生长的其它组分。
[0085]
可选地或除了从碳源(例如,葡萄糖或糖蜜)生产含酪胺的羟基肉桂酸酰胺之外,本公开内容还提供了用生物合成途径中间的一种或多种底物外源性补充发酵罐培养基以生产含酪胺的羟基肉桂酸酰胺。因此,在其它方面,可以将l-苯丙氨酸、l-酪氨酸、肉桂酸、对香豆酸、咖啡酸、阿魏酸、芥子酸和/或s-腺嘌呤基-l-甲硫氨酸外源提供到本公开内容的重组宿主细胞。本领域技术人员将认识到,需要平衡从芳香族氨基酸生产到含酪胺的羟基肉桂酸酰胺的生产的碳流,使得游离芳香族氨基酸的浓度降低对重组宿主细胞的活力或健康无害。因此,在一些实施方案中,可以将l-苯丙氨酸和/或l-酪氨酸外源补充到培养基中以增加含酪胺的羟基肉桂酸酰胺的产生。
[0086]
可以使用本领域已知的方法培养本公开内容的重组宿主细胞。例如,可以通过在合适的培养基中并且在允许目的编码区表达的条件下进行的摇瓶培养、实验室或工业发酵罐中的小规模或大规模发酵培养细胞。当需要商业生产含酪胺的羟基肉桂酸酰胺时,可以应用多种发酵方法。例如,可以通过分批、补料分批或连续发酵工艺生产从重组宿主过表达的特异性基因产物的大规模生产。
[0087]
分批发酵工艺是一个封闭的系统,其中培养基组成在该过程开始时是固定的,并且除了在工艺中维持ph和氧气水平所需的那些之外,不再进行添加。因此,在培养过程开始
时,用所需的有机体接种培养基,并且允许在不向培养基中添加另外来源(即,碳源和氮源)的情况下发生生长或代谢活性。在分批工艺中,系统的代谢物和生物质组成不断变化直到培养终止。在典型的分批工艺中,细胞通过静态迟缓期进行到高生长对数阶段,最后进行到稳定期,其中生长速率降低或停止。如果不加以处理,处于稳定期的细胞将最终死亡。标准分批工艺的一种变型是补料分批工艺,其中在发酵工艺过程中将源连续地加入到发酵罐中。补料分批工艺也适用于本公开内容。当分解代谢物抑制易于抑制细胞的代谢时,或者当需要在任何时候在培养基中具有有限量的源时,补料分批工艺是有用的。在补料分批系统中的源浓度的测量是困难的,因此可以基于可测量因素(如ph、溶解氧和废气(例如co2)的分压)的变化来估计。分批和补料分批培养方法是本领域中常见的和众所周知的,并且实例biotechnology:a可以见于以下教科书中:thomas d.brock of industrial microbiology,2
nd ed.,(1989)sinauer deshpande,mukund v.,(1992).associates sunderland,mass.;或appl.biochem.biotechnol.,36:227。
[0088]
含酪胺的羟基肉桂酸酰胺的商业生产也可以通过连续发酵工艺完成,其中将确定成分培养基连续加入到生物反应器中,同时除去等量的培养物体积用于产物回收。连续培养通常将细胞维持在生长的对数期。对一种因子的连续或半连续调节或影响细胞生长或以恒定的细胞密度结束。培养方法允许产生浓度的任何数量的因子。例如,一种方法可以限制碳源并允许所有其它参数调节代谢。在其它系统中,影响生长的许多因素可以连续改变,同时通过培养基浊度测量的细胞浓度保持恒定。连续系统努力维持稳定状态生长,因此细胞生长速率必须与由于培养基从培养物中取出而导致的细胞损失相平衡。用于连续培养工艺的调节营养物和生长因子的方法,以及使产物形成速率最大化的技术在工业微生物领域中是众所周知的。
[0089]
含酪胺的羟基肉桂酸酰胺可以通过溶剂提取(例如,分配)或沉淀,用活性炭处理,蒸发,过滤,色谱分离或其组合从宿主细胞或从培养上清液中提取。溶剂提取可以使用例如正戊烷、己烷、丁烷、氯仿、二氯甲烷、二乙醚、乙腈、水、丁醇、异丙醇、乙醇、甲醇、冰醋酸、丙酮、诺氟烷(hfa134a)、乙酸乙酯、二甲亚砜、七氟丙烷(hfa227)和亚临界或超临界流体如液体二氧化碳和水或其任意比例的组合进行。当使用诸如上文列出的溶剂时,所得提取物通常含有非特异性脂溶性物质。这可以通过多种方法去除,包括“冬化”,其涉及冷却至指定温度,通常为-20℃,随后过滤或离心以去除蜡制压载物(waxy ballast),用亚临界或超临界二氧化碳或非极性溶剂(例如己烷)萃取和蒸馏。
[0090]
富含含酪胺的羟基肉桂酸酰胺的提取物理想地通过色谱分离获得。色谱分离通常包括柱色谱法,并且可以基于分子大小、电荷、溶解度和/或极性。根据色谱方法的类型,可以用由例如葡聚糖、琼脂糖、聚丙烯酰胺或二氧化硅组成的基质材料进行柱色谱法,并且可以包括溶剂如二甲亚砜、吡啶、水、二甲基甲酰胺、甲醇、盐水、二氯乙烷、氯仿、丙醇、乙醇、异丁醇、甲酰胺、二氯甲烷、丁醇、乙腈、异丙醇、四氢呋喃、二噁烷、氯仿/二氯甲烷等。
[0091]
通常,色谱步骤的产物以多种级分收集,然后可以使用任何合适的分析技术(例如,薄层色谱法、质谱法)测试所需化合物的存在。然后可以选择富集所需化合物的级分用于进一步纯化。
[0092]
作为替代方案或与色谱法结合,可以进行结晶以获得高纯度的含酪胺的羟基肉桂酸酰胺。通过改变温度和/或溶液的组成,例如通过去除乙醇,和/或调节ph以促进沉淀,随
后过滤或离心沉淀的晶体或油,来调节含酪胺的羟基肉桂酸酰胺的溶解度。
[0093]
作为说明,通过将宿主细胞或培养上清液在室温下经受80%乙醇处理,过滤并浓缩80%乙醇提取物,将浓缩的提取物重悬于水中,用己烷分配水溶液,向水层中加入氯仿,并用硅胶对氯仿层进行液相色谱,获得包含n-反式-咖啡酰酪胺的提取物。参见例如ko等人,(2015)internatl.j.mol.med.36(4):1042-8。
[0094]
包含羟基肉桂酸酰胺的提取物的提取可以使用常规技术,如色谱法(hplc)进行或含有的高酪胺使用高效液相薄层色谱法(hptlc)标准化。术语“标准化提取物”是指通过鉴定提取物中存在的特征成分或生物活性标志物而标准化的提取物。表征可以例如通过分析光谱数据如质谱(ms),红外(ir)和核磁共振(nmr)光谱数据来进行。
[0095]
基本上纯的含酪胺的羟基肉桂酸酰胺或包含含酪胺的羟基肉桂酸酰胺的提取物可以与载体组合并且以任何合适的形式提供以供对象食用或施用至对象。合适的可消耗形式包括但不限于膳食补充剂、食品成分或添加剂、食品(例如功能性食品)、医学食品、保健品或药物组合物。
[0096]
食物成分或添加剂是旨在直接或间接导致其成为任何食物的组分或以其它方式影响任何食物特点的可食用物质(包括旨在用于生产、制造、包装、加工、制备、处理、包装、运输或保存食物的任何物质)。食品,特别是功能性食品,是在加工过程中强化或富集以包括另外的补充营养物和/或有益成分的食品。根据本公开内容的食品可以例如呈黄油、人造黄油、甜味或咸味涂抹料、饼干、保健棒、面包、蛋糕、谷物、糖果、糕点糖果、酸奶或发酵乳产品、基于汁液和基于蔬菜的饮料、奶昔、调味水、发酵饮料(例如红茶菌或发酵马黛茶)、方便的小吃如焙烤或油炸的蔬菜片或其它挤压的小吃产品或者任何其它合适食品的形式。
[0097]
膳食补充剂是由口腔摄取的含有本公开内容的化合物或提取物并且旨在补充饮食的产品。保健品是来源于食品来源的产品,除了在食品中发现的基本营养价值之外,其还提供了额外的健康益处。药物组合物被定义为旨在在疾病的诊断、治愈、减轻、治疗或预防中提供药理学活性或其它直接作用,或者影响人或其它动物的身体的结构或任何功能的药物产品的任何组分。膳食补充剂、保健品和药物组合物可以以许多形式存在,如片剂、包衣片剂、丸剂(pills)、胶囊剂、小丸(pellets)、颗粒剂、软凝胶剂(softgels)、软胶囊剂(gelcaps)、液体、散剂、乳剂、混悬剂、酏剂、糖浆剂和任何其它适合使用的形式。
[0098]
本文所用的短语“载体”意指涉及将主题化合物从一个器官或身体的一部分携带或运输至另一个器官或身体的一部分的材料、组合物或媒介物,如液体或固体填充剂、稀释剂、赋形剂、制造助剂(例如润滑剂、滑石粉、硬脂酸镁、硬脂酸钙或硬脂酸锌或硬脂酸)或溶剂封装材料。每种载体应该与制剂的其它成分相容并且对对象无害。可用作载体的材料的一些实例包括:(1)糖,如乳糖、葡萄糖和蔗糖;(2)淀粉,如玉米淀粉和马铃薯淀粉;(3)纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素、乙酸纤维素和羟丙基甲基纤维素;(4)粉末状黄蓍胶;(5)麦芽;(6)明胶;(7)滑石;(8)赋形剂,如可可脂和栓剂蜡;(9)油,如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;(10)二醇,如丙二醇;(11)多元醇,如甘油、山梨糖醇、甘露糖醇和聚乙二醇;(12)酯,如油酸乙酯和月桂酸乙酯;(13)琼脂;(14)缓冲剂,如氢氧化镁和氢氧化铝;(15)藻酸;(16)无热原水;(17)等渗盐水;(18)林格氏溶液;(19)乙醇;(20)ph缓冲溶液;(21)聚酯、聚碳酸酯和/或聚酸酐;(21)磷脂和磷脂衍生物;以及(23)常规制剂中使用的其它无毒相容性物质。
[0099]
对于制备固体组合物,如片剂或胶囊,将化合物或提取物与载体(例如常规的压片成分,如玉米淀粉、乳糖、蔗糖、山梨糖醇、滑石、硬脂酸、硬脂酸镁、磷酸氢钙或树胶)和其它稀释剂(例如水)混合以形成固体组合物。然后将该固体组合物细分为含有有效量的本公开内容的化合物的单位剂型。可以将含有化合物或提取物的片剂或丸剂包衣或以其它方式复合以提供这样的剂型,其提供延长作用和/或潜在地增强吸收的优点。
[0100]
掺入了本公开内容的化合物或提取物用于口服或肠胃外施用的液体形式包括水溶液、适当调味的糖浆剂、水性或油混悬剂和含食用油的调味乳剂以及酏剂和类似媒介物。用于水性混悬剂的合适分散剂或悬浮剂包括合成的天然树胶,如黄蓍胶、阿拉伯胶、藻酸盐、葡聚糖、羧甲基纤维素钠、甲基纤维素、聚乙烯吡咯烷酮或明胶。用于口服施用的液体制剂可以呈例如溶液、糖浆剂或混悬剂的形式,或者它们可以作为干燥产物存在,用于在使用前用水或其它合适的媒介物重构。这种液体制剂可以通过常规手段用可接受的添加剂制备,所述添加剂如悬浮剂(例如,山梨醇糖浆、甲基纤维素或氢化食用脂肪);乳化剂(例如卵磷脂或阿拉伯胶);非水性媒介物(例如,杏仁油、油酯或乙醇);防腐剂(例如,对羟基苯甲酸甲酯或对羟基苯甲酸丙酯或山梨酸);以及人造或天然颜色和/或甜味剂。
[0101]
制备本公开内容的制剂或组合物的方法包括将本公开内容的化合物或提取物与载体和任选的一种或多种辅助和/或活性成分缔合的步骤。通常,制剂通过将本公开内容的化合物或提取物与液体载体或细分散的固体载体或两者均匀地且紧密地缔合,然后,如果需要,使产物成型来制备。因此,所公开的制剂可以由本文所述的化合物或提取物与合适的载体组合组成,或者基本上由其组成。
[0102]
当本公开内容的化合物或提取物作为药物、保健品或膳食补充剂施用至人和动物时,它们可以本身0.1至99%或作为含有例如(更优选地,10至30%)活性成分与可接受的载体组合的组合物施用。
[0103]
虽然预期单独的含酪胺的羟基肉桂酸酰胺可以用于本公开内容的消耗品中,但还预期两种或更多种化合物或提取物可以以任何相对量组合以产生含有所需比例的两种或更多种含酪胺的羟基肉桂酸酰胺的成分的定制组合,从而增强产物功效、改善感官特性或对产物的最终使用重要的一些其它质量测量。实施例1:用于生产含酪胺的羟基肉桂酸酰胺的重组酵母菌株
[0104]
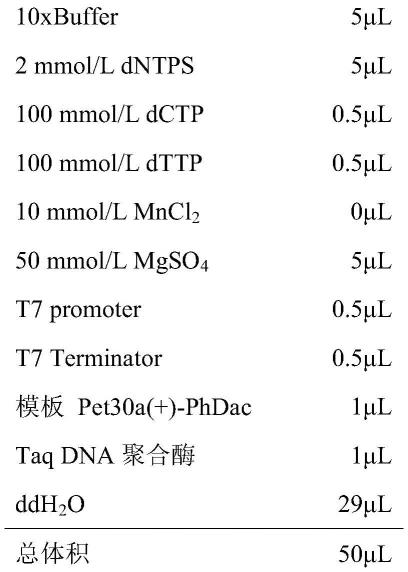
由于含酪胺的羟基肉桂酸酰胺不是内源性代谢物,因此有必要在酵母中重建合成生产途径。合成以所有苯丙素以及苯丙氨酸和/或酪氨酸开始,它们由细胞内源性产生。用于在本公开内容的重组酵母菌株中引入和过表达的基因列于表9中。表9
*基因包括启动子(“p”)序列、编码序列和终止子(“t”)序列。
[0105]
所用的酿酒酵母菌株是同基因单倍体。起始酵母菌株包含营养缺陷型(-ura3、-leu2、his3)标志物基因的敲除。在30℃下在ypd液体培养物(10g/l bacto-酵母提取物、20g/l bacto-蛋白胨和2%葡聚糖)中进行克隆的富集和繁殖。在不存在尿嘧啶或亮氨酸或组氨酸的情况下,在dropout琼脂平板(ynb csm)上选择重组体。尿嘧啶、组氨酸和亮氨酸生物合成途径中的基因缺陷导致营养缺陷型。对于同源重组,使用错配缺陷菌株。通过pcr合成和/或扩增开放阅读框。
[0106]
使用常规克隆和酵母转化方案,将构建体引入酵母中,并在含有葡萄糖作为唯一
碳源的培养基中使细胞生长。当需要另外的底物(例如,苯丙氨酸,酪氨酸或肉桂酸)时,在开始培养后24小时加入所述底物。然后通过高效液相色谱(hplc)分析上清液以鉴定适当的产物。
[0107]
在某些实施方案中,酵母细胞过量产生苯丙氨酸和酪氨酸中的一种或两种。在特定的实施方案中,苯丙氨酸和酪氨酸由重组宿主细胞以近似相等的速率产生。为了避免芳香醇的产生并将途径通量引导至芳香族氨基酸,将aro10(苯基丙酮酸脱羧酶)和pdc5(丙酮酸脱羧酶)的双敲除引入到菌株中。用于生产含酪胺的羟基肉桂酸酰胺的酵母菌株以及生长培养基补充剂提供在表10中。表10
[0108]
呈现出含酪胺的羟基肉桂酸酰胺高生产水平的菌株用于生产含有含酪胺的羟基肉桂酸酰胺的提取物和消耗品。生产菌株在生物反应器中生长足以产生含酪胺的羟基肉桂酸酰胺的时间。发酵完成后,通过离心或过滤从上清液中去除细胞团。然后通过用合适的溶剂,例如含水的醇或乙酸乙酯萃取,从上清液中回收含酪胺的羟基肉桂酸酰胺。然后可以通过溶剂分配和/或色谱法进一步纯化含酪胺的羟基肉桂酸酰胺,并通过改变溶剂,例如通过调节溶液温度和/或组成来结晶。也可以通过加入乙醇或其它合适的溶剂,例如乙酸乙酯,通过将溶剂直接加入到细胞培养物中,然后过滤或离心而直接从细胞团中回收含酪胺的羟基肉桂酸酰胺。从上清液中去除溶剂后,收集晶体(或其它脱溶剂形式,如油或沉淀)。然后通过例如溶剂分配和/或色谱法进一步纯化该物质,并通过改变溶剂的温度和/或组成来结晶,得到高纯度物质,然后回收、洗涤和干燥该物质以产生含酪胺的羟基肉桂酸酰胺的纯化(》90%)来源。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。