1.本发明属于生物敷料领域,具体涉及一种创面修复用弹性蛋白水凝胶材料及其制备方法。
背景技术:
2.每年各种意外事故造成大量皮肤全层缺损亟需进行创面修复的患者。目前,临床治疗创面缺损的方法主要有自体或异体皮肤移植。但自体移植供体有限且造成供区的损伤,异体移植容易带来免疫排斥及安全性的问题。近年来生物材料和再生医学的发展,为创面修复提供了新的希望。生物材料可用作创面敷料或真皮修复填充物,促进创面愈合。其中,水凝胶材料可吸收渗出液为伤口创造一个湿润的环境,并可在创面与外界间形成物理屏障隔绝细菌入侵,因此在创面修复中展现出巨大应用潜力。
3.弹性蛋白(elastin)是由细胞分泌的可溶性弹性蛋白原在体内酶的作用下交联而成的不溶于水的三维网络结构。弹性蛋白存在于皮肤、肺、血管等组织和器官中,起到维持组织和器官弹性的功能。弹性蛋白具有促进皮肤细胞迁移增殖及促血管化作用,因此弹性蛋白基生物材料是理想的创面修复材料。目前弹性蛋白基生物材料主要有两大类:第一类是从动物体内提取的天然弹性蛋白,产量大,成本较低,适合大规模生产应用,但其不溶于水,难以加工,一般将其水解成可溶性弹性蛋白后进行应用;第二类是通过基因工程方法让细菌合成出人弹性蛋白原或类弹性蛋白多肽,但该方法产量低,成本较高。因此,如果将水解后可溶性天然弹性蛋白进行改性,制备成可原位成型的水凝胶材料,那么将可以满足不同深度和形状的创面修复的需要,大大拓展其在创面修复的应用。
4.有文献报道了天然弹性蛋白改性后与聚乙二醇二丙烯酸酯及明胶复合制备水凝胶的研究(polymers,2020,12,670),其具体步骤是:(1)将可溶性弹性蛋白、明胶分别与环状的2-亚氨基硫烷盐酸盐(traut’s试剂)反应,在弹性蛋白、明胶上分别接枝上巯基,该反应需1小时左右,而且接枝上的巯基容易发生分子内交联,从而影响后面反应效率;(2)将接枝有巯基的弹性蛋白、接枝有巯基的明胶分别与聚乙二醇二丙烯酸酯(分子量:8kda;分子链两端各带有一个双键)反应过夜,分别得到弹性蛋白-聚乙二醇(带双键可进一步发生交联反应)水凝胶前驱体、明胶-聚乙二醇前驱体,前驱体中弹性蛋白或明胶重量比大概60%左右;(3)将明胶-聚乙二醇前驱体及弹性蛋白-聚乙二醇前驱体混合,在紫外光作用下进行交联制备弹性蛋白/明胶/聚乙二醇水凝胶。可见,该文献中制备的水凝胶的前期反应步骤多(两步),耗时长(第一步反应1小时,第二步反应需要过夜),且效率低(巯基容易发生分子内交联,影响后面接枝反应;且巯基可同时与聚乙二醇二丙烯酸酯两端的双键发生反应,造成接枝到弹性蛋白上的聚乙二醇二丙烯酸酯失去光交联能力);而且反应中所用的聚乙二醇二丙烯酸酯分子量大,导致终产物中蛋白含量只有60%左右,聚乙二醇含量高可能会削弱水凝胶的细胞粘附性;另外,该反应中接枝率只有60%左右(测量改性前后伯胺基含量变化)。
技术实现要素:
5.本发明的目的在于克服现有技术中存在的缺点,提供一种工艺简单、反应快速、接枝率高、弹性蛋白含量高的创面修复用弹性蛋白水凝胶材料及其制备方法。
6.本发明的目的通过下述技术方案实现:
7.一种创面修复用弹性蛋白水凝胶材料的制备方法,包括下述步骤:
8.(1)将0.5~2质量份可溶性弹性蛋白溶解于100份去离子水或缓冲溶液中,配制成弹性蛋白水溶液;
9.(2)在所述弹性蛋白水溶液中,加入0.1~1质量份丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(ac-peg-nhs)或甲基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(meac-peg-nhs),常温充氮气避光条件下进行反应,得到改性弹性蛋白;
10.(3)将所述改性弹性蛋白在去离子水中透析,将透析后的改性弹性蛋白水溶液置于《-15℃环境中使其结冰,然后在冻干机中冻干,得到干态的改性弹性蛋白;
11.(4)将所述干态的改性弹性蛋白0.5~20质量份溶解于100份去离子水或磷酸盐生理(pbs)缓冲溶液中,加入光引发剂,然后在一定波长的光源下辐照,制备得到弹性蛋白水凝胶材料。
12.优选的,步骤(1)中,所述可溶性弹性蛋白来源于鱼类或哺乳类动物组织中的不溶性弹性蛋白的水解物。
13.优选的,步骤(1)中,所述缓冲溶液为0.01m的磷酸盐生理缓冲溶液或0.01~0.06m的nah2po4缓冲溶液;所述缓冲溶液的ph值为8.0~8.3。
14.优选的,步骤(2)中,ac-peg-nhs或meac-peg-nhs中peg的聚合度为4~20。
15.优选的,步骤(2)中,ac-peg-nhs或meac-peg-nhs与弹性蛋白水溶液的反应时间为0.5~3小时。
16.优选的,步骤(3)中,所述改性弹性蛋白的透析时间为24~48小时,透析袋的截留分子量为1~50kda。
17.优选的,步骤(4)中,磷酸盐生理缓冲溶液的浓度为0.01m,ph值为7.0-7.5。
18.优选的,步骤(4)中,辐照光的波长为365nm或405nm;当采用365nm紫外光辐照时,相应的光引发剂为紫外光引发剂,如2-羟基-4
’‑
(2-羟乙氧基)-2-甲基苯丙酮(irgacure 2959);采用405nm蓝光辐照时,相应的光引发剂为蓝光引发剂,如苯基-2,4,6-三甲基苯甲酰基次膦酸锂(lap)。加入的引发剂的终浓度为0.01%-0.5%。
19.优选的,步骤(4)中,光交联辐照时间为0.5~10分钟。
20.所述步骤(4)中,还可以加入带有光交联官能团的其它水溶性高分子0.1~10质量份,与所述干态的改性弹性蛋白0.5~10质量份一起溶解于100份去离子水或磷酸盐生理缓冲溶液中,再加入0.01~0.5份光引发剂,然后在一定波长的光源下辐照一定时间,形成弹性蛋白复合水凝胶材料。
21.所述带有光交联官能团的其它水溶性高分子包括但不限于下列高分子的原始或改性产物:蛋白类高分子(明胶,胶原,丝素蛋白,多肽,角蛋白),多糖类高分子(海藻酸,透明质酸,壳聚糖,结冷胶,卡拉胶),其它合成的水溶性高分子,或上述高分子的任意组合。
22.一种创面修复用弹性蛋白水凝胶材料,采用上述方法制备得到。
23.本发明的原理是:采用丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(ac-peg-nhs)或甲
基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(meac-peg-nhs),与弹性蛋白进行反应,将可以发生光交联反应的双键接枝到弹性蛋白上。本发明采用的ac-peg-nhs或meac-peg-nhs,在反应时,其羟基琥珀酰亚胺酯基团可以直接与弹性蛋白上的伯胺发生亲核反应,从而将双键接枝到弹性蛋白的伯胺基上。本发明制备的改性弹性蛋白上含有双键,可以在光催化剂及一定波长光源辐照下相互发生加成反应,形成三维交联高分子网络-水凝胶。
24.本发明与现有技术相比具有如下优点和效果:
25.(1)本发明中制备光交联弹性蛋白水凝胶前驱体即改性弹性蛋白的步骤只需一步,而现有技术的方法需要两步,可见本发明的方法更简单。
26.(2)本发明中弹性蛋白接枝双键的改性反应时间可以控制在0.5-3小时,而现有技术的弹性蛋白接枝双键的反应(与聚乙二醇二丙烯酸酯的反应)需要过夜,反应时间较长,可见本发明的方法制备效率高。
27.(3)本发明中弹性蛋白上伯胺基的接枝效率可达90%以上,而现有技术对弹性蛋白上伯胺基的接枝效率只有60%左右,可见本发明的方法改性接枝效率高。
28.(4)本发明用到的接枝物丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(ac-peg-nhs)或甲基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(meac-peg-nhs)中peg聚合度可控制在1-20,分子量可以控制在300-1300da;而现有技术接枝的聚乙二醇二丙烯酸酯分子量为8000;因此本发明的改性终产物的蛋白含量最高可达90%以上,而现有技术的改性终产物的蛋白含量最高为60%左右;由于聚乙二醇具有抗粘附性,本发明中蛋白含量的提高有助于提高本发明水凝胶的细胞粘附性。
29.(5)本发明中制备的弹性蛋白改性产物可以单独制备成光交联水凝胶,而现有技术只是制备出弹性蛋白/明胶/聚乙二醇的复合水凝胶,没有制备出单纯的改性弹性蛋白水凝胶;因此本发明的方法可以在制备弹性蛋白水凝胶上更有优势,也可以验证单纯弹性蛋白水凝胶在创面修复的效果。
附图说明
30.图1为ac-peg-nhs改性弹性蛋白的反应示意图。
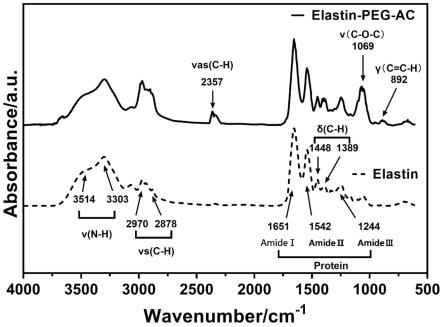
31.图2为实施例9中制备的未改性弹性蛋白(elastin)和改性弹性蛋白(elastin-peg-ac)的傅里叶转换红外光谱图(ftir)。
32.图3为实施例10中制备的弹性蛋白水凝胶外观图。
具体实施方式
33.为了便于理解本发明,下面将结合具体实施例对本发明进行详细说明。以下实施例将有助于本领域的技术人员进一步理解本发明,但是,不以任何形式限制本发明。应该指出的是,对本领域的技术人员来说,在不脱离本发明构思的前提下,本发明还可以做出若干变形和改进,这些都属于本发明的保护范围。
34.实施例1
35.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.05g可溶性弹性蛋白溶解于10ml ph 8.0的0.01m磷酸盐生理缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.01g甲基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚
合度为4),常温充氮气避光搅拌反应3小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。
36.实施例2
37.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.2g可溶性弹性蛋白溶解于10ml ph 8.0的0.01m磷酸盐生理缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.1g甲基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚合度为20),常温充氮气避光搅拌反应0.5小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。
38.实施例3
39.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.15g可溶性弹性蛋白溶解于10ml ph 8.3的0.01m磷酸盐生理缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.08g甲基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚合度为10),常温充氮气避光搅拌反应2小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。
40.实施例4
41.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.05g可溶性弹性蛋白溶解于10ml ph 8.0的0.01m的nah2po4缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.01g甲基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚合度为8),常温充氮气避光搅拌反应1小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。
42.实施例5
43.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.15g可溶性弹性蛋白溶解于10ml ph 8.3的0.01m的nah2po4缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.05g甲基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚合度为10),常温充氮气避光搅拌反应3小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。
44.实施例6
45.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.2g可溶性弹性蛋白溶解于10ml ph 8.3的0.06m的nah2po4缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.1g甲基丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚合度为4),常温充氮气避光搅拌反应0.5小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。
46.实施例7
47.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.08g可溶性弹性蛋白溶解于10ml ph 8.0的0.01m磷酸盐生理缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.02g丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚合度为4),常温充氮气避光搅拌反应3小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。ac-peg-nhs改性弹性蛋白的反应示意图如图1所示。
48.实施例8
49.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.15g可溶性弹性蛋白溶解于10ml ph 8.3的0.01m磷酸盐生理缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.1g丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚合度为20),常温充氮气避光搅拌反应0.5小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。
50.实施例9
51.本实施例提供一种可光交联的弹性蛋白的改性方法,按以下步骤制备:0.1g可溶性弹性蛋白溶解于10ml ph 8.3的0.06m的nah2po4缓冲液中配置成弹性蛋白水溶液。往上述弹性蛋白水溶液中加入0.04g丙烯酸酯-聚乙二醇-n-羟基琥珀酰亚胺(聚乙二醇聚合度为4),常温充氮气避光搅拌反应3小时。将反应物在截留分子量为3kda的透析袋中透析48小时,然后将纯化的蛋白溶液在冻干机中冻干,得到改性弹性蛋白。
52.对实施例1-9中任意实施例所制备的改性弹性蛋白,利用傅里叶转换红外光谱仪进行表征。均可发现改性后的弹性蛋白在892及1069波数处出现新的吸收峰,分别为丙烯酸上碳碳双键c-h的面外弯曲振动及聚乙二醇(peg)上c-o-c伸缩振动吸收峰,证明改性成功,如图2所示。
53.实施例10
54.本实施例提供一种可光交联的弹性蛋白水凝胶的制备方法:在实施例1-9中,取任意实施例制备的冻干的改性弹性蛋白200mg,溶解于2ml含蓝光引发剂苯基-2,4,6-三甲基苯甲酰基次膦酸锂(0.3mg/ml)的磷酸盐生理缓冲溶液中(ph7.4),配置成100mg/ml的弹性蛋白水凝胶前驱体溶液。用移液枪滴加100ul溶液至固定模具中,用蓝光仪(波长405nm)辐照3分钟后原位形成水凝胶。图3为制备的弹性蛋白水凝胶的外观图,水凝胶直径为5mm。
55.实施例11
56.本实施例提供一种可光交联的弹性蛋白水凝胶的制备方法:在实施例1-9中,取任意实施例制备的冻干的改性弹性蛋白200mg,溶解于2ml含蓝光引发剂苯基-2,4,6-三甲基苯甲酰基次膦酸锂(0.5mg/ml)的去离子水中,配置成100mg/ml的弹性蛋白水凝胶前驱体溶液。用移液枪滴加100ul溶液至固定模具中,用蓝光仪(波长405nm)辐照3分钟后原位形成水凝胶。
57.实施例12
58.本实施例提供一种可光交联的弹性蛋白水凝胶的制备方法:在实施例1-9中,取任意实施例制备的冻干的改性弹性蛋白200mg,溶解于2ml含紫外光引发剂2-羟基-4
’‑
(2-羟乙氧基)-2-甲基苯丙酮(0.5mg/ml)的磷酸盐生理缓冲溶液中(ph 7.4),配置成100mg/ml的弹性蛋白水凝胶前驱体溶液。用移液枪滴加100ul溶液至固定模具中,用紫外仪(波长365nm)辐照4分钟后原位形成水凝胶。
59.实施例13
60.本实施例提供一种可光交联的弹性蛋白/明胶复合水凝胶的制备方法:在实施例1-9中,取任意实施例制备的冻干的改性弹性蛋白100mg,溶解于2ml含紫外光引发剂2-羟基-4
’‑
(2-羟乙氧基)-2-甲基苯丙酮(0.5mg/ml)的磷酸盐生理缓冲溶液中(ph 7.4),配置成100mg/ml的弹性蛋白水凝胶前驱体溶液。往该前驱体溶液中加入100mg甲基丙烯酸酯化
明胶并溶解,制备200mg/ml复合水凝胶前驱体溶液。用移液枪滴加100ul溶液至固定模具中,用紫外仪(波长365nm)辐照4分钟后原位形成水凝胶。
61.实施例14
62.本实施例提供一种可光交联的弹性蛋白/透明质酸复合水凝胶的制备方法:在实施例1-9中,取任意实施例制备的冻干的改性弹性蛋白150mg,溶解于2ml含蓝光引发剂苯基-2,4,6-三甲基苯甲酰基次膦酸锂(0.5mg/ml)的去离子水中,配置成150mg/ml的弹性蛋白水凝胶前驱体溶液。往该前驱体溶液中加入50mg甲基丙烯酸酯化透明质酸并溶解,制备200mg/ml复合水凝胶前驱体溶液。用移液枪滴加100ul溶液至固定模具中,用蓝光仪(波长405nm)辐照3分钟后原位形成水凝胶。
63.测试例1
64.以c57bl/6小鼠背部全层皮肤缺损创面为模型,制备直径为10mm的创面,所有小鼠均在创面周围垫一层硅胶圈防止皮肤收缩。采用异体对照,样本量为3。实验分组:本发明制备的弹性蛋白水凝胶组,商品化丙烯酸改性明胶组,空白对照组。实验组处理方式:在实施例1-9中,取任意实施例制备的冻干的改性弹性蛋白200mg,溶解于2ml含蓝光引发剂苯基-2,4,6-三甲基苯甲酰基次膦酸锂(0.3mg/ml)的磷酸盐生理缓冲溶液中(ph 7.4),配置成100mg/ml的弹性蛋白水凝胶前驱体溶液,在0.22μm无菌过滤器中过滤灭菌。用移液枪滴加100ul灭菌弹性蛋白水凝胶前驱体溶液至创面,用蓝光仪辐照3分钟后原位成胶。商品化丙烯酸改性明胶组,蛋白浓度及交联的实验流程与弹性蛋白组一样。对照组不做任何处理。然后使用3m可透气医用胶布包扎创面,再用弹性绷带固定以防止胶布脱落。分别在术后3,7,14天对创面进行拍照观察伤口愈合情况。在每个时间点取创面组织样本进行he染色,马松染色。创面图片显示弹性蛋白水凝胶组愈合速度明显快于空白对照组,与商品化丙烯酸改性明胶组没有明显差异。he染色结果提示弹性蛋白水凝胶组与另外两组相比,有较多血管生成,说明本发明的弹性蛋白水凝胶更有利于真皮层再生。马松染色结果显示含弹性蛋白组与另外两组相比,生成更多、更致密、更粗壮的胶原纤维。因此,本发明中制备的弹性蛋白水凝胶是一种理想的创面修复材料。
65.以上所述仅为本发明的实施例,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均为等效的置换方式,都包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。