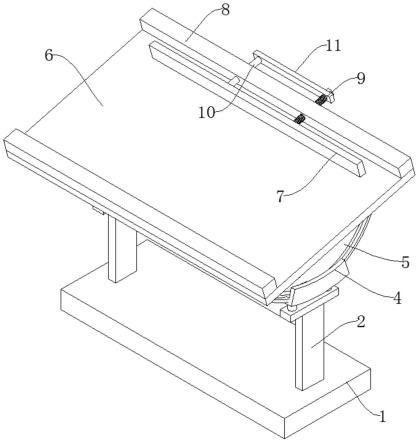
1.本发明涉及一种治疗婴幼儿湿疹的中药制剂,具体涉及一种抗敏消炎治疗婴幼儿湿疹的中药制剂及制备方法(简称“白菊湿疹膏”),属于外用型中药抗湿疹制剂技术领域。
背景技术:
2.婴幼儿湿疹是一种常发于婴幼儿期,具有明显湿疹损害特点的过敏性皮肤病。主要由免疫球蛋白e(ige)介导的变态(过敏)反应所引起。急性湿疹常发于3-6个月婴儿,慢性湿疹常发于1-12岁的幼儿。临床症状与体征主要表现为头、面部和股沟处流脓成片,瘙痒不绝,寝食难安,多用热水和肥皂洗涤而加重。
3.国内外治疗婴幼儿湿疹的传统疗法以内服和外用抗组胺药物为主,但此疗法起效慢,湿疹消退缓慢(二周左右),经常因迁延性而转为慢性湿疹。长期使用抗组胺药治疗湿疹会对婴幼儿肝、肾功能造成明显的损伤,且给父母哺育带来诸多不便。
4.目前,市场上也存在一些治疗湿疹的外用中药制剂,然而,这些中药制剂具有“起效慢、疗程长、治愈率低(低于白菊湿疹膏)、有一定的毒副作用和广谱性差等”缺陷和缺点。
技术实现要素:
5.本发明所要解决的技术问题是针对现有技术中存在的不足,而提供一种抗敏消炎治疗婴幼儿湿疹的中药制剂及制备方法,本发明的中药制剂具有清热、燥、湿,祛风止痒的功效,对各种热邪、湿邪和风邪所致的婴儿湿疹(急性、亚急性和慢性)和瘙痒等症疗效显著,且具有起效快(12小时)、疗程短(2-3天)、治愈率高(100%)、安全性强(100%),以及针对急性、亚急性和慢性婴幼儿湿疹均有同等疗效的优点。
6.为了实现上述目的,本发明采用如下技术方案:
7.本发明首先提供一种抗敏消炎治疗婴幼儿湿疹的中药制剂,包括以下重量百分比的组分:6.5%的内容药物组合物、13.5%的基质和80%的蒸馏水;所述的内容药物组合物包括以下重量百分比的原料药:苦参20-31%;白菊花23-35%;地肤子23-30%;薄荷10-15%;甘草4-8%。
8.上述技术方案中,所述的内容药物组合物优选包括以下重量百分比的原料药:苦参28%;白菊花33%;地肤子25%;薄荷10%;甘草4%。
9.上述技术方案中,所述的内容药物组合物优选包括以下重量百分比的原料药:苦参20%;白菊花35%;地肤子30%;薄荷10%;甘草5%。
10.上述技术方案中,所述的内容药物组合物优选包括以下重量百分比的原料药:苦参28%;白菊花23%;地肤子25%;薄荷16%;甘草8%。
11.上述技术方案中,所述的内容药物组合物优选包括以下重量百分比的原料药:苦参30%;白菊花25%;地肤子25%;薄荷15%;甘草5%。
12.上述技术方案中,所述的内容药物组合物优选包括以下重量百分比的原料药:苦参25%;白菊花30%;地肤子25%;薄荷15%;甘草5%。
13.上述技术方案中,所述的内容药物组合物优选包括以下重量百分比的原料药:苦参31%;白菊花23%;地肤子23%;薄荷15%;甘草8%。
14.上述技术方案中,所述的基质包括以下重量百分比的组分:十八醇13-16%;异十六烷28-32%;单甘脂7-10%;尼泊金丙酯4-7%;尼泊金甲酯4-7%;甘油35-37%。
15.上述技术方案中,所述的基质优选包括以下重量百分比的组分:十八醇15%;异十六烷30%;单甘脂10%;尼泊金丙酯4%;尼泊金甲酯4%;甘油37%。
16.上述技术方案中,所述的基质优选包括以下重量百分比的组分:十八醇13%;异十六烷32%;单甘脂8%;尼泊金丙酯5%;尼泊金甲酯5%;甘油37%。
17.上述技术方案中,所述的基质优选包括以下重量百分比的组分:十八醇16%;异十六烷30%;单甘脂7%;尼泊金丙酯6%;尼泊金甲酯6%;甘油35%。
18.上述技术方案中,所述的基质优选包括以下重量百分比的组分:十八醇13%;异十六烷28%;单甘脂9%;尼泊金丙酯7%;尼泊金甲酯7%;甘油36%。
19.上述技术方案中,所述的抗敏消炎治疗婴幼儿湿疹的中药制剂的剂型为外用膏剂,简称“白菊湿疹膏”,使用时直接涂抹在患处,每次涂抹5至8g(视湿疹面积而定),每天涂抹3次(早、中、晚),一般起效时间在12小时内,2-3天治愈。
20.本发明还提供上述的抗敏消炎治疗婴幼儿湿疹的中药制剂的制备方法,包括以下步骤:
21.(1)将苦参制备成苦参精提粉:
22.苦参原料药依次经干燥、粉碎、过50目筛后加入10倍量质量浓度为60%的乙醇,在70℃水浴条件下加热回流进行提取,提取1小时后过滤,残渣重复提取1次,合并提取液,提取液依次经浓缩干燥、粉碎、过100目筛后得到苦参精提粉,待用;
23.(2)将野白菊制备成白菊精提粉:
24.野白菊原料药依次经干燥、粉碎、过50目筛后加入10倍量质量浓度为60%的乙醇,在70℃水浴条件下加热回流进行提取,提取1小时后过滤,残渣重复提取1次,合并提取液,提取液依次经浓缩干燥、粉碎、过100目筛后得到野白菊精提粉,待用;
25.(3)将地肤子制备成地肤子精提粉:
26.地肤子原料药依次经干燥、粉碎、过50目筛后加入10倍量质量浓度为60%的乙醇,在70℃水浴条件下加热回流进行提取,提取1小时后过滤,残渣重复提取1次,合并提取液,提取液依次经浓缩干燥、粉碎、过100目筛后得到地肤子精提粉,待用;
27.(4)将薄荷和甘草分别用1000目超微粉碎机粉成目数为100目的薄荷超微粉和甘草超微粉,待用;
28.(5)将20-31%苦参精提粉、23-35%白菊花精提粉、23-30%地肤子精提粉、10-15%薄荷超微粉和4-8%甘草超微粉混合均匀,得到内容药物组合物;
29.(6)将13-16%十八醇、28-32%异十六烷、7-10%单甘脂、4-7%尼泊金丙酯、4-7%尼泊金甲酯、35-37%甘油混合均匀得到基质;
30.(7)将6.5%的内容药物组合物、13.5%的基质和80%的蒸馏水混合均匀后混配成膏剂内容物后依次经过装管(牙膏型软管)、包装、钴60消毒、入库后得到所述的中药制剂。
31.上述技术方案中,所述的十八醇、异十六烷、单甘脂、尼泊金丙酯、尼泊金甲酯、甘油按照《中华人民共和国药典》2020年版一部所定标准采购;所述的内容药物组合物、基质
和蒸馏水按《中华人民共和国药典》膏剂的制剂标准与制备要求配混成膏剂内容物。
32.本发明中药制剂的功效:清热、燥、湿,祛风止痒。
33.本发明中药制剂的主治:婴幼儿湿疹症(急性、亚急性和慢性湿疹)。
34.本发明中药制剂的方解:中医理论认为,热邪、湿邪和风邪是婴幼儿湿疹主要致病的病因和病机。治疗当以清热、燥、湿,祛风止痒为主。方中苦参清热、燥、湿,为君药;白(野)菊花和地肤子清热解毒,与苦参配伍能增强清热作用,列为臣药;薄荷辛凉解表能善除风热,兼具止痒功效,列为佐药;甘草调和诸药,列为使药。诸药合用,可共凑清热、燥、湿和祛风止痒之功效。对各种热邪、湿邪和风邪所致的婴儿湿疹和瘙痒等症疗效显著。
35.与现有技术相比,具有以下特点:
36.(1)本发明中药制剂具有清热、燥、湿和祛风止痒之功效,对各种热邪、湿邪和风邪所致的婴儿湿疹(急性、亚急性和慢性)和瘙痒均能迅速有效地达到治愈目的。
37.(2)本发明中药制剂,具有起效快(12小时)、疗程短(2-3天)、治愈率高(100%)、安全性强(100%),以及针对急性、亚急性和慢性婴幼儿湿疹均有同等疗效的优点。
具体实施方式
38.以下对本发明技术方案的具体实施方式详细描述,但本发明并不限于以下描述内容:
39.本发明的以下实施例中,抗敏消炎治疗婴幼儿湿疹的中药制剂的制备方法如下所示:
40.(1)将苦参制备成苦参精提粉:
41.苦参原料药依次经干燥、粉碎、过50目筛后加入10倍量质量浓度为60%的乙醇,在70℃水浴条件下加热回流进行提取,提取1小时后过滤,残渣重复提取1次,合并提取液,提取液依次经浓缩干燥、粉碎、过100目筛后得到苦参精提粉,待用;
42.(2)将野白菊制备成白菊精提粉:
43.野白菊原料药依次经干燥、粉碎、过50目筛后加入10倍量质量浓度为60%的乙醇,在70℃水浴条件下加热回流进行提取,提取1小时后过滤,残渣重复提取1次,合并提取液,提取液依次经浓缩干燥、粉碎、过100目筛后得到野白菊精提粉,待用;
44.(3)将地肤子制备成地肤子精提粉:
45.地肤子原料药依次经干燥、粉碎、过50目筛后加入10倍量质量浓度为60%的乙醇,在70℃水浴条件下加热回流进行提取,提取1小时后过滤,残渣重复提取1次,合并提取液,提取液依次经浓缩干燥、粉碎、过100目筛后得到地肤子精提粉,待用;
46.(4)将薄荷和甘草分别用1000目超微粉碎机粉成目数为100目的薄荷超微粉和甘草超微粉,待用;
47.(5)将20-31%苦参精提粉、23-35%白菊花精提粉、23-30%地肤子精提粉、10-15%薄荷超微粉和4-8%甘草超微粉混合均匀,得到内容药物组合物;
48.(6)将13-16%十八醇、28-32%异十六烷、7-10%单甘脂、4-7%尼泊金丙酯、4-7%尼泊金甲酯、35-37%甘油混合均匀得到基质;所述的十八醇、异十六烷、单甘脂、尼泊金丙酯、尼泊金甲酯、甘油按照《中华人民共和国药典》2020年版一部所定标准采购;
49.(7)将6.5%的内容药物组合物、13.5%的基质和80%的蒸馏水混合均匀后混配成
膏剂内容物,按《中华人民共和国药典》膏剂的制剂标准与制备要求配混成膏剂内容物;然后依次经过装管(牙膏型软管)、包装、钴60消毒、入库后得到所述的中药制剂。
50.下面结合具体的实施例对本发明进行阐述:
51.实施例1:
52.一种抗敏消炎治疗婴幼儿湿疹的中药制剂,包括以下重量百分比的组分:6.5%的内容药物组合物、13.5%的基质和80%的蒸馏水(中药制剂100g,包括6.5g的内容药物组合物、13.5g的基质和80g的蒸馏水);产品简称“白菊湿疹膏”;
53.其中:所述的内容药物组合物包括以下重量百分比的原料药:苦参31%;白菊花23%;地肤子23%;薄荷15%;甘草8%(苦参2g;白菊花1.5g;地肤子1.5g;薄荷1g;甘草0.5g);
54.所述的基质包括以下重量百分比的组分:十八醇14.82%;异十六烷29.63%;单甘脂11.11%;尼泊金丙酯3.7%;尼泊金甲酯3.7%;甘油37%(十八醇2g;异十六烷4g;单甘脂1.5g;尼泊金丙酯0.5g;尼泊金甲酯0.5g;甘油5g)。
55.实施例2:
56.一种抗敏消炎治疗婴幼儿湿疹的中药制剂,包括以下重量百分比的组分:6.5%的内容药物组合物、13.5%的基质和80%的蒸馏水;其中:所述的内容药物组合物包括以下重量百分比的原料药:苦参28%;白菊花33%;地肤子25%;薄荷10%;甘草4%;所述的基质包括以下重量百分比的组分:十八醇13%;异十六烷28%;单甘脂9%;尼泊金丙酯7%;尼泊金甲酯7%;甘油36%。
57.实施例3:
58.一种抗敏消炎治疗婴幼儿湿疹的中药制剂,包括以下重量百分比的组分:6.5%的内容药物组合物、13.5%的基质和80%的蒸馏水;其中:所述的内容药物组合物包括以下重量百分比的原料药:苦参20%;白菊花35%;地肤子30%;薄荷10%;甘草5%;所述的基质包括以下重量百分比的组分:十八醇16%;异十六烷30%;单甘脂7%;尼泊金丙酯6%;尼泊金甲酯6%;甘油35%。
59.实施例4:
60.一种抗敏消炎治疗婴幼儿湿疹的中药制剂,包括以下重量百分比的组分:6.5%的内容药物组合物、13.5%的基质和80%的蒸馏水;其中:所述的内容药物组合物包括以下重量百分比的原料药:苦参28%;白菊花23%;地肤子25%;薄荷16%;甘草8%;所述的基质包括以下重量百分比的组分:十八醇13%;异十六烷32%;单甘脂8%;尼泊金丙酯5%;尼泊金甲酯5%;甘油37%。
61.实施例5:
62.一种抗敏消炎治疗婴幼儿湿疹的中药制剂,包括以下重量百分比的组分:6.5%的内容药物组合物、13.5%的基质和80%的蒸馏水;其中:所述的内容药物组合物包括以下重量百分比的原料药:苦参30%;白菊花25%;地肤子25%;薄荷15%;甘草5%;所述的基质包括以下重量百分比的组分:十八醇15%;异十六烷30%;单甘脂10%;尼泊金丙酯4%;尼泊金甲酯4%;甘油37%。
63.实施例6:
64.一种抗敏消炎治疗婴幼儿湿疹的中药制剂,包括以下重量百分比的组分:6.5%的
内容药物组合物、13.5%的基质和80%的蒸馏水;其中:所述的内容药物组合物包括以下重量百分比的原料药:苦参25%;白菊花30%;地肤子25%;薄荷15%;甘草5%;所述的基质包括以下重量百分比的组分:十八醇13-16%;异十六烷28-32%;单甘脂7-10%;尼泊金丙酯4-7%;尼泊金甲酯4-7%;甘油35-37%。
65.以本发明实施例1得到的中药制剂(简称白菊湿疹膏)作为治疗药物进行以下动物实验,各项动物实验中,白菊湿疹膏设置低、中和高3个计量组,另设正常对照组(或基质对照组)和阳性药对照组。各组给药剂量、药物浓度及动物数量见表1:
66.表1:白菊湿疹膏研究剂量设计
67.组别剂量(mg
·
kg-1
)药物浓度(mg
·
ml-1
)正常对照组00阳性药组1.00低剂量组0.50.1中剂量组1.00.2高剂量组2.00.4
68.一、急性毒性实验:
69.1、实验材料
70.1.1、实验动物:km小鼠100只,18-22g,雌雄各50只,由军事医学科学院实验动物中心提供。小鼠每笼饲养5只,自由饮水,温度为(22
±
2)℃,相对湿度40%-70%。常规饲养管理,自由饮水。
71.1.2、试剂及药品:
72.硫化钠:天津市申泰化学试剂有限公司,批号:121027,ar级。
73.2、实验方法
74.2.1预试验:
75.按照“国家食品药品监督管理局[化学药物刺激性、过敏性和溶血性研究技术指导原则]课题研究组,化学药物刺激性、过敏性和溶血性研究技术知道原则[s]:2005-03”进行,找出引起小鼠100%和0死亡的剂量。取12只小鼠,随机分成3组,每组4只,雌雄各2只,按0.04ml
·
g-1
、0.02ml
·
g-1
、0.01ml
·
g-1
的剂量,灌胃给药。灌胃前12h禁食、不禁水,灌胃后常规饲养,并观察小鼠3d内死亡情况。结果3组小鼠均无死亡,无法测出其半数致死量(ld50),因此采用测定小鼠最大给药量来测定受试药物对小鼠的急性毒性作用。
[0076]
2.2最大给药量试验:
[0077]
按照“徐淑云等,药理实验方法学[m],第3版,北京:人民卫生出版社,2003:152-154”进行,取60只小鼠,随机分成3组:对照组、空白基质组按0.04ml
·
g-1和白菊湿疹膏组按0.04ml
·
g-1
,每组20只,雌雄各10只。按上述剂量一次灌胃给药,对照组按按0.04ml
·
g-1
灌蒸馏水,灌胃前12h禁食、不禁水,灌胃后常规饲养,连续观察7d内动物的中毒反应及有无死亡,以死亡为主要指标,如无死亡,则以此用药量作为小鼠的最大给药量。试验结束时称小鼠的体质量,并参照文献“刘邦国等,纳米银乳膏的过敏及刺激性实验研究[j],实用医药杂志,2012,29(4):343-344”计算灌胃给药组小鼠的最大给药量为拟临床用药剂量的倍数。
[0078]
2.3皮肤给药对小鼠的急性毒性试验
[0079]
取km小鼠40只,体质量18-22g,随机分为两组,即基质对照组和白菊湿疹膏组,每
组20只;实验前小鼠背部郑重剪毛后,以8%的硫化钠溶液脱毛,面积约:2.5cm
×
4cm,24h后用于实验。实验档期,在小鼠背部脱毛区分别涂抹基质和白菊湿疹膏,给药量为0.25g/只,体积10ml
·
kg-1
,给药后连续观察7d,记录死亡数及毒性反应,计算最大给药量。
[0080]
3、实验结果
[0081]
3.1预试验:经预实验测定,结果显示3组小鼠均无死亡,无法测出其半数致死量(ld50),采用测定小鼠最大给药量来测定受试药物对小鼠的急性毒性作用。
[0082]
3.2最大给药量试验:
[0083]
结果显示:空白基质组、白菊湿疹膏组和对照组,按上述剂量一次灌胃给药后常规饲养。连续观察14d内动物均无中毒反应及死亡。观察可见,灌胃白菊湿疹膏后30min内,部分小鼠活动偶有减少,至1h后完全恢复,试验期间给药动物无1只死亡,试验观察期间,小鼠整体体重平稳增长,饮食、皮肤与毛发、行为、活动、分泌物(口、鼻、耳、眼)、排泄物(大小便)等均未见明显异常。试验结束后,处死全部动物,大体解剖、尸检,肉眼观察,各鼠心、肝、脾、肺、肾、脑、胃、肠等主要脏器未见出血、充血、水肿、渗出、溃疡、穿孔,胸腔、腹腔、心包腔无积液。表明白菊湿疹膏灌胃给药小鼠无明显急性毒性,其对小鼠灌胃的最大给药量为40ml
·
kg-1
或40.0g
·
kg-1
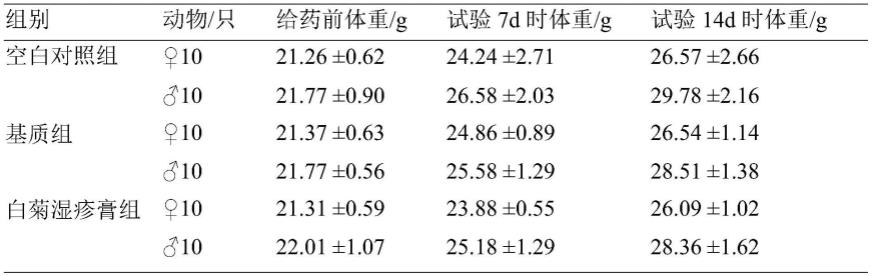
。参照文献“中华人民共和国卫生部药政管理局.中药新药研究指南(药学药理学毒理学)[m],北京:中华人民共和国卫生部药政管理局,1993:209-212”计算灌胃给药组小鼠的最大给药量为拟临床用药剂量的1600倍。试验7d、14d(实验结束时)称小鼠的体重结果见表2。
[0084]
表2 口服给药急性毒性实验对小鼠体重的影响
[0085][0086]
注:各组数据比较差异均不显著(p》0.05)
[0087]
3.3皮肤给药的急性毒性试验:
[0088]
结果显示,白菊湿疹膏后皮肤给药60min内,部分小鼠活动偶有减少,出现感觉不适症状(舔、用后肢挠痒背部涂药处)至2h后完全恢复,试验期间给药动物死亡,试验观察期间,小鼠饮食、行为、活动等均未见明显异常;口、鼻、耳、眼无异常分泌物,排泄物(大小便)等均正常。用药处皮肤未见有红肿、渗岀及溃烂等异常改变。实验7d时,脱毛出皮肤毛发已经全部长出,皮肤光滑平整,用药组同基质组比较未见明显差异。试验结束后,处死全部动物,大体解剖、尸检,肉眼观察,各鼠心、肝、脾、肺、肾、脑、胃、肠等主要脏器未见异常,胸腔、腹腔、心包腔无积液,体重增长结果见表3。
[0089]
表3 皮肤给药的急性毒性试验小鼠体重的变化
[0090][0091]
注:*与对照组比p《0.05,**与对照组比p《0.01
[0092]
4、小结
[0093]
在本实验条件下,km小鼠口服给药白菊湿疹膏组不能求得ld50,其最大给药量为:40g/kg,此剂量约为人(儿童按20kg体重计算)临床拟用剂量(0.025g/kg)的1600倍。皮肤给药白菊湿疹膏组不能求得ld50,其最大给药量为:25g/kg,此剂量约为人(儿童按20kg体重计算)临床拟用剂量(0.025g/kg)的1000倍。
[0094]
二、对家兔皮肤刺激性试验:
[0095]
1、实验材料
[0096]
1.1、实验动物:实验动物为健康成年新西兰白兔16只,体质量2-2.5kg,雌雄各半;北京科宇动物养殖中心提供,合格证号scxk(京)2007-0003。动物实验前适应性饲养1周,自由觅食和饮水,在室温(20
±
2)℃
°
,湿度40%-70%,自然光照条件下饲养。
[0097]
1.2、药物及试剂
[0098]
白菊湿疹膏;医用脱脂纱布.;医用胶带;硫化钠:天津市申泰化学试剂有限公司,批号:121027,ar级。
[0099]
2实验方法
[0100]
新西兰兔16只(雌雄各半),随机分为4组,每组4只,采用自身对照,分别进行单次给药皮肤刺激性实验和多次给药皮肤刺激性实验。于实验前24h,将每只家兔背部脊柱两侧用剪刀去毛但不损伤皮肤,再用8%硫化钠水溶液脱毛,将全部受试家兔背部脊柱两侧去毛(每侧约2.5cmx2.5cm,无红斑、水肿及破损),每只家兔单笼饲养,每组雌雄各2只,设单次涂抹完整皮肤组、单次涂抹破损皮肤组、多次涂抹完整皮肤组、多次涂抹破损皮肤组,均涂抹给药。破损皮肤组,每只家兔背部两侧去毛区在敷药前用针头经乙醇消毒后在敷药部位皮肤划“#”字以渗血为度,左侧为受试区(白菊湿疹膏0.2g/3
×
3cm组和白菊湿疹膏0.4g/3
×
3cm组),右侧为对照区(空白对照组、基质组均匀涂以基质0.4g/3
×
3cm),涂抹后,用一层4cm
×
4cm保鲜膜覆盖保湿,再加纱布覆盖保护,最后用无刺激性胶布和绷带适当固定。单次涂抹组:涂抹后6h,用温水洗去残留的受试药、基质剂及对照药;多次涂抹组:1次/d,连续7d。每次涂抹后6h,用温水洗去残留涂抹物。单次涂抹组去除涂抹物后1,24,48,72h观察涂抹部位有无红斑和水肿等情况。以及上述变化的恢复情况和时间,多次涂抹组在每次去除涂抹物后1h及再次涂抹前观察并记录涂抹部位红斑水肿及是否有色素沉着、出血点、皮肤粗糙或皮肤菲薄等情况发生及其消退时间,并对红斑水肿进行评分,末次给药后去除受试物后1,24,48,72h观察涂抹部位有无红斑和水肿等情况,以及上述变化的恢复情况和时间,多次皮肤刺激实验中每天每只动物平均积分=(红斑形成总分 水肿形成总分)/(合计动物数
×
7)。评分标准见表4和表5。
[0101]
所有动物均用数码相机拍照,根据下列公式计算平均积分值,并进行刺激强度评
价。公式:每组动物平均积分=∑红斑和水肿积分/受试动物
[0102]
记录皮肤刺激性后,在涂药部位切下1.5cm
×
1.5cm全层皮肤组织,浸泡于10%的甲醛溶液中固定,石蜡包埋,he染色,显微镜下观察涂药后皮肤病理变化。
[0103]
表4 皮肤刺激反应评分标准
[0104][0105]
表5 皮肤刺激强度评价标准
[0106][0107]
3.实验结果
[0108]
3.1刺激反应评分
[0109]
对家兔破损皮肤和完整皮肤单次或多次涂抹白菊湿疹膏或基质,刺激反应评分均为0分。结果见表6和表7:
[0110]
表6 单次用药对家兔皮肤刺激实验的影响
[0111][0112]
表7 多次用药对家兔皮肤刺激实验的影响
[0113][0114]
3.2病理组织学检查结果
[0115]
经病理组织学检查,各组皮肤结构正常,层次清晰,皮肤表皮、真皮、皮下及毛囊等各附属器腺均未见异常。
[0116]
4.结论
[0117]
白菊湿疹膏在本实验条件下,对家兔破损皮肤和完整皮肤、单次或多次涂抹白菊湿疹膏或基质,刺激反应评分均为0分。组织切片检查各组之间均未见有明显差异。表示白菊湿疹膏,对家兔破损皮肤和完整皮肤、单次或多次涂抹均无刺激性。
[0118]
三、皮肤过敏试验:
[0119]
1.实验材料
[0120]
1.1实验动物:实验动物为健康豚鼠24只,体质量300-350g,雌雄各半;hartley品
系,普通级,北京市昌杨西山动物养殖中心提供,合格证号scxk(京)2011—0010。
[0121]
1.2实验药品
[0122]
2,4-二硝基氯苯(dinitrochlorobenzene,dncb):山东xiya试剂研究中心,批号:w5656,纯度99%,ar级。使用时配制成1%致敏浓度,0.1%激发浓度。
[0123]
丙酮:天津市耀华化学试剂有限责任公司,批号:20121009,ar级。
[0124]
硫化钠:天津市申泰化学试剂有限公司,批号:121027,ar级。
[0125]
2.方法
[0126]
于实验前24h,采用8%硫化钠水溶液脱毛,将全部受试豚鼠背部脊柱两侧去毛(每侧约2.5cm
×
2.5cm,无红斑、水肿及破损)。24只豚鼠按体质量、性别随机分成4组,每组6只,设白菊湿疹膏给药组、基质组、空白对照组及阳性对照组。将白菊湿疹膏给药组0.2g涂以于左侧脱毛区,同上述方法固定,6h后用温水擦去残留受试药,第7天和14天以同样方法重复,此为致敏接触。空白对照组涂以基质0.2g,阳性对照组涂以1%的2,4-二硝基氯代苯(临用时用丙酮配制,致敏浓度)0.2ml。
[0127]
于未次涂药后14d时进行激发接触,在相应的动物组别右侧脱毛区分别涂白菊湿疹膏0.2g,基质0.2g,阳性对照组涂以0.1%的2,4-二硝基氯代苯(临用时用丙酮配制,激发浓度)0.2ml。6h后去除涂抹物,立即观察,并于24,48,72h重复观察涂抹部位有无红斑和水肿等过敏反应情况。过敏反应平均积分=(红斑形成总分 水肿形成总分)/合计动物数;致敏率(%)=出现皮肤红斑和水肿的动物数/受试动物总数
×
100%。皮肤过敏性反应标准如表8所示:
[0128]
表8皮肤过敏性反应评分标准
[0129][0130]
表8 皮肤敏性反应评价标准
[0131][0132]
3.实验结果
[0133]
实验结果如表9所示:
[0134]
表9 对豚鼠皮肤过敏实验的影响
[0135][0136]
从表9结果可见,白菊湿疹膏膏组和基质对照组在整个观察过程中,未见受试区出现红斑及水肿,阳性对照组自激发给药6h后,受试区有明显轻度红斑出现,无水肿,致敏率100%。
[0137]
4结论
[0138]
白菊湿疹膏膏对豚鼠致敏率为0.反应平均值均为0。表示无致敏性。而2.4-二硝基氯化苯致敏率为100%,为极度致敏性。
[0139]
四、药效学试验—对二甲苯致小鼠肿胀的影响:
[0140]
1.试验材料
[0141]
1.1实验动物
[0142]
清洁级昆明种(km)小鼠,20-25g,雄性,由山西医科大学动物实验中心提供。合格证号:syxk(晋)2017-0001(原scxk(晋)2010-0005)。
[0143]
1.2实验药品与试剂
[0144]
白菊湿疹膏,本发明实施例产品。
[0145]
复方醋酸地塞米松乳膏(皮炎平)20克:15mg。广州白云山制药有限公司白云山何济公制药厂生产,批号:v1037。
[0146]
二甲苯:衡阳有机试剂厂生产,批号:20100327。
[0147]
2,4-二硝基氯苯(dncb):中国医药公司北京分公司,批号:20101026。
[0148]
磷酸组胺:上海耕奔生物技术有限公司,批号:20091130。
[0149]
2实验方法
[0150]
按照文献“王国江,顾军.小鼠背部变应性接触性皮炎模型的建立[j].中国职业医学,2004,31(1):17-19”记载的方法进行:取雄性小鼠50只,随机分为5组,每组10只,分别为低、中、高剂量药物组,阳性对照组及空白对照组。低、中、”高剂量药物组分别在小鼠右耳耳
廓均匀涂抹白菊湿疹乳膏0.5,1.0,2.0g.kg-1
,阳性对照组在小鼠右耳耳廓均匀涂抹皮炎平乳膏1.0g.kg-1
,空白对照组在小鼠右耳耳廓均匀涂抹空白基质1.0g.kg-1
,2次/d,连续3d,第4d涂药1h后,对各组小鼠右耳涂予二甲苯致炎,每只0.05ml,4h后,各组以纯化水洗去小鼠右耳耳廓涂抹的药液,用棉球擦干后将小鼠处死,剪下双耳,用直径为8mm打孔器将双耳同部位打下圆耳片,用电子天平称重,以左耳作对照,左右耳片质量之差为肿胀程度,计算各组肿胀度,求出肿胀抑制率肿胀抑制率=(空白对照组平均肿胀度-给药组平均肿胀度)/空白对照组平均肿胀度
×
100%]。
[0151]
3.实验结果
[0152]
结果如表10所示:
[0153]
表10 对小鼠二甲苯所致耳廓肿胀情况(x土sd,n=10)
[0154][0155]
注:与空白对照组比较:*p《0.05;**p《0.01
[0156]
从表10可见,低、中、高剂量药物组与空白对照组比较,差异有统计学意义(p《0.05或p《0.01)o表明白菊湿疹乳膏能明显抑制二甲苯所致的小鼠耳廓炎症,且随剂量增大效果更明显。
[0157]
4结论
[0158]
白菊湿疹乳膏能明显抑制二甲苯所致的小鼠耳廓炎症,且具有较好的量-效关系,表明白菊湿疹膏对此模型有明显的抗炎作用。
[0159]
五、药效学试验—对磷酸组胺致豚鼠足跖痒致痒阈的影响:
[0160]
1、试验材料
[0161]
1.1实验动物
[0162]
普通级豚鼠(hartley),体重280-320g雌雄各半。由北京昌扬西山养殖场引进,许可证号:scxk(京)2011-0010。
[0163]
1.2实验药品与试剂
[0164]
白菊湿疹膏本发明实施例1产品;
[0165]
复方醋酸地塞米松乳膏(皮炎平)20克:15mgo广州白云山制药有限公司白云山何济公制药厂生产,批号:v1037;
[0166]
磷酸组胺:上海耕奔生物技术有限公司,批号:20091130。
[0167]
2实验方法
[0168]
按照文献“王国江,顾军.小鼠背部变应性接触性皮炎模型的建立[j].中国职业医学,2004,31(1):17-19”记载的方法进行:
[0169]
取300-350g豚鼠60只,随机分为6组,每组10只,雌雄各半,分组与给药量同对二甲
苯致小鼠肿胀的影响试验。实验前1d,给各组豚鼠右后足背剃毛,并涂药1次。实验当日,用0号砂纸擦伤动物右后足背剃毛处,以少量渗血为度,面积为约1cm2,局部再涂药一次,末次给药后30min开始在创面处滴以0.02%磷酸组织胺0.05ml/只,每次间隔时间为3min,直至出现豚鼠回头舔右后足,以开始出现豚鼠回头舔右后足时所给予的磷酸组织胺总量最为致痒阈。记录并比较各组致痒,进行组间t检验。
[0170]
3.实验结果
[0171]
实验结果如表11所示:
[0172]
表11 对豚鼠磷酸组胺致足痒致痒阈的影响(x土s,n=12)
[0173][0174]
注:与空白对照组比较:*p《0.05**p《0.01
[0175]
从表11可知,中~高剂量药物组与空白对照组比较,差异有统计学意义(p《0.05或p《0.01)。高、中剂量药物组对提高磷酸组胺致痒阈的作用比较明显,低剂量药物组虽有一定的作用,但差异无显著性意义。说明湿疹乳膏可显著提高磷酸组胺对豚鼠的致痒阈,且随剂量增大效果更明显。
[0176]
4结论
[0177]
白菊湿疹乳膏能明显提高磷酸组胺对豚鼠的致痒阈,且随剂量增大效果有增强的趋势,表明白菊湿疹膏对磷酸组胺引起豚鼠的致痒模型有明显的抑制作用。
[0178]
六、药效学试验—对dncb诱发小鼠迟发型超敏反应的影响:
[0179]
1.试验材料
[0180]
1.1实验动物
[0181]
清洁级昆明种(km)小鼠,20-25g,雄性,由山西医科大学动物实验中心提供。合格证号:scxk(晋)2010-0005。
[0182]
昆明种小白鼠,雌雄各半,体重20
±
2.0g,中国食品药品检定研究院实验动物资源研究所提供,许可证号:scxk-(京)2009-0017,实验动物质量合格证号:0269607。
[0183]
1.2实验药品与试剂
[0184]
白菊湿疹膏,本发明实施例1产品;
[0185]
复方醋酸地塞米松乳膏(皮炎平)20克:15mg;广州白云山制药有限公司白云山何济公制药厂生产,批号:v1037;
[0186]
2,4-二硝基氯苯(dncb):中国医药公司北京分公司,批号:20101026。
[0187]
2.实验方法
[0188]
取昆明种小鼠60只,随机分为6组,脱毛前处理、涂药方法及分组均同前。白菊湿疹膏低、中、高剂量组均涂抹相应药膏0.5,1.0,2.0g.kg-1
,阳性对照组在小鼠右耳耳廓均匀
涂抹皮炎平乳膏1.0g.kg-1
,空白对照组在小鼠右耳耳廓均匀涂抹0.9%氯化钠注射液0.05ml,基质对照组涂抹空白基质1.0g.kg-1
。每天涂药2次,间隔6h给药1次,连续给药7d。实验第2天与第3天均用5%溶液dncb溶液0.1ml均匀涂抹各组小鼠腹部致敏,第7天于涂药后2h,用l%dncb0.1ml涂各小鼠右耳激发,在激发24h后,颈椎脱臼处死小鼠,剪下双耳,对齐,用8mm打孔器取下圆型耳片,迅速用分析天平称量双耳,并计算肿胀度。称量后耳片固定,做病理切片,观察耳组织病理改变。计量资料以均数土标准差(x
±
s)表示,两组间比较釆用独立样本的t检验进行统计分析。
[0189]
3.实验结果
[0190]
实验结果如表12所示:
[0191]
表12 对小鼠dncb所致小鼠dth耳廓肿胀的影响况(x土s,n=10)
[0192][0193]
注:与空白对照组比较:*p《0.05;**p《0.01。
[0194]
结果可见:白菊湿疹膏对dncb诱发小鼠迟发型超敏反应模型组(空白对照组)出现显著肿胀,说明模型复制成功。与模型组比较,白菊湿疹中、高剂量组和皮炎平组均可显著减轻小鼠迟发型超敏反应模型耳廓皮肤的肿胀质量(p《0.01),,说明白菊湿疹膏可显著改善小鼠退发型超敏反应模型耳廓皮肤病变,且以高剂量效果相对较好。
[0195]
4.结论
[0196]
白菊湿疹乳膏能明显抑制dncb诱发小鼠迟发型超敏反应模型组出现的皮肤肿胀,且具有一定的量-效关系,表明白菊湿疹膏对此模型具有一定的抑制作用。
[0197]
综上所述,本发明进行了以上动物实验通过动物模型试验观察与判定白菊湿疹膏的安全性和药效学作用,为临床试验提供科学依据与参考:
[0198]
实验设白菊湿疹膏制剂低、中、高三个剂量组,正常对照组(基质对照组)和阳性药对照组,白菊湿疹膏的剂量为0.5、1.0和2.0g
·
kg-1
。分别观察了对km小鼠口服的急性毒性、皮肤给药的急性毒性、对豚鼠的皮肤主动过敏实验、家兔的皮肤刺激实验;药效学研究观察了白菊湿疹膏对小鼠二甲苯所致耳肿胀的影响、dncb所致小鼠耳部皮肤迟发性过敏肿胀(dth)的影响,以及对磷酸组胺引起的豚鼠皮肤致痒阈剂量的影响;进行白菊湿疹膏的安全性和药效学作用的评价。
[0199]
结果表明:白菊湿疹膏对小鼠二甲苯所致耳肿胀有明显的降低作用,可减轻dncb所致小鼠耳重量的增加,以及对磷酸组胺引起的豚鼠皮肤致痒阈剂量的影响;安全性实验表明,白菊湿疹膏口服和皮肤给药均不能求得ld
50
,其最大给药量分别为临床拟用剂量的1600倍和1000倍;对豚鼠的皮肤主动过敏实验为阴性;对家兔的完整与破损皮肤均无刺激性。因此,在本实验条件下,新型中药制剂白菊湿疹膏在0.5、1.0和2.0g
·
kg-1
剂量时,对所有实验动物模型是有效和安全的,这些实验结果可为临床进一步观察和使用提供参考。
[0200]
七.临床实验报告
[0201]
1.临床资料
[0202]
1.1一般资料
[0203]
本项实验主要针对婴幼儿湿疹症,展开临床疗效与安全性方面的研究。所有收治的受试者均符合婴儿湿疹临床诊断标准。
[0204]
1.2病情的病类特征:
[0205]
(1)受试患儿的临床症状与体征、实验室血检(免)结果均表现为婴幼儿湿疹的共性与个性特征。
[0206]
(2)受试患儿的临床症状与体征情况均表现为日益加重趋势。
[0207]
(3)受试患儿湿疹病情严重发展已完全或部分影响饮食、睡眠和日常正常活动。
[0208]
(4)受试患儿在收治前均已采用传统疗法和药物治疗,因病情日渐加剧均无明显好转。
[0209]
1.3病程的病类性特征
[0210]
(1)急性婴幼儿湿疹患儿在受试前的病程均在3天以上。
[0211]
(2)亚急性和慢性婴幼儿湿疹患儿在受试前的病程均在30天以内。1.4临床实验日期:2021年5月至2021年11月
[0212]
1.5受试患儿的年龄范围:1月至12岁。具体见表13、14、15。
[0213]
表13 实验组患儿治疗前的自然情况表(10例)
[0214]
编号姓名年龄性别病灶部位发病时间001张依迪9岁女面部6天002李嘉禾2月男面、胸、背部28天003侯奥森2月男面部5天004李星泽4岁男颈、背部2个月005白然圣4岁男颌、耳、眼周部3年006李柯梵8月男会阴部2个月007白宜逍14月女会阴部1个月008李志斌12岁男左手背部3天009白森1月男额、面颊5天010郭赛女12天女颈部2天
[0215]
表14 实验组入组时的症状与体征统计表
[0216]
编号姓名症状与体征备注001张依迪红肿、痒、刺痛重度002李嘉禾红肿、痒、刺痛中度003侯奥森红肿、痒、刺痛轻度004李星泽红肿、痒、刺痛重度005白然圣红肿、痒、刺痛重度006李柯梵红肿、痒、刺痛重度007白宜逍红肿、痒、刺痛重度008李志斌红肿、痒、刺痛重度
009白森红肿、痒、刺痛中度010郭赛女红肿、痒、刺痛轻度
[0217]
表15 受试者年龄与病情分类表(10例)
[0218][0219]
表15统计结果可见,婴幼儿湿疹症的急性和亚急性患病年龄主要集中在1周岁前后,一般在2个月左右开始患病,这与哺乳期的喂养方式和护理不当有关;而1周岁以后慢性与反复发作迁延性的婴幼儿湿疹,主要与遗传因素以及洗护方法不当有关。
[0220]
1.6受试患儿在治疗前的病情与病程
[0221]
在治疗前根据诊断积分对所有受试患儿做病情与病程评估,并按诊断积分归纳区分为重症、中症与轻症三类:其中25分以上为重症,有3例,占总受试人数30%;15至24分为中症患儿,有4例,占40%;5至14分为轻症患儿,有3例,占30%。详见表16。
[0222]
表16 受试患儿治疗前诊断积分表(10例)
[0223]
病情病程积分例数占比率(%)p值重症25分以上330 中症15-24分440 轻症5-14分330 合计 10100 [0224]
经表3、4、5、6统计,在7个月内随机收治的10例患儿中,共分为急性和亚急性湿疹组9例,慢性湿疹组1例,均呈平行试验与治疗,各组间年龄(均属婴幼儿期)、病种(婴幼儿湿疹)、病情与病程等统计参数均无明显差异(p值《0.05),具有统计学意义。
[0225]
1.7试验方式:采取患儿治疗前后自身对照方式进行,主要对照科目:临床症状与体征的观测记录和对比性统计。一般项目检查的观测记录和对比性统计。
[0226]
1.8受试患儿入选的诊断与参照标准
[0227]
《临床外科学》中西医结合
[0228]
《实用外科学》
[0229]
《中医外科疾病诊疗常规》
[0230]
《中医外科学》
[0231]
2.临床试验诊断标准
[0232]
2.1临床诊断
[0233]
根据婴幼儿湿疹的病程和皮损特点,可将婴儿湿疹分为急性、亚急性和慢性湿疹三种;根据皮损发生部位将湿疹又可分为外阴湿疹、肛门湿疹、面部湿疹、手部湿疹、乳房湿疹、腋窝湿疹等各种类型。
[0234]
(1)急性湿疹:皮肤呈多形性,如红斑、丘疹、水泡、糜烂、渗出、痂皮、脱屑,常数种形态同时存在;起病急,自觉灼热和剧烈瘙痒;皮损常对称分布,以头、面、四肢远端和阴部等处多见,亦可泛发全身;可发展成亚急性或慢性湿疹,时轻时重,反复不愈。
[0235]
(2)亚急性湿疹:皮损渗出较少,以丘疹、丘疱疹、结痂、鳞屑为主。有轻度糜烂面,颜色较黯红。亦可见轻度浸润,剧烈瘙痒。
[0236]
(3)慢性湿疹:多局限于某一部位,境界清楚,有明显的肥厚浸润,表面粗糙,或呈苔藓样变,颜色呈褐红或褐色,常伴有丘疱疹、痂皮、抓痕。倾向湿润变化,常反复发作,时轻时重,有阵发性瘙痒。
[0237]
2.2鉴别诊断
[0238]
(1)急性湿疹应与接触性皮炎鉴别:后者常有明确的接触史,病变局限于接触部位,皮疹多单一形态,易起大疱,境界清楚,病程短,去除病因后,易治愈。
[0239]
(2)慢性湿疹需与神经性皮炎相鉴别:后者多见于颈、肘、骶尾部,有典型苔藓样变,无多形性皮损,无渗出倾向。
[0240]
(3)手足部湿疹需与手足癣相鉴别:后者皮损境界清楚,有叶状鳞屑附着,夏季加重,常并发指趾间糜烂,鳞屑内可找到菌丝。
[0241]
3.临床评价
[0242]
本症在临床可用中西医两种方法进行治疗。某些西药除湿止痒作用虽较好,但副作用很大,其一,刺激大,幼儿治疗时依从性差。其二疗程长不易根治。中药治疗相对西药而言,有快速改善临床症状、疗程短和治愈率高等优势,无毒副作用,安全性强。
[0243]
4.临床试验治疗方案
[0244]
4.1试验用药的名称与规格
[0245]
名称:白菊湿疹膏
[0246]
规格:膏剂,牙膏外形盛装,每支膏剂内容物净重量10g。
[0247]
4.2用药方法
[0248]
急性、亚急性和慢性婴儿湿疹的外用(于湿疹皮损部位全覆盖涂抹)方法一致,不需单独加减。日用3次,每次涂抹用药量视皮损面积而定。在试验期间与正常临床应用中,所有病例(包括急性、亚急性和慢性;重度、中度和轻度湿疹)除外用本品治疗外,不需使用其他治疗湿疹症药品(包括外用和内服药品)。
[0249]
5.观察项目
[0250]
5.1安全性观测
[0251]
(1)一般检查项目:体温、脉搏、血压、呼吸、体重和精神。
[0252]
(2)有无不良反应。
[0253]
初诊首日、明显改善日、完全痊愈日各观测检查记录一次。
[0254]
5.2疗效性观测
[0255]
临床症状与体征的观测与检查。
[0256]
初诊首日、明显改善日、完全痊愈日各观测检查记录一次。
[0257]
6.观察记录方法
[0258]
临床试验观察期间,按方案要求的相应时间随诊与检查,并确认填写病例观察表,对各项检查结果按设计的分级量化积分标准分别计分,当实验结束后按统计学方法进行安全性与疗效性统计。
[0259]
7疗效评定标准
[0260]
7.1综合疗效判定标准
[0261]
改善率=(治疗前积分-治疗后积分)
÷
治疗前积分
[0262]
(1)临床痊愈:临床症状、体征完全消失,重点肉眼观察湿疹病灶完全消失。积分减少≥95%。
[0263]
(2)临床显效:临床症状、体征基本消失,肉眼观察湿疹病灶基本消失。积分减少95%,但≥70%。
[0264]
(3)临床有效:临床症状、体征明显改善,肉眼观察湿疹病灶明显缩小或改变,瘙痒症消失。积分减少70%,但≥50%。
[0265]
(4)临床无效:临床症状、体征无明显改善,肉眼观察湿疹病灶未见改变甚至加重。积分减少30%。
[0266]
7.2疗效时间评定标准
[0267]
(1)起效时间:临床症状、体征开始改变,症候积分减少≥30%,《70%。所需时间为起效时间。
[0268]
(2)显效时间:临床症状、体征明显改善,症候积分减少≥70%,《95%。所需时间为显效时间。
[0269]
(3)痊愈时间:临床症状、体征完全消失,症候积分减少≥95%。所需时间为痊愈时间。
[0270]
7.3安全性评价标准
[0271]
1级:安全,无任何不良反应。
[0272]
2级:比较安全,如有不良反应,不需做任何处置能继续用药治疗。
[0273]
3级:有安全性问题,有中等程度的不良反应,做适当处置后仍能继续用药治疗。
[0274]
4级:因不良反应中止试验。
[0275]
7.4中止试验标准
[0276]
(1)为保障受试患儿的安全,治疗开始后第3天检查,临床症状、体征无缓解或加重应中止试验,疗效判定为无效,可马上改为其他药物或疗法治疗。
[0277]
(2)疗程未结束而出现严重不良反应者,根据临床医生判定应立即中止临床试验。但已超过3天疗程者应统计疗效。
[0278]
(3)患儿及家长在临床试验过程中不愿意进行临床试验,向临床主管医生提出中止临床试验的要求,可以中止该患儿的临床试验。但已超过3天疗程者应统计疗效。
[0279]
(4)研究者要认真记录试验中止原因,标明中止与实验的关系,其中包括:自动退出(不能坚持治疗者);发现严重不良反应者;症状无缓解或继续恶化者、必须采取紧急措施者。研究者应详细记录中止时间和疗效评价。
[0280]
7.5临床研究中各类试验项目的积分量化标准
[0281]
7.5.1临床症状与体征的积分量化标准,共12项,每项分4级积分。量化标准:0分为无临床症状与体征表现;1分为有轻度临床症状与体征表现;2分为有中度临床症状与体征表现;3分为有重度临床症状与体征表现。详见表17。
[0282]
表17 临床症状与体征积分量化标准表
[0283]
序号项目积分序号项目积分序号项目积分1红肿0-35渗出0-39肥厚0-32丘疹0-36抓痕0-310粗糙0-33疱疹0-37糜烂0-311结痂0-34瘙痒0-38苔藓0-312鳞屑0-3
[0284]
病情与病程在症状与体征上的量化反映可区分为重度、中度与轻度。临床症状与体征的累计积分在25分(含25分)以上为重度;累计积分在15至24分之间为中度;累计积分在5至14分之间为轻度;累计积分在1至4分之间为临床症状与体征不明显。
[0285]
7.5.2临床症状与体征总积分显示疗效(改善率)的评定标准共分为4级
[0286]
评定标准:疗效为痊愈的临床症状与体征的评定标准为完全恢复正常,积分改善率在95%以上;疗效为显效的临床症状与体征的评定标准为基本恢复正常,积分改善率在70-94%之间;疗效为有效的临床症状与体征的评定标准为有所减轻或改善,积分改善率在45-69%之间;判定无效的临床症状与体征的评定标准为无改善或者加重,积分改善率在44%以下;详见表18。
[0287]
表18 评定临床症状与体征改善率标准表
[0288]
疗效症状与体征积分改善率%痊愈完全恢复95以上显效基本恢复70-94有效减轻改善45-69无效未改加重44以下
[0289]
7.5.3临床试验安全性观察
[0290]
一般检查项目积分量化标准,共6项,每项分4级积分。0分为安全,无任何不良反应;1分为比较安全,如有不良反应,不需做任何处置能继续用药治疗;2分为有安全性问题,有中等程度的不良反应,做适当处置后仍能继续用药治疗;3分为有严重安全性问题,因不良反应需及时中止试验。详见表19。
[0291]
表19 一般检查项目(安全性)积分量化标准表
[0292]
项目检查结果积分项目检查结果积分体温无、轻、中、重0-3呼吸无、轻、中、重0-3
脉搏无、轻、中、重0-3体重无、轻、中、重0-3血压无、轻、中、重0-3精神无、轻、中、重0-3
[0293]
7.5.4一般检查项目的总积分显示临床安全性的评定标准
[0294]
一般检查项目的观测与统计,可严格掌控临床试验中湿疹患儿对试验制剂的任何不良反应情况,亦可通过一般检查项目观察到试验制剂的临床安全性。
[0295]
当总积分安全率达到100%时为安全;当总积分安全率达到90%时,为比较安全;当总积分安全率达到80%,为有安全性问题;当总积分安全率低于70%以下时,为不安全,应中止试验。详见表20。
[0296]
表20 一般检查项目总积分判定安全性标准表
[0297]
安全性分类检查结果总积分安全率%安全无任何不良反应100比较安全有轻度不良反应90有安全问题有中度不良反应80不安全有严重不良反应70
[0298]
7.5.5统计学方法
[0299]
所有数据均采用sas 8.0统计软件进行处理。
[0300]
等级资料用ridit检验。
[0301]
计数资料用卡方检验。
[0302]
计量资料用t检验。
[0303]
在总疗效,临床症状与体征,一般检查(安全性)项目,病情与疗效关系,病程与疗效关系等方面的基础上,进行统计学归纳和评价。
[0304]
8.疗效与实验结果
[0305]
8.1总的疗效比较与结果,详见表21、22。
[0306]
8.1.1治疗前后临床症状与体征的总积分统计结果,详见表21。
[0307]
表21 治疗前后临床症状与体征总积分与改善率统计表(10例)
[0308]
科目例数治前积分治后积分改善率(%)p值红肿10300100 丘疹10300100 疱疹7190100 瘙痒10300100 刺痛10300100 抓痕6160100 渗出460100 糜烂130100 苔藓7180100 粗糙8160100 结痂13166.66》0.05鳞屑58187.50 [0309]
表21统计结果显示,使用中药制剂白菊湿疹膏临床治疗婴幼儿湿疹,尤其对使用
传统疗法与应用常规抑制湿疹药物久治不愈的患儿,疗效显著,主要特征为疗程短,起效快,治愈率高。其中治疗急性和亚急性湿疹的疗程和起效时间以及治疗效果,相比治疗慢性湿疹更为突出。观察与统计中验证了婴幼儿湿疹症的临床症状与体征重点表现在病灶处明显红肿,有大片丘疹与疱疹覆盖,因湿疹与有害微生物菌浸润,产生瘙痒,抓痕和刺痛,进而引起糜烂,渗出。亚急性与慢性湿疹因久治难愈,形成了苔藓样的粗糙皮肤,结痂和鳞屑皮状。
[0310]
8.1.2临床症状与体征总积分显示临床疗效(改善率)的统计结果,详见表22。
[0311]
表22 临床症状与体征总积分显示临床疗效统计表(10例)
[0312][0313][0314]
表22统计结果显示,白菊湿疹膏治疗婴幼儿湿疹症的临床疗效,可以从临床治疗前后的症状与体征总改善率进行分析与判定。结果表明,10例受试患儿中有9例患儿经用白菊湿疹膏治疗后,其临床症状与体征完全消失,达到治愈标准,总治愈率为90%。有1例的临床症状与体征的总改善率为92.30%,其临床的基本症状与体征已消失(只剩脱痂未彻底),归为疗效显著,合计总有效率为100%。
[0315]
8.2临床安全性观测与结果
[0316]
8.2.1临床安全性观测一般检查项目总积分统计与分析结果,详见表23。
[0317]
表23 一般检查项目总积分统计表(10例)
[0318]
观察项目例数治前积分治中积分治后积分改善率(%)p体温91230100 脉搏8800100 血压4500100 呼吸3300100 体重00000 精神91450100 合计334280100 [0319]
表23统计结果显示,白菊湿疹膏在治疗婴幼儿湿疹症临床中,在一般检查项目(体温、脉搏、血压、呼吸、体重和精神)方面,经治前、治中和治后对比检测,均未发生任何不良反应。治疗后因湿疹症引起的体温、脉搏、血压、呼吸和精神等体征与不良反应,均有不同程度的好转与改善。如治前体温总积分为12分,治中总积分为3,治后总积分为0,其改善率为100%;又如治前脉搏总积分为8分,治中总积分为0分,其改善率在治中就达到100%;再如
治前精神总积分为14分,治中总积分为5分,治后总积分为0,其改善率为100%。通过观察与分析,白菊湿疹膏在临床治疗中具备了很好的安全性。
[0320]
8.3典型病例
[0321]
8.3.1病例1:急性婴幼儿湿疹症
[0322]
患儿张
×
迪,女,9岁,因面部急性湿疹于2021年5月7日来我院诊治。查:无既往病史,6天前发现两侧面颊起大片红肿,伴丘、疱疹,瘙痒刺痛,因瘙痒形成抓痕。一般检查时发现:病灶区体温明显高于全身体温,脉搏略快,精神不振。临床诊断为急性婴幼儿湿疹症。给以外抹白菊湿疹膏治疗,初诊日2次,第2日和第3日各一次,共三天4次外抹给药。治疗第2天临床症状与体征均显著改善,第3天全部临床症状与体征均消失。治疗过程未出现不良反应。
[0323]
8.3.2病例2:亚急性婴幼儿湿疹症
[0324]
患儿李
×
禾,男,2月,因面、胸、背多发湿疹于2021年5月28日来我院诊治。查:无遗传因素,28天前洗涤后发现面、胸、背部成片红肿,第3天发现红肿处产生丘、疱疹,患儿哭闹不止,至来院就诊时,患儿已明显出现红肿、丘疹、疱疹、抓痕等临床症状与体征。经查询,可能发病原因与包裹婴儿物质与洗护不当有关。给以白菊湿疹膏(门诊处置)外抹治疗。初诊首日3次给药治疗,第2、3、4日各外抹给药2次,第5日1次给药。临床观察:给药第1天,患儿即恢复正常饮食与睡眠,给药第2天见症状明显改善,第4日观察,临床症状和体征完全消失,在临床治疗中未发生任何应急性不良反应。
[0325]
8.3.3病例3:慢性婴幼儿湿疹症
[0326]
患儿白
×
圣,男,4岁,因下颌、耳和眼周多发湿疹于2021年6月1日来我院诊治。经询查,3年前发病,可能与遗传因素有关(家族有发病史),因此患儿发病未被重视。就诊时患儿临床症状与体征(红肿、丘疹、瘙痒、刺痛、皮肤粗糙(患处))均属中度病情。经查询,可能发病原因与婴儿衣物和洗护不当有关。门诊处置给以白菊湿疹膏治疗。每日外抹给药,日抹1次,3次治愈。治疗过程未见不适。
[0327]
9.小结
[0328]
9.1试验与统计结果
[0329]
从临床症状与体征方面对疗效的统计与分析结果显示:总有效率为100%,其中治愈率为90%,显效率为10%,有效率为0,无效率为0。收治的10例婴幼儿湿疹患儿的临床症状与体征的平均改善率为100%。
[0330]
从一般检查项目的统计与分析结果显示:治中、治后均未发生一例因使用白菊湿疹膏而产生的不良反应,也未引起过敏性事故。
[0331]
9.2结论
[0332]
通过采用外抹方式给药白菊湿疹膏对10例婴幼儿湿疹症患儿进行临床试验与治疗,并重点从体现疗效与安全性研究角度,将临床症状与体征的对比观察,以及一般检查项目的对比与观察,作为综合评价该制剂临床疗效与安全性的客观标准与统计指标,完成了本课题研究。结果显示,白菊湿疹膏作为治疗婴幼儿湿疹症,具有安全显著的疗效。
[0333]
实验结果综合性分析表明,采用白菊湿疹膏治疗婴幼儿湿疹症疗效显著安全性强,具有广泛的临床应用和推广价值。
[0334]
上述实例只是为说明本发明的技术构思以及技术特点,并不能以此限制本发明的
保护范围。凡根据本发明的实质所做的等效变换或修饰,都应该涵盖在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。