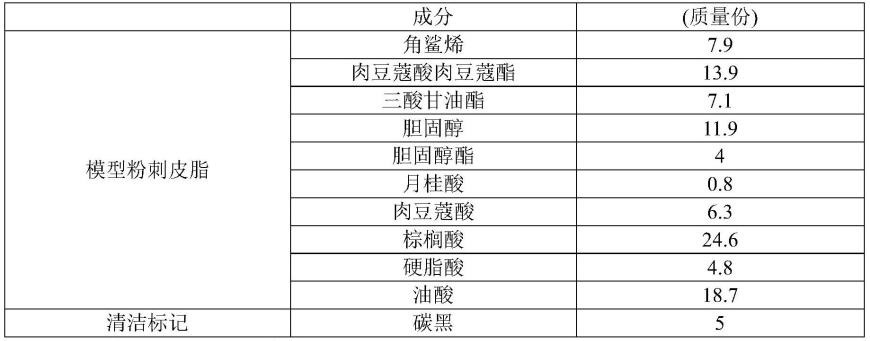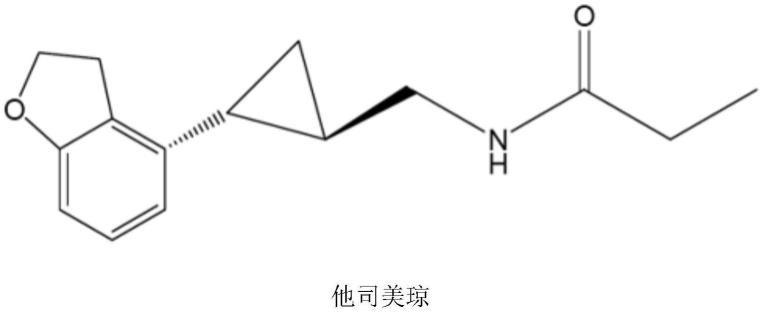
液体他司美琼制剂及其使用方法
1.相关申请的交叉引用
2.本技术要求共同未决的2019年12月13日提交的美国临时专利申请系列号62/947,774、2020年2月11日提交的申请号62/972,902和2020年11月30日提交的申请号63/119,488的优先权,在此以充分阐述的方式将其全文引入。
背景技术:
3.本发明提供了包含他司美琼(参见美国专利5,856,529,权利要求7)或反式n-[[2-(2,3-二氢苯并呋喃-4-基)环丙-1-基]甲基]丙酰胺的液态悬浮液的药学上精致的制剂,所述反式n-[[2-(2,3-二氢苯并呋喃-4-基)环丙-1-基]甲基]丙酰胺为中的活性成分,是批准用于非24小时睡醒障碍(非24)的药物,并且可作为固体口服剂型商购获得,即包含20mg他司美琼的胶囊。
[0004]
制备适于向患者施用的药物的药学上精致的悬浮液(特别是作为液体制剂)存在一系列挑战,其中典型的挑战可以是物理稳定性、含量均匀性、沉降、结块、再悬浮性、晶体生长和不期望的味道或气味。参见alok k.kulshreshtha、onkar n.singh和g.michael wall(编)“pharmaceutical suspensions:from formulation development to manufacturing.”。制备适合施用于患者,特别是儿科患者的他司美琼的药学上精致的液体悬浮液由于以下因素而特别复杂:例如他司美琼的味道令人不快,在合适体积的液体中获得适合测量和施用有效单位剂量的粘度的必要性,液体他司美琼制剂的化学稳定性,其在液体载体中的溶解速率和溶解度,以及制备为他司美琼悬浮液的液体制剂的不透明性。获得他司美琼的药学上精致的制剂需要以成功的方式解决这些复杂因素中的每一个,同时确保所得制剂易于制造。
[0005]
迄今为止,美国专利5 856 529(例如,第17栏)报道了诸如他司美琼等药物的药物组合物可以制备成适合于口服施用的制剂,包括具有用于制备糖浆或水性液体悬浮液的液体载体的组合物,其中可以使用常规添加剂如悬浮剂、乳化剂、润湿剂和防腐剂,以及增味剂和/或着色剂。
[0006][0007]
如本领域另外已知的,他司美琼可以制备为熔点为约78℃(dsc)的白色至灰白色粉末。它在95%乙醇、甲醇、乙腈、乙酸乙酯、异丙醇、聚乙二醇(peg-300和peg-400)中高度
可溶,但在水中溶解性差。他司美琼的饱和水溶液的天然ph为8.5,并且其水溶性基本上不受ph影响。
技术实现要素:
[0008]
本文公开的发明提供了在水性悬浮液中包含他司美琼的药学上精致的液体组合物,其中预定体积的药物组合物(例如0.35至10ml)将提供悬浮于其中的单位剂量的活性成分,使得向个体施用的一个或多个此种单位剂量将提供可有效治疗或预防施用了药物所针对的疾病或病症的量的他司美琼。
[0009]
本发明的药物组合物提供了他司美琼的均匀水性悬浮液,其可包括一种或多种悬浮剂和一种或多种掩味剂。例如,此种组合物可以包括纤维素悬浮剂作为悬浮剂。悬浮液的典型粘度在环境条件下小于或等于约150厘泊(cps)。
[0010]
如上所述的药物组合物可以配制成在环境条件下具有大于1至约1.5的比重。此外,此类制剂可另外包括一种或多种不透明度赋予剂和一种或多种表面活性剂,例如非离子表面活性剂,如聚山梨醇酯80。
[0011]
如上所述的药物组合物可以是下述药物组合物,其中可用于本发明组合物的悬浮剂是甲基纤维素、羟丙基甲基纤维素(hpmc)、羧丙基甲基纤维素钠(cpmc)或羧甲基纤维素钠和微晶纤维素中的一种或多种。作为实例,本发明的药物组合物可以包含不透明度赋予剂、甜味剂和抗氧化剂,其中悬浮剂是微晶纤维素和羧甲基纤维素或其盐。作为另选,悬浮剂可以是微晶纤维素和羧甲基纤维素钠。例如,悬浮剂可以是(1)微晶纤维素,其中60%的微晶纤维素颗粒的直径(其d
60
)小于0.2μm;和(2)羧甲基纤维素钠。
[0012]
如上所述的药物组合物可以是其中悬浮剂可以是rc-591微晶纤维素和羧甲基纤维素钠的药物组合物。
[0013]
本发明的药物组合物的实例是包含甘露醇作为不透明度赋予剂的药物组合物。
[0014]
如上所述的药物组合物可以是其中掩味剂是甜味剂的药物组合物。甜味剂可包括单糖或二糖和高强度甜味剂,例如甜菊糖、阿斯巴甜、三氯蔗糖、纽甜、乙酰磺胺酸钾(ace-k)、糖精、爱德万甜(advantame)或环己氨基磺酸盐。更具体地,单糖或二糖可以是蔗糖并且总固体浓度小于500mg/ml。作为实例,甘露糖醇的浓度可以小于200mg/ml并且蔗糖的浓度可以《300mg/ml,例如,甘露糖醇的浓度可以不超过100mg/ml并且蔗糖的浓度可以不超过200mg/ml,并且总固体浓度可以不超过350mg/ml。
[0015]
根据上文,这些含有他司美琼的组合物可包含:
[0016]
(1)非离子表面活性剂,其为聚山梨醇酯80,以0.5至5mg/ml的浓度存在,包括1至3mg/ml(或更优选1至2mg/ml,或最优选约1mg/ml)的浓度。如上所述的药物组合物可以包括其中他司美琼以1至6mg/ml、2至5mg/ml、1mg/ml或4mg/ml的浓度存在的药物组合物。
[0017]
(2)他司美琼,其以1至6mg/ml或2至5mg/ml或1mg/ml或4mg/ml的浓度存在;和悬浮剂,其为微晶纤维素和羧甲基纤维素钠,以0至30mg/ml或10至20mg/ml或20mg/ml的浓度存在。
[0018]
(3)作为不透明度赋予剂的甘露醇,其以(1)不超过200mg/ml或(2)小于200mg/ml或(3)50至100mg/ml或(4)100mg/ml的浓度存在;作为甜味剂存在的蔗糖,其浓度为(1)不超过300mg/ml或(2)小于300mg/ml或(3)150至250mg/ml或(4)200mg/ml;高强度甜味剂;作为
非离子表面活性剂存在的聚山梨醇酯,其浓度为(1)1至5mg/ml或(2)1至3mg/ml或(3)2mg/ml;抗氧化剂、氯化钠和增味剂。
[0019]
上述组合物可以配制成具有目标ph水平。优选地,配制这些组合物以实现4.0
±
0.5的目标ph。此外,用上述规格配制的组合物旨在表现出以下发行规格:
[0020]
(1)稳定性:在(1)5
±
3℃、(2)25
±
2℃(在60
±
5%相对湿度下)和(3)40
±
2℃(在75
±
5%相对湿度下)各连续储存一个、两个或三个月的时间之后,使用高效液相色谱(hplc)的总杂质不超过1.5重量%,相对于已知杂质不超过0.5重量%,并且相对于未指定杂质不超过0.2重量%;
[0021]
(2)粘度:5至30厘泊(cp或cps),例如约20cps(在环境条件下);
[0022]
(3)比重:1.1至1.3mg/ml;
[0023]
(4)ph:4.0至5.0;
[0024]
(5)粒径分布:d
90
=100至150μm,d
50
=50至70μm,并且d
10
=15至40μm。
[0025]
(6)溶解:在1n hcl中搅拌15分钟(以50转/分钟(rpm))后大于或等于90%。
[0026]
上文关于“粒径分布”的描述是指直径大于、小于或等于所述物理侧的样品内的颗粒的百分比,例如d
50
=50至70μm是指其中相同批次中50%颗粒的直径具有50至70微米之间的直径的样品。如本文所用,粒径分布是指对悬浮在本文所述的药物制剂中的他司美琼颗粒进行的测量。可以使用激光衍射技术,例如使用malvern mastersizer 2000或malvern mastersizer 3000的激光散射检测进行这种粒径测量。
[0027]
本发明的另一方面提供了为有需要的患者治疗史密斯-马吉利综合征(sms)的方法,所述方法包括:确定患者的体重;并且在患者的体重等于或小于28kg的情况下,每天一次向患者施用等于0.7mg/kg的第一剂量的他司美琼;或者在患者的体重大于28kg的情况下,每天一次向患者施用等于20mg的第二剂量的他司美琼。
附图说明
[0028]
结合描述本发明的各种实施方式和方面的附图,从本发明的各种方面的以下详细描述中将更容易理解本发明的这些和其他特征,在附图中:
[0029]
图1显示了他司美琼液体制剂的有效剂量随患者体重变化的曲线;
[0030]
图2显示了根据本发明的实施方式施用他司美琼液体制剂的各个步骤的图示。
[0031]
请注意,附图不是按比例的。附图仅用于描述本发明的典型方面,因此不应被视为限制本发明的范围。
具体实施方式
[0032]
制备他司美琼的药学上精致的液体悬浮液存在许多困难,其中每一个都在下述组合物中得以解决。
[0033]
味道
[0034]
他司美琼在水中的溶解度为约1mg/ml。然而,在制剂赋形剂的存在下,药物可能基本上不溶于大多数悬浮液制剂。然而,痕量溶解并赋予制剂苦味,这难以掩盖。因此,考虑以下配制方法以改善味道。
[0035]
·
包含作为甜味剂/掩味剂的蔗糖、三氯蔗糖和氯化钠的组合。
[0036]
·
包含rc-591,一种作为悬浮剂的亲水性聚合物,其在水的存在下水合和溶胀。一定量的水是适当水合和分散聚合物所必需的,加上额外量的水是溶解抗坏血酸和苯甲酸钠所必需的。结果,可用于溶解蔗糖的水量是有限的,因此200mg/ml的蔗糖被确定为可溶解的最大量。
[0037]
·
由于不能将蔗糖浓度提高到200mg/ml以上,所以还包括1mg/ml的三氯蔗糖作为甜味剂,这使得味道更甜,从而有助于更好地掩盖苦味。
[0038]
·
另外,在5mg/ml的浓度下,包含氯化钠掩盖了苦味并且还改善了整体味道。
[0039]
粘度
[0040]
为了在摇动时保持他司美琼药物物质颗粒处于均匀悬浮状态,需要确定合适的增粘剂及其最佳水平。
[0041]
甲基纤维素-a15c、甲基纤维素-a4m和rc-591(微晶纤维素/cmc钠)可用作悬浮剂。这些等级的甲基纤维素都产生含有未完全水合的聚合物颗粒的悬浮液,且其粘度在高侧,这不利地影响其溶解速率。
[0042]
6mg/ml浓度且未经均化的rc-591提供所需的物理化学特性,例如快速溶解、在轻轻摇动储存的悬浮瓶时完全再分散和令人满意的含量均匀性。
[0043]
化学稳定性
[0044]
他司美琼对氧化降解敏感,导致形成三种降解产物,因此在制剂中需要抗氧化剂。
[0045]
起初考虑了抗氧化剂如亚硫酸氢钠和亚硫酸钠,但可能在儿童中引起过敏反应。
[0046]
抗坏血酸优先经历氧化,从而防止他司美琼的氧化,但在储存时也赋予悬浮液黄色,尤其是当在40℃/75%rh下储存》3个月时,这是在室温下储存的产品的加速储存条件(在40℃/75%rh下需要6个月的令人满意的稳定性,以证明在室温/25℃/60%rh下长期储存是合理的)。由于在40℃/75%rh条件下储存3个月后,颜色由白色/灰白色变为黄色,因此必须将悬浮液储存在5℃条件下,加速储存条件为25℃/60%rh,在此储存条件下可获得长达6个月的令人满意的稳定性数据(即,颜色变化由白色/灰白色变为微黄色)。
[0047]
溶解
[0048]
原型悬浮液制剂的初始溶解速率是快速的(即,类似于胶囊制剂),但对于稳定性样品,在储存时溶解变得更慢。
[0049]
聚山梨醇酯80被评价为表面活性剂/溶解增强剂,并且发现改善了初始溶解曲线,但是在储存时,含有聚山梨醇酯80的几种原型制剂表现出较慢的溶解。
[0050]
仅一种原型制剂(含有他司美琼4mg/ml;蔗糖200mg/ml;甘露醇100mg/ml;rc-591 20mg/ml;樱桃香料5mg/ml;抗坏血酸3mg/ml;苯甲酸钠3mg/ml;三氯蔗糖1mg/ml;和纯净水余量(qs)至1ml)在悬浮液外观、他司美琼检验、溶解、杂质/降解产物和再分散性方面提供了令人满意的结果。基于令人满意的稳定性结果,选择该制剂用于临床研究。
[0051]
不透明度
[0052]
由于他司美琼在悬浮液中的浓度仅为4mg/ml,悬浮液的外观是相当半透明的,并且不完全是悬浮液样的,因此使用100mg/ml的甘露醇作为不透明度赋予剂。
[0053]
尽管甘露醇在水中的溶解度为约200mg/ml,但由于存在溶解或水合的蔗糖、抗坏血酸、苯甲酸钠和rc591,因而制剂中的溶解度可能低得多。这限制了甘露醇在制剂
中的溶解度,其保持为未溶解的颗粒并赋予悬浮液不透明度。可能少量的甘露醇溶解在悬浮液制剂中,从而增加总甜度。
[0054]
制造过程
[0055]
由于制剂含有溶解或分散于纯净水批量中的几种成分,所以制备制剂成分的单独部分(即,将蔗糖溶解于热水中(部分1);将他司美琼、苯甲酸钠、抗坏血酸、三氯蔗糖、聚山梨醇酯80和甘露醇溶解/分散并均化(部分2);通过简单搅拌将rc-591分散于水中而不进行均化(部分3))。然后将这三部分混合以获得最终的均匀悬浮液。
[0056]
rc-591聚合物分散体通过在一部分批量水中简单搅拌聚合物而不进行均化来制备。当聚合物分散体均化时,其变得太粘,这不利地影响溶解速率。
[0057]
由于他司美琼熔点低(约70℃),故需要将悬浮液温度维持在50至55℃范围内,以防止药物融化。
[0058]
用于口服施用的他司美琼的液体药物制剂的制备可能需要不期望的大量溶剂,以确保活性成分保持均匀的溶解状态,特别是在制剂中的活性成分具有有限的水溶性的情况下。为了解决需要不可接受水平的溶剂的可能性,本发明提供了包含他司美琼的药物组合物,其被配制为水性液体悬浮液,所述悬浮液能够使得一个或多个单位剂量的他司美琼被限制在最佳体积(例如,0.35ml至10ml的液体悬浮液)。最特别地,本发明的一个实施方式使得单一单位剂量能够含有可有效治疗正在施用药物的个体的量的他司美琼。
[0059]
通过将他司美琼与悬浮剂混合在水中来制备这种悬浮液。制备的悬浮液可以是均质的,即他司美琼是均匀分散的,并且可以是高度稳定的。他司美琼的这些液体悬浮液采用细分并能够分散在悬浮液中的他司美琼。此外,悬浮的他司美琼在制剂的水性载体中基本上不溶解(例如,至少大于50%、或75%、或90%不溶解)。
[0060]
在示例性实施方式中,当摇动或搅拌药物组合物时,他司美琼均匀或几乎均匀地分散。药物组合物具有足够低的粘度,使得其可以通过匙、杯、注射器、吸管、药物滴管等口服施用,并且容易被个体吞咽,包括难以吞咽丸剂或胶囊的个体,例如一些儿童、老年或残疾患者。
[0061]
在示例性实施方式中,如上所述,本发明的液体悬浮液中他司美琼的浓度为1至6mg/ml。此类实施方式包括2至5mg/ml,或约4mg/ml(例如,3.5至4.5mg/ml),或约1mg/ml(例如,0.5至1.5mg/ml)的浓度。
[0062]
在示例性实施方式中,液体载体是包含悬浮剂和掩味剂的水溶液。悬浮剂是添加到悬浮液中以增加粘度和延迟沉降的物质。此种试剂的实例包括纤维素悬浮剂、粘土(包括例如膨润土和硅酸盐)、多糖胶(包括黄原胶、阿拉伯胶或阿拉伯树胶、和黄蓍胶)、其它多糖(包括琼脂和角叉菜胶)、合成聚合物(包括卡波姆、聚乙烯吡咯烷酮或pvp,以及pvp共聚物,例如pvp-乙酸乙烯酯或pvp-va)和明胶。当以1%至5%的浓度范围存在时,药物组合物中的悬浮剂通常是有效的。
[0063]
相对于其它类型的悬浮剂,纤维素悬浮剂可赋予药物组合物改善的特性。这些包括更好的稳定性、减少的沉降或更好的均匀性。纤维素悬浮剂的实例是甲基纤维素、羟丙基甲基纤维素(hpmc)、羧丙基甲基纤维素钠(cpmc)、羟乙基纤维素、羧甲基纤维素、羧甲基纤维素钠和粉状纤维素。使用甲基纤维素a15c羟丙基甲基纤维素以及rc-591微晶纤维
素 羧甲基纤维素钠可以获得具有特别有利性质的药物组合物。
[0064]
在一个示例性实施方式中,悬浮剂包含含有微晶纤维素(mcc)和羧甲基纤维素钠(cmc)的微晶体的致密粉末颗粒,例如作为rc-591mcc cmc钠(fmc corporation,philadelphia,pa)销售的产品,其包含粒径d
60
《0.2μm的微晶体颗粒,其中颗粒足够致密,使得直径为30μm的颗粒含有约6亿个直径为约0.1μm的mcc cmc微晶体。其它mcc cmc悬浮剂包括以mcg mcc cmc钠(jrs pharma,rosenberg,德国)销售的产品。
[0065]
掩味剂包括甜味剂,例如糖;多元醇,例如甘露醇和山梨醇;以及合成甜味剂,例如糖精和阿斯巴甜。还可以加入增味剂或增香剂(例如樱桃增味剂)以掩盖他司美琼的味道,并使悬浮液更可口,特别是对儿童而言。
[0066]
水溶液中的其它赋形剂可以包括不透明度赋予剂、着色剂、表面活性剂(特别是用作润湿剂的非离子表面活性剂)、甜味剂、抗氧化剂和防腐剂。这些和其它类型的试剂,例如增味剂和着色剂,任选地有助于药物组合物中的他司美琼的稳定性和均匀性,更通常地有助于悬浮液的稳定性和均匀性,并且任选地有助于悬浮液的味道和外观的可接受性。
[0067]
高强度甜味剂是比蔗糖甜数倍的化合物,包括例如甜叶菊、阿斯巴甜、三氯蔗糖、纽甜、乙酰磺胺酸钾(ace-k)、糖精和爱德万甜。
[0068]
不透明度赋予剂,也称为乳浊剂或不透明剂,包括药学上可接受的不溶性(或难溶性)颗粒状固体,其降低半透明性并由此提供悬浮状外观。
[0069]
任选地,制剂中包括试剂以调节其ph,例如酸、碱或缓冲剂,其包括氢氧化钠、磷酸或柠檬酸。
[0070]
虽然不同类别的试剂通过它们在制剂中发挥的功能而在上文中确定,但各种赋形剂可在药物组合物中发挥多于一种功能。此外,本文公开的药物组合物不必限于说明书中公开的具体粒径。
[0071]
例如,使用已知的制备用于制备固体口服剂型(例如胶囊)的他司美琼活性成分的相同化学和制造方法来制备用作药物组合物中的活性成分的他司美琼。参见例如美国公开申请us 20090105333和pct公开申请wo2015/123389。可接受的粒径包括如这些出版物中所述的那些,例如d
50
小于100μm,例如d
50
为20μm至40μm或30μm至50μm。他司美琼活性成分的其它示例性粒径规格尤其包括:
[0072]d10
≤30μm
[0073]d50
≤100μm
[0074]d90
≤200μm
[0075]
或
[0076]d10
≤15μm
[0077]d50
≤45μm
[0078]d90
≤105μm。
[0079]
上述粒径测量可以例如使用激光衍射进行,例如使用malvern mastercizer的激光散射检测。
[0080]
在使用这种装置的示例性粒径分析中,通过将10mg聚山梨醇酯80和1g他司美琼在1l蒸馏水中混合来制备分散体,然后用0.2μm过滤器过滤。用分散剂填充取样器附件(hydro2000s(a)模块)以获得背景测量。然后,将分散在约15ml分散剂中的约80至90mg样品
缓慢添加到取样器附件中,直到获得约15%(例如,10%至20%)的遮蔽。在开始测量之前,样品以约2000rpm再循环约5秒。
[0081]
进行两次样品检测并计算平均结果以获得d
90
、d
50
和/或d
10
值。
[0082]
为了制备本文所公开的悬浮液,除了他司美琼和其它水溶性差的成分(例如抗坏血酸或苯甲酸钠)之外的所有制剂成分可以溶解于纯净水中,任选地预先用氮气鼓泡30分钟。他司美琼和其它水溶性差的成分(如甘露醇)可以例如通过40目筛筛分以制备一个或多个分散相,然后分散在其它制剂成分的溶液中。优选将包含他司美琼的分散相保持在远低于他司美琼熔点(约71℃),例如《35℃。最终的水性悬浮液可以填充到例如50ml或100ml褐色聚对苯二甲酸乙二醇酯(pet)瓶中,并且任选地在封闭瓶之前用氮气吹扫。
[0083]
相比于使用交聚维酮 聚维酮(交聚维酮xl-10 聚维酮k30)、增稠剂/甜味剂、高强度甜味剂、增味剂、抗氧化剂和防腐剂的制剂,如下所述的包含纤维素悬浮剂(甲基纤维素a15c)、不透明度赋予剂、增稠剂/甜味剂、高强度甜味剂、增味剂、抗氧化剂和防腐剂的他司美琼的水性悬浮液可具有改善的粘度和沉降特性。可以例如使用布氏粘度计dv-iii ultra在制备每种水性悬浮液后2小时和24小时进行粘度测量。包含pvp和pvp/va作为悬浮剂的示例性药物组合物示于表1中。
[0084]
表1.水性悬浮液——pvp悬浮剂
[0085]
成分功能用量(mg/ml)他司美琼活性成分4.0抗坏血酸抗氧化剂3.0山梨醇溶液70/02 b增稠剂/甜味剂400.0交聚维酮xl-10悬浮剂6.0聚维酮k30悬浮剂30.0苯甲酸钠防腐剂3.0三氯蔗糖甜味剂2.0香精增味剂5.0纯净水溶剂余量
[0086]
表1的组合物显示出可接受的稳定性。包含纤维素悬浮剂的组合物具有改善的性质,例如增加的粘度和减少的沉降。示例性组成示于表2中。
[0087][0088]
包含蔗糖代替山梨糖醇且包含氯化钠的组合物可具有改善的味道和较少的苦味(或灼烧感)。
[0089]
10至30mg/ml、特别是20mg/ml的微晶纤维素 羧甲基纤维素(cmc)钠悬浮剂可提供改善的稳定性和物理外观(均匀性)。
[0090]
甘露醇可用作不透明度赋予剂,例如当以100至300mg/ml使用时。100至200mg/ml、特别是100mg/ml提供了增强的溶解和粘度,特别是当与从300mg/ml降低至200mg/ml的蔗糖组合时。
[0091]
他司美琼的溶解根据美国药典(usp《711》)确定,例如,
[0092]
设备:设备2(搅拌)
[0093]
容器尺寸/类型:1000ml,透明玻璃,圆底
[0094]
转速:50rpm
[0095]
测试温度:37
±
0.5℃
[0096]
溶解介质:0.1n hcl
[0097]
抽吸体积:5ml
[0098]
替换:否
[0099]
沉降片:否
[0100]
套管:不锈钢
[0101]
过滤器:whatman gf/f0.7μm孔径,注射器过滤器
[0102]
弃去体积:2ml
[0103]
在10至15分钟时的溶解通常为至少50%,例如至少70%,例如至少90%。
[0104]
短期稳定性研究可在(1)5
±
3℃、(2)25
±
2℃(60
±
5%相对湿度)和40
±
2℃(75
±
5%相对湿度)的储存条件下进行1至3个月。在这些条件下,通过hplc测定的药学上可接受的组合物的总杂质,例如相对于已知杂质不超过2.0重量%或不超过0.5重量%,并且相对于未指明的杂质不超过0.2重量%。
[0105]
可以例如使用布氏粘度计dv-iii ultra在制备每种水性悬浮液后2小时和24小时进行粘度测量。粘度值在环境条件(即,约18℃至约24℃,如约20℃,和约1个大气压)下通常高达约150cps,但某些实施方式的粘度水平为5至100cps,例如5至50cps或5至20cps。
[0106]
悬浮液的比重(相对密度)在环境条件下通常大于1mg/ml且至多约1.5mg/ml,例如1.1至1.3mg/ml。
[0107]
令人满意的ph通常为ph 3~7,例如ph 4~5或ph 4.0~4.5。
[0108]
关于粒径,使用包括以下的粒径可获得改善的结果:d90≤150μm,例如100至150μm;d50≤80μm,例如50至70μm;d10≤50μm,例如15至40μm。
[0109]
因此,在一个实施方式中,本发明的制剂至少满足以下关于商业销售的发行规范:
[0110]
稳定性:在(1)5
±
3℃、(2)25
±
2℃(在60
±
5%相对湿度下)和(3)40
±
2℃(在75
±
5%相对湿度下)下储存1、2或3个月后,总杂质(hplc)相对于已知杂质不超过1.5重量%,不超过0.5重量%,并且相对于未指定杂质不超过0.2重量%;
[0111]
粘度:5至30cps,例如20cps(环境条件);
[0112]
比重:1.1至1.3mg/ml;
[0113]
ph:4.0至5.0;
[0114]
粒径:d
90
=100至150μm,d
50
=50至70μm,并且d
10
=15至40μm。
[0115]
溶解:在1n hcl中以50rpm搅拌15分钟后的≥90%。
[0116]
如上所述,可选择的悬浮剂包括多糖胶。例如,用黄原胶获得了合意的结果,例如1至25mg/ml,优选1至5mg/ml。表3中提供了包含多糖胶作为悬浮剂和二氧化钛作为不透明度赋予剂的示例性组合物。
[0117]
表3.多糖胶悬浮剂
[0118][0119]
配量和施用
[0120]
史密斯-马吉利综合征(sms)是一种罕见的临床上可识别的综合征,其特征在于轻度颅面和骨骼异常的独特模式,表达性言语/语言延迟,精神运动和生长迟缓,以及显著的神经行为表型(刻板症、自伤和攻击行为)。sms及其使用他司美琼的治疗描述于例如pct公开wo 2016/036619中,其通过引用并入本文。
[0121]
sms的一个常见症状是长期中断的睡眠模式,其在所有年龄发现。在确定他司美琼在治疗病症(包括sms)中的功效的研究中,口服(20mg胶囊或4mg/ml悬浮液)和静脉内(0.4mg/ml)制剂在就寝前每天一次施用给3至17岁的儿科患者。
[0122]
通过夜间睡眠的改善(即,中断睡眠期的夜间活动减少,睡眠效率改善,睡眠开始的可变性减少,早晨觉醒的可变性减少和/或睡眠质量改善),白天嗜睡减少,行为问题减少(即,攻击行为减少,暴怒发作减少,过度活跃减少和/或注意力缺陷减少)来评估治疗功效。
[0123]
令人惊奇的是,发现对于体重为28kg以下的那些患者,他司美琼的持续有效剂量与体重成比例(0.7mg/kg),但是对于体重大于28kg的那些患者,他司美琼的持续有效剂量为20mg。也就是说,体重大于28kg的儿童的表观清除率是恒定的,并且与成人的表观清除率相似。该结果是预料不到的,不过是一致的且独立于其它变量,包括患者年龄和性别。
[0124]
图1显示他司美琼的有效剂量(测量为表观清除率,其倒数为全身性暴露)随患者体重变化的曲线。可以看出,有效剂量与体重(0.7mg/kg)成比例,直到体重为28kg,此后,相应的有效剂量是恒定的20mg。
[0125]
这样的配量适用于本文所述的含有他司美琼的任何液体制剂或适用于根据这样的配量方案施用的任何其他制剂。例如,此类液体制剂可用于向体重为28kg以下的患者施用0.7mg/kg的日剂量,以及向体重大于28kg的患者施用20mg的日剂量。作为另选,本发明的液体制剂可用于向体重为28kg以下的患者施用0.7mg/kg的日剂量,并且,另一种他司美琼制剂如胶囊剂、片剂或静脉内制剂用于向体重大于28kg的患者施用20mg的日剂量。
[0126]
图2显示了适于根据本发明实施方式施用他司美琼液体制剂的方法的各个步骤的一系列图示。在图块a中,在使用前将含有他司美琼的液体制剂(例如上述那些制剂)的瓶子充分摇动至少15秒(例如至少约30秒)。已显示,该步骤在以下方面是重要的:确保制剂的组分(包括他司美琼)充分混合以实现上述益处,并允许实现他司美琼的一致性和精确的配量。
[0127]
分别在图块b和c中,将瓶子摇动后开盖,并将瓶适配器插入瓶子的颈部。如本领域技术人员将认识到的,使用瓶适配器既不是关键的也不是必需的,但通常有助于在施用所有类型的液体制剂(包括本发明的实施方式的他司美琼的液体制剂)中使用以下描述的注射器。
[0128]
分别在图块d和e中,将注射器插入瓶适配器的开口中,并且将瓶和插入的注射器倒置,以便允许将规定量的液体制剂吸入注射器中。然后所吸取的剂量可以直接从注射器或其它方式口服施用给患者(未示出)。在图块f中,将瓶盖放回瓶子上直到再次使用。
[0129]
在下面的权利要求书中描述了本发明的其它示例性实施方式。与上述制剂和方法类似,这些是说明性的而不是对本发明的限制,本发明包括这些示例性实施方式的修改和变化。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。