类鼻疽伯克霍尔德菌噬菌体vb_bpp_hn01及应用
技术领域
1.本技术涉及新型噬菌体技术领域,尤其涉及类鼻疽伯克霍尔德菌噬菌体 vb_bpp_hn01及应用。
背景技术:
2.类鼻疽伯克霍尔德菌(burkholderia pseudomallei,以下简称bp),为一革兰氏阴性的条件致病菌,可兼性寄生于人体细胞内。目前该疾病治疗最主要的问题是bp 的复杂固有耐药性,前期的临床数据显示其可耐受青霉素、第一/二代头孢菌素、大环内酯类、多粘菌素和氨基糖苷类抗生素的作用。具体耐药机制除可分泌脂多糖形成生物被膜来屏蔽药物的作用外,bp还可编码β内酰胺酶,从而解除头孢菌素类、苯唑西林类等β内酰胺类抗生素的作用,此外菌体内部还具有由转运蛋白、融合蛋白和孔道蛋白所构成的外排泵系统进一步降低抗生素的效果。在单一抗生素的长时间作用坐下,菌株的异质性耐药较为难为避免,还可能因为点突变的积累导致获得性耐药的产生,有研究发现,上述编码内源β内酰胺酶出现单个碱基的突变即可菌株对头孢他啶的耐药性上升85倍。
3.目前针对bp的具有临床应用潜力的噬菌体仅有三株:噬菌体st79(umapornyordpratum,unchalee tattawasart,surasakdi wongratanacheewin,rasana w.sermswan, novel lytic bacteriophages from soil that lyse burkholderia pseudomallei,femsmicrobiology letters,volume 314,issue 1,january 2011,pages 81
–
88)和e094 (muangsombut v,withatanung p,chantratita n,chareonsudjai s,lim j,galyov ee, ottiwet o,sengyee s,janesomboon s,loessner mj,dunne m,korbsrisate s.rapidclinical screening of burkholderia pseudomallei colonies by a bacteriophage tailfiber-based latex agglutination assay.appl environ microbiol.2021may 26;87(12):e0301920.doi:10.1128/aem.03019-20.epub 2021may 26.pmid:33811022; pmcid:pmc8174754),分离自泰国,前者可裂解71%所测试的bp临床株,后者的基因元件被用于开发bp的血清学诊断方法;噬菌体c34(guang-han o,leang-chungc,vellasamy km,mariappan v,li-yen c,vadivelu j.experimental phage therapy forburkholderia pseudomallei infection.plos one.2016jul 7;11(7):e0158213),分离自马来西亚,虽然拥有更窄的裂解谱,但动物实验显示在噬菌体的干预下,有超过1/4的小鼠在感染bp后未出现死亡。
技术实现要素:
4.为探索新型的类鼻疽诊疗方法,本技术发明人先后于2019年完成了海南本土参考株系bp hnbp001的测序工作(genbank编号cp038805,cp038806),以其为宿主,于2021年从海南省东方市采集的100份环境样品(包括稻田土壤、灌溉水源、污水)中,分离获得了一系列可侵染bp的噬菌体,依据噬菌斑形态、能否稳定维持裂解状态以及对临床菌株的感染情况,筛选得到了中国第一株具有广谱bp裂解能力的短尾噬菌体vb_bpp_hn01,并对其形态特
征、裂解特性和感染特点进行了研究,同时对该噬菌体的全基因组进行了测序和必要的生物信息学分析,此外使细胞模型确认了其的体外抗bp能力以及未来与抗生素治疗类鼻疽的可能,具有十分广泛的应用前景。
5.第一方面,本技术实施例公开了一种纯化的噬菌体,其具有包含seqidno.1的核苷酸序列的双链dna的基因组,并具有针对类鼻疽伯克霍尔德菌的拮抗活性。
6.第二方面,本技术实施例公开了一种纯化的噬菌体(burkholderiapseudomalleiphage)vb_bpp_hn01,该噬菌体于2022年4月15日保藏在中国典型培养物保藏中心,保藏地址为中国武汉武汉大学,保藏编号为cctccno:m2022422;该噬菌体可用于拮抗类鼻疽伯克霍尔德菌菌株的生长,可用于类鼻疽疾病、肺部感染和/或菌血症的预防和治疗。
7.第三方面,本技术实施例公开了一种预防和/或治疗感染性疾病的组合物,所述感染性疾病由一种或更多种选自类鼻疽伯克霍尔德菌引起,所述组合物以权利要求1或2所述的噬菌体作为活性成分。
8.第四方面,本技术实施例公开了一种抗生素,以第一或二方面所述的噬菌体作为活性成分。
9.第五方面,本技术实施例公开了一种消毒剂或清洁剂,以第一伙二方面所述的噬菌体作为活性成分。
10.第六方面,本技术实施例公开了第一或二方面所述的噬菌体在制备药物中的用途,所述药物用于诊断细菌感染的成因剂的方法,其包括:
11.(i)培养来自患者的组织样品;
12.(ii)使步骤(i)的培养物与包含第一或二方面的噬菌体的药物接触;
13.(iii)监控所述培养物生长和/或裂解的证据;
14.其中所述培养物裂解的证据指示所述培养物包含类鼻疽伯克霍尔德菌。
15.第七方面,本技术实施例公开了第一或二方面的噬菌体在制备药物中的用途,所述药物用于减少或抑制类鼻疽伯克霍尔德菌在与之接触的生物学表面上的定殖或生长,所述生物学表面是哺乳动物的皮肤、受损皮肤或粘膜。
16.第八方面,本技术实施例公开了有效量的第三方面的药物组合物在制备药物中的用途,所述药物用于通过施用所述药物治疗或减少有此需要的受试者中的细菌感染的发生,所述细菌感染是通过类鼻疽伯克霍尔德菌的感染。
17.第九方面,本技术实施例公开了一种用于减少或抑制类鼻疽伯克霍尔德菌在固体表面上的定殖或生长的非治疗性方法,其包括使所述表面与第一或二方面的噬菌体接触。
附图说明
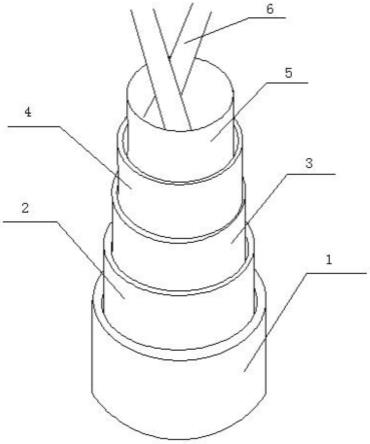
18.图1为本技术实施例提供的噬菌体侵染bphnbp01的噬菌斑情
19.图2为本技术实施例提供的噬菌体对bphnbp01的吸附效率(a)以及该噬菌体在不同感染复数条件下的最终滴度产生情况(b)。
20.图3为本技术实施例提供的噬菌体的一步生长曲线(a)以及相同条件下噬菌体对宿主菌的裂解情况(b)。
21.图4为本技术实施例提供的vb_bpp_hn01噬菌体的基因组构成,重复序列和trna已进行标记。
22.图5为本技术实施例提供的vb_bpp_hn01与已测序bp噬菌体的基因组范围内比对结果;图5a表示与短尾噬菌体、长尾噬菌体以及肌尾噬菌体的同源性比较结果;图5b为viptree结果;图5c为基于门户蛋白的同源性比对结果;图5d为基于末端酶的氨基酸序列的同源性结果。
23.图6为本技术实施例体的细胞保护试验结果图。
具体实施方式
24.为了使本技术的目的、技术方案及优点更加清楚明白,以下结合实施例对本技术进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本技术,并不用于限定本技术。本技术中未详细单独说明的试剂均为常规试剂,均可从商业途径获得;未详细特别说明的方法均为常规实验方法,可从现有技术中获知。
25.第一方面,本技术实施例涉及纯化的噬菌体,其具有针对医院病原体类鼻疽伯克霍尔德菌的一个或多个菌株的抗菌活性。其具有包含seq id no.1的核苷酸序列的双链dna。
26.第二方面,本发申请提供了具有包含seq id no.1的核酸序列或由seq id no.1 的核酸序列的双链dna组成的基因组的细菌噬菌体。依照这个实施方案的特定例子是分离的短尾噬菌体(学名burkholderia pseudomallei phage)vb_bpp_hn01,其靶向类鼻疽伯克霍尔德菌。图4示出了包含seq id no.1的核酸序列的vb_bpp_hn01 基因组的图示结构,图4中还示出了vb_bpp_hn01基因组中的开放读码框(orf)以及其在基因组内的位置,由orf编码的氨基酸序列,同源或相似蛋白质和在编码多肽内的保守结构域,和假定功能蛋白的指定。
27.本技术提供的噬菌体属于短尾噬菌体科(podoviridae)的形态型组,其头部呈对称结构,直径约62nm,尾部长约20nm(如图1c)。如图1a所示,噬菌体在侵染 bp hnbp001后,可在双层平板上形成直径为1-2mm左右的透明噬菌斑,如将培养时间进一步延长,可在噬菌斑的外围观察到荚膜水解环的存在,提示其基因组上具有荚膜多糖水解酶的元件存在(图1b)。
28.本技术发明人收集了海南省东方市这一省内的类鼻疽高发地区用于样品的采集,共获得稻田土壤、果园土壤、鸡鸭粪、灌溉水、污水等共100份样本,并且分离了具有对25株类鼻疽伯克霍尔德菌的特异性杀菌活性和上述特征的本技术的噬菌体,其被命名为类鼻祖伯克霍尔德菌噬菌体(burkholderia pseudomallei phage) vb_bpp_hn01,并于2022年4月15日,保藏在中国典型培养物保藏中心,保藏地址为中国武汉武汉大学,保藏编号为cctcc no:m2022422。与保藏证明的信息一致。
29.另一个方面,本技术涉及预防或治疗感染性疾病的组合物,所述感染性疾病由一种或更多种选自类鼻疽伯克霍尔德菌引起,所述组合物以上述第一或二方面的噬菌体作为活性成分。
30.在一些实施例中,类鼻疽伯克霍尔德菌的具体菌株如表1所示。
31.如本文所用,术语―预防”含义是通过施用所述组合物来遏制或延缓疾病进展的所有行为。如本文所用,术语―治疗”含义是通过施用所述组合物患者的状况已经好转或向有利转变的所有行为。
32.本技术的组合物包括不低于109pfu/ml的vb_bpp_hn01。
33.本技术组合物可以应用的优选的感染性疾病实例包括类鼻疽伯克霍尔德菌引起的畏寒、高热起病、肺部感染、菌血症、败血症等症状的类鼻疽病,但不限于这些。
34.本技术的组合物可以另外包括药学上可接受的载体,并且与所述载体一起配制,以提供抗生素、药物、杀菌剂、防腐剂、消毒剂和细菌感染诊断制剂。请发明人确认,做适当地延展。
35.如本文所用,术语―药学上可接受的载体”指对有机体不引起明显刺激和不消除被施用化合物生物活性和性质的载体或稀释剂。对于将组合物配制成液体制剂,可以使用无菌且生物相容的药学上可接受的载体,如盐水、无菌水、林格氏溶液、缓冲生理盐水、白蛋白注射溶液、葡萄糖溶液、麦芽糊精溶液、甘油和乙醇。这些物质可以单独使用或以其任何组合使用。如果需要,可以添加其它传统的添加剂,如抗氧化剂、缓冲剂、抑菌剂等。进一步,可以另外将稀释剂、分散剂、表面活性剂、粘结剂和润滑剂添加到组合物,以制备可注射制剂如水溶液、悬浮液和乳状液,或口服制剂如丸剂、胶囊、颗粒剂或片剂。
36.本技术的预防或治疗组合物可以被施用或喷雾到患病区域(afflicted area),或通过口服或肠胃外途径给药。肠胃外给药可以包括静脉内给药、腹膜内给药、肌肉内给药、皮下给药或局部给药。
37.适于施用、喷雾或给药本技术组合物的剂量取决于多种因素,包括配制方法、给药方式、被治疗患者或动物的年龄、体重、性别、状况和饮食、给药时间、给药途径、排泄速度和反应敏感性。具有本领域普通技术的医师或兽医可以容易地确定并开出所需组合物的有效量。
38.适于本技术组合物的口服制剂的实例包括片剂、含片、锭剂、水性或乳状悬浮液、粉末或颗粒、乳状液、硬或软胶囊、糖浆或酏剂。对于诸如片剂和胶囊的制剂,有用的是粘结剂如乳糖、蔗糖、山梨醇、甘露醇、淀粉、支链淀粉、纤维素或凝胶,赋形剂如磷酸二钙,崩解剂如玉米淀粉或甘薯淀粉,润滑剂如硬脂酸镁、硬脂酸钙、硬脂富马酸钠或聚乙二醇蜡。对于胶囊,除上述化合物之外,可以进一步使用诸如脂质的液体载体。
39.对于非口服给药,本技术组合物可以配制成皮下、静脉内或肌肉内途径的注射剂、栓剂或经由呼吸道可吸入的喷雾剂,如气雾剂。注射制剂可以通过这样获得:将本技术组合物与稳定剂或缓冲剂一起溶解或悬浮在水中以及将溶液或悬浮液包装在安瓿或小瓶单元中。对于喷雾剂,如气雾剂,用于喷射水分散的浓缩物或湿粉末的推进剂可以结合添加剂使用。
40.另一方面,本技术实施例公开了包括上述噬菌体作为活性成分的抗生素。
41.如本文所用,术语―抗生素”含义是施用于动物以杀死病原体的任何药物,并且在本文其被用作防腐剂、杀菌剂和抗菌剂的一般术语。所述动物是包括人在内的哺乳动物。与传统的抗生素不同,本技术的噬菌体对类鼻疽伯克霍尔德菌具有高度特异性,以便杀死特异性病原体而不影响有益菌,并且不诱导抗性,使得其使用周期(lifecycling) 比较长。
42.在另一方面中,本技术提供以第一或二方面的噬菌体作为活性成分的消毒剂或清洁剂。为了去除bp,包括噬菌体作为活性成分的消毒剂还可喷雾和应用到家畜活动的任何区域、屠宰场、家畜死亡地点、烹饪空间和烹饪设施,但是不限于此。另外,包括噬菌体作为活性成分的清洁剂可用在已经或潜在受bp污染的活的动物的皮肤和身体区域上。
43.在下文中,本技术将参考实施例更详细地描述。然而,这些实施例仅用于说明的目的,本技术不意欲受这些实施例的限制。
44.噬菌体的分离和纯化
45.选择了海南省东方市这一省内的类鼻疽高发地区用于样品的采集,共获得稻田土壤、果园土壤、鸡鸭粪、灌溉水、污水等共100份样本。其中对于固体样品,称取约 5g,放入无菌的50ml离心管中,加入3倍体积的sm缓冲液,充分震荡制备为悬浊液,然后4℃静置过夜,保证噬菌体的充分释放。然后3500g离心20min,对上清进行收集。对于液体样品,吸取20ml至50ml,加入20μl 5m cacl2混匀后,3500 g离心20min收集上清。之后使用0.45μm滤膜对其中的较大的颗粒和部分菌体进行清楚,滤液转移至新的无菌15ml离心管中,4℃保存待用。
46.在进行噬菌体的分离之前对bp hnbp001(类鼻疽伯克霍尔德菌hnbp001,海南医学院p2实验室)进行复苏:挑取单克隆,接种于5ml lb液体培养基中,37℃, 220rpm,培养过夜。第二天,按1%传代摇至对数期。之后依照双层平板法对噬菌体进行分离:吸取含噬菌体的上清10ml,加入5ml 3
×
lb液体培养基以及200μl bp hnbp001,37℃,220rpm,培养过夜。对上述培养物进行4000rpm离心10min,对上清进行收集,使用0.22μm滤膜除菌后,取200μl与400μl对数期的bphnbp001混合,室温放置10min,加入6ml半固体琼脂培养基(55℃,保证培养基仍呈流动状态),倾倒于2%的琼脂平板上,待上层培养基凝固后,37℃倒置培养过夜,次日对是否产生噬菌斑、噬菌斑的大小和透明度进行观察。
47.对其中的单个噬菌斑进行挑取,将其放入含500μl sm buffer的1.5ml无菌 eppendorf管中。置于水平摇床之上4℃浸泡过夜,再次使用0.22μm滤膜除菌过滤,取100μl与100μl对数期bp hnbp001混合,室温放置10min加入6ml55℃的半固体培养基,混匀后浇注2%的琼脂平板。待凝固后,37℃倒置培养过夜。再次观察噬菌斑的形成情况,对此步骤进行5次重复后,对可产生大小均一、透明度相同的噬菌体进行保存:于噬菌斑平板上加入5ml sm buffer,4℃静置过夜,对浸泡液进行收集,并使用1ml sm buffer冲洗平板。对两者进行合并,收集于15ml离心管中,再次使用0.22μm滤膜对菌体进行去除,作为噬菌体溶液4℃待用。对于需长期保存的噬菌体,将其置于30%的甘油中,-80℃超低温冰箱冻存。
48.为获得足够多的噬菌体进行后续的实验,首先准备足量的宿主菌:挑取新鲜平板上的bp hnbp001单克隆于5ml lb中摇菌过夜,第二天按1%比例接种于200mllb液体培养基中,待菌体的od600达到0.5左右,加入4ml上一步获得的噬菌体溶液,同时加入cacl2(5mmol/l)及mgcl2(5mmol/l)。37℃,220rpm培养至液体完全澄清透亮。为了对其中的噬菌体进行收集,先加入固体nacl使其终浓度达到0.5mol/l,完全溶解后,于4℃冰箱静置2小时。之后进行4500rpm离心20min,对上清进行收集,加入peg 8000,使其终浓度达到10%(w/v),待混匀后,进行4℃过夜。然后4℃,6500rpm离心20min,小心弃去上清,对沉淀使用适量tm缓冲液进行重悬,并使用0.22μm滤膜过滤。
49.为获取其具体的滴度,取100μl上述浓缩后的样品,进行1/10的等比例稀释至 10-9
,然后取出10μl稀释后的样品与100μl对数期hnbp001混合,同样依照双层平板法,当产生的噬菌斑彼此之间并无重叠的情况,对其个数进行计算(n),依照下列公示进行滴度计算,滴度(pfu/ml)=n
×
稀释倍数
×
100。
50.噬菌体宿主谱的测定
51.挑取新鲜平板上的待测菌单克隆至5ml lb液体培养基,37℃,220rpm,培养过夜,
第2天按1%比例传代培养至对数期;然后取100μl待测菌至6ml半固体琼脂培养基(55℃)中,混匀后倾倒2%的固体培养基,取2μl 1
×
108滴度的噬菌体滴加于双层平板上,待干燥后倒置37℃培养过夜,第2天依照噬菌斑的产生情况,判断所选宿主菌的敏感性。结果如表1所示。表1中,― ”表示某株细菌被该噬菌体侵染后产生噬菌斑,即细菌细胞被裂解;对不能产生噬菌斑的某株细菌,其敏感性标记为
“‑”
。
52.表1本噬菌体的宿主谱范围
[0053][0054][0055]
a:本次使用的2株洋葱伯克霍尔德菌以及临床常见的革兰氏阳性/阴性菌标准菌
株由海南医学院第二附属医院检验科馈赠
[0056]
由表1可知,除筛选宿主bp hnbp001外,还可裂解所筛选的24株bp临床株中的,仅有一株来源于海口的菌株(bpn012)可以逃逸该噬菌体的作用。同时对于洋葱伯克霍尔德菌、临床常见的其他革兰氏阳性菌/阴性菌的标准菌株,该噬菌体无法完成感染或感染后会转化为溶原状态。
[0057]
电镜观察噬菌体形态特征
[0058]
在噬菌体滴度达到10
11
pfu/ml的前提下,在已浓缩的样本中,加入适量dnasei和rnase a,37℃孵育30min。然后使用100kda超滤膜(amicon)对残留的内毒素以及其他非噬菌体物质进行去除,吸取10μl过滤液滴加于碳支持膜铜网(400 目),经10min吸附后,使用滤纸吸走剩余样品,并利用10μl磷钨酸(2%,w/v) 进行5min的负染。同样使用滤纸吸走多余染料。制备的样品置于室温条件下5小时使其完全干燥,然后依照标准程序进行透射电镜的观察。
[0059]
结果如图1所示,噬菌体在侵染bp hnbp001后,可在双层平板上形成直径为 1-2mm左右的透明噬菌斑(图1a),如将培养时间进一步延长,可在噬菌斑的外围观察到荚膜水解环的存在,提示其基因组上具有编码该酶的元件存在(图1b);利用透射电子显微镜对其微观结构进行观察,确认其为典型的短尾噬噬菌体,头部呈对称结构,直径约62nm,尾部长约20nm(图1c)。为此,筛选和分离得到的噬菌体命名为vb_bpp_hn01,其靶向类鼻疽伯克霍尔德菌。
[0060]
噬菌体吸附试验
[0061]
将bp hnbp001培养至对数期,加入感染复数为0.1的噬菌体vb_bpp_hn01,分别在0min、5min、10min、15min、20min、30min、40min取2
×
100μl样品,一份经12000g、4℃离心5min后,收集上清,依照双层平板法测定滴度ta,另一份未经处理的样品同样依照双层平板法测定滴度tb,依照下述公式对其吸附率进行计算,每个时间点取样三次计算吸附率平均值,整个实验进行三次独立重复。
[0062][0063]
如图2a所示,对样品的稀释,进行感染复数0.001至10的噬菌体侵染实验,进行最终滴度大小的比较,发现当感染复数为0.1时,噬菌体可产生最高的滴度,约10
12 pfu/ml。如图2b所示,同时在此条件下,对其的吸附率进行检测,结果如图2b所示,在共孵育5min后,约有40%的噬菌体完成了吸附,并在第30min,超过95%的噬菌体都完成了吸附。
[0064]
噬菌体一步生长曲线及对宿主菌的侵染速率测定
[0065]
(1)将bp hnbp001培养至对数期,在10ml菌液中加入感染复数为0.1的噬菌体vb_bpp_hn01,37℃孵育10min保证噬菌体对宿主的吸附。12000g离心10 min,弃去游离于上清中的噬菌体,使用10ml lb重悬菌体,置于37℃、220rpm条件下培养。分别于0min、5~40min(取样间隔5min)、50min、60min、80min、 100min、120min取100μl重悬液,依照2.2.2中所描述的方法进行滴度计算,每个时间点取样3份,计算平均值,整个实验重复三次,使用origin(version 7)绘制一步生长曲线。
[0066]
(2)将bp hnbp001培养至od600=0.3,加入感染复数0、0.1的噬菌体,37℃ 220rpm培养。每30min测定其600nm处吸光值的变化,其中使用lb培养基作为空白对照,每个时间点
取样三次,计算od600平均值,此实验独立重复三次。
[0067]
如图3a所示,vb_bpp_hn01对bp hnbp001感染于前20min的潜伏,然后滴度呈爆发式增长持续至40min。如图3b所示,在无噬菌体的作用下(moi=0),bphnbp001菌株的培养液在150min时od600最大达到0.8;而当以moi=0.1接种 vb_bpp_hn01时,bp hnbp001菌体在30min时生长曲线显著下降,直至150min 时,超过95%的菌体被裂解。
[0068]
vb_bpp_hn01噬菌体全基因组测序与生物信息学分析
[0069]
(1)基因组核酸提取
[0070]
通过扩大培养,制备10ml滴度为10
12
pfu/ml或以上的噬菌体溶液,依照试剂盒(zp317,庄盟)对其基因组进行提取:在溶液中加入20μl rnase a(20mg/ml) 及6μl dnase i,对游离的核酸进行消化(37℃孵育30min)。加入5ml噬菌体沉淀液(已提前预冷),混匀后置冰上20min。之后12000rpm、4℃条件下离心15min,对沉淀进行收集,室温干燥2min。使用400μl噬菌体裂解缓冲液,轻柔吹打沉淀物,使其重悬,加入50μl sds对噬菌体外部膜蛋白结构进行破坏。依次加入10μl蛋白酶k,56℃处理60min,500μl缓冲液b、500μl无水乙醇,充分混匀后使噬菌体的核酸析出。之后使用硅胶柱,采用上样-离心的方法时其对噬菌体的核酸进行吸附,并使用70%的无水乙醇,对基因组粗样进行脱盐处理,待乙醇挥发完毕后,使用ddh2o 对柱上的基因组进行洗脱并测定其dna浓度,样品最终置于-20℃保存。
[0071]
(2)全基因组测序
[0072]
该噬菌体基因组核酸寄送至惠通科技生物有限公司(广东,中国),使用illumina 平台对进行全基因组进行测序:使用nexteraxt dna文库制备试剂盒(illumina,sandiego,ca)构建平均长度为350p的dna文库。在illumina novaseq 6000平台上对dna进行测序,得到150bp的配对末端序列。原始的序列reads使用ngs qc toolkit(version 2.3.3)进行编辑,其中高质量的reads使用spades软件(version 3.15.2) 进行拼接组装。基因组上可能含有的开放阅读框(orf)使用genemarks进行预测,并通过blastx比对(www.ncbi.nlm.nih.gov)依照基因同源性进行注释。
[0073]
该噬菌体基因组的测序结果利用phageterm软件进行分析,此外,基于与噬菌体复制和结构有关的末端酶(terminase)和门户蛋白(portal protein)的相似性使用 mega(version 7.0)以neighbor joining法进行了系统发育树的构建。
[0074]
如图4所示,经过生物信息学的基因分析vb_bpp_hn01基因组包含一条如seqid no.1所示的核苷酸序列的双链dna,从测序的原始数据中识别到了一段大小407 bp的重序列(repeat region)为其基因组的起点,该噬菌体基因组结构具有93个orf,其中22个被标记为假设性蛋白质,其orf按负责的功能可分为:7个负责噬菌体外部结构合成的orf,其中orf73编码外壳蛋白,与n4短尾噬菌体同源。orf70和orf90 共同负责噬菌体尾丝结构的组成,并且其长度有orf74和orf80所决定,两者同样与一短尾噬菌体的基因存在较高的同源性。在噬菌体的表面还装饰有orf24的翻译产物;共有9个基因参与到了与噬菌体核酸有关的事件之中,orf51为dna解旋酶,保证基因组复制的起始,其间还有orf62(单链dna结合蛋白)和orf60(引物酶)的参与,整个合成过程由orf53这一多聚酶负责,并有orf38和orf45的协助。此外推测orf76也与dna的复制有关,其与mazg蛋白同源,后者可调节宿主菌内的环境,使其适应于噬菌体的增殖。而整个转录过程受噬菌体自身的转录酶(orf23和 orf67)所控制。
[0075]
进一步对该噬菌体全基因组比对发现:已测序的bp噬菌体相比 较(相关序列来源于源于www.millardlab.org),未发现vb_bpp_hn01 与其存在同源性(图5a),其次blastn给出的所有相似病毒/噬菌体, 在比对过程中,其全基因覆盖率不超过5%,均为无效结果。如使用 viptree进行病毒组的分析,发现vb_bpp_hn01被认定为与可感染 无色杆菌的噬菌体存在亲缘性(图5b),后期分析可能是因为rna 聚合酶、尾丝蛋白等单个基因或部分片段的相似性导致的(图5c和 图5d)。如以末端酶和门户蛋白的同源性进行判断,可发现该噬菌体 可能与欧文氏菌噬菌体或根瘤菌属噬菌体存在一定的亲缘性。
[0076]
vb_bpp_hn01噬菌体的细胞保护实验
[0077]
将a549细胞(ccl-185
tm
)接种于含10%小牛血清的rpmi 1640完全培养基中,以37℃、5%co2的条件进行培养,当细胞的覆盖率超过70%时,依照标准程序对细胞进行传代。然后将2
×
104a549细胞接种于96孔板中,并使用2
×
105cfubp hnbp001对其进行感染。2小时后,在孔板中加入2
×
104pfu噬菌体、40μg/ml 头孢他啶以及两者的混合物(共三组),37℃、5%co2培养18小时后,使用cck-8 试剂盒,依照说明书对其最终在450nm处的吸光度进行测量,记为a
x
。其中未经任何处理的a549细胞组作为阴性对照,同样使用cck-8试剂盒,测量其在450nm处的吸光度,记为ab。依照下述公式对bp hnbp001侵染下、噬菌体/抗生素处理后的细胞存活率进行计算。细胞存活率=(ab—a
x
)/ab×
100%。
[0078]
结果如图6所示,在bp hnbp001的作用下,a549细胞的存活率显著下降,只有未侵染组别的40%左右。而经过moi=0.1的vb_bpp_hn01噬菌体的处理,细胞的死亡率下降,所产生的保护效果要略微由于40μg/ml的头孢他啶的效果,并且如在感染后同时使用vb_bpp_hn01和头孢他啶,a549的存活率会得到进一步地提升。
[0079]
以上所述,仅为本技术较佳的具体实施方式,但本技术的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本技术揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本技术的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。