tmod3和/或adsl在非小细胞癌中的应用
技术领域
1.本发明涉及疾病治疗领域。具体地,本发明涉及tmod3或adsl在非小细胞癌中的应用。
背景技术:
2.非小细胞肺癌(non-small cell lung cancer,nsclc)是我国乃至全球范围内发病率和死亡率最高的恶性肿瘤之一,严重危害人类健康,是迫切需要解决的难题。目前肺癌仍然是人类生命健康的最大威胁之一,其中非小细胞肺癌占80%-85%。近年来,包括非小细胞肺癌靶向治疗、化疗、手术和放疗等治疗手段均取得了较大的进展。然而仍有许多严峻的问题亟待解决,主要包括:异质性带来的药物敏感性问题、耐药和转移带来的复发和预后差的问题,以及缺乏针对性和精准治疗靶点的问题,这些因素都严重影响了nsclc治疗的临床效果。因此,探究新的nsclc致癌基因,对更加精细和深入的理解nsclc的发病机制、发现新的治疗靶点并发展有效的治疗策略,具有重要的理论意义和临床价值,也是目前国内外肺癌研究的重点和难点。
3.病因学分析显示,驱动基因的异常表达和突变是nsclc发生发展的重要因素。另一方面,越来越多的证据表明,铁死亡(ferroptosis)在非小细胞癌的肿瘤发生发展中发挥重要作用。铁死亡是不同于凋亡和自噬的新型程序性细胞死亡,能够抑制肿瘤细胞生长,显著提高肿瘤的治疗效果,已经成为癌症治疗的重要治疗靶标。
4.原肌球调节蛋白tmod3是细胞骨架的重要组成部分,可以阻止尖端肌动蛋白丝的解聚。有研究结果表明,tmod3可能在癌症的发生发展中起到一定的作用。但是,关于tmod3与肿瘤关系的研究十分有限。研究报道,microrna-490-3p能够通过靶向tmod3抑制肝癌细胞的增殖和侵袭。在肿瘤中,tmod3能够通过稳定肌动蛋白-肌球蛋白丝来控制突出结构和收缩结构之间的平衡。tmod3通过激活erk/mapk信号通路促进肝癌细胞的恶性进展。tmod3在前列腺癌中参与血红素加氧酶介导的肿瘤细胞骨架调节。
5.截至目前,tmod3与非小细胞肺癌的关系尚不清楚,非小细胞肺癌细胞铁死亡的调控分子机制同样尚不清楚,是重大的科学问题。因此,本技术探讨tmod3在非小细胞肺癌恶性进展中的作用及其分子机制,具有重要的创新意义。
技术实现要素:
6.为了解决上述技术问题,本技术目的之一在于提供了tmod3及其相互作用基因adsl在制备诊断或治疗非小细胞肺癌产品中的用途。
7.为实现上述目的,本发明具体技术方案如下:
8.第一方面,本发明提供了检测tmod3和/或adsl表达水平的试剂在制备诊断和/或预后评估非小细胞肺癌的产品中的应用。。
9.进一步地,所述tmod3在检测非小细胞肺癌的样本中高表达,并与不良预后正相关;所述adsl在检测非小细胞肺癌的样本中低表达。
10.第二方面,本发明提供了一种诊断或预后评估非小细胞肺癌的试剂盒,其包括检测样本中tmod3表达水平的试剂和/或adsl表达水平的试剂。
11.进一步地,所述试剂选自:
12.特异性识别tmod3或adsl基因的探针;或
13.特异性扩增tmod3或adsl基因的引物;或
14.特异性结合tmod3或adsl蛋白的抗体或配体。
15.第三方面,本发明提供了adsl促进剂在制备治疗非小细胞肺癌的药物中的应用,所述adsl促进剂选自以下至少一种:
16.(a)tmod3抑制剂;
17.(b)铁死亡激活剂;
18.(c)adsl或重组表达adsl的构建物。
19.进一步地,所述治疗非小细胞肺癌的药物包括抑制非小细胞肺癌细胞增值的药物,抑制非小细胞肺癌细胞侵袭、迁移的药物或促进非小细胞肺癌细胞铁死亡的药物。
20.本发明证实tmod3能促进akt信号通路活性,抑制nsclc细胞中的铁死亡,从而对肺癌的发生和发展起到促进作用。
21.进一步地,所述tmod3抑制剂能促进adsl表达;所述tmod3抑制剂包括抑制tmod3表达水平和/或抑制tmod3表达产物功能活性的试剂。
22.进一步地,所述抑制tmod3表达水平的试剂包括tmod3 rna干扰剂或反义寡核苷酸;所述抑制tmod3表达产物功能活性的试剂包括特异性结合tmod3蛋白的抗体。
23.优选地,所述rna干扰剂以tmod3的序列为靶序列、且能够抑制tmod3表达水平的试剂,包括:shrna(小发夹rna)、小干扰rna(sirna)。
24.第四方面,本发明提供了一种治疗非小细胞肺癌的药物组合物,所述药物组合物包括以下至少一种:tmod3抑制剂,铁死亡激活剂,adsl或重组表达adsl的构建物;
25.第五方面,本发明提供了筛选用于预防和/或治疗非小细胞肺癌的候选药物的方法,其包括:
26.(1)在受试试剂存在的情况下,测定tmod3和/或adsl在能够表达细胞中的表达水平;
27.(2)将步骤(1)的测定结果与不存在所述受试试剂时测定的所述tmod3和/或adsl的表达水平进行比较;
28.其中,如果步骤(1)的测定结果与不存在所述受试试剂时的测定结果相比tmod3降低或adsl升高,表明所述受试试剂是预防和/或治疗非小细胞肺癌的候选药物。
29.基于上述技术方案,本发明具有以下有益效果:
30.本发明发现tmod3通过与adsl互作,进而抑制adsl功能,增强nsclc恶性进展。adsl对nsclc是一个抑癌基因,但受到tmod3负调控,抑制了a549&sk-mes-1的铁死亡进程,最终导致恶性进展。
31.本发明揭示了新的nsclc致癌基因tmod3和抑癌基因adsl在非小细胞肺癌恶性进展和铁死亡中发挥重要作用及其潜在分子机制,能为nsclc的诊断、治疗和预后提供依据,为精准治疗提供新的研究方向和理论依据。
附图说明
32.图1 tmod3在非小细胞肺癌临床组织中的表达情况:a:正常肺泡,b:正常支气管,c:高分化腺癌,d:高分化鳞癌,e:低分化腺癌,f:低分化鳞癌。
33.图2 tmod3基因高表达与非小细胞肺癌病人生存率曲线统计学分析。
34.图3 tmod3在非小细胞肺癌细胞中的表达情况分析及干扰筛选,a显示tmod3蛋白在各细胞系中的表达情况,b显示tmod3-sirna转染a549和sk-mes-1细胞后检测tmod3蛋白的表达情况。
35.图4干扰tmod3显著抑制非小细胞肺癌细胞增殖,图a显示mtt检测结果,图b显示克隆形成实验分析结果。
36.图5 transwell实验分析干扰tmod3对非小细胞肺癌侵袭的影响,图a&b a549细胞,图c&d sk-mes-1细胞。
37.图6细胞划痕实验分析干扰tmod3对非小细胞肺癌侵袭的影响,图a&b a549细胞,图c&d sk-mes-1细胞。
38.图7 tmod3干扰处理的非小细胞肺癌细胞株铁死亡分析,图a&b干扰tmod3能够进一步增强erastin对非小细胞肺癌细胞活性的抑制作用,图c&d干扰tmod3能够显著增强非小细胞肺癌细胞中铁离子的含量。
39.图8敲低tmod3在非小细胞肺癌细胞a549(图a)和sk-mes-1(图b)中对akt信号通路的影响。
40.图9 qpcr证实在非小细胞肺癌细胞中tmod3负调控adsl基因;图a a549细胞,图b sk-mes-1细胞。
41.图10 western blot证实在非小细胞肺癌细胞中tmod3负调控adsl蛋白。
42.图11 qpcr检测敲低tmod3非小细胞肺癌细胞中gsh表达水平,其中shtmod3-1和shtmod3-2为tmod3敲低组,shrna-nc为对照组。
43.图12 qpcr检测敲降tmod3与铁死亡激活剂erastin对adsl表达影响,其中shtmod3-1和shtmod3-2为tmod3敲低组,shrna-nc为对照组。
具体实施方式
44.以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。
45.下述实施例所使用的实验方法如无特殊说明,均为常规方法。
46.下述实施例中所有的材料、试剂等,如无特殊说明,均可从商业途径获得。
47.实施例1 tmod3在非小细胞肺癌临床样本中的表达
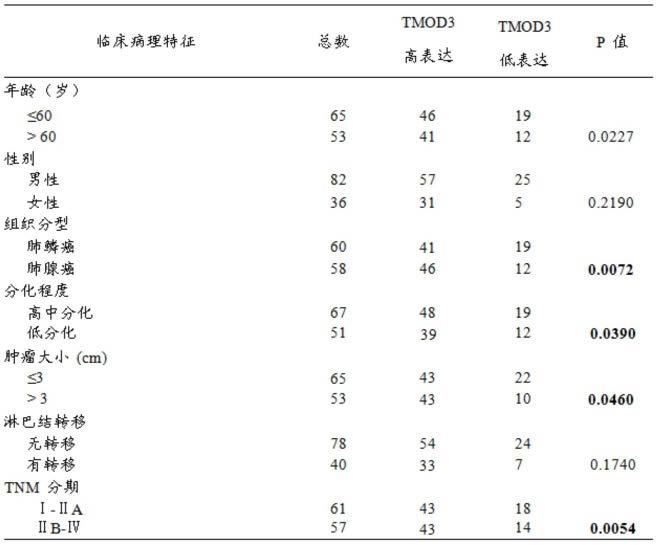
48.选取2014-2016年间,中国医科大学附属第一医院进行手术切除后并经病理确诊的非小细胞肺癌(nsclc)患者病例118例。所有参与本次病理相关性分析的118例患者,均未接受过手术前的放疗和化疗。男性患者(n=82例),女性患者(n=36例),年龄在37至77岁之间。根据国际抗癌联盟(uicc)第八版肺癌tnm分期系统,i-iia期患者(n=61例),iib-iv期患者共(n=57例)。根据who分类系统,鳞状细胞癌(n=58例),腺癌(n=60例),中分化至高分化(n=67例),低分化(n=51例)。肿瘤大小分类,小于等于3cm病例(n=65例),大于3cm病例(n=53例)。淋巴结转移病例(n=40例),淋巴结未转移病例(n=78例)。
49.通过免疫组化染色分析tmod3在正常肺泡组织、正常支气管组织、高分化肺腺癌组织、高分化肺鳞癌组织、低分化肺腺癌组织和低分化肺鳞癌组织中的表达情况。结果发现,与正常肺泡组织和正常支气管组织相比,tmod3在高分化肺腺癌组织、高分化肺鳞癌组织、低分化肺腺癌组织和低分化肺鳞癌组织中呈现显著高表达(图1a-f,表1);同时,通过gepia在线数据库中分析发现,tmod3的高表达与非小细胞肺癌患者不良预后密切相关(图2)。
50.上述结果说明,tmod3在非小细胞肺癌临床组织中高表达,并与不良预后正相关。
51.表1临床样本信息统计表
[0052][0053]
实施例2 tmod3对非小细胞肺癌恶性进展表型的影响
[0054]
1、tmod3在非小细胞肺癌细胞中的表达情况分析及干扰筛选
[0055]
将非小细胞肺癌细胞系a549、h1299、h460和sk-mes-1,正常肺上皮细胞heb2,对照细胞caco2,用25t培养瓶培养,复苏传代2代待细胞状态稳定后可以进行实验。
[0056]
利用western blot分析了tmod3蛋白在非小细胞肺癌细胞系a549、h1299、h460和sk-mes-1细胞中的表达情况,并以hbe2和caco2细胞作为对照组,三次重复实验。结果显示,肺腺癌细胞系a549和肺鳞癌细胞系sk-mes-1呈现出tmod3高表达(图3a)。
[0057]
为进一步探究tmod3在非小细胞肺癌中的作用,发明人设计三个tmod3干扰序列,发明人设计三个tmod3干扰序列,所述干扰序列如下:
[0058]
sirna1(si1):ggacagctgtagaattgga,seq id no.1;
[0059]
sirna2(si2):ggcactgattgatgcgtta,seq id no.2;
[0060]
sirna3(si3):ggcctgtagctgatgcgtta,seq id no.3。
[0061]
通过sirna干扰技术敲降tmod3,具体步骤如下:
[0062]
(1)1.5ml ep管加入200μl je'tprime缓冲液,加入20μm sirna,涡旋震荡10s后瞬时离心,静置5min;
[0063]
(2)加入4μl jetprime reagent转染试剂,涡旋震荡10s后瞬时离心,静置10min;
[0064]
(3)混合物加入含血清/无血清opti-mem培养基中;
[0065]
(4)转染sirna 6h后更换完全培养基;
[0066]
(5)转染48h后收取细胞检测tmod3敲降效率。
[0067]
通过western blot实验,发现sirna1-2均有敲低tmod3效果,其中sirna1具有最为理想的tmod3敲低效率,能够在a549和sk-mes-1细胞中显著抑制tmod3的表达(图3b)。因此,在后续实验中优选tmod3sirna1进行研究。
[0068]
2、干扰非小细胞肺癌细胞中tmod3,检测其对细胞增殖的影响
[0069]
(1)mtt
[0070]
在a549和sk-mes-1细胞中干扰tmod3,应用mtt检测试剂盒(碧云天,st316)结合酶标仪(美国biotek酶标仪epoch),分别在干扰tmod3后24h,48h,72h和96h测定在450nm处的吸光度。结果显示,与对照干扰处理相比,干扰tmod3,细胞活性受到显著抑制,表明干扰tmod3能够显著抑制非小细胞肺癌细胞增殖(图4a)。
[0071]
(2)克隆形成实验
[0072]
在a549和sk-mes-1细胞中干扰tmod3,应用克隆形成实验分析非小细胞肺癌细胞增殖情况,具体步骤如下:
[0073]
细胞铺6孔板,扩增过夜;次日细胞容片率达50-60%,转染sirna,感染tmod3 48h;收取细胞计数,按照数量梯度,重新铺到新的6孔板中,继续培养细胞14days;收取细胞,pbs清洗后,甲醇固定,结晶紫染色30min;双蒸水清洗结晶紫,晾干细胞,拍照。
[0074]
结果显示,与对照干扰处理相比,干扰tmod3,肺癌细胞克隆形成数量显著降低,进一步表明干扰tmod3能够显著抑制非小细胞肺癌细胞增殖(图4b)。
[0075]
上述实验说明,干扰tmod3显著抑制非小细胞肺癌细胞增殖。
[0076]
3、干扰非小细胞肺癌细胞中tmod3,检测其对细胞侵袭和迁移的影响
[0077]
(1)transwell
[0078]
在a549和sk-mes-1细胞中干扰tmod3,利用transwell 6孔细胞培养板进行细胞侵袭力检测,具体步骤如下:
[0079]
(a)铺基质胶:在4℃条件下将matrigel胶用无血清的细胞培养基或pbs缓冲液按照1:8比例稀释,取100μl均匀涂抹于上室的聚碳酸酯膜表面,37℃放置0.5-1h,使其聚合成凝胶;
[0080]
(b)细胞培养:取对数生长期的待测细胞,并用pbs洗涤,接着用无血清培养基悬浮细胞,调整细胞密度为1-10*105/ml;
[0081]
(c)接种细胞:在24孔板下室一般加入500-650μl含5%-10%fbs或趋化因子的培养基,然后用镊子将transwell小室置于24孔板内,取细胞悬液100-200μl加入上室(每孔细胞数量1
×
105),最后放入培养箱中培养12-48h。
[0082]
(d)细胞固定:取出小室,吸走培养基,用棉签轻轻擦拭matrigel和上室内的细胞。取新的24孔板加入4%多聚甲醛600μl,将小室放入后固定20-30min。
[0083]
(e)细胞染色及计数:弃固定液,用0.1-%0.2%结晶紫染色5-10min,pbs洗3遍,除去未与细胞结合的结晶紫,用棉签轻轻擦拭小室的上侧,将非特异性结合于小室上表面的染料擦掉,以便后续镜检。适当风干后,在高倍显微镜下选取5个视野观察细胞并计数。
[0084]
结果显示,与对照干扰处理相比,干扰tmod3显著抑制非小细胞肺癌细胞的侵袭能力(图5)。
[0085]
(2)伤口愈合实验
[0086]
在a549和sk-mes-1细胞中干扰tmod3,利用伤口愈合实验分析tmod3对非小细胞肺癌细胞侵袭的影响,结果显示,与对照干扰处理相比,干扰tmod3显著抑制非小细胞肺癌细胞的侵袭能力(图6)。
[0087]
上述实验说明,干扰tmod3显著抑制非小细胞肺癌细胞的侵袭和迁移。
[0088]
实施例3研究tmod3对非小细胞肺癌细胞铁死亡的影响
[0089]
在a549和sk-mes-1细胞中干扰tmod3,同时利用铁死亡激活剂erastin处理细胞,应用mtt检测试剂盒(abnova,ka0814)结合酶标仪(美国biotek酶标仪epoch)分析,结果显示,erastin单独处理能够抑制非小细胞肺癌细胞活性;而与对照干扰处理相比,干扰tmod3能够进一步增强erastin对非小细胞肺癌细胞活性的抑制作用(图7a和b)。
[0090]
在a549和sk-mes-1细胞中干扰tmod3,应用铁检测试剂盒分析发现,与对照干扰处理相比,干扰tmod3能够显著增强非小细胞肺癌细胞中铁离子的含量(图7c和d)。
[0091]
上述实验说明,干扰tmod3能够诱导非小细胞肺癌细胞的铁死亡。
[0092]
实施例4 tmod3调控非小细胞肺癌细胞恶性进展及铁死亡的分子机制
[0093]
在a549和sk-mes-1细胞中干扰tmod3,利用western blot实验分析非小细胞肺癌细胞中erk、akt和p38的表达及erk、akt和p38的磷酸化水平,结果发现,与对照干扰处理相比,干扰tmod3不能改变erk、akt和p38的表达水平,而能显著抑制erk、akt和p38的磷酸化水平(图8a和b),表明干扰tmod3能够抑制akt信号通路的活性。
[0094]
实施例5 tmod3的相互作用蛋白的研究
[0095]
a549&sk-mes-1细胞转染tmod3-flag外源表达质粒,随后进行免疫沉淀/ip-anti-flag实验,pull down与tmod3互作蛋白;通过蛋白液相质谱分析/ms筛选蛋白,发现pull down的互作蛋白的氨基酸预测序列与adsl蛋白高度相似,怀疑adsl是tmod3互作蛋白。
[0096]
为了验证pull down的蛋白是否为adsl,进行了如下实验:
[0097]
1、为了构建稳定敲降shrna-tmod3基因的细胞系,将sirna1和2序列分别构建到表达载体中,转染至a549&sk-mes-1细胞系中,提取rna,qpcr检测adsl的基因转录表达水平,结果如图9所示,图9a-b证实了tmod3负调控adsl基因的转录。所述adsl引物包括如下:
[0098]
homo-adsl-f:ttacgacatgatgtgatggctc;seq id no.4
[0099]
homo-adsl-r:tccaacatagcaagaagtagcac,seq id no.5。
[0100]
2、收集稳定敲降shrna-tmod3基因的a549&sk-mes-1细胞系进行western blot实验,结果如图10所示,a549&sk-mes-1细胞敲降tmod3后,adsl蛋白表达水平上升,说明tmod3抑制adsl的活性,与qpcr结果趋势相同。
[0101]
3、收集稳定敲降shrna-tmod3基因的a549&sk-mes-1细胞系,并在细胞系中分别加入dmso、5μm浓度erastin、10μm浓度erastin,随后提取rna,qpcr检测肿瘤铁死亡相关因子gsh谷胱甘肽的基因转录表达水平,结果如图11所示,相较于非敲降细胞,a549&sk-mes-1细胞敲降tmod3后,gsh谷胱甘肽表达水平降低,加入铁死亡激活剂erastin促进细胞铁死亡,gsh表达水平进一步降低;在erastiin 10μm浓度刺激下的gsh表达水平下降地更为显著,说明敲降tmod3与铁死亡激活剂erastin的对铁死亡的促进作用呈正相关,并且二者呈协同作用。
[0102]
4、收集稳定敲降shrna-tmod3基因的a549&sk-mes-1细胞系,并在细胞系中分别加
入dmso、5μm浓度erastin、10μm浓度erastin,随后提取rna,qpcr检测adsl的基因转录表达水平,结果如图12所示,相较于非敲降细胞,a549&sk-mes-1细胞敲降tmod3后,adsl表达水平升高,加入铁死亡激活剂erastin促进细胞铁死亡,adsl表达水平进一步升高,说明敲降tmod3与铁死亡激活剂erastin对adsl表达的促进的作用呈正相关,并且二者呈协同作用。
[0103]
结论:tmod3通过与adsl互作,进而抑制adsl功能,增强nsclc恶性进展。adsl对nsclc是一个抑癌基因,但受到tmod3负调控,抑制了a549&sk-mes-1的铁死亡进程,最终导致恶性进展。
[0104]
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。