1.本发明属于氮杂环合成以及光催化有机合成领域,涉及一种喹唑啉酮类化合物的制备,具体涉及一种廉价光敏剂参与的磷酰化喹唑啉酮类化合物的制备方法。
背景技术:
2.目前,可见光介导作为一种强大的合成手段,可实现具有挑战性的化学转化,因此备受有机合成家们的关注,其次其作为一种广泛的清洁能源也受到化学各领域科学家们的关注。近些年,可见光诱导的合成方法被广泛用于合成有机小分子过程中,因其可见光作为反应驱动力,完全符合绿色化学的发展需求。可见光催化通常在温和的条件下进行,操作简便。有机化学领域中,通过可见光氧化还原反应合成新型化合物已成为一种重要的合成策略。由于底物分子通过外层单电子转移形成高活性自由基参与反应,该策略可以为许多难以通过离子型反应直接获得的重要化合物提供直接、高效的合成途径。这些反应条件温和、回收率高、选择性好、底物官能团耐受性高等特点。
3.喹唑啉酮作为一类具有良好生物医药活性的含氮杂环化合物,是150多种生物碱的重要母核结构。很多天然产物、药物活性分子的结构单元中也存在喹唑啉酮结构,如色胺酮、骆驼宁碱a等生物碱都是具有喹唑啉酮类骨架结构。喹唑啉酮还是精细化工和医药合成的重要中间体,如由喹唑啉酮经氯化、氨化后得到的4-氨基喹唑啉是一系列药物的基本骨架。喹唑啉酮及其衍生物在杀菌、消炎、止痛、抗高血压、抗糖尿病、抗疟疾、抗癌等方面均显示出良好的生物活性,如用于疟疾的常山碱、用于安眠药的安眠酮、抗高血压药多沙唑嗪等。因喹唑啉酮类化合物独特的结构特征、广泛的功能基团和广谱的生物活性,引起合成化学家的广泛兴趣。
4.喹唑啉及其衍生物的典型制备方法是在氨存在下加热2-酰基-n-酰苯胺,此种生产方法污染较多,实验过程中危险系数较大。因此,开发新型喹唑啉酮化合物合成方法具有重要的实用价值。目前,国内外还没有利用可见光催化磷酰化喹唑啉酮类化合物的公开文献。
技术实现要素:
5.本发明的目的在于,提供一种光催化磷酰化喹唑啉酮类化合物的制备方法。该方法是在空气气氛、室温环境下,以清洁能源可见光的照射为驱动力,使3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮类化合物的末端非活化烯烃与芳基磷氧自由基环加成生成所需的磷酰化喹唑啉酮类化合物。
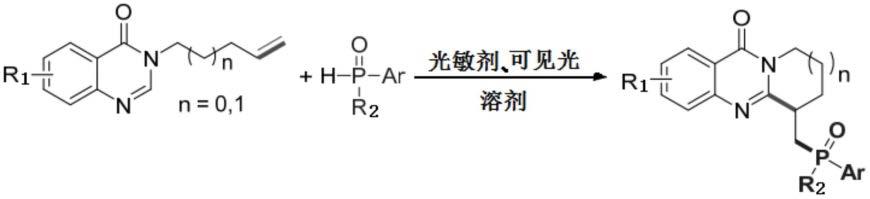
6.为实现上述目的,本发明采用的技术方案为:一种光催化磷酰化喹唑啉酮类化合物的制备方法,其特征在于:该方法是在空气环境中,将3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮类化合物与芳基磷氧类化合物溶于溶剂中,在光敏剂和可见光照射作用下,使3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮类化合物的末端非活化烯烃与芳基磷氧自由基环加成,生成磷酰化喹唑啉酮类化合物,反应通式如下:
[0007][0008]
其中,3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮类化合物通式中,r1为氢、me、nhboc或cf3,芳基磷氧类化合物通式中,r2为苯基、甲氧基苯基或卤素苯基。
[0009]
较佳的,上述光敏剂为四溴荧光素(eosiny);可见光照射波长为450nm;溶剂为2-甲基四氢呋喃;反应温度为室温,时长为12h;反应初始时3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮:芳基磷氧类化合物:光敏剂的摩尔比为2:4:0.1。
[0010]
本发明提供了一种经济、高效的磷酰化喹唑啉酮类化合物合成方法,本方法在可见光照射且廉价光敏剂条件下,3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮类化合物与芳基磷氧类化合物通过自由基环加成途径,以制备磷酰化喹唑啉酮类化合物。本发明方法涉及未活化末端烯烃双功能化和自由基途径,包括芳基磷氧自由基生成、四溴荧光素发生基态—激发态—自由基阴离子—基态循环、超氧根阴离子(o2·-)的形成。本发明的方法原料合成简单,反应高效,具有良好的底物适应性、廉价的光敏剂催化、外加添加剂的参与的特点。
具体实施方式
[0011]
下列实施例将有助于理解本发明,但本发明的内容并不局限于此。
[0012]
实施例1
[0013]
室温下,将底物3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮42.8毫克(0.2mmo l)和二苯基磷氧80.8毫克(0.4mmol)、光敏剂eosin y(0.01mmol)及溶剂2-甲基四氢呋喃2毫升,在空气环境下加入到15毫升封管中。然后将封管放入10瓦450nm光反应器中反应12h。经薄层色谱(tcl)检测直到反应完全,滤液经旋转蒸发后经硅胶柱层析分离(洗脱剂:乙酸乙酯/石油醚=1/1),得66.3毫克黄色固体,产率为80%,经鉴定,其结构式为:表征数据如下:
[0014]1h nmr(400mhz,cdcl3):δ8.22(dd,j=8.0,1.2hz,1h),7.96
–
7.90(m,2h),7.81
–
7.75(m,2h),7.71
–
7.66(m,1h),7.55
–
7.40(m,8h),4.25
–
4.18(m,1h),3.93
–
3.86(m,1h),3.78
–
3.70(m,1h),3.38
–
3.27(m,1h),2.56
–
2.45(m,2h),1.97
–
1.88(m,2h),1.76
–
1.69(m,1h);
[0015]
13
c nmr(101mhz,cdcl3):δ162.11,156.51(d,j=13.2hz,1c),147.05,134.14,133.30(dd,j=163.6,99.8hz,1c),131.97(dd,j=17.3,2.7hz,1c)131.16(d,j=9.3hz,1c),130.67(d,j=9.5hz,1c),129.87(dd,j=14.7,11.8hz,1c),126.86(d,j=13.6hz,1c),126.49,120.31,41.60,36.00(d,j=1.4hz,1c),32.26(d,j=72.4hz,1c),26.85(d,j=1.9hz,1c),20.90;
[0016]
31
p nmr(162mhz,cdcl3):δ32.49;hrms(esi)m/z calcd.for c
25h23
n2nao2p[m na]
:437.1389,found 437.1395。
[0017]
实施例2
[0018]
室温下,将底物6-甲基-3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮45.6毫克(0.2mmol)和二苯基磷氧80.8毫克(0.4mmol)、光敏剂eosin y(0.01mmol)及溶剂2-甲基四氢呋喃2毫升,在空气环境下加入到15毫升封管中。然后将封管放入10瓦450nm光反应器中反应12h。经薄层色谱(tcl)检测直到反应完全,滤液经旋转蒸发后经硅胶柱层析分离(洗脱剂:乙酸乙酯/石油醚=1/1),得54.8毫克白色固体,产率为64%。
[0019]
该固体经鉴定,结构式为表征数据如下:
[0020]1h nmr(500mhz,cdcl3):δ8.02
–
7.98(m,1h),7.94
–
7.90(m,2h),7.80
–
7.75(m,2h),7.52
–
7.46(m,5h),7.45
–
7.41(m,3h),4.23
–
4.17(m,1h),3.90
–
3.84(m,1h),3.73(ddd,j=15.5,9.4,3.0hz,1h),3.90
–
3.84(m,1h),2.57
–
2.49(m,1h),2.49
–
2.42(m,4h),1.97
–
1.85(m,2h),1.74
–
1.66(m,1h);
[0021]
13
c nmr(126mhz,cdcl3):δ162.06,155.57(d,j=13.0hz),145.04,136.56,135.60,134.56(dd,j=200.7,99.8hz),132.00(dd,j=19.9,2.7hz),131.16(d,j=9.4hz),130.67(d,j=9.5hz),128.84(dd,j=16.0,11.8hz),126.40(d,j=73.4hz),120.00,41.50,35.82(d,j=1.5hz),32.67(d,j=72.3hz),26.82(d,j=2.0hz),21.38,20.89;
[0022]
31
p nmr(202mhz,cdcl3):δ32.97;hrms(esi)m/z calcd.for c
26h25
n2nao2p[m na]
:451.1546,found 451.1549。
[0023]
实施例3
[0024]
室温下,将底物(4-氧代-3-(戊-4-烯-1-基)-3,4-二氢喹唑啉-6-基)氨基甲酸叔丁酯65.8毫克(0.2mmol)和二苯基磷氧80.8毫克(0.4mmol)、光敏剂eosin y(0.01mmol)及溶剂2-甲基四氢呋喃2毫升,在空气环境下加入15毫升封管中。然后将封管放入10瓦450nm光反应器中反应12h。经薄层色谱(tcl)检测直到反应完全,滤液经旋转蒸发后经硅胶柱层析分离(洗脱剂:乙酸乙酯/石油醚=1/1)得76.2毫克白色固体,产率为73%。
[0025]
经鉴定,该固体结构式为表征数据如下:
[0026]1h nmr(500mhz,cdcl3):δ8.15(s,1h),8.01(d,j=2.6hz,1h),7.96
–
7.89(m,2h),7.81
–
7.74(m,2h),7.55
–
7.47(m,5h),7.46
–
7.42(m,2h),7.28(s,1h),4.26
–
4.21(m,1h),3.92
–
3.86(m,1h),3.73(ddd,j=15.5,9.3,2.9hz,1h),3.34
–
3.27(m,1h),2.53
–
2.46(m,2h),1.98
–
1.88(m,2h),1.75
–
1.69(m,1h),1.53(s,9h);
[0027]
13
c nmr(126mhz,cdcl3):δ161.88,154.87(d,j=13.3hz,1c),152.94,142.82,137.46,133.48(dd,j=206.8,99.5hz,1c),131.92(dd,j=21.7,2.7hz,1c),131.18(d,j=9.2hz,1c),130.68(d,j=9.4hz,1c),128.86(dd,j=17.6,11.7hz,1c),127.88,125.65,120.61,80.98,41.60,35.88,32.26(d,j=72.3hz,1c),28.50,26.92(d,j=1.7hz,1c),20.97;
[0028]
31
p nmr(202mhz,cdcl3):δ31.94;hrms(esi)m/z calcd.for c
30h32
n3nao4p[m na]
:552.2023,found 552.2025.
[0029]
实施例4
[0030]
室温下,将底物3-(戊-4-烯-1-基)-6-(三氟甲基)喹唑啉-4(3h)-酮56.4毫克(0.2mmol)和二苯基磷氧80.8毫克(0.4mmol)、光敏剂eosiny(0.01mmol)及溶剂2-甲基四氢呋喃2毫升,在空气环境下加入到15毫升封管中。然后将封管放入10瓦450nm光反应器中反应12h。经薄层色谱(tcl)检测直到反应完全,滤液经旋转蒸发后经硅胶柱层析分离(洗脱剂:乙酸乙酯/石油醚=1/1),得68.5毫克白色固体,产率为71%。
[0031]
经鉴定,该固体结构式为表征数据如下:
[0032]1h nmr(500mhz,cdcl3):δ8.51(s,1h),7.93
–
7.85(m,3h),7.79
–
7.71(m,3h),7.54
–
7.48(m,3h),7.46
–
7.40(m,2h),7.32(dt,j=7.5,3..0hz,1h),4.25
–
4.19(m,1h),3.94
–
3.89(m,1h),3.68(ddd,j=15.4,9.6,3.2hz,1h),3.42
–
3.33(m,1h),2.61
–
2.53(m,1h),2.50
–
2.44(m,1h),2.00
–
1.91(m,2h),1.79
–
1.71(m,1h);
[0033]
13
c nmr(126mhz,cdcl3):δ161.37,158.92(d,j=12.4hz,1c),149.13,133.20(d,j=182.2,99.3hz,1c),132.07(dd,j=19.6,2.7hz,1c),131.67,131.12(d,j=9.4hz,1c),130.68(d,j=9.5hz,1c),130.22,130.19,128.92(dd,j=16.3,11.9hz,1c),127.91,120.13,41.85,36.24(d,j=1.6hz,1c),32.18(d,j=72.1hz,1c),26.69(d,j=2.2hz,1c),20.81;
[0034]
19
f nmr(471mhz,cdcl3):δ-62.26.;
[0035]
31
p nmr(202mhz,cdcl3):δ32.29;hrms(esi)m/z calcd.for c
26h22
f3n2nao2p[m
na]
:505.1263,found 505.1269。
[0036]
实施例5
[0037]
室温下,将底物3-(戊-4-烯-1-基)-6-(三氟甲基)喹唑啉-4(3h)-酮40.0毫克(0.2mmol)和二苯基磷氧80.8毫克(0.4mmol)、光敏剂eosin y(0.01mmol)及溶剂1,2-二氯乙烷2毫升,在空气环境下加入到15毫升封管中。然后将封管放入10瓦450nm光反应器中反应12h。经薄层色谱(tcl)检测直到反应完全,滤液经旋转蒸发后经硅胶柱层析分离(洗脱剂:乙酸乙酯/石油醚=1/1),得62.4毫克b白色油状液体,产率为78%。
[0038]
经鉴定,该液体结构式为表征数据如下:
[0039]1h nmr(400mhz,cdcl3):δ8.23(d,j=7.9hz,1h),7.91
–
7.86(m,2h),7.80(dd,j=11.7,7.3hz,2h),7.72
–
7.64(m,2h),7.57
–
7.40(m,7h),4.29
–
4.24(m,1h),3.86
–
3.79(m,1h),3.59
–
3.48(m,1h),3.46
–
3.40(m,1h),2.60
–
2.52(dt,j=15.8,8.7hz,1h),2.49
–
2.42(m,1h),2.03
–
2.02(m,1h);
[0040]
13
c nmr(101mhz,cdcl3):δ160.82,160.61(d,j=16.6hz,1c),148.91,134.24,132.47(t,j=100.5hz,1c),132.25(dd,j=12.4,2.5hz,1c),131.05(d,j=9.4hz,1c),130.75(d,j=9.6hz,1c),128.99(dd,j=19.0,11.8hz,1c),126.93,126.57(d,j=1.4hz,1c),120.85,45.03,38.76(d,j=2.4hz,1c),31.93(d,j=72.4hz,1c),28.04;
[0041]
31
p nmr(162mhz,cdcl3):δ31.42(d,j=6.9hz);hrms(esi)m/z calcd.for c
24h21
n2nao2p[m na]
:423.1233,found 423.1335。
[0042]
实施例6
[0043]
室温下,将底物3-(2-(丙-1-烯-2-基)苯基)喹唑啉-4(3h)-酮52.4毫克(0.2mmol)和二苯基磷氧80.8毫克(0.4mmol),光敏剂eosin y(0.01mmo l)及溶剂2-甲基四氢呋喃2毫升,在空气环境下加入到15毫升封管中。然后将封管放入10瓦450nm光反应器中反应12h。经薄层色谱(tcl)检测直到反应完全,滤液经旋转蒸发后经硅胶柱层析分离(乙酸乙酯/石油醚=1/1)得75.8毫克白色固体,产率为74.9%。
[0044]
经鉴定,该固体结构式为表征数据如下:
[0045]1h nmr(500mhz,cdcl3):δ8.35(d,j=8.1hz,1h),8.20(d,j=8.0hz,1h),7.63
–
7.57(m,2h),7.52
–
7.49(m,2h),7.39
–
7.35(m,2h),7.31(t,j=1.3hz,2h),7.26
–
7.25(m,2h),7.12(dd,j=2.8,2.0hz,2h),7.05
–
6.98(m,2h),6.86
–
6.83(m,2h),3.42(dd,j=15.2,8.5hz,1h),3.03(dd,j=15.2,12.6hz,1h),1.60(s,3h);
[0046]
13
c nmr(126mhz,cdcl3):δ162.70(d,j=2.5hz,1c),159.54,147.17,138.79,133.91,133.35(d,j=2.7hz,1c),132.54(d,j=2.8hz,1c),131.27(dd,j=38.5,2.6hz,
1c),130.63(d,j=11.5hz,1c),130.44(d,j=16.1,9.7hz,1c),128.86(dd,j=68.8,58.1hz,1c),128.68,128.45(d,j=11.7hz,1c),127.77(d,j=11.8hz,1c),126.62(d,j=10.6hz,1c),124.52,121.61,116.78,46.26(d,j=4.0hz,1c),39.70(d,j=70.5hz,1c),29.64(d,j=12.4hz,1c);
31
p nmr(202mhz,cdcl3):δ25.44;
[0047]
hrms(esi)m/z calcd.for c
29h23
n2nao2p[m na]
:485.1389,found485.1391。
[0048]
实施例7
[0049]
室温下,将底物3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮42.8毫克(0.2mmo l)和双(4-甲氧基苯基)氧化磷104.8毫克(0.4mmol)、光敏剂eosin y(0.01mmol)及溶剂2-甲基四氢呋喃2毫升,在空气环境下加入到15毫升封管中。然后将封管放入10瓦450nm光反应器中反应12h。经薄层色谱(tcl)检测直到反应完全,滤液经旋转蒸发后经硅胶柱层析分离(洗脱剂:乙酸乙酯/石油醚=1/1),得74.9毫克黄色油状液体,产率为79%。
[0050]
经鉴定,该液体结构式为表征数据如下:
[0051]1h nmr(500mhz,cdcl3):δ8.23(dd,j=8.0,1.6hz,1h),7.83(dd,j=11.1,8.7hz,2h),7.72
–
7.65(m,3h),7.58(d,j=8.2hz,1h),7.43
–
7.40(m,1h),6.99(dd,j=8.8,2.2hz,2h),6.93(dd,j=8.8,2.3hz,2h),4.23
–
4.18(m,1h),3.93
–
3.87(m,1h),3.82(d,j=4.4hz,6h),3.66(ddd,j=15.5,9.6,2.9hz,1h),3.34
–
3.26(m,1h),2.54
–
2.42(m,2h),1.99
–
1.87(m,2h),1.77
–
1.70(m,1h);
[0052]
13
c nmr(126mhz,cdcl3):161.37(dd,j=20.7,2.8hz,1c),160.99,155.56(d,j=13.2hz,1c),145.99,132.95,131.92(d,j=10.7hz,1c),131.43(d,j=10.9hz,1c),125.72(d,j=16.1hz,1c),125.29,119.20,113.27(dd,j=21.9,12.7hz,1c),54.32,40.50,34.93,31.49(d,j=73.1hz,1c),28.68,25.62,19.74(d,j=9.1hz,1c);
[0053]
31
p nmr(202mhz,cdcl3):δ33.13;hrms(esi)m/z calcd.for c
27h27
n2nao4p[m na]
:497.1601,found 497.1603。
[0054]
实施例8
[0055]
室温下,将底物3-(戊-4-烯-1-基)喹唑啉-4(3h)-酮42.8毫克(0.2mmo l)和双(4-氯苯基)氧化膦108.0毫克(0.4mmol)、光敏剂eosin y(0.01mmol)及溶剂2-甲基四氢呋喃2毫升,在空气环境下加入到15毫升封管中。然后将封管放入10瓦450nm光反应器中反应12h。经薄层色谱(tcl)检测直到反应完全,滤液经旋转蒸发后经硅胶柱层析分离(洗脱剂:乙酸乙酯/石油醚=1/1),得68.5毫克白色油状液体,产率为71%。
[0056]
经鉴定,该液体结构式为表征数据如下:
[0057]1h nmr(500mhz,cdcl3):δ8.22(d,j=7.9hz,1h),7.85(dd,j=11.1,8.2hz,2h),7.71
–
7.66(m,3h),7.50
–
7.46(m,3h),7.43
–
7.40(m,3h),4.21
–
4.16(m,1h),3.95
–
3.90(m,1h),3.70(ddd,j=15.6,9.2,3.0hz,1h),3.34
–
3.25(m,1h),2.54
–
2.43(m,2h),1.99
–
1.89(m,2h),1.77
–
1.69(m,1h);
[0058]
13
c nmr(126mhz,cdcl3):162.00,156.09(d,j=12.6hz,1c),146.84,138.85(dd,j=25.5,3.3hz,1c),134.21,132.51(d,j=10.2hz,1c),131.97(d,j=10.3hz,1c),129.41(d,j=12.4hz,1c),129.26(d,j=12.4hz,1c),126.82,126.67(d,j=13.1hz,1c)120.25,41.68,35.87(d,j=1.5hz,1c),32.30(d,j=73.2hz,1c),26.97(d,j=1.9hz,1c),20.88;
31
p nmr(202mhz,cdcl3):δ31.86;
[0059]
hrms(esi)m/z calcd.for c
25h21
cl2n2nao2p[m na]
:505.0610,found505.0611。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
