抗ca19-9的抗体、其应用和检测ca19-9的试剂盒
技术领域
1.本发明涉及抗体技术领域,具体而言,涉及一种抗ca19-9的抗体、其应用和检测ca19-9的试剂盒。
背景技术:
2.肿瘤标志物(tumor marker)是反映肿瘤存在的化学类物质。它们不存在于正常成人组织而仅见于胚胎组织,或在肿瘤组织中的含量大大超过在正常组织里的含量,它们的存在或量变可以提示肿瘤的性质,借以了解肿瘤的组织发生、细胞分化和细胞功能,以帮助肿瘤的诊断、分类、预后判断以及治疗指导。
3.20世纪80年代,专家利用杂交瘤技术获得了能识别肿瘤特异性大分子的糖蛋白抗原(carbohydrate antigen,ca),并研制了单克隆抗体识别系统。ca是肿瘤细胞的相关抗原。常用的ca系列有:ca 125(卵巢癌相关抗原);ca 19-9(胰腺、肠癌相关抗原);ca15-3(乳腺癌相关抗原)。1983年limdholm等人用人结直肠癌细胞cold205免疫小鼠得到系列抗体以后相继发现了与这些抗体相应的系列抗原,包括ca19-9,ca50,ca242等。这一系列抗原出现于同种粘蛋白的表面,且抗原决定簇均为糖链结构,但有不同的肿瘤特异性,因此可作为不同的肿瘤标志物。
4.肿瘤标志物糖类抗原199(ca19-9)是一种黏蛋白型的糖类蛋白,是细胞膜上的糖脂质,分子量大于1000kd,因其由鼠单克隆抗体116ns19-9识别而命名,是迄今为止报道的对胰腺癌敏感性最高的肿瘤标志物。ca19-9的增高多提示有胰腺炎、肝硬化、糖尿病、消化道肿瘤的可能。在血清中它以唾液粘蛋白形式存在,分布于正常胎儿胰腺、胆囊、肝、肠和正常成年人胰腺、胆管上皮等处,是存在于血液循环的胃肠道肿瘤相关抗原。ca19-9在正常胰,胆管细胞,胃,结肠和唾液腺上皮细胞均可表达,血清正常值小于37u/ml。
5.ca19-9与ca50的抗原决定簇结构非常类似,仅仅多了一个岩藻糖结构(lewsi阳性人群特有结构),可分布与正常人的胰腺、胆管上皮等处。当导管上皮细胞发生癌变时,一些调控黏蛋白表达的基因发生活化,促使ca19-9表达明显升高。此外,分泌ca19-9过程中,因为胰腺小导管被肿瘤细胞阻塞,使得ca19-9逸出癌灶,进入血液当中,导致胰腺癌患者血清ca19-9浓度大幅升高。糖类抗原ca19-9与糖类抗原ca242为消化系统较为敏感的肿瘤标志物,对胰腺癌敏感性最好。目前认为ca19-9在胰腺癌诊断、放化疗疗效评估、预后评估、总生存期判断等方面有重要的临床价值。此外,ca19-9对胆管癌、结直肠癌等消化系统肿瘤也具有较高的诊断价值。
6.目前在临床实验室检测ca19-9的方法主要是放射免疫分析(ria)、免疫比浊法、酶联免疫吸附分析(elisa)、时间分辨荧光免疫分析和化学发光技术,其中ria必须用放射性元素标记,检测设备复杂昂贵,其放射性元素的半衰期短,不能长期保存,检测结果不稳定,同时存在放射性污染也给实验操作人员带来了伤害;酶免疫分析法灵敏度低,影响因素较多,易造成假阴性和假阳性。其中化学发光技术兴起于上个世纪80年代,是继酶联免疫技术和放射性免疫技术之后发展起来的新兴技术,由于其高灵敏度、高特异性,同时方法简便、
快速,标记结合物稳定,相对时间分辨荧光免疫法分析成本低廉、操作简便,无放射性同位素损伤和污染等特点,得到了飞速发展。
7.目前,国内用于检测ca19-9的单克隆抗体基本自外国采购,在活性、临床特异性上都存在缺陷。
8.鉴于此,特提出本发明。
技术实现要素:
9.本发明的目的在于提供一种抗ca19-9的抗体及其应用和检测试剂盒。该抗体对ca19-9具有较好的检测特异性以及结合活性,能够用于检测样本ca19-9,具有较好的灵敏度和特异性,本发明为ca19-9的检测和以ca19-9为标志物的相关肿瘤的诊断或辅助诊断提供了更丰富的抗体选择。
10.本发明是这样实现的:
11.一方面,本发明提供一种抗ca19-9的抗体或其功能性片段,所述抗体或其功能性片段具有如下互补决定区:
12.cdr-vh1:g-f-x1-f-s-x2-a-w-m-x3;其中:x1是t或s;x2是n或d;x3是d或e;
13.cdr-vh2:e-x1-g-n-k-x2-n-n-h-a-t-y-y-a-x3-s-x4-k-g;其中:x1是i或l;x2是a或g;x3是e或d;x4是l、v或i;
14.cdr-vh3:x1-t-x2-f-a-y;其中:x1是s或t;x2是n、q或r;
15.cdr-vl1:k-a-s-q-d-x1-n-x2-y-x3-s;其中:x1是i、v或l;x2是s或t;x3是i、v或l;
16.cdr-vl2:r-x1-n-r-x2-x3-d;其中:x1是g或a;x2是l、v或i;x3是l、v或i;
17.cdr-vl3:x1-q-y-d-e-x2-p-r;其中:x1是l、v或i;x2是y或f。
18.本发明提供的抗ca19-9的抗体具有上述的互补决定区结构,其能够特异性结合ca19-9,对ca19-9具有较高的活性,用于检测ca19-9,具有较好的灵敏度和特异性。该抗体可用于诊断或辅助诊断以ca19-9为标志物的相关肿瘤,例如胰腺癌、胆管癌、结肠癌和直肠癌等。本发明为ca19-9的检测和以ca19-9为标志物的相关肿瘤的诊断或辅助诊断提供更丰富的抗体选择。
19.在可选的实施方式中,cdr-vh1中,x2是n;cdr-vh2中,x1是l;cdr-vh3中,x1是s;cdr-vl1中,x2是t;cdr-vl2中,x1是g;cdr-vl3中,x2是y。
20.通过进一步地的创造性劳动,发现当cdr-vh1中,x2是n;cdr-vh2中,x1是l;cdr-vh3中,x1是s;cdr-vl1中,x2是t;cdr-vl2中,x1是g;cdr-vl3中,x2是y时,该抗体表现出更好的结合活性。
21.在可选的实施方式中,cdr-vh1中,x1是t。
22.在可选的实施方式中,cdr-vh1中,x1是s。
23.在可选的实施方式中,cdr-vh1中,x3是d。
24.在可选的实施方式中,cdr-vh1中,x3是e。
25.在可选的实施方式中,cdr-vh2中,x2是a。
26.在可选的实施方式中,cdr-vh2中,x2是g。
27.在可选的实施方式中,cdr-vh2中,x3是e。
28.在可选的实施方式中,cdr-vh2中,x3是d。
29.在可选的实施方式中,cdr-vh2中,x4是l。
30.在可选的实施方式中,cdr-vh2中,x4是v。
31.在可选的实施方式中,cdr-vh2中,x4是i。
32.在可选的实施方式中,cdr-vh3中,x2是n。
33.在可选的实施方式中,cdr-vh3中,x2是q。
34.在可选的实施方式中,cdr-vh3中,x2是r。
35.在可选的实施方式中,cdr-vl1中,x1是i。
36.在可选的实施方式中,cdr-vl1中,x1是v。
37.在可选的实施方式中,cdr-vl1中,x1是l。
38.在可选的实施方式中,cdr-vl1中,x3是i。
39.在可选的实施方式中,cdr-vl1中,x3是v。
40.在可选的实施方式中,cdr-vl1中,x3是l。
41.在可选的实施方式中,cdr-vl2中,x2是i。
42.在可选的实施方式中,cdr-vl2中,x2是v。
43.在可选的实施方式中,cdr-vl2中,x2是l。
44.在可选的实施方式中,cdr-vl2中,x3是l。
45.在可选的实施方式中,cdr-vl2中,x3是v。
46.在可选的实施方式中,cdr-vl2中,x3是t。
47.在可选的实施方式中,cdr-vl3中,x1是l。
48.在可选的实施方式中,cdr-vl3中,x1是v。
49.在可选的实施方式中,cdr-vl3中,x1是i。
50.在可选的实施方式中,所述抗体或其功能性片段的各互补决定区选自如下突变组合1-65中的任意一种:
51.[0052][0053]
在可选的实施方式中,cdr-vh1中,x2是n;cdr-vh2中,x1是l;cdr-vh3中,x1是s;cdr-vl1中,x2是t;cdr-vl2中,x1是g;cdr-vl3中,x2是y。
[0054]
在可选的实施方式中,所述抗体或其功能性片段的各互补决定区选自如下突变组合66-72中的任意一种:
[0055][0056][0057]
在可选的实施方式中,所述抗体包括序列依次如seq id no:1-4所示的轻链骨架区fr1-l、fr2-l、fr3-l及fr4-l,和/或,序列依次如seq id no:5-8所示的重链骨架区fr1-h、fr2-h、fr3-h及fr4-h。
[0058]
通常情况下,重链可变区(vh)和轻链的可变区(vl)可由以下编号的cdr与fr按如下组合排列连接获得:fr1-cdr1-fr2-cdr2-fr3-cdr3-fr4。
[0059]
需要说明的是,在其他的实施例中,本发明提供的抗体或其功能性片段的各骨架区氨基酸序列可以与上述对应骨架区(seq id no:1、2、3、4、5、6、7或8)具有至少80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同源性。
[0060]
在可选的实施方式中,所述抗体还包含恒定区。
[0061]
在可选的实施方式中,所述恒定区选自igg1、igg2、igg3、igg4、iga、igm、ige和igd中的任意一者的恒定区。
[0062]
在可选的实施方式中,所述恒定区的种属来源为绵羊、山羊、牛、马、乳牛、猪、大鼠、狗、猫、兔、骆驼、驴、小鼠、鹿、貂、鸭、鹅、火鸡、斗鸡、鸡或人。
[0063]
在可选的实施方式中,所述恒定区来源于小鼠。
[0064]
在可选的实施方式中,所述恒定区的轻链恒定区序列如seq id no:9所示,所述恒定区的重链恒定区序列如seq id no:10所示。
[0065]
在可选的实施方式中,所述功能性片段选自所述抗体的f(ab’)2、fab、scfv、fab’和fv中的任意一种。
[0066]
上述抗体的功能性片段通常具有与其来源抗体相同的结合特异性。本领域技术人员根据本发明记载的内容容易理解到,上述抗体的功能性片段可以通过比如酶消化的方法(包括胃蛋白酶或木瓜蛋白酶)和/或通过化学还原分裂二硫键的方法获得。在本发明公开了完整抗体的结构基础上,本领域技术人员容易获得上述的功能性片段。
[0067]
上述抗体的功能性片段还可以通过也是本领域技术人员所知的重组遗传学技术或通过例如自动肽合成仪,比如applied biosystems等销售的自动肽合成仪合成获得。
[0068]
另一方面,本发明提供如上任一项所述的抗ca19-9的抗体或其功能性片段在制备用于肿瘤的诊断或辅助诊断的试剂或试剂盒中的应用,所述肿瘤的标志物包括ca19-9。
[0069]
本发明提供的抗体可以用于检测ca19-9,因此,其可用于检测以ca19-9为标志物的相关肿瘤的诊断或辅助诊断。上述肿瘤包括但不限于胰腺癌、胆管癌、结肠癌和直肠癌。
[0070]
本领域技术人员知晓胰腺癌、胆管癌、结肠癌和直肠癌的标志物之一是ca19-9,但基于本领域技术人员的常识以及本发明抗体对ca19-9的特异性结合能力,本发明的抗体可以用于检测任何以ca19-9为标志物的肿瘤。因此,将本发明提供的抗体用于其他以ca19-9为标志物之一的相关肿瘤也是属于本发明的保护范围。
[0071]
另一方面,本发明提供用于以ca19-9作为标志物的相关肿瘤的诊断或辅助诊断的试剂或试剂盒,其包括如上任一项所述的抗ca19-9的抗体或其功能性片段。
[0072]
另一方面,本发明提供一种检测ca19-9的试剂或试剂盒,其包括如上任一项所述的抗ca19-9的抗体或其功能性片段。
[0073]
在可选的实施方式中,上述试剂或试剂盒中所述抗体或其功能性片段标记有可被检测的标记物。
[0074]
可被检测的标记物是指具有能够被肉眼直接观察或被仪器检测或探测到的特性例如发光、显色、放射性等特性的一类物质,通过该特性可以实现对相应目标物的定性或定量检测。
[0075]
在可选的实施方式中,所述可被检测的标记物包括但不限于荧光染料、催化底物显色的酶、放射性同位素、化学发光试剂和纳米颗粒类标记物。
[0076]
在实际的使用过程中,本领域技术人员可以根据检测条件或实际需要选择合适的标记物,无论使用何种标记物,其均属于本发明的保护范围。
[0077]
在可选的实施方式中,所述荧光染料包括但不限于荧光素类染料及其衍生物(例如包括但不限于异硫氰酸荧光素(fitc)羟基光素(fam)、四氯光素(tet)等或其类似物)、罗丹明类染料及其衍生物(例如包括但不限于红色罗丹明(rbitc)、四甲基罗丹明(tamra)、罗丹明b(tritc)等或其类似物)、cy系列染料及其衍生物(例如包括但不限于cy2、cy3、cy3b、cy3.5、cy5、cy5.5、cy3等或其类似物)、alexa系列染料及其衍生物(例如包括但不限于alexafluor350、405、430、488、532、546、555、568、594、610、33、647、680、700、750等或其类似物)和蛋白类染料及其衍生物(例如包括但不限于藻红蛋白(pe)、藻蓝蛋白(pc)、别藻蓝蛋白(apc)、多甲藻黄素-叶绿素蛋白(precp)等)。
[0078]
在可选的实施方式中,所述催化底物显色的酶包括但不限于辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶、葡萄糖氧化酶、碳酸酐酶、乙酰胆碱酯酶以及6-磷酸葡萄糖脱氧酶。
[0079]
在可选的实施方式中,所述放射性同位素包括但不限于
212
bi、
131
i、
111
in、
90
y、
186
re、
211
at、
125
i、
188
re、
153
sm、
213
bi、
32
p、
94
mtc、
99
mtc、
203
pb、
67
ga、
68
ga、
43
sc、
47
sc、
110
min、
97
ru、
62
cu、
64
cu、
67
cu、
68
cu、
86
y、
88
y、
121
sn、
161
tb、
166
ho、
105
rh、
177
lu、
172
lu和
18
f。
[0080]
在可选的实施方式中,所述化学发光试剂包括但不限于鲁米诺及其衍生物、光泽精、甲壳动物荧光素及其衍生物、联吡啶钌及其衍生物、吖啶酯及其衍生物、二氧环乙烷及其衍生物、洛粉碱及其衍生物和过氧草酸盐及其衍生物。
[0081]
在可选的实施方式中,所述纳米颗粒类标记物包括但不限于纳米颗粒、胶体、有机纳米颗粒、磁性纳米颗粒、量子点纳米颗粒和稀土络合物纳米颗粒。
[0082]
在可选的实施方式中,所述胶体包括但不限于胶体金属、分散型染料、染料标记的微球和乳胶。
[0083]
在可选的实施方式中,所述胶体金属包括但不限于胶体金、胶体银和胶体硒。
protocols in molecular biology)》(f.m.ausubel等人编,1987);《pcr:聚合酶链反应(pcr:the polymerase chain reaction)》(mullis等人编,1994);以及《当代免疫学方法(current protocols in immunology)》(j.e.coligan等人编,1991),所述文献中的每个文献均通过引用明确并入本文中。
[0094]
以下结合实施例对本发明的特征和性能作进一步的详细描述。
[0095]
实施例1
[0096]
本实施例中限制性内切酶、prime star dna聚合酶购自takara公司。magextractor-rna提取试剂盒购自toyobo公司。bd smart
tm
race cdna amplification kit试剂盒购自takara公司。pmd-18t载体购自takara公司。质粒提取试剂盒购自天根公司。引物合成和基因测序由invitrogen公司完成。
[0097]
1重组质粒的构建
[0098]
(1)抗体基因制备
[0099]
从分泌抗ca19-9抗体的杂交瘤细胞株中提取mrna,通过rt-pcr方法获得dna产物,该产物用rtaq dna聚合酶进行加a反应后插入到pmd-18t载体中,转化到dh5α感受态细胞中,长出菌落后分别取heavy chain及light chain基因克隆各4个克隆,送基因测序公司进行测序。
[0100]
(2)抗体可变区基因的序列分析
[0101]
将上述测序得到的基因序列放在imgt抗体数据库中进行分析,并利用vnti11.5软件进行分析确定重链和轻链引物对扩增出的基因都是正确的,其中light chain扩增出的基因片段中,vl基因序列为324bp,属于vkii基因家族,其前方有57bp的前导肽序列;heavy chain引物对扩增出的基因片段中,vh基因序列为345bp,属于vh1基因家族,其前方有57bp的前导肽序列。
[0102]
(3)重组抗体表达质粒的构建
[0103]
pcdna
tm
3.4vector为构建的重组抗体真核表达载体,该表达载体已经引入hindiii、bamhi、ecori等多克隆酶切位点,并命名为pcdna3.4a表达载体,后续简称3.4a表达载体;根据上述pmd-18t中抗体可变区基因测序结果,设计该抗体的vl和vh基因特异性引物,两端分别带有hindiii、ecori酶切位点和保护碱基,通过pcr扩增方法扩出0.73kb的light chain基因片段和1.4kb的heavy chain基因片段。
[0104]
heavy chain和light chain基因片段分别采用hindiii/ecori双酶切,3.4a载体采用hindiii/ecori双酶切,将片段和载体纯化回收后heavy chain基因和light chain基因分别连接3.4a表达载体中,分别得到heavy chain和light chain的重组表达质粒。
[0105]
2稳定细胞株筛选
[0106]
(1)重组抗体表达质粒瞬时转染cho细胞,确定表达质粒活性
[0107]
质粒用超纯水稀释至40μg/100μl,调节cho细胞1.43
×
107cells/ml于离心管中,100μl质粒与700μl细胞混合,转入电转杯,电转,第3、5、7天取样计数,第7天收样检测。
[0108]
包被液(主要成分nahco3)稀释羊抗鼠igg 1ug/ml进行微孔板包被,每孔100μl,4℃过夜;次日,洗涤液(主要成份na2hpo4 nacl)清洗2次,拍干;加入封闭液(20%bsa 80%pbs),每孔120μl,37℃,1h,拍干;加入稀释后的细胞上清,100μl/孔,37℃,60min;甩掉板内液体,拍干;加入20%鼠阴性血封闭,每孔120μl,37℃,1h;甩掉板内液体,拍干,加入稀释的
ca199人腹水,每孔100ul,37℃,40min;洗涤液清洗5次,拍干;加入标记hrp的ca199单克隆抗体,每孔100ul,37℃,30min;加入显色液a液(50ul/孔),加入显色液b液(50ul/孔),10min;加入终止液,50ul/孔;酶标仪上450nm(参考630nm)处读od值。
[0109]
结果显示细胞上清稀释1000倍后反应od仍大于1.0,未加细胞上清孔反应od小于0.1,表明质粒瞬转后产生的抗体对ca199人腹水有活性。
[0110]
(2)重组抗体表达质粒线性化
[0111]
准备下述试剂:buffer 50μl、dna100μg/管、puvⅰ酶10μl、无菌水补至500μl,37℃水浴酶切过夜;先用等体积酚/氯仿/异戊醇(下层)25:24:1,再用氯仿(水相)依次进行抽提;0.1倍体积(水相)3m醋酸钠和2倍体积乙醇冰上沉淀,70%乙醇漂洗沉淀,去除有机溶剂,待乙醇挥发完全用适量的灭菌水进行复融,最后进行浓度的测定。
[0112]
(3)重组抗体表达质粒稳定转染,加压筛选稳定细胞株
[0113]
质粒用超纯水稀释至40μg/100μl,调节cho细胞1.43
×
107cells/ml于离心管中,100μl质粒与700μl细胞混合,转入电转杯,电转,次日计数;25μmol/l msx 96孔加压培养约25天。
[0114]
显微镜下观察标记长有细胞的克隆孔,并记录汇合度;取培养上清,送样检测;挑选抗体浓度、相对浓度高的细胞株转24孔,3天左右转6孔;3天后保种批培,调整细胞密度0.5
×
106cells/ml,2.2ml进行批培养,细胞密度0.3
×
106cells/ml,2ml进行保种;7天6孔批培上清送样检测,挑选抗体浓度及细胞直径较小的细胞株转tpp保种传代。
[0115]
3重组抗体生产
[0116]
(1)细胞扩培
[0117]
细胞复苏之后先在125ml规格的摇瓶中培养,接种体积为30ml,培养基为100%dynamis培养基,放置于转速120r/min,温度为37℃,二氧化碳为8%的摇床中。培养72h,以50万cells/ml接种密度接种扩培,扩培体积根据生产需求进行计算,培养基为100%dynamis培养基。之后每72h扩培一次。当细胞量满足生产需求时,严格控制接种密度为50万cells/ml左右进行生产。
[0118]
(2)摇瓶生产及纯化
[0119]
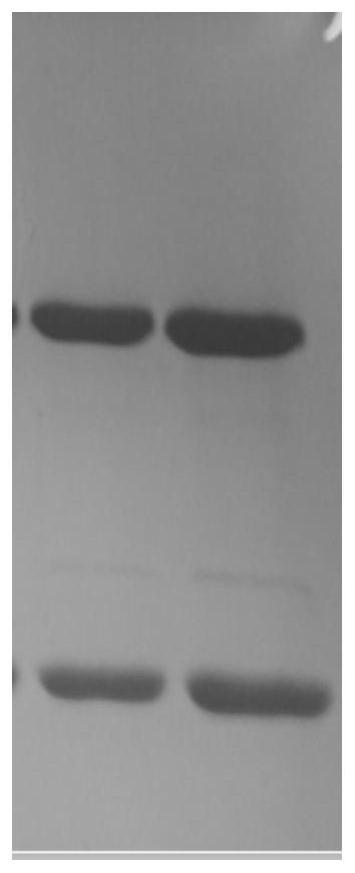
摇瓶参数:转速120r/min,温度为37℃,二氧化碳为8%。流加补料:在摇瓶中培养至72h时开始每天补料,hyclonetm cell boosttm feed 7a每天流加初始培养体积的3%,feed 7b每天流加量为初始培养体积的千分之一,一直补到第12天(第12天补料)。葡萄糖在第六天补加3g/l。第13天收样。用proteina亲和层析柱进行亲和纯化。取4μg纯化的抗体进行还原性sds-page,4μg外来对照抗体作为对照,电泳图如下图1所示,在还原性sds-page后显示两条带,1条mr为50kd(重链,seq id no:14),另一条mr为28kd(轻链,seq id no:13)。
[0120]
实施例2
[0121]
抗体的性能检测
[0122]
(1)实施例1抗体及其突变体的活性检测
[0123]
分析通过实施例1的抗体(wt),其重链可变区氨基酸序列如seq id no:12所示,其中,各互补决定区的氨基酸序列如下:
[0124]
cdr-vh1:g-f-s(x1)-f-s-n(x2)-a-w-m-e(x3);
[0125]
cdr-vh2:e-l(x1)-g-n-k-a(x2)-n-n-h-a-t-y-y-a-d(x3)-s-i(x4)-k-g;
[0126]
cdr-vh3:s(x1)-t-r(x2)-f-a-y;
[0127]
其轻链可变区氨基酸序列如seq id no:11所示,其中,轻链的各互补决定区的氨基酸序列如下:
[0128]
cdr-vl1:k-a-s-q-d-l(x1)-n-t(x2)-y-l(x3)-s;
[0129]
cdr-vl2:r-g(x1)-n-r-l(x2)-i(x3)-d;
[0130]
cdr-vl3:i(x1)-q-y-d-e-y(x2)-p-r。
[0131]
在实施例1的抗ca19-9抗体(wt)基础上,通过大量的分析,在互补决定区中对于抗体活性有关的位点进行突变,其中,x1、x2、x3、x4均为突变位点。见下表1。
[0132]
表1与抗体活性有关的突变位点
[0133][0134]
对表1中的抗体结合活性检测:
[0135]
包被液(主要成分nahco3)稀释羊抗鼠igg 1μg/ml进行微孔板包被,每孔100μl,4℃过夜;次日,洗涤液(主要成份na2hpo4 nacl)清洗2次,拍干;加入封闭液(20%bsa 80%pbs),每孔120μl,37℃,1h,拍干;加入稀释后的纯化抗体,100μl/孔,37℃,60min;甩掉板内液体,拍干,加入20%鼠阴性血封闭,每孔120μl,37℃,1h;甩掉板内液体,拍干,加入稀释的ca19-9人腹水(来自临床样本),每孔100μl,37℃,40min;洗涤液清洗5次,拍干;加入标记hrp的ca19-9单克隆抗体(同上述纯化抗体),每孔100μl,37℃,30min;加入显色液a液(50μl/孔,含2.1g/l柠檬酸、12.25g/l柠檬酸、0.07g/l乙酰苯胺和0.5g/l过氧化脲),加入显色液b液(50μl/孔,含1.05g/l柠檬酸、0.186g/ledta
·
2na、0.45g/l tmb和0.2ml/l浓hcl),10min;加入终止液(50μl/孔,含0.75g/edta
·
2na和10.2ml/l浓h2so4);酶标仪上450nm(参考630nm)处读od值。结果见下表2。
[0136]
表2wt抗体及其突变体的活性数据
[0137][0138][0139]
注:
“-”
代表没活性。
[0140]
从表1数据可以看出,相较于突变5-突变7,wt以及突变1-突变4都具有较好的结合活性,其中,突变1的结合活性最佳。
[0141]
(2)抗体及其突变体的活性检测
[0142]
(a)在突变1的基础上,对其他位点进行突变,各突变的序列见下表3。
[0143]
表3与抗体活性有关的突变位点
[0144]
[0145][0146]
活性分析:按照上述方式,对表3中抗体的活性进行检测。结果见下表4。
[0147]
表4活性检测数据
[0148]
[0149]
[0150]
[0151][0152]
从表4数据可以看出,突变1及其系列突变体对ca19-9都具有较高的结合活性,说明在突变1的基础上,按表3的突变方式突变得到的抗体均能取得针对ca19-9的较高结合活性。
[0153]
(b)在wt的基础上,对其他位点进行突变,并检测各突变体的活性,各突变的序列见下表5,对应的活性数据见表6。
[0154]
表5以wt为骨架进行的突变
[0155][0156]
表6wt抗体及其突变体的活性检测结果
[0157]
抗体浓度(ng/ml)12.56.253.1251.5630.3910wt1.9180.7720.3650.1760.0760.067wt 11.8460.8670.3910.1980.0940.054wt 21.8770.7740.3980.2020.0970.053wt 31.8220.8360.3770.1910.0730.051wt 41.8980.7330.3550.2040.0690.050wt 51.8520.7060.3190.1690.0610.051wt 61.8940.7330.3920.1990.1030.052
[0158]
从表6数据可以看出,wt及其系列突变体也都具有较好的结合活性,说明在wt的基础上,根据表5的突变方式突变,得到的突变体均具有极好的结合活性。
[0159]
(3)裸抗稳定性考核
[0160]
将上述抗体置于4℃(冰箱)、-80℃(冰箱)、37℃(恒温箱)放置21天,取7天、14天、21天样品进行状态观察,并对21天样品进行活性检测,结果显示三种考核条件下抗体放置
21天均未见明显蛋白状态变化,活性也未随考核温度的升高呈明显下降趋势,说明上述抗体稳定。下表7为突变1抗体考核21天的酶免活性检测od结果。
[0161]
表7
[0162]
抗体浓度(ng/ml)12.53.12504℃,21天样品1.9360.7060.073-80℃,21天样品1.9590.7280.06337℃,21天样品1.9580.8830.066
[0163]
(4)性能评价
[0164]
将上述实施例的抗体自身配对使用,采用双抗体夹心法,标记抗体和包被抗体为相同的抗体,用碱性磷酸酶作为标记物,在化学发光平台测试上述抗体的性能。使用仪器:luminoskan,反应模式:1.20μl样本 70μl bio(生物素)标记的抗体(抗体浓度0.25μg/ml) 70μl ap(碱性磷酸酶)标记的抗体(抗体浓度1μg/ml),在37℃条件下反应10min;2.加入40μl链霉亲和素标记的磁珠溶液,浓度0.05%,37℃下反应10min,用pbst洗6次;3.加入100μl ap(碱性磷酸酶)底物,37℃下反应5min。检测300份医院定值标本,突变1抗体检测结果与医院定值相关性95.4%,而wt检测结果与医院定值相关性93.7%。用不同样品浓度下测试的发光值做相关性曲线,具体结果如下表8所示:
[0165]
表8
[0166][0167]
可以看出,采用本发明实施例提供的抗体在实际检测中具有较高的相关性,能够取得较为准确的检测结果。
[0168]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。