治疗心理和脑部疾病的方法
1.联邦基金声明
2.本发明是在美国国立卫生研究院授予的授权号为mh086828的政府支持下完成的。政府对本发明享有一定的权利。
3.相关申请的交叉引用
4.本国际申请根据美国法典第35卷第119节(e)款要求2019年8月13日提交的序号为62/886,090的美国临时申请的优先权,将该申请的整体并入此文。
技术领域
5.本发明涉及精神疾病领域。更具体地,本发明涉及通过操纵脑部的血清素能系统(serotonergic system)来治疗心理和脑部疾病的方法。
背景技术:
6.数千年来,迷幻物质一直被人类用于精神和药用目的(1)。临床研究最近开始提供证据支持它们作为许多神经精神疾病治疗剂的用途,包括作为强迫症、创伤后应激障碍和难治性抑郁症(trd)的治疗剂(2)。
7.例如,最近显示将光盖伞素(psilocybin)单独给药可在1周后显著改善患者报告的抑郁评分,该改善持续长达6个月(3)。自那以后,美国食品及药物管理局(fda)已将光盖伞素列入抑郁症治疗的快速通道,并且正在进行其他临床试验。
8.虽然在其他方面是安全的(4),但光盖伞素引起的对感官知觉和意识的改变是其广泛使用的一个重大障碍,需要在给药期间在住院环境中进行6-8小时昂贵的全程心理支持。如果可以在不损害抗抑郁反应的情况下阻断迷幻反应,这些障碍将大大减少。
9.无论是在药物开发方面还是在提高社会接受程度方面,通过更好地理解迷幻药物治疗效果的机制,将促进迷幻药物作为治疗神经精神疾病药物的发展。目前,迷幻药物的治疗效果还没有在神经精神疾病的临床前动物模型中得到充分验证。特别地,尚缺乏关于光盖伞素有益作用所需的关键血清素受体的证据。
10.光盖伞辛是光盖伞素的活性代谢物,是几乎所有5-羟色胺受体(5-htr,血清素受体)的强效激动剂,亲和力范围在3-500nm之间(5),与血清素相当。在人体内,光盖伞素引起的知觉变化的强度与血清素2a受体(5-ht2ar)的激活相关(6)。用酮色林(ketanserin)阻断5-ht2r可显著减弱自我报告的知觉扭曲(7)。
11.然而,人们普遍认为,光盖伞素引起的意识变化对抗抑郁反应至关重要(2、8)。例如,在健康受试者中,光盖伞素引起的处理负面情绪刺激的急性变化被酮色林阻止(9)。然而,光盖伞素可能通过快速激活其他一些关键的5-htr来缓解抑郁症状。
12.人类患抑郁症是遗传易感性和环境因素(如应激)共同作用的结果。快感缺乏(anhedonia),即无法从之前令人愉快的活动中体验快乐,是抑郁症的核心症状。与人类抑郁症一样,各种形式的慢性应激会引起啮齿动物出现快感缺乏状态,其特征是对之前奖励刺激的行为反应减弱(10)。重要地,应激动物对奖励刺激的反应可以通过施用对人类具有
抗抑郁功效的化合物来恢复,分别包括急性给药的速效化合物(如氯胺酮,ketamine)和长期给药的慢效化合物(如ssri类药物)(10)。
13.因此,本领域需要改进对心理和脑部疾病和障碍的治疗。本发明满足了本领域的这种长期需要和愿望。
技术实现要素:
14.本发明涉及一种预防或治疗心理疾病的方法。该方法包括将血清素激动剂与血清素受体2拮抗剂联合给药的步骤,其中激动剂与拮抗剂分开、依次或同时给药。
15.本发明还涉及另一种预防或治疗心理疾病的方法。该方法包括将血清素受体激动剂与血清素受体2拮抗剂联合给药的步骤,其中激动剂与拮抗剂分开、依次或同时给药。
附图说明
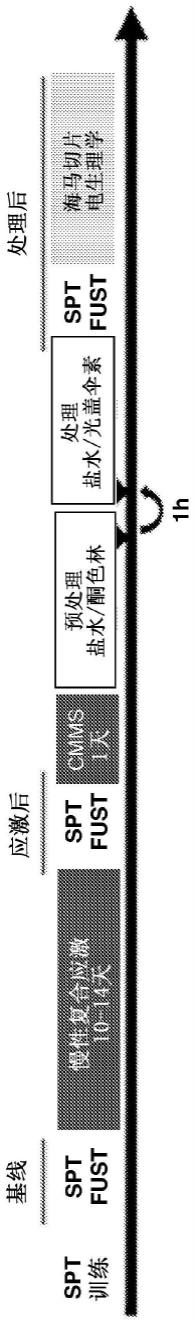
16.图1a-1c示出了光盖伞素对慢性应激后享乐行为的恢复不受酮色林的影响。图1a:实验时间表,说明了与慢性复合应激(cmms)和药物处理相关的享乐行为在何时测量。图1b:在所有处理组中与基线相比,慢性复合应激显著降低蔗糖偏好(sp):载体-载体(灰色;p=0.0012;n=12)、酮色林-载体(蓝色;p=0.0012;n=6)、载体-光盖伞素(黄色;p=0.0012;n=13),酮色林-光盖伞素(绿色;p=0.0012;n=7)。无论动物是用酮色林(2mg/kg;p=0.041)还是用载体对照(p=0.0012)作预处理,与慢性复合应激后的值相比,用光盖伞素处理(1mg/kg,i.p.)均显著增加了蔗糖偏好。与载体一起注射(p=0.075)或单独注射酮色林(p=0.87;n=6)对慢性复合应激后的蔗糖偏好均没有显著影响。三因素重复测量方差分析显示了应激的显著影响(f
2,68
=55.00,p《0.0001),以及应激
×
光盖伞素的显著相关性(f
2,68
=4.64,p=0.013)。图1c:与基线相比,慢性复合应激显著降低雌性尿液偏好:载体-载体(p=0.013;n=6)、酮色林-载体(p=0.0012;n=4)、载体-光盖伞素(p=0.0012;n=5)、酮色林-光盖伞素(p=0.0012;n=4)。无论动物是用酮色林(p=0.0024)还是载体(p=0.0012)预处理,与慢性复合应激后的值相比,用光盖伞素处理均显著增加了雌性尿液气味偏好。与载体一起注射(p=0.43)或单独注射酮色林(p=0.072;n=4)对慢性复合应激后的雌性尿液偏好均没有显著影响。应激显著降低了所有组的雌性尿液偏好(f
2,30
=43.41,p《0.0001),三因素重复测量方差分析显示应激
×
光盖伞素之间存在显著的相关性(f
2,30
=4.26,p《0.024)。图的示意条代表组的平均值
±
sem。所报告的事后比较使用holm-sidak方法进行校正。*p《0.05,**p《0.005;ns,不显著。
17.图2a-2d示出了光盖伞素增强慢性复合应激后海马的ta-ca1突触。图2a:在用dnqx(50μm)及apv(80μm)进行内洗以分离ampa-和nmdar-介导的组分后,在无镁离子(mg
2
)的人工脑脊液(acsf)中记录的来自每组一个海马切片的单个刺激强度的示例性场兴奋性突触后电位(fepsp)。图2b:与仅给予载体(灰色,n=12)或酮色林(蓝色,n=7)的应激小鼠相比,施加cmms后用光盖伞素处理的小鼠具有更高的ampa:nmda比率,无论它们是用酮色林(绿色,n=7;p=0.0002)还是用载体(黄色,n=13;p=0.0003)预处理。双因素重复测量方差分析显示了光盖伞素的显著影响(f
1,34
=34.79,p《0.0001)。图2c:光盖伞素增加了fepsp的ampa:fv比率(双因素方差分析:f
1,34
=4.378,p=0.044)。图2d:用光盖伞素处理不会改变fepsp的nmda:fv比率(双因素方差分析:f
1,34
=2.077,p=0.16)。每只动物的ampa:nmda、
ampa:fv和nmda:fv与组平均值
±
sem一起显示。*p《.05,**p《.005,***p《.0005。
18.图3示出了光盖伞素对抗应激的动物没有影响。抗应激的小鼠被定义为在14天慢性复合应激后表现出高蔗糖偏好(》65%)的小鼠。注射光盖伞素(1mg/kg,ip)对抗应激动物(n=3,红色)的蔗糖偏好没有影响,注射载体(n=7,蓝色)也没有影响。双因素重复测量方差分析:f
1,14
=0.14,p=0.72。蔗糖偏好表示为来自每只动物的数据叠加的组平均值
±
sem。
19.图4a-4b示出了酮色林的注射增加了自主活动。在第二次注射光盖伞素(1mg/kg)或等体积的盐水载体后,记录动物90分钟。分析视频以量化每组的总移动距离(cm)和移动时间(s):载体-载体(灰色,n=7)、载体-光盖伞素(黄色,n=7)、酮色林-载体(蓝色,n=6),酮色林-光盖伞素(绿色,n=7)。图4a显示,光盖伞素
×
酮色林(f
1,23
=1.47,p=0.24)对总移动距离不存在显著的相关性,但酮色林对总移动距离具有显著影响(f
1,23
=6.14,p=0.021)。图4b显示,光盖伞素
×
酮色林(f
1,23
=0.40,p=0.53)对平均移动时间不存在显著的相关性,但酮色林对平均移动时间有显著影响(f
1,23
=4.53,p=0.044)。图的示意条代表组的平均值
±
sem。*p《0.05。
具体实施方式
20.本文所用的术语“一个(a)”或“一个(an)”,当在权利要求书和/或说明书中与术语“包含(comprising)”一起使用时,可能意味着“一个”,但它也与“一个或多个”、“至少一个”和“一个或一个以上”的含义一致。本发明的一些实施例可能由或基本上由本发明的一个或多个要素、方法步骤和/或方法组成。按照设想,本发明描述的任何方法可以结合本发明描述的任何其他方法进行实施。
21.本文所用的术语“或”在权利要求书中是指“和/或”,除非明确表明仅指替代方案或替代方案相互排斥,尽管本公开支持仅指替代方案和“和/或”的定义。
22.本文所用的术语“包含(comprise)”及其变体,如“包含comprises”和“包含comprising”将被理解为意味着包含规定的项目、要素或步骤,或者包含一组项目、要素或步骤,但是不排除任何其他项目、要素或步骤,或者任何其他一组项目、要素或步骤,除非上下文另有要求。类似地,“另一个(another)”或“另外的(other)”可能指至少另一个或者另外多个相同或不同的权利要求要素或其组成部分。
23.在本发明的一个实施例中,提供了用于预防或治疗心理疾病的方法,包括将血清素激动剂与血清素受体2a拮抗剂联合给药的步骤,其中激动剂与血清素受体2a拮抗剂分开、依次或同时给药。可用的血清素激动剂的代表性例子包括但不限于光盖伞素、光盖伞辛、甲基裸盖伞素(baeocystin)、甲基裸盖伞素脱甲基类似物(norbaeocystin)、麦角乙脲(lisurgide)、麦角乙二胺(lsd)、二甲基色胺或羧基酰胺基色胺、伊博格碱、3,4-亚甲基二氧基甲基苯丙胺(mdma)或促进血清素释放的化合物或其组合。
24.在该实施例的一个优选方面,血清素激动剂是光盖伞素或光盖伞辛或其衍生物。可用的光盖伞素或光盖伞辛衍生物的代表性例子包括但不限于[3-(2-二甲基氨基乙基)-1h-吲哚-4-基]磷酸二氢盐、4-羟基-n,n-二甲基色胺、[3-(2-甲基氨基乙基)-1h-吲哚-4-基]磷酸二氢盐、4-羟基-n-甲基色胺、[3-(氨基乙基)-1h-吲哚-4-基]磷酸二氢盐、4-羟基色胺、[3-(2-三甲基氨基乙基)-1h-吲哚-4-基]磷酸二氢盐或4-羟基-n,n,n-三甲基色胺。
在这方面,光盖伞素或光盖伞辛以来自蘑菇和/或松露(菌核)的提取物的形式存在。此类可用的蘑菇或松露的代表性例子包括但不限于来自光盖伞属(psilocybe)、裸伞属(gymnopilus)、花褶伞属(panaeolus)、灰斑褶菇属(copelandia)、韧伞属(hypholoma)、光柄菇属(pluteus)、丝盖伞属(inocybe)、锥盖伞属(conocybe)、疣孢斑褶菇属(panaeolina)、老伞属(gerronema)、田头菇属(agrocybe)、盔孢伞属(galerina)和/或小菇属(mycena)。更优选地,蘑菇或松露是蓝光盖伞(p.azurescens)、半光盖伞(p.semilanceata)、暗蓝光盖伞(p.cyanescens)、古巴光盖伞(p.cubensis)、亚古巴光盖伞(p.subcubensis)、p.tampanensis、墨西哥光盖伞(p.mexicana)、亚特兰蒂斯光盖伞(p.atlantis)和/或半光盖伞(p.semilanceata)。
[0025]
在该实施例的另一个优选方面,促进血清素释放的化合物是3,4-亚甲基二氧基甲基苯丙胺或其代谢物。可用的3,4-亚甲基二氧基甲基苯丙胺代谢物的代表性例子是3,4-亚甲基二氧基苯丙胺(mda)、4-羟基-3-甲氧基甲基苯丙胺(hmma)、4-羟基-3-甲氧基苯丙胺(hma)、3,4-二羟基苯丙胺(dha)、3,4-亚甲基二氧基苯丙酮(mdp2p)或3,4-亚甲基二氧基-n-羟基苯丙胺(mdoh)。
[0026]
在该实施例中,可用的血清素受体2a拮抗剂的代表性例子包括但不限于mdl-11,939、酮色林、利坦色林、阿坦色林、乙酰丙嗪、米安色林、喹硫平、sb204741、sb206553、sb242084、ly272015、sb243213、布南色林、sb2006、rs102221、奈法唑酮或mdl-100,907。具体地,血清素受体2a拮抗剂也可以是用于或同时拮抗其他血清素受体(例如血清素受体2b或血清素受体2c)的拮抗剂。
[0027]
在该实施例及其各个方面中,可以通过本发明方法治疗的心理疾病的代表性例子包括但不限于抑郁症、精神病性障碍、精神分裂症、精神分裂症样障碍(急性精神分裂症发作)、分裂情感性障碍;双相型障碍i型(躁狂症、躁狂障碍、躁狂抑郁性精神病)、双相型障碍ii型、具有精神病特征的重度抑郁障碍(精神病性抑郁症)、妄想性障碍(妄想症)、共有性精神病性障碍(共有性妄想症)、短暂性精神病性障碍(其他和未指明的反应性精神病)、非特指的精神病(未指明的精神病)、偏执型人格障碍、分裂样人格障碍、分裂型人格障碍、焦虑症、恐慌症、惊恐发作、广场恐惧症、注意力缺陷综合症、经前烦躁症、经前期综合征、注意力缺陷多动障碍(adhd)、注意力不足过动症(add)、神经性厌食症、反社会人格障碍、自闭症、成瘾、回避型人格障碍、双相情感障碍、神经性贪食症、边缘型人格障碍、紧张性精神分裂症、慢性运动或发声抽动障碍、转换障碍、循环性精神病、依赖性人格障碍、精神错乱、痴呆、人格解体障碍、抑郁症、dhat综合征、分离性遗忘症、分离性神游症、分离性身份障碍、分离性障碍、未指明的分离性障碍、情绪障碍症、达科斯塔综合征、恋青少年症(ephobophilia)、暴露癖、广泛性焦虑症、妄想症、疑病症、囤积症、间歇性爆发性障碍、嫉妒、盗窃癖、克鲁弗-布西综合征、孕期精神病、智力低下、偏执狂、蒙克豪森综合征、恐音症、自恋型人格障碍、强迫症、购买癖、器质性人格障碍、恐惧症、偏执型人格障碍、偏执妄想、被动攻击型人格、病态性赌博、病态性说谎、未指明的人格障碍、广泛性发育障碍、异食癖、疼痛障碍、脑炎后综合征、产后抑郁症、创伤后应激障碍、精神病、药物滥用引起的精神障碍、纵火癖、抱怨性妄想、反刍症、精神分裂症、分裂情感性障碍、分裂样人格障碍、分裂型人格障碍、分离焦虑、社交恐惧症、躯体化障碍、躯体妄想、躯体形式障碍、卡普格拉斯综合征、科塔德综合征、甘瑟综合征、抽动秽语综合征、选择性缄默症、戏剧性人格障碍、拔毛癖或未分化躯体形式障碍。可
用于本发明方法的血清素激动剂和血清素受体2拮抗剂为本领域普通技术人员所熟知,因此剂量、给药途径和给药形式(如丸剂、片剂或糖浆剂)都是完全在本领域技术人员的技能范围内。
[0028]
在本发明的另一个实施例中,提供了用于预防或治疗心理疾病的方法,包括将血清素受体激动剂与血清素受体2拮抗剂联合给药的步骤,其中激动剂与拮抗剂分开、依次或同时给药。血清素受体激动剂的代表性例子是血清素受体1b、血清素受体4、血清素受体6或血清素受体7的激动剂。
[0029]
在一方面,血清素受体1b激动剂的代表性例子包括但不限于麦角胺、羟甲唑啉、舒马曲坦、佐米曲普坦、5-羧基酰胺基色胺、cgs-12066a、cp-93,129、cp-94,253、cp-122,288、cp135,807、ru24969、沃替西汀、光盖伞素、光盖伞辛、甲基裸盖伞素、甲基裸盖伞素脱甲基类似物、麦角乙脲(lisurgide)、lsd、二甲基色胺或羧基酰胺基色胺或其组合。在另一方面,血清素受体4激动剂的代表性例子包括但不限于bimu-8、西沙必利、cj-033、ml-10302、莫沙必利、普芦卡必利、伦扎必利、rs-67506、rs-67333、sl65.0155、替加色罗、扎考必利、甲氧氯普胺、舒必利、光盖伞素、光盖伞辛、甲基裸盖伞素、甲基裸盖伞素脱甲基类似物、麦角乙脲(lisurgide)、lsd、二甲基色胺或羧基酰胺基色胺或其组合。在另一方面,血清素受体6激动剂的代表性例子包括但不限于emd 386088、e-6801、way 181187或way 208466。在另一个方面,血清素受体7激动剂的代表性例子包括但不限于5-羧基酰胺基色胺、5-甲氧基色胺、8-oh-dpat、阿立哌唑、as-19、e-55888、e-57431、4-(2-二苯基)-n-(1,2,3,4-四氢萘-1-基)-1-哌嗪己酰胺、4-[2-(甲硫基)苯基]-n-(1,2,3,4-四氢-1-萘基)-1-哌嗪己酰胺、lp-211、msd-5a、n-甲基血清素、n-1,2,3,4-四氢萘-1-基)-4-芳基-1-哌嗪己酰胺、n,n-二甲基色胺、agh-107、ah-494、agh-192、光盖伞素、光盖伞辛、甲基裸盖伞素、甲基裸盖伞素脱甲基类似物、麦角乙脲(lisurgide)、lsd、二甲基色胺或羧基酰胺基色胺或其组合。
[0030]
在一个优选的方面,血清素激动剂是光盖伞素或光盖伞辛的衍生物。光盖伞素或光盖伞辛衍生物的代表性例子包括但不限于[3-(2-二甲基氨基乙基)-1h-吲哚-4-基]磷酸二氢盐、4-羟基-n,n-二甲基色胺、[3-(2-甲基氨基乙基)-1h-吲哚-4-基]磷酸二氢盐、4-羟基-n-甲基色胺、[3-(氨基乙基)-1h-吲哚-4-基]磷酸二氢盐、4-羟基色胺、[3-(2-三甲基氨基乙基)-1h-吲哚-4-基]磷酸二氢盐或4-羟基-n,n,n-三甲基色胺。
[0031]
在该方法的该优选方面,光盖伞素或光盖伞辛以来自蘑菇和/或松露(菌核)的提取物的形式存在。蘑菇或松露可以来自光盖伞属(psilocybe)、裸伞属(gymnopilus)、花褶伞属(panaeolus)、灰斑褶菇属(copelandia)、韧伞属(hypholoma)、光柄菇属(pluteus)、丝盖伞属(inocybe)、锥盖伞属(conocybe)、疣孢斑褶菇属(panaeolina)、老伞属(gerronema)、田头菇属(agrocybe)、盔孢伞属(galerina)和/或小菇属(mycena)。更优选地,蘑菇或松露是蓝光盖伞(p.azurescens)、半光盖伞(p.semilanceata)、暗蓝光盖伞(p.cyanescens)、古巴光盖伞(p.cubensis)、亚古巴光盖伞(p.subcubensis)、p.tampanensis、墨西哥光盖伞(p.mexicana)、亚特兰蒂斯光盖伞(p.atlantis)和/或半光盖伞(p.semilanceata)。
[0032]
在该实施例中,血清素受体2a拮抗剂的代表性例子包括但不限于mdl-11,939、酮色林、利坦色林、阿坦色林、乙酰丙嗪、米安色林、喹硫平、sb204741、sb206553、sb242084、ly272015、sb243213、布南色林、sb200646、rs102221、奈法唑酮或mdl-100,907。血清素受体
2a拮抗剂也可以是用于或同时拮抗其他血清素受体(例如但不限于5血清素受体2b或血清素受体2c)的拮抗剂。
[0033]
在该实施例及其所有方面中,心理疾病的代表性例子选自但不限于抑郁症、精神病性障碍、精神分裂症、精神分裂症样障碍(急性精神分裂症发作)、分裂情感性障碍;双相型障碍i型(躁狂症、躁狂障碍、躁狂抑郁性精神病)、双相型障碍ii型、具有精神病特征的重度抑郁障碍(精神病性抑郁症)、妄想性障碍(妄想症)、共有性精神病性障碍(共有性妄想症)、短暂性精神病性障碍(其他和未指明的反应性精神病)、非特指的精神病(未指明的精神病)、偏执型人格障碍、分裂样人格障碍、分裂型人格障碍、焦虑症、恐慌症、惊恐发作、广场恐惧症、注意力缺陷综合症、经前烦躁症、经前期综合征、注意力缺陷多动障碍(adhd)、注意力不足过动症(add)、神经性厌食症、反社会人格障碍、自闭症、成瘾、回避型人格障碍、双相情感障碍、神经性贪食症、边缘型人格障碍、紧张性精神分裂症、慢性运动或发声抽动障碍、转换障碍、循环性精神病、依赖性人格障碍、精神错乱、痴呆、人格解体障碍、抑郁症、dhat综合征、分离性遗忘症、分离性神游症、分离性身份障碍、分离性障碍、未指明的分离性障碍、情绪障碍症、达科斯塔综合征、恋青少年症(ephobophilia)、暴露癖、广泛性焦虑症、妄想症、疑病症、囤积症、间歇性爆发性障碍、嫉妒、盗窃癖、克鲁弗-布西综合征、孕期精神病、智力低下、偏执狂、蒙克豪森综合征、恐音症、自恋型人格障碍、强迫症、购买癖、器质性人格障碍、恐惧症、偏执型人格障碍、偏执妄想、被动攻击型人格、病态性赌博、病态性说谎、未指明的人格障碍、广泛性发育障碍、异食癖、疼痛障碍、脑炎后综合征、产后抑郁症、创伤后应激障碍、精神病、药物滥用引起的精神障碍、纵火癖、抱怨性妄想、反刍症、精神分裂症、分裂情感性障碍、分裂样人格障碍、分裂型人格障碍、分离焦虑、社交恐惧症、躯体化障碍、躯体妄想、躯体形式障碍、卡普格拉斯综合征、科塔德综合征、甘瑟综合征、抽动秽语综合征、选择性缄默症、戏剧性人格障碍、拔毛癖或未分化躯体形式障碍。
[0034]
给出以下实施例的目的是为了说明本发明的各种实施例,并不意味着以任何方式限制本发明。
[0035]
实施例1
[0036]
方法
[0037]
所有程序均经马里兰大学巴尔的摩动物使用和护理委员会批准,并完全按照美国国立卫生研究院实验动物护理和使用指南进行。
[0038]
动物
[0039]
在本研究中使用了两组同系列的雄性c57bl/6j小鼠,并在室内饲养。它们在实验开始时为8周龄,保持12小时的光照/黑暗循环(早上7点开始光照),并提供食物和水让其随意采食。在实验之前将动物分组饲养,但在行为和应激实验方案开始时单独饲养直到研究结束。基于应激后评估的享乐行为将小鼠平衡分配到实验组和对照组。
[0040]
慢性复合应激
[0041]
慢性复合应激用于在动物中诱导情感缺乏样表型(10)。慢性复合应激方案由4小时/天的约束应激组成,其中小鼠被固定在适当大小的塑料约束管中,并暴露于频闪灯和白噪声以最大限度地减少适应性,连续进行10-14天。应激在早上开始,在上午9-10点之间,接近动物光照周期的开始。在应激结束之后,啮齿动物被送回它们的笼子并单独饲养。
[0042]
享乐行为
afferent,ta)。使用clampex软件(pclamp 10系列,molecular devices)、放大(x1000,npi electronic)、过滤(3khz)和数字化(10khz,digidata 1440a,molecular devices)获得场兴奋性突触后电位(fepsp)。以0.1hz的频率并以0.01-1.0ma的五种不同强度对切片进行刺激(100μs),以收集约为0.1mv的纤维群峰(fv)的一系列响应。然后用dnqx(50μm)冲洗到切片上15分钟,以阻断fepsp的amap组分并显示nmda组分。在与dnqx处理前记录的相同刺激强度下再次采集五个fepsp。然后将nmdar拮抗剂d-apv(80μm)冲洗到切片上15分钟,以确认dnqx处理后仍然存在的fepsp反应确实是nmdar介导的。
[0051]
如前所述(15)对ta-ca1 fepsp的ampa:nmda比率进行量化,从而提供来自不同小鼠的切片之间突触强度的测量。首先对每个强度的所有轨迹进行平均,并对fv的振幅进行量化。fepsp的ampa组分被量化为每个刺激强度响应的线性部分的最早部分超过1.5ms的斜率,通常为从其开始的0.1-2.0ms。fepsp斜率的nmda组分在apv完全消除dnqx后响应的最早时间点被量化为超过4ms。ampa和nmda的斜率都被标准化为各自的fv。为了进行量化,选择相同刺激强度的反应对,其中在dnqx存在下的反应振幅最接近0.1mv。每个切片的ampa:nmda比率(1-6/小鼠)被平均以计算每只动物的平均ampa:nmda比率。作为突触强度的独立测量,我们还计算了ampa:fv和nmda:fv的比率,计算数据来自用于计算ampa:nmda比率的同一对响应。实验人员在量化过程中对处理条件不知情,并且由第二名实验人员进行确认数值。
[0052]
药物处理
[0053]
光盖伞素购自开曼生物(密歇根州安娜堡)(cayman chemical(ann arbor,mi)),并在无菌0.9%盐水中稀释至1mg/ml。酮色林( )-酒石酸盐购自密理博西格玛(马萨诸塞州伯灵顿)(milliporesigma(burlington,ma)),同样稀释至1mg/ml。酮色林在注射载体对照或光盖伞素前60分钟给药,这与之前关于酮色林在人类(7)和啮齿动物(11)中阻断致幻行为反应的能力的研究一致。以1mg/kg的剂量注射光盖伞素,以2mg/kg的剂量注射酮色林(这与之前的啮齿动物研究(11、18、19)一致),或注射同等体积的盐水。这些剂量与之前在人体研究中使用的口服剂量相当(光盖伞素(3)ca.0.5mg/kg;酮色林(11)ca.1mg/kg)。每只实验动物接受两次注射以作为任何注射或操作作用的对照。
[0054]
数据统计
[0055]
统计分析包括使用graphpad prism 8进行学生t检验、双因素和三因素方差分析,以及在excel(microsoft)中对感兴趣的比较数据手动进行holm-sidak多重比较校正。来自两组动物的结果在统计学上没有差异,因此进行合并。使用的统计测试在图例中显示。如有显示,n=动物数量。
[0056]
实施例2
[0057]
结果
[0058]
将8周龄的雄性c57bl/6j小鼠暴露于慢性复合应激范式中,并通过两项涉及不同感官的欲望选择任务来分析享乐状态:两瓶蔗糖偏好测试,比较了1%蔗糖溶液和水的消耗量,以及雌性尿液嗅探测试,比较了与浸有雄性小鼠和发情期雌性小鼠尿液的棉签的互动(图1a)。
[0059]
小鼠在基线时表现出对蔗糖溶液和雌性尿液的强烈偏好,并且在连续10-14天的慢性复合应激后,蔗糖和雌性尿液的偏好显著降低(图1b-1c)。然后给小鼠单次经腹腔
(i.p.)注射光盖伞素(1mg/kg)。
[0060]
暴露于慢性复合应激的小鼠在注射光盖伞素后24-48小时显示出对蔗糖溶液和雌性尿液偏好的显著恢复,而给予盐水载体注射的小鼠则保持较低的蔗糖和雌性尿液偏好。在慢性复合应激后未表现出蔗糖偏好丧失的抗应激小鼠在注射光盖伞素后其反应未表现出任何显著变化(图3)。这些数据首次展示证据证明了在应激引起的抑郁相关行为的临床前模型中,光盖伞素的快速抗快感缺乏反应。
[0061]
检查了促幻觉的5-ht2r的激活对于光盖伞素的抗抑郁样反应是否是必要的。5-ht2r拮抗剂酮色林可减少光盖伞素引起的人类知觉改变7和啮齿动物行为改变(11)。在这些相同的慢性复合应激组中,应激易感的小鼠接受酮色林(2mg/kg,i.p.)注射,1小时后注射光盖伞素(1mg/kg,i.p.)或载体(0.9%盐水),这在之前的啮齿动物行为研究中显示是有效的(11)。
[0062]
在酮色林预处理小鼠中,光盖伞素显著增加了应激后蔗糖和雌性尿液偏好(图1b-1c),但是单独的酮色林预处理对任何一种行为都没有显著影响。无论是否注射了作为酮色林阳性对照的光盖伞素,酮色林预处理小鼠均显示出活动性显著增强,这可能是通过阻断5-ht2cr来实现的(12)(图4)。与之相反,本研究中使用的光盖伞素剂量对头部抽搐或活动性没有显著影响(11)。
[0063]
光盖伞素的抗抑郁样行为反应的产生机制是什么?将应激与抗抑郁药的治疗作用联系起来的一个共同因素是它们都对兴奋性突触有影响,但影响是相反的。慢性应激会对多个大脑区域的兴奋性突触结构和功能产生有害影响,这些区域与认知、奖励、情感和为奖励而工作的动机相关(13,14)。与之相反,抗抑郁药促进慢性应激后奖励回路中兴奋性突触传递的恢复(15)和人体内功能连接性的恢复(16)。有解剖学证据表明,光盖伞素可通过5-ht2r依赖性机制促进前额叶皮层的突触连接(17)。
[0064]
本发明检查了光盖伞素对享乐状态的恢复是否伴随着兴奋性突触强度的恢复,量化为由glua(ampa)和glun(nmda)受体介导的场epsp的组分比率。行为分析完成后,制备海马脑片,并使用细胞外记录来测量由temporoammonic通路传入到ca1锥体细胞远端树突而形成的典型应激敏感兴奋性突触的ampa:nmda比率(ta-ca1;图2a)(15)。
[0065]
在取自注射了光盖伞素的慢性复合应激易感小鼠的切片中,其ampa:nmda比值显著大于取自接受慢性复合应激并仅注射载体或酮色林的动物切片的比值(图2b)。对各切片的单个组分的突触反应的纤维群峰振幅进行标准化揭示了,在接受光盖伞素处理的小鼠中,ampap介导的组分反应具有更大的振幅(图2c)以及nmdar介导的组分没有显著变化(图2d)。这些结果表明,在啮齿动物中单独给药光盖伞素可在其从体内清除数天(数小时)内,促进抑郁症相关大脑区域中持续的突触强化,就像光盖伞素对人脑功能连接的持续影响一样(18)。
[0066]
与行为结果一致,用酮色林预处理不会削弱光盖伞素恢复ampa:nmda比率的能力(图2b)。在慢性复合应激动物的切片中,给予光盖伞素的ampa:nmda比率显着高于给予载体的,无论小鼠是否用酮色林进行预处理。因此,小鼠中对光盖伞素的抗快感缺乏行为反应和海马突触反应都不依赖于5-ht2r的激活。
[0067]
本发明首次提供证据证明光盖伞素在经过充分研究和充分验证的慢性应激引起的抑郁相关享乐行为缺陷模型中发挥快速的有益作用。此前在选择性繁殖大鼠系的强迫游
泳测试中,光盖伞素对行为的影响是不一致的(18、19)。尽管抑郁症是一种独特的人类疾病,但动物实验的结果可以为光盖伞素的作用机制提供独特的见解,而这些结果在人类中很难获得,例如受体药理学。事实上,这些结果概括了光盖伞素对人类的快速和持久的抗抑郁作用以及之前报道的对大脑连接的持续改变。尽管开发用于精神病学的迷幻化合物的主流观点是这些化合物改变思维的效果有助于治疗或者就是具有治疗益处的原因(2、8),但是本发明证明光盖伞素的抗抑郁反应可能不需要通过5-ht2r以及迷幻反应来实现。因此,光盖伞素和5-ht2r拮抗剂(例如酮色林)的联合使用提供了一种安全有效的方法来消除、减弱或缩短光盖伞素引起的知觉改变的持续时间,同时保留其治疗益处。
[0068]
重置负责整合奖励和情感的中皮质边缘回路中的突触强度,就像这里展示的那样,可以为心理处理的持久改善提供神经生物学基础。事实上,对健康志愿者和trd患者的人体研究表明,在光盖伞素给药后的这些相同回路中,静息状态功能连接持续增加(20、21)。5-htr是否光盖伞素这种反应的基础仍然有待验证,但是它们的定义可以提供开发光盖伞素替代方案的策略,这些方案更偏向于突触强化,而不是知觉改变。之前的研究工作表明5-ht1br有助于ssri类药物的突触和行为抗抑郁样作用(22)。对5-ht1br具有高亲和力(5)的光盖伞素可能通过快速激活5-ht1br发挥其有益作用。虽然动物模型没有提供关于迷幻体验与传统心理疗法的潜在协同作用的启示,其中单独给药光盖伞素可能促进情感洞察力和自我意识,但是通过对光盖伞素作用的药理学和生理学基础的更好的临床前理解,这些相互作用的有效性可能会得到提升。
[0069]
参考文献如下所示:
[0070]
1.nichols de.pharmacol rev.68:264-35,2016.
[0071]
2.nutt et al.cell 181:24-28,2020.
[0072]
3.carhart-harris et al.psychopharmacol.235:399-408,2018.
[0073]
4.johnson et al.neuropharmacol 142:143-16,2018.
[0074]
5.halberstadt et al.neuropharmacology 61:364-381,2011.
[0075]
6.madsen et al.neuropsychopharmacol.44:1328-133,2019.
[0076]
7.vollenweider et al.neuroreport 9:3897-390,1998.
[0077]
8.roseman et al.front.pharmacol.8:974,2018.
[0078]
9.kometer m,et al.p biol psychiatry 72:898-90,2012.
[0079]
10.willner p.tneurobiol stress.6:78-9,2016.
[0080]
11.winter et al.pharmacol biochem behav 87:472-48,2007.
[0081]
12.canel et al.neuropharmacol.70:112-121,2013.
[0082]
13.thompson et al.trends neurosci.38:279-294,2015.
[0083]
14.duman et al.neuron 102:75-90,2019.
[0084]
15.kallarackal et al.j.neurosci.33:15669-15674,2013.
[0085]
16.evans et al.biol.psychiatry 84:582-590,2018.
[0086]
17.ly et al.cell reports 23:3170-3182,2018.
[0087]
18.jefsen et al.acta neuropsychiatr.31:213-219,2019.
[0088]
19.hibicke et al.acs chem.neurosci.11:864-871,2020.
[0089]
20.barrett et al.sci.rep.10:2214,2020.
[0090]
21.carhart-harris et al.sci.rep.7:1
–
11,2017.
[0091]
22.cai et al.nat.neurosci.16:464-472,2013.
[0092]
23.belmaker rh and agam g.n engl j med 358:55-68,2008.
[0093]
24.kessler et al.jama 289:3095-3105,2003.
[0094]
25.kessler et al.arch gen psychiatry 62:593-602,2005.
[0095]
26.gaynes et al.psychiatr serv.60:1439-1445,2009.
[0096]
27.et al.science 364(6436),2019.
[0097]
28.legates et al.nature 564:258-262,2018.
[0098]
29.van dyke et al.neuropharmacol 150:38-45,2019.
[0099]
30.nestler et al.neuron 34:13-25,2002.
[0100]
31.fava et al.neuron 28:335-341,2000.
[0101]
32.hamet et al.metabolism 54:0-15,2005.
[0102]
33.billings et al.j abnormal psychol 92:119-133,1983.
[0103]
34.mcewen bs.ann rev neurosci 22:105
–
122,1999.
[0104]
35.nestler ej and carlezon wa.biol psychiatry 59:1151-1159,2006.
[0105]
36.drysdale et al.nature med 23:28-38,2017.
[0106]
37.boulenguez et al.neuropharmacol 35:1521-1529,1996.
[0107]
38.tye et al.nature 493:537-541,2013.
[0108]
39.lim et al.nature 487:183-189,2012.
[0109]
40.yuen et al.neuron 73:962-977,2012.
[0110]
41.brun et al.science 296:2243-2246,2002.
[0111]
42.remondes m and schuman em.nature 431:699-703,2004.
[0112]
43.li et al.nature 470:535-539,2011.
[0113]
44.nutt et al.lancet 376:558-1565,2010.
[0114]
45.vollenweider fx and kometer m.nat rev neurosci 11:642-651,2010.
[0115]
46.engel et al.naunyn schmiedebergs arch pharmacol 332:1-7,1986.
[0116]
47.gothert m and schlicker e.j cardiovasc pharmacol 10 suppl 3:s3-s7,1987.
[0117]
48.maura et al.naunyn schmiedebergs arch pharmacol 334:323-326,1986.
[0118]
49.carr gv and lucki i.psychopharmacol(berl)213:265-287,2011.
[0119]
50.svenningsson et al.science 311:77-80,2006.
[0120]
51.furay et al.behav brain res 224:350-357,2011.
[0121]
52.neumaier et al.neuropsychopharmacol 15:515-522,1996.
[0122]
53.legates et al.neuropsychopharmacol 44:140-154,2019.
[0123]
54.chan et al.neuropsychopharmacol 42:1749-1751,2017.
[0124]
55.gerfen et al.science 250:1429-1432,1990.
[0125]
56.mathur et al.j neurosci 31:7402-7411,2011.
[0126]
57.et al.nature 501:179-184,2013.
[0127]
58.roth et al.crit.rev.neurobiol 12:319-338,1998.
[0128]
59.lee et al.j neurophysiol 103:479-489,2010.
[0129]
60.hasler et al.pharm acta helv 72:175-184,1997.
[0130]
61.nautiyal et al.neuron 86:813-826,2015.
[0131]
62.hoyer et al.pharmacol rev 46:157-203,1994.
[0132]
63.weisstaub et al.science 313:536-540,2006.
[0133]
64.burmeister et al.neuropsychopharmacol.29:660-668,2004.
[0134]
65.burgdorf et al.j neurosci 37:11894-11911,2017.
[0135]
66.prnewswire.com/news-releases/compass-pathways-receives-fda-breakthrough-therapy-desi gnation-for-psilocybin-therapy-for-treatment-resistant-depression-834088100.
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。