一种c端改造的人乳头瘤病毒6型l1蛋白及其用途
技术领域
1.本技术涉及生物技术领域,具体涉及一种改造的人乳头瘤病毒蛋白、及由其形成的五聚体或病毒样颗粒、以及人乳头瘤病毒蛋白、五聚体或人乳头瘤病毒病毒样颗粒在制备预防乳头瘤病毒感染及感染诱发的疾病的疫苗中的用途。
背景技术:
2.人乳头瘤病毒(human papillomavirus,hpv)是一类感染上皮组织的无包膜小dna病毒,病毒基因组为双链闭环dna,大小约7.2-7.9kb,有8个开放读码框,分别编码e1、e2、e4、e5、e6、e7合计6个早期基因,及l1、l2合计2个晚期基因;此外,还含有长调控区。病毒颗粒的直径约为45-44nm,外壳为t=7的正二十面体,由72个l1五聚体及72个l2蛋白构成。
3.目前已鉴定200余型,其中40余型主要感染肛周、泌尿生殖器及口咽部的粘膜及附近皮肤;根据感染诱发病变性质不同,分为诱发恶性肿瘤的致癌型(hpv16、-18、-31、-33、-45、-52、-58等)和诱发疣状增生的低危型(hpv6、-11等)。目前致癌型hpv约有20多型,其中12种常见的致癌型为高危型。分子流行病学研究发现,致癌型hpv持续感染可诱发约100%的宫颈癌、88%的肛门癌、70%的阴道癌、50%的阴茎癌、43%的阴户癌及72%的头颈癌。低危型hpv目前鉴定出了12种型别,分别是hpv6、-7、-11、-13、-32、-40、-42、-43、-44、-54、-74、-91。其中,hpv6型和hpv11型是世界范围内肛周生殖器及咽部黏膜疣的主要流行型别。对我国自1990年1月至2013年12期间发表的67篇文献,累计10757例尖锐湿疣(ca)患者的hpv分析发现,ca患者的hpv感染阳性率为86.7%(9328),hpv6和/或hpv 11阳性率为81.2%(3671/4623)、hpv6的为43.8%(2445/6134)、hpv11的为38.3%(2155/6134),hpv16、hpv 18和/或hpv 11阳性率为21.7%(870/3781)。对哥伦比亚地区的261例经活检组织学确诊的生殖器疣(gw)患者(其中女性155例,男性106例)的hpv分析显示,女性gw患者的hpv检出率为87.7%,男性为90.6%;其中hpv6的检出率最高,达59.7%(155.8/261),在女性和男性的检出率分别为62%及56%;其次是hpv11,检出率为29.8%(77.8/261);hpv16的检出率位居第三,检出率为16%;hpv6、hpv11感染阳性率合计为80.3%。
4.l1蛋白体外表达后,可组装成vlp。表达体系主要有酵母表达体系、昆虫细胞表达体系、大肠杆菌表达体系等。采用昆虫细胞表达体系生产的l1vlp疫苗的优势在于:蛋白可溶性表达水平高、细胞容易破碎、不含内毒素。目前上市的3种l1vlp疫苗分别是merck公司采用酵母表达体系生产的gardasil四价苗(hpv16/18/6/11l1vlp,磷酸铝硫酸盐佐剂)、gardasil-9九价苗(hpv16/18/6/11/31/33/45/52/58l1vlp,磷酸铝硫酸盐佐剂)及gsk公司采用昆虫细胞表达体系生产的cervarix二价苗(hpv16/18l1vlp,as04佐剂)。
5.临床研究发现,cervarix中,较低剂量的16l1vlp(20μg/剂)及相同剂量的18l1vlp(20μg/剂)分别诱发产生的hpv16及hpv18特异性中和抗体的滴度、th细胞反应、及记忆性b细胞数目均较gardasil诱发的高(单剂gardasil中16l1vlp的含量为40μg,18l1vlp的为20μg)。
6.提高hpv l1vlp在昆虫细胞内的表达水平,可显著提高l1vlp的纯化得率,降低疫
苗的生产成本。在原核表达体系中,采用n端截短法对hpv16、-18、-31、-33、-45、-52、-58、-6、-11型别的l1进行改造,发现可上调l1表达水平的n端截短的氨基酸数目因型别不同而异,且没有规律。在昆虫表达系统中,采用c端截短的方法对bpv1 l1进行改造,发现截短型的bpv l1的组装效率提高3倍;对hpv58型的截短型l1的vlp虽有报道,但未见c端截短对蛋白表达量的影响的报道。利用酵母表达体系,生产6型l1vlp均是采用密码子优化的全长基因。
7.本技术发现,通过对l1的c端改造,可以显著提高6l1vlp表达水平及产量,而且生产获得的hpv6 l1vlp可诱发高滴度的型别特异性中和抗体。
技术实现要素:
8.本技术提供了一种新的c端改造的hpv6 l1蛋白、由其组成的五聚体或病毒样颗粒,及含该五聚体或病毒样颗粒的疫苗,并研究该疫苗在预防hpv感染和感染相关疾病中的用途。
9.本发明人经研究出人意料地发现,适当地对hpv6 l1蛋白的c端碱性氨基酸进行置换,可提高hpv6 l1蛋白在昆虫细胞表达系统中的表达量,该截短蛋白可组装成vlp,并可诱发针对hpv6的保护性免疫反应。
10.因此,根据本技术的一些实施方案,涉及一种与野生型hpv6 l1蛋白(例如ncbi数据库np040304.1序列对应的氨基酸序列)相比,其c端31个氨基酸内的1个或多个碱性氨基酸被置换为极性不带电荷氨基酸、非极性氨基酸和/或酸性氨基酸。
11.具体地,本技术提供了一种c端改造的hpv6 l1蛋白,其中所述改造的hpv6l1蛋白与野生型hpv6 l1蛋白相比,其c端31个氨基酸内的1个或多个精氨酸(r)和/或赖氨酸(k)被置换为极性不带电荷氨基酸、非极性氨基酸和/或酸性氨基酸。优选地,所述极性不带电荷氨基酸选自甘氨酸(g)、丝氨酸(s)或苏氨酸(t),所述非极性氨基酸选自丙氨酸(a)或缬氨酸(v),所述酸性氨基酸为天冬氨酸(d)或谷氨酸(e)。
12.在具体的实施方案中,本技术所述c端改造的hpv6 l1蛋白在seq id no.1所示序列(ncbi数据库np040304.1序列对应的氨基酸序列)基础上进行改造;特别优选地,所述c端改造的hpv6 l1蛋白选自6l1cs1、6l1cs2、6l1cs3、6l1cs4、6l1cs5、6l1cs6、6l1cs7、6l1cs8,其氨基酸序列如seq id no.2、seq id no.3、seq id no.4、seq id no.5、seq id no.6、seq id no.7、seq id no.8或seq id no.9所示。
13.野生型hpv6 l1蛋白也可来自但不限于ncbi数据库aac80447.1、aac80442.1、cdk36706.1、aac80450.1、cdk37192.1、cdk36967.1、cdk36699.1、cdk36544.1、ccj09340.1等来自hpv6变异株的l1蛋白,相应变异株的c端改造l1蛋白,其特征为c端31个氨基酸与上述c端改造的hpv6 l1蛋白相同,如通过序列比较来评价。
14.根据本技术的一些实施方案,涉及编码本技术c端改造的hpv6 l1蛋白的多核苷酸。优选的,所述多核苷酸采用常用的表达系统的密码子优化,如大肠杆菌表达系统、酵母表达系统、昆虫细胞表达系统等。特别优选地,所述多核苷酸采用昆虫细胞密码子优化。
15.根据本技术的一些实施方案,涉及含有上述所述多核苷酸的载体,优选地,所述载体选自质粒、重组bacmid和重组杆状病毒。
16.根据本技术的一些实施方案,涉及包含上述载体的细胞,优选地,所述细胞为大肠
杆菌细胞、酵母细胞或昆虫细胞,特别优选地,所述细胞为昆虫细胞。
17.根据本技术的一些实施方案,涉及一种hpv6 l1多聚体或病毒样颗粒,该多聚体(例如五聚体)或病毒样颗粒含有上述c端改造的hpv6 l1蛋白,或由上述c端改造的hpv6 l1蛋白组成。
18.根据本技术的一些实施方案,涉及一种预防hpv感染或hpv感染相关疾病的疫苗,该疫苗含有上述hpv6 l1多聚体或病毒样颗粒,其中hpv6 l1病毒样颗粒的含量为能诱发保护性免疫反应的有效量。优选地,该疫苗还可包含至少一种选自其他嗜黏膜组和/或嗜皮肤组的hpv的五聚体或病毒样颗粒,这些五聚体或病毒样颗粒的含量分别为能诱发保护性免疫反应的有效量。上述疫苗通常还包含疫苗用赋形剂或载体。
19.优选地,所述疫苗含有上述的hpv6 l1多聚体或病毒样颗粒,以及至少一种选自hpv2、-5、-7、-8、-11、-16、-18、-26、-27、-28、-29、-30、-31、-32、-33、-34、-35、-38、-39、-40、-43、-44、-45、-51、-52、-53、-56、-57、-58、-59、-61、-66、-67、-68、-69、-70、-73、-74、-77、-81、-82、-83、-85、-91的l1病毒样颗粒,这些病毒样颗粒的含量分别为能诱发保护性免疫反应的有效量。
20.进一步优选地,所述疫苗含有上述的hpv6 l1多聚体或病毒样颗粒,以及hpv11、-16、-18、-26、-31、-33、-35、-39、-45、-51、-52、-56、-58、-59、-68及-73的l1病毒样颗粒,这些病毒样颗粒的含量分别为能诱发保护性免疫反应的有效量。
21.进一步优选地,所述疫苗含有上述hpv6 l1多聚体或病毒样颗粒,以及hpv11、-16、-18、-31、-33、-35、-39、-45、-52及-58的l1病毒样颗粒,这些病毒样颗粒的含量分别为能诱发保护性免疫反应的有效量。
22.进一步优选地,所述疫苗含有上述hpv6 l1多聚体或病毒样颗粒,以及hpv11、-16、-18、-52及-58的l1病毒样颗粒,这些病毒样颗粒的含量分别为能诱发保护性免疫反应的有效量。
23.进一步优选地,所述疫苗含有上述hpv6 l1多聚体或病毒样颗粒,以及hpv16、-18及-58的l1病毒样颗粒,这些病毒样颗粒的含量分别为能诱发保护性免疫反应的有效量。
24.特别优选地,所述疫苗含有上述hpv6 l1多聚体或病毒样颗粒,以及hpv11的l1病毒样颗粒,这些病毒样颗粒的含量分别为能诱发保护性免疫反应的有效量。
25.根据本技术的一些实施方案,涉及一种新型疫苗,其包含上述hpv6 l1多聚体或病毒样颗粒及佐剂,可进一步提高免疫反应。优选地,所使用的佐剂为人用疫苗佐剂。
26.根据本技术的一些实施方案,涉及上述疫苗在预防hpv感染或hpv感染相关疾病中的用途。
27.相关术语的说明及解释
28.根据本技术,术语“昆虫细胞表达系统”包括昆虫细胞、重组杆状病毒、重组bacmid及表达载体。其中昆虫细胞来源于市场上可得到的细胞,在此举例但不限于:sf9、sf21、high five。
29.根据本技术,术语“野生型hpv6 l1蛋白”的例子包括但不限于ncbi数据库中编号为np040304.1的序列对应的l1蛋白。
30.根据本技术,术语“赋形剂或载体”是指选自一种或多种,包括但不限于:ph调节剂、表面活性剂、离子强度增强剂。例如,ph调节剂举例但不限于磷酸盐缓冲液,表面活性剂
包括阳离子、阴离子或非离子型表面活性剂,举例但不限于聚山梨酯80(tween-80),离子强度增强剂举例但不限于氯化钠。
31.根据本技术,术语“佐剂”是指在临床上可应用于人体的佐剂,包括当前已获得批准的和将来可能获得批准的各种佐剂。
32.根据本技术,本技术的疫苗可采用患者可接受的形式,包括但不限于口服或者注射,优选注射。
33.根据本技术,本技术疫苗优选单位剂型使用,其中单位剂型中c端改造的hpv6 l1蛋白病毒样颗粒的剂量为5μg-80μg,优选20μg-40μg。
附图说明
34.图1显示了本技术实施例4中c端改造的hpv6 l1在昆虫细胞中的表达鉴定。结果显示,8种c端改造的hpv6 l1均可在昆虫细胞中高水平表达。泳道1至9分别表示6l1(野生型)、6l1cs1、6l1cs2、6l1cs3、6l1cs4、6l1cs5、6l1cs6、6l1cs7、6l1cs8。
35.图2a至图2c显示了本技术实施例6中纯化后获得的野生型hpv6l1、6l1cs4及6l1cs6突变体蛋白的动态光散射分析结果。结果显示野生型hpv6l1、6l1cs4及6l1cs6重组蛋白形成的病毒样颗粒水化动力学直径分别为97.48nm、131.3nm和127.1nm,颗粒组装的百分比均为100%。图2a表示野生型hpv6l1;图2b表示6l1cs4;图2c表示6l1cs6。
36.图3a至图3b显示了本技术实施例7中纯化后获得的6l1cs4及6l1cs6的vlp的透射电镜观察结果。视野中可见大量的直径约30-55nm的病毒样颗粒,颗粒的大小与理论值相符,均一度好。bar=100nm。图3a及图3b分别表示6l1cs4及6l1cs6。
37.图4显示了本技术实施例8中的野生型hpv6l1、6l1cs4、6l1cs6 vlp接种小鼠后免疫血清hpv6中和抗体滴度的分析。ns:p》0.05,**:p《0.01。
具体实施方式
38.下面将通过非限制性实施例进一步说明本技术,本领域技术人员公知,在不背离本技术精神的情况下,可以对本技术做出许多修改,这样的修改也落入本技术的范围。下面的实施例仅用于说明本技术,而不应视为限定本技术的范围,因为实施方案必然是多样的。本说明书中使用的用语仅是为了阐述特定的实施方案,而非作为限制,本技术的范围已界定在所附的权利要求中。
39.除非特别说明,本说明书中所使用的所有技术和科学用语均和本案所属技术领域的技术人员所普遍明了的意义相同。下面就本技术的优选方法和材料加以叙述,但是与本说明书中所述方法和材料类似或等效的任何方法和材料均可用以实施或测试本技术。下述实验方法如无特别说明,均为常规方法或产品说明书所描述的方法,所使用的实验材料如无特别说明,均可容易地从商业公司获取。本说明书中所提到的所有公开文献均被并入于此作为参考,以揭示并说明所述公开文献中的方法和/或材料。
40.实施例1:c端改造的hpv6l1基因的扩增及表达载体构建
41.用做模版的全长hpv6l1基因由上海生工生物工程技术服务有限公司全基因合成(seq id no.18所示),其对应的氨基酸序列为seq id no.1所示的序列。
42.用于构建c端改造的hpv6l1基因的引物由上海生工生物工程技术服务有限公司合
成。
43.1)6l1cs1基因:以seq id no.18为模版,使用6l1f/6l1cs1r1为引物,pcr扩增获得6l1cs1-1中间产物,然后以6l1cs1-1中间产物为模板,使用6l1f/6l1cs1r2为引物,pcr扩增获得6l1cs1-2中间产物,最后以6l1cs1-2中间产物为模板,使用6l1f/6l1cs1r3为引物,pcr扩增获得6l1cs1基因,其序列如seq id no.10所示;
44.2)6l1cs2基因:以seq id no.18为模版,使用6l1f/6l1cs2r1为引物,pcr扩增获得6l1cs2-1中间产物,然后以6l1cs2-1中间产物为模板,使用6l1f/6l1cs2r2为引物,pcr扩增获得6l1cs2-2中间产物,最后以6l1cs2-2中间产物为模板,使用6l1f/6l1cs2r3为引物,pcr扩增获得6l1cs2基因,其序列如seq id no.11所示;
45.3)6l1cs3基因:以seq id no.18为模版,使用6l1f/6l1cs3r1为引物,pcr扩增获得6l1cs3-1中间产物,然后以6l1cs3-1中间产物为模板,使用6l1f/6l1cs3r2为引物,pcr扩增获得6l1cs3-2中间产物,最后以6l1cs3-2中间产物为模板,使用6l1f/6l1cs3r3为引物,pcr扩增获得6l1cs3基因,其序列如seq id no.12所示;
46.4)6l1cs4基因:以seq id no.18为模版,使用6l1f/6l1cs4r1为引物,pcr扩增获得6l1cs4-1中间产物,然后以6l1cs4-1中间产物为模板,使用6l1f/6l1cs4r2为引物,pcr扩增获得6l1cs4-2中间产物,最后以6l1cs4-2中间产物为模板,使用6l1f/6l1cs4r3为引物,pcr扩增获得6l1cs4基因,其序列如seq id no.13所示;
47.5)6l1cs5基因:以seq id no.18为模版,使用6l1f/6l1cs5r1为引物,pcr扩增获得6l1cs5-1中间产物,然后以6l1cs5-1中间产物为模板,使用6l1f/6l1cs5r2为引物,pcr扩增获得6l1cs5-2中间产物,最后以6l1cs5-2中间产物为模板,使用6l1f/6l1cs5r3为引物,pcr扩增获得6l1cs5基因,其序列如seq id no.14所示;
48.6)6l1cs6基因:以seq id no.18为模版,使用6l1f/6l1cs6r1为引物,pcr扩增获得6l1cs6-1中间产物,然后以6l1cs6-1中间产物为模板,使用6l1f/6l1cs6r2为引物,pcr扩增获得6l1cs6-2中间产物,最后以6l1cs6-2中间产物为模板,使用6l1f/6l1cs6r3为引物,pcr扩增获得6l1cs6基因,其序列如seq id no.15所示;
49.7)6l1cs7基因:以seq id no.18为模版,使用6l1f/6l1cs7r1为引物,pcr扩增获得6l1cs7-1中间产物,然后以6l1cs7-1中间产物为模板,使用6l1f/6l1cs7r2为引物,pcr扩增获得6l1cs7-2中间产物,最后以6l1cs7-2中间产物为模板,使用6l1f/6l1cs7r3为引物,pcr扩增获得6l1cs7基因,其序列如seq id no.16所示;
50.8)6l1cs8基因:以seq id no.18为模版,使用6l1f/6l1cs8r1为引物,pcr扩增获得6l1cs8-1中间产物,然后以6l1cs8-1中间产物为模板,使用6l1f/6l1cs8r2为引物,pcr扩增获得6l1cs8-2中间产物,最后以6l1cs8-2中间产物为模板,使用6l1f/6l1cs8r3为引物,pcr扩增获得6l1cs8基因,其序列如seq id no.16所示。
51.pcr扩增的方法都是公知的,例如专利cn 101293918 b。
52.采用ecori/xbai酶切位点,分别对上述pcr扩增得到的基因进行酶切,并分别插入商业化表达载体pfastbac1(invitrogen公司生产)中,得到包含c端改造的hpv6l1基因的重组表达载体:pfastbac1-6l1cs1、pfastbac1-6l1cs2、pfastbac1-6l1cs3、pfastbac1-6l1cs4、pfastbac1-6l1cs5、pfastbac1-6l1cs6、pfastbac1-6l1cs7、pfastbac1-6l1cs8。上述酶切、连接及克隆构建的方法都是公知的,例如专利cn101293918b。
53.实施例2:c端改造的hpv6l1基因的重组bacmid及重组杆状病毒的构建体
54.分别使用包c端改造的hpv6l1基因的重组表达载体pfastbac1-6l1cs1、pfastbac1-6l1cs2、pfastbac1-6l1cs3、pfastbac1-6l1cs4、pfastbac1-6l1cs5、pfastbac1-6l1cs6、pfastbac1-6l1cs7、pfastbac1-6l1cs8转化大肠杆菌dh10bac感受态,筛选获得重组bacmid,然后用重组bacmid转染昆虫细胞sf9,在sf9内扩增重组杆状病毒。重组bacmid的筛选及重组杆状病毒的扩增方法都是公知的,例如专利cn 101148661 b。
55.实施例3:c端改造的hpv6l1基因在sf9细胞中的表达
56.sf9细胞分别接种野生型hpv6l1的优化基因及8种c端改造的hpv6l1基因的重组杆状病毒,进行c端改造的hpv6l1蛋白的表达,27℃培养约88h后收发酵液,3000rpm离心15min,弃上清,用pbs洗涤细胞后,用于表达鉴定及纯化。感染表达的方法是公开的,例如专利cn 101148661 b。
57.实施例4:c端改造的hpv6l1的表达鉴定
58.取实施例3中所述表达不同c端改造的hpv6l1的细胞各1
×
106个,重悬于200μl pbs溶液中,加入6
×
上样缓冲液50μl,75℃变性8分钟,分别取10μl进行sds-page电泳及western印记鉴定。结果如图1所示,8种c端改造的hpv6l1蛋白均可在昆虫细胞中表达,其大小约55kda。sds-page电泳及western印记鉴定的方法是公开的,例如专利cn 101148661 b。
59.实施例5:c端改造的hpv6l1蛋白与野生型hpv6l1蛋白的表达量比较
60.取实施例3中所述表达c端改造的hpv6l1蛋白及野生型hpv6l1的细胞各1
×
106个,重悬于200μl pbs溶液中,采用超声破碎法(宁波新芝超声破碎仪,2#探头,100w,超声5s,间隔7s,总时间3min)破碎细胞,12000rpm高速离心10分钟。收取裂解上清,采用夹心elisa法检测上清中的l1含量,该方法是公知的,例如专利cn104513826a。
61.使用本发明人制备的hpv6l1单克隆抗体包被酶标板,80ng/孔,4℃孵育过夜;使用5%bsa-pbst室温封闭2h,再用pbst洗板3次。用pbs将裂解上清进行连续2倍稀释,并且将hpv6l1 vlp标准品也进行梯度稀释,浓度从2μg/ml-0.0625μg/ml,分别加入酶标板,每孔100μl,37℃孵育1h。用pbst洗板3次,加入1:3000稀释的hpv6l1兔多抗,每孔100μl,37℃孵育1h。用pbst洗板3次,加入1:3000稀释的hrp标记的山羊抗小鼠igg(1:3000稀释,中杉金桥公司),37℃孵育45分钟。用pbst洗板5次,每孔加入100μl opd底物(sigma公司),37℃显色5分钟,用50μl 2m硫酸终止反应,在490nm处测定吸光值。依据标准曲线计算裂解上清中c端改造的hpv6l1蛋白及野生型hpv6l1蛋白的浓度。
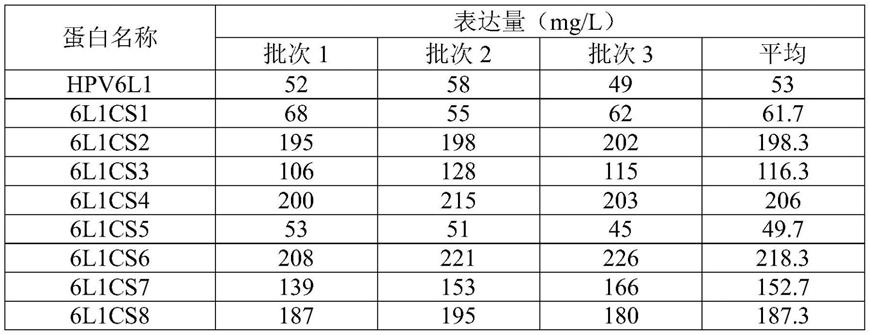
62.结果如表1所示,本技术的6l1cs1、6l1cs2、6l1cs3、6l1cs4、6l1cs6、6l1cs7、6l1cs8的表达量均高于野生型hpv6l1蛋白,6l1cs5的表达量与野生型hpv6l1蛋白相当。
63.表1.hpv6l1蛋白表达量分析
[0064][0065]
实施例6:c端改造的hpv6l1蛋白的纯化及动态光散射粒径分析
[0066]
取野生型hpv6l1或c端改造的hpv6l1的细胞发酵液50ml,使用10ml pbs重悬细胞,加pmsf至终浓度1mg/ml,超声破碎(宁波新芝超声破碎仪,6#探头,100w,超声5s,间隔7s,总时间5min),取破碎上清进行纯化,纯化步骤在室温进行。在裂解液中加入4%β-巯基乙醇(w/w)对vlp进行解聚,然后使用0.22μm滤器过滤样品,依次使用dmae阴离子交换层析(20mm tris,180mm nacl,4%β-me,ph7.9洗脱)、tmae阴离子交换层析(20mm tris,180mm nacl,4%β-me,ph7.9洗脱)及羟基磷灰石层析(100mm nah2po4,30mm nacl,4%β-me,ph 6.0洗脱)纯化。纯化产物采用planova超滤系统进行浓缩,并更换缓冲液(20mm nah2po4,500mm nacl,ph6.0)促使vlp组装。6l1cs1、6l1cs2、6l1cs3、6l1cs4、6l1cs6、6l1cs7、6l1cs8的纯化得率在25-50mg/l,6l1cs5的纯化得率为15mg/l,而野生型hpv6l1的纯化得率仅为8mg/l。以上纯化方法均是公开的,例如专利cn101293918b、cn1976718a等。
[0067]
取纯化后的野生型hpv6l1蛋白或c端改造的hpv6l1蛋白溶液进行dls粒径分析(zetasizer nano zs 90动态光散射仪,malvern公司),结果如表2所示,其中野生型hpv6l1、6l1cs4及6l1cs6的dls分析图如图2a至2c所示。
[0068]
表2.hpv6l1蛋白dls分析
[0069][0070]
实施例7:c端改造的hpv6l1 vlp的透射电镜观察
[0071]
按实施例6所述的层析纯化方法,对c端改造的hpv6l1 vlp分别进行纯化,使用透析后的vlp制备铜网,并用1%醋酸铀进行染色,充分干燥后使用jem-1400电镜(奥林巴斯)进行观察。部分结果如图3a至图3b所示,c端改造的hpv6l1vlp直径约为30-55nm,形状规则。铜网制备及电镜观察的方法均是公开的,例如专利cn 101148661 b。
[0072]
实施例8:c端改造的hpv6l1 vlp的小鼠免疫及中和抗体滴度测定
[0073]
取4-6周龄的balb/c小鼠,随机分组,每组5只,分别用野生型hpv6l1 vlp及c端改造的hpv6l1 vlp免疫小鼠。肌肉注射,l1 vlp的免疫剂量为0.1μg,于第0,2周免疫,共2次。第2次免疫后2周尾静脉采血,分离血清。
[0074]
使用hpv6假病毒对免疫血清的hpv6中和抗体滴度进行检测,结果如图4所示,野生型hpv6l1 vlp、6l1cs4 vlp及6l1cs6 vlp免疫小鼠后均可有效诱发中和抗体,其中6l1cs4 vlp诱发的中和抗体滴度与野生型hpv6l1 vlp诱发的无统计学差异;6l1cs6 vlp诱发的中和抗体滴度显著低于野生型hpv6l1 vlp诱发的(p《0.01)。本技术包括的其他6种c端改造的hpv6l1突变体vlp采用上述策略免疫小鼠后,诱发的hpv6中和抗体水平均在400-1600之间,与野生型hpv6l1 vlp相比亦无差异。
[0075]
假病毒制备及假病毒中和实验的方法均是公开的,例如专利cn 104418942a。
[0076]
综上所述,发明人发现,对hpv6l1的c端进行氨基酸置换改造,获得的突变体表达水平各不相同,且没有明显的规律,其组装成的vlp的免疫活性也存在一定的差异,因此,采用c端置换改造的方法获得表达水平高、可有效组装、免疫活性好的hpv6l1突变体,具有不可预见性。本技术中筛选获得的c端氨基酸置换改造的hpv6l1突变体可用于多价hpv预防性疫苗的配制及广谱hpv预防性疫苗的构建,具有很好的研发前景。
[0077]
序列说明:
[0078]
seq id no.1:hpv6l1
[0079]
mwrpsdstvy vpppnpvskv vatdayvtrt nifyhasssr llavghpyfs ikranktvvp kvsgyqyrvf kvvlpdpnkf alpdsslfdp ttqrlvwact glevgrgqpl gvgvsghpfl nkyddvensg sggnpgqdnr vnvgmdykqt qlcmvgcapp lgehwgkgkq ctntpvqagd cpplelitsv iqdgdmvdtg fgamnfadlq tnksdvpidi cgttckypdy lqmaadpygd rlffflrkeq mfarhffnragevgepvpdt liikgsgnrt svgssiyvnt psgslvssea qlfnkpywlq kaqghnngic wgnqlfvtvv dttrstnmtl casvttssty tnsdykeymr hveeydlqfi fqlcsitlsa evmayihtmn psvledwnfg lspppngtle dtyryvqsqa itcqkptpek ekpdpyknls fwevnlkekf sseldqyplg rkfllqsgyr grssirtgvk rpavskasaa pkrkraktkr
[0080]
seq id no.2:6l1cs1
[0081][0082]
seq id no.3:6l1cs2
[0083]
[0084][0085]
seq id no.4:6l1cs3
[0086][0087]
seq id no.5:6l1cs4
[0088]
[0089][0090]
seq id no.6:6l1cs5
[0091]
[0092][0093]
seq id no.7:6l1cs6
[0094][0095]
seq id no.8:6l1cs7
[0096]
ggc aat cag ctc ttc gtc acc gtc gtg gac aca acc agg tcc acc aac atg acc ttg tgc gcc agc gtc acc acc agc tcc acc tac acc aac agc gac tac aaa gag tac atg agg cac gtc gaa gaa tac gac ctg caa ttc atc ttc cag ctc tgc tca atc acc ctg agc gcc gag gtg atg gct tac atc cat acc atg aac ccc agc gtc ctc gaa gat tgg aat ttc ggt ctg agc ccc ccc ccc aac ggc acc ctc gaa gac acc tac cgc tac gtg caa agc caa gct atc aca tgc caa aag cct acc ccc gag aag gag aag cca gac cct tac aaa aac ctg tcc ttc tgg gaa gtc aat ctg aag gag aaa ttc agc tcc gag ctg gac caa tac cct ttg ggc agg aaa ttc ctg ctc cag tcc ggc tac cga ggc gga tcc agc atc cga acc ggc gtg gat gga ccc gcc gtc agc aag gct agc gcc gct cct gat gga agc aga gct gat aca aag cgt taat
[0111]
seq id no.15:6l1cs6nt
[0112]
atg tgg cgt ccc tca gat tca acc gtg tac gtc ccc ccc cct aat ccc gtg tcc aaa gtc gtc gct acc gac gcc tac gtc acc agg aca aat atc ttc tac cac gct tca tcc agc cgc ttg ttg gcc gtc ggc cac ccc tac ttc agc att aag cgc gct aat aag acc gtc gtg ccc aaa gtc agc ggc tac cag tac cgc gtc ttc aaa gtg gtc ctc ccc gac ccc aat aaa ttc gcc ctg ccc gac agc tcc ctc ttc gat cct acc acc caa agg ctg gtg tgg gcc tgt acc ggc ctc gaa gtg ggt cgc ggc cag ccc ctg ggt gtc ggc gtc tcc ggc cac ccc ttc ttg aat aag tac gac gac gtg gag aac tcc ggc tcc ggc ggc aac ccc ggc caa gac aac cgc gtc aac gtg ggc atg gac tac aag cag aca caa ttg tgc atg gtc ggt tgc gcc ccc ccc ctg ggc gag cac tgg ggc aaa ggc aag cag tgc acc aac aca cct gtg cag gct ggc gat tgt cct ccc ctc gag ttg atc aca tcc gtc atc caa gac ggc gat atg gtc gac acc ggt ttc ggc gcc atg aac ttc gcc gat ctg cag aca aac aag agc gac gtc cct atc gac atc tgc ggc acc acc tgt aag tac ccc gac tac ctc cag atg gcc gcc gat ccc tac ggc gac cgc ctc ttc ttc ttc ctc agg aaa gag cag atg ttc gcc cgc cat ttc ttc aac cgc gct ggc gag gtc ggc gag ccc gtc ccc gac acc ctc atc atc aag ggc tcc ggt aat cgc acc agc gtg ggc tcc tcc atc tac gtg aac acc ccc tcc ggt agc ctc gtc agc agc gaa gcc cag ctg ttc aac aag ccc tac tgg ttg cag aaa gcc caa ggc cac aat aac ggc atc tgt tgg ggc aat cag ctc ttc gtc acc gtc gtg gac aca acc agg tcc acc aac atg acc ttg tgc gcc agc gtc acc acc agc tcc acc tac acc aac agc gac tac aaa gag tac atg agg cac gtc gaa gaa tac gac ctg caa ttc atc ttc cag ctc tgc tca atc acc ctg agc gcc gag gtg atg gct tac atc cat acc atg aac ccc agc gtc ctc gaa gat tgg aat ttc ggt ctg agc ccc ccc ccc aac ggc acc ctc gaa gac acc tac cgc tac gtg caa agc caa gct atc aca tgc caa aag cct acc ccc gag aag gag aag cca gac cct tac aaa aac ctg tcc ttc tgg gaa gtc aat ctg aag gag aaa ttc agc tcc gag ctg gac caa tac cct ttg ggc agg aaa ttc ctg ctc cag tcc ggc tac cga ggc gga tcc agc atc cga acc ggc gtggga agt ccc gcc gtc agc agt gct agc gcc gct cct agt gga agt ggt gct ggg aca gga cgt taat
[0113]
seq id no.16:6l1cs7nt
caa agc caa gct atc aca tgc caa aag cct acc ccc gag aag gag aag cca gac cct tac aaa aac ctg tcc ttc tgg gaa gtc aat ctg aag gag aaa ttc agc tcc gag ctg gac caa tac cct ttg ggc agg aaa ttc ctg ctc cag tcc ggc tac agg ggc cga tcc agc atc agg acc ggc gtg aaa agg ccc gcc gtc agc aaa gct agc gcc gct cct aag agg aag agg gct aag aca aag cgt taat
[0119]
6l1f(seq id no.19):
[0120]5’‑
ggaattcgccgccaccatgtg-3’;
[0121]
6l1cs1r1(seq id no.20):
[0122]5’‑
cccacgccggttgcgatgctggatcggcctccgtagccggactggagcaggaatt tcct-3’;
[0123]
6l1cs1r2(seq id no.21):
[0124]5’‑
gcaggagcggcgctagctccgctgacggcgggtgctcccacgccggttgcgatgc tgga-3’;
[0125]
6l1cs1r3(seq id no.22):
[0126]5’‑
gctctagaattaacgctttgtcccagctgcggctcctgcaggagcggcgctagct ccgc-3’;
[0127]
6l1cs2r1(seq id no.23):
[0128]5’‑
cacgccggttcggatgctggatccgcctcggtagccggactg-3’;
[0129]
6l1cs2r2(seq id no.24):
[0130]5’‑
aggagcggcgctagccttgctgacggcgggacttcccacgccggttcggatgct-3’;
[0131]
6l1cs2r3(seq id no.25):
[0132]5’‑
gctctagaattaacgctttgtcccagctccgcttccatcaggagcggcgctagcc ttgc-3’;
[0133]
6l1cs3r1(seq id no.26):
[0134]5’‑
cacgccggttcggatgctggatccgcctcggtagccggactg-3’;
[0135]
6l1cs3r2(seq id no.27):
[0136]5’‑
aggagcggcgctagccttgctgacggcgggtccatccacgccggttcggatgct-3’;
[0137]
6l1cs3r3(seq id no.28):
[0138]5’‑
gctctagaattaacgctttgtcccagctctgcttccatcaggagcggcgctagcc ttgc-3’;
[0139]
6l1cs4r1(seq id no.29):
[0140]5’‑
cacgccggttcggatgctggatccgcctcggtagccggactg-3’;
[0141]
6l1cs4r2(seq id no.30):
[0142]5’‑
aggagcggcgctagccttgctgacggcgggacttcccacgccggttcggatgct-3’;
[0143]
6l1cs4r3(seq id no.31):
[0144]5’‑
gctctagaattaacgctttgtatcagctctgcttccatcaggagcggcgctagcc ttgc-3’;
[0145]
6l1cs5r1(seq id no.32):
[0146]5’‑
cacgccggtt cggatgctgg atccgcctcg gtagccggac tg-3’;
[0147]
6l1cs5r2(seq id no.33):
[0148]5’‑
aggagcggcgctagccttgctgacggcgggtccatccacgccggttcggatgct-3’;
[0149]
6l1cs5r3(seq id no.34):
[0150]5’‑
gctctagaattaacgctttgtatcagctctgcttccatcaggagcggcgctagcc ttgc-3’;
[0151]
6l1cs6r1(seq id no.35):
[0152]5’‑
cacgccggtt cggatgctgg atccgcctcg gtagccggac tg-3’;
[0153]
6l1cs6r2(seq id no.36):
[0154]5’‑
aggagcggcgctagcactgctgacggcgggacttcccacgccggttcggatgct-3’;
[0155]
6l1cs6r3(seq id no.37):
[0156]5’‑
gctctagaattaacgtcctgtcccagcaccacttccactaggagcggcgctagca ctgc-3’;
[0157]
6l1cs7r1(seq id no.38):
[0158]5’‑
cacgccggtt gcgatgctgg atccgcctcg gtagccggactg-3’;
[0159]
6l1cs7r2(seq id no.39):
[0160]5’‑
aggagcggcgctagccttgctgacggcgggtccatccacgccggttgcgatgct-3’;
[0161]
6l1cs7r3(seq id no.40):
[0162]5’‑
gctctagaattaacgctttgtcccagctccgcttccactaggagcggcgctagcc ttgc-3’;
[0163]
6l1cs8r1(seq id no.41):
[0164]5’‑
cacgccggtt cggatgctgg agtcgcctcg gtagccggac tg-3’;
[0165]
6l1cs8r2(seq id no.42):
[0166]5’‑
aggagcggcgctagccttgctgacggcgggtcgatccacgccggttcggatgct-3’;
[0167]
6l1cs8r3(seq id no.43):
[0168]5’‑
gctctagaattaacgtcctgtcttagcactctttgcatcaggagcggcgctagcc ttgc-3’。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。