异鼠李素在制备蛋白质酪氨酸磷酸酶shp-1抑制剂中的应用
技术领域
1.本发明涉及生物医药技术领域,尤其是涉及一种异鼠李素在制备蛋白质酪氨酸磷酸酶shp-1抑制剂中的应用。
背景技术:
2.shp-1(sh2-containing tyrosine phosphatase 1)是主要表达于造血细胞的酪氨酸磷酸酶,以前也称造血细胞磷酸酶(hcp)、shptp-1、shp、ptp1c、ptpn6。20世纪90年代初由华盛顿大学等研究组相继分离纯化,并成功克隆其cdna,现已知shp1基因位于第12号染色体的p12-p13区,含17个外显子,全长17kb。sh2结构域最先发现于src样激酶中,这种结构域和某些特定多肽序列内的磷酸酪氨酸残基有很强的亲合力。因此,shp-1的sh2结构域也发挥着同样的功能并借此将shp-1招募至其底物附近。
3.shp-1在造血细胞信号转导中发挥负调节作用,与造血细胞的激活、增生、分化、转化和细胞间的信号转导等有关。几乎在所有的淋巴瘤、白血病细胞株中都发现了shp-1mrna和蛋白水平表达的降低或丧失。
4.随着研究发现,shp-1能够在多种疾病的调控中发挥重要作用,这预示着对shp-1进行有效调控,有可能对疾病产生理想的控制能力。
5.有鉴于此,特提出本发明。
技术实现要素:
6.本发明的目的之一在于提供一种异鼠李素在制备蛋白质酪氨酸磷酸酶shp-1抑制剂中的应用,以至少解决现有技术中存在的技术问题之一。
7.本发明的目的之二在于提供蛋白质酪氨酸磷酸酶shp-1抑制剂在制备预防和/或治疗高血脂的药物中的应用。
8.本发明的目的之三在于提供蛋白质酪氨酸磷酸酶shp-1抑制剂在制备预防和/或治疗高血糖的药物中的应用。
9.为了实现本发明的上述目的,特采用以下技术方案:
10.本发明提供了异鼠李素在制备蛋白质酪氨酸磷酸酶shp-1抑制剂中的应用。
11.进一步的,所述异鼠李素对蛋白质酪氨酸磷酸酶shp-1的半数抑制浓度为12.3μmol/l。
12.进一步的,所述异鼠李素结构对蛋白质酪氨酸磷酸酶shp-1的解离常数为15.60μm。
13.进一步的,所述抑制剂包括竞争性抑制剂。
14.本发明还提供了蛋白质酪氨酸磷酸酶shp-1抑制剂在制备预防和/或治疗高血脂的药物中的应用,所述蛋白质酪氨酸磷酸酶shp-1抑制剂包括异鼠李素。
15.进一步的,所述预防和/或治疗高血脂的药物的有效给药剂量为4~8mg/kg。
16.进一步的,所述药物还包括药学上可接受的辅料。
17.进一步的,所述药物的剂型包括口服制剂和注射剂。
18.进一步的,所述口服制剂包括片剂、胶囊剂、颗粒剂、丸剂、糖浆剂、口服溶液剂、口服混悬剂或口服乳剂。
19.进一步的,所述注射制剂包括注射液或粉针剂。
20.与现有技术相比,本发明至少具备如下有益效果:
21.本发明通过大量的体外实验证实,异鼠李素可以显著抑制蛋白质酪氨酸磷酸酶shp-1的活性,同时经体内实验证实,通过蛋白质酪氨酸磷酸酶shp-1活性的抑制,降低血清中tc、tg和ldl-c的水平,说明异鼠李素对高血脂具有良好的治疗作用。通过将异鼠李素应用在制备预防和/或治疗高血脂的药物中,能够有效降低血脂浓度,从而大大提升高血脂的治疗效果,为临床实验提供依据,也为新药的研发提供新途径。
附图说明
22.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
23.图1为本发明实施例提供的反应溶液中异鼠李素的浓度和抑制率的点线图;
24.图2为本发明实施例提供的以1/v0为纵坐标以1/[s]为横坐标绘制的点线图;
[0025]
图3为本发明实施例提供的以[i]为横坐标κ为纵坐标作图绘制的点线图;
[0026]
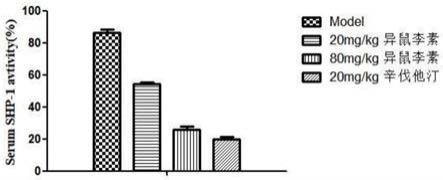
图4为本发明实施例提供的不同实验组对小鼠血清中
△
shp-1的抑制效果图。
具体实施方式
[0027]
除非本文另有定义,连同本发明使用的科学和技术术语应具有本领域普通技术人员通常理解的含义。术语的含义和范围应当清晰,然而,在任何潜在不明确性的情况下,本文提供的定义优先于任何字典或外来定义。在本技术中,除非另有说明,“或”的使用意味着“和/或”。此外,术语“包括”及其他形式的使用是非限制性的。
[0028]
一般地,连同本文描述的细胞和组织培养、分子生物学、免疫学、微生物学、遗传学以及蛋白和核酸化学和杂交使用的命名法和其技术是本领域众所周知和通常使用的那些。除非另有说明,本发明的方法和技术一般根据本领域众所周知,且如各种一般和更具体的参考文献中所述的常规方法来进行,所述参考文献在本说明书自始至终引用和讨论。酶促反应和纯化技术根据制造商的说明书、如本领域通常实现的或如本文所述来进行。连同本文描述的分析化学、合成有机化学以及医学和药物化学使用的命名法、以及其实验室程序和技术是本领域众所周知和通常使用的那些。
[0029]
下面将结合实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0030]
异鼠李素的化学式为c
16h12
o7,是一种植物类黄酮,其结构式如式(ⅰ)所示:
[0031][0032]
目前,广泛知晓的异鼠李素的药理作用包括:止咳祛痰,消食化滞,活血散瘀。用于咳嗽痰多、消化不良、食积腹痛、跌扑瘀肿、瘀血经闭。
[0033]
本发明的发明人通过大量的体外实验证实,异鼠李素对蛋白质酪氨酸磷酸酶shp-1的半数抑制浓度为12.3μmol/l,对蛋白质酪氨酸磷酸酶shp-1的解离常数为15.60μm,可以显著抑制蛋白质酪氨酸磷酸酶shp-1的活性。因此,本发明的第一个方面提供了异鼠李素在制备蛋白质酪氨酸磷酸酶shp-1抑制剂中的应用。
[0034]
需要注意的是,本发明所述的异鼠李素,既可以为实验室制备得到的,也可以是市售直接购得的,只要满足式(ⅰ)的化学结构式即可。
[0035]
基于上述研发结果,本发明的发明人进一步研究发现,通过施用异鼠李素抑制蛋白质酪氨酸磷酸酶shp-1的活性后,实验小鼠血清中tc、tg和ldl-c水平均有不同程度的降低,因此,在本发明的第二个方面提供了蛋白质酪氨酸磷酸酶shp-1抑制剂在制备预防和/或治疗高血脂的药物中的应用,所述蛋白质酪氨酸磷酸酶shp-1抑制剂包括异鼠李素。
[0036]
需要说明的是,本发明通过研究发现异鼠李素具有抑制蛋白质酪氨酸磷酸酶shp-1的活性的功能后,同理,与抑制蛋白质酪氨酸磷酸酶shp-1的活性相关的疾病均可以异鼠李素作为抑制剂产生相应的预防和/或治疗作用,因此,与抑制蛋白质酪氨酸磷酸酶shp-1的活性相关的疾病均应在本发明的保护范围内,例如高血糖、抗氧化等,而非局限于高血脂。
[0037]
可以理解的是,本发明中的预防和/或治疗指的是,施用异鼠李素既可以起到对高血脂的预防作用,又可以起到对高血脂的治疗作用。根据是预防性处理还是治疗性处理可以选择相应的给药剂量和频率。例如,在预防性应用中,以相对低频率的间隔长期给予相对低的剂量。在治疗性应用中,有时需要以相对短的间隔给予相对高的剂量,直至疾病的进展被延缓或停止,并优选地直至个体表现出疾病症状的部分或完全改善,在此之后,可以给予患者预防方案。
[0038]
在一些优选地实施方式中,所述预防和/或治疗高血脂的药物的有效给药剂量为4~8mg/kg,例如可以为,但不限于4mg/kg、5m g/kg、6m g/kg、7mg/kg或8mg/kg。
[0039]
可选地,当将异鼠李素作为预防和/或治疗高血脂的药物时,所述药物还包括药学上可接受的辅料。
[0040]
药学上可接受的辅料是指生产药品和调配处方时,使用的赋形剂和附加剂,是指除活性成分外,在安全性方面已进行了合理的评估,并且包含在药物制剂中的物质。同一药用辅料可用于不同给药途径的药物制剂,且有不同的作用和用途。在本发明提供的药物中添加的药学上可接受的辅料,能够起到赋型、充当载体或提高稳定性的作用,此外,还具有
增溶、助溶或缓控释等重要功能。
[0041]
典型但非限制性的药学上可接受的辅料包括:溶剂、抛射剂、增溶剂、助溶剂、乳化剂、着色剂、黏合剂、崩解剂、填充剂、润滑剂、湿润剂、渗透压调节剂、稳定剂、助流剂、矫味剂、防腐剂、助悬剂、包衣材料、芳香剂、抗黏着剂、抗氧剂、螯合剂、渗透促进剂、ph调节剂、缓冲剂、增塑剂、表面活性剂、发泡剂、消泡剂、增稠剂、包合剂、保湿剂、吸收剂、稀释剂、絮凝剂与反絮凝剂、助滤剂或释放阻滞剂中的一种或多种。
[0042]
可选地,所述药物的剂型包括口服制剂和注射剂,口服制剂例如可以为,但不限于片剂、胶囊剂、颗粒剂、丸剂、糖浆剂、口服溶液剂、口服混悬剂或口服乳剂;注射剂例如可以为,但不限于注射液或粉针剂。
[0043]
此外,本发明还提供了蛋白质酪氨酸磷酸酶shp-1抑制剂在制备预防和/或治疗高血糖的药物中的应用,所述蛋白质酪氨酸磷酸酶shp-1抑制剂包括异鼠李素。
[0044]
下面通过实施例对本发明作进一步说明。如无特别说明,实施例中的材料为根据现有方法制备而得,或直接从市场上购得。
[0045]
实施例1抑制率测定实验
[0046]
1.异鼠李素对shp-1抑制率的测定
[0047]
1.1反应体系
[0048]
25mm mops-naoh(ph 7.0)、1mm dtt、0.1m nacl、1mm edta、1mg/ml bsa、4mmp-npp、蛋白样品(10μg/ml)、异鼠李素。
[0049]
1.2实验方法
[0050]
按上述体系将各溶液加入酶标板中于微量振荡器上混匀,置37℃恒温培养箱中反应30min后,于405nm处测定吸收值。
[0051]
1.3计算方法
[0052]
以未加入待测样品的实验体系为空白对照,测定其在405nm处的吸收值为a0,其余加入异鼠李素的各实验体系的吸收值为a,异鼠李素对shp-1的抑制率为:
[0053][0054]
1.4 ic
50
的测定
[0055]
1.4.1 ic
50
及计算原理
[0056]
ic
50
即半数抑制浓度,是使酶活性降至原活性一半时的抑制剂浓度。可以用来做抑制剂抑制能力大小的评判标准。以不同浓度的抑制剂与相同条件下的酶-底物反应体系相互作用,在单位时间内将产物的增加量与未加抑制剂的反应体系对比,可以得到抑制剂对酶的抑制能力的曲线,选择合适的抑制剂浓度,就可以得到ic
50
的数值。
[0057]
1.4.2 ic
50
的测定方法
[0058]
实验体系及方法同1,将异鼠李素提取液稀释成不同浓度(分别稀释5、10、20、40、80、100、160、250、320、400、500、640倍),分别测定其对shp-1的抑制率,以抑制率对提取液的浓度作图,计算ic
50
,如图1所示。
[0059]
1.5.抑制类型的确定
[0060]
实验体系及方法同1,分别在确定的异鼠李素浓度下,改变p-npp的浓度(10mm、
20mm、40mm、60mm、80mm、100mm、120mm、160mm、200mm),测定异鼠李素对shp-1的抑制率,根据下列公式计算反应速率:
[0061][0062]
其中,ε:摩尔消光系数
[0063]
l:比色皿内径(cm)
[0064]
t:反应时间(min)
[0065]
根据检测结果得到酶促反应的初速率(v0),其结果列于表1中。
[0066]
表1 酶促反应的初速率和初始底物浓度
[0067]
[s](mmol/l)0.250.5124v0(μmol/l*min)0.050.1250.2514
[0068]
表1中[s]为初始底物浓度即p-npp的初始浓度。
[0069]
根据表2的数据以1/v0为纵坐标,以1/[s]为横坐标绘制点线图,如图2所示。
[0070]
结合表1和图2可知,不同抑制剂浓度的l-b方程交于y轴上,证明异鼠李素对shp-1的抑制为竞争性抑制。
[0071]
1.6解离常数的确定
[0072]
根据公式2计算κ,其结果列于表2中:
[0073][0074]
其中km为米氏常数,vm是酶促反应的最大速度,[i]是抑制剂浓度,ki是抑制常数。
[0075]
表2 解离常数和抑制剂浓度的数据
[0076]
[i](μmol/l)0125250κ0146331
[0077]
以[i]为横坐标,κ为纵坐标作图,得一直线,如图3所示。由图可知其与x轴的交点确定异鼠李素对shp-1解离常数为15.6μmol/l。
[0078]
实施例2体内抑制实验
[0079]
40只昆明小鼠,适应性饲喂1周,随机分组每组10只(n=10)。分为正常组、低剂量给药组、高剂量给药组和阳性组,均为4~6g/d只,自由饮水。灌胃给药:阳性对照组小鼠体灌胃0.01g/(kg
·
d)辛伐他汀,高剂量组每天给与80mg/kg异鼠李素,低剂量组每天给与20mg/kg异鼠李素,连续灌胃30d,末次灌喂前16h停食停水,末次灌喂1h后即眼眶静脉采血。各组采血后检测血清中
△
shp-1的表达量。
[0080]
结果显示,不同剂量的异鼠李素在给药后小鼠的血清对
△
shp-1有明显的抑制作用,且随着给药剂量的增大,抑制作用越明显。其中高剂量组小鼠的血清对
△
shp-1的抑制作用达到了74.4%,低剂量组的抑制率分别是45.9%,辛伐他汀组的抑制率是80%,如图4所示。
[0081]
实施例3降血脂实验
[0082]
3.1高脂模型小鼠建立
[0083]
50只昆明小鼠,适应性饲喂1周,随机分组每组10只(n=10)。分为正常组、模型组、低剂量给药组、高剂量给药组和阳性组,正常组饲喂基础饲料,模型组和给药组饲喂高脂饲料,均为4~6g/d只,自由饮水。连续饲喂30d。每5天称重并记录体重,灌胃给药:阳性对照组小鼠体灌胃0.01g/(kg
·
d)辛伐他汀,高脂模型组和空白对照组以相同方法灌胃等体积生理盐水,连续灌胃30d,每天称重1次,末次灌喂前16h停食停水,末次灌喂1h后即眼眶静脉采血。各组采血后血样室温放置1h后4℃冰箱过夜,3 000r/min离心15min,分离上层血清,-20℃保存,测各项指标按试剂盒说明书测定tc、tg、ldl-c、hdl-c。
[0084]
3.2实验结果:
[0085]
结果显示:从第二周开始,高脂组的体重就明显高于正常组,和模型组相比,给药组小鼠血清中tc、tg和ldl-c水平均有不同程度的降低(见表3)。
[0086]
表3 各实验组小鼠的血清血脂指标
[0087]
实验组tctgldl-chdl-c正常组2.62
±
0.311.31
±
0.230.52
±
0.531.56
±
0.25高脂模型组5.71
±
0.621.62
±
0.360.83
±
0.462.57
±
0.3820mg/kg异鼠李素组4.94
±
0.531.52
±
0.520.85
±
0.632.48
±
0.5980mg/kg异鼠李素组4.35
±
0.421.46
±
0.370.71
±
0.851.86
±
0.6820mg/kg辛伐他汀4.27
±
0.371.49
±
0.380.64
±
0.491.95
±
0.52
[0088]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。