1.本发明涉及药物化学领域,具体涉及一种可以用作5-羟色胺再摄取抑制剂和/或5-ht
1a
受体激动剂的取代的嘧啶哌嗪化合物的制备方法。
背景技术:
2.5-羟色胺(5-hydroxytryptamine,5-ht),一种在大脑和神经系统中传递信号的神经递质,在中枢神经系统(cns)功能障碍中,尤其是焦虑、抑郁、侵略和冲动情绪中,扮演着重要的角色。拮抗或激动一定类型的5-羟色胺受体可以有效地调控中枢神经系统功能障碍。5-ht
1a
受体,一种g蛋白偶联受体,广泛分布在能接受到源于中缝核的5-羟色胺的区域;激活突触前膜的5-ht
1a
受体可以抑制酪氨酸羟化酶的合成和谷氨酸通道(产生于内侧前额叶皮质,指向中缝核)的活性,从而间接降低5-羟色胺的输运(jonathan savitz,irwin lucki,wayne c.drevets.5-ht
1a receptor function in major depressive disorder.prog neurobiol.2009,88(1):17-31)。
3.专利申请cn109574993a公开了一类具有选择性5-羟色胺再摄取抑制活性和/或5-ht
1a
受体激动活性的化合物,具体公开了具有式(i)所示结构的取代的嘧啶哌嗪化合物及其制备方法。
[0004][0005]
其中,具体公开了如下所示的式(i)所示化合物的制备方法:
[0006][0007]
其中,上述方法中,氯化氢的乙酸乙酯溶液的用量较大(约10.0倍当量),且易挥发,容易造成空气污染,同时它的制备过程复杂,不适合工业化生产。而最后一步取代反应
的反应时间长(36小时),也不适合工业化生产;进一步研究发现,在放大生产时,最后一步反应的反应时间需进一步延长,且反应过程不可控。
技术实现要素:
[0008]
为克服现有技术中的上述缺陷,本发明提供了一种制备式(i)所示化合物的新方法。该方法原料便宜且易得,条件温和、环保,反应时间短,且安全可控,总收率高,特别适合工业化生产。
[0009]
一方面,本发明提供一种制备式(i)所示化合物的方法,包括:
[0010]
步骤1:式(ii)所示化合物在溶剂1中,在碱1的作用下反应得到式(i)所示化合物,
[0011][0012]
在一些实施方案中,所述碱1为氢氧化钠或碳酸铯。
[0013]
在另一些实施方案中,所述碱1的用量为式(ii)所示化合物的多倍当量;在又一些实施方案中,所述碱1的用量为式(ii)所示化合物的1.0-3.0倍当量。
[0014]
在一些实施方案中,所述溶剂1是指醇类溶剂。在另一些实施方案中,所述溶剂1为甲醇、乙醇、异丙醇或其组合。
[0015]
在一些实施方案中,所述步骤1的反应是在一定反应温度下进行的;在另一些实施方案中,所述反应温度为40℃到65℃;在另一些实施方案中,所述反应温度为40℃到60℃;在另一些实施方案中,所述反应温度为50℃到65℃;在另一些实施方案中,所述反应温度为40℃、50℃、60℃或65℃。
[0016]
在一些实施方案中,本发明所述的制备式(i)所示化合物的方法还包括式(ii)所示化合物的制备方法,其包括:
[0017]
步骤2:式(iii)所示化合物和式(iv)所示化合物在溶剂2中,在碱2和催化剂的作用下反应得到式(ii)所示化合物,
[0018][0019]
在另一些实施方案中,所述步骤2中使用的催化剂为碘化钠或碘化钾。
[0020]
在另一些实施方案中,所述催化剂的用量为式(iii)所示化合物的0.1-0.4倍当量;优选地,所述催化剂的用量为式(iii)所示化合物的0.2倍当量。在另一些实施方案中,所述催化剂的用量为式(iii)所示化合物的0.1-0.2倍当量。
[0021]
在另一些实施方案中,所述溶剂2为n-甲基吡咯烷酮或n,n-二甲基甲酰胺。
[0022]
在另一些实施方案中,所述碱2为碳酸钠或碳酸钾。
[0023]
在另一些实施方案中,所述碱2的用量为式(iii)所示化合物的多倍当量;在又一些实施方案中,所述碱2的用量为式(iii)所示化合物的2.0-12.0倍当量;在又一些实施方
案中,所述碱2的用量为式(iii)所示化合物的2.0-6.0倍当量;在又一些实施方案中,所述碱2的用量为式(iii)所示化合物的2.0-4.0倍当量;在又一些实施方案中,所述碱2的用量为式(iii)所示化合物的3.0-4.0倍当量;在又一些实施方案中,所述碱2的用量为式(iii)所示化合物的2.0倍当量、3.0倍当量、3.5倍当量、4.0倍当量、4.5倍当量、5.0倍当量或6.0倍当量。
[0024]
在另一些实施方案中,所述步骤2的反应是在一定反应温度下进行的;在又一些实施方案中,所述步骤2的反应温度为60℃-90℃。在又一些实施方案中,所述步骤2的反应温度为70℃-90℃;在又一些实施方案中,所述步骤2的反应温度为75℃-90℃;在又一些实施方案中,所述步骤2的反应温度为75℃;在又一些实施方案中,所述步骤2的反应温度为80℃;在又一些实施方案中,所述步骤2的反应温度为90℃。
[0025]
在另一些实施方案中,所述步骤2的反应时间为2-8小时;在又一些实施方案中,所述步骤2的反应时间为4-6小时。在又一些实施方案中,所述步骤2的反应时间为4小时;在又一些实施方案中,所述步骤2的反应时间为5小时;在又一些实施方案中,所述步骤2的反应时间为6小时。
[0026]
在一些实施方案中,本发明所述的制备式(i)所示化合物的方法还包含式(iii)所示化合物的制备方法,包括:
[0027]
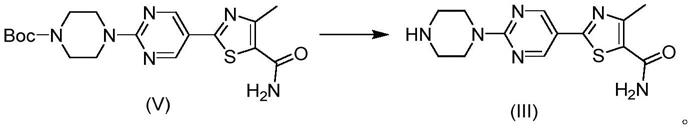
步骤3:式(v)所示化合物在溶剂3中在酸的作用下反应脱除保护基得到式(iii)所示化合物,
[0028][0029]
在另一些实施方案中,所述溶剂3为二氯甲烷。
[0030]
在另一些实施方案中,所述酸为硫酸、对甲苯磺酸、磷酸或其溶液。其中,所述酸可以配制成溶液来施用,一般选择对步骤3反应惰性的溶剂来进行配制,所述溶液包括但不限于,酸的乙酸乙酯溶液。
[0031]
在另一些实施方案中,所述酸为硫酸的乙酸乙酯溶液、对甲苯磺酸的乙酸乙酯溶液或磷酸的乙酸乙酯溶液。
[0032]
在另一些实施方案中,所述酸的用量为式(v)所示化合物的多倍当量。在又一些实施方案中,所述酸的用量为式(v)所示化合物的2.0-6.0倍当量;优选地,所述酸的用量为式(v)所示化合物的3.0-6.0倍当量。
[0033]
在另一些实施方案中,所述步骤3的反应在水的存在下进行。
[0034]
在又一些实施方案中,所述水的用量为式(v)所示化合物的1.0-4.0倍当量。
[0035]
在又一些实施方案中,所述酸的用量为式(v)所示化合物的多倍当量。在又一些实施方案中,所述酸的用量为是式(v)所示化合物的2.0-6.0倍当量;优选地,所述酸的用量为式(v)所示化合物的2.5-4.0倍当量;更优选地,所述酸的用量为式(v)所示化合物的3.0倍当量。
[0036]
优选地,所述步骤3中,式(v)所示化合物在水的存在下,在硫酸的作用下反应脱除保护基得到式(iii)所示化合物。其中,所述硫酸可以配制成硫酸的乙酸乙酯溶液来施用;
和“所述”旨在包括“至少一个”或“一个或多个”。因此,本文所使用的这些冠词是指一个或多于一个(即至少一个)宾语的冠词。例如,“一组分”指一个或多个组分,即可能有多于一个的组分被考虑在所述实施方案的实施方式中采用或使用。
[0051]
在本发明的上下文中,所有在此公开了的数字均为近似值。每一个数字的数值有可能会出现1%、2%、5%、7%、8%或10%等差异。每当公开一个具有n值的数字时,任何具有n /-1%,n /-2%,n /-3%,n /-5%,n /-7%,n /-8%或n /-10%值以内的数字会被明确地公开,其中“ /
‑”
是指加或减。每当公开一个数值范围中的一个下限,dl,和一个上限,du,时,任何处于该公开了的范围之内的数值会被明确地公开。
[0052]
本发明所述的“产物含量”或“产物比例”指的是该反应反应完毕后,经hplc检测的反应体系中产物的含量。
[0053]
本发明中“室温”指的是温度由大约10℃到大约40℃。在一些实施例中,“室温”指的是温度由大约20℃到大约30℃;在另外一些实施例中,“室温”指的是20℃,22.5℃,25℃,27.5℃等等。
实施例
[0054]
实施例1 4-甲基-2-(2-(哌嗪-1-基)嘧啶-5-基)噻唑-5-甲酰胺的合成
[0055][0056]
将酸慢慢加入乙酸乙酯(50ml)中,配制待用。将4-(5-(5-甲酰胺基-4-甲基噻唑-2-基)嘧啶-2-基)哌嗪-1-甲酸叔丁酯(10.0g,24.72mmol)(制备方法参见专利申请cn109574993a)、二氯甲烷(100ml)和水加入反应瓶中,加入酸的乙酸乙酯溶液。室温反应12小时,取样送检hplc,抽滤,滤饼置于50℃真空干燥烘干,得到浅黄色固体。示例1-12的实验结果如表a所示。
[0057]
表a
[0058]
示例水的用量酸酸的用量产物含量示例1n/a对甲苯磺酸6.0倍当量99.03%示例2n/a三氟乙酸6.0倍当量0.69%示例3n/a乙酸6.0倍当量0.08%示例4n/a磷酸6.0倍当量88.90%示例5n/a硫酸6.0倍当量82.31%示例6n/a硫酸2.0倍当量75.99%示例7n/a硫酸3.0倍当量76.09%示例81.0倍当量硫酸3.0倍当量92.61%示例92.0倍当量硫酸3.0倍当量98.17%示例104.0倍当量硫酸3.0倍当量98.56%示例112.0倍当量硫酸2.5倍当量94.36%示例122.0倍当量硫酸4.0倍当量98.55%
[0059]
注:“n/a”表示示例中的反应并未使用该物料。“当量”是指所述物料相对于反应底
物4-(5-(5-甲酰胺基-4-甲基噻唑-2-基)嘧啶-2-基)哌嗪-1-甲酸叔丁酯的摩尔量的倍数,例如,2.0倍当量,表示所述物料的摩尔量是反应底物4-(5-(5-甲酰胺基-4-甲基噻唑-2-基)嘧啶-2-基)哌嗪-1-甲酸叔丁酯的摩尔量的2倍。
[0060]
示例13:
[0061]
将硫酸(1.82kg,18.54mol)慢慢加入乙酸乙酯(12.5l)中,配制待用。将4-(5-(5-甲酰胺基-4-甲基噻唑-2-基)嘧啶-2-基)哌嗪-1-甲酸叔丁酯(2.50kg,6.18mol)、二氯甲烷(25l)和水(222g,12.36mol)加入反应釜中,加入硫酸的乙酸乙酯溶液。室温反应12小时,取样送检hplc,产物含量97.94%,停止反应,抽滤,收集滤饼。将滤饼、水(38l)和碳酸钠(3.93kg,37.08mol)加入反应釜中,室温搅拌2小时,抽滤,滤饼置于50℃真空干燥烘干,得到浅黄色固体(1.86kg,收率:98.9%)。
[0062]
表征数据:
[0063]
ms(esi,pos.ion)m/z:305.10[m h]
;
[0064]1h nmr(400mhz,d2o)δ(ppm):8.36(d,j=39.5hz,2h),3.98(t,j=18.6hz,4h),3.29(d,j=4.7hz,4h),2.30(d,j=23.8hz,3h).
[0065]
实施例2 2-(2-(4-(3-(5-氰基-1-对甲苯磺酰基-1h-吲哚-3-基)丙基)哌嗪-1-基)嘧啶-5-基)-4-甲基噻唑-5-甲酰胺的合成
[0066][0067]
将4-甲基-2-(2-(哌嗪-1-基)嘧啶-5-基)噻唑-5-甲酰胺(2.0g,6.57mmol)、3-(3-氯丙基)-1-对甲苯磺酰基-1h-吲哚-5-腈(2.45g,6.57mmol)、溶剂(20ml)、一定量的碱和碘化钠(197mg,1.31mmol)加入反应瓶中,加热至一定温度搅拌反应4小时,取样送检hplc,停止反应,抽滤,滤液加入反应瓶中,再慢慢加入水(10ml),室温搅拌4小时,抽滤,滤饼用水(20ml)洗涤,滤饼在60℃真空干燥得到黄色固体。示例1-14的实验结果如表b所示。
[0068]
表b
[0069]
示例反应温度碱碱的用量反应溶剂产物含量示例190℃碳酸钾4.0倍当量n,n-二甲基甲酰胺71.5%示例290℃碳酸钠4.0倍当量n,n-二甲基甲酰胺72.01%示例390℃三乙胺4.0倍当量n,n-二甲基甲酰胺40.64%示例490℃n,n-二异丙基乙胺4.0倍当量n,n-二甲基甲酰胺50.28%示例590℃碳酸钠4.0倍当量n,n-二甲基甲酰胺72.01%示例690℃碳酸钠4.0倍当量n-甲基吡咯烷酮88.04%示例790℃碳酸钠4.0倍当量乙腈13.27%示例890℃碳酸钠4.0倍当量丙酮15.61%示例960℃碳酸钠4.0倍当量n-甲基吡咯烷酮24.93%示例1070℃碳酸钠4.0倍当量n-甲基吡咯烷酮76.74%示例1175℃碳酸钠4.0倍当量n-甲基吡咯烷酮87.28%示例1280℃碳酸钠4.0倍当量n-甲基吡咯烷酮86.48%
示例1375℃碳酸钠3.0倍当量n-甲基吡咯烷酮84.38%示例1475℃碳酸钠2.0倍当量n-甲基吡咯烷酮83.28%
[0070]
注:“当量”是指所述物料相对于反应底物4-甲基-2-(2-(哌嗪-1-基)嘧啶-5-基)噻唑-5-甲酰胺的摩尔量的倍数,例如,2.0倍当量,表示所述物料的摩尔量是反应底物4-甲基-2-(2-(哌嗪-1-基)嘧啶-5-基)噻唑-5-甲酰胺的摩尔量的2倍。
[0071]
示例15:
[0072]
将按照实施例1示例13方法制备得到的4-甲基-2-(2-(哌嗪-1-基)嘧啶-5-基)噻唑-5-甲酰胺(1.86kg,6.11mol)、3-(3-氯丙基)-1-对甲苯磺酰基-1h-吲哚-5-腈(2.28kg,6.11mol)、n-甲基吡咯烷酮(18.6l)、碳酸钠(2.59kg,24.44mol)和碘化钠(0.18kg,1.22mol)加入反应釜中,在75℃下搅拌反应6小时,取样送检hplc,产物含量89.58%,停止反应,抽滤,滤液加入反应釜中,再慢慢加入水(9l),搅拌4小时,抽滤,滤饼用水(19l)室温打浆2小时,抽滤,滤饼经60℃真空干燥得到黄色固体(3.32kg,收率:85.1%)。
[0073]
表征数据:
[0074]
ms(esi,pos.ion)m/z:641.15[m h]
;
[0075]1h nmr(400mhz,dmso-d6)δ(ppm):8.83(s,2h),8.23(s,1h),8.08(d,j=8.6hz,1h),7.90(d,j=8.3hz,2h),7.80(s,1h),7.74(d,j=8.6hz,1h),7.58(s,2h),7.40(d,j=8.2hz,2h),3.79(brs,4h),2.72(t,j=7.3hz,2h),2.60(s,3h),2.39(brs,4h),2.32(s,3h),2.29(d,j=7.2hz,2h).
[0076]
实施例3 2-(2-(4-(3-(5-氰基-1h-吲哚-3-基)丙基)哌嗪-1-基)嘧啶-5-基)-4-甲基噻唑-5-甲酰胺的合成
[0077][0078]
将2-(2-(4-(3-(5-氰基-1-对甲苯磺酰基-1h-吲哚-3-基)丙基)哌嗪-1-基)嘧啶-5-基)-4-甲基噻唑-5-甲酰胺(2.00g,3.12mmol),溶剂(20ml)和一定量的碱加入反应瓶中,升温至一定温度搅拌反应5小时,取样送检hplc,停止反应,降温至室温,抽滤,滤饼用水(10ml)洗涤,滤饼在60℃真空干燥得到淡黄色固体。示例1-12的实验结果如表c所示。
[0079]
表c
[0080][0081][0082]
注:“当量”是指所述物料相对于反应底物2-(2-(4-(3-(5-氰基-1-对甲苯磺酰基-1h-吲哚-3-基)丙基)哌嗪-1-基)嘧啶-5-基)-4-甲基噻唑-5-甲酰胺的摩尔量的倍数,例如,2.0倍当量,表示所述物料的摩尔量是反应底物2-(2-(4-(3-(5-氰基-1-对甲苯磺酰基-1h-吲哚-3-基)丙基)哌嗪-1-基)嘧啶-5-基)-4-甲基噻唑-5-甲酰胺的摩尔量的2倍。
[0083]
示例13:
[0084]
将按照实施例2示例15的方法制备得到的2-(2-(4-(3-(5-氰基-1-对甲苯磺酰基-1h-吲哚-3-基)丙基)哌嗪-1-基)嘧啶-5-基)-4-甲基噻唑-5-甲酰胺(3.30kg,5.15mol)、甲醇(33l)和碳酸铯(3.36kg,10.30mol)加入反应釜中,升温至60℃搅拌反应5小时,取样送检hplc,产物含量97.51%,停止反应,降温至室温,抽滤,滤饼用水(33l)洗涤,滤饼在60℃真空干燥得到淡黄色固体(2.30kg,收率:92.0%)。
[0085]
表征数据:
[0086]
ms(esi,pos.ion)m/z:487.90[m h]
;
[0087]1h nmr(400mhz,dmso-d6)δ(ppm):11.38(s,1h),8.82(s,2h),8.10(s,1h),7.57(s,2h),7.50(d,j=8.4hz,1h),7.40(d,j=8.4hz,1h),7.35(s,1h),3.84(brs,4h),2.76(t,j=7.1hz,2h),2.60(s,3h),2.43(brs,4h),2.36(t,j=6.7hz,2h),1.91~1.75(m,2h)。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。