1.本发明属于医药化工技术领域,具体涉及一种酰胺化合物的晶型及其制备方法。
背景技术:
2.aticaprant(cas号:1174130-61-0)是一种可渗透中枢神经的kappa opioid(k阿片样)受体拮抗剂,目前处于治疗重度抑郁症的临床试验中。
3.aticaprant结构如下式所示:
[0004][0005]
因药物的晶型形式对药物的制备、药物制剂的制备、储层、应用和溶出、生物利用度等存在重要影响,不同晶型可能在多方面存在差异,可能导致药物制剂的药效、安全性及应用存在明显差异或易不符合质量要求的问题,因此需要研究药物的晶型形式。发明人对aticaprant的晶型进行了相关研究,发现了可以应用的新晶型。
技术实现要素:
[0006]
发明概述
[0007]
本发明主要涉及化合物aticaprant的新晶型。本发明提供的新晶型具有稳定、有利于实施应用的特性。
[0008]
另一方面,本发明还提供了新晶型的制备方法和组合物等。
[0009]
术语定义
[0010]
本发明意图涵盖所有的替代、修改和等同技术方案,它们均包括在如权利要求定义的本发明范围内。本领域技术人员应认识到,许多与本文所述类似或等同的方法和材料能够用于实践本发明。本发明绝不限于本文所述的方法和材料。在所结合的文献、专利和类似材料的一篇或多篇与本技术不同或相矛盾的情况下(包括但不限于所定义的术语、术语应用、所描述的技术等等),以本技术为准。
[0011]
应进一步认识到,本发明的某些特征,为清楚可见,在多个独立的实施方案中进行了描述,但也可以在单个实施例中以组合形式提供。反之,本发明的各种特征,为简洁起见,在单个实施方案中进行了描述,但也可以单独或以任意合适的子组合提供。
[0012]
除非另外说明,本发明所使用的所有科技术语具有与本发明所属领域技术人员的通常理解相同的含义。本发明涉及的所有专利和公开出版物通过引用方式整体并入本发明。
[0013]
除非另外说明,应当应用本文所使用的下列定义。出于本发明的目的,化学元素与元素周期表cas版,和1994年第75版《化学和物理手册》一致。此外,有机化学一般原理可参
考"organic chemistry",thomas sorrell,university science books,sausalito:1999,和"march's advanced organic chemistry”by michael b.smith and jerry march,john wiley&sons,new york:2007中的描述,其全部内容通过引用并入本文。
[0014]
术语“包含”或“包括”为开放式表达,即包括本发明所指明的内容,但并不排除其他方面的内容。
[0015]
术语“相对强度”是指将归属于某一晶型的一组衍射峰中的第一强峰的强度定义为100%时,其它峰的强度与第一强峰的强度的比值。
[0016]
在本发明的上下文中,x-射线粉末衍射图中的2θ(又称2theta或衍射峰)值均以度(
°
)为单位。
[0017]
当提及图谱和/或图中数据,术语“衍射峰”是指本领域的技术人员不会归属于背景噪音的一个特征。
[0018]
所述晶体的x-射线粉末衍射峰,其x-射线粉末衍射图谱的2θ或衍射峰的量度有实验误差,在一台机器和另一台机器之间以及一个样品和另一个样品之间,x-射线粉末衍射图谱的2θ或衍射峰的量度可能会略有差别,所述实验误差或差别的数值可能是 /-0.2个单位或 /-0.1个单位或 /-0.05个单位,因此所述2θ或衍射峰的数值不能视为绝对的。
[0019]
所述晶体的差示扫描量热曲线(dsc)有实验误差,在一台机器和另一台机器之间以及一个样品和另一个样品之间,吸热峰的位置和峰值可能会略有差别,实验误差或差别的数值可能小于等于4℃,或小于等于3℃,或小于等于2℃,或小于等于1℃,因此所述dsc吸热峰的峰位置或峰值的数值不能视为绝对的。
[0020]
所述晶体的热重分析曲线(tga)有实验误差,在一台机器和另一台机器之间以及一个样品和另一个样品之间,吸热曲线或失重率可能会略有差别,实验误差或差别的数值可能小于等于0.004%或0.003%或0.002%或0.001%,因此所述热重分析曲线或其失重率不能视为绝对的。
[0021]
在本发明上下文中,无论是否使用“大约”或“约”等字眼,所有在此公开了的数字均为近似值,基于原数值,每一个数字的数值有可能会出现 /-1%, /-2%,或 /-5%等差异。当大约用来形容x-射线粉末衍射峰的2θ(又称2theta或衍射峰)值时,大约表示所述2θ值可能有 /-0.2个单位或 /-0.1个单位或 /-0.05个单位差异。
[0022]“室温”是指温度在大约20℃-35℃或大约23℃-28℃或大约25℃。
[0023]
术语“良溶剂”可以是单一溶剂或混合溶剂,指样品在该单一溶剂或混合溶剂中的溶解度大于1g/l,或大于2g/l,或大于3g/l,或大于4g/l,或大于5g/l,或大于6g/l,或大于7g/l,或大于8g/l,或大于9g/l,或大于10g/l,或大于15g/l,或大于20g/l,或大于30g/l,或大于40g/l,或大于50g/l,或大于60g/l,或大于70g/l,或大于80g/l,或大于100g/l。在一些实施例中,样品在良溶剂中的溶解度比反溶剂大;在一些实施例中,良溶剂和反溶剂对样品的溶解度之差大约为10%,20%,30%,40%,50%,60%,70%,80%或90%;在一些实施例中,良溶剂对样品的溶解度比反溶剂大,大于10%,20%,30%,40%,50%,60%,70%,80%或90%。
[0024]
发明详述
[0025]
专利申请wo2009094260等现有技术公开了aticaprant的制备方法,但未公开晶型相关信息。发明人根据这些公开的方法获得产物,经过检测,发现可以获得两种不同的晶
型,分别称为晶型i和晶型ii。
[0026]
所得晶型i的x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为3.7,4.4,5.1,6.1,8.7,10.2,12.3,14.2,15.3,15.7,18.1,18.3,19.2和22.7的位置有衍射峰。
[0027]
所述晶型i的x-射线粉末衍射(xrpd)图如图1所示。
[0028]
所述晶型i的差示扫描量热曲线(dsc)在65℃-80℃具有吸热峰,峰顶值为78℃,其差示扫描量热曲线(dsc)如图2所示。
[0029]
所述晶型i的重分析曲线(tga)在50℃-125℃有失重,失重量为0.24%,其热重分析曲线(tga)如图3所示。
[0030]
所得晶型ii,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.60,7.85,10.20,11.80,13.83,15.11,15.78,17.63,21.96,6.80,15.36,18.41,18.77,19.26,19.88,20.34,20.60,22.86,24.11,25.15,26.80,27.60,28.00和34.41的位置具有衍射峰,其x-射线粉末衍射(xrpd)图如图4所示。
[0031]
所述晶型ii的差示扫描量热曲线(dsc)中在93℃-98℃具有吸热峰,峰顶值为97℃,其差示扫描量热曲线(dsc)如图5所示。
[0032]
所述晶型ii样品的热重分析曲线在50℃-200℃间无明显失重,失重量为0.12%,其热重分析曲线(tga)如图6所示。
[0033]
进一步研究发现,晶型i在60℃、相对湿度75%的条件下放置5天,可以发生转晶,转变为本发明下述的晶型e。晶型ii在高温、高湿或光照条件下较为稳定,不易发生晶型转变,但晶型ii对有机溶剂具有较高的溶解性或润湿性,类似于化合物因水潮解,这种性质对某些制剂的制备带来不利影响,特别是需要达到长效或者缓释的制剂。
[0034]
对于需要达到长效或者缓释的制剂而言,原料药稳定、具有一定的溶解性是有利的,对于存在多晶型的原料药来说,稳定而又溶解性相对低的晶型更具有优势。
[0035]
鉴于现有技术所得晶型存在不足,发明人对aticaprant的晶型进行了深入研究。经过研究,发明人开发了aticaprant的新晶型。
[0036]
一方面,发明人通过研究开发了aticaprant的新晶型,包括晶型d,晶型e,晶型f,晶型g或晶型h。
[0037]
一种aticaprant的新晶型,称为晶型d,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.06,4.79,7.96,10.33,11.86,13.99,15.05,15.77,18.02,18.96,19.70,20.63和22.70的位置有衍射峰。
[0038]
在一些实施方式中,所述晶型d的x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.06,4.79,6.99,7.96,10.33,11.86,13.99,15.05,15.77,17.70,18.02,18.96,19.70,20.63,20.86,22.39,22.70,24.29,24.95和27.13的位置有衍射峰。
[0039]
在一些实施方式中,晶型d的x-射线粉末衍射(xrpd)图如图7所示。
[0040]
所述晶型d还具有如下特性,其差示扫描量热曲线(dsc)在95℃-104℃具有吸热峰。在一些实施方式中,晶型d的差示扫描量热曲线(dsc)在97℃-104℃具有吸热峰,峰顶值为101℃。在一些实施方式中,晶型d的差示扫描量热曲线(dsc)如图8所示。
[0041]
所述晶型d还具有如下特性,其热重分析曲线(tga)在50℃-200℃间有失重,失重量约为0.23%。在一些实施方式中,晶型d的热重分析曲线(tga)如图9所示。
[0042]
经过研究发现,晶型d在高温条件下不稳定,易发生转晶,其在60℃、相对湿度75%
的条件下放置5天,转变为前述的晶型ii。
[0043]
一种aticaprant的新晶型,称为晶型e,其x-射线粉末衍射图谱具有至少3个选自2θ(单位:度,
°
)为9.31,11.87,12.96,13.39,14.64,15.19,18.25,19.06,19.80,20.83,23.53,24.09,24.39,26.29和26.98的衍射峰。
[0044]
一些实施方式中,所述晶型e,其x-射线粉末衍射图谱具有至少6个或9个或12个选自2θ(单位:度,
°
)为9.31,11.87,12.96,13.39,14.64,15.19,18.25,19.06,19.80,20.83,23.53,24.09,24.39,26.29和26.98的衍射峰。
[0045]
一些实施方式中,所述晶型e,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为9.31,11.87,12.96,13.39,14.64,15.19,18.25,19.06,19.80,20.83,23.53,24.09,24.39,26.29和26.98的位置有衍射峰。
[0046]
一些实施方式中,所述晶型e的x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为9.31,11.87,12.96,13.39,14.64,15.19,17.35,18.25,19.06,19.80,20.83,21.65,22.26,22.68,23.53,24.09,24.39,25.50,26.29和26.98的位置有衍射峰。
[0047]
一些实施方式中,所述晶型e的x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为3.20,9.31,11.87,12.14,12.96,13.39,14.64,15.19,16.73,17.35,18.05,18.25,18.64,19.06,19.80,20.83,21.41,21.65,22.26,22.68,23.10,23.53,24.09,24.39,24.83,25.50,26.29,26.98,28.77,30.79和33.00的位置有衍射峰。
[0048]
在一些实施方式中,晶型e的x-射线粉末衍射(xrpd)图如图10所示。
[0049]
所述晶型e还具有如下特性,其差示扫描量热曲线(dsc)中在100℃-105℃具有吸热峰,峰顶值为104℃。在一些实施方式中,晶型e的差示扫描量热曲线(dsc)如图11所示。
[0050]
所述晶型e还具有如下特性,其热重分析曲线(tga)在50℃-200℃间基本无失重,失重量约为0.05%。
[0051]
在一些实施方式中,晶型e的热重分析曲线(tga)如图12所示。根据晶型e的dsc和tga检测结果,认为晶型e是一种非溶剂化物晶型,不含水或其他溶剂。
[0052]
经过研究发现,晶型e是一种稳定晶型,其在高温、高湿、光照条件下稳定,不会发生转晶。
[0053]
一种aticaprant的新晶型,称为晶型f,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.12,5.09,6.01,10.12,11.25,12.60,14.83,15.86,16.19,16.81,18.27,18.77,19.13,19.91和22.58的位置有衍射峰。
[0054]
所述晶型f,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.12,5.09,6.01,7.94,8.17,10.12,11.25,12.60,14.83,15.21,15.86,16.19,16.81,18.27,18.77,19.13,19.91,20.20和22.58的位置有衍射峰。
[0055]
所述晶型f的x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.12,5.09,6.01,7.94,8.17,9.52,10.12,11.25,11.96,12.60,13.27,14.83,15.21,15.86,16.19,16.81,18.27,18.77,19.13,19.91,20.20,21.46,22.58,22.97,23.34,25.60和29.98的位置有衍射峰。
[0056]
在一些实施方式中,晶型f的x-射线粉末衍射(xrpd)图如图13所示。
[0057]
所述晶型f还具有如下特性,其差示扫描量热曲线(dsc)在60℃-95℃具有吸热峰。在一些实施方式中,晶型f的差示扫描量热曲线(dsc)在65℃-80℃具有吸热峰,峰顶值为77℃。在一些实施方式中,晶型f的差示扫描量热曲线(dsc)如图14所示。
[0058]
所述晶型f还具有如下特性,其热重分析曲线(tga)在50℃-100℃间有失重,失重量约为2.9%。在一些实施方式中,晶型f的热重分析曲线(tga)如图15所示。
[0059]
研究发现,晶型f对热不稳定,在高温条件下,发生转晶,在60℃、相对湿度75%的条件下放置5天,转变为前述的晶型e。
[0060]
一种aticaprant的新晶型,称为晶型g,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.69,7.76,10.15,11.66,13.83,14.77,18.05,18.88,20.90和22.41的位置有衍射峰。
[0061]
所述晶型g,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.69,6.91,7.76,10.15,11.66,13.83,14.77,15.28,15.54,17.53,18.05,18.88,20.28,20.48,20.90和22.41的位置有衍射峰。
[0062]
所述晶型g,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.69,6.91,7.76,10.15,11.66,12.51,13.83,14.77,15.28,15.54,17.53,18.05,18.88,19.45,20.28,20.48,20.90,22.41,24.09,25.32,27.11和29.55的位置有衍射峰。
[0063]
在一些实施方式中,晶型g的x-射线粉末衍射(xrpd)图如图16所示。
[0064]
所述晶型g还具有如下特性,其差示扫描量热曲线(dsc)在90℃-110℃具有吸热峰。在一些实施方式中,晶型g的差示扫描量热曲线(dsc)在95℃-105℃具有吸热峰,峰顶值为102℃。在一些实施方式中,晶型g的差示扫描量热曲线(dsc)如图17所示。
[0065]
所述晶型g还具有如下特性,其热重分析曲线(tga)在50℃-120℃间有失重,失重量约为1.72%。在一些实施方式中,晶型g的热重分析曲线(tga)如图18所示。
[0066]
根据研究发现,晶型g为一种亚稳态晶型,其高温,高湿和强光都存在不稳定性,易发生转晶,在60℃,相对湿度75%的条件下放置5天,或者在相对湿度92.5%条件下放置5天,或者在光照4500lx
±
500lx条件下放置5天,都发生转晶,转变为前述的晶型ii。
[0067]
一种aticaprant的新晶型,称为晶型h,其x-射线粉末衍射的图谱中,在2θ(单位:度,
°
)为4.43,5.04,9.55,13.61,13.98,14.71,15.08,17.61,18.34,19.14,22.26和21.43的位置有衍射峰。
[0068]
所述晶型h,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.43,5.04,7.54,9.55,10.00,12.82,13.61,13.98,14.71,15.08,17.61,18.34,19.14,20.22,20.71,21.43,22.79,24.76和27.82的位置有衍射峰。
[0069]
所述晶型h,其x-射线粉末衍射图谱中,在2θ(单位:度,
°
)为4.43,5.04,7.54,9.55,10.00,12.56,12.82,13.61,13.98,14.71,15.08,16.03,17.20,17.61,18.34,19.14,20.22,20.71,21.43,22.26,22.79,23.92,24.41,24.76和27.82的位置有衍射峰。
[0070]
在一些实施方式中,晶型h的x-射线粉末衍射(xrpd)图如图19所示。
[0071]
所述晶型h还具有如下特性,其差示扫描量热曲线(dsc)在70℃-105℃具有吸热峰。在一些实施方式中,晶型h的差示扫描量热曲线(dsc)在80℃-100℃具有吸热峰,峰顶值为95℃。在一些实施方式中,晶型h的差示扫描量热曲线(dsc)如图20所示。
[0072]
所述晶型h还具有如下特性,其热重分析曲线(tga)在50℃-120℃间有失重,失重量约为2.25%。在一些实施方式中,晶型h的热重分析曲线(tga)如图21所示。
[0073]
研究发现,晶型h是一种对热不稳定晶型,在高温条件下,可发生转晶,其在在60℃、相对湿度75%的条件下放置5天,发生转晶,转变为前述的晶型e。
[0074]
前述的晶型中,晶型e存在较好的稳定性,有利于储存、转移、生产工艺中操作,可与药学上可接受的载体制备成其药用组合物。且所述的晶型e为具有良好外观和流动性的粉末,在溶出度、流动性等方面具有良好的性能,有利于与药学上可接受的载体制备成其药用组合物。
[0075]
另一方面,本发明提供了前述的晶型的制备方法。
[0076]
一种制备aticaprant晶体的方法,包括:将化合物aticaprant溶于良溶剂中,加入反溶剂,过滤,干燥,得到aticaprant晶体;或者将化合物aticaprant与结晶溶剂混合,搅拌,除去溶剂,得到aticaprant晶体,其中任选加入诱导剂。
[0077]
所述良溶剂为甲基异丁基甲酮和/或叔丁醇,所述反溶剂为正庚烷,得到晶型i。
[0078]
所述良溶剂为乙腈,甲醇,乙醇,异丙醇等与水相溶的溶剂中的至少之一,所述反溶剂为水,得到晶型ii。在一些实施方式中,所述良溶剂为乙醇或乙腈或其组合,反溶剂为水,得到晶型ii。
[0079]
所述良溶剂为酯类溶剂如乙酸甲酯,乙酸乙酯,甲酸乙酯中的至少之一,所述反溶剂为烷烃如正庚烷,正己烷等,得到晶型d。
[0080]
在一些实施方式中,将化合物aticaprant与结晶溶剂混合,任选加入诱导剂,搅拌,除去溶剂,得到前述的晶型e。所述结晶溶剂为乙醇,任选加入诱导剂,得到晶型e。在一些实施方式中,所述结晶溶剂为乙醇,诱导剂为肉桂酰胺,得到晶型e。在一些实施方式中,所述结晶溶剂为丙酮,诱导剂为哌嗪或其水合物,得到晶型e。
[0081]
所述结晶溶剂为醚类溶剂如异丙醚,得到晶型f。
[0082]
所述结晶溶剂为甲苯,得到晶型g。
[0083]
所述良溶剂为甲苯,所述反溶剂为环己烷,得到晶型h。
[0084]
在一些实施方式中,将化合物aticaprant溶于良溶剂中,加入反溶剂,过滤,干燥,得到aticaprant晶型ii,其中,所述良溶剂为乙腈,甲醇,乙醇,异丙醇中的至少之一,所述反溶剂为水。
[0085]
在一些实施方式中,化合物aticaprant与乙醇混合,溶清,室温下蒸发除去溶剂,得到晶型e;或者化合物aticaprant与肉桂酰胺、乙醇混合,搅拌,过滤,除去溶剂,得到晶型e;或者化合物aticaprant与哌嗪或其六水合物、丙酮混合,搅拌,过滤,除去溶剂,得到晶型e。
[0086]
另一方面,本发明还提供一种组合物。
[0087]
一种组合物,其包括:前述的晶型d,晶型e,晶型f,晶型g和晶型h中的至少一种晶型和药学上可接受的辅料。在一些实施方式中,所述组合物包括前述的晶型e。
[0088]
在一些实施方式中,所述组合物中,按照质量比计算,所述晶型为aticaprant的至少90%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型为aticaprant的至少95%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型为aticaprant的至少97%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型为aticaprant的至少99%。
[0089]
在一些实施方式中,所述组合物中,按照质量比计算,所述晶型为aticaprant的至少5%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型为aticaprant的至少1%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型为aticaprant的至少
0.5%。
[0090]
在一些实施方式中,所述组合物中,按照质量比计算,所述晶型不超过aticaprant的10%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型不超过aticaprant的6%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型不超过aticaprant的5%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型不超过aticaprant的3%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型不超过aticaprant的1%。在一些实施方式中,所述组合物中,按照质量比计算,所述晶型不超过aticaprant的0.5%。
[0091]
在一些实施方式中,所述组合物中,按照质量比计算,所述晶型为组合物总质量的至少0.05%-95%或1%-95%。
[0092]
在一些实施方式中,所述组合物包括前述的晶型e,还可以包括前述的晶型ii。
[0093]
在一些实施方式中,前述组合物中,所述晶型为晶型e。
[0094]
所述药学上可接受的辅料,包括稀释剂,崩解剂,粘合剂,或润滑剂等。
[0095]
在一些实施方式中,前述的组合物为长效制剂或缓释制剂。所述长效制剂或缓释制剂是指:相比速释制剂,相同治疗周期内,相同总剂量情况下,减少了给药次数的制剂;或者相比速释制剂,相同治疗周期内,减少了总剂量的制剂。
附图说明
[0096]
图1示晶型i的x-射线粉末衍射图(xrpd);
[0097]
图2示晶型i的差示扫描量热曲线(dsc);
[0098]
图3示晶型i的热重分析曲线图(tga)。
[0099]
图4示晶型ii的x-射线粉末衍射图;
[0100]
图5示晶型ii的差示扫描量热曲线(dsc);
[0101]
图6示晶型ii的热重分析曲线图(tga)。
[0102]
图7示晶型d的x-射线粉末衍射图;
[0103]
图8示晶型d的差示扫描量热曲线(dsc);
[0104]
图9示晶型d的热重分析曲线图(tga)。
[0105]
图10示晶型e的x-射线粉末衍射图;
[0106]
图11示晶型e的差示扫描量热曲线(dsc);
[0107]
图12示晶型e的热重分析曲线图(tga)。
[0108]
图13示晶型f的x-射线粉末衍射图;
[0109]
图14示晶型f的差示扫描量热曲线(dsc);
[0110]
图15示晶型f的热重分析曲线图(tga)。
[0111]
图16示晶型g的x-射线粉末衍射图;
[0112]
图17示晶型g的差示扫描量热曲线(dsc);
[0113]
图18示晶型g的热重分析曲线图(tga)。
[0114]
图19示晶型h的x-射线粉末衍射图;
[0115]
图20示晶型h的差示扫描量热曲线(dsc);
[0116]
图21示晶型h的热重分析曲线图(tga)。
具体实施方式
[0117]
为了使本领域的技术人员更好地理解本发明的技术方案,下面进一步披露一些非限制实施例对本发明作进一步的详细说明。
[0118]
本发明所使用的试剂均可以从市场上购得或者可以通过本发明所描述的方法制备而得。
[0119]
本发明中,mg表示毫克,ml表示毫升,rpm表示转/每分钟,h表示小时,rh表示相对湿度。
[0120]
仪器参数
[0121]
除非参数中另行规定,以下所有分析都在室温下进行。
[0122]
粉末x-射线衍射(xrpd)研究
[0123]
在装配有自动化3*15零背景样品架的透射反射样品台的荷兰panalytical empyrean x-射线衍射仪上收集x-射线粉末衍射(xrpd)图案。所用辐射源为(cu,kα,1.540598;1.544426;kα2/kα1强度比例:0.50),其中电压设定在45kv,电流设定在40ma.x-射线的束发散度,即样品上x-射线约束的有效尺寸,为6.6mm.采用θ-θ连续扫描模式,得到3
°
~60
°
的有效2θ范围。取适量样品在环境条件(约18℃~32℃)下于零背景样品架圆形凹槽处,用洁净的载玻片轻压,得到一个平整的平面,并将零背景样品架固定。将样品以0.0167
°
的扫描步长在3~60
°
2θ
±
0.2
°
范围内产生传统的xrpd图案。用于数据收集的软件为data collector,数据用data viewer和highscore plus分析和展示。
[0124]
差示扫描量热法(dsc)
[0125]
dsc测量在ta instrumentstm型号q2000中用密封盘装置进行。将样品(约1~3mg)在铝盘中称量,用tzero压盖,精密记录到百分之一毫克,并将样品转移至仪器中进行测量。仪器用氮气以50ml/min吹扫。在30℃到300℃之间以10℃/min的加热速率收集数据。以吸热峰向下进行绘图,数据用ta universal analysis分析和展示。
[0126]
热重分析法(tga)
[0127]
在ta instruments q500上采集tga数据。使用认证的镍校准仪器的温度。通常将8-12mg样品加载到预称重的铂金坩埚上,并以10℃/min从30℃加热至300℃。在样品上方保持60ml/min的氮气清扫。在tga图中,横坐标表示温度(temperature,℃),纵坐标表示失重的百分含量(weight(%))。
[0128]
晶型i的制备
[0129]
方法1:将30mg的aticaprant加入到0.15ml的甲基异丁基甲酮中溶清,再加入0.2ml正庚烷;体系中生成了白色固体,搅拌12h,过滤,得到产物,为晶型i;检测x射线粉末衍射,dsc,tga,结果参见图1-图3。
[0130]
方法2:把80mg的aticaprant加入到0.4ml的叔丁醇中溶清,再加入0.8ml正庚烷,把体系敞口置于50℃环境中搅拌蒸发12h,得到固体,检测确认为晶型i。
[0131]
晶型ii的制备
[0132]
方法1:将20mg的原料aticaprant加入到0.5ml的乙腈中溶解,滴加0.2ml纯化水;然后把体系敞口置于50℃环境中搅拌蒸发12h,得到白色晶态物质;抽滤并置于干燥箱内50℃真空干燥12h,得到晶型ii,检测,x-射线粉末衍射,dsc,tga,结果参见图4-图6。
[0133]
方法2:将50mg的aticaprant加入到0.15ml的乙醇中溶解,再加入0.25ml纯化水,
立即生成了白色固体,搅拌12h,过滤,得到固体,检测确认为晶型ii。
[0134]
实施例1晶型d的制备
[0135]
将30mg的aticaprant加入到0.15ml的乙酸乙酯中溶清,再加入0.3ml正庚烷,有白色固体生成,搅拌12h,过滤,得到产物晶型d,检测x射线粉末衍射,dsc,tga,结果参见图7-图9。
[0136]
实施例2晶型e的制备
[0137]
方法1:将20mg的aticaprant晶型i敞口置于60℃、75%相对湿度的试验箱中5天,得到晶型e;检测x射线粉末衍射,dsc,tga,结果参见图10-图12。
[0138]
方法2:在玻璃管中加入10mg的aticaprant,再加入0.1ml乙醇,原料快速溶解;打开瓶盖,室温蒸发溶剂12-24小时,得到白色固体,检测,确认为晶型e。
[0139]
方法3:称取10mg的aticaprant加入到一支ep管中,再加入3.7mg的肉桂酰胺,再加入0.1ml乙醇溶解,开盖室温搅拌12小时,过滤,室温下固体干燥,检测,确认得到晶型e。
[0140]
方法4:称取20mg的aticaprant加入到一支ep管中,再加入9.7mg的哌嗪六水合物,再加入0.5ml丙酮溶解,开盖室温搅拌12小时,过滤,室温下固体干燥,检测,确认得到晶型e。
[0141]
实施例3晶型f的制备
[0142]
将80mg的aticaprant加入到2ml异丙醚中混悬,敞口搅拌12h,得到固体,为晶型f,检测x射线粉末衍射,dsc,tga,结果参见图13-15。
[0143]
实施例4晶型g的制备
[0144]
将100mg的aticaprant加入到1.5ml甲苯中溶清,把体系敞口置于50℃环境中搅拌蒸发12h,得到晶型g,检测x射线粉末衍射,dsc,tga,结果参见图16-图18。
[0145]
实施例5晶型h的制备
[0146]
将30mg的aticaprant加入到0.3ml甲苯中溶清,再加入0.6ml环己烷,过夜搅拌,得到晶型g产物。经测定,其x射线粉末衍射图谱与图19基本一致,其dsc图谱与图20基本一致,tga图谱与图21基本一致。
[0147]
实施例6稳定性测试
[0148]
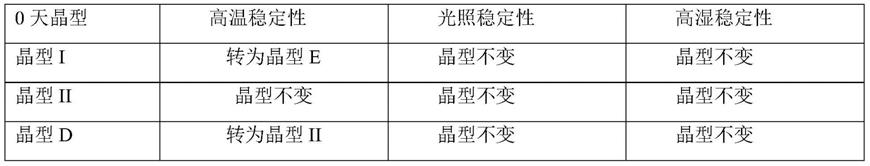
根据药物制剂稳定性试验指导原则,对样品进行影响因素实验,包括高温试验、高湿试验和强光照射试验,考察不同条件下各晶型的稳定性情况,结果参见下表1。
[0149]
实验条件:
[0150]
高温试验:分别取样品适量,平铺置称量瓶中,敞口,在60
±
5℃、rh75
±
5%恒温恒湿箱中放置,然后分别于0、5和15天取上述样品约10mg,采用粉末x-射线衍射(xrpd)、差示扫描量热法(dsc)测试其晶型情况。
[0151]
高湿试验:分别取样品适量,平铺置称量瓶中,敞口,在25℃、rh92.5
±
5%恒温恒湿箱中放置,然后分别于0、5和15天取上述样品约10mg,采用粉末x-射线衍射(xrpd)、差示扫描量热法(dsc)测试其晶型情况。
[0152]
光照试验:分别取样品适量,平铺至称量瓶中,敞口,在可见光4500lux
±
500lux(vis)、紫外光1.7w*h/m2(uv)的恒温恒湿箱(25℃、rh60%
±
5%)条件下放置,然后分别于0、5和15天取上述样品约10mg,采用粉末x-射线衍射(xrpd)、差示扫描量热法(dsc)测试其晶型情况。
[0153]
实验结果:各样品的检测结果参见表1。
[0154]
表1:稳定性实验结果
[0155][0156][0157]
实施例7溶解度测试
[0158]
分别取10mg晶型ii和晶型e样品于2支试管中。在每支试管中加入0.5ml的1%sds磷酸盐缓冲液。把试管置于37℃恒温阱中,搅拌2小时,样品没有溶清,则继续在试管中加入0.5ml缓冲液,再搅拌2小时,观察其溶解情况。当加入4ml缓冲液时,晶型ii样品溶清;当加入5ml缓冲液时,晶型e样品溶清;晶型ii溶解度计算为2.5mg/ml;晶型e溶解度计算为2mg/ml。根据两种晶型的溶解性数据看,二者溶解性接近,而又都具有较好的稳定性,因此,晶型ii和晶型e相对其他晶型,更具有制剂应用性,对于需要长效或者缓释的制剂而言,晶型e因其稳定性、相对较高的熔点和相对稍低的溶解性,相对更有优势。
[0159]
本发明的方法已经通过较佳实施例进行了描述,相关人员明显能在本发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
