1.本发明属于分析化学领域,特别涉及一种通过衍生化方法检测双氢青蒿素片溶出度的检测方法。
背景技术:
2.双氢青蒿素是从青蒿(herba artemisiae annuae)中提取分离出的抗疟有效单体-青蒿素的衍生物,其化学名为(3r,5as,6r,8as,9r,12s,12ar)-八氢-3,6,9-三甲基-3,12-桥氧-12h-吡喃并[4,3-j]-1,2-苯并二塞平-10(3h)-醇,分子式为c
15h24
o5,分子量为284.35,结构式如下:
[0003][0004]
双氢青蒿素是除了可有效的治疗各种疟疾,特别对多药耐药性疟疾疗效显著,还发现双氢青蒿素具有抗肿瘤、抗炎及治疗卡氏肺孢子虫、红斑狼疮等方面的作用。双氢青蒿素制成的制剂最主要形式为双氢青蒿素片,并分别收录于2015和2020年版《中国药典》。由于青蒿素类化合物难溶于水、稀酸、稀碱、表面活性剂,但易溶于非极性有机溶剂,双氢青蒿素为低溶解性、高渗透性药物,属于生物药剂学分类系统(bcs)中的ii类药物,即具有较高的膜渗透性,但因溶解性太低,以致不能被完全吸收,溶解度是限制双氢青蒿素吸收的重要因素。其片剂处方为:双氢青蒿素、一水乳糖、微晶纤维素、羧甲基淀粉钠、十二烷基硫酸钠、聚乙烯吡咯烷酮、硬脂酸镁。目前片剂在在药典溶出度测定双青蒿素片的方法是以0.15%氢氧化钠-乙醇(4∶1)为溶出介质,用紫外-可见分光光度法在241nm下检测,而双氢青蒿素在此波长并无吸收,且空白辅料在检测波长处会有吸收,影响测定结果的准确性。
[0005]
另外据报道双氢青蒿素在碱性和酸性条件下会发生降解,因此,此方法所检测的物质为双氢青蒿素碱降解产物,给表征双氢青蒿素的溶出度带来影响。在《international journal of pharmaceutics》,274(2004),第245-260页公开了,美国药典建议使用0.1n hcl作为溶解介质,但是一小时后二氢青蒿素似乎已在0.1nhcl中降解,紫外光谱将降解确认为可检测到的紫外线化合物,最大波长为250nm。并在其他文献中,已发表了几项研究,证明青蒿素化合物在酸性溶液中转化为可检测紫外线的产物。托马斯1992年提出,当接受5mhcl时,双氢青蒿素在45分钟内降解。赵和曾表明青蒿素与氢氧化钠反应后,转化为最大波长为290nm的q290化合物,随后加入hcl导致形成最大波长为260nm的q260化合物。
[0006]
中国药房2017年第28卷第15期第207-208页,《改进双氢青蒿素哌喹片中双氢青蒿素的溶出度测定方法》,公开了采用hplc柱前衍生化外标法测定双氢青蒿素哌喹片中双氢青蒿素的溶出度,在测定过程中加入了双氢青蒿素衍生化步骤:分别以水、0.1mol/l盐酸溶液、ph 4.0醋酸盐缓冲液和ph 6.8磷酸盐缓冲液为溶出介质;取样衍生化方法:用3.6%氢
氧化钠溶液稀释至刻度,置于60℃水浴中反应30min,取出放冷至室温,精密加入磷酸0.7ml,摇匀,经0.45μm微孔滤膜滤过,取续滤液,即得色谱柱:ymc-pack ods-a(250mm
×
4.6mm,5μm),流动相:0.02mol/l磷酸氢二钠溶液(用磷酸调节ph为2.4)-乙腈(65∶35,v/v),流速:1.0ml/min,检测波长:237nm;柱温:30℃,进样量:20μl。
[0007]
另外在2019年3月第44卷第6期,中国医药杂志,《新工艺双氢青蒿素片溶出度测定方法研究》公开了类似的一种双氢青蒿素片溶出度测定方法,其溶出介质为:0.25%十二烷基硫酸钠水溶液、20%乙醇溶液、人工胃液、ph=3.8醋酸盐缓冲溶液、人工肠液、ph=7.2磷酸盐缓冲液、水;高效液相色谱法测定:agilent eclipse xdb-c18色谱柱(4.6mm
×
150mm,5μm),取溶液5ml,滤过,精密量取续滤液2ml,置10ml量瓶中,用2%氢氧化钠溶液稀释至刻度,流动相乙腈-水(40∶60)、流速:1.0ml/min、柱温:30℃、检测波长:216nm、进样量:100μl。
[0008]
现有技术中双氢青蒿素片溶出度检测方法,存在需要同时解决双氢青蒿素溶解性低、紫外吸收弱、hplc检测需要增加大进样量、产品稳定性、精准检测等一系列问题,为了解决上述问题,本发明提供一种能更准确的测定双氢青蒿素片的溶出度,更好地模拟体内的溶出的溶出度检测方法。
技术实现要素:
[0009]
本发明提供一种更高精准、更灵敏测点双青蒿素片溶出度的检测方法。
[0010]
本发明提供一种双青蒿素片溶出度的检测方法,包括对溶出液进行衍生化处理,所述衍生化处理采用氢氧化钠在加热条件下进行前置处理,再用酸进行中和至ph为中性,得供试品溶液。
[0011]
进一步地,所述的检测方法溶出液衍生化前置处理采用氢氧化钠的质量浓度为1.5%-2.5%,优选2.0-2.5%,更优选为2.0%。
[0012]
进一步地,所述的检测方法溶出液衍生化前置处理采用氢氧化钠加热条件为水浴加热,加热温度为30-80℃,优选为50-70℃,更优选为60℃,加热时间选自20-60min,优选为20-40min,更优选为30min。
[0013]
进一步地,所述的检测方法溶出液衍生化前置处理后采用酸中和调整ph值为中性,所述的酸选自盐酸、醋酸、磷酸、硫酸中的一种或者几种,优选为醋酸;所述酸的用量根据衍生物化处理的碱量调整ph至中性进行调整。
[0014]
进一步地,所述的检测方法溶出液经过衍生物处理后,得供试品溶液,采用高效液相检测,所述的检测方条件:色谱柱为luna-c8(2)(4.6
×
150mm,5μm),流动相为磷酸盐缓冲液(ph5.8)-甲醇45∶55,检测波长为200-400nm,优选为波长为238nm,流速为1.0ml/min,柱温为30℃,检测器为vwd,进样量为30μl。
[0015]
进一步地,所述的检测方法溶出液的溶出条件为:照《中国药典》溶出度与释放度测定法(通则0931第二法),以0.25%十二烷基硫酸钠水溶液500ml为溶出介质,转速为每分钟50转。
[0016]
本发明有益效果如下:
[0017]
(1)因供试品前处理方式由传统的溶出液直接进样变更为衍生化后再进样检测,提高了检测灵敏度,所以溶出介质的量可以增加到500ml,溶出度检测法可以由第三法(小杯法)变为第二法。
[0018]
(2)双氢青蒿素溶解度较低,现有技术中采用的有机溶剂乙醇为溶出介质,但是药审中心一般不推荐使用,本技术选用0.25%十二烷基硫酸钠水溶液500ml为溶出介质,避免了溶出度实验中使用有机溶剂提高双氢青蒿素的溶解度。
[0019]
(3)供试品溶液衍生化后最大吸收波长由原来的205nm变成238nm,在hplc的检测中紫外吸收变强,可以改善加大进样量导致测定结果不准确的带来的问题,将进样量由100μl降低至30μl。
附图说明
[0020]
图1为本发明分别在0.1%,0.15%,0.2%,0.25%的十二烷基硫酸钠(sds)水溶液四种介质中的溶出曲线示意图;
[0021]
图2为本发明前置处理naoh质量浓度与响应因子关系图,naoh质量浓度分别为0.5%、1.0%、1.5%、2.0%、2.5%;
[0022]
图3为本发明前置处理衍生化温度与响应值关系图,温度分别为30℃、40℃、50℃、55℃、60℃、65℃、70℃、80℃;
[0023]
图4为本发明前置处理衍生化破坏时间与响应值关系图,破坏时间分别为20min,30min,40min,50min,60min;
[0024]
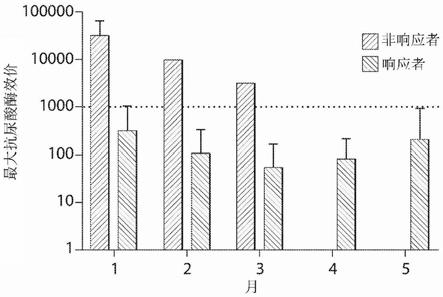
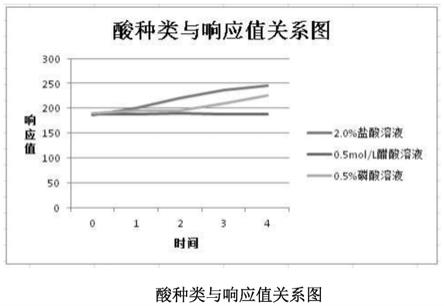
图5为本发明衍生化处理不同酸中和与响应值的关系图,酸分别为盐酸、醋酸、磷酸。
[0025]
图6为本发明双氢青蒿素在测试浓度与响应值呈线性关系图。
具体实施方式
[0026]
本技术涉及的仪器设备如下:
[0027][0028]
药品与试剂:本技术双氢青蒿素片来自cn107982228a所述的处方制得的商业规模样品。
[0029]
溶出液一般是指:是指照溶出度与释放度测定法(通则0931第一法),以0.25%十二烷基硫酸钠水溶液500ml为溶出介质,转速为每分钟50转,依法操作,在规定的取样时间点,取出的溶液。
[0030]
中和至ph为中性,一般是指本领域人员常规认识ph=7
±
0.5,优先认为ph=7
±
0.2,更优先认为ph=7
±
0.1,进一步认为ph=7。
[0031]
双氢青蒿素衍生化处理一般是指对青蒿素进行改性,等量形成紫外吸收更强的衍生物,所述的衍生物指《international journal of pharmaceutics》,274(2004),第245-260页所述的结构。因为双氢青蒿素中无共轭结构和发色基团,不宜用分光光度法和hplc法直接测定。但使用衍生化法处理后,使其产生稳定和紫外吸收更强的衍生物,加入的碱能促
使双氢青蒿素完全转化为双氢青蒿素衍生物,用双氢青蒿素对照品按照衍生化条件进行线性测定,线性测定结果表明:双氢青蒿素在测试浓度(4.0μg/ml)10%~500%的范围内,其浓度与响应值呈良好的线性关系,其线性范围为:0.4~20.0μg/ml(r=0.9999,n=7),具体如表1和图6所示。
[0032][0033][0034]
表1浓度与响应值呈线性关系
[0035]
下面结合说明书附图对本发明实施例作进一步详细描述。
[0036]
实施例1-4
[0037]
溶出介质的选择
[0038]
取双氢青蒿素片,分别以0.1%,0.15%,0.2%,0.25%的十二烷基硫酸钠(sds)水溶液作为溶出介质,体积为500ml,转速为50rmp/min,照2015版药典溶出度测定法(通则0931第二法)操作,于5,10,15,20,30,45,60min时取样10ml(同时补充相应的溶出介质10ml),过滤,取续滤液5ml于50ml量瓶中,加5ml无水乙醇及20ml2%氢氧化钠试液,摇匀,置60℃水浴保温30分钟,迅速冷却,作为供试品溶液;
[0039]
采用以下检测方法进样测定,色谱柱:luna-c8(2)(4.6
×
150mm,5μm);流动相:磷酸盐缓冲液(ph5.8)-甲醇45∶55;流速:1.0ml/min;柱温:30℃;检测器:vwd;检测波长:238nm;进样量:30μl。
[0040]
样品在4种溶出介质中的平均累积溶出度,结果见图1。由图1可知,样品在4种溶出介质中的溶出行为均相似。但在0.2%的sds水溶液中的各溶出时间点的平均累积溶出度均较高,区分力相对较好。
[0041]
实施例5-9
[0042]
溶出液衍生化氢氧化钠浓度的考察
[0043]
分别精密称取双氢青蒿素5mg各5份进行后续处理,置25ml量瓶中,加无水乙醇溶解并稀释至刻度,摇匀,精密移取2.5ml于25ml量瓶中,加2.5ml无水乙醇,并分别对应加入质量浓度为0.5%,1.0%,1.5%,2.0%,2.5%的氢氧化钠试液,置60℃水浴保温30分钟,迅速冷却,在进样前分别用醋酸溶液调节ph至中性,摇匀,进样分析。
[0044]
采用以下检测方法进样测定,色谱柱:luna-c8(2)(4.6
×
150mm,5μm);流动相:磷酸盐缓冲液(ph5.8)-甲醇45∶55;流速:1.0ml/min;柱温:30℃;检测器:vwd;检测波长:238nm;进样量:30μl。
[0045]
最后不同氢氧化钠浓度显示响应因子结果见图2,响应因子=峰面积/浓度。随着的增加,响应因子不断增大(响应因子=峰面积/浓度),到2.0%时趋于稳定,故衍生化碱浓度最优为2.0%。
[0046]
实施例10-17
[0047]
溶出液衍生化温度的考察
[0048]
分别精密称取双氢青蒿素20mg,于50ml量瓶中,加无水乙醇溶解并稀释至刻度,再精密移取10ml于100ml量瓶中,加无水乙醇定容至刻度,得储备液a。精密量取储备液a 5ml于50ml量瓶中,加20ml2%氢氧化钠试液,5ml0.2%sds水溶液,分别置30℃、40℃、50℃、55℃、60℃、65℃、70℃、80℃水浴温度下保温30分钟每个破坏温度平行破坏2份溶液,共16份,迅速冷却,另取相应试剂同法制成各自空白溶液,加0.5mol/l的醋酸溶液定容至刻度。
[0049]
采用以下检测方法进样测定,色谱柱:luna-c8(2)(4.6
×
150mm,5μm),流动相:磷酸盐缓冲液(ph5.8)-甲醇45∶55,流速:1.0ml/min,柱温:30℃,检测器:vwd,检测波长:238nm,进样量:30μl。
[0050]
最后不同衍生化温度显示响应因子结果见图3,计算响应因子(响应因子=峰面积/浓度)。在一定温度范围内随着破坏温度的升高,响应值不断增大,70℃时响应值降低。
[0051]
实施例18-22
[0052]
溶出液衍生化破坏时间的考察:
[0053]
精密称取双氢青蒿素约20mg,于100ml量瓶中,加无水乙醇溶解并稀释至刻度,精密移取2ml至20ml量瓶中(平行5份),加2ml无水乙醇,8ml2%氢氧化钠试液,将其置于60℃水浴中,保温时间分别为20min,30min,40min,50min,60min时取出,迅速冷却,在进样前用0.5mol/l的醋酸溶液定容,摇匀,进样分析。
[0054]
分析方法如实施例1所示,溶出液衍生化破坏响应值结果见图4。由图可知,在一定破坏时间范围内,随着破坏时间的增加,响应值不断增大,但从40分钟后就呈现下降趋势,30分钟与40分钟时接近平稳。
[0055]
实施例19-21
[0056]
溶出液衍生化不同酸种类中和的考察:
[0057]
精密称取双氢青蒿素约20mg,于100ml量瓶中,加无水乙醇溶解并稀释至刻度,精密移取2ml至20ml量瓶中,加2ml无水乙醇,8ml 2%氢氧化钠试液,将其置于60℃水浴中,保温时间为30min时取出,迅速冷却,在进样前用分别用2.0%的盐酸溶液、0.5mol/l的醋酸溶液、0.5%磷酸进行中和(用ph计控制调供试品溶液ph=7
±
0.5),摇匀,进样分析,并考察溶液稳定性。
[0058]
分析方法如实施例1所示,溶出液衍生化不同酸处理响应值结果见图5。
[0059]
结果显示,采用2.0%的盐酸和0.5%磷酸溶液中和,随着时间的推移,峰面积不断增大(有可能有副反应产生,生产其他衍生物,不具有线性关系),改用醋酸中和后,溶液相对稳定。
[0060]
不同种类酸衍生化后的测定结果
[0061][0062]
表2酸种类随时间与响应值关系
[0063]
实施例22-25
[0064]
溶出液衍生化酸浓度的考察
[0065]
因naoh浓度为0.5%,1.0%,1.5%,2.0%时相对应醋酸浓度为0.2mol/l,0.4mol/l,0.6mol/l,0.8mol/l,最初选择加入同等体积的醋酸溶液进行中和供试品溶液,但结果显示溶液不稳定,即随着时间的推移,响应值增大,通过ph测定发现样品偏酸性,能在酸性条件下破坏产物会被继续破坏,导致吸光物质不断增加。经过对酸浓度的筛选,最终确定醋酸浓度在实验过程中采用酸碱等摩尔比例加入,结果显示溶液在12小时内稳定性良好。
[0066]
显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。