一种重组iii型人源化胶原蛋白、核酸、载体及植入剂
技术领域
1.本发明涉及基因工程技术领域,具体涉及一种重组iii型人源化胶原蛋白、核酸、载体及植入剂。
背景技术:
2.胶原蛋白(collagen)是体内含量最多的一种蛋白质,是细胞外基质(ecm)的主要成分,其对维护细胞、组织、器官的正常生理功能和损伤修复具有重要作用,已广泛应用于医药、保健品及化妆品行业中。在分子结构上,每条胶原肽链主要由gly-x-y结构肽链构成(x、y是gly之外的任何氨基酸残基),这种肽链结构是形成胶原纤维高级结构所必需的,决定了胶原蛋白优良的生物相容性和低免疫原性。
3.胶原蛋白的主要来源是从动物组织中提取,而随着生物技术的发展,利用基因重组技术,通过微生物发酵法获得重组胶原蛋白,已被广泛的应用。2021年3月15日国家药监局发布了《重组胶原蛋白生物材料命名指导原则》,原则中对重组胶原蛋白进行分类命名,将目前的重组胶原蛋白分为重组人胶原蛋白、重组人源化胶原蛋白、重组类胶原蛋白三类,其中的重组人胶原蛋白是指人胶原蛋白特定型别基因编码的全长氨基酸序列,且有三螺旋结构,但这一类重组胶原因存在技术难题,暂时未在市场中得到应用;第二类是重组人源化胶原蛋白,由dna重组技术制备的人胶原蛋白特定型别基因编码的全长或部分氨基酸序列片段,或是含人胶原蛋白功能片段的组合;第三类是重组类胶原蛋白,由dna重组技术制备的经设计、修饰后的特定基因编码的氨基酸序列或其片段,或是这类功能性氨基酸序列片段的组合。其基因编码序列或氨基酸序列与人胶原蛋白的基因编码序列或氨基酸序列同源性低。目前,市场中应用并已形成产品的主要有重组人源化胶原蛋白和重组类胶原蛋白,但二者各有优缺点,重组人源化胶原蛋白氨基酸序列与天然人序列相同,生物相容性好,安全性更高,但在实际生产和应该中存在稳定性差、易降解的问题,为了提高终产品的稳定性,目前上市的植入类重组人源人胶原蛋白产品制剂以制备成冻干粉的形式保存;而重组类胶原蛋白为了改变稳定性的问题对序列中的部分氨基酸进行优化修改,虽然稳定性得到很大改善,但因序列的改进后与人的天然序列同源性较低,导致相容性和安全性降低,影响其应用。
技术实现要素:
4.本发明目的在于为克服现有的技术缺陷,提供一种重组iii型人源化胶原蛋白、核酸、载体及植入剂,以解决现有技术中重组人源化胶原蛋白以液体剂型保存和使用过程中稳定性差,易降解,限制其在临床中的应用的缺陷。
5.为了解决上述技术问题,本发明提供了以下技术方案:
6.第一方面,提供了一种重组iii型人源化胶原蛋白,所述重组iii型人源化胶原蛋白由单体重复串联组成,所述单体的氨基酸序列如seq.id.no.5所示;所述单体的串联个数为2~15。
7.优选地,所述单体由如下氨基酸肽段依次拼接而成:
8.iii型人胶原蛋白α1链中549-560aa肽段,氨基酸序列如seq.id.no.1所示;
9.iii型人胶原蛋白α1链中597-613aa肽段,氨基酸序列如seq.id.no.2所示;
10.iii型人胶原蛋白α1链中881-902aa肽段,氨基酸序列如seq.id.no.3所示;
11.iii型人胶原蛋白α1链中648-662aa肽段,氨基酸序列如seq.id.no.4所示。
12.优选地,所述重组iii型人源化胶原蛋白的分子量为10kd~100kd。
13.所述重组iii型人源化胶原蛋白的制备过程包括如下步骤:
14.(1)重组iii型人源化胶原蛋白的结构设计及基因获得
15.将iii型胶原蛋白α1链中549-560aa、597-613aa、881-902aa、648-662aa四段肽链按顺序拼接组成单体,单体序列见seq.id.no.5,包含66个氨基酸。
16.单体氨基酸序列根据毕赤酵母密码子偏好性设计对应核苷酸序列,同时为了后继的酶切连接,该dna序列在5’端添加有xho i限制性内切酶酶切位点ctcgag和kex2酶切位点aaaaga以及xba i限制内切酶酶切位点gctagc,在3’端添加有nhe i限制性内切酶酶tctaga切位点和ecor i限制性内切酶酶切位点gaattc;将设计的核苷酸序列seq.id.no.6进行全基因合成(北京擎科生物)。之后,根据设计序列中xba i和nhe i为同尾酶的特性,在全基因合成的质粒(puc57-col3)中反复进行xba i ecor i和nhe i ecor i双酶切、连接,即可获得不同重复单体串联序列(2~15)质粒,质粒命名为puc57-col3-2,puc57-col3-3,puc57-col3-4......puc57-col3-15等。
17.(2)表达载体的构建
18.将上述获得的多重复质粒、毕赤酵母表达载体ppic9k同时进行xho i和ecor i双酶切,之后连接转化获得多重复串联表达质粒:ppic9k-col3-2、ppic9k-col3-3、ppic9k-col3-4......puc57-col3-15等。
19.(3)基因工程菌的构建
20.将上述获得的表达载体ppic9k-col3-2、ppic9k-col3-3、ppic9k-col3-4......puc57-col3-15等经电转化导入毕赤酵母宿主菌,g418抗生素筛选转化正确的高拷贝菌株,使用摇瓶鉴定各菌株的表达情况,选择最优的菌株作为生产用基因工程菌。
21.(4)重组iii型人源化胶原蛋白的发酵及纯化
22.以无机盐bsm培养基作为底料,使用10l发酵罐进行发酵,氨水调控ph5.0,温度29.0℃,溶氧控制在30%左右,菌体湿重达180~200mg/ml时开始甲醇诱导,诱导40~50小时,放罐,离心收取发酵上清液。利用中空纤维超滤系统对发酵上清液经除杂过滤浓缩后,然后用mmc bestarose 6ff进行离子交换层析,获得纯度为95%以上的重组iii型人源化胶原蛋白。
23.第二方面,提供了一种核酸分子,所述核酸分子包含编码第一方面所述的重组iii型人源化胶原蛋白的核苷酸序列或其互补序列。
24.优选地,所述核酸分子的核苷酸序列如seq.id.no.6所示。
25.第三方面,提供了一种载体,所述载体含有第二方面所述的核酸分子。
26.第四方面,提供了一种植入剂,包括第一方面所述的重组iii型人源化胶原蛋白。
27.优选地,按质量百分比计,所述植入剂由以下物质制成:重组iii型人源化胶原蛋白:0.1-2%;透明质酸钠:1-10%;注射用水:余量。
28.优选地,按质量百分比计,所述植入剂由以下物质制成:重组iii型人源化胶原蛋白:1%;透明质酸钠:5%;注射用水:余量。
29.第五方面,提供了根据第一方面所述的重组iii型人源化胶原蛋白、第二方面所述的核酸分子、第三方面所述的载体、第四方面所述的植入剂在组织工程和医美产品中的应用。
30.与现有技术相比,本发明具有以下有益效果:
31.本发明选取天然人iii型胶原蛋白α1链中经长期筛选获得的稳定性佳的序列肽段549-560aa、597-613aa、881-902aa、648-662aa,将四段肽链按顺序拼接组成单体,然后对单体进行串联表达。经发酵纯化,所获得的重组iii型人源化胶原蛋白稳定性高,有效地解决了重组iii型人源化胶原蛋白在临床使用过程中降解的问题,可制备成液体制剂保存和使用。同时,本发明还可以通过串联表达生产不同分子量的重组iii型人源化胶原蛋白,以满足下游应用的需求。
32.本发明附加的方面和优点将在下面的描述中部分给出,这些将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
33.此处所说明的附图用来提供对本发明的进一步理解,构成本技术的一部分,并不构成对本发明的不当限定,在附图中:
34.图1为单体十重复重组iii型人源化胶原蛋白摇瓶表达结果示意图;
35.图2为单体十重复重组iii型人源化胶原蛋白10l发酵不同时间段取样电泳结果示意图;
36.图3为单体十重复重组iii型人源化胶原蛋白纯化后电泳结果示意图;
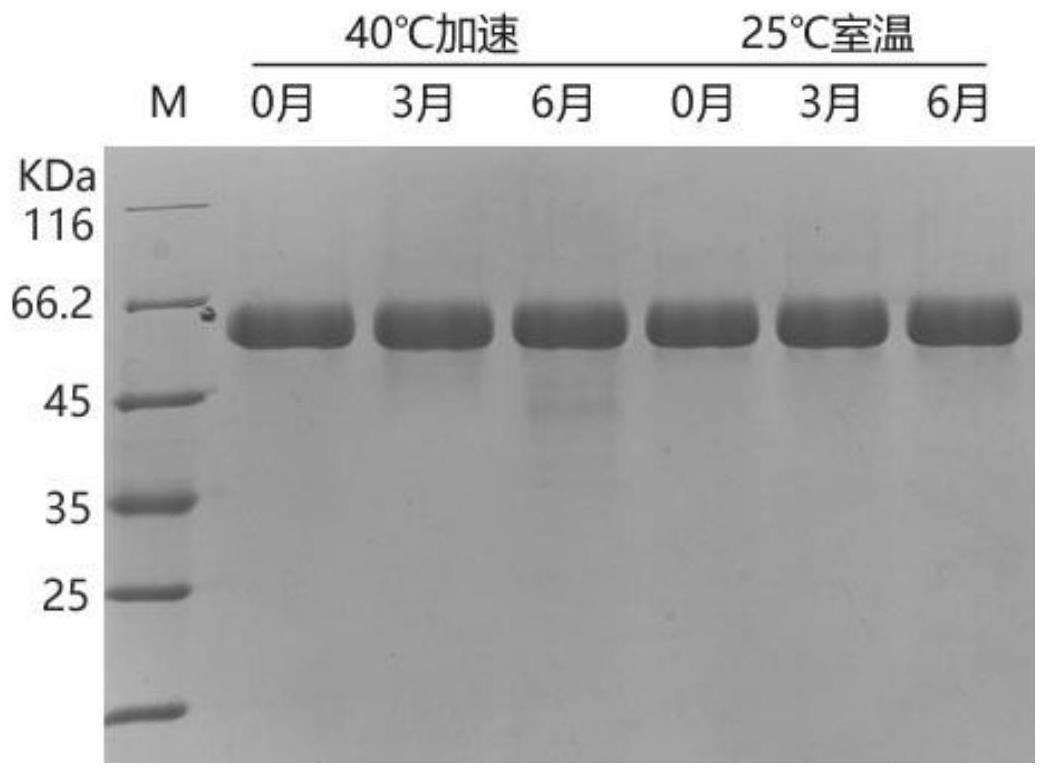
37.图4为单体十重复重组iii型人源化胶原蛋白加速稳定性和室温稳定性电泳结果示意图。
具体实施方式
38.为了更充分的理解本发明的技术内容,下面将结合附图和具体实施例对本发明作进一步介绍和说明;显然,以下所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例;基于本发明中的实施例,本领域技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
39.对于本领域的技术人员来说,通过阅读本说明书公开的内容,本发明的特征、有益效果和优点将变得显而易见。
40.除非另外指明,所有百分比、分数和比率都是按本发明组合物的总质量计算的。本文术语“质量含量”可用符号“%”表示。
41.在本发明中,各组分在组合物和化妆品中的占比相同。
42.本文中“包括”、“包含”、“含”、“含有”、“具有”或其它变体意在涵盖非封闭式包括,这些术语之间不作区分。术语“包含”是指可加入不影响最终结果的其它步骤和成分。术语“包含”还包括术语“由...组成”和“基本上由...组成”。本发明的组合物和方法/工艺可包含、由其组成和基本上由本文描述的必要元素和限制项以及本文描述的任一的附加的或任
选的成分、组分、步骤或限制项组成。
43.实施例1
44.(一)重组iii型人源化胶原蛋白的结构设计
45.本发明根据天然人源iii型胶原蛋白α1链序列(参考序列genebank登录号:nm_000090.3)549-560aa、597-613aa、881-902aa、648-662aa四段肽链按顺序拼接组成单体,单体氨基酸序列见seq.id.no.5。
46.本发明以上述四肽段组成的单体进行重复串联表达。
47.(二)制备重组iii型人源化胶原蛋白
48.2.1基因的获得
49.上述单体氨基酸序列根据毕赤酵母密码子偏好性设计对应核苷酸序列,同时为了后续的分子操作,该dna序列在5’端添加有xho i限制性内切酶酶切位点ctcgag和kex2酶切位点aaaaga以及xba i限制内切酶酶切位点gctagc,在3’端添加有nhe i限制性内切酶酶切位点tctaga和ecor i限制性内切酶酶切位点gaattc,序列见seq.id.no.6,将设计的核苷酸序列进行全基因合成(北京擎科生物)。之后,根据设计序列中xba i和nhe i为同尾酶的特性,在全基因合成的质粒(puc57-col3)中反复进行xba i ecor i和nhe i ecor i双酶切、连接,即可获得不同重复单体串联序列(2~15)质粒,质粒可命名为puc57-col3-2,puc57-col3-3,puc57-col3-4......puc57-col3-15等。
50.2.2表达载体的构建
51.将上述获得的多重复质粒puc57-col3(2~15)和毕赤酵母表达载体ppic9k同时进行xho i和ecor i双酶切,之后t4 dna连接酶连接,转化大肠杆菌dh5α,氨苄青霉素筛选并经测序鉴定获得多重复串联表达质粒:ppic9k-col3-2、ppic9k-col3-3、ppic9k-col3-4......puc57-col3-15等。
52.2.3基因工程菌构建
53.将获得的多重复串联表达质粒,质粒中量提取后,利用限制性内切酶sal i酶切线性化,然后通过电穿孔仪转化毕赤酵母宿主菌gs115(invitrogen),经g418筛选(4mg/ml,ypd培养基)高拷贝转化子,并通过摇瓶发酵(29℃、200rpm,bmmy培养基,间隔24小时甲醇补料1%)确定表达情况。摇瓶发酵上清液经sds-page电泳检测目的蛋白表达情况。
54.(三)重组iii型人源化胶原蛋白的发酵及纯化生产
55.对多重复重组iii型人源化胶原蛋白基因工程菌,进行发酵罐发酵,以无机盐bsm培养基作为底料,使用10l发酵罐进行发酵(氨水调控ph5.0,温度29.0℃,溶氧控制在30%左右),菌体湿重达180~200mg/ml时开始甲醇诱导,诱导40~50小时,放罐,离心收取发酵上清液,然后对发酵上清液用孔径为0.22μm中空纤维微滤系统进行微滤,收集滤过液,然后用mmc bestarose6ff进行层析纯化,20mm ph5.0柠檬酸缓冲液进行柱平衡,样品ph5.0、电导4.0ms/cm左右上样,20mm ph5.5缓冲液洗脱,即可获得纯度为95%以上的重组iii型人源化胶原蛋白。
56.实施例2:
57.单体十重复重组iii型人源化胶原蛋白的制备
58.(一)基因工程菌构建
59.将实施例一中获得的多重复串联表达质粒,优选十重复串联ppic9k-col3-10质粒
中量提取后,利用限制性内切酶sal i酶切线性化,然后通过电穿孔仪转化毕赤酵母宿主菌gs115(invitrogen),经g418筛选(4mg/ml,ypd培养基)高拷贝转化子,并通过摇瓶发酵(29℃、200rpm,bmmy培养基,间隔24小时甲醇补料1%)确定表达情况。摇瓶发酵上清液经sds-page电泳检测,从图1中可看出,在60kd左右处位置有明显的电泳条带,确定获得单体十重复重组iii型人源化胶原蛋白基因工程菌。
60.(二)发酵及纯化
61.对单体十重复重组iii型人源化胶原蛋白基因工程菌,进行发酵罐发酵,以无机盐bsm培养基作为底料,使用10l发酵罐进行发酵(氨水调控ph5.0,温度29.0℃,溶氧控制在30%左右),菌体湿重达180~200mg/ml时开始甲醇诱导,诱导40~50小时,放罐(发酵过程检测如图2),离心收取发酵上清液,对发酵上清液用孔径为0.22μm中空纤维微滤系统进行微滤,收集滤过液,然后用mmc bestarose 6ff进行层析纯化,20mm ph5.0柠檬酸缓冲液进行柱平衡,样品ph5.0、电导4.0ms/cm左右上样,20mm ph5.5缓冲液洗脱,最后使用截留分子量10kd的卷式超滤膜超滤脱盐,冷冻干燥,即可获得纯度大于95%的重组iii型人源化胶原蛋白(纯度电泳分析如图3)。
62.实施例3:
63.对获得的重组iii型人源化胶原蛋白冻干粉使用纯化水配制成0.1%液体,无菌过滤后密封分装,放置于温度40℃
±
2℃、相对湿度75%
±
5%的条件下进行加速实验,在25℃
±
2℃、相对湿度60%
±
5%常温试验,经不同时间点取样,sds-page电泳检测重组iii型人源化胶原蛋白的完整性。测试结果如图4所示;从图4中可以看出,在25℃室温条件下,3个月、6个月取样,蛋白条带完整,几乎无降解;40℃加速条件下,3个月、6个月取样,3月时,蛋白完整,几乎无降解,6月取样,蛋白出现少许降解。从上述实验结果可得,本发明获得的重组iii型人源化胶原蛋白可以以液体形式作为产品剂型,而无需做冻干剂型,这使终产品在生产过程中可大大节约设备、人力和时间成本。
64.通过上述实施例的数据可以看出,本发明设计并制备得到的重组iii型人源化胶原蛋白纯度高,稳定性好,为重组iii型人源化胶原蛋白的应用奠定基础,同时也提示了重组iii型人源化胶原蛋白组织工程和医美产品中的应用,其能够以液体形式作为产品剂型,而无需做冻干剂型,可大大节约生产过程中设备、人力和时间成本。
65.实施例4:
66.本实施例进一步制备单体串联个数在2~15的重组iii型人源化胶原蛋白,制备方法参见实施例2;本实施例通过试验(具体试验步骤参见实施例3)得出,单体串联个数在2~15内制得的重组iii型人源化胶原蛋白与实施例2的单体十重复重组iii型人源化胶原蛋白相似,均具有纯度高,稳定性好的优点。
67.实施例5:
68.本实施例提供一种植入剂,采用本发明实施例2或实施例4中获得的重组iii型人源化胶原蛋白制备植入剂,按重量百分比计,所述植入剂由以下物质制成:
69.重组iii型人源化胶原蛋白(冻干粉):0.1-2%;透明质酸钠:1-10%;注射用水:余量。
70.作为更优选的方案,上述植入剂由以下物质制成:重组iii型人源化胶原蛋白:1%;透明质酸钠:5%;注射用水:余量。
71.本实施例的植入剂的制备方法如下所示:
72.取重组iii型人源化胶原蛋白冻干粉和透明质酸钠,溶解于注射用水中,0.22um无菌过滤分装于西林瓶中,4℃储存,用于面部真皮组织填充以达到去除皱纹的目的。
73.以上对本发明实施例所提供的技术方案进行了详细介绍,本文中应用了具体个例对本发明实施例的原理以及实施方式进行了阐述,以上实施例的说明只适用于帮助理解本发明实施例的原理;同时,对于本领域的一般技术人员,依据本发明实施例,在具体实施方式以及应用范围上均会有改变之处,综上所述,本说明书内容不应理解为对本发明的限制。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。