1.本发明涉及高分子材料技术领域,具体提供一种用于癌细胞靶向识别的材料、方法及应用。
背景技术:
2.这里的陈述仅提供与本发明有关的背景信息,而不必然构成现有技术。
3.癌症是100多种相关疾病的统称。当身体内细胞发生突变后,癌细胞会不断地分裂,不受身体控制,最后形成癌症。人们身体内所有器官都是由细胞组成。细胞增长和分化可满足身体需要,这种有序的过程可保持人们身体健康。然而,如果细胞继续分裂,这些额外的大量细胞就形成肿瘤。恶性肿瘤的细胞能侵犯、破坏邻近的组织和器官。而且,癌细胞可从肿瘤中穿出,进入血液或淋巴系统,这就是癌症如何从原发的部位到其它器官形成新的肿瘤,这个过程就叫癌症转移,癌症及癌症转移严重影响患者健康,甚至生命安全,为诊断或治疗癌症,癌细胞的识别尤为重要。
4.磁性四氧化三铁纳米颗粒是一种非常重要的磁性材料,因其具有独特的磁学性能,可以广泛用作生物分离和检测领域等。同时,因磁性四氧化三铁纳米粒子具有小尺寸效应、良好的磁导向性、生物相容性、生物降解性和活性功能基团等特点,在核磁共振成像、靶向药物、酶的固定、免疫测定等生物医学领域表现出潜在的应用前景。
5.叶酸对叶酸受体具有高度的亲和性,并且是细胞增殖时碱基合成所必须的维生素,很多研究发现叶酸受体在多种恶性肿瘤细胞表面高水平表达。叶酸靶向纳米载体诊疗肿瘤已经成为近年来国内外研究的热点。
技术实现要素:
6.本发明的目的之一是提供一种特定癌细胞靶向识别功能的荧光磁性纳米粒子。
7.本发明一个或一些实施方式中,提供一种用于癌细胞靶向识别的材料,所述用于癌细胞靶向识别的材料以磁性纳米粒子为核心,外层包裹高分子材料,高分子材料上负载量子点,高分子材料表面用癌细胞识别分子修饰。
8.优选的,所述高分子材料为聚苯乙烯;
9.或,所述磁性纳米粒子为四氧化三铁;
10.或,所述量子点为cdte量子点;
11.或,所述癌细胞识别分子为叶酸。
12.本发明一个或一些实施方式中,提供上述用于癌细胞靶向识别的材料的制备方法,包括如下步骤:首先合成磁性纳米粒子,然后制备聚苯乙烯包裹的磁性纳米球,再制备cdte量子点,然后采用反微乳法合成荧光磁性纳米粒子,最后用叶酸进行修饰,即得。
13.本发明的制备方法简单易行,主要是溶液间的混合及加热,温升,主要方法也是常规的混合及水热反应,便于操作推广,适合工业化大规模生产。
14.优选的,采用共沉淀法合成磁性纳米粒子。
15.优选的,所述cdte量子点的制备方法包括如下步骤:
16.在惰性气体保护下,将含te盐溶液与含cd盐溶液混合,为cdte量子点前驱体溶液,将cdte量子点前驱体溶液置于水热反应釜中进行水热反应,即得;
17.优选的,所述惰性气体为氮气;
18.优选的,所述含te盐溶液包括nate和/或kte;
19.优选的,含te盐溶液的制备方法包括如下步骤:以nabh4和te粉作为原料,溶解制备得到nate水溶液,
20.进一步优选的,在氮气保护下,将nabh4和te粉溶于去离子水中,在搅拌作用下,继续通氮气,常温下反应得到淡粉色透明的nate水溶液。
21.优选的,所述含te盐溶液与含cd盐溶液混合包括如下步骤:将二者剧烈搅拌,同时在剧烈搅拌下通n2脱氧,混合溶液立即变为红褐色,继续通n2,并且不断搅拌,得到cdte量子点前驱体溶液;
22.优选的,所述水热反应在聚四氟乙烯内衬的水热合成反应釜中进行;
23.所述水热反应温度为120
‑
200℃,优选为160℃;
24.优选的,所述脱氧时间为20
‑
40min,优选为30min。
25.优选的,所述叶酸修饰包括如下步骤:制备含叶酸的活化反应液,加入荧光磁性纳米粒子溶液,通氮气保持恒温避光反应一段时间.反应结束后,将反应液在搅拌下加入到冰无水乙醇中,经过静置过夜,洗涤,干燥,即得癌细胞靶向识别的材料粗产物。
26.将粗产物避光,透析,冻干后,即得。
27.优选的,所述氮气恒温为20
‑
40℃,优选为30℃;
28.或,所述避光反应时间为40
‑
55h,优选为48h;
29.或,所述含叶酸的活化反应液制备方法包括如下步骤:将叶酸溶于dmso中,然后按照加入催化剂dmap和edc,室温避光磁力搅拌活化一段时间,得活化反应液;
30.优选的,室温避光磁力搅拌活化时间为1.5
‑
3h,进一步优选为2h。
31.本发明一个或一些实施方式中,提供上述癌细胞靶向识别的材料或上述癌细胞靶向识别的材料的制备方法制得的产品在制备抗癌药物中的应用。
32.本发明一个或一些实施方式中,提供上述癌细胞靶向识别的材料或上述癌细胞靶向识别的材料的制备方法制得的产品在癌症检测仪器中的应用。
33.本发明在磁性纳米粒子的基础上进行研究,由于磁性纳米粒子在现有技术中常常用来载药,因此,本发明所述的叶酸修饰的荧光磁性纳米粒子fa
‑
fmnps为抗癌药物的研究提供了经验。
34.上述技术方案中的一个或一些技术方案具有如下优点或有益效果:
35.1)本发明在fmnps的表面修饰了叶酸,既保留了fmnps包含量子点,易与细胞结合的能力,又保留了叶酸的靶向作用,还包含了四氧化三铁的磁性分离富集功能。本发明利用高分子材料将叶酸、四氧化三铁与量子点结合,三者融合度较好,避免在进入细胞过程中发生分散,影响细胞识别。因此,本发明的叶酸靶向磁性显色纳米粒可以广泛地应用于肿瘤细胞的分离和检测。
36.2)本发明的制备方法简单易行,主要是溶液间的混合及加热,温升,主要方法也是常规的混合及水热反应,便于操作推广,适合工业化大规模生产。
37.3)本发明在磁性纳米粒子的基础上进行研究,由于磁性纳米粒子在现有技术中常常用来载药,因此,本发明所述的叶酸修饰的荧光磁性纳米粒子fa
‑
fmnps为抗癌药物的研究提供了经验。
附图说明
38.构成本发明一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
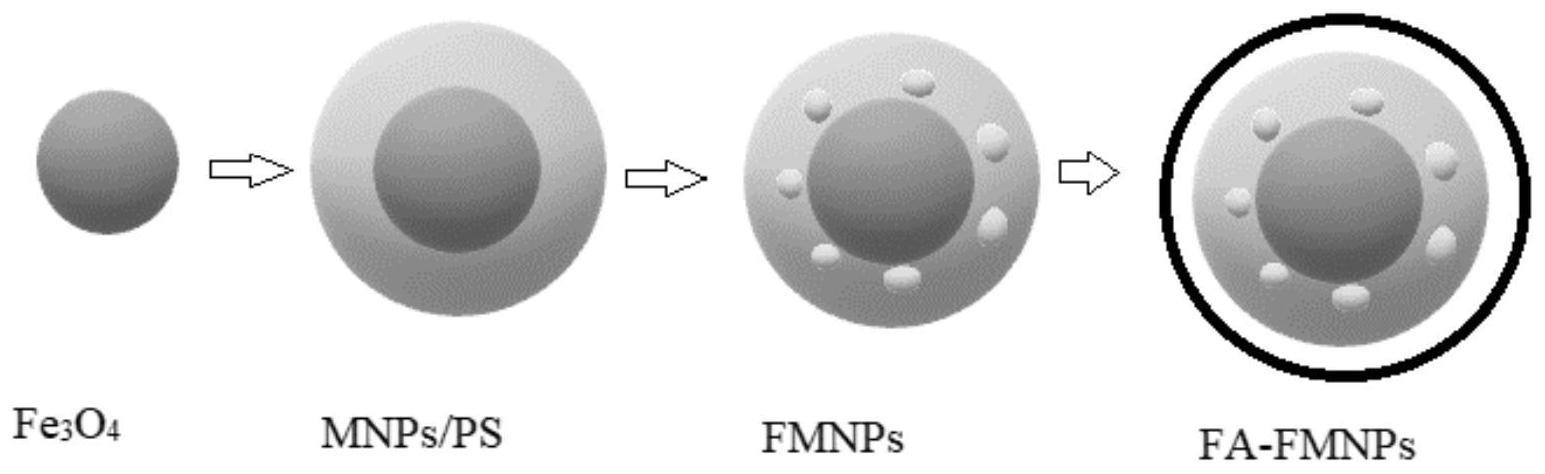
39.图1为实施例1制得的叶酸修饰的荧光磁性纳米粒子fa
‑
fmnps步骤示意图;
40.图2为实施例1制得的叶酸修饰的荧光磁性纳米粒子fa
‑
fmnps透射电镜照片;
41.图3为实施例2中荧光探针在显微镜下观察示意图。
具体实施方式
42.下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明的一部分实施例,而不是全部实施例。基于本发明的实施例,本领域技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
43.本发明所用试剂均来自于阿拉丁试剂公司,
44.实施例1
45.本实施例提供叶酸修饰的荧光磁性纳米粒子fa
‑
fmnps的制备方法,包括如下步骤:
46.如图1所示,本实施例首先采用共沉淀法合成磁性纳米粒子(fe3o4),然后制备聚苯乙烯包裹的磁性纳米球(mnps/ps),再制备cdte量子点(qds),然后采用反微乳法合成荧光磁性纳米粒子(fmnps),最后用叶酸(fa)进行修饰,得到fa
‑
fmnps。
47.制备fe3o4或mnps/ps的方案现有技术中皆以成熟,在此不再赘述。
48.制备cdte量子点(qds)具体包括如下步骤:取去离子水3ml置于10ml反应瓶中,通氮气除氧一段时间后,向反应瓶中加入一定量的nabh4和te粉,在磁力搅拌下,继续通氮气,常温下反应得到淡粉色透明的nate水溶液,密封保存备用。称取0.4567gcdcl2·
2.5h2o于250ml三口烧瓶中,加入100ml去离子水使其全部溶解,在剧烈搅拌下通n2脱氧30min,然后迅速加入上述新制备的无氧nate溶液,混合溶液立即变为红褐色,继续通n2,并且不断搅拌,得到cdte量子点前驱体溶液,将前驱体溶液转移至聚四氟乙烯内衬的水热合成反应釜中,并将反应釜放入160℃烘箱中加热制得透明的cdte量子点溶液。
49.制备fmnps的具体包括如下步骤:在圆底烧瓶中加入12.5ml的环己烷,4ml的tritonx
‑
100,3.5ml的正己醇,机械搅拌30min,然后加入10ml的cdte量子点和500μlmnps/ps,机械搅拌30min,再加入150μl的正硅酸四乙酯,机械搅拌30min后,形成油包水的微乳体系,加入150μl的氨水调节溶液ph值为碱性,继续搅拌反应24h得到fmnps,通过磁分离的方法分别用无水乙醇和去离子水分别洗涤粒子三次,最后将fmnps分散在5ml的超纯水中得到浓度为5mg/ml的溶液待用。
50.fmnps表面修饰叶酸包括如下步骤:将88.2mg(0.2mmol)fa溶于5mldmso中,然后按照加入催化剂0.8moldmap和20moledc,室温避光磁力搅拌活化2h,得活化反应液。量取5mlfmnps,与3mldmso混合,超声溶解后将其逐滴加入到恒温30℃的活化反应液中,通氮气
保持恒温30℃避光反应48h.反应结束后,将反应液在搅拌下加入到10倍量的冰无水乙醇中,经过静置过夜,洗涤,干燥,即得fa
‑
fmnps粗产物.在避光条件下,粗产物中加入6mlna2co3‑
nahco3(ph=10)缓冲溶液搅拌混匀,转移至透析袋(截留分子量为8000~14000)内,置于na2co3‑
nahco3(ph=10)缓冲溶液中进行透析,直至透析液于283nm处吸光度接近0时,再将透析液更换为蒸馏水继续避光透析2d,然后将透析袋内液体冻干,即得。
51.从图2可以看出,本实施例制备的叶酸修饰的荧光磁性纳米粒子fa
‑
fmnp分散性较好,各组分间没有明显分界,显然各组分间融合度较好。
52.实施例2
53.本实施例对实施例1制得的荧光磁性纳米粒子fa
‑
fmnps进行癌细胞检测,包括如下步骤:
54.mgc803细胞培养在18mm的玻片上,放置在12孔细胞培养板中培养,培养基为含10%胎牛血清的高糖dmem。3天后用pbs将细胞洗涤3次,
55.将细胞用500μl含50μg/mlfa
‑
fmnps纳米探针细胞培养缓冲液孵育30min,之后分别用pbs洗涤细胞3次,并用4%的多聚甲醛室温下固定细胞30min,然后用hoechst33258进行细胞核染色,最后封片后在荧光显微镜下观察。
56.实验结果如图3所示,从图3可以看出,在荧光显微镜下,采用实施例1所示的荧光探针,可以清晰的观测到癌症细胞。
57.以上所揭露的仅为本发明的优选实施例而已,当然不能以此来限定本发明之权利范围,因此依本发明申请专利范围所作的等同变化,仍属本发明所涵盖的范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。