用于靶实体检测的系统、组合物和方法
1.相关申请的交叉引用
2.本技术要求于2019年3月1日提交的美国临时申请号62/812,878和于2020年1月17日提交的美国临时申请号62/962,722的权益,所述申请中的每一个的内容在此整体并入本文。
背景技术:
3.癌症的早期检测大大增加了成功治疗的机会。然而,许多癌症仍然缺乏有效的筛选建议。癌症筛选测试的典型挑战包括有限的灵敏度和特异性。假阳性结果率高可能特别令人担忧,因为它会给不想不必要地施用(或接受)可能具有不希望的副作用的抗癌疗法的临床医生和患者带来困难的管理决策。相反,假阴性结果率高无法满足筛选测试的目的,因为错过了需要治疗的患者,从而导致治疗延迟,并因此降低成功的可能性。
技术实现要素:
4.本公开尤其提供了用于实现有效癌症筛选的见解和技术。在一些实施方案中,所提供的技术对于早期癌症的检测是有效的。在一些实施方案中,所提供的技术即使在应用于包含无症状个体或由无症状个体组成的人群时也是有效的(例如,由于足够高的灵敏度和/或低的假阳性和/或假阴性结果率)。在一些实施方案中,所提供的技术在应用于包含没有发展癌症的遗传风险的个体(例如,无症状个体)或由所述个体组成的人群时是有效的。在一些实施方案中,所提供的技术可以是或包括一种或多种组合物(例如,分子实体或复合物、系统、细胞、集合、组合、试剂盒等)和/或方法(例如,制造、使用、评估等方法),如对于阅读本文提供的公开的本领域技术人员来说将是清楚的。
5.在一些实施方案中,本公开用某些现有技术(包括例如癌症检测和诊断的某些常规方法)确定问题的根源。例如,本公开认识到许多常规诊断测定(例如,基于无细胞核酸、循环肿瘤细胞、蛋白质、血清蛋白质和/或细胞外囊泡的批量分析)可能是耗时的、昂贵的和/或缺乏足以提供可靠且全面的诊断评估的灵敏度和/或特异性。在一些实施方案中,本公开尤其提供了通过开发基于个体靶实体(例如,生物实体)上分子或表位的相互作用和/或共定位的靶实体检测方法来解决此类问题的技术(包括系统、组合物和方法)。
6.在一些实施方案中,本公开尤其提供了以下见解:对无症状个体进行筛选(例如,在出现症状之前或以其他方式在没有出现症状的情况下进行定期筛选)可能是有益的,并且甚至对于癌症的有效管理(例如,成功治疗)是重要的。替代地或另外,在一些实施方案中,本公开还提供了以下见解:针对不同类型的癌症(例如,针对多种不同癌症)进行筛选(例如,定期筛选)可能是有益的,并且甚至对于癌症的有效管理(例如,成功治疗)是重要的。在一些实施方案中,本公开提供了癌症筛选系统,在一些实施方案中,所述癌症筛选系统可被实施以例如检测无症状个体(例如,没有癌症遗传风险)中的癌症,包括早期癌症。在一些实施方案中,所提供的技术被实施以实现对无症状个体(例如,没有癌症遗传风险)和/或针对多种癌症的定期筛选。本公开提供了例如组合物(例如,试剂、试剂盒、组分等)以及
提供和/或使用它们的方法,包括涉及对一个或多个个体(例如,无症状个体)进行定期测试的策略。本公开定义了此类系统的有用性,并提供了用于实现它们的组合物和方法。
7.在一些实施方案中,所提供的技术实现对癌症和/或多种癌症的一个或多个特征(例如,发病、进展、对治疗的反应性、复发等)的检测(例如,早期检测,例如,在一个或多个无症状个体和/或一个或多个人群中),其中灵敏度和/或特异性(例如,假阳性和/或假阴性结果的比率)适用于允许将所提供的技术有用地应用于单次和/或定期(例如,周期性)评估。在一些实施方案中,所提供的技术可用于与个体的周期性体检结合。在一些实施方案中,所提供的技术可用于与一种或多种治疗方案结合;在一些实施方案中,所提供的技术可改善这样的一种或多种治疗方案的一个或多个特征(例如,根据接受的参数的成功率)。
8.在一些方面,提供了用于检测包含至少两个或更多个靶标(例如,分子靶标)的关注的实体(例如,生物或化学实体,诸如细胞、细胞外囊泡或分析物等)的技术,在一些实施方案中,这样的至少两个或更多个靶标可为相同的,而在一些实施方案中,这样的至少两个或更多个靶标可为不同的。在一些实施方案中,本公开提供了包含多个(例如,至少两个、至少三个或更多个)检测探针的系统,每个检测探针针对特定的这种靶标。在一些实施方案中,所提供的系统可包含两个或更多个(例如,3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个或更多个)检测探针。在一些实施方案中,单独的检测探针可针对不同的靶标。在一些实施方案中,两个或更多个单独的检测探针可针对相同的靶标。在一些实施方案中,所提供的系统包含针对不同靶标的两个或更多个不同的检测探针,并且任选地可包括也针对另一检测探针所针对的靶标的至少一个另外的检测探针。在一些实施方案中,所提供的系统包含多个检测探针子集,其中每个子集包含针对相同的靶标的两个或更多个检测探针。
9.通常,如本文所提供和/或使用的检测探针包含靶结合部分和偶联至靶结合部分的寡核苷酸结构域,寡核苷酸结构域包含双链部分和从寡核苷酸结构域的至少一端延伸的单链悬突。在许多实施方案中,单链悬突的至少一部分被设计成使得与第二检测探针的单链悬突互补,从而通过互补单链悬突的杂交与第二检测探针形成双链复合物。在许多实施方案中,检测探针的寡核苷酸结构域被配置成具有这样的长度,使得当第一检测探针和第二检测探针结合到同一关注的实体上(例如,关注的特定生物实体上)各自的靶标时,第一单链悬突和第二单链悬突足够紧密接近以允许杂交。
10.在涉及如本文所述和/或使用的检测探针的一些实施方案中,相应的寡核苷酸结构域具有长度为至少4至15个核苷酸的单链悬突。在一些实施方案中,单链悬突具有优先选择用于通过关注的特定核酸连接酶(例如,dna连接酶,诸如t4或t7连接酶)连接的核苷酸序列。例如,此种单链悬突可具有gagt的核苷酸序列。
11.在涉及如本文所述和/或使用的检测探针的一些实施方案中,相应的寡核苷酸结构域的长度可随例如关注的实体(例如,关注的生物实体)的物理特征和/或关注的实体(例如,关注的生物实体)中靶标(例如,分子靶标)的选择和定位而变化。例如,当生物实体是或包含细胞外囊泡(例如,外泌体)时,检测探针的寡核苷酸结构域可各自独立地具有例如约20nm至约200nm的长度,使得当相应的检测探针结合到同一细胞外囊泡时,它们各自的单链悬突足够紧密接近以彼此退火。
12.在涉及如本文所述和/或利用的系统中的至少一组两个(即,至少一对)检测探针
的一些实施方案中,此类检测探针的寡核苷酸结构域被配置成使得当第一检测探针和第二检测探针的单链悬突彼此退火以形成双链复合物时,每个相应的靶结合部分位于双链复合物的每一端。在此种双链复合物的一些实施方案中,双链复合物的两条链在核酸连接酶的存在下可连接以例如用于扩增和/或检测。
13.在涉及如本文所述和/或使用的系统中的至少三个或更多个(n≥3)检测探针的一些实施方案中,当检测探针的单链悬突退火于每个相应的配偶体以形成双链复合物时,至少(n
‑
2)个靶结合部分存在于双链复合物的一个或多个内部位置。在此种双链复合物的一些实施方案中,期望在双链复合物的单链中存在内部靶结合部分,使得双链复合物的另一条链不含任何内部靶结合部分,并且因此在存在核酸连接酶的情况下可连接以例如用于扩增和/或检测。
14.在一些实施方案中,本公开使用一组检测探针(例如,两个或更多个检测探针),它们一起对癌症(例如,如本文所述的特定癌症和/或癌症阶段)具有特异性,尽管一个或多个单独的此类探针可针对本身不对癌症具有特异性的靶标。例如,在一些实施方案中,一组有用的检测探针可包含针对对相关癌症具有特异性的靶标(即,癌症特异性靶标)的至少一个检测探针,并且还可包含针对不一定或完全特异于相关癌症的靶标(例如,也可在非癌性、非特定癌症和/或非特定关注的阶段的一些或所有细胞上发现)的至少一个检测探针。也就是说,如阅读本说明书的本领域技术人员将理解的,只要根据本发明使用的检测探针组是或包含多个单独的检测探针,它们一起对关注的相关靶生物实体(例如,关注的癌细胞或癌细胞分泌的细胞外囊泡)(即,将用于检测的相关靶生物实体(例如,关注的癌细胞或癌细胞分泌的细胞外囊泡)与用于检测的不受关注的其他生物实体区分开来)具有特异性,根据本发明的某些实施方案,所述组是有用的。
15.在双链复合物的链包含至少一个或多个内部靶结合部分的一些实施方案中,所述链包含内部靶结合部分所偶联的检测探针的寡核苷酸链末端与另一个检测探针的寡核苷酸链末端之间的缺口。在一些实施方案中,双链复合物的链内的缺口大小足够大,使得所述链在核酸连接酶的存在下变得不可连接。在一些实施方案中,缺口的大小可为至少2至8个核苷酸。在一些实施方案中,缺口的大小为约6个核苷酸。
16.在涉及如本文所述和/或使用的检测探针的一些实施方案中,靶结合部分是或包含针对特定靶标(例如,特定分子靶标)的抗体剂。在一些实施方案中,靶结合部分是或包含用于特定靶标(例如,特定分子靶标)的适体。例如,在一些实施方案中,检测探针的靶结合部分可以是或包含针对癌症相关靶标诸如癌症相关表位的抗体剂。例如,在一些实施方案中,癌症相关靶标可以是或包含与多于一种癌症(即,至少两种或更多种癌症)相关的靶标。在一些实施方案中,癌症相关可以是或包含通常与癌症相关的通用靶标。在一些实施方案中,癌症相关靶标可以是或包含与特定组织的癌症相关的靶标。在一些实施方案中,癌症相关靶标可以是或包含对特定癌症具有特异性的靶标。
17.在涉及如本文所述和/或使用的检测探针的一些实施方案中,检测探针的靶结合部分可针对组织特异性靶标(例如,存在于正常健康组织和/或诸如肿瘤的患病组织中)。在一些实施方案中,靶结合部分可针对与受试者的正常健康状况特异性相关的靶标。
18.在涉及如本文所述和/或使用的检测探针的一些实施方案中,寡核苷酸结构域通过共价连接(例如,通过键和/或接头)与靶结合部分偶联。将寡核苷酸共价偶联至各种试剂
(例如,肽、核酸或抗体)的方法是本领域已知的,并且可用于将寡核苷酸结构域偶联至靶结合部分以形成如本文所提供和/或使用的检测探针。
19.在一些实施方案中,适合根据本公开使用的系统可包含对照探针(例如,除了靶特异性检测探针之外)。例如,在一些实施方案中,对照探针被配置为结合到对照参考,使得其与关注的实体(例如,关注的生物实体)的结合抑制或阻止检测信号的产生(例如,通过抑制或阻止两个或更多个检测探针的连接和/或模板(诸如由两个或更多个检测探针的连接产生的模板)的扩增)。
20.在一些实施方案中,本文所述的技术尤其可用于通过与两个或更多个靶标(例如,分子靶标,其在一些实施方案中可表示单个分子靶标、复合物、剂等上的不同位点,或更常见地,可在不同分子靶标上)的相互作用来检测样品中(例如,生物、环境或其他样品中)的一种或多种关注的实体(例如,一种或多种生物和/或化学实体)。阅读本公开的本领域技术人员将认识到,所提供的技术可用于多种应用和/或目的。此种技术人员将进一步理解,本文所述的某些特定实施方案涉及使用如本文所述和/或使用的多个(例如,至少2个、至少3个或更多个)检测探针的方法。在一些实施方案中,方法包括将样品中的关注的实体(例如,生物实体)与适合根据本公开使用的一组检测探针接触。
21.在一些实施方案中,本文提供的方法可包括将待分析的关注的实体(例如,生物实体)固定在固体基底上。示例性固体基底可以是或包含珠或表面。在一些实施方案中,固体基底可以是或包含分析室的捕获表面(例如,实体捕获表面),包括例如珠、过滤器、基质、膜、板、管和/或孔。
22.在一些实施方案中,本文提供的方法包括允许一组检测探针(例如,如本文所述和/或使用的)结合到样品中的一个或多个关注的实体(例如,一个或多个生物实体),使得检测探针结合到关注的实体(例如,生物实体)中的相应的靶标(例如,分子靶标)(如果存在的话),以形成一种或多种双链复合物。在一些实施方案中,双链复合物通过与关注的实体(例如,生物实体)结合的检测探针的互补单链悬突的直接杂交或退火而形成。因此,在至少一些实施方案中,不需要连接器寡核苷酸来间接连接检测探针的寡核苷酸结构域;在一些实施方案中,不使用此类连接器寡核苷酸。因此,在一些实施方案中,本文提供的方法不包括在关注的实体(例如,生物实体)与多个检测探针接触后添加能够结合到第一检测探针的寡核苷酸结构域的至少一部分和第二检测探针的寡核苷酸结构域的至少一部分的连接器寡核苷酸。
23.双链复合物(由使关注的实体(例如,生物实体)与例如如本文所述和/或使用的检测探针接触而产生)可与核酸连接酶接触以产生连接模板,所述连接模板至少包含第一检测探针的寡核苷酸链和第二检测探针的寡核苷酸链。对此种连接模板的检测提供了关于样品中关注的实体(例如,生物实体)对于检测探针所针对的靶标是阳性还是阴性的信息。例如,可检测水平(例如,高于参考水平例如至少10%或更多的水平,其中在一些实施方案中,参考水平可为在阴性对照样品(诸如其中包含此类靶标的关注的实体不存在的样品)中观察到的水平)的这种连接模板指示测试的受关注实体(例如,生物实体)包含关注的靶标(例如,分子靶标),而不可检测水平(例如,低于可检测水平阈值的水平)的这种连接模板指示关注的靶标(例如,分子靶标)中的至少一个不存在于测试的受关注实体(例如,生物实体)中。
24.可通过本领域已知的适当的核酸检测方法检测连接模板。例如,在一些实施方案中,通过对连接模板进行扩增来检测连接模板,任选地随后检测扩增产物的存在。示例性核酸检测方法涉及定量聚合酶链反应。
25.本文所提供的技术可应用于包含待测定的关注的实体(例如,生物或化学实体,诸如细胞外囊泡和/或分析物)的关注的样品。例如,在一些实施方案中,样品可以是或包含生物样品。在一些实施方案中,样品可以是或包含环境样品。在一些实施方案中,样品可以是或包含原始样品。在一些实施方案中,样品可以是或包含处理的样品。例如,在一些实施方案中,可对样品进行处理以分离待测定的一个或多个关注的实体。
26.在样品包含或是生物样品的一些实施方案中,此种样品可来源于需要此种测定的受试者(例如,人受试者)的血浆或血液样品。在一些实施方案中,生物样品可以是或包含来自需要此种测定的受试者(例如,人受试者)的原始样品(例如,组织或肿瘤样品)。在一些实施方案中,可对生物样品进行处理,以将一个或多个关注的实体与关注的非靶实体分开和/或使一个或多个关注的实体富集。在一些实施方案中,存在于样品中的关注的实体可以是或包含生物实体,例如细胞或细胞外囊泡(例如,外泌体)。在一些实施方案中,可对此种生物实体进行处理或将其与化学试剂接触,以例如稳定和/或交联生物实体中待测定的靶标和/或减少与检测探针的非特异性结合。在一些实施方案中,生物实体是或包含细胞,可任选地用例如化学试剂对其进行处理,以用于稳定和/或交联靶标(例如,分子靶标)和/或用于减少非特异性结合。在一些实施方案中,生物实体是或包含细胞外囊泡(例如,外泌体),可任选地用例如化学试剂对其进行处理,以用于稳定和/或交联靶标(例如,分子靶标)和/或用于减少非特异性结合。
27.在一些实施方案中,本公开尤其提供了通过检测个体细胞外囊泡中癌症的靶生物标记物特征的共定位来解决与常规癌症诊断(例如,基于无细胞核酸、血清蛋白和/或细胞外囊泡的批量分析)相关的问题的技术(包括系统、组合物和方法),所述细胞外囊泡包含至少一种细胞外囊泡相关膜结合多肽和选自由以下组成的组的至少一个靶生物标记物:表面蛋白生物标记物、内部蛋白生物标记物和rna生物标记物。在一些实施方案中,本公开尤其提供了通过使用基于个体细胞外囊泡中至少两个或更多个靶实体(例如,靶生物标记物特征)的相互作用和/或共定位的靶实体检测方法(例如,本文所述的方法)检测癌症的此类生物标记物特征来解决此类问题的技术(包括系统、组合物和方法)。
28.在一些方面,提供了用于将受试者(例如,无症状受试者)分类为患有癌症或易患癌症的技术。在一些实施方案中,本公开提供了用于将受试者(例如,无症状受试者)分类为患有癌症或易患癌症的方法或测定。在一些实施方案中,所提供的方法或测定包括(a)在来自有需要的受试者的血液来源的样品中检测表达癌症的靶生物标记物特征的细胞外囊泡,所述靶生物标记物特征包含:至少一种细胞外囊泡相关膜结合多肽和选自由以下组成的组的至少一个靶生物标记物:表面蛋白生物标记物、囊泡内蛋白生物标记物和囊泡内rna生物标记物;(b)将指示血液来源的样品中表达靶生物标记物特征的细胞外囊泡的水平的样品信息与包括参考阈值水平的参考信息进行比较;以及(c)当血液来源的样品示出相对于参考阈值水平升高水平的表达靶生物标记物特征的细胞外囊泡时,将受试者分类为患有癌症或易患癌症。
29.在一些实施方案中,用于本文使用和/或描述的癌症的靶生物标记物特征的细胞
外囊泡相关膜结合多肽可以是或包含肿瘤特异性生物标记物和/或组织特异性生物标记物。在一些实施方案中,此种细胞外囊泡相关膜结合多肽可以是或包含非特异性标记物,例如,其存在于一种或多种非靶肿瘤和/或一种或多种非靶组织中。
30.在一些实施方案中,癌症的靶生物标记物特征可包含细胞外囊泡相关膜结合多肽和至少一种另外的靶表面蛋白生物标记物。
31.在一些实施方案中,癌症的靶生物标记物特征可包含细胞外囊泡相关膜结合多肽和至少一种靶囊泡内rna(例如,mrna)生物标记物。
32.在一些实施方案中,癌症的靶生物标记物特征可包含细胞外囊泡相关膜结合多肽(例如,本文所述的那些)和至少一种另外的靶囊泡内蛋白生物标记物。
33.在一些实施方案中,用于本文所述的所提供的方法或测定中的参考阈值水平通过在来自非癌症受试者群体的可比样品中观察到的表达靶生物标记物特征的细胞外囊泡的水平来确定。
34.在一些实施方案中,可使用基于抗体的剂检测包括在靶生物标记物特征中的细胞外囊泡相关膜结合多肽。在一些实施方案中,可使用包含基于抗体的剂的捕获测定检测此种细胞外囊泡相关膜结合多肽。例如,在一些实施方案中,用于检测细胞外囊泡中细胞外囊泡相关膜结合多肽的存在的捕获测定可涉及使包含细胞外囊泡的血液来源的样品与针对此种细胞外囊泡相关膜结合多肽的捕获剂接触。在一些实施方案中,此种捕获剂可包含针对细胞外囊泡相关膜结合多肽(例如,本文所述的那些)的结合部分,所述结合部分可任选地缀合至固体基底。在不受限制的情况下,用于细胞外囊泡相关膜结合多肽的示例性捕获剂可以是或包含固体基底(例如,磁珠)和针对细胞外囊泡相关膜结合多肽的结合部分(例如,抗体剂)。
35.在一些实施方案中,可使用本领域已知的适当方法检测包括在靶生物标记物特征中的靶生物标记物,所述适当方法可随着待检测分析物的类型(例如,表面蛋白、囊泡内蛋白、囊泡内rna(例如,mrna))而变化。例如,阅读本公开的本领域技术人员将理解,在一些实施方案中可使用基于抗体的剂来检测表面蛋白生物标记物和/或囊泡内蛋白生物标记物,而在一些实施方案中,可使用基于核酸的剂(例如使用定量逆转录pcr)检测囊泡内rna(例如,mrna)生物标记物。
36.例如,在靶生物标记物是或包含表面蛋白生物标记物和/或囊泡内蛋白标记物的一些实施方案中,可例如在捕获测定(例如,如本文所述的那些)捕获表达细胞外囊泡相关膜结合多肽的细胞外囊泡(例如,如本文使用和/或描述的那些)之后涉及邻近连接测定来检测此种靶生物标记物。在一些实施方案中,此种邻近连接测定可包括使包含细胞外囊泡的血液来源的样品与一组检测探针接触,每个检测探针针对靶生物标记物,所述组包含至少两个不同的检测探针,使得产生包含细胞外囊泡和检测探针组的组合,其中所述两个检测探针各自包含:(i)针对表面蛋白生物标记物和/或囊泡内蛋白生物标记物的结合部分;以及(ii)偶联至结合部分的寡核苷酸结构域,寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突部分。检测探针的此类单链悬突部分的特征在于它们在检测探针结合至相同的细胞外囊泡时可彼此杂交。然后将包含细胞外囊泡和检测探针组的此种组合保持在允许检测探针组与其在细胞外囊泡上的各自靶标结合的条件下,使得检测探针可结合至相同的细胞外囊泡以形成双链复合物。此种双链复合物可通过使双链复合物与核
酸连接酶接触产生连接模板;并检测连接模板来检测。此种连接模板的存在指示对癌症的靶生物标记物特征呈阳性的细胞外囊泡的存在。虽然此种邻近连接测定可执行得更好,例如具有比其他现有邻近连接测定更高的特异性和/或灵敏度,但阅读本公开的本领域技术人员将理解,可替代地使用本领域已知的其他形式的邻近连接测定。
37.在靶生物标记物是或包含囊泡内rna(例如,mrna)标记物的一些实施方案中,可涉及核酸检测测定来检测此种靶生物标记物。在一些实施方案中,示例性核酸检测测定可以是或包含逆转录pcr。
38.在靶生物标记物是或包含囊泡内生物标记物(例如,囊泡内蛋白生物标记物和/或囊泡内rna(例如,mrna)生物标记物)的一些实施方案中,可在检测测定(例如,如本文所述的邻近连接测定)之前涉及样品处理(例如,固定和/或透化)使用于随后检测的一种或多种囊内生物标记物暴露来检测此种靶生物标记物。
39.本公开尤其认识到,基于批量样品(例如,细胞外囊泡的批量样品)而不是以单个细胞外囊泡的分辨率对单个癌症相关血清蛋白或生物标记物或多个癌症相关生物标记物进行检测通常在确定从其获得样品的受试者是否可能患有或易患癌症方面不提供足够的特异性和/或灵敏度。本公开尤其提供了解决此类问题的技术,包括系统、组合物和/或方法,包括例如通过具体要求用于检测的个体靶实体(例如,个体生物实体,诸如个体细胞外囊泡)以存在靶标(例如,分子靶标)的组合为特征。在一些实施方案中,此种靶标组合可以是靶生物标记物特征,其包含至少一种或多种细胞外囊泡相关膜结合多肽和至少一种或多种靶生物标记物的组合。在特定的实施方案中,本公开教导需要此类个体实体(例如,生物实体,诸如细胞外囊泡)的技术以存在(例如,通过表达)具有癌症特异性的靶标(例如,分子靶标)的组合(即相关癌症的“靶生物标记物特征”)为特征,而不包含靶向组合(例如,靶生物标记物特征)的生物实体(例如,细胞外囊泡)不产生可检测的信号(例如,高于参考水平例如至少10%或更多的水平,其中在一些实施方案中,参考水平可为在阴性对照样品(诸如其中不存在包含此种靶向组合(例如,靶生物标记物特征)的个体生物实体(例如,个体细胞外囊泡)的样品)中观察到的水平)。
40.因此,在一些实施方案中,本文提供的技术可用于检测受试者和/或整个受试者群体中癌症的发病或复发。在一些实施方案中,可选择靶标的组合(例如,靶生物标记物特征)以用于癌症检测。在一些实施方案中,可选择靶标的组合(例如,靶生物标记物特征)以检测特定的癌症或其阶段和/或其亚型。在一些实施方案中,生物标记物的组合(例如,靶生物标记物特征)可通过检测探针的多个(例如,至少两个或更多个)成对或正交组合来检测,其中每对检测探针可针对至少一个不同的靶标。在一些实施方案中,生物标记物的组合(例如,靶生物标记物特征)可通过一组检测探针检测,每个检测探针被设计成彼此杂交以形成线性复合物。在一些实施方案中,可选择生物标记物的多个(例如,至少两个或更多个)组合以用于癌症检测。在一些实施方案中,可选择生物标记物的多个(例如,至少两个或更多个)组合以检测特定的癌症或其阶段和/或其亚型。在一些实施方案中,可选择生物标记物的多个(例如,至少两个或更多个)正交组合以用于癌症检测。在一些实施方案中,可选择生物标记物的多个(例如,至少两个或更多个)正交组合以检测特定的癌症或其阶段和/或其亚型。在一些实施方案中,可选择多个(例如,至少两个或更多个)靶生物标记物特征以用于癌症检测。在一些实施方案中,可选择多个(例如,至少两个或更多个)靶生物标记物特征以检测特
定的癌症或其阶段和/或其亚型。在一些实施方案中,本文提供的技术可定期(例如,每年)用于筛选人受试者或整个人受试者群体的早期癌症或癌症复发。
41.在一些实施方案中,可选择检测探针的组合(例如,一组)以检测特定癌症的系统或方法(例如,本文所述的那些)。在一些实施方案中,选择检测探针的组合(例如,一组)以检测一种或多种癌症的系统或方法(例如,本文所述的那些)。在一些实施方案中,检测探针的组合(例如,一组)可包括检测探针的多个(例如,至少两个或更多个)成对或正交组合,其中每对检测探针可针对至少一个不同的靶。在一些实施方案中,以组合(例如,一组)形式的检测探针可各自被设计成彼此杂交以形成线性复合物。在一些实施方案中,可通过本文提供的技术检测的癌症的实例包括但不限于急性淋巴细胞性白血病、急性髓系白血病、胆管癌、膀胱癌、脑癌、乳腺癌、宫颈癌、慢性淋巴细胞性白血病、慢性髓系白血病、结直肠癌、子宫内膜癌、食道癌、胃肠癌、霍奇金淋巴瘤(hodgkin lymphoma)、肾癌、肝癌、肺癌、多发性骨髓瘤、非霍奇金淋巴瘤、卵巢癌、胰腺癌、前列腺癌、肉瘤、皮肤癌和胃癌。
42.在一些实施方案中,适用于本文提供的用于检测癌症的发病或复发的技术的受试者可为无症状人受试者和/或整个无症状人群。此种无症状受试者可为具有癌症家族史的受试者、先前接受过癌症治疗的受试者、在癌症治疗后有癌症复发风险的受试者、在癌症治疗后有所缓解的受试者和/或先前或定期筛选至少一种癌症生物标记物的存在的受试者。替代地,在一些实施方案中,无症状受试者可为先前未经癌症筛选的受试者、未诊断为癌症的受试者和/或先前未接受癌症治疗的受试者。
43.在一些实施方案中,可基于一个或多个特征来选择受试者或受试者群体,所述一个或多个特征诸如年龄、种族、遗传史、病史、个人史(例如,吸烟、酒精、药物、致癌剂、饮食、肥胖、身体活动、光暴露、放射暴露、暴露于诸如病毒的感染性因子和/或职业危害)。
44.在一些实施方案中,本文提供的技术可用于选择针对患有或易患癌症的受试者的疗法。在一些实施方案中,可根据基于本文提供的技术的发现来选择癌症疗法和/或辅助疗法。
45.在一些实施方案中,本文提供的技术可用于监测和/或评估施用于受试者(例如,癌症受试者)的疗法的功效。
46.在一些实施方案中,本公开提供了用于管理患者护理的技术,以用于例如一个或多个个体受试者和/或整个受试者群体。仅举几个实例,在一些实施方案中,本公开提供了可用于筛选(例如,临时或偶然动机的筛选和/或非临时或偶然动机的筛选,例如周期性筛选,诸如年度、半年、两年或以某种其他频率)的技术。例如,在一些实施方案中,所提供的用于临时动机筛选的技术可用于筛选具有特定年龄或年龄组(例如,超过某个年龄(例如,超过20、25、30、35、40、45、50、55、60、65、70岁或以上))的一个或多个个体受试者或整个受试者(例如,无症状受试者)群体。在一些实施方案中,所提供的用于偶然动机筛选的技术可用于筛选可能经历了促使筛选如本文所述的癌症的事故或事件的个体受试者。例如,在一些实施方案中,与确定癌症或其易患性的一个或多个指标相关的偶然动机可以是或包括例如,基于他们的家族史的事故(例如,近亲诸如血缘亲属先前被诊断为癌症);鉴定癌症的一个或多个风险因素(例如,吸烟、酒精、饮食、肥胖、职业危害等);和/或来自基因测试(例如,基因组测序)和/或成像诊断测试(例如,超声、计算机断层扫描(ct)和/或磁共振成像(mri)扫描)的先前偶然发现;发展具有癌症特征的一种或多种体征或症状(例如,可能指示肺癌
的持续咳嗽;可能指示乳腺癌的乳腺组织中的肿块;可能指示gi癌的胃肠(gi)道出血;或可能指示卵巢癌的女性经期异常出血等)。
47.在一些实施方案中,所提供的用于管理患者护理的技术可通知治疗和/或支付(例如,治疗的报销)决定和/或行动。例如,在一些实施方案中,所提供的技术可提供对个体受试者是否具有疾病或病症(例如,癌症)的发病或复发的一个或多个指标的确定,从而通知医师和/或患者何时根据此类发现开始治疗。另外或替代地,在一些实施方案中,所提供的技术可例如基于特定反应性生物标记物(例如,癌症反应性生物标记物)的发现来通知医师和/或患者治疗选择。在一些实施方案中,所提供的技术可例如基于与疾病、病症或病状(例如,癌症)相关的一个或多个分子靶标水平的变化的发现来提供对个体受试者是否对当前治疗有反应的确定,从而通知医师和/或患者此类治疗的功效和/或根据此类发现保持或改变治疗的决定。
48.在一些实施方案中,所提供的技术可通知关于健康保险提供者是否报销(或不报销)例如以下的决定:(1)筛选本身(例如,报销仅可用于周期性/定期筛选或仅可用于临时和/或偶然动机的筛选);和/或(2)根据所提供的技术的发现开始、保持和/或改变治疗。例如,在一些实施方案中,本公开提供了与以下有关的方法:(a)接收如本文所述的筛选结果,并且还接收对筛选和/或特定治疗方案的报销请求;(b)如果根据适当的时间表或对相关事故的反应对受试者进行筛选,则批准报销筛选;和/或如果治疗方案根据接收的筛选结果代表适当治疗,则批准治疗的报销方案;以及任选地(c)实现报销或提供报销被拒绝的通知。在一些实施方案中,如果接收的筛选结果检测到代表相关治疗方案的批准的生物标记物(例如,如处方信息标签和/或通过批准的伴随诊断所述)的生物标记物,则根据接收的筛选结果,治疗方案是合适的。替代地或另外,本公开设想允许或促进如本文所述的筛选结果和/或报销决定的报告和/或处理的报告系统(例如,通过一个或多个适当的电子装置和/或一个或多个通信系统实施)。
49.本文提供的一些方面涉及用于所提供的技术的系统和试剂盒。在一些实施方案中,系统或试剂盒包含至少一组检测探针(例如,如本文所述和/或使用的),每个检测探针都针对靶标。在一些实施方案中,所提供的系统或试剂盒中的一组检测探针包含两个或更多个(例如,3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个或更多个)检测探针。在一些实施方案中,单独的检测探针可针对不同的靶标。在一些实施方案中,两个或更多个单独的检测探针可针对相同的靶标。在一些实施方案中,所提供的系统或试剂盒包含针对不同靶标的两个或更多个不同的检测探针,并且任选地可包括也针对另一检测探针所针对的靶标的至少一个另外的检测探针。
50.本文提供的一些方面涉及用于所提供的与生物标记物检测和/或表征相关的技术的系统和试剂盒。在一些实施方案中,系统或试剂盒可包含针对疾病或病症(例如,癌症)的靶生物标记物特征的检测剂。在一些实施方案中,此种系统或试剂盒可包含捕获剂,其用于存在于与疾病或病症(例如,癌症)相关的细胞外囊泡中的细胞外囊泡相关膜结合多肽;以及(b)至少一种或多种检测剂,其针对此种疾病或病症(例如,癌症)的靶生物标记物特征的一种或多种靶生物标记物,其可以是或包含另外的一种或多种表面蛋白生物标记物、一种或多种囊泡内蛋白生物标记物和/或一种或多种囊泡内rna(例如,mrna)生物标记物。
51.在一些实施方案中,包括在系统和/或试剂盒中的捕获剂可包含针对细胞外囊泡
相关膜结合多肽的结合部分。在一些实施方案中,此种结合部分可缀合至固体基底,其在一些实施方案中可以是或包含固体基底。在一些实施方案中,此种固体基底可以是或包含磁珠。在一些实施方案中,包括在所提供的系统和/或试剂盒中的示例性捕获剂可以是或包含固体基底(例如,磁珠)和针对与其缀合的细胞外囊泡相关膜结合多肽的抗体剂。
52.在靶生物标记物包括表面蛋白生物标记物和/或囊泡内蛋白生物标记物的一些实施方案中,系统和/或试剂盒可包括用于进行邻近连接测定的检测剂(例如,如本文所述的检测剂)。在一些实施方案中,用于进行邻近连接测定的此类检测剂可包含一组检测探针,每个检测探针针对靶生物标记物特征的靶生物标记物,所述组包含至少两个检测探针,其中所述两个检测探针各自包含:(i)针对靶生物标记物的多肽结合部分;以及(ii)偶联至结合部分的寡核苷酸结构域,寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突部分,其中检测探针的单链悬突部分的特征在于它们在检测探针结合至相同的细胞外囊泡时可彼此杂交。
53.在一些实施方案中,所提供的系统和/或试剂盒可包含多个(例如,2、3、4、5个或更多个)检测探针组,其中每组包含两个或更多个(例如,3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个或更多个)检测探针。在一些实施方案中,每组可针对用于不同疾病、病症或病状的检测。在一些实施方案中,两组或更多组可针对用于相同疾病、病症或病状的检测。在一些实施方案中,至少一组或多组(例如,至少一组、至少两组、至少三组、至少四组、至少五组或更多组)检测探针可针对用于癌症的检测。例如,在一些实施方案中,每组可针对用于不同癌症(例如,与相同或不同组织相关联的不同癌症类型)的检测。在一些实施方案中,两组或更多组可针对相同癌症的检测。在一些实施方案中,所提供的系统和/试剂盒可包含用于检测一种癌症的至少一组检测探针和用于检测不同癌症(例如,胰腺癌)的至少一组检测探针。在一些实施方案中,两个或更多个检测探针可针对不同的癌症亚型和/或类别。在一些实施方案中,两组或更多组可针对不同阶段的癌症的检测。在一些实施方案中,两组或更多组可针对相同阶段的癌症的检测。
54.在一些实施方案中,所提供的试剂盒中的检测探针可作为容器中的单一混合物提供。在一些实施方案中,多组检测探针可作为单独容器中的单独混合物提供。在一些实施方案中,每个检测探针在单独的容器中单独地提供。
55.在靶生物标记物包括囊泡内rna(例如,mrna)生物标记物的一些实施方案中,此种系统和/或试剂盒可包括用于进行核酸检测测定的检测剂。在一些实施方案中,此种系统和/或试剂盒可包括用于进行定量逆转录pcr的检测剂,例如,所述定量逆转录pcr可包含针对一个或多个囊泡内rna(例如,mrna)靶标的引物。
56.在一些实施方案中,所提供的系统和/或试剂盒可包含至少一种化学试剂,以例如处理样品和/或其中关注的实体(例如,细胞外囊泡)。在一些实施方案中,所提供的系统和/或试剂盒可包含至少一种化学试剂以处理样品中的关注的实体(例如,关注的生物实体,诸如细胞外囊泡),所述至少一种化学试剂包括例如但不限于固定剂、透化剂和/或封闭剂。在一些实施方案中,所提供的系统和/或试剂盒可包含核酸连接酶和/或核酸聚合酶。在一些实施方案中,所提供的系统和/或试剂盒可包含一个或多个引物和/或探针。在一些实施方案中,所提供的系统和/或试剂盒可包含一对或多对引物,以例如用于pcr,例如定量pcr(qpcr)反应。在一些实施方案中,所提供的系统和/或试剂盒可包含一个或多个探针,例如
像在一些实施方案中可被设计为增加qpcr的特异性的水解探针(例如,taqman探针)。在一些实施方案中,所提供的系统和/或试剂盒可包含一个或多个多路复用探针,例如当采用同时或并行qpcr反应时可能是有用的(例如,以促进或改进读出)。
57.在一些实施方案中,所提供的系统和/或试剂盒可用于筛选(例如,定期筛选)和/或其他评估个体(例如,无症状或有症状受试者)以便检测(例如,早期检测)疾病或病症(例如,癌症)。在一些实施方案中,所提供的系统和/或试剂盒可用于筛选和/或其他评估易患疾病或病症(例如,癌症)的个体(例如,具有已知遗传、环境或经验风险等的个体)。在一些实施方案中,所提供的系统和/或试剂盒可用于监测先前接受过治疗的受试者的疾病或病症(例如,癌症)的复发。在一些实施方案中,所提供的系统和/或试剂盒可结合用于患有疾病或病症(例如,癌症)的受试者的疗法用作伴随诊断。在一些实施方案中,所提供的系统和/或试剂盒可用于监测或评估施用于患有疾病或病症(例如,癌症)的受试者的疗法的功效。在一些实施方案中,所提供的系统和/或试剂盒可用于为患有疾病或病症(例如,癌症)的受试者选择疗法。在一些实施方案中,所提供的系统和/或试剂盒可用于为具有与疾病或病症(例如,癌症)相关的一种或多种症状(例如,非特异性症状)的受试者做出治疗决定和/或选择疗法。
58.在一些实施方案中,可选择在试剂盒或系统中提供和/或使用的一组检测探针以筛选(例如,定期筛选)或诊断特定癌症(包括例如但不限于急性淋巴细胞性白血病、急性髓系白血病、胆管癌、膀胱癌、脑癌、乳腺癌、宫颈癌、慢性淋巴细胞性白血病、慢性髓系白血病、结直肠癌、子宫内膜癌、食道癌、胃肠癌、霍奇金淋巴瘤、肾癌、肝癌、肺癌、多发性骨髓瘤、非霍奇金淋巴瘤、卵巢癌、胰腺癌、前列腺癌、肉瘤、皮肤癌和胃癌)。
59.在一些实施方案中,所提供的试剂盒或系统可包含多个检测探针组,每组包含用于检测不同癌症的至少两个或更多个检测探针。例如,此种试剂盒可用于在单次测定中筛选(例如,定期筛选)受试者或整个受试者群体的各种癌症(包括例如但不限于急性淋巴细胞性白血病、急性髓系白血病、胆管癌、膀胱癌、脑癌、乳腺癌、宫颈癌、慢性淋巴细胞性白血病、慢性髓系白血病、结直肠癌、子宫内膜癌、食道癌、胃肠癌、霍奇金淋巴瘤、肾癌、肝癌、肺癌、多发性骨髓瘤、非霍奇金淋巴瘤、卵巢癌、胰腺癌、前列腺癌、肉瘤、皮肤癌和胃癌)。
60.由与关注的实体(例如,化学或生物实体,诸如细胞外囊泡或分析物)结合的至少两个或更多个检测探针(例如,如本文所述和/或使用的)形成的双链复合物也在本公开的范围内。
61.通过进行本文所述的方法和/或使用本文所述的系统和/或试剂盒形成的复合物也在本公开的范围内。例如,在一些实施方案中,复合物包含:(a)表达靶生物标记物特征的细胞外囊泡,其中至少两个包括至少一种细胞外囊泡相关膜结合多肽和选自由以下组成的组的至少一个靶生物标记物:表面蛋白生物标记物、囊泡内蛋白生物标记物和囊泡内rna生物标记物,其中细胞外囊泡固定在包含针对此种细胞外囊泡相关膜结合多肽的结合部分的固体基底上。此种复合物还包含针对存在于细胞外囊泡中的靶生物标记物特征的至少一个靶生物标记物的至少两个检测探针,其中每个检测探针结合到此种靶生物标记物,并且各自包含:(i)针对靶生物标记物的结合;以及(ii)偶联至结合部分的寡核苷酸结构域,寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突部分,其中检测探针的单链悬突部分彼此杂交。
62.这些以及本公开所涵盖的其他方面在下文和权利要求中更详细地描述。
附图说明
63.图1是说明剖析单个细胞外囊泡(ev)的示例性工作流程的示意图。所述图示出了使用尺寸排阻色谱法(sec)从血浆中纯化ev和免疫亲和捕获显示出特定膜结合蛋白标记物的ev(图a);使用根据本文所述的一些实施方案的靶实体检测测定法检测捕获的ev上的共定位靶标记物(例如,囊泡内蛋白质或表面蛋白质)(图b)。
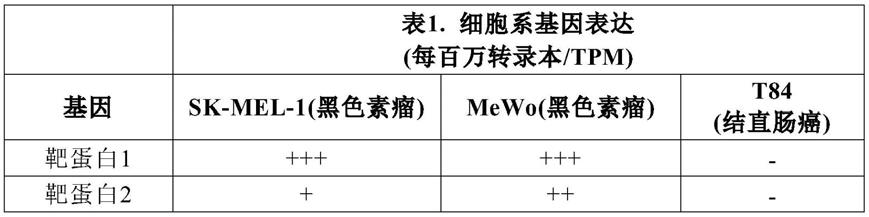
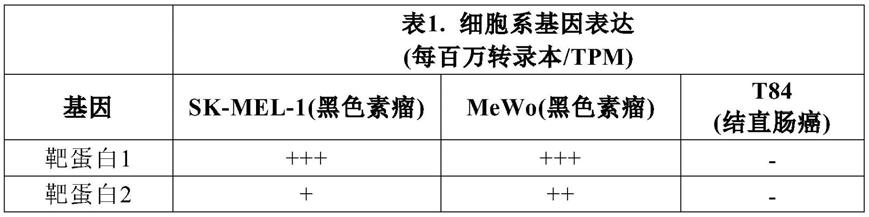
64.图2a至图2b是说明根据本文所述的一些实施方案的靶实体检测测定的示意图。在一些实施方案中,图2a示出了使用检测探针的组合的靶实体检测测定,所述组合对癌症的检测具有特异性。在一些实施方案中,将包括针对靶蛋白1(例如,癌症标记物1)的第一检测探针和针对靶蛋白2(例如,癌症标记物2)的第二检测探针的双链体系统添加到包含生物实体(例如,细胞外囊泡或分析物)的样品中。在一些实施方案中,检测探针各自包含偶联至寡核苷酸结构域的靶结合部分(例如,针对靶蛋白的抗体剂),所述寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突。当第一检测探针和第二检测探针的不同靶结合部分(例如,分别针对靶蛋白1和靶蛋白2的抗体剂)紧密接近同一生物实体(例如,细胞外囊泡或分析物)定位使得相应的单链悬突彼此杂交,从而允许它们的寡核苷酸结构域发生连接时,产生检测信号。例如,对照实体(例如,来自健康受试者样品的生物实体)不表达靶蛋白1(例如,癌症标记物1)和靶蛋白2(例如,癌症标记物2)中的一个或两个,因此不能产生信号检测。然而,当来自癌症样品的生物实体表达靶蛋白1和靶蛋白2,并且靶蛋白以彼此足够短的距离存在于同一生物实体(例如,细胞外囊泡)中时,产生检测信号。图2b示出了包含第一检测探针和第二检测探针的双链复合物的非限制性实例,所述第一检测探针和第二检测探针通过它们各自的单链悬突的直接杂交而彼此连接。
65.图3是示出含有或不含dna连接酶(例如,t4或t7连接酶)的连接模板的qpcr检测的图。
66.图4是示出不同的细胞样品(例如,癌细胞样品,诸如t84、mewo或sk
‑
mel
‑
1细胞样品)中连接模板的qpcr检测的图。
67.图5a是说明根据本文所述的一些实施方案的靶实体检测测定的示意图。所述图示出了示例性三链体靶实体检测系统,其中在一些实施方案中,可将三个或更多个检测探针(每个针对靶蛋白)添加到包含生物实体(例如,细胞外囊泡)的样品中。在一些实施方案中,检测探针各自包含偶联至寡核苷酸结构域的靶结合部分(例如,针对靶蛋白的抗体剂),所述寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突。当所有三个或更多个检测探针的相应单链悬突彼此杂交以形成线性双链复合物,并且双链复合物的至少一条链发生连接时,产生检测信号,从而允许检测所得的连接产物。图5b是包含四个检测探针的双链复合物的非限制性实例,所述检测探针通过它们各自的单链悬突的杂交以线性排列彼此连接。
68.图6是示出当所有三个不同检测探针的相应寡核苷酸结构域存在时连接产物的qpcr检测的图。
69.图7是示出当三个检测探针中的两个(例如,针对靶标1和靶标3)存在时连接产物的qpcr检测的图。
70.图8是示出当三个检测探针中的两个(例如,针对靶标1和靶标2)存在时连接产物的qpcr检测的图。
71.图9是示出当三个检测探针中的两个(例如,针对靶标2和靶标3)存在时连接产物的qpcr检测的图。
72.图10是说明本文所述的示例性实施方案的靶实体检测测定的示意图。在一些实施方案中,将多个检测探针(每个针对不同的靶标)添加到包含生物实体(例如,细胞外囊泡)的样品中。在一些实施方案中,检测探针各自包含偶联至寡核苷酸结构域的靶结合部分(例如,抗体剂),所述寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突。当所有检测探针都紧密接近同一生物实体(例如,细胞外囊泡或分析物)定位使得相应的单链悬突杂交以形成线性双链复合物,并且所得的线性双链复合物的至少一条链发生连接时,产生检测信号,从而允许检测连接产物。
73.图11是说明本文所述的示例性实施方案的靶实体检测测定的示意图。在一些实施方案中,靶实体检测测定利用检测探针的组合,所述组合对癌症(例如,特定癌症,例如像黑色素瘤和/或癌症的特定阶段)的检测具有特异性。在一些实施方案中,检测探针的此种组合包括至少两个或更多个靶特异性检测探针,每个针对靶蛋白(其在一些实施方案中可为相同的靶蛋白,或在一些实施方案中可为不同的蛋白质),以及至少一个或多个对照探针,例如,阴性对照探针,其结合抑制或阻止检测探针的连接;在一些实施方案中,对照探针可针对例如与癌症无关的蛋白质或肽,诸如在关注的实体(例如,生物实体)中的存在指示关注的实体对于疾病、病症或病状(例如,癌症)为阴性的蛋白质或肽。在一些实施方案中,将检测探针的此种组合添加到包含生物实体(例如,细胞外囊泡或分析物)的样品中。在一些实施方案中,检测探针各自包含偶联至寡核苷酸结构域的靶结合部分(例如,抗体剂或适体),所述寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突。当所有靶特异性检测探针(例如,分别针对靶蛋白1、靶蛋白2和靶蛋白3)而不是对照探针紧密接近同一生物实体(例如,细胞外囊泡或分析物)定位时,产生检测信号。靶特异性检测探针的相应单链悬突杂交以形成双链复合物,并且所得的双链复合物的至少一条链发生连接,从而允许检测连接产物。例如,即使当对照实体(例如,来自健康受试者样品的生物实体)表达所有三种靶蛋白时,也不能产生检测信号,因为存在与癌症无关的对照蛋白。然而,当来自癌症样品(例如,黑色素瘤)的生物实体在与癌症无关的对照蛋白不存在的情况下表达所有三种靶蛋白,并且靶蛋白以彼此足够短的距离存在于同一生物实体(例如,细胞外囊泡或分析物)中时,可产生检测信号。在一些实施方案中,包括对照探针可选择性地去除假阳性,从而提高检测的特异性。
74.图12是说明涉及竞争性抑制连接的本文所述的示例性实施方案的靶实体检测测定的示意图。如图11所示,当对照探针与其他靶标特异性检测探针定位于同一生物实体时,不能形成连接产物。在一些实施方案中,对照探针被设计使得(i)它布置在两个靶特异性检测探针之间;并且(ii)对照探针的一端为平端,并因此不能与其他检测探针连接。另外或替代地,对照探针可在链的一端具有双脱氧核苷酸以使其不可连接。
75.图13a至图13b是示出包含黑色素瘤细胞系(mewo)衍生的细胞外囊泡、结直肠癌细胞系(t84)衍生的细胞外囊泡且不含模板(阴性对照)的样品中连接模板的qpcr检测的图。图13a示出了从示例性双链体系统(例如,如本文所述)获得的实验数据。图13b示出了从示
例性三链体系统(例如,如本文所述)获得的实验数据。
76.图14a至图14d是示出使用示例性双链体检测测定法(其中检测探针针对如表4所示的一组特定的生物标记物)测定掺加已知量的癌细胞系衍生的细胞外囊泡的血浆样品中的细胞外囊泡而获得的平均δct值(使用健康患者样品作为基线)的图。图14a示出了基于针对靶标记物a和靶标记物b(组合1)的检测探针的使用的数据。图14b示出了基于针对靶标记物e和靶标记物f(组合2)的检测探针的使用的数据。图14c示出了基于针对靶标记物e和靶标记物a(组合3)的检测探针的使用的数据。图14d示出了基于针对靶标记物g和靶标记物f(组合4)的检测探针的使用的数据。
77.图15a至图15c是示出使用示例性双链体检测测定法(其中检测探针针对靶标记物e和靶标记物a的组合(如表4所示的组合3))测定获自iv期肺腺癌患者和正常健康受试者的血浆样品中的细胞外囊泡而获得的实验数据的图。图15a示出了平均δct值(使用健康患者样品a作为基线)。图15b示出了归一化信号,计算为2
δ_ct
。图15c示出了将样品分类为健康或iv期肺腺癌的受试者工作特征(roc)曲线,其阈值为平均健康归一化信号加三个标准偏差。
78.图16a至图16c是示出使用示例性双链体检测测定法(其中检测探针针对靶标记物e和靶标记物h的组合(如表4所示的组合5))测定获自iv期肺腺癌患者和正常健康受试者的血浆样品中的细胞外囊泡而获得的实验数据的图。图16a示出了平均δct值(使用健康患者样品a作为基线)。图16b示出了归一化信号,计算为2
δ_ct
。图16c示出了将样品分类为健康或iv期肺腺癌的受试者工作特征(roc)曲线,其阈值为平均健康归一化信号加三个标准偏差。
79.图17示出了使用分别如图15b和图16b所示的组合3标记物和组合5标记物获得的归一化信号之间的相关性。
80.图18是示出可用于减少或抑制非特异性连接模板产生可检测信号,从而减少背景信号的示例性抑制剂寡核苷酸的示意图。
81.图19示出了在不同细胞系衍生的细胞外囊泡样品中,来自例如使用图1或图2a至图2b中所示的测定的连接样品的qpcr检测的实验数据。在一些实施方案中,靶实体检测测定包括用于捕获基于癌症标记物1的细胞外囊泡的剂(“癌症标记物1捕获器”)以及例如涉及至少两个检测探针的示例性双链体系统,每个检测探针包含针对偶联至不同的寡核苷酸结构域的癌症标记物2(例如,抗癌标记物2抗体)的结合部分,所述寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突(“癌症标记物2 癌症标记物2抗体探针”)。图a示出了对生物标记物阳性癌细胞系ev(阳性细胞系)与生物标记物阴性癌细胞系ev(阴性细胞系)的检测进行比较的qpcr数据的图。图b示出了使用阴性对照细胞系(例如,生物标记物阴性癌细胞系)作为基线的相应平均δct值。
82.图20是示出包括在癌症患者血浆样品研究中的患者的人口统计资料的图,其示出了通过示例性测定评估的患者群组的年龄和群组大小。
83.图21是示出在两个不同截止值处用于检测涉及基于具有癌症标记物2 癌症标记物2抗体探针的癌症标记物1捕获器的双链体系统(例如,如图1或图2a至图2b中所述)的靶癌的示例性测定的性能的图。截止值1与99.8%的特异性有关,并且截止值2与98%的特异性有关。
84.图22是示出用于检测靶癌症的示例性测定与靶癌症的当前护理标准相比的性能(血清蛋白和/或成像)的一组数据。对特异性(图a和图d)、灵敏度(图b和图e)和阳性预测值
(图c和图f)进行比较,以筛选处于靶癌症的遗传风险(图a、图b和图c)和平均风险(图d、图e和图f)的受试者。
85.图23是示出在来自癌细胞系与阴性对照细胞系的ev中检测到靶生物标记物1mrna的一组图。(图a)使用rt
‑
qpcr检测批量ev中的靶生物标记物1mrna。(图b)与批量ev相比,检测使用抗靶生物标记物2功能化珠捕获的ev中的靶生物标记物1mrna。
86.图24是示出说明寡核苷酸长度对测定信号的影响的原始qpcr数据的图。使用抗靶1功能化磁珠捕获细胞系ev,并且使用用于本文所述的示例性双链体靶实体检测系统的抗靶1和抗靶2检测探针生成信号。
87.图25是示出使用示例性双链体检测测定法(其中检测探针针对如表6所示的组合1)测定细胞系ev获得的平均δct值(使用健康血浆样品作为基线)的图。
88.图26是说明本文所述的示例性实施方案的靶实体检测测定的示意图。在一些实施方案中,靶实体检测测定利用检测探针的组合,所述组合在一些实施方案中对靶标具有特异性,以例如检测来自关注的组织(如图26所示的组织a)的靶实体。在一些实施方案中,检测探针的此种组合包括至少两个或更多个靶特异性检测探针,每个检测探针针对存在于关注的实体中的靶标(其在一些实施方案中可为相同的靶标,或在一些实施方案中可为不同的靶标)。在一些实施方案中,检测探针各自包含偶联至寡核苷酸结构域的靶结合部分(例如,抗体剂或适体),所述寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突。在一些实施方案中,此种靶实体检测测定还包含至少一个或多个至少一个或多个对照探针,例如,被设计来减少与非靶标的交叉反应性的抑制剂探针。例如,在一些实施方案中,抑制剂探针被设计成使其与非靶实体的结合在允许与另一探针(例如,检测探针)连接的情况下抑制或阻止连接模板的扩增。例如,如图26所示,在一些实施方案中,抑制剂探针可针对非靶标,例如,与靶组织无关的标记物,或与待诊断的疾病、病症或病状(例如,癌症)无关的标记物。在一些此类实施方案中,抑制剂探针类似于如本文所述的检测探针,使得当检测探针和抑制剂探针紧密接近时,它们的单链悬突彼此杂交,从而允许连接。然而,与本文所述的检测探针不同,此种抑制剂探针的寡核苷酸结构域的至少一条链不具有引物位点,因此阻止可能由于检测探针和抑制剂探针之间的相互作用而形成的任何连接模板的扩增。在一些实施方案中,将检测探针和一个或多个抑制剂探针的组合添加到包含生物实体(例如,细胞外囊泡或分析物)的样品中。当所有靶特异性检测探针(例如,针对来自组织a的靶标1、来自组织a的靶标2)而不是抑制剂探针紧密接近同一生物实体(例如,细胞外囊泡或分析物)定位时,产生检测信号。靶特异性检测探针的相应单链悬突杂交以形成双链复合物,并且所得的双链复合物的至少一条链发生连接,从而允许检测连接产物。在存在与非靶实体(例如,来自不同组织的生物实体)结合的抑制剂探针的情况下,不能产生检测信号,因为抑制剂探针抑制模板的扩增。在一些实施方案中,包括此种抑制剂探针可选择性地去除假阳性,从而提高检测的特异性。
89.图27是示出来自如所示的13种不同模板组合的原始qpcr数据的图。
90.图28是示出在具有和不具有如所示的抑制剂探针的溶液中连接模板的qpcr检测的图:(1 3) (2 4)链;(1 3) (2 4) 1x(1i 3i)链;(1 3) (2 4) 1x(2i 4i)链;(1 3) (2 4) 2x(1i 3i)链;(1 3) (2 4) 2x(2i 4i)链;和(1 3) (2 4) 1x(1i 3i) 1x(2i 4i)链。
91.图29是示出在存在或不存在抑制剂探针的情况下(例如,如图26所示)使用具有检
测探针的示例性双链体检测测定法测定细胞系ev产生的原始qpcr数据的图。
92.某些定义
93.施用:如本文所用,术语“施用(administering/administration)”通常是指将组合物施用于受试者,以实现将是组合物或包括在组合物中的剂递送到靶位点或待治疗的位点。本领域普通技术人员将了解在适当的情况下可用于施用于受试者(例如人)的多种途径。例如,在一些实施方案中,施用可为胃肠外的。在一些实施方案中,施用可为口服的。在一些实施方案中,施用可仅涉及单剂量。在一些实施方案中,施用可涉及应用固定数量的剂量。在一些实施方案中,施用可涉及间歇性(例如,在时间上分开的多个剂量)和/或周期性(例如,由相同的时间段分开的个人剂量)给药的给药。在一些实施方案中,施用可涉及连续给药(例如,灌注)至少一段选定的时间。
94.扩增:术语“扩增(amplification和amplify)”是指导致核酸分子的量和/或水平相对于其初始量和/或水平增加的模板依赖性过程。模板依赖性过程通常是涉及引物分子的模板依赖性延伸的过程,其中新合成的核酸链的序列由众所周知的互补碱基配对规则决定(参见例如,watson,j.d.等人,于:molecular biology of the gene,第4版,w.a.benjamin,inc.,menlo park,calif.(1987))。
95.分析物:如本文所用,术语“分析物”是指待测定的样品中的实体、物质、成分或复合物。在一些实施方案中,分析物可以是或包含生物分析物。在一些实施方案中,分析物可以是或包含化学分析物。在一些实施方案中,分析物可以是或包含多肽或蛋白质。在一些实施方案中,分析物可以是或包含核酸。在一些实施方案中,分析物可以是或包含细胞或微生物,包括病毒或其片段或产物(包括例如但不限于细胞内分子、由细胞或微生物分泌的分子、细胞表面分子、细胞外囊泡表面分子或膜结合细胞)。在一些实施方案中,分析物是包含待使用本文所述的技术检测的至少一个靶标的实体(例如,涉及根据本公开的针对相同靶标的至少2个检测探针)。在一些实施方案中,分析物是包含待使用本文所述的技术检测的至少两个靶标或更多个(包括例如至少2个、至少3个、至少4个或更多个靶标)的实体(例如,涉及根据本公开的针对不同靶标的至少2个或更多个检测探针)。在一些实施方案中,分析物可为单个实体或包含两个或更多个分子亚基的复合物,所述两个或更多个分子亚基彼此可共价连接或可不共价连接,和/或其可为相同或不同的。在一些实施方案中,分析物可以是或包含蛋白质复合物。此种复合物可为同源多聚体或异源多聚体。分子的聚集体(例如蛋白质或多肽)或与多肽或蛋白质(例如,调节因子,诸如转录因子)复合或聚集的核酸(例如,dna或rna)也可为靶分析物。
96.抗体剂:如本文所用,术语“抗体剂”是指与特定抗原特异性结合的剂。在一些实施方案中,术语涵盖包括足以赋予特异性结合的免疫球蛋白结构组件的任何多肽或多肽复合物。示例性抗体剂包括但不限于单克隆抗体或多克隆抗体。在一些实施方案中,抗体剂可包括作为小鼠、兔、灵长类动物或人抗体特征的一个或多个恒定区序列。在一些实施方案中,抗体剂可包括如本领域已知的人源化、灵长类化、嵌合等的一个或多个序列组件。在许多实施方案中,术语“抗体剂”用于指用于在替代呈现中利用抗体结构和功能特征的本领域已知或开发的构建体或形式中的一种或多种。例如,实施方案中,根据本发明使用的抗体剂的形式选自但不限于完整的iga、igg、ige或igm抗体;双特异性抗体或多特异性抗体(例如,等);抗体片段,诸如fab片段、fab'片段、f(ab')2片段、fd'片段、fd片段和分离
protocols(methods in molecular biology).michael steinitz.humana press(2013年9月30日))。
98.抗体可通过标准技术产生,例如通过用适当的多肽或其一个或多个部分进行免疫,或通过使用噬菌体展示文库。如果需要多克隆抗体,则用带有一个或多个所需表位的免疫原性多肽对所选哺乳动物(例如,小鼠、兔、山羊、马等)进行免疫,所述免疫原性多肽任选地半抗原化到另一多肽。根据宿主物种,可使用各种佐剂来增加免疫反应。此类佐剂包括但不限于弗氏、矿物凝胶(诸如氢氧化铝)和表面活性物质(诸如溶血卵磷脂、普洛尼克多元醇(pluronic polyol)、聚阴离子、肽、油乳剂、匙孔血蓝蛋白和二硝基苯酚)。收集来自免疫动物的血清,并根据已知程序进行处理。如果含有针对所需表位的多克隆抗体的血清含有针对其他抗原的抗体,则可通过免疫亲和色谱法或本领域已知的任何其他方法来纯化多克隆抗体。用于生产和加工多克隆抗血清的技术是本领域众所周知的。
99.大约或约.如本文所用,当应用于一个或多个关注的值时,术语“大约”或“约”是指与所述参考值相似的值。一般来讲,熟悉上下文的本领域技术人员将理解所述上下文中“约”或“大约”所涵盖的相关差异程度。例如,在一些实施方案中,术语“大约”或“约”可涵盖在参考值的25%、20%、19%、18%、17%、16%、15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%、1%或更小范围内的值范围。
100.适体.如本文所用,术语“适体”通常是指与特定靶分子(例如,表位)结合的核酸分子或肽分子。在一些实施方案中,核酸适体可由核苷酸序列描述,并且长度通常为约15
‑
60个核苷酸。核酸适体可以是或包含单链和/或双链结构。在一些实施方案中,核酸适体可以是或包含dna。在一些实施方案中,核酸适体可以是或包含rna。不希望受任何理论束缚,设想适体中的核苷酸链形成分子内相互作用,所述分子内相互作用将分子折叠成复杂的三维形状,并且此三维形状允许适体与其靶分子的表面紧密结合。在一些实施方案中,肽适体可被描述为具有由蛋白质支架展示的一个或多个可变序列肽环。肽适体可从组合文库中分离出来,并且通常随后通过定向突变或多轮可变区诱变和选择进行改善。鉴于存在于所有可能的核苷酸和/或肽序列的范畴中的分子形状的非凡多样性,可获得用于广泛分子靶标的适体,包括蛋白质和小分子。除了高特异性之外,适体通常对其靶标具有非常高的亲和力(例如,对于蛋白质或多肽的亲和力在皮摩尔至低纳摩尔范围内)。因为适体通常是合成分子,所以适体适于进行各种修饰,这可以优化它们在特定应用中的功能。
101.关联:如果一个事件或实体的存在、水平和/或形式与另一个事件或实体的存在、水平和/或形式相关,则两个事件或实体彼此“关联”,如本文所用的术语。例如,如果特定生物学现象(例如,特定生物标记物的表达)的存在与特定疾病、病症或病状(例如,特定类型的癌症和/或癌症阶段)的发病和/或易患性(例如,在相关人群中)相关,则认为特定生物学现象与所述疾病、病症或病状关联。
102.生物实体:在适当的情况下,如本领域技术人员将从上下文中清楚的那样,术语“生物实体”可用于指存在于例如在一些实施方案中来源于或获自受试者的生物样品中的实体或组分,所述生物样品在一些实施方案中可以是或包含细胞或生物体,诸如动物或人,或在一些实施方案中可以是或包含生物组织或流体。在一些实施方案中,生物实体是或包含细胞或微生物,或其部分、提取物或组分(包括例如,由细胞或微生物分泌的细胞内组分和/或分子)。例如,在一些实施方案中,生物实体是或包含细胞。在一些实施方案中,生物实
体是或包含细胞外囊泡。在一些实施方案中,生物实体是或包含生物分析物(例如,代谢物、碳水化合物、蛋白质或多肽、酶、脂质、细胞器、细胞因子、受体、配体及其任何组合)。在一些实施方案中,存在于样品中的生物实体处于天然状态(例如,蛋白质或多肽保持在天然存在的构象结构中)。在一些实施方案中,例如通过从样品中分离或来源于天然存在的生物实体来处理生物实体。例如,可用一种或多种化学剂处理生物实体,使得利用本文提供的技术进行检测更为理想。仅作为实例,生物实体可为与固定剂(例如但不限于甲醇和/或甲醛)接触以使存在于细胞或细胞外囊泡中的蛋白质和/或肽形成交联的细胞或细胞外囊泡。在一些实施方案中,生物实体呈分离的或纯的形式(例如,从血液或血浆样品中分离)。在一些实施方案中,生物实体可存在于复杂基质(例如,血液或血浆样品)中。
103.生物标记物.术语“生物标记物”通常是指其存在、水平、程度、类型和/或形式与特定的生物事件或关注的状态相关的实体、事件或特征,因此被认为是所述事件或状态的“标记物”。仅举几个实例,在一些实施方案中,生物标记物可以是或包含针对特定疾病状态或针对特定疾病、病症或病状可能发展、发病或复发的可能性的标记物。在一些实施方案中,生物标记物可以是或包含针对特定疾病或治疗结果或其可能性的标记物。在一些实施方案中,生物标记物可以是或包含针对特定组织(例如但不限于脑、乳腺、结肠、卵巢和/或与女性生殖系统相关的其他组织、胰腺、前列腺和/或与男性生殖系统相关的其他组织、肝脏、肺和皮肤)的标记物。在一些实施方案中,针对特定组织的此种标记物可对健康组织具有特异性,对患病组织具有特异性,或在一些实施方案中可存在于正常健康组织和患病组织(例如,肿瘤)中;阅读本公开的本领域技术人员将理解每种此类生物标记物的适当上下文。在一些实施方案中,生物标记物可以是或包含癌症特异性标记物(例如,对特定癌症具有特异性的标记物)。在一些实施方案中,生物标记物可以是或包含非特异性癌症标记物(例如,存在于至少两种或更多种癌症中的标记物)。在一些实施方案中,非特异性癌症标记物可以是或包含针对癌症的通用标记物(例如,通常存在于癌症中的标记物,无论组织类型如何),或在一些实施方案中,针对特定组织(例如但不限于脑、乳腺、结肠、卵巢和/或与女性生殖系统相关的其他组织、胰腺、前列腺和/或与男性生殖系统相关的其他组织、肝脏、肺和皮肤)的癌症的标记物。因此,在一些实施方案中,生物标记物是预测性的;在一些实施方案中,生物标记物是预后的;在一些实施方案中,生物标记物是相关生物事件或关注的状态的诊断物。生物标记物可以是或包含任何化学类别的实体,并且可以是或包含实体的组合。例如,在一些实施方案中,生物标记物可以是或包含核酸、多肽、脂质、碳水化合物、小分子、无机剂(例如,金属或离子)或其组合。在一些实施方案中,生物标记物是或包含特定分子、复合物或结构的一部分;例如,在一些实施方案中,生物标记物可以是或包含表位。在一些实施方案中,生物标记物是生物实体(例如,细胞外囊泡)的表面标记物(例如,表面蛋白标记物)。在一些实施方案中,生物标记物是细胞内标记物。在一些实施方案中,在细胞外检测到生物标记物(例如,在细胞外分泌或以其他方式产生或存在),例如在体液中,诸如血液、血浆、尿液、眼泪、唾液、脑脊液等。在一些实施方案中,生物标记物是囊泡内的(例如,存在于细胞外囊泡中的蛋白质或rna标记物)。在一些实施方案中,生物标记物可以是或包含遗传或表观遗传特征。在一些实施方案中,生物标记物可以是或包含基因表达特征。在一些实施方案中,适合根据本公开使用的“生物标记物”可指存在于靶标记物中的分子实体(例如,表位)的存在、水平和/或形式。例如,在一些实施方案中,作为分子实体(例如,表位)的两个或
更多个“生物标记物”可存在于相同的靶标记物(例如,标记物蛋白,诸如存在于生物实体(例如,细胞外囊泡)中的表面蛋白)上。
104.血液来源的样品:如本文所用,术语“血液来源的样品”是指来源于有需要的受试者的血液样品(即,全血样品)的样品。血液来源的样品的实例包括但不限于血浆(包括例如新鲜冷冻血浆)、血清、血液部分、血浆部分、血清部分、包含红细胞(rbc)、血小板、白细胞等的血液部分,以及包括其部分的细胞裂解物(例如,细胞(诸如红细胞、白细胞等)可被收获并裂解以获得细胞裂解物)。在一些实施方案中,与本文所述的方法、系统和/或试剂盒一起使用的血液来源的样品是血浆样品。
105.癌症.术语“癌症”通常在本文中用于指其中关注的组织的细胞表现出相对异常、不受控制和/或自主生长,使得它们表现出特征为细胞增殖显着失去控制的异常生长表型的疾病或病状。在一些实施方案中,癌症可包含癌前(例如,良性)、恶性、转移前、转移性和/或非转移性细胞。在一个方面,本公开提供了用于检测癌症的技术。在一些实施方案中,癌症可通过实体瘤表征。在一些实施方案中,癌症可通过血液肿瘤表征。一般来讲,本领域已知的不同类型的癌症的实例包括例如造血系统癌症,包括白血病、淋巴瘤(霍奇金氏和非霍奇金氏)、骨髓瘤和骨髓增生性病症;肉瘤、黑色素瘤、腺瘤、实体组织癌、口腔、咽喉、喉和肺的鳞状细胞癌、肝癌、泌尿生殖系统癌症(诸如前列腺癌、宫颈癌、膀胱癌、子宫癌和子宫内膜癌)以及肾细胞癌、骨癌、胰腺癌、皮肤癌、皮肤或眼内黑色素瘤、内分泌系统癌、甲状腺癌、甲状旁腺癌、头颈癌、卵巢癌、乳腺癌、胶质母细胞瘤、结直肠癌、胃肠癌和神经系统癌症、良性病变诸如乳头状瘤等。
106.紧密接近:如本文所用,术语“紧密接近”是指两个检测探针(例如,成对的两个检测探针)之间的距离足够近,使得预期检测探针之间的相互作用(例如,通过各自的寡核苷酸结构域)可能发生。例如,在一些实施方案中,当两个检测探针在特定条件下(例如,当检测探针结合到关注的实体(例如,细胞外囊泡)中的相应靶标时)彼此足够紧密接近时,它们在一段时间内彼此相互作用(例如,通过各自的寡核苷酸结构域)的概率为至少50%或更多,包括例如至少60%、至少70%、至少80%、至少90%或更多。在一些实施方案中,当两个检测探针彼此足够紧密接近时,它们之间的距离可在大约0.1
‑
1000nm、或0.5
‑
500nm、或1
‑
250nm之间的范围内。在一些实施方案中,当两个检测探针彼此足够紧密接近时,它们之间的距离可在大约0.1
‑
10nm之间或大约0.5
‑
5nm之间的范围内。在一些实施方案中,当两个检测探针彼此足够紧密接近时,它们之间的距离可小于100nm或更短,包括例如小于90nm、小于80nm、小于70nm、小于60nm、小于50nm、小于40nm、小于30nm、小于20nm、小于10nm、小于5nm、小于1nm或更短。在一些实施方案中,当两个检测探针彼此足够紧密接近时,它们之间的距离可在大约40
‑
1000nm或40nm
‑
500nm之间的范围内。
107.相当的:如本文所用,术语“相当的”是指两种或更多种剂、实体、情况、条件组等,它们可能彼此不相同,但是足够相似以允许在它们之间进行比较,使得本领域技术人员将理解,可基于观察到的差异或相似性合理地得出结论。在一些实施方案中,相当的条件组、环境、个体或群体的特征在于多个基本相同的特征和一个或少量不同特征。本领域普通技术人员将理解,在上下文中,在任何给定情况下,两种或更多种此类剂、实体、情况、条件组等被认为是相当的需要何种程度的同一性。例如,本领域普通技术人员将理解,当以足够数量和类型的基本相同的特征为特征时,环境、个体或群体组彼此可比,以保证合理结论,即
在不同的环境、个体或群体组的情况下获得的结果或观察到的现象的差异是由那些变化的特征的变化引起或指示的。
108.互补:如本文所用,术语“互补”用于指通过碱基配对规则相关的寡核苷酸杂交。例如,序列“c
‑
a
‑
g
‑
t”与序列“g
‑
t
‑
c
‑
a”互补。互补性可为部分的或全部的。因此,只要部分互补性允许寡核苷酸杂交,任何程度的部分互补性都旨在包括在术语“互补性”的范围内。部分互补性是其中根据碱基配对规则,一个或多个核酸碱基不匹配。核酸之间的全部或完全互补性是其中每个核酸碱基在碱基配对规则下与另一个碱基匹配。
109.疾病:如本文所用,术语“疾病”是指通常损害受试者(例如,人受试者)的组织或系统的正常功能并且通常通过特征性体征和/或症状来表现的病症或病状。根据本公开适合检测的疾病的实例包括但不限于自身免疫性疾病、炎症性疾病、骨疾病、代谢疾病、神经和神经退行性疾病、癌症、心血管疾病、过敏和哮喘、阿尔茨海默氏病和激素相关疾病。
110.检测:术语“检测”在本文中广泛使用以包括在样品与如本文所述和/或使用的检测探针接触之后确定关注的实体的存在或不存在或关注的实体的任何形式的测量(例如,连接模板)的适当方式。因此,“检测”可包括以任何方式确定、测量、评估或分析与靶生物标记物特征的一部分对应的关注的实体(例如,表面蛋白生物标记物和/或囊泡内蛋白生物标记物和/或囊泡内rna生物标记物,和/或指示前述关注的实体的测量形式,例如,指示表面蛋白生物标记物和/或囊泡内蛋白生物标记物的连接模板或指示囊泡内mrna的pcr扩增产物)的存在或不存在、水平、量和/或位置。包括定量和定性确定、测量或评估,包括半定量。此类确定、测量或评估可为相对的,例如当相对于对照参考检测关注的实体(例如,表面蛋白生物标记物和/或囊泡内蛋白生物标记物和/或囊泡内rna生物标记物,和/或指示前述关注的实体的测量形式,例如,指示表面蛋白生物标记物和/或囊泡内蛋白生物标记物的连接模板或指示囊泡内mrna的pcr扩增产物)时;或为绝对的。因此,当在量化关注的实体(例如,表面蛋白生物标记物和/或囊泡内蛋白生物标记物和/或囊泡内rna生物标记物,和/或指示前述关注的实体的测量形式,例如,指示表面蛋白生物标记物和/或囊泡内蛋白生物标记物的连接模板或指示囊泡内mrna的pcr扩增产物)的上下文中使用时,术语“量化”可指绝对量化或相对量化。绝对量化可通过将关注的实体(例如,表面蛋白生物标记物和/或囊泡内蛋白生物标记物和/或囊泡内rna生物标记物,和/或指示前述关注的实体的测量形式,例如,指示表面蛋白生物标记物和/或囊泡内蛋白生物标记物的连接模板或指示囊泡内mrna的pcr扩增产物)的检测水平与已知对照标准相关联(例如,通过生成标准曲线)来完成。替代地,相对量化可通过比较两个或更多个不同的关注的实体(例如,不同的表面蛋白生物标记物、和/或囊泡内蛋白生物标记物、和/或囊泡内rna生物标记物)之间的检测水平或量来完成,以提供两个或更多个不同的关注的实体中的每个的相对量化,即相对于彼此。
111.检测标记:如本文所用,术语“检测标记”是指可检测的任何元素、分子、官能团、化合物、片段或部分。在一些实施方案中,单独地提供或使用检测标记。在一些实施方案中,联合(例如,结合)另一种剂提供和/或使用检测标记。检测标记的实例包括但不限于:各种配体、放射性核素(例如,3h、
14
c、
18
f、
19
f、
32
p、
35
s、
135
i、
125
i、
123
i、
64
cu、
187
re、
111
in、
90
y、
99m
tc、
177
lu、
89
zr等)、荧光染料、化学发光剂(例如像吖啶酯、稳定的二氧杂四环酮等)、生物发光剂、光谱可分辨的无机荧光半导体纳米晶体(即量子点)、金属纳米颗粒(例如,金、银、铜、铂等)纳米簇、顺磁性金属离子、酶、比色标记(例如像染料、胶体金等)、生物素、地高辛
(dioxigenin)、半抗原以及抗血清或单克隆抗体可用的蛋白质。
112.检测探针:术语“检测探针”通常是指针对特异性靶标的检测的探针。根据本公开,检测探针是指包含直接或间接偶联至寡核苷酸结构域的靶结合实体的组合物,其中靶结合实体特异性结合相应的靶标(例如,分子靶标),并且其中寡核苷酸结构域的至少一部分被设计成允许与针对不同靶标的另一检测探针的寡核苷酸结构域的一部分杂交。在许多实施方案中,适合根据本公开使用的寡核苷酸结构域包含双链部分和至少一个单链悬突。在一些实施方案中,寡核苷酸结构域可包含双链部分和位于双链部分的每一端的单链悬突。
113.双链:如本文所用,在寡核苷酸结构域的上下文中,术语“双链”被本领域技术人员理解为以氢键螺旋排列存在的一对寡核苷酸,其通常与例如核酸(诸如dna)相关。除了双链寡核苷酸的100%互补形式之外,如本文所用的术语“双链”还意指包括错配(例如,部分互补性)和/或作为凸起、环或发夹的结构特征的那些形式。
114.双链复合物:如本文所用,术语“双链复合物”通常是指包含至少两个或更多个(包括例如,2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个或更多个)检测探针(例如,如本文提供和/或使用的),每个检测探针针对靶标(其可为相同的靶标或不同的靶标),通过检测探针的互补单链悬突的杂交以线性排列彼此连接或偶联。在一些实施方案中,此种双链复合物可包含生物实体(例如,细胞外囊泡),其中检测探针各自的靶结合部分同时结合到生物实体(例如,细胞外囊泡)。
115.表位:如本文所用,术语“表位”包括由免疫球蛋白(例如,抗体或受体)结合组分或适体特异性识别的任何部分。在一些实施方案中,表位由抗原上的多个化学原子或基团组成。在一些实施方案中,当抗原采用相关三维构象时,此类化学原子或基团暴露于表面。在一些实施方案中,当抗原采用此种构象时,此类化学原子或基团在空间上在物理上彼此接近。在一些实施方案中,当抗原采用替代构象(例如,线性化)时,至少一些此类化学原子或基团在物理上彼此分离。
116.细胞外囊泡:如本文所用,术语“细胞外囊泡”通常是指细胞外的囊泡,例如由细胞分泌的囊泡。分泌囊泡的实例包括但不限于外泌体、微囊泡、微粒、核外粒体、原癌小体和凋亡小体。不希望受理论束缚,外泌体是内吞起源的纳米尺寸囊泡(例如,在40nm和120nm之间),其可通过多囊泡内体(mve)的界膜向内出芽形成,而微囊泡通常从细胞表面出芽,并且它们的大小可在50nm和1000nm之间变化。在一些实施方案中,细胞外囊泡是或包含外泌体和/或微囊泡。在一些实施方案中,包含细胞外囊泡的样品基本上不含凋亡小体。在一些实施方案中,包含细胞外囊泡的样品可包含从一个或多个组织(例如,癌性组织和/或非癌性或健康组织)脱落或衍生的细胞外囊泡。在一些实施方案中,样品中的细胞外囊泡可从与疾病、病症或病状相关的组织脱落或衍生。在一些实施方案中,样品中的细胞外囊泡可从靶癌症的肿瘤脱落或衍生;在一些实施方案中,细胞外囊泡从非靶癌症的肿瘤脱落或衍生。在一些实施方案中,细胞外囊泡从健康组织脱落或衍生。在一些实施方案中,细胞外囊泡从良性肿瘤脱落或衍生。在一些实施方案中,细胞外囊泡从具有与癌症相关的症状(例如,非特异性症状)的受试者的组织脱落或衍生。
117.细胞外囊泡相关膜结合多肽.如本文所用,此种术语是指存在于细胞外囊泡的膜中的多肽。在一些实施方案中,此种多肽可为肿瘤特异性的。在一些实施方案中,此种多肽可为组织特异性的(例如,对靶组织诸如皮肤、肺、胰腺、生殖系统等具有特异性的组织)。在
一些实施方案中,此种多肽可为非特异性的,例如,其存在于一种或多种非靶肿瘤和/或一种或多种非靶组织中。
118.杂交:如本文所用,术语“杂交(hybridizing/hybridize/hybridization)”、“退火(annealing/anneal)”在提及使用核酸链通过碱基配对与互补链结合以形成杂交复合物的任何过程配对互补核酸时可互换使用。杂交和杂交强度(例如,核酸之间的结合强度)受各种因素影响,包括例如核酸之间的互补程度、所涉及条件的严格性、所形成的杂交复合物的解链温度(t)以及核酸内的g:c比率。
119.囊泡内蛋白生物标记物:如本文所用,术语“囊泡内蛋白生物标记物”是指指示存在于生物实体(例如,细胞或细胞外囊泡)内的多肽的状态(例如,存在、水平和/或活性)的标记物。在许多实施方案中,囊泡内蛋白生物标记物与细胞外囊泡相关或存在于细胞外囊泡内。
120.囊泡内rna生物标记物:如本文所用,术语“囊泡内rna生物标记物”是指指示存在于生物实体(例如,细胞或细胞外囊泡)内的rna(例如,mrna)的状态(例如,存在和/或水平)的标记物。在许多实施方案中,囊泡内rna生物标记物与细胞外囊泡相关或存在于细胞外囊泡内。
121.连接酶:如本文所用,术语“连接酶”或“核酸连接酶”是指用于连接核酸的酶。在一些实施方案中,连接酶是用于将多核苷酸的3'端连接到多核苷酸的5'端的酶。在一些实施方案中,连接酶是用于进行粘端连接的酶。在一些实施方案中,连接酶是用于进行平端连接的酶。在一些实施方案中,连接酶是或包含dna连接酶。
122.连接:如本文所用,术语“连接(ligate/ligating/ligation)”是指本领域已知的用于连接两个寡核苷酸或多核苷酸的方法或组合物。连接可以是或包括粘端连接或平端连接。在一些实施方案中,所提供的技术中涉及的连接是或包括粘端连接。在一些实施方案中,连接是指将多核苷酸的3'端连接到多核苷酸的5'端。在一些实施方案中,通过使用核酸连接酶促进连接。
123.非癌症受试者:如本文所用,术语“非癌症受试者”通常是指未患有关注的非良性癌症的受试者。例如,在一些实施方案中,非癌症受试者为健康受试者。在一些实施方案中,非癌症受试者为特定年龄组的健康受试者。在一些实施方案中,非癌症受试者为患有与靶癌症无关的疾病、病症或病状的受试者。在一些实施方案中,非癌症受试者为患有良性肿瘤的受试者。
124.核酸/寡核苷酸:如本文所用,术语“核酸”是指具有至少10个或更多个核苷酸的聚合物。在一些实施方案中,核酸是或包含dna。在一些实施方案中,核酸是或包含rna。在一些实施方案中,核酸是或包含肽核酸(pna)。在一些实施方案中,核酸是或包含单链核酸。在一些实施方案中,核酸是或包含双链核酸。在一些实施方案中,核酸包含单链和双链部分。在一些实施方案中,核酸包含含有一个或多个磷酸二酯键联的主链。在一些实施方案中,核酸包含含有磷酸二酯键联和非磷酸二酯键联的主链。例如,在一些实施方案中,核酸可包含含有一个或多个硫代磷酸酯或5'
‑
n
‑
亚磷酰胺键联和/或一个或多个肽键的主链,例如,如在“肽核酸”中。在一些实施方案中,核酸包含一个或多个或所有天然残基(例如,腺嘌呤、胞嘧啶、脱氧腺苷、脱氧胞苷、脱氧鸟苷、脱氧胸苷、鸟嘌呤、胸腺嘧啶、尿嘧啶)。在一些实施方案中,核酸包含一个或多个或所有非天然残基。在一些实施方案中,非天然残基包含核苷类似
物(例如,2
‑
氨基腺苷、2
‑
硫胸苷、肌苷、吡咯并嘧啶、3
‑
甲基腺苷、5
‑
甲基胞苷、c
‑
5丙炔基
‑
胞苷、c
‑
5丙炔基
‑
尿苷、2
‑
氨基腺苷、c5
‑
溴尿苷、c5
‑
氟尿苷、c5
‑
碘尿苷、c5
‑
丙炔基
‑
尿苷、c5
‑
丙炔基
‑
胞苷、c5
‑
甲基胞苷、2
‑
氨基腺苷、7
‑
脱氮腺苷、7
‑
脱氮杂鸟苷
‑
氧代腺苷、8
‑
氧代腺苷、8
‑
氧代鸟苷、6
‑
o
‑
甲基鸟嘌呤、2
‑
硫胞苷、甲基化碱基、插入的碱基及其组合)。在一些实施方案中,与天然残基中的糖相比,非天然残基包含一种或多种修饰的糖(例如,2'
‑
氟核糖、核糖、2'
‑
脱氧核糖、阿拉伯糖和己糖)。在一些实施方案中,核酸具有编码功能基因产物诸如rna或多肽的核苷酸序列。在一些实施方案中,核酸具有包含一个或多个内含子的核苷酸序列。在一些实施方案中,核酸可通过从天然来源分离、酶促合成(例如,通过基于互补模板的聚合,例如在体内或体外)、在重组细胞或系统中复制或化学合成来制备。在一些实施方案中,核酸为至少3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、1 10、120、130、140、150、160、170、180、190、20、225、250、275、300、325、350、375、400、425、450、475、500、600、700、800、900、1000、1500、2000、2500、3000、3500、4000、4500、5000、5500、6000、6500、7000、7500、8000、8500、9000、9500、10,000、10,500、11,000、11,500、12,000、12,500、13,000、13,500、14,000、14,500、15,000、15,500、16,000、16,500、17,000、17,500、18,000、18,500、19,000、19,500或20,000个或更多个残基或核苷酸长。
125.核苷酸:如本文所用,术语“核苷酸”是指其领域公认的含义。当使用多个核苷酸作为大小的指示时,例如寡核苷酸的大小,一定数量的核苷酸是指例如寡核苷酸的单链上的核苷酸数量。
126.患者:如本文所用,术语“患者”是指患有疾病或病症或病状或处于疾病或病症或病状的风险的任何生物体。典型的患者包括动物(例如,哺乳动物,诸如小鼠、大鼠、兔、非人灵长类动物和/或人)。在一些实施方案中,患者为人。在一些实施方案中,患者患有或易患一种或多种疾病或病症或病状。在一些实施方案中,患者表现出疾病或病症或病状的一种或多种症状。在一些实施方案中,患者已被诊断为患有一种或多种疾病或病症或病状。在一些实施方案中,适用于所提供的技术的疾病或病症或病状是或包括癌症,或一种或多种肿瘤的存在。在一些实施方案中,患者正在接受或已经接受某些疗法以诊断和/或治疗疾病、病症或病状。
127.多肽:如本文所用,术语“多肽”通常具有至少三个或更多个氨基酸的聚合物的领域公认的含义。本领域普通技术人员将理解,术语“多肽”旨在足够通用,以便不仅涵盖具有本文所述的完整序列的多肽,而且还涵盖表示此类完整多肽的功能性、生物活性或特征性片段、部分或结构域(例如,保留至少一种活性的片段、部分或结构域)的多肽。在一些实施方案中,多肽可含有l
‑
氨基酸、d
‑
氨基酸或两者和/或可含有本领域已知的多种氨基酸修饰或类似物中的任一种。有用的修饰包括例如末端乙酰化、酰胺化、甲基化等。在一些实施方案中,多肽可包含天然氨基酸、非天然氨基酸、合成氨基酸及其组合(例如,可以是或包含拟肽)。
128.预防(prevent/prevention):如本文所用,当与疾病、障碍和/或病症的发生相关联时,“预防(prevent/prevention)”是指降低发展疾病、病症和/或病状的风险和/或延迟疾病、病症或病状的一个或多个特征或症状的发作。当疾病、病症或病状的发作已延迟预定时间段时,可认为预防是完全的。
129.引物:如本文所用,术语“引物”是指当置于诱导与核酸链互补的引物延伸产物的
合成的条件下(例如,在核苷酸和诱导剂(诸如dna聚合酶)的存在下以及在合适的温度和ph下)时能够充当合成起始点的寡核苷酸。引物优选为单链以最大化扩增效率。引物必须足够长以在诱导剂的存在下引发延伸产物的合成。引物的确切长度可取决于许多因素,例如温度。
130.参考:如本文所用,“参考”描述了与之进行比较的标准或对照。例如,在一些实施方案中,将关注的剂、动物、个体、群体、样品、序列或值与参考或对照剂、动物、个体、群体、样品、序列或值进行比较。在一些实施方案中,参考或对照与关注的测试或确定基本上同时测试和/或确定。在一些实施方案中,参考或对照是历史参考或对照,任选地体现在有形介质中。在一些实施方案中,在靶标的参考水平的上下文中的参考或对照是指正常健康受试者或正常健康受试者群体中的靶标水平。在一些实施方案中,在靶标的参考水平的上下文中的参考或对照是指治疗前受试者体内的靶标水平。通常,如本领域技术人员所理解的,参考或对照是在与评估中的那些相当的条件或情况下确定或表征的。当存在足够的相似性来证明对特定的可能参考或对照的依赖和/或比较时,本领域技术人员将理解。
131.风险:从上下文中可以理解,疾病、病症和/或病状的“风险”是指特定个体发展疾病、病症和/或病状的可能性。在一些实施方案中,风险表示为百分比。在一些实施方案中,风险为0%、1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、20%、30%、40%、50%、60%、70%、80%、90%至100%。在一些实施方案中,风险表示为相对于与参考样品或参考样品组相关的风险的风险。在一些实施方案中,参考样品或参考样品组具有疾病、病症、病状和/或事件的已知风险。在一些实施方案中,参考样品或参考样品组来自与特定个体相当的个体。在一些实施方案中,相对风险为0、1、2、3、4、5、6、7、8、9、10或更大。
132.样品:如本文所用,术语“样品”通常是指从关注的来源获得或衍生的材料的等分试样。在一些实施方案中,样品是从关注的环境来源(包括例如土壤、水、空气、接触表面等)获得或衍生的。在一些实施方案中,样品是从关注的生物来源(例如,组织或生物体或细胞培养物)获得或衍生的。在一些实施方案中,关注的来源可以是或包括细胞或生物体,诸如动物或人。在一些实施方案中,关注的来源是或包括生物组织或流体。在一些实施方案中,生物组织或流体可以是或包含羊水、房水、腹水、胆汁、骨髓、血液、母乳、脑脊液、耳垢、乳糜、食糜(chime)、精液(ejaculate)、内淋巴、渗出物、粪便、胃酸、胃液、淋巴、粘液、心包液、外淋巴、腹膜液、胸膜液、脓液、泪水、唾液、皮脂、精液(semen)、血清、包皮垢、痰、滑液、汗液、眼泪、尿液、阴道分泌物、玻璃体液、呕吐物和/或其组合或一个或多个组分。在一些实施方案中,生物流体可以是或包含细胞内液、细胞外液、囊内液(血浆)、间质液、淋巴液和/或跨细胞液。在一些实施方案中,生物组织或样品可通过例如抽吸、活检(例如,细针或组织活检)、拭子(例如,口腔、鼻、皮肤或阴道拭子)、刮擦、手术、洗涤或灌洗(例如,支气管肺泡、导管、鼻、眼、口腔、子宫、阴道或其他洗涤或灌洗)获得。在一些实施方案中,生物样品是或包含液体活检。在一些实施方案中,生物样品是或包含从个体获得的细胞。在一些实施方案中,样品是通过任何适当的方式直接从关注的来源获得的“原始样品”。在一些实施方案中,从上下文中将清楚,术语“样品”是指通过处理原始样品(例如,通过去除其中的一种或多种组分和/或通过向其中添加一种或多种剂)获得的制剂。例如,样品是通过使用半透膜或基于亲和力的方法(诸如基于抗体的方法)处理以将关注的生物实体与其他非靶实体分离的制剂。例如,此种“经处理的样品”在一些实施方案中可包含细胞外囊泡,而在一些实施方案
中可包含从样品中提取的核酸和/或蛋白质等。在一些实施方案中,可通过使原始样品经受一种或多种技术(诸如核酸的扩增或逆转录、某些组分的分离和/或纯化等)来获得经处理的样品。
133.选择性或特异性:当在本文中用于提及具有活性的剂时,术语“选择性”或“特异性”将被本领域技术人员理解为意指所述剂区分潜在的靶实体、状态或细胞。例如,在一些实施方案中,如果在存在一个或多个竞争性替代靶标的情况下,剂优先与其靶标结合,则称所述剂“特异性”结合其靶标。在许多实施方案中,特异性相互作用取决于靶实体的特定结构特征(例如,表位、裂口、结合位点)的存在。应当理解,特异性不必是绝对的。在一些实施方案中,可相对于一个或多个其他潜在靶实体(例如,竞争者)的靶结合部分的特异性来评估特异性。在一些实施方案中,相对于参考特异性结合部分的特异性评估特异性。在一些实施方案中,相对于参考非特异性结合部分的特异性评估特异性。在一些实施方案中,靶结合部分在与其靶实体结合的条件下不可检测地结合到竞争性替代靶标。在一些实施方案中,与一个或多个竞争性替代靶标相比,靶结合部分以更高的结合速率、更低的解离速率、增加的亲和力、减少的解离和/或增加的稳定性与其靶实体结合。
134.小分子:如本文所用,术语“小分子”意指低分子量有机和/或无机化合物。一般来讲,“小分子”是大小小于约5千道尔顿(kd)的分子。在一些实施方案中,小分子小于约4kd、3kd、约2kd或约1kd。在一些实施方案中,小分子小于约800道尔顿(d)、约600d、约500d、约400d、约300d、约200d或约100d。在一些实施方案中,小分子小于约2000g/mol、小于约1500g/mol、小于约1000g/mol、小于约800g/mol或小于约500g/mol。在一些实施方案中,小分子不是聚合物。在一些实施方案中,小分子不包括聚合部分。在一些实施方案中,小分子不是蛋白质或多肽(例如,不是寡肽或肽)。在一些实施方案中,小分子不是多核苷酸(例如,不是寡核苷酸)。在一些实施方案中,小分子不是多糖。在一些实施方案中,小分子不包含多糖(例如,不是糖蛋白、蛋白聚糖、糖脂等)。在一些实施方案中,小分子不是脂质。在一些实施方案中,小分子具有生物活性。在一些实施方案中,合适的小分子可通过诸如以下的方法来鉴定:筛选化合物的大文库(beck
‑
sickinger&weber(2001)combinational strategies in biology and chemistry(john wiley&sons,chichester,sussex);通过核磁共振的结构
‑
活性关系(shuker等人(1996)"discovering high
‑
affinity ligands for proteins:sar by nmr.”science 274:1531
‑
1534);编码的自组装化学文库(melkko等人(2004)"encoded self
‑
assembling chemical libraries."nature biotechnol.22:568
‑
574);dna模板化学(gartner等人(2004)"dna
‑
templated organic synthesis and selection of a library of macrocycles.”science 305:1601
‑
1605);动态组合化学(ramstrom&lehn(2002)"drug discovery by dynamic combinatorial libraries."nature rev.drug discov.1:26
‑
36);拴系(arkin&wells(2004)"small
‑
molecule inhibitors of protein
‑
protein interactions:progressing towards the dream.”nature rev.drug discov.3:301
‑
317);以及速度筛选(muckenschnabel等人(2004)"speedscreen:label
‑
free liquid chromatography
‑
mass spectrometry
‑
based high
‑
throughput screening for the discovery of orphan protein ligands."anal.biochem.324:241
‑
249)。在一些实施方案中,小分子可具有纳摩尔范围内的靶标的解离常数。
135.特异性结合:如本文所用,术语“特异性结合”是指在发生结合的环境中区分可能
的结合配偶体的能力。当存在其他潜在靶标时,与一个特定靶标相互作用的靶结合部分被称为“特异性结合”与其相互作用的靶标。在一些实施方案中,通过检测或确定靶结合部分与其配偶体之间的缔合程度来评估特异性结合;在一些实施方案中,通过检测或确定靶结合部分
‑
配偶体复合物的解离程度来评估特异性结合;在一些实施方案中,通过检测或确定靶结合部分竞争其配偶体与另一实体之间的替代相互作用的能力来评估特异性结合。在一些实施方案中,通过在一定浓度范围内进行此类检测或确定来评估特异性结合。
136.癌症阶段:如本文所用,术语“癌症阶段”是指对癌症进展水平的定性或定量评估。在一些实施方案中,用于确定癌症阶段的标准可包括但不限于以下中的一项或多项:癌症在体内的位置、肿瘤大小、癌症是否已扩散至淋巴结、癌症是否已扩散到体内的一个或多个不同部位等。在一些实施方案中,可使用ajcc分阶段系统对癌症进行分阶段。ajcc分阶段系统是由美国癌症联合委员会(american joint committee on cancer)开发的用于描述癌症患者中疾病进展的程度的分类系统,所述系统部分地利用了tnm评分系统:肿瘤大小、受影响的淋巴结、转移。在一些实施方案中,可使用部分涉及tnm评分系统的分类系统对癌症进行分阶段,根据所述系统,t是指主要肿瘤(通常称为原发性肿瘤)的大小和程度;n是指附近有癌症的淋巴结数量;并且m是指癌症是否已转移。在一些实施方案中,癌症可被称为阶段0(存在异常细胞但未扩散到附近组织,也称为原位癌,或cis;cis不是癌症,但它可能变成癌症)、阶段i至阶段iii(存在癌症;数字越大,肿瘤越大,并且扩散到附近组织的程度越高)或阶段iv(癌症已扩散到身体的远处部位)。在一些实施方案中,癌症可被指定为选自由以下组成的组的阶段:原位(存在异常细胞但未扩散到附近组织);局部(癌症仅限于它开始的地方,没有扩散的迹象);区域性(癌症已扩散到附近的淋巴结、组织或器官);远处(癌症已经扩散到身体的远处部位);以及未知(没有足够的信息来确定阶段)。
137.受试者:如本文所用,术语“受试者”是指从其获得样品的生物体,以例如用于实验、诊断、预防和/或治疗目的。典型的受试者包括动物(例如,哺乳动物,诸如小鼠、大鼠、兔、非人灵长类动物、家养宠物等)和人。在一些实施方案中,受试者为人受试者。在一些实施方案中,受试者患有疾病、病症或病状(例如,癌症)。在一些实施方案中,受试者易患疾病、病症或病状(例如,癌症)。在一些实施方案中,受试者表现出疾病、病症或病状(例如,癌症)的一种或多种症状或特征。在一些实施方案中,受试者表现出疾病、病症或病状(例如,癌症)的一种或多种非特异性症状。在一些实施方案中,受试者不表现出疾病、病症或病状(例如,癌症)的任何症状或特征。在一些实施方案中,受试者是具有以疾病、病症或病状(例如,癌症)的易患性或风险为特征的一个或多个特征的人。在一些实施方案中,受试者为患者。在一些实施方案中,受试者为施用和/或已施用诊断和/或治疗的个体。在一些实施方案中,受试者为确定为患有良性肿瘤或肿块的受试者。在一些实施方案中,受试者为无症状受试者。此种有症状受试者可为处于平均群体风险或具有疾病、病症或病状(例如,特定癌症)的遗传风险的受试者。例如,此种无症状受试者可为具有癌症家族史的受试者、先前接受过癌症治疗的受试者、在癌症治疗后有癌症复发风险的受试者、在癌症治疗后有所缓解的受试者和/或先前或定期筛选至少一种癌症生物标记物的存在的受试者。替代地,在一些实施方案中,无症状受试者可为先前未经癌症筛选的受试者、未诊断为癌症的受试者和/或先前未接受癌症治疗的受试者。在一些实施方案中,适用于所提供的技术的受试者是基于诸如以下的一个或多个特征选择的个体:年龄、种族、遗传史、病史、个人史(例如,吸烟、酒精、药
物、致癌剂、饮食、肥胖、身体活动、光暴露、放射暴露、暴露于诸如病毒的感染性因子和/或职业危害)。
138.患有:“患有”疾病、病症和/或病状的个体已被诊断为患有和/或表现出疾病、病症和/或病状的一种或多种症状。
139.表面多肽或表面蛋白:如在本文中可互换使用的,术语“表面多肽”、“表面蛋白”和“膜结合多肽”是指具有存在于生物实体(例如,细胞、细胞外囊泡等)的膜表面中和/或其上的一个或多个结构域或区域的多肽或蛋白质。在一些实施方案中,表面蛋白可包含跨越生物实体(例如,细胞、细胞外囊泡等)的质膜和/或与其相关的一个或多个结构域或区域。在一些实施方案中,表面蛋白可包含跨越生物实体(例如,细胞、细胞外囊泡等)的质膜和/或与其相关并且还从囊泡内和/或囊泡内空间突出的一个或多个结构域或区域。在一些实施方案中,表面蛋白可包含例如通过一个或多个非肽键与生物实体(例如,细胞、细胞外囊泡等)的质膜相关的一个或多个结构域或区域。在一些实施方案中,表面蛋白可包含锚定到生物实体(例如,细胞、细胞外囊泡等)的质膜任一侧的一个或多个结构域或区域。在一些实施方案中,表面蛋白与细胞外囊泡相关或存在于细胞外囊泡内。在一些实施方案中,表面多肽或膜结合多肽可与来自受试者的细胞外囊泡(例如,从患有或易患疾病、病症或病状(例如,癌症)的受试者的血液或血液来源的样品获得或衍生的细胞外囊泡)相关或存在于其内。如本领域技术人员将理解的,检测细胞外囊泡上/内的表面多肽或表面蛋白的至少一部分的存在可促进细胞外囊泡与来自受试者的生物样品(例如,血液或血液来源的样品)的分开和/或分离。在一些实施方案中,检测表面多肽或表面蛋白的存在可以是或包括检测此种表面多肽或表面蛋白的囊泡内部分(例如,囊泡内表位)。在一些实施方案中,检测表面多肽或表面蛋白的存在可以是或包括检测此种表面多肽或表面蛋白的跨膜部分。在一些实施方案中,检测表面多肽或表面蛋白的存在可以是或包括检测此种表面多肽或表面蛋白的囊泡外部分。
140.表面蛋白生物标记物:如本文所用,术语“表面蛋白生物标记物”是指指示生物实体(例如,细胞或细胞外囊泡)的表面蛋白(例如,如本文所述)的状态(例如,存在、水平和/或活性)的标记物。在一些实施方案中,表面蛋白是指具有位于生物实体(例如,细胞或细胞外囊泡)的膜表面内或表面上的一个或多个结构域或区域的多肽或蛋白质。在一些实施方案中,表面蛋白生物标记物可以是或包含存在于膜内侧(囊泡内)或外侧(囊泡外)的表位。在一些实施方案中,表面蛋白生物标记物与细胞外囊泡相关或存在于细胞外囊泡中。
141.易患:“易患”疾病、病症和/或病状的个体是比公众成员有更高风险发展所述疾病、病症和/或病状的人。在一些实施方案中,易患疾病、病症和/或病状的个体可能未被诊断为患有所述疾病、病症和/或病状。在一些实施方案中,易患疾病、病症和/或病状的个体可表现出所述疾病、病症和/或病状的症状。在一些实施方案中,易患疾病、病症和/或病状的个体可不表现出所述疾病、病症和/或病状的症状。在一些实施方案中,易患疾病、病症和/或病状的个体将发展所述疾病、病症和/或病状。在一些实施方案中,易患疾病、病症和/或病状的个体不会发展所述疾病、病症和/或病状。
142.靶结合部分:一般来讲,术语“靶结合部分”和“结合部分”在本文中可互换使用以指结合关注的靶标(例如,关注的分子靶标,诸如生物标记物或表位)的任何实体或部分。在许多实施方案中,关注的靶结合部分是与其靶标(例如,靶生物标记物)特异性结合的部分,
因为它将其靶标与特定相互作用环境中的其他潜在结合配偶体区分开来。一般来讲,靶结合部分可以是或包含任何化学类别的实体或部分(例如,聚合物、非聚合物、小分子、多肽、碳水化合物、脂质、核酸等)。在一些实施方案中,靶结合部分是单个化学实体。在一些实施方案中,靶结合部分是在相关条件下通过非共价相互作用彼此缔合的两个或更多个离散化学实体的复合物。例如,本领域技术人员将理解,在一些实施方案中,靶结合部分可包含“通用”结合部分(例如,生物素/抗生物素蛋白/链霉抗生物素和/或类别特异性抗体中的一种)和与通用结合部分的配偶体连接的“特异性”结合部分(例如,具有特定分子靶标的抗体或适体)。在一些实施方案中,此种方法可允许通过不同特异性结合部分与通用结合部分配偶体的连接来模块化组装多个靶结合部分。
143.靶生物标记物特征:如本文所用,术语“靶生物标记物特征”是指(例如,至少2个或更多个,包括例如至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个、至少11个、至少12个、至少13个、至少14个、至少15个、至少16个、至少17个、至少18个、至少19个、至少20个、至少25个、至少30个或更多个)生物标记物的组合,所述组合与特定生物事件或关注的状态相关,使得本领域技术人员将理解,其可适当地被认为是所述事件或状态的“特征”。仅举几个实例,在一些实施方案中,靶生物标记物特征可与特定疾病或疾病状态相关,和/或与特定疾病、病症或病状可能发展、发生或复发的可能性相关。在一些实施方案中,靶生物标记物特征可与特定疾病或治疗结果或其可能性相关。在一些实施方案中,靶生物标记物特征可与特定癌症和/或其阶段和/或其亚型相关。在一些实施方案中,靶生物标记物特征包含(例如,至少2个或更多个,包括例如至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个、至少11个、至少12个、至少13个、至少14个、至少15个、至少16个、至少17个、至少18个、至少19个、至少20个、至少25个、至少30个或更多个)生物标记物的组合,它们一起对特定癌症或其亚型和/或其疾病阶段具有特异性,尽管此种组合中的一个或多个生物标记物可针对对癌症不具有特异性的靶标(例如,表面蛋白生物标记物、囊泡内蛋白生物标记物和/或囊泡内rna)。在一些实施方案中,构成靶生物标记物特征的生物标记物的组合可通过检测探针的多个(例如,至少两个或更多个)成对或正交组合来检测,其中每对检测探针可针对至少一个不同的靶标。在一些实施方案中,构成靶生物标记物特征的生物标记物的组合可通过一组检测探针检测,每个检测探针被设计成彼此杂交以形成线性复合物(参见例如,如图5a
‑
5b和图10中所示)。例如,在一些实施方案中,靶生物标记物特征可包含对特定癌症或其阶段和/或亚型具有特异性的至少一种生物标记物(即,癌症特异性靶标),并且还可包含不一定或完全对癌症具有特异性的生物标记物(例如,也可在一些或所有生物实体(例如像细胞、细胞外囊泡等)上发现,所述生物实体不是癌性的、不是相关癌症的和/或不属于关注的特定阶段和/或亚型)。也就是说,如阅读本说明书的本领域技术人员将理解的,只要在靶生物标记物特征中使用的生物标记物的组合是或包含多个生物标记物,所述生物标记物一起对关注的相关靶生物实体(例如,关注的癌细胞或癌细胞分泌的细胞外囊泡)具有特异性(即,充分区分用于检测的相关靶生物实体(例如,关注的癌细胞或癌细胞分泌的细胞外囊泡)与用于检测的其他不受关注的生物实体),根据本公开的某些实施方案,生物标记物的此种组合是有用的靶生物标记物特征。
144.治疗剂:如在本文中可互换使用的,短语“治疗剂”或“疗法”是指当施用于受试者或患者时具有治疗效果和/或引发所需生物学和/或药理学的剂或干预。在一些实施方案
中,治疗剂或疗法是可用于减轻、改善、缓解、抑制、预防、延迟疾病、病症和/或病状的一种或多种症状或特征的发作、降低其严重性和/或降低其发病的任何物质。在一些实施方案中,治疗剂或疗法是可执行以减轻、缓解、抑制、呈现、延迟疾病、病症和/或病状的一种或多种症状或特征的发作、降低其严重性和/或降低其发病的医学干预(例如,手术、放射、光照疗法)。
145.阈值水平(例如,截止值):如本文所用,术语“阈值水平”是指用作获得关于测量结果(例如,在测定中获得的测量结果)的信息和/或对其进行分类的参考的水平。例如,在一些实施方案中,阈值水平(例如,截止值)意指在定义群体的两个子集(例如,正常和/或非癌症与关注的癌症)之间的分界线的测定中测量的值。因此,等于或高于阈值水平的值定义了群体的一个子集,并且低于阈值水平的值定义了群体的另一个子集。阈值水平可基于一个或多个对照样品或跨越对照样品群体来确定。可在进行关注的测量之前、同时或之后确定阈值水平。在一些实施方案中,阈值水平可为值的范围。
146.治疗:如本文所用,术语“治疗(treat、treatment或treating)”是指用于部分或完全减轻、改善、缓解、抑制、预防、延迟疾病、病症和/或病状的一种或多种症状或特征的发作、降低其严重程度和/或降低其发病。可向未表现出疾病、病症和/或病状迹象的受试者施用治疗。在一些实施方案中,可向仅表现出疾病、病症和/或病状的早期迹象的受试者施用治疗,例如为了降低发展与疾病、病症和/或病状相关的病理的风险的目的。在一些实施方案中,可向处于疾病、病症和/或病状的晚期阶段的受试者施用治疗。
147.标准技术可用于重组dna、寡核苷酸合成以及组织培养和转化(例如,电穿孔、脂质转染)。酶促反应和纯化技术可根据制造商的说明书或如本领域中通常完成的或如本文所述来进行。前述技术和程序通常可根据本领域众所周知的常规方法进行,并且如在本说明书通篇引用和讨论的各种一般性和更具体的参考文献中所述。参见例如,sambrook等人,molecular cloning:a laboratory manual(2d ed.,cold spring harbor laboratory press,cold spring harbor,n.y.(1989)),其出于任何目的以引用的方式并入本文。
具体实施方式
148.本公开尤其提供了与基于关注的个体实体(例如,生物实体)上或其中的分子或表位的相互作用和/或共定位的靶实体检测方法有关的技术。此类技术可用于检测用于不同应用和/或目的的各种类型样品中的关注的实体。例如,本公开尤其提供了用于实现疾病或病症(例如,癌症)的有效筛选的见解和技术。在一些实施方案中,所提供的技术对于早期癌症的检测是有效的。在一些实施方案中,本公开提供了用于筛选处于早期癌症的遗传和平均风险的受试者的技术。在一些实施方案中,所提供的技术即使在应用于包含无症状或有症状个体或由所述个体组成的人群时也是有效的(例如,由于足够高的灵敏度和/或低的假阳性和/或假阴性结果率)。在一些实施方案中,所提供的技术在应用于包含没有发展癌症的遗传风险的个体(例如,无症状或有症状个体)或由所述个体组成的人群时是有效的。在一些实施方案中,所提供的技术在应用于包含具有发展癌症的遗传风险的个体(例如,无症状或有症状个体)或由所述个体组成的人群时是有效的。在一些实施方案中,所提供的技术在应用于包含易患癌症的个体(例如,具有已知遗传、环境或经验风险等的个体)或由所述个体组成的人群时是有效的。在一些实施方案中,所提供的技术可以是或包括一种或多种
组合物(例如,分子实体或复合物、系统、细胞、集合、组合、试剂盒等)和/或方法(例如,制造、使用、评估等方法),如对于阅读本文提供的公开的本领域技术人员来说将是清楚的。
149.在一些实施方案中,所提供的技术提供了优于某些现有技术(包括例如癌症检测和诊断的某些常规方法)的技术优点。例如,本公开认识到许多常规诊断测定(例如,基于无细胞核酸、循环肿瘤细胞、蛋白质、血清蛋白质和/或细胞外囊泡的批量分析)可能是耗时的、昂贵的和/或缺乏足以提供可靠且全面的诊断评估的灵敏度和/或特异性。具体地,本公开尤其认识到,基于批量样品而不是以单个生物实体的分辨率对生物实体(例如,细胞外囊泡)中的单个癌症相关生物标记物或多个癌症相关生物标记物进行检测通常在确定从其获得生物实体的受试者是否可能患有或易患癌症方面不提供足够的特异性和/或灵敏度。本公开尤其提供了解决此类问题的技术,包括系统、组合物和方法,包括例如通过具体要求用于检测的个体实体以存在靶标(例如,分子靶标)的组合为特征。在特定实施方案中,本公开教导要求此类个体实体以存在(例如,通过表达)癌症特异性分子靶标(即,相关癌症的“靶生物标记物特征”)的组合(例如,一组)为特征的技术,而不包含靶向组合的生物实体不会产生可检测的信号。
150.在一些实施方案中,本公开尤其提供了以下见解:对无症状个体进行筛选(例如,在出现症状之前或以其他方式在没有出现症状的情况下进行定期筛选)可能是有益的,并且甚至对于癌症的有效管理(例如,成功治疗)是重要的。替代地或另外,在一些实施方案中,本公开还提供了以下见解:针对不同类型的癌症(例如,针对多种不同癌症)进行筛选(例如,定期筛选)可能是有益的,并且甚至对于癌症的有效管理(例如,成功治疗)是重要的。在一些实施方案中,本公开提供了癌症筛选系统,在一些实施方案中,所述癌症筛选系统可被实施以例如检测无症状个体(例如,没有癌症遗传风险)中的癌症,包括早期癌症。在一些实施方案中,所提供的技术被实施以实现对无症状个体(例如,有或没有癌症遗传风险)和/或针对多种癌症的定期筛选。在一些实施方案中,所提供的技术被实施以实现对有症状个体(例如,有或没有癌症遗传风险)的定期筛选。在一些实施方案中,所提供的技术实现对癌症(例如,特定癌症和/或多种癌症)的一个或多个特征(例如,发病、进展、对治疗的反应性、复发等)的检测(例如,例如在一个或多个无症状个体和/或一个或多个人群中的早期检测),其中灵敏度和/或特异性(例如,假阳性和/或假阴性结果的比率)适用于允许将所提供的技术有用地应用于单次和/或定期(例如,周期性)评估。在一些实施方案中,所提供的技术可用于与个体的周期性体检结合。在一些实施方案中,所提供的技术可用于与一种或多种治疗方案结合;在一些实施方案中,所提供的技术可改善这样的一种或多种治疗方案的一个或多个特征(例如,根据接受的参数的成功率)。本公开提供了例如组合物(例如,试剂、试剂盒、组分等)以及提供和/或使用它们的方法,包括涉及对一个或多个个体(例如,患有或易患疾病或病症诸如癌症的一个或多个无症状个体)进行测试(例如,定期测试)的策略。本公开定义了此类系统的有用性,并提供了用于实现它们的组合物和方法。
151.i.所提供的靶实体检测系统
152.本公开提供了用于在一些实施方案中,在单个实体水平上检测样品(例如,生物、环境或其他样品)中包含至少两个或更多个靶标(例如,分子靶标)的关注的实体(例如,关注的生物或化学实体,诸如细胞外囊泡或分析物)的靶实体检测系统。阅读本公开的本领域技术人员将认识到,所提供的靶实体检测系统可用于多种应用和/或目的。例如,在一些实
施方案中,所提供的靶实体检测系统可用于医学应用和/或目的。在一些实施方案中,所提供的靶实体检测系统可用于筛选(例如,定期筛选)个体(例如,无症状个体)的疾病或病状(例如,癌症)。在一些实施方案中,所提供的靶实体检测系统可用于筛选(例如,定期筛选)个体(例如,无症状个体)的不同类型的癌症(例如,多种不同的癌症)。在一些实施方案中,所提供的靶实体检测系统即使在应用于包含无症状个体或由无症状个体组成的人群时也是有效的(例如,由于足够高的灵敏度和/或低的假阳性和/或假阴性结果率)。在一些实施方案中,所提供的靶实体检测系统可用作与疾病治疗结合的伴随诊断。
153.在一些实施方案中,靶实体检测系统包括多个检测探针,每个检测探针针对特定靶标(例如,分子靶标或靶生物标记物特征的生物标记物)。在一些实施方案中,此种系统可包含至少2个、至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个、至少15个、至少20个、至少25个、至少30个、至少40个、至少50个或更多个检测探针,每个检测探针针对特定靶标(例如,分子靶标或靶生物标记物特征的生物标记物)。在一些实施方案中,此种系统可包含2
‑
50个检测探针,每个检测探针针对特定靶标(例如,分子靶标或靶生物标记物特征的生物标记物)。在一些实施方案中,此种系统可包含2
‑
30个检测探针,每个检测探针针对特定靶标(例如,分子靶标或靶生物标记物特征的生物标记物)。在一些实施方案中,此种系统可包含2
‑
25个检测探针,每个检测探针针对特定靶标(例如,分子靶标或靶生物标记物特征的生物标记物)。在一些实施方案中,此种系统可包含5
‑
30个检测探针,每个检测探针针对特定靶标(例如,分子靶标或靶生物标记物特征的生物标记物)。在一些实施方案中,此种系统可包含5
‑
25个检测探针,每个检测探针针对特定靶标(例如,分子靶标或靶生物标记物特征的生物标记物)。在一些实施方案中,一组此类检测探针中的至少两个可针对相同的靶标(例如,相同的分子靶标或靶生物标记物特征的相同的生物标记物)。在一些实施方案中,一组此类检测探针中的至少两个可针对相同靶标(例如,相同的分子靶标或靶生物标记物特征的相同的生物标记物)的相同表位。在一些实施方案中,一组此类检测探针中的至少两个可针对相同靶标(例如,相同的分子靶标或靶生物标记物特征的相同的生物标记物)的不同表位。
154.在一些实施方案中,适合在本文提供的靶实体检测系统中使用的检测探针可用于检测单个疾病或病状,例如特定癌症。在一些实施方案中,适合在本文提供的靶实体检测系统中使用的检测探针可允许检测至少两种或更多种疾病或病状,例如不同类型的癌症(例如,皮肤癌与卵巢癌)或特定癌症的不同亚型;和/或特定癌症的不同阶段。在一些实施方案中,适合在本文提供的靶实体检测系统中使用的检测探针可允许检测某些亚型的特定癌症。仅以举例的方式,在用于卵巢癌检测的一些实施方案中,适合在靶实体检测系统中使用的检测探针可允许检测一种或多种卵巢癌亚型,包括例如但不限于高级别浆液性卵巢癌、子宫内膜样卵巢癌、透明细胞卵巢癌、低级别浆液性卵巢癌和/或粘液性卵巢癌。在一些实施方案中,适合在本文提供的靶实体检测系统中使用的检测探针可允许检测某些阶段(包括例如阶段i、阶段ii、阶段iii和/或阶段iv)的特定癌症。因此,在一些实施方案中,适合在本文提供的靶实体检测系统中使用的检测探针可包含多个(例如,至少2个、至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个或更多个)组的检测探针,其中每组针对不同疾病或不同类型的疾病或病状的检测。例如,在一些实施方案中,适合在本文提供的靶实体检测系统中使用的检测探针可包含多个(例如,至少2个、至少3个、至少4个、
至少5个、至少6个、至少7个、至少8个、至少9个、至少10个或更多个)组的检测探针,其中在一些实施方案中,每组针对不同类型的癌症的检测,或在一些实施方案中,每组针对不同亚型和/或阶段的相同癌症的检测。
155.检测探针
156.在一些实施方案中,如本文所提供和/或使用的检测探针包含靶结合部分和偶联至靶结合部分的寡核苷酸结构域。在一些实施方案中,偶联至靶结合部分的寡核苷酸结构域可包含双链部分和从寡核苷酸结构域的至少一端延伸的单链悬突。在一些实施方案中,偶联至靶结合部分的寡核苷酸结构域可包含双链部分和从寡核苷酸结构域的每一端延伸的单链悬突。
157.a.靶结合部分
158.偶联至寡核苷酸结构域的靶结合部分是特异性结合靶标(例如,分子靶标或疾病、病症或病状(例如,癌症)的靶生物标记物特征的生物标记物)的实体或剂。在一些实施方案中,靶结合部分可具有至少约10
‑4m、至少约10
‑5m、至少约10
‑6m、至少约10
‑7m、至少约10
‑8m、至少约10
‑9m或更低的对靶标(例如,分子靶标)的结合亲和力(例如,如通过解离常数测量的)。本领域技术人员将理解,在一些情况下,结合亲和力(例如,如通过解离常数测量的)可受两个分子之间的非共价分子间相互作用(诸如氢键、静电相互作用、疏水性和范德华力)的影响。替代地或另外,配体与其靶分子之间的结合亲和力可受其他分子的存在的影响。本领域技术人员将熟悉用于根据本公开测量结合亲和力和/或解离常数的多种技术,包括例如但不限于elisa、凝胶迁移测定、下拉测定、平衡透析、分析超速离心、表面等离子体共振(spr)、生物层干涉测量、光栅耦合干涉技术和光谱测定。
159.在一些实施方案中,靶结合部分可以是或包含任何化学类别(例如像碳水化合物、核酸、脂质、金属、多肽、小分子等和/或其组合)的剂。在一些实施方案中,靶结合部分可以是或包含抗体剂和/或适体。在一些实施方案中,靶结合部分是或包含抗体剂,例如,特异性结合靶标或其表位(例如,疾病、病症或病状(例如,癌症)的靶生物标记物特征的生物标记物或其表位)的抗体剂。在一些实施方案中,靶结合部分是或包含适体,例如,特异性结合靶标或其表位(例如,疾病、病症或病状(例如,癌症)的靶生物标记物特征的生物标记物或其表位)的适体。在一些实施方案中,靶标可以是或包含与癌症相关的靶标。例如,在一些此类实施方案中,癌症相关靶标可以是或包含与多于一种癌症(即,至少两种或更多种癌症)相关的靶标。在一些实施方案中,癌症相关靶标可以是或包含通常与癌症相关的靶标。在一些实施方案中,癌症相关靶标可以是或包含与特定组织的癌症相关的靶标。在一些实施方案中,癌症相关靶标可以是或包含对特定癌症具有特异性的靶标。
160.在一些实施方案中,靶结合部分识别并特异性结合存在于生物实体(包括例如但不限于细胞和/或细胞外囊泡)中的靶标。例如,在一些实施方案中,靶结合部分可识别肿瘤相关抗原或其表位。在一些实施方案中,肿瘤相关抗原可以是或包含与癌症相关的抗原,所述癌症例如像急性淋巴细胞性白血病、急性髓系白血病、胆管癌、膀胱癌、脑癌(包括例如胶质母细胞瘤)、乳腺癌、宫颈癌、慢性淋巴细胞性白血病、慢性髓系白血病、结直肠癌、子宫内膜癌、食道癌、胃肠癌、霍奇金淋巴瘤、肾癌、肝癌、肺癌、多发性骨髓瘤、非霍奇金淋巴瘤、卵巢癌、胰腺癌、前列腺癌、肉瘤、皮肤癌和胃癌。在一些实施方案中,靶结合部分可识别并特异性结合与皮肤癌(例如,黑色素瘤)相关的肿瘤抗原。在一些实施方案中,靶结合部分可识
别与肺癌(例如,非小细胞肺癌)相关的肿瘤抗原。在一些实施方案中,靶结合部分可识别与乳腺癌相关的肿瘤抗原。在一些实施方案中,靶结合部分可识别与卵巢癌(例如,上皮来源的卵巢癌,诸如高级别浆液性卵巢癌)相关的肿瘤抗原。
161.在一些实施方案中,靶结合部分可特异性结合细胞内靶标。在一些实施方案中,靶结合部分可特异性结合囊泡内靶标,例如囊泡内蛋白质或rna(例如,mrna)。
162.在一些实施方案中,靶结合部分可特异性结合表面靶标。例如,在一些实施方案中,靶结合部分可特异性结合存在于细胞表面上/内的表面靶标。在一些实施方案中,靶结合部分可特异性结合存在于细胞外囊泡上/内的表面靶标,例如,存在于与疾病、病症或病状(例如,癌症)相关的细胞外囊泡上/内的膜结合多肽。
163.在一些实施方案中,靶结合部分针对特定病状或疾病(例如,癌症)的生物标记物,所述生物标记物通过或已通过例如分析患者活检和/或患者数据的群体或文库(例如,数十个、数百个、数千个、数万个、数十万个或更多个)鉴定此种生物标记物(例如,预测性生物标记物)来确定。
164.在一些实施方案中,相关生物标记物可为例如通过数据分析鉴定和/或表征的生物标记物。在一些实施方案中,例如,可通过机器学习和/或计算建模来分析一组不同的数据(例如,在一些实施方案中,包括批量rna测序、单细胞rna(scrna)测序、质谱、组织学、翻译后修饰数据、体外和/或体内实验数据中的一个或多个)进行分析,以鉴定对疾病或病状(例如,癌症)具有高度特异性的生物标记物(例如,预测标记物)。
165.在一些实施方案中,靶结合部分针对组织特异性靶标,例如与特定组织相关的靶标,所述组织例如像脑、乳腺、结肠、卵巢和/或与女性生殖系统相关的其他组织、胰腺、前列腺和/或与男性生殖系统相关的其他组织、肝脏、肺和皮肤。在一些实施方案中,此种组织特异性靶标可与正常健康组织和/或患病组织(诸如肿瘤)相关。在一些实施方案中,靶结合部分针对与受试者的正常健康状况特异性相关的靶标。
166.在一些实施方案中,在多个检测探针(例如,如本文所述和/或使用的)中使用的个体靶结合部分针对不同的靶标。在一些实施方案中,此类不同的靶标可代表不同的标记物蛋白或多肽。在一些实施方案中,此类不同的靶标可代表相同标记物蛋白或多肽的不同表位。在一些实施方案中,在多个检测探针(例如,如本文所述和/或使用的)中使用的两个或更多个个体靶结合部分可针对相同的靶标。
167.在一些实施方案中,在用于检测疾病、病症或病状(例如,癌症)的多个检测探针中使用的个体靶结合部分可针对特定疾病、病症或病状(例如,特定癌症)的靶生物标记物特征的不同靶生物标记物。在一些实施方案中,在用于检测疾病、病症或病状(例如,癌症)的多个检测探针中使用的个体靶结合部分可针对特定疾病、病症或病状(例如,特定癌症)的靶生物标记物特征的相同靶生物标记物。在一些实施方案中,此类靶结合部分可针对特定疾病、病症或病状(例如,特定癌症)的此种靶生物标记物特征的相同靶生物标记物的相同或不同表位。
168.b.寡核苷酸结构域
169.在一些实施方案中,根据本公开使用的寡核苷酸结构域(例如,其可与靶结合部分偶联)可包含双链部分和从寡核苷酸结构域的一端或两端延伸的单链悬突。在寡核苷酸结构域包含从每一端延伸的单链悬突的一些实施方案中,单链悬突从双链部分的不同链延
伸。在寡核苷酸结构域包含从寡核苷酸结构域的一端延伸的单链悬突的一些实施方案中,寡核苷酸结构域的另一端可为平端。
170.在涉及寡核苷酸结构域的一些实施方案中,双链部分的至少一条链包含用于扩增的引物位点。在一些此类实施方案中,此种引物位点可位于双链部分的末端部分。
171.在一些实施方案中,寡核苷酸结构域可包含核糖核苷酸、脱氧核糖核苷酸、能够参与沃森
‑
克里克(watson
‑
crick)类型或类似碱基对相互作用的合成核苷酸残基及其任何组合。在一些实施方案中,寡核苷酸结构域是或包含dna。在一些实施方案中,寡核苷酸结构域是或包含肽核酸(pna)。
172.在一些实施方案中,寡核苷酸的长度可至少部分地例如通过例如待检测的关注的实体(例如生物实体,诸如细胞外囊泡)的物理特征和/或在待检测的关注的实体(例如,生物实体,诸如细胞外囊泡)中分子靶标的选择和定位来确定。在一些实施方案中,检测探针的寡核苷酸结构域被配置成具有这样的长度,使得当第一检测探针和第二检测探针结合到关注的实体(例如,生物实体,诸如细胞外囊泡)时,第一单链悬突和第二单链悬突足够紧密接近以允许单链悬突之间的相互作用(例如,杂交)。例如,当关注的实体(例如,生物实体)是细胞外囊泡(例如,外泌体)时,检测探针的寡核苷酸结构域可各自独立地具有这样的长度,使得当相应的检测探针结合到同一细胞外囊泡时,它们各自的单链悬突足够紧密接近以彼此退火或相互作用。例如,在一些实施方案中,用于检测细胞外囊泡(例如,外泌体)的检测探针的寡核苷酸结构域可各自独立地具有约20nm至约200nm、约40nm至约500nm、约40nm至约300nm或约50nm至约150nm的长度。在一些实施方案中,用于检测细胞外囊泡(例如,外泌体)的检测探针的寡核苷酸结构域可各自独立地具有约20nm至约200nm的长度。在一些实施方案中,一组检测探针的寡核苷酸结构域的长度可各自独立地变化,以增加和/或最大化在它们同时结合到相同的关注的实体时它们相互发现的概率。
173.因此,在一些实施方案中,用于本文提供的技术的寡核苷酸结构域的长度可在约30个至约1000个核苷酸的范围内。在一些实施方案中,寡核苷酸结构域的长度可在约30个至约500个核苷酸、约30个至约250个核苷酸、约30个至约200个核苷酸、约30个至约150个核苷酸、约40个至约150个核苷酸、约40个至约125个核苷酸、约40个至约100个核苷酸、约50个至约90个核苷酸、约50个至约80个核苷酸的范围内。在一些实施方案中,寡核苷酸结构域的长度可为至少30个或更多个核苷酸,包括例如至少40个、至少50个、至少60个、至少70个、至少80个、至少90个、至少100个、至少250个、至少500个、至少750个、至少1000个核苷酸或更多。在一些实施方案中,寡核苷酸结构域的长度可为不超过1000个核苷酸或更少,包括例如不超过900个、不超过800个、不超过700个、不超过600个、不超过500个、不超过400个、不超过300个、不超过200个、不超过100个、不超过90个、不超过80个、不超过70个、不超过60个、不超过50个、不超过40个核苷酸或更少。在一些实施方案中,寡核苷酸结构域的长度可在约50个核苷酸至约90个核苷酸的范围内。在一些实施方案中,寡核苷酸结构域的长度可在约30个核苷酸至约50个核苷酸的范围内。在一些实施方案中,寡核苷酸结构域的长度可在约10个核苷酸至约30个核苷酸的范围内。
174.在一些实施方案中,寡核苷酸结构域的长度可为约20nm至约500nm。在一些实施方案中,寡核苷酸结构域的长度可为约20nm至约400nm、约30nm至约200nm、约50nm至约100nm、约30nm至约70nm或约40nm至约60nm。在一些实施方案中,寡核苷酸结构域的长度可为至少
约20nm或更长,包括例如至少约30nm、至少约40nm、至少约50nm、至少约60nm、至少约70nm、至少约80nm、至少约90nm、至少约100nm、至少约200nm、至少约300nm、至少约400nm或更长。在一些实施方案中,寡核苷酸结构域的长度可为不超过1000nm或更短,包括例如不超过900nm、不超过800nm、不超过700nm、不超过600nm、不超过500nm、不超过400nm、不超过300nm、不超过200nm、不超过100nm或更短。
175.在一些实施方案中,用于本文提供的技术的寡核苷酸结构域的双链部分的长度可在约30个至约1000个核苷酸的范围内。在一些实施方案中,寡核苷酸结构域的双链部分的长度可在约30个至约500个核苷酸、约30个至约250个核苷酸、约30个至约200个核苷酸、约30个至约150个核苷酸、约40个至约150个核苷酸、约40个至约125个核苷酸、约40个至约100个核苷酸、约50个至约90个核苷酸、约50个至约80个核苷酸的范围内。在一些实施方案中,寡核苷酸结构域的双链部分的长度可为至少30个或更多个核苷酸,包括例如至少40个、至少50个、至少60个、至少70个、至少80个、至少90个、至少100个、至少250个、至少500个、至少750个、至少1000个核苷酸或更多。在一些实施方案中,寡核苷酸结构域的双链部分的长度可为不超过1000个核苷酸或更少,包括例如不超过900个、不超过800个、不超过700个、不超过600个、不超过500个、不超过400个、不超过300个、不超过200个、不超过100个、不超过90个、不超过80个、不超过70个、不超过60个、不超过50个、不超过40个核苷酸或更少。在一些实施方案中,寡核苷酸结构域的双链部分的长度可在约50个核苷酸至约90个核苷酸的范围内。在一些实施方案中,寡核苷酸结构域的双链部分的长度可在约30个核苷酸至约50个核苷酸的范围内。在一些实施方案中,寡核苷酸结构域的双链部分的长度可在约10个核苷酸至约30个核苷酸的范围内。
176.在一些实施方案中,寡核苷酸结构域的双链部分的长度可为约20nm至约500nm。在一些实施方案中,寡核苷酸结构域的双链部分的长度可为约20nm至约400nm、约30nm至约200nm、约50nm至约100nm、约30nm至约70nm或约40nm至约60nm。在一些实施方案中,寡核苷酸结构域的双链部分的长度可为至少约20nm或更长,包括例如至少约30nm、至少约40nm、至少约50nm、至少约60nm、至少约70nm、至少约80nm、至少约90nm、至少约100nm、至少约200nm、至少约300nm、至少约400nm或更长。在一些实施方案中,寡核苷酸结构域的双链部分的长度可为不超过1000nm或更短,包括例如不超过900nm、不超过800nm、不超过700nm、不超过600nm、不超过500nm、不超过400nm、不超过300nm、不超过200nm、不超过100nm或更短。
177.在一些实施方案中,寡核苷酸结构域的双链部分的特征在于,当检测探针通过各自的互补单链悬突(例如,如本文所述和/或使用的)的杂交而彼此连接时,相应寡核苷酸结构域(如果有的话,包括将靶结合部分连接到寡核苷酸结构域的接头)的组合长度足够长,以允许各自的靶结合实体基本上跨越关注的实体(例如,细胞外囊泡)的全部特征长度(例如,直径)。例如,在细胞外囊泡是关注的实体的一些实施方案中,当检测探针彼此完全连接时,检测探针的寡核苷酸结构域(如果有的话,包括将靶结合部分连接到寡核苷酸结构域的接头)的组合长度可为大约50nm至200nm。
178.在一些实施方案中,寡核苷酸结构域的双链部分可包含引物的结合位点。在一些实施方案中,引物的此种结合位点可包含被设计成降低或最小化错误引发或引物二聚体的可能性的核苷酸序列。在一些实施方案中,此种特征可降低检测下限,并因此增加本文提供的系统的灵敏度。在一些实施方案中,引物的结合位点可包含被设计成具有与另一引物结
合位点相似的退火温度的核苷酸序列。
179.在一些实施方案中,寡核苷酸结构域的双链部分可包含被设计成减少或最小化与通常与受试者(例如,人受试者)的基因组和/或基因转录物(例如,基因组dna和/或rna,诸如基因的mrna)相关的核酸序列(例如,dna和/或rna序列)的重叠的核苷酸序列。在一些实施方案中,此种特征可减少或最小化在检测期间可能存在(例如,作为污染物)于样品中的受试者的任何基因组dna和/或mrna转录物的干扰。
180.在一些实施方案中,寡核苷酸结构域的双链部分可具有被设计成减少或最小化自身二聚体、同源二聚体或异源二聚体的形成的核苷酸序列。
181.在一些实施方案中,用于本文提供的技术的寡核苷酸结构域的单链悬突的长度可为约2个至约20个核苷酸。在一些实施方案中,寡核苷酸结构域的单链悬突的长度可为约2个至约15个核苷酸、约2个至约10个核苷酸、约3个至约20个核苷酸、约3个至约15个核苷酸、约3个至约10个核苷酸。在一些实施方案中,单链悬突可具有至少1个至5个核苷酸的长度。在一些实施方案中,寡核苷酸结构域的单链悬突的长度可为至少2个或更多个核苷酸,包括例如至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个、至少11个、至少12个、至少13个、至少14个、至少15个、至少20个核苷酸或更多。在一些实施方案中,寡核苷酸结构域的单链悬突的长度可为不超过20个核苷酸或更少,包括例如不超过15个、不超过14个、不超过13个、不超过12个、不超过11个、不超过10个、不超过9个、不超过8个、不超过7个、不超过6个、不超过5个、不超过4个核苷酸或更少。
182.在一些实施方案中,寡核苷酸结构域的单链悬突的长度可为约1nm至约10nm。在一些实施方案中,寡核苷酸结构域的单链悬突的长度可为约1nm至约5nm。在一些实施方案中,寡核苷酸结构域的单链悬突的长度可为至少约0.5nm或更长,包括例如至少约1nm、至少约1.5nm、至少约2nm、至少约3nm、至少约4nm、至少约5nm、至少约6nm、至少约7nm、至少约8nm、至少约9nm、至少约10nm或更长。在一些实施方案中,寡核苷酸结构域的单链悬突的长度可为不超过10nm或更短,包括例如不超过9nm、不超过8nm、不超过7nm、不超过6nm、不超过5nm、不超过4nm、不超过3nm、不超过2nm、不超过1nm或更短。
183.寡核苷酸结构域的单链悬突被设计成包含与第二检测探针的单链悬突的至少一部分互补的核苷酸序列,使得包含第一检测探针和第二检测探针的双链复合物可通过互补单链悬突的杂交形成。在一些实施方案中,选择互补单链悬突的核苷酸序列以在适当核酸连接酶存在下获得最佳连接效率。在一些实施方案中,单链悬突具有优先选择用于通过关注的特定核酸连接酶(例如,dna连接酶,诸如t4或t7连接酶)有效连接的核苷酸序列。例如,此种单链悬突可具有gagt的核苷酸序列,例如,如描述于song等人,“enzyme
‑
guided dna sewing architecture”scientific reports 5:17722(2015)中。
184.当两个检测探针通过各自的互补单链悬突的杂交偶联在一起时,它们各自的包含杂交单链悬突的寡核苷酸结构域在一些实施方案中的组合长度可为关注的实体(例如,生物实体)的特征长度(例如,直径)的约90%至110%或约95%至105%。例如,在一些实施方案中,当生物实体为外泌体时,组合长度可为约50nm至约200nm、或约75nm至约150nm、或约80nm至约120nm。
185.c.靶结合部分与寡核苷酸结构域之间的偶联
186.寡核苷酸结构域和靶结合部分可通过共价键联和/或通过非共价结合(例如像蛋
白质
‑
蛋白质相互作用,诸如链霉亲和素
‑
生物素相互作用和/或离子相互作用)在检测探针中偶联在一起。在一些实施方案中,适合根据本公开使用的检测探针为包含靶结合部分与寡核苷酸结构域的缀合物分子,其中所述两种组分通常例如直接通过键或间接通过一个或多个接头彼此共价偶联。在一些实施方案中,靶结合部分通过共价键联(例如,直接通过键或间接通过一个或多个接头)和/或通过非共价结合(例如像蛋白质
‑
蛋白质相互作用,诸如链霉亲和素
‑
生物素相互作用和/或离子相互作用)偶联到寡核苷酸结构域的两条链中的一条。
187.在使用接头的情况下,在一些实施方案中,选择接头以提供靶结合部分通过所选接头共价连接至寡核苷酸结构域的一条或两条链。在一些实施方案中,选择接头以使得靶结合部分与寡核苷酸结构域的一条或两条链的所得共价连接保持靶结合部分对其靶标的期望的结合亲和力。在一些实施方案中,选择接头以增强靶结合部分对其靶标的结合特异性。关注的接头和/或缀合方法可根据靶结合部分(例如,其大小和/或电荷)而广泛变化。在一些实施方案中,接头为生物学惰性的。
188.用于将靶结合部分偶联至寡核苷酸的多种接头和/或方法是本领域普通技术人员已知的,并且可根据本公开使用。在一些实施方案中,接头可包含在任一端具有能够共价连接到靶结合部分的反应性官能团的间隔基团。可用于接头中的间隔基团的实例包括但不限于脂肪族和不饱和烃链(包括例如c4、c5、c6、c7、c8、c9、cio、c11、c12、c13、c14、c15、c16、c17、c18、c19、c20或更长)、含有杂原子诸如氧(例如,醚诸如聚乙二醇)或氮(多胺)的间隔基、肽、碳水化合物、可能含有杂原子的环状或非环状系统。促进共价连接的反应性官能团的非限制性实例包括亲核官能团(例如,胺、醇、硫醇、酰肼)、亲电官能团(例如,醛、酯、乙烯基酮、环氧化物、异氰酸酯、马来酰亚胺)、能够进行环加成反应、形成二硫键或与金属结合的官能团。在一些实施方案中,示例性反应性官能团但不限于伯胺和仲胺、异羟肟酸、n
‑
羟基琥珀酰亚胺(nhs)酯、二苯并环辛炔(dbco)
‑
nhs酯、叠氮基
‑
nhs酯、叠氮乙酸nhs酯、炔丙基
‑
nhs酯、反式环辛烯
‑
nhs酯、n
‑
羟基琥珀酰亚胺碳酸酯、氧羰基咪唑、硝基苯酯、三氟乙酯、缩水甘油醚、乙烯基砜、马来酰亚胺、叠氮苯甲酰肼、n
‑
[4
‑
(对叠氮水杨酸氨基)丁基]
‑3‑
[2'
‑
吡啶基二硫基]丙酰胺)、双(磺基琥珀酸亚酰胺)辛二酸酯、己二亚氨酸二甲酯、酒石酸二琥珀酰亚胺、n
‑
马来酰亚胺基丁酰氧基琥珀酰亚胺酯、n
‑
羟基磺基琥珀酰亚胺基
‑4‑
叠氮苯甲酸酯、n
‑
琥珀酰亚胺基[4
‑
叠氮苯基]
‑
1,3'
‑
二硫代丙酸酯、n
‑
琥珀酰亚胺基[4
‑
碘乙酰基]氨基苯甲酸酯、戊二醛和4
‑
[n
‑
马来酰亚胺基甲基]环己烷
‑1‑
羧酸琥珀酰亚胺基酯、3
‑
(2
‑
吡啶基二硫基)丙酸n
‑
羟基琥珀酰亚胺酯(spdp)、4
‑
(n
‑
马来酰亚胺甲基)
‑
环己烷
‑1‑
羧酸n
‑
羟基琥珀酰亚胺酯(smcc)及其任何组合。
[0189]
在一些实施方案中,使用n
‑
羟基琥珀酰亚胺(nhs)酯化学法将靶结合部分(例如,靶结合抗体剂)偶联或缀合至寡核苷酸结构域的一条或两条链。nhs酯与游离伯胺反应,并导致稳定的共价连接。在一些实施方案中,伯氨基可位于具有间隔基团的末端,例如但不限于脂肪族和不饱和烃链(例如,c6或c12间隔基团)。
[0190]
在一些实施方案中,可使用本领域已知的位点特异性缀合方法将靶结合部分(例如,靶结合抗体剂)偶联或缀合至寡核苷酸结构域的一条或两条链,以例如增强缀合的靶结合部分(例如,缀合的靶结合抗体剂)的结合特异性。位点特异性缀合方法的实例包括但不限于通过二硫键、c端、碳水化合物残基或聚糖和/或非天然氨基酸标记进行偶联或缀合。在
靶结合部分是或包含抗体剂或肽适体的一些实施方案中,寡核苷酸可通过存在于靶结合部分中的至少一个或多个游离胺基偶联或缀合至靶结合部分。在一些实施方案中,寡核苷酸可通过存在于靶结合部分中的至少一个或多个反应性硫醇基团偶联或缀合至是或包含抗体剂或肽适体的靶结合部分。在一些实施方案中,寡核苷酸可通过存在于靶结合部分中的至少一个或多个碳水化合物残基偶联或缀合至是或包含抗体剂或肽适体的靶结合部分。
[0191]
在一些实施方案中,多个寡核苷酸(例如,至少2个、至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个或更多个)可偶联或缀合至靶结合部分(例如,靶结合抗体剂)。
[0192]
示例性双链体靶实体检测系统
[0193]
在一些实施方案中,如本公开所提供的靶实体检测系统(并且可用于例如在单个实体水平上检测包含至少一个或多个靶标(例如,分子靶标)的关注的实体(例如,关注的生物实体))可包含针对第一靶标(例如,第一靶生物标记物)的第一检测探针(例如,如本文所述和/或使用的)的第一群和针对第二靶标(例如,第二靶生物标记物)的第二检测探针(例如,如本文所述和/或使用的)的第二群。在一些实施方案中,第一检测探针和第二检测探针分别针对的第一靶标(例如,第一靶生物标记物)和第二靶标(例如,第二靶生物标记物)是或包含相同的靶标(例如,相同的靶生物标记物)。在一些实施方案中,第一检测探针和第二检测探针分别针对的第一靶标(例如,第一靶生物标记物)和第二靶标(例如,第二靶生物标记物)是不同的靶标(例如,不同的靶生物标记物)。
[0194]
图2a至图2b说明了用于在单个实体水平上检测关注的实体(例如,生物实体,诸如细胞外囊泡)的示例性双链体靶实体检测系统,其包含(i)至少一个靶标(例如,疾病、病症或病状(例如,癌症)的靶生物标记物特征的靶生物标记物),其表达水平足够高以使得发现相同靶标的两个分子紧密接近,或(ii)至少两个或更多个不同的靶标(例如,疾病、病症或病状(例如,癌症)的靶生物标记物特征的生物标记物)。第一检测探针包含第一靶结合部分(例如,针对靶标1,诸如靶癌症标记物1)和偶联至第一靶结合部分的第一寡核苷酸结构域,第一寡核苷酸结构域包含第一双链部分和从第一寡核苷酸结构域的一端延伸的第一单链悬突。如图2a所示,第一寡核苷酸结构域可由较长链(链3)和较短链(链1)杂交产生,从而在一端形成双链部分和单链悬突。在一些实施方案中,第一靶结合部分(例如,针对靶标1,诸如靶癌症标记物1)偶联(例如,共价偶联)至第一寡核苷酸结构域的链(例如,链1)的5'端或3'端。在一些实施方案中,偶联至第一靶结合部分的链的5'端或3'端可用接头(例如,如本文所述和/或使用的,带有或不带有间隔基团)修饰。在一些实施方案中,第一寡核苷酸结构域的另一条链(例如,链3)的5'端具有游离磷酸酯基团。
[0195]
在图2a所示的实施方案中,第二检测探针包含第二靶结合部分(例如,针对靶标2,诸如靶癌症标记物2)和偶联至第二靶结合部分的第二寡核苷酸结构域,第二寡核苷酸结构域包含第二双链部分和从第二寡核苷酸结构域的一端延伸的第二单链悬突。如图2a所示,第二寡核苷酸结构域可由较长链(链4)和较短链(链2)杂交产生,从而在一端形成双链部分和单链悬突。在一些实施方案中,第二靶结合部分(例如,针对靶标2,诸如靶癌症标记物2)偶联(例如,共价偶联)至第二寡核苷酸结构域的链(例如,链2)的5'端。在一些实施方案中,偶联至第二靶结合部分的链的5'端可用接头(例如,如本文所述和/或使用的,带有或不带有间隔基团)修饰。在一些实施方案中,第二寡核苷酸结构域的另一条链(例如,链4)的5'端
具有游离磷酸酯基团。
[0196]
第一单链悬突和第二单链悬突的至少部分彼此互补,使得当它们足够紧密接近时(例如,当第一检测探针和第二检测探针同时结合相同的关注的实体(例如,生物实体,诸如细胞外囊泡)时),它们可杂交以形成双链复合物。在一些实施方案中,第一单链悬突和第二单链悬突具有相等的长度,使得当它们杂交以形成双链复合物时,它们各自的寡核苷酸结构域之间没有缺口(除了待连接的切口),并且每个相应的靶结合部分位于双链复合物的相对端。例如,在图2b所示的实施方案中,双链复合物在连接发生之前形成,其中双链复合物包含通过它们各自的单链悬突(例如,长度为4个核苷酸)的直接杂交而彼此偶联的第一检测探针和第二检测探针,其中每个相应的靶结合部分(例如,分别针对靶标1和靶标2)存在于双链复合物的相对端。在此类实施方案中,双链复合物的两条链(在各自的寡核苷酸结构域之间含有切口)都是可连接的,以例如用于扩增和检测。虽然图2b示出了第一检测探针与第二检测探针的杂交,并且未示出此类检测探针与关注的实体(例如,生物实体,诸如细胞外囊泡)的结合,但在一些实施方案中,双链复合物(例如,在连接发生之前)可包含关注的实体(例如,生物实体,诸如细胞外囊泡),其中第一靶结合部分(例如,针对靶标1,诸如靶癌症标记物1)和第二靶结合部分(例如,针对靶标2,诸如靶癌症标记物2)同时与关注的实体结合。
[0197]
在一些实施方案中,第一靶结合部分可针对与正常健康细胞和/或组织(例如,从其衍生癌细胞)特异性相关的生物标记物,并且第二靶结合部分可针对与多于一种癌症相关(但不存在于正常健康细胞和/或组织中)的生物标记物。例如,在一些实施方案中,第二靶结合部分可针对癌症的通用生物标记物(无论组织类型如何)。
[0198]
在一些实施方案中,第一靶结合部分可针对组织特异性癌症生物标记物(例如,通常与特定组织的癌症相关的生物标记物),并且第二靶结合部分可针对与癌症的相同组织特异性相关但处于正常健康状态的生物标记物。
[0199]
在一些实施方案中,第一靶结合部分和第二靶结合部分可各自针对不同的癌症相关生物标记物。例如,在一些实施方案中,第一靶结合部分和第二靶结合部分可各自针对与不同癌症(例如,与相同组织或不同组织相关的癌症)相关的生物标记物。在一些实施方案中,第一靶结合部分和第二靶结合部分可各自针对与相同癌症相关的生物标记物。
[0200]
在用于检测疾病、病症或病状(例如,癌症)的双链体靶实体检测系统的一些实施方案中,第一检测探针的第一靶结合部分可针对第一靶表面蛋白生物标记物,而第二检测探针的第二靶结合部分可针对第二靶表面蛋白生物标记物。在一些实施方案中,第一检测探针的第一靶结合部分可针对第一靶囊泡内蛋白生物标记物,而第二检测探针的第二靶结合部分可针对第二靶囊泡内蛋白生物标记物。在一些实施方案中,第一靶结合部分和第二靶结合部分可针对相同靶表面蛋白生物标记物或相同靶囊泡内蛋白生物标记物的相同或不同表位。在一些实施方案中,第一靶结合部分和第二靶结合部分可针对不同的靶表面蛋白生物标记物或不同的靶囊泡内蛋白生物标记物。
[0201]
在一些实施方案中,第一寡核苷酸结构域和第二寡核苷酸结构域的双链部分可为相同的。在一些实施方案中,第一寡核苷酸结构域和第二寡核苷酸结构域的双链部分可为不同的。
[0202]
示例性三链体或多链体(n≥3)靶实体检测系统
[0203]
在一些实施方案中,如本公开所提供的靶实体检测系统(并且可用于例如在单个实体水平上检测关注的实体(例如,关注的生物实体)可包含n个不同的探针群(例如,如本文所述和/或使用的),其中n≥3(例如,n=3、4、5或更大)。例如,在一些实施方案中,当n=3时,靶实体检测系统可包含用于第一靶标的第一检测探针(例如,如本文所述和/或使用的)、用于第二靶标的第二检测探针群(例如,如本文所述和/或使用的)和用于第三靶标的第三检测探针群(例如,如本文所述和/或使用的)。在一些实施方案中,第一靶标、第二靶标和第三靶标是相同的靶标。在一些实施方案中,第一靶标、第二靶标和第三靶标是不同的靶标。在一些实施方案中,第一靶标、第二靶标和第三靶标中的至少两个是不同的靶标。
[0204]
图5a说明了用于在单个实体水平上检测包含至少一个或多个靶标(例如,分子靶标)的关注的实体(例如,生物实体,诸如细胞外囊泡)的示例性三链体靶实体检测系统。第一检测探针包含第一靶结合部分(例如,抗靶1抗体剂,诸如抗癌标记物1抗体剂)和偶联至第一靶结合部分的第一寡核苷酸结构域,第一寡核苷酸结构域包含第一双链部分和从第一寡核苷酸结构域的一端延伸的第一单链悬突。如图5a所示,第一寡核苷酸结构域可由较长链(链8)和较短链(链1)杂交产生,从而在一端形成双链部分和单链悬突。在一些实施方案中,第一靶结合部分(例如,抗靶1抗体剂,诸如抗癌标记物1抗体剂)偶联(例如,共价偶联)至第一寡核苷酸结构域的链(例如,链1)的5'端。在一些实施方案中,偶联至第一靶结合部分的链的5'端可用接头(例如,如本文所述和/或使用的,带有或不带有间隔基团)修饰。在一些实施方案中,第一寡核苷酸结构域的另一条链(例如,链8)的5'端具有游离磷酸酯基团。
[0205]
在图5a所示的实施方案中,第二检测探针包含第二靶结合部分(例如,抗靶3抗体剂,诸如抗癌标记物3抗体剂)和偶联至第二靶结合部分的第二寡核苷酸结构域,第二寡核苷酸结构域包含第二双链部分和从第二寡核苷酸结构域的一端延伸的第二单链悬突。如图5a所示,第二寡核苷酸结构域可由较长链(链4)和较短链(链2)杂交产生,从而在一端形成双链部分和单链悬突。在一些实施方案中,第二靶结合部分(例如,抗靶3抗体剂,诸如抗癌标记物3抗体剂)偶联(例如,共价偶联)至第二寡核苷酸结构域的链(例如,链2)的5'端。在一些实施方案中,偶联至第二靶结合部分的链的5'端可用接头(例如,如本文所述和/或使用的,带有或不带有间隔基团)修饰。在一些实施方案中,第二寡核苷酸结构域的另一条链(例如,链4)的5'端不具有游离磷酸酯基团。
[0206]
第三检测探针包含第三靶结合部分(例如,抗靶2抗体剂,诸如抗癌标记物2抗体剂)和偶联至第三靶结合部分的第三寡核苷酸结构域,第三寡核苷酸结构域包含第三双链部分和从第三寡核苷酸结构域的每一端延伸的单链悬突。例如,单链悬突从第三寡核苷酸结构域的链的一端延伸,而另一单链悬突从第三寡核苷酸结构域的不同链的相对端延伸。如图5a所示,第三寡核苷酸结构域可由两条链(例如,链9和链10)的部分杂交产生,从而在每一端形成双链部分和单链悬突。例如,在第三检测探针的链9的5'端形成单链悬突(3a),其中链9的'5端具有游离磷酸酯基团。另外,在相同的第三检测探针的链10的5'端形成单链悬突(3b),并且第三靶结合部分(例如,抗靶2抗体剂,诸如抗癌标记物2抗体剂)也偶联(例如,共价偶联)至链10的5'端。在一些实施方案中,偶联至第三靶结合部分的链(例如,链10)的5'端可用接头(例如,如本文所述和/或使用的,带有或不带有间隔基团)修饰。
[0207]
当所有三个检测探针足够紧密接近时,例如,当所有三个检测探针同时结合相同
的关注的实体(例如,生物实体)时,(i)第三检测探针的单链悬突(例如,3a)的至少一部分与第二检测探针的单链悬突的相应互补部分杂交,并且(ii)第三检测探针的另一个单链悬突(例如,3b)的至少一部分与第一检测探针的单链悬突的相应互补部分杂交。结果,通过相应单链悬突的直接杂交形成包含以线性排列彼此偶联的所有三个检测探针的双链复合物。参见例如,图5a。
[0208]
在涉及在所提供的技术中使用至少三个或更多个(n≥3)检测探针的一些实施方案中,当检测探针的单链悬突退火于每个相应的配偶体以形成双链复合物时,至少(n
‑
2)个靶结合部分存在于双链复合物的一个或多个内部位置。在此类实施方案中,期望在双链复合物的单链中存在内部靶结合部分,使得双链复合物的另一条链不含任何内部靶结合部分,并且因此可连接以形成例如用于扩增和/或检测的连接模板。参见例如,图5a(使用三个检测探针)、图5b(使用四个检测探针)和图10(使用n个检测探针)。
[0209]
在双链复合物的链包含至少一个或多个内部靶结合部分的一些实施方案中,所述链包含内部靶结合部分所偶联的检测探针的寡核苷酸链末端与另一个检测探针的寡核苷酸链末端之间的缺口。缺口的大小足够大,使得所述链在核酸连接酶的存在下变得不可连接。在一些实施方案中,缺口可为2至8个核苷酸大小或2至6个核苷酸大小。在一些实施方案中,缺口的大小为6个核苷酸。在一些实施方案中,重叠(单链悬突之间的杂交区)可为2至15个核苷酸长度或4至10个核苷酸长度。在一些实施方案中,重叠(单链悬突之间的杂交区)的长度为8个核苷酸。选择缺口和/或杂交区的大小以提供与连接模板(不包含内部靶结合部分)和非连接模板(包含至少一个内部靶结合部分)的最佳信号分离。应当注意,虽然图5a至图5b和图10未示出检测探针与关注的实体(例如,生物实体)的结合,但双链复合物(例如,在连接发生之前)可包含关注的实体(例如,生物实体,诸如细胞外囊泡),其中至少三个或更多个靶结合部分同时结合到关注的实体。
[0210]
在一些实施方案中,对用于本文提供的靶实体检测系统(例如,本文所述的双链体、三链体或多链体靶实体检测系统)的检测探针的组合(例如,一组)的选择(例如,检测探针和/或特定生物标记物的数量)基于例如被认为对于特定应用是最佳的期望特异性和/或期望灵敏度。例如,在一些实施方案中,选择检测探针的组合来检测癌症(例如,对于i期、ii期、iii期或iv期),使得其提供的特异性为至少95%或更高,包括例如至少96%、至少97%、至少98%、至少99%、至少99.5%、至少99.7%、至少99.8%或更高。在一些实施方案中,选择检测探针的组合来检测癌症(例如,对于i期、ii期、iii期或iv期),使得其提供的灵敏度为至少30%或更高,包括例如至少40%、至少50%、至少60%、至少70%、至少80%、至少90%、至少95%或更高。在一些实施方案中,选择检测探针的组合来检测癌症(例如,对于i期、ii期、iii期或iv期),使得其提供的阳性预测值为至少8%或更高,包括例如至少9%、至少10%、至少15%、至少20%、至少25%、至少30%、至少40%、至少50%或更高。在一些实施方案中,选择检测探针的组合来检测癌症(例如,对于i期、ii期、iii期或iv期),使得其提供的检测限(lod)低于1x107ev/ml样品或更低,包括例如低于7x106ev/ml样品、低于6x106ev/ml样品、低于5x106ev/ml样品、低于4x106ev/ml样品、低于3x106ev/ml样品、低于2x106ev/ml样品、低于1x106ev/ml样品或更低。在一些实施方案中,此类癌症检测测定可用于检测不同的癌症或特定癌症的亚型和/或阶段。在一些实施方案中,可使用此种检测测定法检测的一种或多种癌症可包括以下中的一种或多种:急性淋巴细胞性白血病、急性髓系白血病、胆管
癌、膀胱癌、脑癌(包括例如胶质母细胞瘤)、乳腺癌、宫颈癌、慢性淋巴细胞性白血病、慢性髓系白血病、结直肠癌、子宫内膜癌、食道癌、胃肠癌、霍奇金淋巴瘤、肾癌、肝癌、肺癌、多发性骨髓瘤、非霍奇金淋巴瘤、卵巢癌、胰腺癌、前列腺癌、肉瘤、皮肤癌和胃癌。在一些实施方案中,检测测定法(例如,本文所述的那些)可用于检测皮肤癌(例如,黑色素瘤)。在一些实施方案中,检测测定法(例如,本文所述的那些)可用于检测肺癌(例如,非小细胞肺癌)。在一些实施方案中,检测测定法(例如,本文所述的那些)可用于检测乳腺癌。在一些实施方案中,检测测定法(例如,本文所述的那些)可用于检测上皮来源的卵巢癌,诸如高级别浆液性卵巢癌)。
[0211]
在一些实施方案中,检测探针的组合(例如,一组)而不是单独的检测探针赋予检测疾病、病症或病状(例如,如本文所述的特定癌症和/或癌症阶段)特异性,例如,一个或多个单独的探针可针对本身对此种疾病、病症或病状(例如,癌症)没有特异性的靶标。例如,在一些实施方案中,本文提供的靶实体检测系统(例如,本文所述的双链体、三链体或多链体靶实体检测系统)中检测探针的有用组合可包含针对特异于相关疾病、病症或病状的靶标(即,对相关疾病、病症或病状具有特异性的靶标)的至少一种检测探针,并且还可包含针对不一定或完全特异于相关疾病、病症或病状的靶标的至少一种检测探针(例如,也可在健康的、不属于特定疾病、病症或病状和/或不属于关注的特定疾病阶段的一些或所有细胞上发现)。也就是说,如阅读本说明书的本领域技术人员将理解的,只要根据本发明使用的检测探针组是或包含一起对检测相关疾病、病症或病状具有特异性的多个单独的检测探针(即,充分区分与相关疾病、病症或病状相关的用于检测的生物实体与用于检测的不受关注的其他生物实体),则所述组根据本公开的某些实施方案是有用的。
[0212]
在一些实施方案中,本文提供的靶实体检测系统(例如,本文所述的双链体、三链体或多链体靶实体检测系统)中的有用检测探针可包含以下检测探针中的至少一种或多种类型:
[0213]
a.针对与正常健康细胞、细胞外囊泡和/或组织(例如,从其衍生患病细胞(例如,癌细胞)的正常健康细胞、细胞外囊泡和/或细胞)特异性相关的生物标记物的检测探针;
[0214]
b.针对与多于一种疾病(例如像多于一种癌症)相关(但不存在于正常健康细胞、细胞外囊泡和/或组织中)的生物标记物,例如针对癌症的通用生物标记物(无论组织类型如何)的检测探针;和
[0215]
c.针对组织特异性疾病生物标记物(例如,组织特异性癌症生物标记物,例如像与特定组织的癌症特异性相关的生物标记物,所述组织例如但不限于脑、乳腺、结肠、卵巢和/或与女性生殖系统相关的其他组织、胰腺、前列腺和/或与男性生殖系统相关的其他组织、肝脏、肺和皮肤)的检测探针。
[0216]
在一些实施方案中,用于检测癌症的检测探针的有用组合(例如,一组)可包含第一检测探针,所述第一检测探针针对与正常健康细胞、细胞外囊泡和/或组织(例如,从其衍生癌细胞)特异性相关的生物标记物,以及第二检测探针,所述第二检测探针针对与多于一种癌症相关(但不存在于正常健康细胞、细胞外囊泡和/或组织中)的生物标记物。例如,在一些实施方案中,此种第二检测探针可针对癌症的通用生物标记物(无论组织类型如何)。
[0217]
在一些实施方案中,用于检测癌症的检测探针的组合可包含第一检测探针,所述第一检测探针针对组织特异性癌症生物标记物(例如,通常与特定组织的癌症相关的生物
标记物),以及第二检测探针,所述第二检测探针针对与癌症的相同组织特异性相关但处于正常健康状态的生物标记物。
[0218]
在一些实施方案中,用于检测癌症的检测探针的组合可包含各自针对不同的癌症相关生物标记物的第一检测探针和第二检测探针。例如,在一些实施方案中,第一检测探针和第二检测探针可各自针对与不同癌症(例如,与相同组织或不同组织相关的癌症)相关的生物标记物。在一些实施方案中,第一检测探针和第二检测探针可各自针对与相同癌症相关的生物标记物。在一些实施方案中,第一检测探针和第二检测探针可各自针对与不同阶段的相同癌症相关的生物标记物。
[0219]
在一些实施方案中,本文提供的靶实体检测系统(例如,本文所述的双链体、三链体或多链体靶实体检测系统)可包含至少一个或多个(例如,至少2个或更多个)对照探针(除了靶特异性检测探针,例如,如本文所述和/或使用的,以例如在一些实施方案中识别疾病特异性生物标记物,诸如癌症特异性生物标记物和/或组织特异性生物标记物)。在一些实施方案中,对照探针被设计成使得其与关注的实体(例如,生物实体)的结合可促进检测信号的产生。在一些实施方案中,对照探针被设计成使得其与关注的实体(例如,生物实体)的结合抑制(完全或部分地)检测信号(“抑制剂探针”)的产生。例如,在一些实施方案中,对照探针可被设计成抑制在非靶实体中发生的连接。在一些实施方案中,对照探针可被设计成抑制来自非靶实体的连接模板的扩增。
[0220]
在一些实施方案中,对照探针包含对照结合部分和偶联至对照结合部分的寡核苷酸结构域(例如,如本文所述和/或使用的),寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突。对照结合部分是与对照参考结合的实体或部分。在一些实施方案中,对照参考可以是或包含优先与正常健康细胞或细胞外囊泡相关的生物标记物。在一些实施方案中,对照参考可以是或包含优先与非靶组织相关的生物标记物。在一些实施方案中,包括对照探针可选择性地去除或最小化由假阳性(例如,包含对照参考的关注的实体,任选地与待检测的一个或多个靶标组合)产生的可检测信号。
[0221]
例如,如图11至图12所示,靶实体检测系统(例如,本文所述的那些)可包含多个(例如,至少2个、至少3个或更多个)靶特异性检测探针和至少一个对照探针(以例如识别正常健康细胞或细胞外囊泡和/或来自非特异性组织的细胞或细胞外囊泡)。可设计并确定靶特异性检测探针和对照探针的寡核苷酸结构域,使得当对照探针结合关注的实体(例如,生物实体,诸如细胞外囊泡)时,即使在同一关注的实体(例如,生物实体,诸如细胞外囊泡)中结合靶特异性检测探针中的至少一个或所有也不一定导致形成连接模板。在不存在与同一关注的实体结合的对照的情况下,所有靶特异性检测探针与单个关注的实体(例如,生物实体,诸如细胞外囊泡)的结合导致优先形成连接模板并因此形成可检测信号。仅出于说明目的,图12示出了作为连接的竞争性抑制剂的对照探针的示例性使用。例如,在不存在与关注的实体(例如,生物实体)结合的对照探针(例如,识别正常健康细胞或细胞外囊泡和/或来自非特异性组织的细胞或细胞外囊泡)的情况下,将第一靶特异性检测探针和第二靶特异性探针结合到相同的关注的实体允许它们足够紧密接近,以通过它们各自的寡核苷酸结构域的单链悬突的直接杂交而彼此相互作用,从而形成连接模板。对照探针可被设计成通过与靶特异性检测探针中的至少一个竞争其各自的靶结合配偶体来防止靶特异性检测探针之间的这种杂交。仅以举例的方式且仅出于说明目的,图12示出了对照探针的一端被设计
成结合靶特异性检测探针(例如,靶特异性检测探针2),而对照探针的另一端被设计成不能与在对照探针不存在的情况下以其他方式结合前者(例如,靶特异性检测探针2)的另一个靶特异性检测探针(例如,靶特异性检测探针1)相互作用。在一些实施方案中,对照探针的一端被设计为平端,使得其不能与另一检测探针的单链悬突杂交。在一些实施方案中,对照探针的寡核苷酸链(例如,如图12所示的对照探针的链9)的3'端可具有双脱氧核苷酸,使得不允许连接。
[0222]
在一些实施方案中,对照探针可被设计成抑制来自非靶实体的连接模板的扩增。仅出于说明目的,图26示出了示例性抑制剂探针,所述抑制剂探针被设计成使其与非靶实体的结合在允许与另一探针(例如,检测探针)连接的情况下抑制或阻止连接模板的扩增。在一些实施方案中,抑制剂探针可针对非靶标,例如,与靶组织无关的标记物,或与待诊断的疾病、病症或病状(例如,癌症)无关的标记物。在一些此类实施方案中,抑制剂探针可类似于检测探针(例如,本文所述的那些),使得当检测探针和抑制剂探针紧密接近时,它们的单链悬突彼此杂交,从而允许连接。然而,与检测探针(例如,本文所述的那些)不同,此种抑制剂探针的寡核苷酸结构域的至少一条链不具有引物位点,因此阻止可能由于检测探针和存在于非靶实体中的抑制剂探针之间的相互作用而形成的任何连接模板的扩增。在存在与非靶实体(例如,来自不同组织的生物实体)结合的抑制剂探针的情况下,不能产生检测信号,因为没有引物位点的抑制剂探针不允许扩增模板。在一些实施方案中,包括此种抑制剂探针可选择性地去除假阳性,从而提高检测的特异性。
[0223]
在涉及本文所述的一个或多个对照探针的一些实施方案中,这样的一种或多种对照探针中使用的寡核苷酸结构域的长度可与在检测探针(例如,本文所述的那些)中使用的寡核苷酸结构域的长度相当或不同。例如,在一些实施方案中,对照探针的寡核苷酸结构域的长度可在约30个至约1000个核苷酸的范围内。在一些实施方案中,对照探针的寡核苷酸结构域的长度可在约30个至约500个核苷酸、约30个至约250个核苷酸、约30个至约200个核苷酸、约30个至约150个核苷酸、约40个至约150个核苷酸、约40个至约125个核苷酸、约40个至约100个核苷酸、约50个至约90个核苷酸、约50个至约80个核苷酸的范围内。在一些实施方案中,对照探针的寡核苷酸结构域的长度可在约50个核苷酸至约90个核苷酸的范围内。在一些实施方案中,对照探针的寡核苷酸结构域的长度可在约30个核苷酸至约50个核苷酸的范围内。在一些实施方案中,对照探针的寡核苷酸结构域的长度可在约10个核苷酸至约30个核苷酸的范围内。阅读本公开的本领域技术人员将理解,可调整寡核苷酸结构域的长度以改进检测测定中对照探针的性能。
[0224]
在一些实施方案中,本公开尤其提供了以下见解:如本文所述或使用的检测探针可非特异性地结合到固体基底表面,并且甚至在多次洗涤以去除任何过量或未结合的检测探针之后,其中一些仍可保留在测定样品中;并且此类非特异性结合的检测探针可从固体基底表面脱落并在连接反应中自由浮动,从而允许它们彼此相互作用以生成产生不希望的背景信号的非特异性连接模板。因此,在一些实施方案中,本文提供的靶实体检测系统(例如,本文所述的双链体、三链体或多链体靶实体检测)可包含至少一种或多种(例如,至少2种或更多种)抑制剂寡核苷酸,其被设计来捕获未与关注的实体结合但在连接反应中作为游离剂保留的残留检测探针,从而防止此类自由浮动的检测探针与其他自由浮动的互补检测探针相互作用以产生不希望的背景信号。在一些实施方案中,抑制剂寡核苷酸可以是或
包含单链或双链寡核苷酸,所述单链或双链寡核苷酸包含用于检测探针(例如,如本文所述或使用的)的单链悬突的结合结构域,其中抑制剂寡核苷酸不包含引物结合位点。抑制剂寡核苷酸中不存在此种引物结合位点防止引物结合到由可检测探针与抑制剂寡核苷酸连接产生的非特异性连接模板,从而减少或抑制非特异性连接模板例如通过聚合酶链反应的扩增和/或检测。
[0225]
在一些实施方案中,抑制剂寡核苷酸包含用于检测探针(例如,如本文所述或使用的)的单链悬突的结合结构域,其中结合结构域是或包含与检测探针的单链悬突基本互补的核苷酸序列,使得具有互补单链悬突的游离的、未结合的检测探针可与抑制剂寡核苷酸的结合结构域结合。在一些实施方案中,抑制剂寡核苷酸可在一端具有发夹。在一些实施方案中,抑制剂寡核苷酸可为单链寡核苷酸,其在一端包含用于检测探针的单链悬突的结合结构域,其中单链寡核苷酸的一部分可自杂交以在另一端形成发夹,例如,如图18所示。
[0226]
在一些实施方案中,本文提供的靶实体检测系统(例如,本文所述的双链体、三链体或多链体靶实体检测系统)不包含将检测探针的寡核苷酸结构域与另一检测探针的寡核苷酸结构域相关联的连接器寡核苷酸。在一些实施方案中,连接器寡核苷酸被设计成桥接任何两个检测探针的寡核苷酸结构域,所述两个检测探针在与关注的实体结合时不以其他方式彼此相互作用。在一些实施方案中,连接器寡核苷酸被设计成与检测探针的寡核苷酸结构域的至少一部分和另一检测探针的寡核苷酸结构域的至少一部分杂交。连接器寡核苷酸可为单链的、双链的或其组合。连接器寡核苷酸不含任何靶结合部分(例如,如本文所述和/或使用的)或对照结合部分。在至少一些实施方案中,不需要连接器寡核苷酸来间接连接检测探针的寡核苷酸结构域;在一些实施方案中,不使用此类连接器寡核苷酸,部分是因为如本文所提供和/或使用的检测探针被设计成使得它们各自的寡核苷酸结构域具有足够的长度以在它们足够紧密接近时(例如,当检测探针同时结合关注的实体(例如,生物实体,诸如细胞外囊泡)时)彼此接触并相互作用。
[0227]
在一些实施方案中,靶实体检测系统包括(i)多个检测探针(例如,如本文所述的那些),每个检测探针针对特定靶标(例如,分子靶标或靶生物标记物特征的生物标记物);以及(ii)用于捕获关注的靶实体(例如,生物实体,诸如细胞外囊泡)的剂。在一些实施方案中,此种捕获剂是或包含固体基底(例如,如本文所述的那些,例如像在一些实施方案中为磁珠),所述固体基底包含与其缀合的靶捕获部分。在一些实施方案中,靶捕获部分可以是或包含针对关注的靶实体(例如,生物实体,诸如细胞外囊泡)的抗体剂。
[0228]
ii.使用所提供的靶实体检测系统的示例性方法
[0229]
所提供的靶实体检测系统可用于检测样品(例如,生物、环境或其他样品)中的关注的实体(例如,生物实体,诸如细胞外囊泡)以用于各种应用和/或目的,例如,在与特定疾病、病症或病状(例如,癌症)或多种疾病、病症或病状(例如,多种癌症)的检测相关的一些实施方案中。因此,本文提供的一些方面涉及使用适合根据本公开使用的多个(例如,至少2个、至少3个或更多个)检测探针的方法。在一些实施方案中,方法包括使样品(例如,来自人受试者的血液或血液衍生样品)中的关注的实体(例如,生物实体,诸如细胞外囊泡)与包含如本文所述和/或使用的至少2个或更多个(包括例如至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个、至少11个、至少12个、至少13个、至少14个、至少15个、至少16个、至少17个、至少18个、至少19个、至少20个或更多个)检测探针的一组检测探
针接触。在一些实施方案中,方法包括使包含关注的实体(例如,生物实体,诸如细胞外囊泡)的样品经受靶实体检测系统(例如,如本文所提供的)。多个检测探针(例如,至少两个或更多个)可同时或在不同时间(例如,顺序地)添加到包含关注的实体(例如,生物实体,诸如细胞外囊泡)的样品中。
[0230]
在一些实施方案中,可将对特定疾病、病症或病状(例如,癌症)的检测具有特异性的一组检测探针添加到单个测定室中。在一些实施方案中,可将对多种疾病、病症或病状(例如,多种癌症)的检测具有特异性的一组检测探针添加到单个测定室中。在一些实施方案中,一组检测探针可分成多个子集(例如,每个子集针对不同疾病或病状的检测),其中每个子集可添加到来自同一样品的等分试样中。因此,在一些实施方案中,可将样品分成等分试样,使得可将不同组的检测探针(例如,每个针对不同疾病或病状的检测)添加到不同的等分试样中。在此类实施方案中,所提供的技术可以一次一个等分试样或一次多个等分试样实施(例如,用于平行测定以增加吞吐量)。
[0231]
在一些实施方案中,添加到样品中的检测探针的量在混合物中提供足够低浓度的检测探针,以确保检测探针在没有与关注的实体(例如,生物实体)结合的情况下不会随机地彼此紧密接近,至少没有达到任何很大或实质性的程度。因此,在许多实施方案中,当检测探针通过检测探针的各自的靶结合部分与关注的实体(例如,生物实体)的结合位点之间的结合相互作用同时结合到相同的关注的实体(例如,生物实体)时,检测探针彼此足够紧密接近以形成双链复合物(例如,如本文所述的)。在一些实施方案中,与样品组合后的混合物中检测探针的浓度可在约1fm至1μm的范围内,诸如约1pm至约1nm,包括约1pm至约100nm。
[0232]
在一些实施方案中,样品中关注的实体(例如,生物实体)的浓度足够低,使得在不存在与同一关注的实体(例如,生物实体)结合的相应检测探针的情况下,结合到一个关注的实体(例如,生物实体)的检测探针不会随机地与结合到另一个关注的实体(例如,生物实体)的另一个检测探针紧密接近,至少没有达到任何很大或实质性的程度。仅以举例的方式,样品中关注的实体(例如,生物实体)的浓度足够低,使得结合到关注的非靶实体(例如,非癌性生物实体,诸如包含第一靶标的细胞外囊泡)的第一靶检测探针不会随机地与结合到另一个关注的非靶实体(例如,非癌性生物实体,诸如细胞外囊泡)的另一个不同的靶检测探针紧密接近,至少没有达到任何很大或实质性的程度来产生假阳性可检测信号。
[0233]
在一些实施方案中,在使关注的实体与适合根据本公开使用的检测探针接触之前,可将关注的实体(例如,生物实体,诸如细胞外囊泡)捕获或固定到固体基底上。在一些实施方案中,关注的实体可通过非特异性相互作用(包括例如吸附)捕获在固体基底表面上。在一些实施方案中,关注的实体可选择性地捕获在固体基底表面上。例如,在一些实施方案中,固体基底表面可涂覆有特异性结合关注的实体的剂(例如,特异性靶向关注的实体诸如细胞外囊泡或癌症相关细胞外囊泡的抗体剂)。在一些实施方案中,固体基底表面可涂覆有亲和结合对的成员,并且待捕获的关注的实体可缀合至亲和结合对的互补成员。在一些实施方案中,示例性亲和结合对包括例如但不限于生物素和抗生物素蛋白样分子,诸如链霉亲和素。如本领域技术人员将理解的,其他适当的亲和结合对也可用于促进将关注的实体捕获到固体基底表面上。在一些实施方案中,关注的实体(例如,生物实体,诸如细胞外囊泡)可通过施加电流而捕获到固体基底表面上,例如,如描述于ibsen等人acs nano.,11:6641
‑
6651(2017)和lewis等人acs nano.,12:3311
‑
3320(2018)中,两者都描述了使用交流
电动微阵列芯片装置从未稀释的人血液或血浆样品中分离细胞外囊泡。
[0234]
固体基底可以适合于捕获关注的实体(例如,生物实体,诸如细胞外囊泡)并且不干扰下游处理、加工和/或检测的形式提供。例如,在一些实施方案中,固体基底可以是或包含珠(例如,磁珠)。在一些实施方案中,固体基底可以是或包含表面。例如,在一些实施方案中,此种表面可为测定室(包括例如管、孔、微孔、板、过滤器、膜、基质等)的捕获表面。因此,在一些实施方案中,本文所述的方法包括在使关注的实体(例如,生物实体)与多个检测探针接触之前,将关注的实体捕获或固定到固体基底上。
[0235]
在一些实施方案中,在将关注的实体捕获到固体基底表面上之前,可处理包含关注的实体的样品,以例如去除不需要的实体,诸如细胞碎片或细胞。例如,在一些实施方案中,可对此种样品进行离心,以例如去除细胞碎片、细胞和/或其他颗粒。另外或替代地,在一些实施方案中,可对此种样品进行基于尺寸排阻的纯化或过滤。各种基于尺寸排阻的纯化或过滤是本领域已知的,并且本领域技术人员将理解,在一些情况下,可基于特定分子量或粒径截止值对样品进行离心柱纯化。本领域技术人员还将理解,可例如基于关注的实体(例如,生物实体,诸如细胞外囊泡)的大小来选择用于纯化目的的适当分子量或粒径截止值。例如,在一些实施方案中,尺寸排阻分离方法可应用于包含细胞外囊泡的样品以分离具有特定尺寸(例如,30nm至1000nm)的细胞外囊泡的一部分。在一些实施方案中,尺寸排阻分离方法可应用于包含细胞外囊泡的样品以分离大于70nm且不超过200nm的细胞外囊泡的一部分。
[0236]
在一些实施方案中,可在使关注的实体与本文所述和/或使用的多个检测探针接触之前对样品中的关注的实体(例如,生物实体)进行处理。可进行不同的样品处理和/或制备以例如稳定待检测的关注的实体(例如,生物实体)中的靶标(例如,分子靶标),和/或促进靶标(例如,分子靶标,诸如细胞内靶标)暴露于检测探针,和/或减少检测探针的非特异性结合。此类样品处理和/或制备的实例是本领域已知的,并且包括但不限于交联分子靶标(例如,固定)、使生物实体(例如,细胞或细胞外囊泡)透化和/或封闭非特异性结合位点。
[0237]
在使样品中的关注的实体(例如,生物实体)与一组检测探针接触后,可将此种混合物孵育足以使检测探针结合关注的实体中的相应靶标(例如,分子靶标)(如果存在的话)的一段时间,以形成双链复合物(例如,如本文所述)。在一些实施方案中,在约10℃至约50℃范围内(包括约20℃至约37℃)的温度下将此种混合物孵育约5分钟至约5小时范围内(包括约30分钟至约2小时)的时间段。
[0238]
然后可使双链复合物(由使关注的实体诸如生物实体与检测探针接触而产生)随后与核酸连接酶接触以进行检测探针的寡核苷酸链的游离3'端羟基和5'端磷酸端的核酸连接,从而产生包含至少两个或更多个检测探针的寡核苷酸链的连接模板。在一些实施方案中,在使包含双链复合物的测定样品与核酸连接酶接触之前,可将至少一种或多种抑制剂寡核苷酸(例如,如本文所述)添加至测定样品,使得抑制剂寡核苷酸可捕获可在连接反应期间以其他方式彼此相互作用的任何残留的自由浮动检测探针。
[0239]
如本领域中已知的,当两个紧邻的核酸退火或杂交到与它们互补的第三核酸序列时,连接酶催化两个紧邻的核酸的并列的3'
‑
羟基和5'
‑
磷酸末端之间形成磷酸二酯键。可使用任何已知的核酸连接酶(例如,dna连接酶),包括但不限于温度敏感和/或热稳定连接酶。温度敏感连接酶的非限制性实例包括噬菌体t4 dna连接酶、噬菌体t7连接酶和大肠杆
菌(e.coli)连接酶。热稳定连接酶的非限制性实例包括taq连接酶、tth连接酶和pfu连接酶。热稳定连接酶可从嗜热或超嗜热生物获得,包括但不限于原核生物、真核生物或古细菌生物。在一些实施方案中,核酸连接酶为dna连接酶。在一些实施方案中,核酸连接酶可为rna连接酶。
[0240]
在一些实施方案中,在连接步骤中,合适的核酸连接酶(例如,dna连接酶)和必要和/或期望的任何试剂与反应混合物组合,并保持在足以发生杂交的连接寡核苷酸的连接的条件下。连接反应条件是本领域技术人员所熟知的。在连接期间,在一些实施方案中,可将反应混合物保持在约20℃至约45℃范围内(诸如约25℃至约37℃)的温度下约5分钟至约16小时范围内(诸如约1小时至约4小时)的时间段。在其他实施方案中,可将反应混合物保持在约35℃至约45℃范围内(诸如约37℃至约42℃,例如,是或约38℃、39℃、40℃或41℃)的温度下约5分钟至约16小时范围内(诸如约1小时至约10小时,包括约2小时至约8小时)的时间段。
[0241]
对此种连接模板的检测可提供关于样品中关注的实体(例如,生物实体)对于检测探针所针对的靶标是阳性还是阴性的信息。例如,此种连接模板的可检测水平指示包含关注的靶标(例如,分子靶标)的关注的受试实体(例如,生物实体)。在一些实施方案中,可检测水平是高于参考水平例如至少10%或更多(包括例如至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、至少90%或更多)的水平。在一些实施方案中,参考水平可为在阴性对照样品(诸如其中不存在包含此类靶标的关注的实体的样品)中观察到的水平。相反,此种连接模板的不可检测水平(例如,低于可检测水平的阈值的水平)指示关注的受试实体(例如,生物实体)中不存在关注的靶标(例如,分子靶标)中的至少一个。本领域技术人员将理解,可基于例如被认为对于每个应用和/或目的是最佳的期望灵敏度水平和/或期望特异性水平来确定将可检测水平与不可检测水平分开的阈值。例如,在一些实施方案中,可使用本文提供的系统来实现99.7%的特异性,例如通过设置比参考水平(例如,在阴性对照样品中观察到的水平,例如像来自一个或多个正常健康个体的样品)高三个标准偏差的阈值。另外或替代地,本领域技术人员将理解,可检测水平的阈值(例如,如由检测信号强度所反映的)可比参考水平高1至100倍。
[0242]
在一些实施方案中,本文提供的方法包括在连接之后,检测连接模板例如作为样品中关注的实体的存在和/或量的量度。在各种实施方案中,连接模板的检测可为定性的或定量的。因此,在检测为定性的一些实施方案中,方法提供了对被测定的样品中是否存在包含至少两个或更多个靶标(例如,分子靶标)的关注的实体(例如,生物实体)的读数或评价,例如评估。在其他实施方案中,方法提供了对被测定的样品中是否存在包含至少两个或更多个靶标(例如,分子靶标)的关注的实体(例如,生物实体)的定量检测,例如评价或评估被测定的样品中包含至少两个或更多个靶标(例如,分子靶标)的关注的实体(例如,生物实体)的实际量。在一些实施方案中,此种定量检测可为绝对的或相对的。
[0243]
可通过本领域已知的适当方法检测通过使用本文提供的技术而形成的连接模板。本领域技术人员将理解,可基于例如期望的灵敏度水平和/或实践方法的应用来选择适当的检测方法。在一些实施方案中,可直接检测连接模板而无需任何扩增,而在其他实施方案中,可扩增连接模板以使得连接模板的拷贝数增加,以例如增强特定测定的灵敏度。在不进行扩增的检测是可行的情况下,可以多种不同的方式检测连接模板。例如,检测探针的寡核
苷酸结构域(例如,如本文所述和/或使用的)可被直接标记,例如荧光标记或放射性同位素标记,使得连接模板被直接标记。例如,在一些实施方案中,检测探针的寡核苷酸结构域(例如,如本文所提供和/或使用的)可包含可检测标记。可检测标记可为通过光谱、光化学、生物化学、免疫化学、电、光学或化学方式可检测的组合物。此类标记包括用于用标记的链霉亲和素缀合物染色的生物素、磁珠(例如,)、荧光染料(例如,荧光素、德克萨斯红、罗丹明、绿色荧光蛋白等)、放射性标记(例如,3h、
125
i、
34
s、
14
c或
32
p)、酶(例如,辣根过氧化物酶、碱性磷酸酶和elisa中常用的其他酶)和量热标记,诸如胶体金或有色玻璃或塑料(例如,聚苯乙烯、聚丙烯、乳胶等)珠。在一些实施方案中,直接标记的连接模板可与反应混合物的其余部分(包括未连接的直接标记的连接寡核苷酸)大小分离,以便检测连接模板。
[0244]
在一些实施方案中,连接模板的检测可包括扩增步骤,其中连接核酸的拷贝数增加,以例如增强测定的灵敏度。根据需要,扩增可为线性的或指数的,其中扩增可包括但不限于聚合酶链反应(pcr);定量pcr、等温扩增、基于核酸序列的扩增(nasba)、数字液滴pcr等。
[0245]
用于实现pcr扩增的各种技术是本领域已知的;本领域技术人员将非常熟悉pcr技术的多种实施方案,并且将能够容易地选择适合扩增使用本文提供的技术产生的连接模板的实施方案。例如,在一些实施方案中,包括连接模板的反应混合物与在引物延伸反应中使用的一个或多个引物组合,例如pcr引物(诸如在几何(或指数)扩增中使用的正向和反向引物或在线性扩增中使用的单个引物)。与一个或多个连接模板接触的寡核苷酸引物应具有足够的长度,以在适当的退火条件下提供与互补模板dna的杂交。引物的长度通常为至少10bp,包括例如长度为至少15bp、长度为至少20bp、长度为至少25bp、长度为至少30bp或更长。在一些实施方案中,引物的长度通常可在约15bp至50bp长度、约18bp至30bp或约20bp至35bp长度的范围内。连接模板可与单个引物或一组两个引物(正向和反向引物)接触,这取决于是否需要模板dna的引物延伸、线性或指数扩增。
[0246]
除了上述组分之外,包含连接模板的反应混合物通常还包括聚合酶和脱氧核糖核苷三磷酸(dntp)。所需的聚合酶活性可由一种或多种不同的聚合酶提供。在制备反应混合物以例如用于连接模板的扩增时,各种组成成分可以任何方便的顺序组合。例如,适当的缓冲液可与一个或多个引物、一种或多种聚合酶和待检测的连接模板组合,或各种组成成分中的所有可同时组合以产生反应混合物。
[0247]
iii.对个体生物实体(例如,细胞外囊泡)中的一个或多个靶组合(例如,一个或多个靶生物标记物特征)的检测
[0248]
在一些实施方案中,本文提供的技术(包括例如系统、组合物和方法)可用于检测个体生物实体(例如,细胞外囊泡)中的一个或多个靶组合(例如,疾病、病症或病状(例如,癌症)的一个或多个靶生物标记物特征)。在一些实施方案中,本公开提供了通过检测单个细胞外囊泡中疾病、病症或病状(例如,癌症)的一个或多个靶标组合(例如,一个或多个靶生物标记物特征)的共定位来解决许多常规诊断测定(例如,基于无细胞核酸、血清蛋白和/或细胞外囊泡的批量分析)的问题的技术(包括系统、组合物和方法)。在一些实施方案中,根据本公开待检测的靶生物标记物特征包含至少一个细胞外囊泡相关膜结合多肽和选自由以下组成的组的至少一个靶生物标记物:表面蛋白生物标记物、内部蛋白生物标记物和存在于与此种疾病、病症或病状(例如,癌症)相关的细胞外囊泡中的rna生物标记物。在一
些实施方案中,可通过生物信息学分析来鉴定此种靶生物标记物特征。
[0249]
在一个方面,本公开尤其提供了用于检测个体生物实体(例如,细胞外囊泡)中的一个或多个生物标记物特征的组合物(例如,系统和试剂盒)和方法。在许多实施方案中,此种靶生物标记物特征对疾病、病症或病状(例如,癌症)具有特异性。在一些实施方案中,此类靶生物标记物特征可通过多管齐下的生物信息学分析和生物学方法来鉴定,例如,在一些实施方案中,所述方法涉及对不同数据集的计算分析,例如,在一些实施方案中,所述数据集包括测序数据、表达数据、质谱、组织学、翻译后修饰数据和/或通过机器学习和/或计算建模的体外和/或体内实验数据中的一个或多个。
[0250]
在一些实施方案中,生物标记物的组合(例如,靶生物标记物特征)可通过检测探针的多个(例如,至少两个或更多个)成对或正交组合来检测,其中每对检测探针可针对至少一个不同的靶标。在一些实施方案中,生物标记物的组合(例如,靶生物标记物特征)可通过一组检测探针检测,每个检测探针被设计成彼此杂交以形成线性复合物。在一些实施方案中,可选择生物标记物的多个(例如,至少两个或更多个)组合以用于癌症检测。在一些实施方案中,可选择生物标记物的多个(例如,至少两个或更多个)组合以检测特定的癌症或其阶段和/或其亚型。在一些实施方案中,可选择生物标记物的多个(例如,至少两个或更多个)正交组合以用于癌症检测。在一些实施方案中,可选择生物标记物的多个(例如,至少两个或更多个)正交组合以检测特定的癌症或其阶段和/或其亚型。在一些实施方案中,可选择多个(例如,至少两个或更多个)靶生物标记物特征以用于癌症检测。在一些实施方案中,可选择多个(例如,至少两个或更多个)靶生物标记物特征以检测特定的癌症或其阶段和/或其亚型。仅以举例的方式,在一些实施方案中,可选择至少生物标记物组合a和生物标记物组合b以检测特定癌症或其阶段和/或其亚型,其中生物标记物组合a可以是或包含靶标1和靶标2;并且生物标记物组合b可以是或包含靶标1和靶标3。在一些实施方案中,可选择至少生物标记物组合a和生物标记物组合b以检测特定癌症或其阶段和/或其亚型,其中生物标记物组合a可以是或包含靶标1和靶标2;并且生物标记物组合b可以是或包含靶标3和靶标4。
[0251]
在一些实施方案中,疾病、病症或病状(例如,癌症)的靶生物标记物特征包含至少一个或多个(例如,1、2、3、4、5、6、7、8个或更多个)细胞外囊泡相关膜结合多肽(例如,存在于与疾病、病症或病状(例如,癌症)相关的细胞外囊泡中的表面多肽)和选自由以下组成的组的至少一个或多个(例如,1、2、3、4、5、6、7、8个或更多个)靶生物标记物:一个或多个表面蛋白生物标记物、一个或多个囊泡内蛋白生物标记物和一个或多个囊泡内rna生物标记物,使得当使用本文提供的技术(例如,本文所述的靶实体检测系统)检测到这样的一个或多个细胞外囊泡相关膜结合多肽和这样的一个或多个靶生物标记物的组合呈现疾病、病症或病状(例如,癌症)的靶生物标记物特征时,所述组合提供(a)高特异性(例如,大于99%或更高,诸如大于99.5%)以最小化假阳性的数量,以及(b)对待诊断的疾病、病症或病状(例如,癌症或预后最有利的早期癌症)的高灵敏度(例如,大于40%)。在一些实施方案中,疾病、病症或病状(例如,癌症)的靶生物标记物特征包含至少一个细胞外囊泡相关膜结合多肽(例如,存在于与疾病、病症或病状(例如,癌症)相关的细胞外囊泡中的表面多肽)和选自由以下组成的组的至少一个靶生物标记物:一个或多个表面蛋白生物标记物、一个或多个囊泡内蛋白生物标记物和一个或多个囊泡内rna生物标记物,使得当使用本文提供的技术(例
如,本文所述的靶实体检测系统)检测到这样的一个或多个细胞外囊泡相关膜结合多肽和这样的一个或多个靶生物标记物的组合呈现疾病、病症或病状(例如,癌症)的靶生物标记物特征时,所述组合提供至少10%或更高(包括例如至少15%或以上)的阳性预测值(ppv)。
[0252]
在一些实施方案中,疾病、病症或病状(例如,癌症)的靶生物标记物特征包含至少一个或多个(例如,1、2、3、4、5、6、7、8个或更多个)细胞外囊泡相关膜结合多肽和至少一个或多个(例如,1、2、3、4、5、6、7、8个或更多个)表面蛋白生物标记物,其中一个或多个细胞外囊泡相关膜结合多肽和一个或多个表面蛋白生物标记物是不同的。
[0253]
在一些实施方案中,疾病、病症或病状(例如,癌症)的靶生物标记物特征包含至少一个或多个(例如,1、2、3、4、5、6、7、8个或更多个)细胞外囊泡相关膜结合多肽(例如,本文所述的那些)和至少一个或多个(例如,1、2、3、4、5、6、7、8个或更多个)囊泡内蛋白生物标记物(例如,本文所述的那些)。在一些此类实施方案中,一个或多个细胞外囊泡相关膜结合多肽和一个或多个囊泡内蛋白生物标记物可由相同的基因编码,而前者在细胞外囊泡的膜中表达,并且后者在细胞外囊泡内表达。在一些此类实施方案中,一个或多个细胞外囊泡相关膜结合多肽和一个或多个囊泡内蛋白生物标记物可由不同的基因编码。
[0254]
在一些实施方案中,疾病、病症或病状(例如,癌症)的靶生物标记物特征包含至少一个或多个(例如,1、2、3、4、5、6、7、8个或更多个)细胞外囊泡相关膜结合多肽和至少一个或多个(例如,1、2、3、4、5、6、7、8个或更多个)囊泡内rna(例如,mrna)生物标记物。在一些此类实施方案中,一个或多个细胞外囊泡相关膜结合多肽和一个或多个囊泡内rna(例如,mrna)生物标记物可由相同的基因编码。在一些此类实施方案中,一个或多个细胞外囊泡相关膜结合多肽和一个或多个囊泡内rna(例如,mrna)生物标记物可由不同的基因编码。
[0255]
iv检测一个或多个靶生物标记物特征的示例性方法
[0256]
一般而言,本公开提供了在包含来自有需要的受试者的细胞外囊泡的血液衍生样品中分析和/或评估靶生物标记物特征所根据的技术;在一些实施方案中,基于此类分析和/或评估做出诊断或治疗决定。阅读本公开的本领域普通技术人员将认识到,本文所述的检测方法的各种组合可用于检测样品中的一个或多个靶生物标记物特征。例如,在一些实施方案中,批量ev分析和单个ev谱分析的组合可用于检测样品中的一个或多个靶生物标记物特征。在一些实施方案中,涉及靶实体检测系统(例如,如本文所述和/或使用的那些)的单个ev谱分析可与用于检测靶生物标记物特征的一个或多个基于蛋白质和/或核酸的生物标记物的一种或多种方法(例如,如本文所述)组合使用。在一些实施方案中,可将包含细胞外囊泡的样品分成多个等分试样,这可允许使用本文所述和/或使用的不同检测技术在单个样品中检测靶生物标记物特征的多个(例如,至少两个或更多个)生物标记物。
[0257]
例如,在一些实施方案中,检测靶生物标记物特征的一个或多个靶生物标记物的方法可包括用于检测作为蛋白质的靶生物标记物特征的一个或多个标记物的方法。检测一个或多个标记物的示例性基于蛋白质的方法包括但不限于邻近连接测定、质谱(ms)和免疫测定,诸如免疫沉淀;蛋白质印迹;elisa;免疫组化;免疫细胞化学;流式细胞术;和免疫pcr。在一些实施方案中,免疫测定可为化学发光免疫测定。在一些实施方案中,免疫测定可为高通量和/或自动化免疫测定平台。
[0258]
在一些实施方案中,在样品中检测作为蛋白质的靶生物标记物特征的一个或多个标记物的方法包括使样品与针对这样的一个或多个关注的标记物的一种或多种抗体剂接
触。在一些实施方案中,此类方法还包括使此种样品与一个或多个检测标记接触。在一些实施方案中,抗体剂用一个或多个检测标记进行标记。
[0259]
在一些实施方案中,检测关注的生物标记物和针对关注的生物标记物的抗体剂之间的结合包括确定一种或多种检测剂的吸亮度值或发射值。例如,吸亮度值或发射值指示由细胞外囊泡表达的关注的生物标记物的量和/或浓度(例如,较高的吸亮度指示由细胞外囊泡表达的关注的生物标记物的水平较高)。在一些实施方案中,检测剂的吸亮度值或发射值高于阈值。在一些实施方案中,检测剂的吸亮度值或发射值为阈值的至少1.3倍、至少1.4倍、至少1.5倍、至少1.6倍、至少1.7倍、至少1.8倍、至少1.9倍、至少2.0倍、至少2.5倍、至少3.0倍、至少3.5倍或更大。在一些实施方案中,阈值是在对照组或参考组(例如,在癌症检测的背景下为健康受试者或非癌症受试者)群体中确定的。
[0260]
在一些实施方案中,检测靶生物标记物特征的一个或多个靶生物标记物的方法可包括用于检测作为核酸的一个或多个标记物的方法。检测一个或多个标记物的示例性基于核酸的方法包括但不限于进行核酸扩增方法,诸如聚合酶链反应(pcr)、逆转录聚合酶链反应(rt
‑
pcr)、转录介导的扩增(tma)、连接酶链反应(lcr)、链置换扩增(sda)和基于核酸序列的扩增(nasba)。在一些实施方案中,检测一个或多个标记物的基于核酸的方法包括检测一个或多个核酸探针与编码关注的生物标记物的一个或多个核苷酸之间的杂交。在一些实施方案中,核酸探针各自与编码关注的生物标记物的一个或多个核苷酸中的一个的至少一部分互补。在一些实施方案中,编码关注的生物标记物的核苷酸包括dna(例如,cdna)。在一些实施方案中,编码关注的生物标记物的核苷酸包括rna(例如,mrna)。
[0261]
在一些实施方案中,检测靶生物标记物特征的一个或多个靶生物标记物的方法可涉及邻近连接免疫定量聚合酶链反应(pliq
‑
pcr)。与其他技术相比,pliq
‑
pcr在分析ev方面可具有某些优点。例如,pliq
‑
pcr的灵敏度可比其他标准免疫测定法(诸如elisa)高三个数量级(darmanis等人,2010)。在一些实施方案中,pliq
‑
pcr反应可被设计成具有超低lod,这使得能够检测到微量水平的肿瘤来源的ev,例如低至1000ev/ml。
[0262]
在一些实施方案中,用于检测靶生物标记物特征的一个或多个靶生物标记物的方法可涉及用于检测ev的其他技术,包括例如纳米等离子体外泌体(nplex)传感器(im等人,2014)和集成磁电化学外泌体(imex)传感器(jeong等人,2016年),它们分别报告了约103ev和约104ev的lod(shao等人,2018)。
[0263]
在一些实施方案中,用于检测细胞外囊泡中靶生物标记物特征的一个或多个靶生物标记物的方法可涉及批量ev样品分析。
[0264]
在一些实施方案中,用于检测细胞外囊泡中靶生物标记物特征的一个或多个靶生物标记物的方法可基于分析单个ev(例如,单个ev谱测定),这在下面的标题为“所提供的用于分析个体细胞外囊泡(ev)的方法”的部分中进一步讨论。
[0265]
在一些实施方案中,在检测根据本公开的靶生物标记物特征的一个或多个靶生物标记物之前,样品中的细胞外囊泡可捕获或固定在固体基底上。在一些实施方案中,细胞外囊泡可通过非特异性相互作用(包括例如吸附)捕获在固体基底表面上。在一些实施方案中,细胞外囊泡可选择性地捕获在固体基底表面上。例如,在一些实施方案中,固体基底表面可涂覆有特异性结合细胞外囊泡的剂(例如,特异性靶向例如与疾病、病症或病状(例如,癌症)相关的细胞外囊泡的抗体剂)。在一些实施方案中,固体基底表面可涂覆有亲和结合
对的成员,并且待捕获的关注的实体(例如,细胞外囊泡)可缀合至亲和结合对的互补成员。在一些实施方案中,示例性亲和结合对包括例如但不限于生物素和抗生物素蛋白样分子,诸如链霉亲和素。如本领域技术人员将理解的,其他适当的亲和结合对也可用于促进将关注的实体捕获到固体基底表面上。在一些实施方案中,关注的实体可通过施加电流而捕获到固体基底表面上,例如,如描述于ibsen等人acs nano.,11:6641
‑
6651(2017)和lewis等人acs nano.,12:3311
‑
3320(2018),两者都描述了使用交流电动微阵列芯片装置从未稀释的人血液或血浆样品中分离细胞外囊泡。
[0266]
固体基底可以适合于捕获细胞外囊泡并且不干扰下游处理、加工和/或检测的形式提供。例如,在一些实施方案中,固体基底可以是或包含珠(例如,磁珠)。在一些实施方案中,固体基底可以是或包含表面。例如,在一些实施方案中,此种表面可为测定室(包括例如管、孔、微孔、板、过滤器、膜、基质等)的捕获表面。因此,在一些实施方案中,本文所述的方法包括在检测样品中提供的生物标记物之前,将细胞外囊泡捕获或固定到固体基底上。
[0267]
在一些实施方案中,在将细胞外囊泡捕获到固体基底表面上之前,可处理样品,以例如去除不需要的实体,诸如细胞碎片或细胞。例如,在一些实施方案中,可对此种样品进行离心,以例如去除细胞碎片、细胞和/或其他颗粒。另外或替代地,在一些实施方案中,可对此种样品进行基于尺寸排阻的纯化或过滤。各种基于尺寸排阻的纯化或过滤是本领域已知的,并且本领域技术人员将理解,在一些情况下,可基于特定分子量或粒径截止值对样品进行离心柱纯化。本领域技术人员还将理解,可例如基于细胞外囊泡的大小来选择用于纯化目的的适当分子量或粒径截止值。例如,在一些实施方案中,尺寸排阻分离方法可应用于包含细胞外囊泡的样品以分离具有特定尺寸(例如,大于30nm且不超过1000nm或大于70nm且不超过200nm)的细胞外囊泡的一部分。通常,细胞外囊泡的直径可在30纳米至几微米的范围内。参见例如,chuo等人,“imaging extracellular vesicles:current and emerging methods”journal of biomedical sciences 25:91(2018),其提供不同细胞外囊泡(ev)亚型的大小信息:迁移小体(0.5μm至3μm)、微囊泡(0.1μm至1μm)、原癌小体(1μm至10μm)、外泌颗粒(exomere)(<50nm)、小外泌体(60nm至80nm)和大外泌体(90nm至120nm)。在一些实施方案中,尺寸排阻分离方法可应用于包含细胞外囊泡的样品以分离一个或多个特定ev亚型。
[0268]
在一些实施方案中,可在检测疾病、病症或病状(例如,癌症)的靶生物标记物特征的一个或多个靶生物标记物之前处理样品中的细胞外囊泡。可进行不同的样品处理和/或制备以例如稳定待检测的细胞外囊泡中的靶标(例如,靶生物标记物),和/或促进靶标(例如,囊泡内蛋白质和/或rna,诸如mrna)暴露于检测探针(例如,如本文所述),和/或减少非特异性结合。此类样品处理和/或制备的实例是本领域已知的,并且包括但不限于交联分子靶标(例如,固定)、使生物实体(例如,细胞或细胞外囊泡)透化和/或封闭非特异性结合位点。
[0269]
在一个方面,本公开提供了一种用于检测疾病、病症或病状(例如像癌症)的靶生物标记物特征是否存在于来自有需要的受试者的生物样品中的方法,所述生物样品在一些实施方案可为包含细胞外囊泡的血液来源的样品。在一些实施方案中,此种方法包括(a)在生物样品诸如来自受试者的血液来源的样品(例如,血浆样品)中检测表达疾病、病症或病状(例如像癌症)的靶生物标记物特征的关注的生物实体(包括例如细胞外囊泡);以及(b)将指示生物样品(例如,血液来源的样品)中表达靶生物标记物特征的关注的生物实体(例
如,细胞外囊泡)的水平的样品信息与包括参考阈值水平的参考信息进行比较。在一些实施方案中,参考阈值水平对应于在来自参考受试者(例如,非癌症受试者)群体的可比样品中表达此种靶生物标记物特征的关注的生物实体(例如,细胞外囊泡)的水平。在一些实施方案中,示例性非癌症受试者包括健康受试者(例如,指定年龄范围的健康受试者,例如像20岁至30岁、或30岁至40岁、或40岁至50岁、或50岁至60岁、或60岁至70岁、或大于70岁或更大)、患有非癌症相关健康疾病、病症或病状的受试者(包括例如具有炎症性肠病或病症的症状的受试者)、患有良性肿瘤或肿块的受试者及其组合。
[0270]
在一些实施方案中,当样品示出相对于参考阈值水平升高水平的表达靶生物标记物特征的细胞外囊泡(例如,本文所述的那些)时,确定样品具有表达靶生物标记物特征的细胞外囊泡(例如,本文所述的那些)。在一些实施方案中,如果与参考阈值水平相比,样品的水平为至少30%或更高,包括例如至少40%、至少50%、至少60%、至少70%、至少80%、至少90%、至少95%或更高,则确定样品对表达靶生物标记物特征的细胞外囊泡呈阳性。在一些实施方案中,如果与参考阈值水平相比,样品的水平为至少2倍或更高,包括例如至少3倍、至少4倍、至少5倍、至少6倍、至少7倍、至少8倍、至少9倍、至少10倍、至少50倍、至少100倍、至少250倍、至少500倍、至少750倍、至少1000倍、至少2500倍、至少5000倍或更高,则确定样品对表达靶生物标记物特征的细胞外囊泡呈阳性。
[0271]
在一些实施方案中,二元分类系统可用于确定样品是否对表达靶生物标记物特征的细胞外囊泡呈阳性。例如,在一些实施方案中,如果样品的水平处于或高于参考阈值水平,例如截止值,则确定样品对表达靶生物标记物特征的细胞外囊泡呈阳性。在一些实施方案中,此种参考阈值水平(例如,截止值)可基于健康受试者(例如,指定年龄范围的)的对数正态分布和实现关注的特异性(例如,至少95%或更高的特异性[包括例如至少96%、至少97%、至少98%、至少99%或更高的特异性],诸如在一些实施方案中为至少99.8%的特异性)所需的标准偏差(sd)的数量的选择(例如,至少1.5sd、至少1.6sd、至少1.7sd、至少1.8sd、至少1.9sd、至少2sd、至少2.1sd、至少2.2sd、至少2.3sd、至少2.4sd、至少2.5sd、至少2.6sd、至少2.7sd、至少2.8sd、至少2.9sd、至少3sd、至少3.1sd、至少3.2sd、至少3.3sd、至少3.4sd、至少3.5sd、至少3.6sd或更高的sd)来确定,例如,基于疾病、病症或病状(诸如某种癌症)的患病率。
[0272]
本公开尤其还提供了用于确定受试者是否患有或易患疾病、病症或病状(例如像癌症)的技术。例如,在一些实施方案中,当来自有需要的受试者的血液来源的样品示出表达靶生物标记物特征的细胞外囊泡的水平处于或高于参考阈值水平(例如,截止值)时,则将受试者分类为患有或易患疾病、病症或病状,例如像癌症。在一些此类实施方案中,参考阈值水平(例如,截止值)可基于健康受试者(例如,指定年龄范围的)的对数正态分布和实现关注的特异性(例如,至少95%或更高的特异性[包括例如至少96%、至少97%、至少98%、至少99%或更高的特异性],诸如在一些实施方案中为至少99.8%的特异性)所需的标准偏差(sd)的数量的选择(例如,至少1.5sd、至少1.6sd、至少1.7sd、至少1.8sd、至少1.9sd、至少2sd、至少2.1sd、至少2.2sd、至少2.3sd、至少2.4sd、至少2.5sd、至少2.6sd、至少2.7sd、至少2.8sd、至少2.9sd、至少3sd、至少3.1sd、至少3.2sd、至少3.3sd、至少3.4sd、至少3.5sd、至少3.6sd或更高的sd)来确定,例如,基于疾病、病症或病状(诸如某种癌症)的患病率。在一些实施方案中,当来自有需要的受试者的血液来源的样品示出相对于参考阈
值水平升高水平的表达靶生物标记物特征的细胞外囊泡时,则将受试者分类为患有或易患疾病、病症或病状,例如像癌症。在一些实施方案中,当有需要的受试者的血液来源的样品示出与参考阈值水平相比,表达靶生物标记物特征的细胞外囊泡的水平为至少30%或更高,包括例如至少40%、至少50%、至少60%、至少70%、至少80%、至少90%、至少95%或更高时,将此种受试者归类为患有或易患疾病、病症或病状,例如像癌症。在一些实施方案中,当有需要的受试者的血液来源的样品示出与参考阈值水平相比,表达靶生物标记物特征的细胞外囊泡的水平为至少2倍或更高,包括例如至少3倍、至少4倍、至少5倍、至少6倍、至少7倍、至少8倍、至少9倍、至少10倍、至少20倍、至少30倍、至少40倍、至少50倍、至少60倍、至少70倍、至少80倍、至少90倍、至少100倍、至少250倍、至少500倍、至少750倍、至少1000倍或更高时,将此种受试者归类为患有或易患疾病、病症或病状,例如像癌症。当来自有需要的受试者的血液来源的样品示出与参考阈值水平相当的水平(例如,在10%至20%内)时,则将受试者归类为不太可能患有或不太可能易患疾病、病症或病状,例如像癌症。在一些此类实施方案中,参考阈值水平对应于在来自参考受试者(例如,非癌症受试者)群体的可比样品中表达靶生物标记物特征的细胞外囊泡的水平。在一些实施方案中,示例性非癌症受试者包括健康受试者(例如,指定年龄范围的健康受试者,例如像低于20岁(例如,包括婴儿)、20岁至30岁、或30岁至40岁、或40岁至50岁、或50岁至60岁、或60岁至70岁、或大于70岁或更大)、患有非癌症相关健康疾病、病症或病状的受试者(包括例如具有炎症性肠病或病症的症状的受试者)、患有良性肿瘤或肿块的受试者及其组合。
[0273]
v所提供的用于分析个体细胞外囊泡(ev)的方法
[0274]
在一些实施方案中,用于分析个体细胞外囊泡的测定(例如,单一ev谱测定)可用于检测一种或多种疾病、病症或病状(例如,癌症)的一个或多个靶生物标记物特征。例如,在一些实施方案中,此种测定可涉及(i)通过靶向疾病、病症或病状(例如,癌症)的靶生物标记物特征的一个或多个标记物的捕获测定和(ii)此种靶生物标记物特征的至少一个或多个另外提供的标记物的一种或多种检测测定,其中此种捕获测定在此种检测测定之前进行。
[0275]
在一些实施方案中,进行捕获测定以从有需要的受试者的血液或血液来源的样品(例如,血浆样品)中选择性地捕获细胞外囊泡。在一些实施方案中,进行捕获测定以选择性捕获具有特定大小范围和/或一个或多个特定特征的细胞外囊泡,例如与疾病、病症或病状(例如,癌症)相关的细胞外囊泡。在一些此类实施方案中,在捕获测定之前,可对血液或血液来源的样品进行预处理以去除非细胞外囊泡,包括例如但不限于可溶性蛋白质和干扰实体,例如像细胞碎片。例如,在一些实施方案中,使用尺寸排阻色谱法从受试者的血液或血液来源的样品中纯化细胞外囊泡。在一些此类实施方案中,可使用尺寸排阻色谱法从血液或血液来源的样品中直接纯化细胞外囊泡,这在一些实施方案中可去除至少90%或更高(包括例如至少93%、95%、97%、99%或更高)的可溶性蛋白质和其他干扰剂,例如像细胞碎片。
[0276]
在一些实施方案中,捕获测定包括使血液或血液来源的样品与至少一种捕获剂接触的步骤,所述捕获剂包含与疾病、病症或病状(例如,癌症)的靶生物标记物特征的至少一个生物标记物结合的靶捕获部分。在一些实施方案中,可多路复用捕获测定,其包括使血液或血液来源的样品与一组捕获剂接触的步骤,每种捕获剂包含与疾病、病症或病状(例如,
癌症)的靶生物标记物特征的不同生物标记物结合的靶捕获部分。在一些实施方案中,靶捕获部分针对细胞外囊泡相关膜结合多肽。
[0277]
在一些实施方案中,此种靶捕获部分可固定在固体基底上。因此,在一些实施方案中,用于捕获测定的捕获剂是或包含固体基底,所述固体基底包含至少一个或多个(例如,1、2、3、4、5个或更多个)与其缀合的靶捕获部分,每个靶捕获部分针对细胞外囊泡相关膜结合多肽(例如,如本文所述和/或使用的那些)。固体基底可以适合于捕获细胞外囊泡并且不干扰下游处理、加工和/或检测的形式提供。例如,在一些实施方案中,固体基底可以是或包含珠(例如,磁珠)。在一些实施方案中,固体基底可以是或包含表面。例如,在一些实施方案中,此种表面可为测定室(包括例如管、孔、微孔、板、过滤器、膜、基质等)的捕获表面。在一些实施方案中,捕获剂是或包含磁珠,所述磁珠包含与其缀合的靶捕获部分。
[0278]
在一些实施方案中,进行检测测定以检测通过捕获测定捕获的细胞外囊泡(例如,如上所述)中靶生物标记物特征的一个或多个生物标记物(例如,与捕获测定中靶向的生物标记物不同的生物标记物)。在一些实施方案中,检测测定可包括免疫pcr。在一些实施方案中,免疫pcr可涉及靶向靶生物标记物特征的单个生物标记物的至少一个探针。在一些实施方案中,免疫pcr可涉及针对靶生物标记物特征的相同生物标记物的不同表位的多个(例如,至少两个、至少三个、至少四个或更多个)探针。在一些实施方案中,免疫pcr可涉及多个(例如,至少两个、至少三个、至少四个或更多个)探针,每个探针针对靶生物标记物特征的不同生物标记物。
[0279]
在一些实施方案中,检测测定可包括逆转录聚合酶链反应(rt
‑
pcr)。在一些实施方案中,rt
‑
pcr可涉及靶向靶生物标记物特征的单个生物标记物的至少一个引物/探针组。在一些实施方案中,rt
‑
pcr可涉及多个(例如,至少两个、至少三个、至少四个或更多个)引物/探针组,每个组针对靶生物标记物特征的不同生物标记物。
[0280]
在一些实施方案中,检测测定可包括邻近连接免疫定量聚合酶链反应(pliq
‑
pcr),以例如确定细胞外囊泡(例如,表达至少一种细胞外囊泡相关膜结合多肽的捕获的细胞外囊泡)内靶生物标记物特征的生物标记物蛋白的共定位。
[0281]
在一些实施方案中,检测测定采用本文所述的靶实体检测系统(例如,如标题为“所提供的靶实体检测系统”的部分中所述),其部分地基于个体细胞外囊泡中的靶生物标记物特征的相互作用和/或共定位。例如,此种靶实体检测系统可在一些实施方案中,在单个实体水平上检测样品(例如,生物、环境或其他样品)中包含至少一个或多个(例如,至少两个或更多个)靶标(例如,分子靶标)的关注的实体(例如,关注的生物或化学实体,诸如细胞外囊泡或分析物)。阅读本公开的本领域技术人员将认识到,所提供的靶实体检测系统可用于多种应用和/或目的,包括例如用于检测疾病、病症或病状(例如,癌症)。例如,在一些实施方案中,所提供的靶实体检测系统可用于医学应用和/或目的。在一些实施方案中,所提供的靶实体检测系统可用于筛选(例如,定期筛选)个体(例如,无症状个体)的疾病或病状(例如,癌症)。在一些实施方案中,所提供的靶实体检测系统可用于筛选(例如,定期筛选)个体(例如,无症状个体)的不同类型的癌症。在一些实施方案中,所提供的靶实体检测系统即使在应用于包含无症状个体或由无症状个体组成的人群时也是有效的(例如,由于足够高的灵敏度和/或低的假阳性和/或假阴性结果率)。在一些实施方案中,所提供的靶实体检测系统可用作与疾病治疗(例如,治疗疾病、病症或病状,例如像癌症)结合的伴随诊
断。
[0282]
在一些实施方案中,可进行多个(例如,至少两个或更多个)检测测定以检测细胞外囊泡(例如,通过捕获测定捕获的细胞外囊泡(例如,如上所述))中一个或多个靶生物标记物特征的多个生物标记物(例如,至少两个或更多个)(例如,与捕获测定中靶向的生物标记物不同的生物标记物)。在一些实施方案中,多个检测测定可包括(i)所提供的靶实体检测系统或本文所述的系统(例如,如标题为“所提供的靶实体检测系统”的部分中所述);以及(ii)免疫pcr。在一些实施方案中,多个检测测定可包括(i)所提供的靶实体检测系统或本文所述的系统(例如,如标题为“所提供的靶实体检测系统”的部分中所述);以及(ii)rt
‑
pcr。
[0283]
vi.用途
[0284]
在一些实施方案中,本文提供的技术可应用于包含待测定的生物实体的关注的样品。在一些实施方案中,本文所述的技术可用于筛选样品存在或不存在靶标的组合(例如,一组)。因此,所提供的技术可用于各种研究和/或医疗应用。此类应用的实例包括但不限于研究复合物中分子(例如,蛋白质、转录因子和/或核酸分子)的相互作用、筛选患者的特定疾病或病状、监测疾病或病状的复发和/或进展、为患有疾病或病状的患者选择疗法和/或评估和/或监测施用于有需要的受试者的治疗的功效。可通过本文所述的技术检测或筛选的疾病的实例包括但不限于自身免疫性疾病、炎症性疾病、骨疾病、代谢疾病、神经和神经退行性疾病、癌症、心血管疾病、过敏和哮喘、阿尔茨海默氏病和激素相关疾病。
[0285]
在一些实施方案中,可使用如本文所述的检测和/或测定方法在包含生物实体(包括例如细胞、循环肿瘤细胞、无细胞dna、细胞外囊泡等)的样品中检测疾病、病症或病状(例如,癌症)的一个或多个靶生物标记物特征。在一些实施方案中,可使用如本文所述的检测和/或测定方法在包含细胞外囊泡的样品中检测疾病、病症或病状(例如,癌症)的一个或多个靶生物标记物特征。
[0286]
在一些实施方案中,样品可以是或包含生物样品。在一些实施方案中,生物样品可来源于需要此种测定的受试者(例如,人受试者)的血液或血液来源的样品。在一些实施方案中,生物样品可以是或包含来自需要此种测定的受试者(例如,人受试者)的原始样品(例如,组织或肿瘤样品)。在一些实施方案中,可对生物样品进行处理,以将一个或多个关注的实体(例如,生物实体)与关注的非靶实体分开和/或使一个或多个关注的实体(例如,生物实体)富集。在一些实施方案中,存在于样品中的关注的实体可以是或包含生物实体,例如细胞或细胞外囊泡(例如,外泌体)。在一些实施方案中,可对此种生物实体(例如,细胞外囊泡)进行处理或将其与化学试剂接触,以例如稳定和/或交联生物实体中待测定的靶标(例如,所提供的靶生物标记物)和/或减少与检测探针的非特异性结合。在一些实施方案中,生物实体是或包含细胞,可任选地用例如化学试剂对其进行处理,以用于稳定和/或交联靶标(例如,分子靶标)和/或用于减少非特异性结合。在一些实施方案中,生物实体是或包含细胞外囊泡(例如,外泌体),可任选地用例如化学试剂对其进行处理,以用于稳定和/或交联靶标(例如,分子靶标)和/或用于减少非特异性结合。
[0287]
在一些实施方案中,本文提供的技术可用于管理患者护理,以用于例如一个或多个个体受试者和/或整个受试者群体。仅以举例的方式,在一些实施方案中,所提供的技术可用于筛选,例如,可定期进行,诸如每年、每半年、每两年或以本领域技术人员认为适当的
一些其他频率进行。在一些实施方案中,此种筛选可为临时动机的或偶然动机的。例如,在一些实施方案中,所提供的技术可用于临时动机地筛选大于某个(例如,超过某个年龄(例如,超过20、25、30、35、40、45、50、55、60、65、70、75、80岁或以上))的一个或多个个体受试者或整个受试者(例如,无症状受试者)群体。如本领域技术人员将理解的,在一些实施方案中,可基于例如但不限于疾病、病症或病状(例如,癌症)的患病率来确定筛选年龄和/或频率。在一些实施方案中,所提供的技术可用于临时动机地筛选可能经历了促使筛选特定疾病、病症或病状(例如,癌症)的事故或事件的个体受试者。例如,在一些实施方案中,与确定疾病、病症或病状(例如,癌症)或其易患性的一个或多个指标相关的偶然动机可以是或包括例如,基于他们的家族史的事故(例如,近亲诸如血缘亲属先前被诊断为此种疾病、病症或病状诸如癌症);鉴定疾病、病症或病状(例如,癌症)的一个或多个风险因素;和/或来自基因测试(例如,基因组测序)和/或成像诊断测试(例如,超声、计算机断层扫描(ct)和/或磁共振成像(mri)扫描)的先前偶然发现;发展具有特定疾病、病症或病状特征的一种或多种体征或症状(例如,在癌症的情况下,可能指示肺癌的持续咳嗽;可能指示乳腺癌的乳腺组织中的肿块;可能指示gi癌的胃肠(gi)道出血;可能指示卵巢癌的女性经期异常出血等)和/或如本领域技术人员将理解的其他事故或事件。
[0288]
在一些实施方案中,所提供的用于管理患者护理的技术可通知治疗和/或支付(例如,治疗的报销)决定和/或行动。例如,在一些实施方案中,所提供的技术可提供对个体受试者是否具有疾病、病症或病状(例如,癌症)的风险、发病或复发的一个或多个指标的确定,从而通知医师和/或患者何时根据此类发现提供/接受治疗性或预防性建议和/或何时开始此种治疗。在一些实施方案中,此类个体受试者可为无症状受试者,可以定期频率(例如,每年、每半年、每两年或本领域技术人员认为适当的其他频率)对其进行暂时动机或偶然动机的筛选。
[0289]
另外或替代地,在一些实施方案中,所提供的技术可例如基于特定反应性生物标记物(例如,癌症反应性生物标记物)的发现来通知医师和/或患者治疗选择。在一些实施方案中,所提供的技术可例如基于与疾病相关的一个或多个分子靶标水平的变化的发现来提供对个体受试者是否对当前治疗有反应的确定,从而通知医师和/或患者此类治疗的功效和/或根据此类发现保持或改变治疗的决定。在一些实施方案中,所提供的技术可例如基于预测推荐的治疗对个体受试者的治疗效果的分子靶标(例如,疾病、病症或病状的靶生物标记物特征)的发现来提供对个体受试者是否可能对推荐的治疗有反应的确定,从而通知医师和/或患者此类治疗的潜在功效和/或根据此类发现实施或改变治疗的决定。
[0290]
在一些实施方案中,所提供的技术可通知关于健康保险提供者是否报销(或不报销)例如以下的决定:(1)筛选本身(例如,报销仅可用于周期性/定期筛选或仅可用于临时和/或偶然动机的筛选);和/或(2)根据所提供的技术的发现开始、保持和/或改变治疗。例如,在一些实施方案中,本公开提供了与以下有关的方法:(a)接收采用所提供的技术的筛选结果,并且还接收对筛选和/或特定治疗方案的报销请求;(b)如果根据适当的时间表(例如基于筛选年龄,诸如超过某个年龄,例如超过20岁、25岁、30岁、35岁、40岁、45岁、50岁、55岁、60岁、65岁、70岁、75岁、80岁或以上,和/或筛选频率,例如像每3个月、每6个月、每年、每2年、每3年或以一些其他频率)或对相关事故的反应对受试者进行筛选,则批准报销筛选;和/或如果治疗方案根据接收的筛选结果代表适当治疗,则批准治疗的报销方案;以及任选
地(c)实现报销或提供报销被拒绝的通知。在一些实施方案中,如果接收的筛选结果检测到代表相关治疗方案的批准的生物标记物(例如,如处方信息标签和/或通过批准的伴随诊断所述)的生物标记物,则根据接收的筛选结果,治疗方案是合适的。
[0291]
替代地或另外,本公开设想允许或促进如本文所述的筛选结果(例如,如根据本公开产生的)和/或报销决定的报告和/或处理的报告系统(例如,通过一个或多个适当的电子装置和/或一个或多个通信系统实施)。各种报告系统是本领域已知的;本领域技术人员将非常熟悉各种此类实施方案,并且将能够容易地选择适合实现的实施方案。
[0292]
示例性用途
[0293]
a.癌症发病或复发的检测
[0294]
本公开尤其认识到,基于批量样品而不是以单个生物实体(例如,个体细胞外囊泡)的分辨率对生物实体(例如,细胞外囊泡)中的单个癌症相关生物标记物或多个癌症相关生物标记物进行检测通常在确定从其获得生物实体的受试者是否可能患有或易患癌症方面不提供足够的特异性和/或灵敏度。本公开尤其提供了解决此类问题的技术,包括组合物和/或方法,包括例如通过具体要求用于检测的实体(例如,细胞外囊泡)以存在靶标的组合为特征。例如,在一些实施方案中,本文提供的技术可用于通过至少两个或更多个靶标的组合的存在来表征实体(例如,细胞外囊泡)。例如,在一些此类实施方案中,可涉及所提供的靶实体检测系统来检测至少两个或更多个靶标。替代地,在一些此类实施方案中,至少一个靶标可通过捕获测定(例如,如本文所述和/或使用的)检测,而至少一个其他靶标可通过检测测定(例如,涉及本文所述和/或使用的靶实体检测系统)检测。在特定实施方案中,本公开教导要求此类实体(例如,细胞外囊泡)以存在(例如,通过表达)对癌症具有特异性的分子靶标(即,相关癌症(例如,癌症)的“靶生物标记物特征”)的组合为特征的技术,而不包含靶向组合(例如,靶生物标记物特征)的生物实体(例如,细胞外囊泡)不会产生可检测的信号。因此,在一些实施方案中,本文提供的技术可用于检测受试者中癌症的风险、发病和/或复发。例如,在一些实施方案中,选择针对至少一个或多个靶标(包括例如至少2个、至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个、至少15个、至少20个或更多个靶标)的两个或更多个检测探针(例如,本文所述的那些)的组合以检测特定癌症或各种癌症。在一些实施方案中,可通过分析癌症患者活检和/或患者数据的群体或文库(例如,数十个、数百个、数千个、数万个、数十万个或更多个)鉴定此种预测性组合来确定针对用于检测一种或多种癌症的靶生物标记物特征的至少一个或多个靶标(包括例如至少2个、至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个、至少10个、至少15个、至少20个或更多个靶标)的检测探针(例如,本文所述的那些)的特定组合。在一些实施方案中,生物标记物的相关组合可为例如通过数据分析鉴定和/或表征的生物标记物。在一些实施方案中,例如,可通过机器学习和/或计算建模来分析一组不同的癌症相关数据(例如,在一些实施方案中,包括批量rna测序、单细胞rna(scrna)测序、质谱、组织学、翻译后修饰数据、体外和/或体内实验数据中的一个或多个)进行分析,以鉴定对癌症具有高度特异性的预测标记物的组合。在一些实施方案中,可基于对与癌症不同阶段相关的不同数据(例如,在一些实施方案中,包括批量rna测序、scrna测序、质谱、组织学、翻译后修饰数据、体外和/或体内实验数据)的比较和分析来在计算机中确定区分癌症阶段的预测标记物的组合。例如,在一些实施方案中,本文提供的技术可用于区分癌症受试者与非癌症受试者,包括例如
健康受试者、诊断为患有良性肿瘤或肿块的受试者以及患有非癌症相关疾病、病症和/或病状的受试者(例如,患有炎症性肠病或病症的受试者)。在一些实施方案中,本文提供的技术可用于癌症的早期检测,例如阶段i或阶段ii的癌症的检测。在一些实施方案中,本文提供的技术可用于将黑色素瘤阶段i、阶段ii、阶段iii和阶段iv与彼此和健康患者区分开来。在一些实施方案中,本文提供的技术可用于将肺腺癌阶段i、阶段ii、阶段iii和阶段iv与彼此和健康患者区分开来。在一些实施方案中,本文提供的技术可用于将结直肠癌阶段i、阶段ii、阶段iii和阶段iv与彼此和健康患者区分开来。在一些实施方案中,本文提供的技术可用于将卵巢癌阶段i、阶段ii、阶段iii和阶段iv与彼此和健康患者区分开来。在一些实施方案中,本文提供的技术可用于检测一种或多种癌症亚型。仅以举例的方式,在一些实施方案中,本文提供的技术可用于检测一种或多种卵巢癌亚型,包括例如高级别浆液性卵巢癌、子宫内膜样卵巢癌、透明细胞卵巢癌、低级别浆液性卵巢癌和/或粘液性卵巢癌。在一些实施方案中,本文提供的技术可用于筛选处于早期癌症的遗传或平均风险的受试者。
[0295]
在一些实施方案中,本文提供的技术可用于在单次测定中筛选受试者的特定癌症的风险、发病或复发。例如,在一些实施方案中,本文提供的技术可用于筛选受试者的乳腺癌的风险、发病或复发。在一些实施方案中,本文提供的技术可用于筛选受试者的肺癌(例如但不限于非小细胞肺癌)的风险、发病和/或复发。在一些实施方案中,本文提供的技术可用于筛选皮肤癌(例如但不限于黑色素瘤)的风险、发病和/或复发。在一些实施方案中,本文提供的技术可用于筛选受试者的卵巢癌的风险、发病或复发。在一些实施方案中,本文提供的技术可用于在单次测定中筛选受试者的特定癌症或多种(例如,至少2种、至少3种或更多种)癌症的风险或发病。例如,在一些实施方案中,本文提供的技术可用于在单次测定中筛选受试者的多种癌症,其中在一些实施方案中,待筛选的癌症可选自由以下组成的组:急性淋巴细胞性白血病、急性髓系白血病、胆管癌、膀胱癌、脑癌(包括例如胶质母细胞瘤)、乳腺癌、宫颈癌、慢性淋巴细胞性白血病、慢性髓系白血病、结直肠癌、子宫内膜癌、食道癌、胃肠癌、霍奇金淋巴瘤、肾癌、肝癌、肺癌、多发性骨髓瘤、非霍奇金淋巴瘤、卵巢癌、胰腺癌、前列腺癌、肉瘤、皮肤癌和胃癌。
[0296]
在一些实施方案中,可定期(例如,每年、每两年、每三年等)使用所提供的技术来筛选人受试者的癌症(例如,早期癌症)或癌症复发。在一些实施方案中,适用于此类筛选的人受试者可为婴儿、儿童、成人或老年人。在一些实施方案中,适用于此类筛选的人受试者的年龄可为约2岁至80岁、或约12岁至约70岁、或约18岁至约65岁。在一些实施方案中,适用于此类筛选的人受试者可为老年受试者,例如,65岁以上、70岁以上、至少75岁以上、至少80岁或以上。在一些实施方案中,适用于此类筛选的人受试者的年龄可为约50岁或以上。在一些实施方案中,适用于此类筛选的人受试者的年龄可为约50岁或以下。在一些实施方案中,适用于此类筛选的人受试者的年龄可为35岁以上。
[0297]
在一些实施方案中,适用于所提供的用于检测癌症的发病或复发的技术的受试者可为无症状人受试者和/或整个无症状人群。此种无症状受试者和/或无症状人群可为具有癌症家族史的一个或多个受试者(例如,具有一个或多个有癌症史的一级亲属的受试者)、先前接受过癌症治疗的受试者、在癌症治疗后有癌症复发风险的受试者、在癌症治疗后有所缓解的受试者和/或先前或定期筛选癌症的受试者,例如通过筛选至少一种癌症生物标记物的存在。替代地,在一些实施方案中,无症状受试者可为先前未经癌症筛选的受试者、
未诊断为癌症的受试者和/或先前未接受癌症治疗的受试者。在一些实施方案中,无症状受试者可为患有良性肿瘤或组织肿块的受试者。在一些实施方案中,无症状受试者可为易患癌症(例如,处于平均人群风险或具有癌症遗传风险)的受试者。
[0298]
在一些实施方案中,可基于一个或多个特征来选择适用于所提供的用于检测癌症的技术的受试者或受试者群体,所述一个或多个特征诸如年龄、种族、遗传史、病史、个人史(例如,吸烟、酒精、药物、致癌剂、饮食、肥胖、身体活动、光暴露、放射暴露、暴露于诸如病毒的感染性因子和/或职业危害)。例如,在一些实施方案中,适用于所提供的用于检测癌症的技术的受试者或受试者群体可为被确定在一个或多个癌症相关基因中具有一个或多个种系突变的受试者(例如,人受试者)或受试者群体,所述癌症相关基因包括例如但不限于brca1、brca2和tp53及其组合。
[0299]
在一些实施方案中,适用于所提供的用于检测癌症的技术的受试者或受试者群体可为诊断为具有经成像证实的组织肿块的受试者或受试者群体。
[0300]
在一些实施方案中,适用于所提供的用于检测癌症的技术的受试者或受试者群体可为在经历降低风险的手术干预之前处于癌症遗传风险的受试者或受试者群体。
[0301]
在一些实施方案中,适用于所提供的用于检测癌症的技术的受试者或受试者群体可为具有癌症的一个或多个非特异性症状的受试者或受试者群体。在一些实施方案中,癌症的示例性非特异性症状可包括例如但不限于咳嗽、吞咽困难、疲倦、食欲不振、腹痛、体重减轻等。
[0302]
在一些实施方案中,适用于所提供的用于检测癌症的技术的受试者或受试者群体可为亚洲人、非裔美国人、白种人、夏威夷原住民或其他太平洋岛民、西班牙裔或拉丁裔、美国印第安人或阿拉斯加原住民、非西班牙裔黑人或非西班牙裔白人受试者或受试者群体。在一些实施方案中,适用于所提供的用于检测癌症的技术的受试者或受试者群体可为任何种族和/或任何民族的受试者。
[0303]
在一些实施方案中,本文提供的技术可与其他诊断测定组合使用,包括例如但不限于(i)个体的年度体检,(ii)筛选血浆中与癌症相关的循环肿瘤dna和/或蛋白生物标记物的基因突变的基因测定;(iii)涉及免疫荧光染色以鉴定细胞表型和标记物表达的测定,之后扩增和通过下一代测序进行分析;以及(iv)种系和体细胞突变测定(例如,brca1和/或brca2),或涉及无细胞肿瘤dna、液体活检、血清蛋白和无细胞dna和/或循环肿瘤细胞的测定。
[0304]
b.治疗的选择(例如,癌症治疗)
[0305]
在一些实施方案中,所提供的技术可用于为患者(例如,患有或易患癌症的患者)选择适当的治疗。例如,本文提供的一些实施方案涉及用于治疗(例如,癌症和/或辅助治疗)的患者分类的伴随诊断测定,其包括使用本文提供的技术在患者样品(例如,来自患者(例如,癌症患者)的血液或血液来源的样品)中评估分层和/或响应性生物标记物的选定组合。基于此种测定结果,被确定更可能对治疗(例如,癌症治疗和/或辅助治疗)作出反应的患者可施用此种治疗,或被确定对特定的此类治疗无反应的患者可施用不同的疗法。
[0306]
c.治疗功效(例如,癌症治疗功效)的评估
[0307]
在一些实施方案中,本文提供的技术可用于监测和/或评估施用于患者(例如,癌症患者)的疗法的功效。例如,可在第一时间点从治疗(例如,抗癌治疗)之前或正在接受所
述治疗的患者(例如,癌症患者)收集血液或血液来源的样品,以检测或测量对患者的疾病、病症或病状具有特异性的生物标记物的组合。在一些实施方案中,可在第一时间点从抗癌治疗之前或正在接受抗癌治疗的癌症患者收集血液或血液来源的样品以检测或测量肿瘤负荷,例如通过检测包含对癌症检测具有特异性的生物标记物的选定组合的细胞外囊泡的存在或量。在一段时间的治疗后,可从同一患者身上收集第二血液或血液来源的样品,以检测这样的一个或多个疾病特异性生物标记物的变化。例如,在一些此类实施方案中,可在治疗一段时间后从同一癌症患者收集第二血液或血液来源的样品以检测肿瘤负荷的变化,例如通过检测包含对癌症检测具有特异性的生物标记物的选定组合的不存在或量的减少。通过在治疗过程中监测疾病特异性生物标记物和/或肿瘤负荷的水平和/或变化,可采取适当的行动过程,例如增加或减少治疗剂的剂量,和/或施用不同的治疗剂。
[0308]
vii.试剂盒
[0309]
还提供了可用于实践如上所述的技术的试剂盒。在一些实施方案中,试剂盒包含多个检测探针(例如,如本文所述和/或使用的)。在一些实施方案中,所提供的试剂盒可包含两个或更多个(例如,3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个或更多个)检测探针。在一些实施方案中,单独的检测探针可针对不同的靶标。在一些实施方案中,两个或更多个单独的检测探针可针对相同的靶标。在一些实施方案中,所提供的试剂盒包含针对不同靶标的两个或更多个不同的检测探针,并且任选地可包括也针对另一检测探针所针对的靶标的至少一个另外的检测探针。在一些实施方案中,所提供的试剂盒包含多个检测探针子集,其中每个子集包含针对相同的靶标的两个或更多个检测探针。在一些实施方案中,多个检测探针可作为容器中的混合物提供。在一些实施方案中,多个检测探针子集可作为单独容器中的单独混合物提供。在一些实施方案中,每个检测探针在单独的容器中单独地提供。
[0310]
在一些实施方案中,用于癌症检测的试剂盒包含:(a)捕获剂,其包含针对细胞外囊泡相关膜结合多肽的靶捕获部分;以及(b)一组检测探针,所述组包含至少两个检测探针,每个检测探针针对癌症的靶生物标记物特征的靶生物标记物,其中检测探针各自包含:(i)靶结合部分,其针对癌症的靶生物标记物特征的靶生物标记物;以及(ii)偶联至靶结合部分的寡核苷酸结构域,寡核苷酸结构域包含双链部分和从寡核苷酸结构域的一端延伸的单链悬突部分,其中所述至少两个检测探针的单链悬突部分的特征在于它们在所述至少两个检测探针结合至相同的细胞外囊泡时可彼此杂交。在这些实施方案中,癌症的此种靶生物标记物特征包含:至少一种细胞外囊泡相关膜结合多肽和选自由以下组成的组的至少一个靶生物标记物:表面蛋白生物标记物、囊泡内蛋白生物标记物和囊泡内rna生物标记物,其中当所述至少一个靶生物标记物选自表面蛋白生物标记物中的一个或多个时,选定的一个或多个表面蛋白生物标记物和至少一种细胞外囊泡相关膜结合多肽是不同的。
[0311]
在一些实施方案中,试剂盒中提供的至少两个检测探针的靶结合部分各自针对靶生物标记物特征的相同靶生物标记物。在一些此类实施方案中,这样的至少两个检测探针的寡核苷酸结构域是不同的。
[0312]
在一些实施方案中,试剂盒中提供的至少两个检测探针的靶结合部分各自针对靶生物标记物特征的不同靶生物标记物。
[0313]
在一些实施方案中,试剂盒可包含至少一种化学试剂,诸如固定剂、透化剂和/或
封闭剂。
[0314]
在一些实施方案中,试剂盒可包含一种或多种核酸连接试剂(例如,核酸连接酶,诸如dna连接酶和/或缓冲溶液)。
[0315]
在一些实施方案中,试剂盒可包含至少一种或多种扩增试剂,诸如pcr扩增试剂。在一些实施方案中,试剂盒可包含一种或多种核酸聚合酶(例如,dna聚合酶)、一对或多对引物、核苷酸和/或缓冲溶液。
[0316]
在一些实施方案中,试剂盒可包含用于捕获关注的实体(例如,生物实体)的固体基底。例如,此种固体基底可以是或包含珠(例如,磁珠)。在一些实施方案中,此种固体基底可以是或包含表面。在一些实施方案中,表面可以是或包含测定室的捕获表面(例如,实体捕获表面),例如像过滤器、基质、膜、板、管、孔(例如但不限于微孔)等。在一些实施方案中,固体基底的表面(例如,捕获表面)可涂覆有用于关注的实体(例如,生物实体)的捕获剂(例如,多肽或抗体剂)。
[0317]
在一些实施方案中,可选择在试剂盒中提供的一组检测探针以诊断特定癌症(包括例如但不限于急性淋巴细胞性白血病、急性髓系白血病、胆管癌、膀胱癌、脑癌、乳腺癌、宫颈癌、慢性淋巴细胞性白血病、慢性髓系白血病、结直肠癌、子宫内膜癌、食道癌、胃肠癌、霍奇金淋巴瘤、肾癌、肝癌、肺癌、多发性骨髓瘤、非霍奇金淋巴瘤、卵巢癌、胰腺癌、前列腺癌、肉瘤、皮肤癌和胃癌)。
[0318]
在一些实施方案中,试剂盒可包含多个检测探针组,其中每组检测探针针对特定癌症的检测并且包含至少2个或更多个检测探针。例如,此种试剂盒可用于在单次测定中筛选(例如,定期筛选)受试者或整个受试者群体的各种癌症(包括例如但不限于急性淋巴细胞性白血病、急性髓系白血病、胆管癌、膀胱癌、脑癌、乳腺癌、宫颈癌、慢性淋巴细胞性白血病、慢性髓系白血病、结直肠癌、子宫内膜癌、食道癌、胃肠癌、霍奇金淋巴瘤、肾癌、肝癌、肺癌、多发性骨髓瘤、非霍奇金淋巴瘤、卵巢癌、胰腺癌、前列腺癌、肉瘤、皮肤癌和胃癌)。
[0319]
在一些实施方案中,本文提供的试剂盒可包括用于实践本文所述的方法的说明书。这些说明书可以多种形式存在于试剂盒中,所述形式中的一种或多种可存在于所述试剂盒中。这些说明书可存在的一种形式是在合适的介质或基底上打印信息,例如,在试剂盒的包装、包装说明书等中打印信息的一张或多张纸。另一种方式可为计算机可读介质,例如,磁盘、cd、usb驱动器等,其上记录了教学信息。可能存在的另一种方式是网站地址,所述网站地址可通过互联网用于访问教学信息。试剂盒中可存在任何方便的方式。
[0320]
在试剂盒用作伴随诊断的一些实施方案中,此类试剂盒可包括用于鉴定可能对治疗剂作出反应的患者的说明(例如,鉴定指示患者对治疗剂反应性的生物标记物)。在一些实施方案中,此类试剂盒可包含与伴随诊断测试串联使用的治疗剂。
[0321]
本发明的其他特征将在以下示例性实施方案的描述过程中变得明显,给出所述示例性实施方案是为了说明本发明,并且不旨在限制本发明。
[0322]
例示
[0323]
实施例1:检测单个生物实体中存在的两个或更多个靶标(例如,分子靶标)
[0324]
本实施例描述了针对不同靶标的检测探针的合成,每个靶标包含靶结合部分和偶联至靶结合部分的寡核苷酸结构域(包含双链部分和单链悬突)。本实施例进一步证明,使用此类检测探针来检测包含两个或更多个靶标(所述靶标可为相同或不同的)的生物实体
的存在或不存在。
[0325]
在一些实施方案中,检测探针可包含双链寡核苷酸,其一端具有对靶蛋白具有特异性的抗体剂且另一端具有单链悬突。当两个或更多个检测探针结合到同一生物实体(例如,细胞或细胞外囊泡)时,检测探针的单链悬突紧密接近,使得它们可相互杂交以形成双链复合物,其可随后被连接并扩增以进行检测。
[0326]
虽然本研究使用了两个检测探针,每个检测探针用于特定的靶标(例如,分子靶标),但也可使用三个或更多个检测探针,每个检测探针用于特定的靶标(例如,分子靶标)。此外,描述于本实施例中的组合物和方法可扩展到除了在本实施例中用作模型生物实体的生物细胞之外的不同生物样品(例如,包含细胞外囊泡)中的应用。
[0327]
在一些实施方案中,实体检测测定利用两个检测探针,每个检测探针识别靶标(例如,在一些实施方案中,每个检测探针识别不同的癌症特异性表位,或在一些实施方案中,一个检测探针识别与正常细胞和/或组织特异性相关的生物标记物,而另一个识别癌症的通用生物标记物;或在一些实施方案中,两者识别相同的靶标)。例如,使用成对的双链模板dna,每个双链模板dna都具有与其配偶体上的5'悬突互补的特定单链5'悬突(例如,四碱基5'悬突)。对靶表位(例如,癌症表位)具有特异性的每种抗体剂与两个双链dna模板中的一个缀合。当抗体结合它们的靶表位时,相应dna模板的粘性末端(例如,单链悬突)能够杂交。在pcr扩增之前,这些粘性末端然后通过dna连接酶(例如,t7连接酶)连接在一起。为了在两个dna模板之间发生杂交,两个抗体需要彼此紧密接近(例如,在50nm至60nm内,即dna接头和抗体剂的长度)。结合但保持未杂交/连接的任何模板都不会产生pcr产物,如图2a所示。
[0328]
在本实施例中,使用了图2a所示的两种抗体和两个引物(使用evagreen荧光染料作为标记探针)的双链体系统。虽然在本实施例中使用荧光染料作为标记探针,但也可使用已知标记核酸或寡核苷酸的其他可检测标记。选择靶标1(例如,靶蛋白1)和靶标2(例如,靶蛋白2),使得它们通常不在任何其他细胞类型中共表达,但在特定癌症(例如,黑色素瘤)的细胞中共表达,尽管可能存在可通过将第三靶标(例如,第三靶蛋白)添加到癌症(例如,黑色素瘤)指纹来解释的例外情况。为了评估双链体系统(例如,本文所述的那些),对两种黑色素瘤细胞系sk
‑
mel
‑
1和mewo以及一种阴性对照结直肠癌细胞系t84进行实验。如表1所示,t84是以非常低的水平表达靶蛋白1和靶蛋白2的结直肠细胞系。相反,sk
‑
mel
‑
1和mewo是以高水平表达靶蛋白1和靶蛋白2的黑色素瘤细胞系。如本文所述,应当注意,“每百万转录本”或“tpm”是指对rna测序的归一化,这意味着“对于rna测序样品中的每1,000,000个rna分子,x来自如指定的基因转录物。”[0329][0330]
示例性方法:
[0331]
寡核苷酸
[0332]
在一些实施方案中,寡核苷酸可具有以下序列结构和修饰:
[0333]
链1:
[0334]
/5ammc12/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0335]
链2:
[0336]
/5ammc12/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0337]
链3:
[0338]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0339]
链4:
[0340]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggacttcgtaggtctggtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0341]
链5:
[0342]
cagtctgactcaccactcgt
[0343]
链6:
[0344]
caccagacctacgaagtcca
[0345]
poly t:
[0346]
ttttttttttttttttttttttttttt
[0347]
连接和扩增的验证
[0348]
为了验证dna模板是否连接并可通过pcr扩增,对成对的链1和链3以及成对的链2和链4进行杂交。然后使用dna连接酶(例如,t7或t4连接酶)连接杂交的链1 3和2 4,并且使用evagreen荧光染料以及链5和链6作为引物进行qpcr。
[0349]
为了杂交dna,例如使用以下方案在热循环仪中熔化500pm等体积量的链1和链3以及链2和链4:95℃10秒,65℃30秒,保持在4℃。在使dna双链后,进行dna连接(例如,使用t4和t7连接酶),例如,在20ul反应中使用9ul杂交的250pm dna。阴性对照不接受连接酶但含有相同的缓冲液。连接在热循环仪中进行,例如在25℃下进行20分钟。连接后的产物(以及不含连接酶的样品)经历qpcr,例如,使用不含逆转录酶(rt)的luna主混合物。所有qpcr反应均以三联体进行,并使用被动参考(例如,rox)将qpcr信号归一化。然后对数据进行分析并绘图。
[0350]
抗体剂
‑
dna缀合
[0351]
为了将寡核苷酸(例如,杂交的链1和链3以及杂交的链2和链4)与靶结合部分(例如,针对靶蛋白的抗体剂)缀合,将成对的单链杂交以形成双链寡核苷酸,其在一端具有单链悬突,然后例如使用商业dna
‑
寡核苷酸缀合试剂盒(例如,abcam,ab218260)在另一端将靶结合部分(例如,针对靶蛋白的抗体剂)缀合至双链寡核苷酸。
[0352]
为了使两条单链dna杂交以形成双链dna,例如使用以下方案对50ul的100um等摩尔和体积的dna进行热循环:1.加热至95℃并保持温度2min。2.通过每3分钟下降5℃直至25℃,在45min内冷却至25℃。3.保持在4℃。使用50um双链dna产物,将多个双链dna(例如,五
条双链dna)退火于每种抗体剂。
[0353]
细胞培养
[0354]
可使用本领域已知的任何方法培养细胞。例如,使t84细胞在具有5%无外泌体胎牛血清(fbs)和50单位的青霉素/链霉素/ml的1:1达尔伯克改良伊格尔培养基(dulbecco’smodified eagle medium(dmem)):汉姆氏f12(ham’s f12)培养基中生长。使sk
‑
mel
‑
1和mewo细胞均在具有10%无外泌体fbs和50单位的青霉素/链霉素/ml的伊格尔最小必需培养基(emem)中生长。所有细胞系均保持在5%co2和37℃下,并且传代数低于15。
[0355]
细胞固定和封闭
[0356]
可使用本领域已知的任何方法固定、透化并封闭细胞。例如,在固定之前,例如使用tryple蛋白酶将粘附的t84和mewo细胞从它们的基底上分离。sk
‑
mel
‑
1的粘附性较弱,并且可例如通过摇动烧瓶来从烧瓶基底中释放出来。一旦在溶液中,将细胞在室温下以300rcf沉淀5分钟。将细胞在10ml 1x pbs中洗涤一次,并如上所述进行沉淀。然后将每个细胞系固定并透化。例如,可将细胞在冰冷的甲醇中同时固定和透化,并在
‑
25℃下孵育至少20分钟。在封闭之前,通过将细胞首先在1000rcf下沉淀2分钟(一旦固定,它们可承受更大的重力),然后在1x pbs中洗涤一次,从而使细胞再水化。然后将洗涤且再水化的沉淀重悬于封闭缓冲液中。
[0357]
细胞系的抗体剂
‑
dna缀合物标记和洗涤
[0358]
在添加dna缀合的抗体之前,将三种甲醇固定的细胞系(sk
‑
mel
‑
1、mewo和t84)中的每一种在1ml封闭缓冲液中的1.5ml protein lo bind eppendorf管中分成三个等分试样,以封闭非特异性结合。对于三种细胞系中的每一种,设计了三个管,一个不含抗体剂,一个含有1ug/ml的dna缀合的抗体(一个针对靶蛋白1,并且另一个针对靶蛋白2),并且一个含有10ng/ml的dna缀合的抗体(一个针对靶蛋白1,并且另一个针对靶蛋白2)。将抗体在封闭缓冲液中预稀释,之后添加到1ml封闭细胞中,并且将抗体剂
‑
dna缀合物与细胞一起孵育30分钟。抗体孵育后,通过在室温下以1,000rcf离心2分钟来洗涤细胞,例如在1ml的1x pbs中洗涤四次。
[0359]
标记细胞的连接和qpcr
[0360]
例如使用以下方案完成封闭、标记且洗涤的细胞的dna连接(例如,t7连接):1.制备dna连接酶主混合物以在最终洗涤后以50ul的体积将细胞重悬。dna连接酶主混合物含有例如5%(体积/体积)t7连接酶、50%(体积/体积)2x t7连接酶缓冲液和45%(体积/体积)无核酸酶的水。2.将细胞系中的每种重悬于50ul dna连接酶主混合物中后,将细胞
‑
连接酶混合物置于热循环仪中,例如在25℃下20分钟。3.制备qpcr主混合物,例如使用500nm浓度的引物(例如,链5和链6)、1x evagreen荧光染料和luna qpcr主混合物以实现25ul的最终反应体积。4.向25ul qpcr反应中的每个中添加约8ul细胞连接酶产物。5.例如使用以下pcr方案例如在96孔板中进行qpcr:在95℃下保持1分钟,进行在95℃下持续10秒和在60℃下持续30秒的50个循环,以及标准解链曲线。选择的温度变化率是标准的(例如,每秒2℃)。所有qpcr反应均以三联体进行,并使用被动参考(例如,rox)将qpcr信号归一化。然后对数据进行分析并绘图。
[0361]
结果:
[0362]
qpcr图的解释
[0363]
qpcr图确定了来自插入双链dna的evagreen的荧光信号增加到超出背景的ct(循环阈值)。由于对任何类型的双链dna都使用了非特异性染料,因此在引物二聚体扩增约35个循环后不会出现模板对照(ntc)。此外,进入pcr反应的任何少量模板都将导致ct值低于预期的ct值,这是当ntc的ct值低于30(图4中出现的ntc的低于30的ct值)时发生的情况。此种污染可例如通过用杂交探针进行扩增来控制,仅在模板被扩增时产生荧光(或者标记探针或检测标记可被水解)。
[0364]
连接酶是扩增所需要的
[0365]
连接酶的存在对于实现高于引物二聚体背景的qpcr信号是必要的,如图3所示。此外,t7和t4连接酶产生相似的ct值和一致的结果。
[0366]
qpcr结果一致
[0367]
如图4所示,不含任何抗体剂的组在细胞系中具有高ct值(
‑
33 )。相反,用1ug/ml抗体剂标记的组的ct值低至18。信号最强的细胞系为mewo,其次为sk
‑
mel
‑
1和t84细胞系。此观察结果与表达靶蛋白1和靶蛋白2的mewo最多,表达靶蛋白1和靶蛋白2的sk
‑
mel
‑
1第二多,并且表达靶蛋白1和靶蛋白2的t84细胞系最少一致。最后,较低浓度的抗体剂(10ng/ml)具有高得多的ct值,类似于无抗体剂对照的ct值。
[0368]
讨论:
[0369]
证明双链体系统(例如,本文所述的那些)鉴定细胞系中共定位的靶蛋白1和靶蛋白2。首先,模板连接并可扩增,如图3所示。其次,在将这些dna模板与两种不同的抗体和染色细胞系缀合后,观察到表达依赖性信号。即mewo细胞系表达最高水平的靶蛋白1和靶蛋白2(表1)且相应地具有最强的靶蛋白1和靶蛋白2信号,sk
‑
mel
‑
1细胞系表达靶蛋白1和靶蛋白2比mewo低约4.4倍且信号较弱,并且t84细胞系不表达至几乎不表达靶蛋白1和靶蛋白2且信号最弱。阴性t84细胞也具有高ct值,与非特异性背景一致。然而,1ug/ml抗体剂下的t84仍有一个ct值低至23。此ct值是另外两个ct值27的异常值,并且可能是由于细胞聚集或其他非特异性引发相互作用或污染。在一些实施方案中,可通过进行更彻底的洗涤来增加最强和最弱信号之间的差异。
[0370]
虽然本文证明双链体系统(例如,上述那些)准确地鉴定表达靶蛋白1和靶蛋白2的细胞,但此种系统也可用于鉴定包含靶蛋白1和靶蛋白2的其他生物实体(例如,细胞外囊泡)。例如,细胞外囊泡可在固定和任何下游处理之前被捕获到固体基底(例如,二氧化硅珠)上。
[0371]
实施例2:检测单个生物实体中存在的三个或更多个靶标(例如,分子靶标)
[0372]
本实施例描述了针对三个靶标的检测探针的合成,每个靶标包含靶结合部分和偶联至靶结合部分的寡核苷酸结构域(包含双链部分和单链悬突)。本实施例进一步证明了三个双链寡核苷酸(每个都具有单链悬突)可用于混合物中以进行连接和扩增,这表明当此类双链寡核苷酸与抗体缀合时,可进行三链体系统(例如,如图5a所示)以鉴定都位于同一生物实体(例如,单个细胞外囊泡)中的三个靶标(例如,分子靶标)。在一些实施方案中,这三个靶标可为相同的靶标。在一些实施方案中,这三个靶标可为不同的靶标。在一些实施方案中,这三个靶标中的至少两个可为相同的靶标。
[0373]
示例性方法:
[0374]
寡核苷酸
[0375]
在一些实施方案中,寡核苷酸可具有以下序列结构和修饰:
[0376]
链1:
[0377]
/5ammc12/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0378]
链2:
[0379]
/5ammc12/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0380]
链4(无5'磷酸酯):
[0381]
/5’actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggacttcgtaggtctggtg
[0382]
链5:
[0383]
cagtctgactcaccactcgt
[0384]
链6:
[0385]
caccagacctacgaagtcca
[0386]
链8:
[0387]
/5phos/ttccaactat/ccaactat/ctat/ tttttt/tt acacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0388]
链9:
[0389]
/5phos/gagtgtgaggatgtcagtgtgtctc/tt/ccaa,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0390]
链10:
[0391]
/5ammc12/atagttggaagagacacactgacatcctcac,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0392]
注意:“/”表示给定dna链的变体。选择了三种不同长度的链8和链9,其中链8中有两个不同的缺口。
[0393]
连接和扩增的验证
[0394]
为了验证dna模板是否连接并可通过pcr扩增,对成对的链1和链8、成对的链9和链10以及成对的链2和链4进行杂交。然后使用dna连接酶(例如,t7或t4连接酶)连接杂交的链1 8、9 10和2 4,并且使用evagreen荧光染料以及链5和链6作为引物进行qpcr。
[0395]
为了杂交dna,例如使用以下方案在热循环仪中熔化1um等体积量的链1和链8、链9和链10以及链2和链4:95℃10秒,65℃30秒,保持在4℃。在使dna双链后,进行dna连接(例如,使用t4和t7连接酶),例如,在20ul反应中使用9ul杂交的100nm dna。阴性对照不接受连接酶但含有相同的缓冲液。连接在热循环仪中进行,例如在25℃下进行20分钟。然后例如使用taqman fast advanced主混合物对连接后的产物(或不含连接酶)进行qpcr。例如使用以下pcr方案例如在96孔板中进行qpcr:在50℃下保持2分钟,在95℃下保持2分钟,进行在95℃下持续5秒和在60℃下持续15秒的55个循环,并且进行标准解链曲线。所有qpcr反应均以
三联体进行,并使用被动参考(例如,rox)将qpcr信号归一化。然后对数据进行分析并绘图。
[0396]
结果:
[0397]
稳健的ct值需要连接酶
[0398]
连接酶的存在对于产生稳健的ct值是必要的,如图6所示。
[0399]
强信号需要所有三个模板
[0400]
每对三个模板dna在反应中连接,如图7至图9所示。在只有三条链中的两条时,信号为大约弱13到14个ct值。这些发现表明,三链体dna系统可被扩增,其中所有三条链都需要稳健的信号。
[0401]
实施例3:检测单个细胞外囊泡中存在的两个或更多个靶标
[0402]
本实施例证明,分别如实施例1和实施例2所述的双链体系统和三链体系统可用于检测不同类型的生物实体(例如,细胞外囊泡)中靶标的组合(例如,一组)的存在,而不是检测靶标中的至少一个缺失的生物实体(例如,细胞外囊泡)。本实施例描述了还针对单个靶标的检测探针的合成,每个靶标包含靶结合部分和偶联至靶结合部分的寡核苷酸结构域(包含双链部分和单链悬突)。
[0403]
为了评估双链体系统在检测包含两个靶标(例如,分子靶标)的细胞外囊泡方面的性能,在一些实施方案中,使用了与实施例1中所述不同的靶生物标记物的组合。在一些实施方案中,可检测探针(诸如实施例1中使用的evagreen荧光染料)被水解探针取代。在一些实施方案中,靶标记物a为细胞外囊泡的通用标记物。在一些实施方案中,靶标记物b仅在正常皮肤和黑色素瘤中表达,而不在其他癌症中表达。如表2所示,t84是不可检测地(在此测定的条件下)表达靶标记物b,但以低于mewo细胞的水平表达靶标记物a的结直肠细胞系。相反,mewo黑色素瘤细胞系以高水平表达靶标记物a和靶标记物b。
[0404]
表2.细胞系来源的细胞外囊泡基因表达
[0405]
(每百万转录本/tpm)
[0406]
靶标mewo(tpm)t84(tpm)靶标记物a 靶标记物b
‑
[0407]
为了评估三链体系统在检测包含三个靶生物标记物的细胞外囊泡方面的性能,使用了三个靶标记物,每个在mewo细胞中的表达水平高于t84细胞,或者在mewo细胞中高表达,而在t84中完全不表达。在本实施例中,选择三个靶标记物的组合,使得靶标记物中的至少一个在t84细胞外囊泡中不可检测地表达(在此测定的条件下)。
[0408]
表3.细胞系来源的细胞外囊泡基因表达
[0409]
(每百万转录本/tpm)
[0410]
靶标mewo(tpm)t84(tpm)靶标记物a 靶标记物c 靶标记物d
[0411]
示例性方法:
[0412]
寡核苷酸
[0413]
在一些实施方案中,寡核苷酸可具有以下序列结构和修饰。应当注意,下面的链数
对应于与图2a和图5a所示的链相关的数值。
[0414]
链1:
[0415]
/5ammc12/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0416]
链2:
[0417]
/5ammc12/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0418]
链3:
[0419]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0420]
链4:
[0421]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggacttcgtaggtctggtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0422]
链4(在三链体系统中使用时无5'磷酸酯):
[0423]
/5’actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggacttcgtaggtctggtg
[0424]
链5:
[0425]
cagtctgactcaccactcgt
[0426]
链6:
[0427]
caccagacctacgaagtcca
[0428]
poly t:
[0429]
ttttttttttttttttttttttttttt
[0430]
链8:
[0431]
/5phos/ccaactatttttttacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0432]
链9:
[0433]
/5phos/gagtgtgaggatgtcagtgtgtctctt,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0434]
链10:
[0435]
/5ammc12/atagttggaagagacacactgacatcctcac,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0436]
抗体
‑
dna缀合
[0437]
对于双链体系统,在一些实施方案中,包含链1和链3的寡核苷酸与对靶标记物a具有特异性的靶结合部分缀合,而包含链2和链4的寡核苷酸与对靶标记物b具有特异性的靶结合部分缀合。在一些实施方案中,一种用于如实施例1中所述将靶结合部分(例如,抗体剂)缀合至寡核苷酸的方法用于使双链dna的大约两条链退火于每个靶结合部分(例如,抗体剂)。
[0438]
对于三链体系统,在一些实施方案中,包含链1和链8的寡核苷酸与对靶标记物c具有特异性的靶结合部分缀合;包含链10和链9的寡核苷酸与对靶标记物a具有特异性的靶结合部分缀合;并且包含链2和链4的寡核苷酸(其中链4不具有游离的5'磷酸酯)与对靶标记物d具有特异性的靶结合部分缀合。在一些实施方案中,一种用于如实施例1中所述将靶结合部分(例如,抗体剂)缀合至寡核苷酸的方法用于使双链dna的大约两条链退火于每个靶结合部分(例如,抗体剂)。
[0439]
细胞培养
[0440]
使t84细胞在具有5%无外泌体胎牛血清(fbs)和50单位的青霉素/链霉素/ml的1:1达尔伯克改良伊格尔培养基(dmem):汉姆氏f12培养基中生长。使mewo细胞在具有10%无外泌体fbs和50单位的青霉素/链霉素/ml的伊格尔最小必需培养基(emem)中生长。所有细胞系均保持在5%co2和37℃下,并且传代数低于20。
[0441]
从细胞培养基中纯化细胞外囊泡
[0442]
在一些实施方案中,mewo和t84细胞在它们各自的培养基中生长,直到它们达到约80%汇合。收集细胞培养基并在室温(rt)下以300x rcf旋转5分钟以去除细胞和碎片。然后收集上清液并在
‑
80℃下冷冻。
[0443]
使用前,将储存在
‑
80℃下的冷冻上清液解冻,然后澄清细胞和大的(例如,直径大于1微米)细胞碎片。使用离心澄清解冻的上清液。
[0444]
在一些实施方案中,使澄清的废培养基(例如,约500ul)通过尺寸排阻纯化柱。为每个样品收集具有约65nm至约200nm大小范围的纳米颗粒。
[0445]
细胞外囊泡生物素化
[0446]
在一些实施方案中,按照制造商的说明,例如使用nanodrop测量纯化的细胞外囊泡的蛋白质浓度。此测量用于计算添加到每个样品中的生物素的量。按照制造商的说明,例如使用ez
‑
link micro nhs
‑
peg4生物素化试剂盒将细胞外囊泡生物素化。将生物素添加到样品中后,将其摇动45分钟。使用两次连续的5ml,40kda mwco柱旋转(例如,来自zeba
tm
)去除过量的生物素。
[0447]
颗粒计数
[0448]
例如用使用ts400芯片的spectrodyne颗粒计数仪器获得颗粒计数,以测量65nm和200nm之间的纳米颗粒范围。
[0449]
将生物素化的细胞外囊泡捕获或固定到链霉亲和素包被的96孔板上
[0450]
在一些实施方案中,向链霉亲和素包被的捕获表面(例如,96孔板的孔)添加等量的生物素化的细胞外囊泡,例如对于所测定的每个样品条件,一式三份。将板在室温下孵育并摇动一段时间。
[0451]
细胞外囊泡固定
[0452]
在一些实施方案中,将适当浓度的甲醛(在1x pbs中)添加到捕获在链霉亲和素包被的表面上的细胞外囊泡。然后洗涤固定的细胞外囊泡,以用于后续步骤。
[0453]
样品封闭和细胞外囊泡透化
[0454]
将包含固定的细胞外囊泡的样品与封闭缓冲液混合。在一些实施方案中,封闭缓冲液可包含在缓冲溶液诸如无磷酸盐缓冲液(例如,来自candor bioscience的bioscience的)中的适当浓度的triton x
‑
100或皂苷和鲑鱼精子dna。
[0455]
检测探针结合
[0456]
将检测探针(例如,以基于抗体剂的量的约0.5ug/ml至约3.5ug/ml的浓度)添加到包含细胞外囊泡(例如,被固定、封闭且任选地透化的完整细胞外囊泡)的样品中。然后在使检测探针与包含靶生物标记物的细胞外囊泡结合的条件下孵育混合物。
[0457]
结合后洗涤
[0458]
在一些实施方案中,将样品在适当的缓冲液中洗涤。
[0459]
连接
[0460]
洗涤以去除未结合的检测探针后,将检测探针结合的细胞外囊泡(捕获在固体基底表面上)与连接混合物接触。将混合物在rt下孵育20分钟。
[0461]
pcr
[0462]
连接后,将检测探针结合的细胞外囊泡(捕获在固体基底表面上)与pcr混合物接触。例如,在quant studio 3上使用以下示例性pcr方案进行pcr:在95℃下保持1分钟,进行在95℃下持续5秒和在62℃下持续15秒的50个循环,以及标准解链曲线。选择的温度变化率是标准的(每秒2℃)。所有qpcr均以双联体或三联体进行,并且将rox用作被动参考以将qpcr信号归一化。然后从quant studio 3机器下载数据,并在python 3.7中进行分析和绘制。
[0463]
结果:
[0464]
图13a和图13b中所示的qpcr结果表明,使用本文所述的系统(例如,双链体和/或三链体系统)可检测到含有靶生物标记物特征(例如,蛋白质表达模式)的细胞外囊泡并将其与不具有此种靶生物标记物特征的细胞外囊泡区分开来。使用本文所述的系统(例如,双链体和/或三链体系统),亲本细胞系的差异基因表达在各个细胞系衍生的细胞外囊泡中很容易鉴定。mewo细胞及从其衍生的细胞外囊泡比t84细胞及从其衍生的细胞外囊泡表达更高水平的每个靶标记物(对于双链体系统为靶标记物a和靶标记物b;对于三链体系统为靶标记物a、靶标记物c和靶标记物d)。因此,在本实施例中进行的双链体和三链体测定中,mewo细胞外囊泡随后具有比从t84细胞外囊泡获得的ct更低的ct(低约6ct)。这些结果与每个细胞系中的mrna表达一致,如表2至表3所示。
[0465]
讨论:
[0466]
本实施例表明,鉴定共定位的靶标记物a和靶标记物b的双链体系统在标记细胞外囊泡的水平上起作用,其中观察到表达依赖性信号。具体而言,相对于t84细胞及从其衍生的细胞外囊泡,mewo细胞及从其衍生的细胞外囊泡表达更高水平的靶标记物a和靶标记物b(表2),并且因此在含有mewo细胞外囊泡的样品中产生更强的信号。
[0467]
本实施例还表明,鉴定靶标记物a、靶标记物c和靶标记物d的组合的三链体系统在细胞外囊泡的水平上起作用,其中观察到表达依赖性信号。与在t84细胞及从其衍生的细胞外囊泡中表达的那些相比,mewo细胞及从其衍生的细胞外囊泡表达更高水平的所有三种标记物。特别地,靶标记物中的一个(靶标记物a)在t84细胞及从其衍生的细胞外囊泡中不表达。与t84细胞外囊泡相比,这三个标记物在mewo细胞外囊泡中的这种更高表达导致明显更强的信号(26为强约64倍)。
[0468]
不希望受理论束缚,在一些实施方案中,检测探针的靶结合部分(例如,抗体剂)的非特异性结合可有助于在t84样品中检测到噪声信号(与无模板阴性对照相比)。因此,在一
些实施方案中,可对包含细胞外囊泡的样品进行处理以减少或最小化检测探针的非特异性结合。
[0469]
实施例4:使用示例性系统检测患者血浆样品中的癌症相关细胞外囊泡的癌症检测
[0470]
本实施例证明本文所述的系统可用于检测复杂样品基质(例如,来自受试者的血浆样品)中的靶生物实体。例如,将靶生物实体(例如,癌症相关细胞外囊泡)掺入血浆样品(例如,来自人受试者)中,并且以浓度依赖性方式在包含靶生物实体的样品中检测连接模板的信号。
[0471]
本实施例还证明本文所述的系统可用于癌症检测。具体而言,本实施例显示本文所述的系统可用于将癌症患者的细胞外囊泡与正常健康受试者的细胞外囊泡区分开来。此外,本实施例表明此种癌症检测测定提供高敏感度和/或特异性。
[0472]
虽然本实施例使用从肺腺癌患者获得的样品(例如,血浆样品)来证明本文所述的系统检测癌症相关细胞外囊泡的能力,但阅读本公开的本领域技术人员将理解,本文所述的此类系统可用于使用至少两个或更多个靶标记物的不同适当组合来检测其他类型的癌症。此外,阅读本公开的本领域技术人员将理解,本文所述的此类系统还可用于使用至少两个或更多个靶标记物的适当组来诊断癌症的不同阶段。
[0473]
如在本实施例中证明的能力不限于在本实施例中评估的双链体系统(即,包含对靶生物实体具有特异性的一组两个不同的检测探针)。对于阅读本公开的本领域技术人员显而易见的是,本文所述的其他系统(例如,包含一组至少三个或更多个不同检测探针的三链体或n链体系统)也可用于检测复杂样品基质中的靶生物实体,例如,用于癌症检测。阅读本公开的本领域技术人员还将理解,在一些实施方案中,包含针对不同靶标的另外的检测探针将增加检测测定的特异性和/或灵敏度。
[0474]
掺入实验:在一个方面,评估了双链体系统检测复杂样品基质中的细胞外囊泡的能力。例如,将癌症相关细胞外囊泡(ev)掺入受试者(例如,人受试者)的血浆样品中。然后将掺入的血浆样品纯化以分离ev。在进行双链体系统测定(例如,如本文所述)之前,分离或纯化的ev可被捕获或吸附在固体基底表面(例如,pcr板)上。在一些实施方案中,从肺腺癌细胞系hcc
‑
4006获得癌症相关细胞外囊泡。在一些实施方案中,从黑色素瘤细胞系sk
‑
mel1获得癌症相关细胞外囊泡。
[0475]
在此掺入实验中,在双链体系统测定中评估了生物标记物的四种不同的示例性组合。另外,水解探针取代了可检测的荧光团标记sybr green。四种不同的示例性组合如下所示:
[0476]
·
靶标记物a 靶标记物b(本测定中使用的用于检测黑色素瘤相关细胞外囊泡的组合标记物)
[0477]
·
靶标记物e 靶标记物f(本测定中使用的用于检测肺腺癌相关细胞外囊泡的组合标记物)
[0478]
·
靶标记物e 靶标记物a(本测定中使用的用于检测肺腺癌相关细胞外囊泡的组合标记物)
[0479]
·
靶标记物g 靶标记物f(本测定中使用的用于检测肺腺癌相关细胞外囊泡的组合标记物)
[0480]
下表4总结了不同癌症相关细胞外囊泡中各种靶标记物的表达。应当注意,表4中的组合5未在掺入实验中进行评估,但在实验(如下所述)中用于筛选患者样品。
[0481]
表4.如在肺腺癌细胞系(hcc4006)和黑色素瘤细胞系(skmel1)中表示的五种组合的每百万转录本(tpm)分数。
[0482][0483]
靶标记物e、靶标记物f、靶标记物g和靶标记物h在肺腺癌中的表达高于其他组织。应当注意,靶标记物e也在健康组织的其他地方表达,但通常比luad中的水平低。如实施例3中所讨论的,靶标记物b在黑色素瘤中的表达比在其他组织中的表达更高,在本实施例中用作黑色素瘤相关细胞外囊泡的阳性对照。如实施例3中所讨论的,靶标记物a是细胞外囊泡的通用标记物,因为它存在于许多类型的细胞外囊泡中。
[0484]
健康与阶段iv肺腺癌(luad)血浆实验:在另一方面,评估了双链体系统区分健康与阶段iv luad患者的血浆样品中的细胞外囊泡的能力。例如,从阶段iv luad患者以及年龄和性别匹配的健康受试者的血浆样品中纯化或分离细胞外囊泡,然后使用一组至少两个或更多个检测探针对其进行分析,例如针对如上表4所示的组合3或组合5的检测探针。
[0485]
示例性方法:
[0486]
寡核苷酸
[0487]
在一些实施方案中,寡核苷酸可具有以下序列结构和修饰。应当注意,下面的链数对应于与图2a中所示的链相关的数值。
[0488]
链1:
[0489]
/5ammc12/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0490]
链2:
[0491]
/5ammc12/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0492]
链3:
[0493]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0494]
链4:
[0495]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggacttcgtaggtctggtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0496]
链5:
[0497]
cagtctgactcaccactcgt
[0498]
链6:
[0499]
caccagacctacgaagtcca
[0500]
抗体剂
‑
dna缀合
[0501]
在一些实施方案中,进行抗体剂与寡核苷酸的缀合以最小化或避免抗体剂的抗原结合部分的改变。在一些实施方案中,寡核苷酸是或包含杂交的链1和链3或杂交的链2和链4。在一些实施方案中,可使用如实施例1和实施例3中所述的方法将抗体剂缀合至寡核苷酸。在一些实施方案中,抗体剂可通过抗体剂的游离氨基缀合至寡核苷酸。在一些实施方案中,抗体剂可通过抗体剂的反应性硫醇基团缀合至寡核苷酸。在一些实施方案中,抗体剂可通过抗体剂中存在的碳水化合物残基缀合至寡核苷酸。
[0502]
细胞培养
[0503]
使sk
‑
mel
‑
1细胞在具有10%无外泌体fbs和50单位的青霉素/链霉素/ml的伊格尔最小必需培养基(emem)中生长。使hcc
‑
4006细胞在具有10%无外泌体fbs和50单位的青霉素/链霉素/ml的roswell park memorial institute(rpmi 1640)中生长。所有细胞系均保持在5%co2和37℃下,并且传代数低于20。
[0504]
从细胞培养基中纯化细胞外囊泡
[0505]
在一些实施方案中,sk
‑
mel
‑
1和hcc4006细胞在它们各自的培养基中生长,直到它们达到
‑
80%汇合。收集细胞培养基并在室温(rt)下以300x ref旋转5分钟以去除细胞和碎片。然后收集上清液并在
‑
80℃下冷冻。
[0506]
使用前,将储存在
‑
80℃下的冷冻上清液解冻,然后澄清细胞和大的(例如,大于1微米直径)细胞碎片。
[0507]
在一些实施方案中,使澄清的废培养基(例如,
‑
500ul)通过尺寸排阻纯化柱。为每个样品收集具有约65nm至约200nm大小范围的纳米颗粒。
[0508]
将细胞系衍生的细胞外囊泡添加到正常血浆样品中
[0509]
对于掺入研究,将不同体积(例如,50ul、100ul和400ul)的纯化的sk
‑
mel
‑
1和hcc
‑
4006细胞外囊泡以相同浓度(每ml大约3el0个直径大于80nm的纳米颗粒,例如,在spectradyne ncs1 ts400柱体上测得的)掺入来自健康患者bl3的血浆(“bl3血浆”)。从500ul bl3血浆开始,加入不同体积(例如,0ul、50ul、100ul或400ul)的纯化的细胞系衍生的细胞外囊泡。然后加入缓冲溶液,例如pbs,使得每个样品在细胞外囊泡纯化之前达到900ul的体积。下面的“从健康和阶段iv血浆中纯化细胞外囊泡”部分中描述了从血浆样品中纯化细胞外囊泡的示例性方案,不同之处在于尺寸排阻柱纯化后细胞外囊泡浓缩至400ul,将其在elisa捕获缓冲液中稀释至每ml约3e9个直径大于80nm的纳米颗粒,并以30ul
接种到pcr板上。
[0510]
从健康和阶段iv血浆中纯化细胞外囊泡
[0511]
在一些实施方案中,对血浆细胞外囊泡进行澄清,并且随后立即将其加载到尺寸排阻纯化柱上。为每个样品收集具有约65nm至约200nm大小范围的纳米颗粒。
[0512]
颗粒计数
[0513]
如实施例3中所述进行颗粒计数。
[0514]
将细胞外囊泡捕获或固定到pcr板孔中
[0515]
在一些实施方案中,将细胞外囊泡捕获到pcr板上。例如,涂覆有靶向癌症细胞外囊泡的抗体的表面可用于选择性捕获癌症细胞外囊泡。另一个实例是细胞外囊泡的生物素化和在链霉亲和素(例如,来自biotez)包被的pcr孔上的捕获。
[0516]
细胞外囊泡固定
[0517]
在一些实施方案中,将适当浓度的甲醛(在ix pbs中)添加到吸附在pcr板表面上的细胞外囊泡。然后洗涤固定的细胞外囊泡,以用于后续步骤。
[0518]
样品封闭和细胞外囊泡透化
[0519]
将包含固定的细胞外囊泡的样品与封闭缓冲液混合。在一些实施方案中,封闭缓冲液包含在缓冲溶液诸如无磷酸盐缓冲液(例如,来自candor bioscience的bioscience的)中的适当浓度的triton x
‑
100和鲑鱼精子dna。
[0520]
检测探针结合
[0521]
将检测探针(例如,以基于抗体剂的量的约1ug/ml的浓度)添加到包含细胞外囊泡(例如,被固定、封闭且任选地透化的完整细胞外囊泡)的样品中。然后在使检测探针与包含靶生物标记物的细胞外囊泡结合的条件下孵育混合物。
[0522]
结合后洗涤
[0523]
在一些实施方案中,将样品在适当的缓冲液中洗涤(例如,多次洗涤)。
[0524]
连接
[0525]
洗涤以去除未结合的检测探针后,将检测探针结合的细胞外囊泡(捕获在固体基底表面上)与连接混合物接触。将混合物在rt下孵育20分钟。
[0526]
pcr
[0527]
连接后,将检测探针结合的细胞外囊泡(捕获在固体基底表面上)与pcr混合物接触。例如,在quant studio 3上使用以下示例性pcr方案进行pcr:在95℃下保持1分钟,进行在95℃下持续5秒和在62℃下持续15秒的50个循环,以及标准解链曲线。选择的温度变化率是标准的(每秒2℃)。所有qpcr均以双联体或三联体进行,并且将rox用作被动参考以将qpcr信号归一化。然后从quant studio 3机器下载数据,并在python 3.7中进行分析和绘制。
[0528]
结果和讨论
[0529]
掺入实验
[0530]
获得检测探针的四种不同组合(针对靶标记物的不同组合,如表4所示)的原始qpcr图(数据未显示),然后对其进行分析以生成δct图(如图14a至图14d所示),其中将bl3血浆样品(健康血浆样品)作为零基线。
[0531]
对于所有sk
‑
mel
‑
1细胞外囊泡浓度,组合1(如表4所示)产生最大的δct(图14a),
因为组合1的靶标记物b主要在sk
‑
mel
‑
1中表达,但不在肺腺癌诸如hcc4006中表达。sk
‑
mel
‑
1细胞外囊泡血浆样品的δct值高于hcc4006细胞外囊泡血浆样品的δct值,因此表明使用针对此组合标记物的检测探针的系统可用于检测黑色素瘤。对于较高浓度(100ul和400ul)的hcc4006细胞外囊泡,组合2(如表4所示)产生更大的δct(图14b)。对于含有肺腺癌细胞外囊泡hcc4006的血浆样品,组合3(如表4所示)产生最大的δct(图14c)。hcc4006细胞外囊泡血浆样品的δct值高于sk
‑
mel
‑
1细胞外囊泡血浆样品的δct值,因此表明使用针对此组合标记物的检测探针的系统可用于检测肺腺癌。对于所有水平的hcc4006细胞外囊泡,组合4(如表4所示)未显示强信号(图14d)。
[0532]
掺入实验模拟了黑色素瘤和肺腺癌患者的血浆样品,以评估生物标记物的不同组合在癌症筛选中的效用。如上所讨论的,组合1能够区分所有水平的sk
‑
mel
‑
1细胞外囊泡掺入的血浆与所测试的所有其他样品,如图14a所示。给定组合1为sk
‑
mel
‑
1掺入的样品提供了最强信号,阅读本公开的本领域技术人员将理解,本文所述的系统(例如,具有针对组合1中的靶标记物的检测探针)在筛选患者样品时可对黑色素瘤具有灵敏度和特异性。如上所讨论的,组合3对于所有三个浓度的hcc4006加标物(spike in)具有最强的信号(图14c),这使其成为对肺腺癌患者样品进行测试的最佳候选者。
[0533]
健康对照和肺腺癌(luad)患者血浆样品中的组合3和组合5
[0534]
鉴于使用组合3在hcc4006细胞外囊泡掺入的血浆样品中检测到的强信号,选择组合3来评估luad患者血浆样品。如图15a至图15c所示,组合3能够以非常高的灵敏度和特异性区分luad患者样品(stiv样品)与健康对照(hc样品)。图15c示出在一些实施方案中,此种测定可提供100%的灵敏度和100%的特异性。
[0535]
除了组合3之外,还选择组合5(如表4所示)来评估luad患者血浆样品。如图16a至图16c所示,组合5能够以非常高的灵敏度和特异性区分luad患者样品(stiv样品)与健康对照(hc样品)。图16c示出在一些实施方案中,此种测定可提供100%的灵敏度和100%的特异性。
[0536]
有趣的是,组合3和组合5的归一化信号之间存在非常高的相关性(r2=0.99),如图17所示,这表明本文中呈现的结果的一致性。例如,样品stiv a中信号的强度在其他luad样品信号中一直是最大的,这可提供预示治疗反应的预后价值。
[0537]
本文呈现的发现显示,涉及针对生物标记物的适当组合的检测探针(例如,如本文所述)的系统和方法可用于区分不同类型的癌症患者(例如,肺腺癌患者与黑色素瘤患者)或区分癌症患者与正常健康受试者。
[0538]
在一些实施方案中,本文所述的系统和方法可用于鉴定癌症的阶段(例如,阶段i、阶段ii、阶段iii和阶段iv)。
[0539]
实施例5:检测与癌症相关的单个细胞外囊泡
[0540]
本实施例描述了针对不同靶标的检测探针的合成,每个靶标包含靶结合部分和偶联至靶结合部分的寡核苷酸结构域(包含双链部分和单链悬突)。本实施例进一步展示了使用此类检测探针来检测包含两个或更多个不同靶标的生物实体(例如,细胞外囊泡)的存在或不存在。
[0541]
在一些实施方案中,检测探针可包含双链寡核苷酸,其一端具有对靶癌症生物标记物具有特异性的抗体剂且另一端具有单链悬突。当两个或更多个检测探针结合到同一生
物实体(例如,细胞外囊泡)时,检测探针的单链悬突紧密接近,使得它们可相互杂交以形成双链复合物,其可随后被连接并扩增以进行检测。
[0542]
虽然此研究使用两个检测探针,每个检测探针针对相同的靶生物标记物,但是阅读本公开的本领域技术人员将理解何时两个检测探针针对不同的靶生物标记物,或何时使用三个或更多个检测探针,每个检测探针针对不同的靶蛋白。此外,描述于本实施例中的组合物和方法可扩展到不同生物样品(例如,包含细胞外囊泡)中的应用。
[0543]
本实施例显示来自某些实验的实验数据,所述实验证明本文提供的技术能够使用癌症的靶生物标记物组合(癌症标记物1和癌症标记物2,例如,在一些实施方案中,使用癌症标记物1作为捕获靶标,其中检测探针针对癌症标记物2)检测患者样品中的癌症(例如,卵巢囊腺癌)。第一个实验展示了在pbs中使用本文所述的双链体系统测定检测两种不同的癌细胞系衍生的细胞外囊泡(cld
‑
ev)。参见例如,图19。
[0544]
使用此种能够检测cld
‑
ev的双链体系统测定,进行了含有来自每个阶段(阶段i至阶段iv)和/或亚型的癌症以及来自不同对照组(例如,健康受试者、患有良性肿瘤的受试者和非靶癌症受试者)的患者样品的研究。请参见实施例6和图21至图22,其显示了用于检测癌症(例如,卵巢癌)的示例性双链体系统测定的性能。
[0545]
示例性测定概述
[0546]
在一些实施方案中,本文所述的靶实体检测系统为双链体系统。在一些实施方案中,此种双链体系统(例如,如图2a所示)使用各自识别不同表位的两种抗体。成对的双链模板dna也用于qpcr,每个双链模板dna都具有与其配偶体上的5'悬突互补的特定四碱基5'悬突。每个抗体都与两个双链dna模板中的一个缀合。当抗体结合它们的靶表位时,相应模板的粘性末端可杂交。在pcr扩增之前,这些粘性末端然后通过t7连接酶连接在一起。为了在两个dna模板之间发生杂交,两个抗体需要彼此足够紧密地结合(在50nm至60nm内,即dna接头和抗体的长度)。结合但保持未连接的任何模板都不会产生pcr产物,如图2a所示。
[0547]
健康对照与阶段i、阶段ii、阶段iii和阶段iv癌症患者血浆:
[0548]
对来自健康对照和癌症患者(例如,患有卵巢癌的患者)的血浆样品进行处理以获得纯化的细胞外囊泡,使用如下所述的示例性测定对其进行询问。
[0549]
使用与抗癌标记物1抗体共价缀合的磁珠捕获纯化的ev。使用一组两个检测探针对由珠捕获的ev进行分析,每个检测探针包含针对癌症标记物2的抗体和不同的寡核苷酸结构域(例如,如本文所述的那些)。
[0550]
仔细选择癌症标记物1和癌症标记物2的生物标记物组合,以最小化与健康组织来源的细胞外囊泡的交叉反应。此种生物标记物组合与健康组织的交叉反应性部分地是通过使用靶癌症(例如,卵巢囊腺癌)中差异表达的mrna的热图进行生物信息学预测的。因此,可预测与来自健康组织的细胞外囊泡表面相比,癌症相关细胞外囊泡表面上的标记物的不同组合要丰富得多。
[0551]
表5.以下生物标记物组合的转录表达分数,如在某些癌细胞系与阴性对照细胞系(例如,非癌细胞系)中表达的
[0552]
基因阳性细胞系1阳性细胞系2阴性细胞系癌症标记物1
‑
癌症标记物2
‑
[0553]
示例性方法:
[0554]
寡核苷酸
[0555]
在一些实施方案中,寡核苷酸可具有以下序列结构和修饰。应当注意,下面的链数对应于与图2a中所示的链相关的数值。
[0556]
链1v1:
[0557]
/5aziden/cagtctgacacagcagtcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5aziden/是指通过nhs酯接头连接到5'寡核苷酸末端的叠氮基团,或
[0558]
/5ammc12/cagtctgacacagcagtcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基),或
[0559]
/5thiolmc6/cagtctgacacagcagtcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5thiolmc6/是指通过6碳间隔基连接到5'寡核苷酸末端的硫醇。
[0560]
链2v1:
[0561]
/5aziden/gacctgacctacagtgaccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5aziden/是指通过nhs酯接头连接到5'寡核苷酸末端的叠氮基团,或
[0562]
/5ammc12/gacctgacctacagtgaccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammcl/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基),或
[0563]
/5thiolmc6/gacctgacctacagtgaccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5thiolmc6/是指通过6碳间隔基连接到5'寡核苷酸末端的硫醇
[0564]
链3v1:
[0565]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgactgctgtgtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0566]
链4v1:
[0567]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggtcactgtaggtcaggtc,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0568]
链5v1:
[0569]
cagtctgacacagcagtcgt
[0570]
链6v1:
[0571]
gacctgacctacagtgacca
[0572]
链7(探针)v1:
[0573]
/56
‑
fam/tggctagac/zen/agaggtgtactcctagtgaga/3iabkfq/,其中/56
‑
fam/是指位于5'寡核苷酸末端的荧光素(例如,6
‑
fam);并且/3iabkfq/是指位于3'寡核苷酸末端的荧光素猝灭剂
[0574]
在一些实施方案中,寡核苷酸可具有以下序列结构和修饰。应当注意,下面的链数对应于与图2a中所示的链相关的数值。
[0575]
链1v2:
[0576]
/5aziden/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5aziden/是指通过nhs酯接头连接到5'寡核苷酸末端的叠氮基团,或
[0577]
/5ammc12/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基),或
[0578]
/5thiolmc6/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5thiolmc6/是指通过6碳间隔基连接到5'寡核苷酸末端的硫醇
[0579]
链2v2:
[0580]
/5aziden/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5aziden/是指通过nhs酯接头连接到5'寡核苷酸末端的叠氮基团,或
[0581]
/5ammc12/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammcl/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基),或
[0582]
/5thiolmc6/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5thiolmc6/是指通过6碳间隔基连接到5'寡核苷酸末端的硫醇
[0583]
链3v2:
[0584]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0585]
链4v2:
[0586]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggacttcgtaggtctggtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0587]
链5v2:
[0588]
cagtctgactcaccactcgt
[0589]
链6v2:
[0590]
caccagacctacgaagtcca
[0591]
链7(探针)v2:
[0592]
/56
‑
fam/tggctagac/zen/agaggtgtactcctagtgaga/3iabkfq/,其中/56
‑
fam/是指位于5'寡核苷酸末端的荧光素(例如,6
‑
fam);并且/3labkfq/是指位于3'寡核苷酸末端的荧光素猝灭剂
[0593]
抗体
‑
寡核苷酸(例如,抗体
‑
dna)缀合:
[0594]
例如,使用无铜点击化学,将针对靶标记物(例如,癌症标记物2)的抗体的60ug等分试样与杂交的链1 3和链2 4缀合。第一步是制备dbco功能化抗体以参与与叠氮化物修饰的寡核苷酸结构域(例如,dna结构域)的缀合反应。这开始于抗体与dbco
‑
peg5
‑
nhs异源双功能交联剂的反应。在室温下使nhs酯和可用赖氨酸基团之间的反应进行2小时,之后使用离心超滤去除未反应的交联剂。为了完成缀合,使叠氮化物修饰的寡核苷酸结构域(例如,dna结构域)和dbco功能化抗体在室温下反应过夜。
[0595]
细胞培养
[0596]
使阴性对照细胞(例如,非靶癌细胞,诸如黑色素瘤细胞或健康细胞)在具有10%无外泌体fbs和50单位的青霉素/链霉素/ml的伊格尔最小必需培养基(emem)中生长。使癌细胞(例如,卵巢癌细胞)在具有10%无外泌体fbs和50单位的青霉素/链霉素/ml的roswell park memorial institute(rpmi 1640)中生长。可用于开发用于检测癌症的测定法的示例
性癌细胞系(例如,如本文所述的那些)包括但不限于a2780、caov
‑
3、cov413a、es2、ovcar
‑
3、ov90、pa
‑
1、sk
‑
ov
‑
3、sw 626、tov
‑
112以及描述于ince等人,“characterization of twenty
‑
five ovarian tumor cell lines that phenocopy primary tumours”nature communications 6:7419(2015)中的细胞系。所有细胞系均保持在5%co2和37℃下,并且传代数低于20。
[0597]
从细胞培养基中纯化细胞外囊泡
[0598]
在一些实施方案中,癌细胞(例如,卵巢癌细胞)和阴性对照细胞在它们各自的培养基中生长,直到它们达到
‑
80%汇合。收集细胞培养基并在室温(rt)下以300x ref旋转5分钟以去除细胞和碎片。然后收集上清液并在
‑
80℃下冷冻。
[0599]
使用前,将储存在
‑
80℃下的冷冻上清液解冻,然后澄清细胞和大的(例如,直径大于1微米)细胞碎片。使用离心澄清解冻的上清液。
[0600]
在一些实施方案中,使澄清的细胞培养基(例如,
‑
500ul)通过尺寸排阻纯化柱。为每个样品收集具有约65nm至约1000nm大小范围的纳米颗粒。在一些实施方案中,可能需要较小的颗粒范围。
[0601]
颗粒计数:
[0602]
例如用使用ts400芯片的spectrodyne颗粒计数仪器获得颗粒计数,以测量65nm和1000nm之间的纳米颗粒范围。在一些实施方案中,可能需要较小的颗粒范围。
[0603]
全血浆澄清:
[0604]
在ev纯化之前,不参与样品处理的人员对样品进行盲检。患者身份信息仅在实验完成后才显示出来,以便进行数据分析。从
‑
80℃下的储存中取出1ml等分的全血浆,并对其进行三次澄清旋转以去除细胞、血小板和碎片。
[0605]
从澄清血浆中纯化ev的尺寸排阻色谱法:
[0606]
每个澄清的血浆样品都通过单次使用的尺寸排阻纯化柱来分离ev。为每个样品收集具有约65nm至约1000nm大小范围的纳米颗粒。在一些实施方案中,可能需要较小的颗粒范围。
[0607]
捕获抗体与磁性捕获珠的缀合:
[0608]
将抗体缀合至磁珠。简而言之,在无菌环境中对珠进行称重并将其重悬于缓冲液中。将抗体与功能化珠混合,并在直立圆筒混合的情况下发生缀合反应。使用缀合试剂盒提供的洗涤缓冲液将珠洗涤数次,并在4℃下储存在所提供的储存缓冲液中。
[0609]
使用抗体缀合的磁珠直接捕获纯化的血浆ev:
[0610]
对于ev捕获,例如在室温下,将纯化的血浆ev的稀释样品与缀合有针对ev靶标(例如,癌症标记物1)的抗体的磁珠一起孵育适当的时间段。
[0611]
抗体
‑
寡核苷酸缀合物与结合在磁性捕获珠上的ev的结合:
[0612]
抗体
‑
寡核苷酸缀合物(“抗体探针”)以其最佳浓度在适当的缓冲液中稀释,所述抗体
‑
寡核苷酸缀合物针对不同于ev捕获测定(例如,上文所述的测定)中使用的ev靶标(例如,癌症标记物2)。允许抗体探针与包含结合在磁性捕获珠上的ev的样品相互作用。
[0613]
结合后洗涤:
[0614]
在一些实施方案中,将样品在适当的缓冲液中洗涤(例如,多次洗涤)。
[0615]
连接:
[0616]
洗涤以去除未结合的抗体
‑
寡核苷酸缀合物后,将具有结合的细胞外囊泡和结合的抗体
‑
寡核苷酸缀合物的珠与连接混合物接触。将混合物在rt下孵育20分钟。
[0617]
pcr:
[0618]
连接后,将具有结合的细胞外囊泡和结合的抗体
‑
寡核苷酸缀合物的珠与pcr混合物接触。例如,在quant studio3上使用以下示例性pcr方案在96孔板中进行pcr:在95℃下保持1分钟,进行在95℃下持续5秒和在62℃下持续15秒的50个循环。选择的温度变化率是标准的(每秒2℃)。每次实验重复进行一次qpcr反应,并且将rox用作被动参考以将qpcr信号归一化。然后从quant studio3机器下载数据,并在python 3.7中进行分析和绘制。
[0619]
数据分析:
[0620]
在一些实施方案中,二元分类系统可用于数据分析。在一些实施方案中,可基于参考信号将来自检测测定的信号归一化。例如,在一些实施方案中,通过选择参考样品来计算单个抗体双链体的归一化信号。在一些实施方案中,用于计算任意样品i的归一化信号的方程如下,其中signalmax是来自最高浓度细胞系ev标准的信号。
[0621]
δct
i
=ct
ref
‑
cti
[0622]
信号i=2
δcti
[0623][0624]
代表性结果:
[0625]
体外细胞系实验
[0626]
将纯化的细胞系ev在适当的缓冲液中稀释至最佳浓度,并使用癌症标记物1功能化珠(1ml重复)捕获。使用一对抗体探针分析捕获的ev,每个检测探针针对癌症标记物2。图19中提供了代表性qpcr数据和act值。数据显示,所测试的生物标记物组合(例如,与示例性测定组合,诸如像,如本实施例中所述和图1至图2b中所示)能够区分癌症衍生的ev与阴性对照细胞系,其信号强度与两个标记物的表达密切相关(参见表5)。
[0627]
试验性癌症患者血浆研究
[0628]
图20中提供了包括在试验性研究中的癌症患者(例如,卵巢癌患者)的人口统计资料。小心地在不同的样品群组中尽可能地匹配年龄和性别。
[0629]
如上所述对一毫升患者血浆样品进行澄清,并使用尺寸排阻色谱法纯化ev。使用抗癌标记物1磁珠捕获ev。使用针对癌症标记物2的抗体探针对由抗癌标记物1磁珠捕获的ev进行分析。请参见实施例6和图21至图22,其显示了用于检测癌症(例如,卵巢癌)的示例性双链体系统测定的性能。
[0630]
讨论:
[0631]
本实施例证明了与针对第二靶生物标记物的双链体检测测定(例如,如本实施例中所述和图1至图2b中所示)组合的针对第一靶生物标记物的捕获测定(例如,如本文所使用和/或描述的)(使得第一靶生物标记物和第二靶生物标记物的组合对靶癌症的检测具有特异性)能够以>99.5%的特异性检测早期癌症(例如,卵巢囊腺癌)。
[0632]
在一些实施方案中,可使用可为每个抗体添加多达16条寡核苷酸结构域(例如,dna)链的树枝化基元来代替每个抗体的一条或两条dna链,以例如增强信噪比。
[0633]
实施例6:癌症液体活检测定的开发
[0634]
本实施例描述了例如用于筛选遗传风险和平均风险受试者的癌症液体活检测定的开发。尽管是所有癌症中的第五大女性杀手(howlader等人,2019),但目前没有针对平均风险女性的推荐的卵巢癌筛选工具。这部分地是因为提出的卵巢癌筛选技术的性能不佳。鉴于平均风险女性的卵巢癌发病,检测特异性不足(<99.5%)导致假阳性结果超过真阳性结果不止一个数量级。这给医疗保健系统和接受筛选的女性带来了沉重负担,因为假阳性结果会导致另外的检查、不必要的手术和情绪/身体困扰(buys等人,2011)。因此,可能需要开发卵巢癌筛选测试,所述测试可表现出两个特征以提供临床效用:(1)超高特异性(>99.5%),以最小化假阳性数量,以及(2)当预后最有利时,对阶段i和阶段ii卵巢癌具有高灵敏度(>40%)。此种测试的开发有可能每年挽救数万人的生命。
[0635]
已经针对卵巢癌液体活检测定研究了几种不同的生物标记物类别,包括循环肿瘤dna(ctdna)、循环肿瘤细胞(ctc)、批量蛋白质和细胞外囊泡(ev)。相对于ctdna和ctc,ev由于其在血流中的丰度和稳定性而特别有希望,这表明ev对早期癌症的灵敏度有所提高。此外,ev含有源自同一细胞的货物(例如,蛋白质、rna、代谢物),从而提供优于批量蛋白质测量的特异性。虽然已经研究了ev的诊断效用,但大部分工作都与批量ev测量或低通量单ev分析有关。
[0636]
本实施例描述了通过使用如本文所述和/或使用的技术对人血浆中的单个细胞外囊泡(ev)进行分析来进行早期癌症检测的示例性方法的一个方面。ev(包括外泌体和微囊泡)含有共定位的蛋白质、rna、代谢物和代表其起源细胞的其他化合物(kosaka等人,2019)。检测单个ev内的共定位标记物可使得能够鉴定具有超高特异性的细胞类型,包括区分癌细胞与正常组织的能力。与依赖细胞死亡以使生物标记物进入血液(即cfdna)的其他癌症诊断方法相反,ev由功能细胞以高速率释放。已显示单细胞在体外每天释放多达10,000个ev(balaj等人,2011)。另外,人们普遍认为癌细胞比健康细胞释放ev的速率更高(bebelman等人,2018年)。
[0637]
在一个方面,用于检测测定的癌症相关生物标记物(例如,如本文所述和/或使用的)包括在癌症与健康组织中上调的基因,其可例如使用申请人的专有生物信息学生物标记物发现过程来鉴定。使用示例性个体ev测定(参见例如,图1或图2a至图2b中所示和/或本文所述),检测到此类生物标记物在单个囊泡上的共定位,这表明生物标记物的分组源自相同的细胞。鉴于许多上调的癌症生物标记物由一种或多种健康组织表达,这为批量生物标记物测量(包括批量ev测定)提供了优越的特异性。在一些实施方案中,本公开提供了具有超高特异性的技术,其作为癌症筛选测试特别有用,例如对于疾病患病率低且需要高阳性预测值(>10%)的卵巢癌(seltzer等人,1995年)。
[0638]
生物标记物发现
[0639]
在一些实施方案中,生物标记物发现过程利用对大型数据库的生物信息学分析以及对癌症(例如,卵巢癌)和细胞外囊泡的生物学的理解。
[0640]
单个细胞外囊泡分析
[0641]
检测血液中肿瘤来源的ev需要具有足够选择性和灵敏度的测定,以在来自各种各样的健康组织的100亿个ev的背景下检测每毫升血浆中相对较少的肿瘤来源的ev。本公开尤其提供了解决此挑战的技术。例如,在一些实施方案中,用于单个细胞外囊泡分析的测定在图1中说明,其在如下概述的三个关键步骤中进行:
[0642]
1.使用尺寸排阻色谱(sec)从患者血浆中纯化ev,所述尺寸排阻色谱去除超过99%的可溶性蛋白质和其他干扰化合物。
[0643]
2.使用对膜结合蛋白具有特异性的抗体功能化磁珠捕获肿瘤特异性ev。
[0644]
3.进行邻近连接免疫定量聚合酶链反应(pliq
‑
pcr)的改良版本,以确定包含在捕获的ev上或其中的另外的蛋白生物标记物的共定位。
[0645]
在pliq
‑
pcr测定的改良版本的许多实施方案中,将两种或多种不同的抗体
‑
寡核苷酸缀合物添加到由抗体功能化磁珠捕获的ev,并且抗体随后与其蛋白质靶标结合。寡核苷酸由具有互补的单链悬突的dsdna组成,并因此在紧密接近时(即,当相应的蛋白质靶标位于同一ev上时)能够杂交。在洗去未结合的抗体
‑
寡核苷酸物种后,使用标准dna连接酶反应连接相邻结合的抗体
‑
寡核苷酸物种。连接模板链的后续qpcr使得能够对共定位的蛋白质物种进行检测和相对定量。在一些实施方案中,可将二至二十种不同的抗体
‑
寡核苷酸探针并入例如涉及所提供的靶实体检测系统的此种测定中。
[0646]
与其他技术相比,pliq
‑
pcr在分析ev方面具有许多优点。例如,pliq
‑
pcr的灵敏度比其他标准免疫测定法(诸如elisa)高三个数量级(darmanis等人,2010)。良好优化的pliq
‑
pcr反应的超低lod使得能够检测微量水平的肿瘤来源的ev,低至一千个ev/ml。这与其他新兴的ev分析技术相比更为有利,所述技术包括纳米等离子体外泌体(nplex)传感器(im等人,2014)和集成磁电化学外泌体(imex)传感器(jeong等人,2016年),它们分别报告了约103ev和约104ev的lod(shao等人,2018)。此外,在一些实施方案中,pliq
‑
pcr方法的改良版本不需要复杂的设备,并且可独特地检测多个生物标记物在单个ev上的共定位。
[0647]
在一些实施方案中,为了进一步提高单个ev谱分析的灵敏度和特异性,包括mrna和囊泡内蛋白质(除了ev表面蛋白质之外)的其他类别的ev生物标记物可被鉴定并包括在测定中。
[0648]
初步工作
[0649]
通过初步研究,开发了工作流程,其中验证生物标记物候选物存在于ev中,并且能够被可商购获得的抗体或mrna引物探针组检测到。对于给定的关注的生物标记物,培养表达(阳性对照)和不表达关注的生物标记物(阴性对照)的一个或多个细胞系可通过浓缩其细胞培养基并进行纯化以分离具有关注的大小范围的纳米颗粒(例如,使用sec)来培养以收获其ev。通常,细胞外囊泡的直径可在30纳米至几微米的范围内。参见例如,chuo等人,“imaging extracellular vesicles:current and emerging methods”journal of biomedical sciences 25:91(2018),其提供不同细胞外囊泡(ev)亚型的大小信息:迁移小体(0.5pm至3pm)、微囊泡(0.1pm至1pm)、原癌小体(1pm至10pm)、外泌颗粒(exomere)(<50nm)、小外泌体(60nm至80nm)和大外泌体(90nm至120nm)。在一些实施方案中,可分离大小范围为约30nm至1000nm的纳米颗粒以用于检测测定。在一些实施方案中,可分离一个或多个特定ev亚型以用于检测测定。
[0650]
通过专有的生物标记物发现过程,鉴定了在癌症(例如,卵巢癌)与健康组织中上调的两种膜结合蛋白生物标记物,并将其用于细胞系ev和癌症患者样品的概念验证实验。
[0651]
为了检测来自含有共定位的癌症标记物1和癌症标记物2的ev的测定信号,所述组合是癌症(例如,卵巢癌)的特异性检测,在一些实施方案中,开发了涉及针对癌症标记物1的免疫亲和捕获和针对癌症标记物2的两个不同抗体
‑
寡核苷酸探针的测定配置。
[0652]
使用抗癌标记物1功能化磁珠捕获纯化的细胞系ev。例如,图19(图a)提供了两种阳性对照细胞系和一种阴性对照细胞系的代表性qpcr轨迹。数据表明基因表达对测定信号的影响,其中较高表达的细胞系相对于较低表达的细胞系表现出信号增加36倍(2
5.2
)。这些结果表明,在一些实施方案中,单个ev谱测定(例如,本文所述的那些)能够以非常高的灵敏度检测单个ev上的共定位的膜结合蛋白标记物。
[0653]
在用癌细胞系ev验证涉及捕获测定和检测测定的组合的癌症检测测定(例如,如图1和图2a至图2b中所示或本文所述)之后,使用优化且操作员盲法的测定方案对癌症患者血浆样品(例如,卵巢癌患者血浆样品)进行试验性研究(最终扩展到320个患者样品)。所有血浆样品均购自同一来源,根据相同的采血方案对其进行处理,并且在开始任何治疗之前(即治疗初期(treatment naive))收集患者样品。本实施例的研究中包括的患者群组在图20中进行了描述。
[0654]
此临床试验性研究的结果在图21中提供。通过假设所有健康对照(n=172)周围的对数正态分布,并且对于99.8%的特异性,将截止值设置为高于平均值(截止值1)2.879个标准偏差,且对于98%的特异性,将截止值设置为高于平均值(截止值2)2.055个标准偏差。仅以举例的方式,在卵巢癌的情况下,99.8%的特异性用于评估筛选平均风险女性的ppv,其中使用了每10,000名女性中5.7名的患病率。98%的特异性截止值用于计算筛选遗传风险女性的ppv,其中患病率为约每100名女性中1名。建立这些单独的截止值是为了解释不同患者群体之间假阳性耐受性的差异。这些结果表明,在一些实施方案中,单个ev谱测定(例如,如本文所述)具有用作癌症筛选测试的巨大潜力。在一些实施方案中,可例如通过包括针对一个或多个另外的生物标记物的一组或多组检测探针(例如,如本文所述)来提高此种测定的灵敏度。在一些实施方案中,一个或多个此类生物标记物可包括例如但不限于膜结合蛋白和囊泡内mrna/蛋白。
[0655]
在一些实施方案中,证明了使用批量纯化的细胞系ev进行ev
‑
mrna检测的可行性,如图23(图a)所示,用于检测与靶癌症相关的转录物。通过对膜结合蛋白标记物的免疫亲和捕获,此种方法使得能够检测两个共定位的生物标记物。此外,ev
‑
mrna检测需要更简单的方案,因为rt
‑
qpcr可在免疫亲和捕获后直接进行。图23(图b)展示了使用ev的mrna检测,其中首先使用抗ev标记物1修饰的磁珠捕获ev,并检测到ev标记物2mrna。阳性细胞系和阴性细胞系都表达ev标记物2,然而,只有阳性细胞系表达ev标记物1。证明了使用此种检测系统,即使在比阴性细胞系ev浓度高一个数量级的情况下,也能选择性地检测到阳性细胞系。
[0656]
在一些实施方案中,用于检测单个ev中的靶生物标记物特征(包含多个靶生物标记物)的癌症液体活检测定包括:(a)免疫亲和捕获测定(例如,如本文所述),其针对至少一个或多个靶生物标记物(“一个或多个捕获生物标记物”);以及(b)包含本文所述的靶实体检测系统(例如,如图2a所示)的检测测定,其针对与一个或多个捕获生物标记物不同的靶生物标记物特征的至少一个或多个靶生物标记物。在一些实施方案中,此种检测测定还可包括针对此种靶生物标记物特征的一个或多个靶生物标记物的ev
‑
mrna检测测定(例如,如上所述)。
[0657]
实施例7:检测探针的寡核苷酸结构域的长度对测定信号的影响
[0658]
本实施例描述了针对不同靶标的检测探针的合成,每个靶标包含靶结合部分和偶联至靶结合部分的各种长度的寡核苷酸结构域(包含双链部分和单链悬突)。本实施例进一
步证明检测探针的寡核苷酸结构域的长度可影响靶实体检测系统(例如,本文所述的那些)和/或使用所述系统的方法的性能。
[0659]
为了评估寡核苷酸结构域长度对靶实体检测系统(例如,本文所述的双链体靶实体检测系统)的性能(例如,测定信号)的影响,合成了具有与三种不同长度(如下所述)的寡核苷酸结构域缀合的抗体剂的检测探针:
[0660]
·
长度1(“长”):69个至73个核苷酸(69个核苷酸长的双链部分,其中单链悬突的长度为4个核苷酸)
[0661]
·
长度2(“中等”):40个至44个核苷酸(40个核苷酸长的双链部分,其中单链悬突的长度为4个核苷酸)
[0662]
·
长度3(“短”):20个至24个核苷酸(20个核苷酸长的双链部分,其中单链悬突的长度为4个核苷酸)
[0663]
两种细胞系细胞外囊泡(ev)用作此实验的阳性对照:hcc4006和t84。此实验的阴性对照是不含ev的捕获珠。使用抗靶1功能化磁珠捕获ev,并使用抗靶1和抗靶2检测探针产生测定信号。表6总结了这些蛋白质在细胞系ev中的表达。
[0664]
表6.每百万转录本(tpm)分数,以hcc4006和t84细胞系表示。
[0665][0666]
示例性方法:
[0667]
寡核苷酸
[0668]
在一些实施方案中,寡核苷酸可具有以下序列结构和修饰。应当注意,下面的链数对应于与图2a中所示的链相关的数值。还应注意,寡核苷酸官能化可从一个官能团切换到另一个官能团(例如,从胺到叠氮化物到硫醇等)。
[0669]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成长度1(“长”)的寡核苷酸结构域:
[0670]
链1v1:
[0671]
/5ammc12/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基);或
[0672]
链2v1:
[0673]
/5ammc12/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0674]
链3v1:
[0675]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0676]
链4v1:
[0677]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggacttcgtaggtctggtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0678]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成长度1(“长”)的寡核苷酸结构域:
[0679]
链1v2:
[0680]
/5ammc12/cagtctgacacagcagtcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基);或
[0681]
链2v2:
[0682]
/5ammc12/gacctgacctacagtgaccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0683]
链3v2:
[0684]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgactgctgtgtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0685]
链4v2:
[0686]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggtcactgtaggtcaggtc,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0687]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成长度2(“中等”)的寡核苷酸结构域:
[0688]
链1v1
‑
中等:
[0689]
/5ammc12/cagtctgactcaccactcgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0690]
链2v1
‑
中等:
[0691]
/5ammc12/caccagacctacgaagtccattggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0692]
链3v1
‑
中等:
[0693]
/5phos/gagtacacctctgtctagccagtcacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0694]
链4v1
‑
中等:
[0695]
/5phos/actcctagtgagaccaggagccaatggacttcgtaggtctggtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0696]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成长度2(“中等”)的寡核苷酸结构域:
[0697]
链1v2
‑
中等:
[0698]
/5ammc12/cagtctgacacagcagtcgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0699]
链2v2
‑
中等:
[0700]
/5ammc12/gacctgacctacagtgaccattggctcctggtctcactag,其中/5ammc12/是指通
过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0701]
链3v2
‑
中等:
[0702]
/5phos/gagtacacctctgtctagccagtcacgactgctgtgtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0703]
链4v2
‑
中等:
[0704]
/5phos/actcctagtgagaccaggagccaatggtcactgtaggtcaggtc,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0705]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成长度3(“短”)的寡核苷酸结构域:
[0706]
链1v1
‑
短:
[0707]
/5ammc12/cagtctgactcaccactcgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0708]
链2v1
‑
短:
[0709]
/5ammc12/caccagacctacgaagtcca,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0710]
链3v1
‑
短:
[0711]
/5phos/gagtacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0712]
链4v1
‑
短:
[0713]
/5phos/actctggacttcgtaggtctggtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0714]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成长度3(“短”)的寡核苷酸结构域:
[0715]
链1v2
‑
短:
[0716]
/5ammc12/cagtctgacacagcagtcgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0717]
链2v2
‑
短:
[0718]
/5ammc12/gacctgacctacagtgacca,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0719]
链3v2
‑
短:
[0720]
/5phos/gagtacgactgctgtgtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0721]
链4v2
‑
短:
[0722]
/5phos/actctggtcactgtaggtcaggtc,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0723]
链5v1:
[0724]
cagtctgacacagcagtcgt
[0725]
链6v1:
[0726]
gacctgacctacagtgacca
[0727]
链5v2:
[0728]
cagtctgactcaccactcgt
[0729]
链6v2:
[0730]
caccagacctacgaagtcca
[0731]
抗体
‑
寡核苷酸(例如,抗体
‑
dna)缀合:
[0732]
如先前实施例中所述,将针对所需靶标的抗体缀合至寡核苷酸。本领域技术人员将理解,可使用其他已知的缀合方法来形成抗体
‑
寡核苷酸缀合物。
[0733]
细胞培养
[0734]
使hcc
‑
4006细胞在具有10%无外泌体fbs和50单位的青霉素/链霉素/ml的roswell park memorial institute(rpmi 1640)中生长。使t84细胞在具有5%无外泌体胎牛血清(fbs)和50单位的青霉素/链霉素/ml的1:1达尔伯克改良伊格尔培养基(dmem):汉姆氏f12培养基中生长。所有细胞系均保持在5%co2和37℃下,并且传代数低于20。
[0735]
从细胞培养基中纯化细胞外囊泡
[0736]
在一些实施方案中,细胞在它们各自的培养基中生长,直到它们达到
‑
80%汇合。收集细胞培养基并在室温(rt)下以300x ref旋转5分钟以去除细胞和碎片。然后收集上清液并在
‑
80℃下冷冻。
[0737]
使用前,将储存在
‑
80℃下的冷冻上清液解冻,然后澄清细胞和大的(例如,直径大于1微米)细胞碎片。使用离心澄清解冻的上清液。
[0738]
在一些实施方案中,使澄清的细胞培养基(例如,
‑
500ul)通过尺寸排阻纯化柱。为每个样品收集具有约65nm至约1000nm大小范围的纳米颗粒。在一些实施方案中,可能需要较小的颗粒范围。
[0739]
颗粒计数:
[0740]
例如用使用ts400芯片的spectrodyne颗粒计数仪器获得颗粒计数,以测量65nm和1000nm之间的纳米颗粒范围。在一些实施方案中,可能需要较小的颗粒范围,例如65nm和200nm之间。
[0741]
捕获抗体与磁性捕获珠的缀合:
[0742]
将抗体缀合至磁珠。简而言之,在无菌环境中对珠进行称重并将其重悬于缓冲液中。将抗体与功能化珠混合,并在直立圆筒混合的情况下发生缀合反应。使用缀合试剂盒提供的洗涤缓冲液将珠洗涤数次,并在4℃下储存在所提供的储存缓冲液中。
[0743]
使用抗体缀合的磁珠直接捕获纯化的血浆ev:
[0744]
对于ev捕获,例如在室温下,将细胞系ev的稀释样品与缀合有针对ev靶标(例如,靶标1)的抗体的磁珠一起孵育适当的时间段。
[0745]
抗体
‑
寡核苷酸缀合物与结合在磁性捕获珠上的ev的结合:
[0746]
抗体
‑
寡核苷酸缀合物(“抗体探针”)以其最佳浓度在适当的缓冲液中稀释,所述抗体
‑
寡核苷酸缀合物针对不同于ev捕获测定(例如,上文所述的测定)中使用的ev靶标(例如,靶标2)。允许抗体探针与包含结合在磁性捕获珠上的ev的样品相互作用。
[0747]
结合后洗涤:
[0748]
在一些实施方案中,将样品在适当的缓冲液中洗涤(例如,多次洗涤)。
[0749]
连接:
[0750]
洗涤以去除未结合的抗体
‑
寡核苷酸缀合物后,将具有结合的细胞外囊泡和结合的抗体
‑
寡核苷酸缀合物的珠与连接混合物接触。将混合物在rt下孵育20分钟。
[0751]
pcr:
[0752]
连接后,将具有结合的细胞外囊泡和结合的抗体
‑
寡核苷酸缀合物的珠与pcr混合物接触。例如,在quant studio 3上使用以下示例性pcr方案在96孔板中进行pcr:在95℃下保持1分钟,进行在95℃下持续5秒和在62℃下持续15秒的50个循环。选择的温度变化率是标准的(每秒2℃)。每次实验重复进行一次qpcr反应,并且将rox用作被动参考以将qpcr信号归一化。然后从quant studio 3机器下载数据,并在python 3.7中进行分析和绘制。
[0753]
代表性结果:
[0754]
寡核苷酸结构域长度实验的原始qpcr图在图24中提供,并且相应的δct数据在图25中提供。数据表明,对于此种生物标记物组合,寡核苷酸长度的减少导致更强的测定信号。将dna长度从69个至73个核苷酸减少到20个至24个核苷酸导致信号增加约2.5ct。此外,较短的dna长度不会显着增加测定背景信号(无ev数据),从而导致背景增加少于1ct。
[0755]
讨论:
[0756]
在此实验中,减少寡核苷酸长度导致来自免疫亲和捕获的ev的测定信号增加。短寡核苷酸产生比长寡核苷酸强约2.5ct的信号,其中测定背景仅稍微增加(<1ct)。然而,不希望受理论束缚,此观察结果可能不适用于某些生物标记物组合。在一些实施方案中,当靶标1和靶标2可彼此相互作用以形成同源二聚体和/或异源二聚体,和/或紧密接近地存在于ev的膜上时,较短的dna长度可能更理想。在一些实施方案中,当靶标1和靶标2彼此不相互作用和/或稀疏地存在于ev的膜上时,较长的dna长度可能更理想。因此,这些结果表明寡核苷酸长度可被配置为提高本文所述的靶实体检测系统和/或测定的性能。
[0757]
实施例8:在靶实体检测系统中结合检测探针使用一个或多个抑制剂探针
[0758]
本实施例描述了针对不同靶标的检测探针的合成,每个靶标包含靶结合部分和偶联至靶结合部分的寡核苷酸结构域(包含双链部分和单链悬突)。本实施例还描述了针对非靶标(例如,与靶实体无关和/或与疾病、病症或病状无关的那些)的抑制剂探针的合成。本实施例证明添加不含引物位点的寡核苷酸结构域(例如,包含双链dna部分)可防止由非靶实体产生的连接模板的扩增。本实施例还证明将此种寡核苷酸结构域(不含引物位点)与针对非靶实体(例如,交叉反应性靶标)的靶结合实体缀合可减少来自非靶实体的背景信号,从而增加本文所述的靶实体检测测定的信噪比。在一些实施方案中,本实施例证明将此种寡核苷酸结构域(包含双链dna部分而不含引物位点,例如,如图26所示)与针对非靶实体(例如,交叉反应性靶标)的靶结合实体(例如,抗体剂)缀合可减少来自非靶实体(例如,来自非靶标组织的细胞外囊泡)的背景信号,从而增加本文所述的检测靶实体(例如,来自靶组织的细胞外囊泡)的靶实体检测测定的信噪比。在一些此类实施方案中,结合靶特异性检测探针使用此类抑制剂探针可用于检测癌症特异性细胞外囊泡。
[0759]
实验1:溶液中不含靶结合部分的抑制剂探针的评估:首先,评估由600pm浓度(或在2x抑制剂链的情况下为1200pm)的以下dna溶液产生的连接模板的相对数量。应当注意,下面的数字是指与图26中所示的链相关的数值对应的链数。“i”表示抑制剂探针的链。还应注意,寡核苷酸官能化可从一个官能团切换到另一个官能团(例如,从胺到叠氮化物到硫醇等)。
[0760]
1.(1 3)
[0761]
2.(2 4)
[0762]
3.(1i 3i)
[0763]
4.(2i 4i)
[0764]
5.(1 3) (2 4)
[0765]
6.(1 3) (2i 4i)
‑
如圖26所示
[0766]
7.(1i 3i) (2 4)
[0767]
8.(1i 3i) (2i 4i)
[0768]
9.(1 3) (2 4) (1i 3i)
[0769]
10.(1 3) (2 4) (2i 4i)
[0770]
11.(1 3) (2 4) 2x(1i 3i)
[0771]
12.(1 3) (2 4) 2x(2i 4i)
[0772]
13.(1 3) (2 4) (1i 3i) (2i 4i)
[0773]
示例性dna链序列在下面的示例性方法部分中提供。双链dna(例如,(1 3)、(2 4)等)是通过将适当的单链序列退火在一起来制备的。
[0774]
按照制造商建议的时间和温度,在室温下将每个双链dna或双链dna的组合在30pl t4连接酶溶液中以600pm的浓度孵育20分钟。连接后,将5μl连接酶混合物以一式两份转移到25pl pcr混合物中,其中所述pcr混合物含有taqman advanced master mix (thermo)、引物、evagreen、dmso和水。通过标准qpcr方案分析pcr混合物,并且测量可扩增转录物的相对丰度。
[0775]
示例性方法:
[0776]
寡核苷酸
[0777]
在一些实施方案中,寡核苷酸可具有以下序列结构和修饰。如上所述,下面的链数对应于与图26中所示的链相关的数值。寡核苷酸官能化可从一个官能团切换到另一个官能团(例如,从胺到叠氮化物到硫醇等)。
[0778]
i.用于检测探针的寡核苷酸结构域的寡核苷酸
[0779]
在一些实施方案中,下面提供了一组示例性寡核苷酸以形成检测探针的寡核苷酸结构域。
[0780]
链1:
[0781]
/5ammc12/cagtctgactcaccactcgttaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5
′
寡核苷酸末端的氨基(例如,伯氨基)
[0782]
链2:
[0783]
/5ammc12/caccagacctacgaagtccatagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0784]
链3:
[0785]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattaacgagtggtgagtcagactg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0786]
链4:
[0787]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctatggacttcgtaggtctggtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0788]
链5:
[0789]
cagtctgactcaccactcgt
[0790]
链6:
[0791]
caccagacctacgaagtcca
[0792]
在一些实施方案中,如实施例7中所述的不同长度的任何示例性寡核苷酸组可用于形成检测探针的寡核苷酸结构域。
[0793]
ii.用于抑制剂探针的寡核苷酸结构域的寡核苷酸
[0794]
在一些实施方案中,可合成具有三种不同长度(如下所述)的寡核苷酸结构域(不含引物位点)的抑制剂探针:
[0795]
·
长度1(“长”):69个至73个核苷酸(69个核苷酸长的双链部分,其中单链悬突的长度为4个核苷酸)
[0796]
·
长度2(“中等”):40个至44个核苷酸(40个核苷酸长的双链部分,其中单链悬突的长度为4个核苷酸)
[0797]
·
长度3(“短”):20个至24个核苷酸(20个核苷酸长的双链部分,其中单链悬突的长度为4个核苷酸)
[0798]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成用于抑制剂探针的长度1(“长”)的寡核苷酸结构域:
[0799]
链1i:
[0800]
/5ammc12/gcacacacctcatcgtcttgtaatcgtcgctgctacccttgacatccgtgactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0801]
链2i:
[0802]
/5ammc12/cacaatctcgaccacgcaagtagccttgcctgattagccactgtccagtttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0803]
链3i:
[0804]
/5phos/gagtacacctctgtctagccagtcacggatgtcaagggtagcagcgacgattacaagacgatgaggtgtgtgc,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0805]
链4i:
[0806]
/5phos/actcctagtgagaccaggagccaaactggacagtggctaatcaggcaaggctacttgcgtggtcgagattgtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0807]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成用于抑制剂探针的长度2(“中等”)的寡核苷酸结构域:
[0808]
链1i
‑
中等:
[0809]
/5ammc12/gcacacacctcatcgtcttggactggctagacagaggtgt,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0810]
链2i
‑
中等:
[0811]
/5ammc12/cacaatctcgaccacgcaagttggctcctggtctcactag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0812]
链3i
‑
中等:
[0813]
/5phos/gagtacacctctgtctagccagtccaagacgatgaggtgtgtgc,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0814]
链4i
‑
中等:
[0815]
/5phos/actcctagtgagaccaggagccaacttgcgtggtcgagattgtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0816]
在一些实施方案中,以下提供了一组示例性寡核苷酸以形成用于抑制剂探针的长度3(“短”)的寡核苷酸结构域:
[0817]
链1i
‑
短:
[0818]
/5ammc12/gcacacacctcatcgtcttg,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0819]
链2i
‑
短:
[0820]
/5ammc12/cacaatctcgaccacgcaag,其中/5ammc12/是指通过12碳间隔基连接到5'寡核苷酸末端的氨基(例如,伯氨基)
[0821]
链3i
‑
短:
[0822]
/5phos/gagtcaagacgatgaggtgtgtgc,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0823]
链4i
‑
短:
[0824]
/5phos/actccttgcgtggtcgagattgtg,其中/5phos/是指连接到5'寡核苷酸末端的磷酸酯基团
[0825]
实验2:细胞系ev中的抑制剂探针的评估:对于此实验,使用与ev捕获剂(例如,针对ev表面蛋白的抗体(标记物1)缀合的磁珠)捕获细胞系ev。在添加或不添加针对非靶标(标记物3)的抑制剂探针的情况下,使用包含两个检测探针的双链体靶实体检测系统产生测定信号,每个检测探针针对靶标,即标记物2(其对于两个探针可为相同的靶标,或对于每个探针可为不同的靶标)。
[0826]
表7.每百万转录本(tpm)分数,以特定细胞系表示。
[0827][0828]
抗体
‑
寡核苷酸(例如,抗体
‑
dna)缀合:
[0829]
如先前实施例中所述,将针对所需靶标的抗体缀合至寡核苷酸。本领域技术人员将理解,可使用其他已知的缀合方法来形成抗体
‑
寡核苷酸缀合物。
[0830]
捕获抗体与磁性捕获珠的缀合:
[0831]
如先前实施例中所述,将抗体缀合至磁珠。
[0832]
使用抗体缀合的磁珠直接捕获纯化的细胞系ev:
[0833]
对于ev捕获,例如在室温下,将细胞系ev的稀释样品与缀合有针对ev靶标(例如,靶标1)的抗体的磁珠一起孵育适当的时间段。
[0834]
抗体
‑
寡核苷酸缀合物与结合在磁性捕获珠上的ev的结合:
[0835]
抗体
‑
寡核苷酸缀合物(“标记物2 标记物2探针”;也称为“抗体探针”)以其最佳浓度在适当的缓冲液中稀释,所述抗体
‑
寡核苷酸缀合物针对不同于ev捕获测定(例如,上文所述的测定)中使用的ev靶标(例如,靶标2)。允许抗体探针与包含结合在磁性捕获珠上的ev的样品相互作用。另外,还将抑制剂探针添加到混合物中,从而允许与包含结合在磁性捕获珠上的ev的样品相互作用。
[0836]
结合后洗涤:
[0837]
在一些实施方案中,将样品在适当的缓冲液中洗涤(例如,多次洗涤)。
[0838]
连接:
[0839]
洗涤以去除未结合的抗体
‑
寡核苷酸缀合物后,将具有结合的细胞外囊泡和结合的抗体
‑
寡核苷酸缀合物的珠与连接混合物接触。将混合物在rt下孵育20分钟。
[0840]
pcr:
[0841]
连接后,将具有结合的细胞外囊泡和结合的抗体
‑
寡核苷酸缀合物的珠与pcr混合物接触。例如,在quant studio 3上使用以下示例性pcr方案在96孔板中进行pcr:在95℃下保持1分钟,进行在95℃下持续5秒和在62℃下持续15秒的50个循环。选择的温度变化率是标准的(每秒2℃)。每次实验重复进行一次qpcr反应,并且将rox用作被动参考以将qpcr信号归一化。然后从quant studio 3机器下载数据,并在python 3.7中进行分析和绘制。
[0842]
代表性结果和讨论:
[0843]
实验1:溶液中抑制剂探针(不含靶结合部分)的评估:原始qpcr数据显示在图27中。如图28所示,每个抑制剂探针(不含靶结合部分)的ct值都存在浓度依赖性增加。添加相同浓度(600pm)的抑制剂探针导致信号降低大约ict。进一步添加抑制剂探针(不含靶结合部分)使信号再降低1ct。相对于2x浓度的单个抑制剂探针(不含靶结合部分),同时添加两个抑制剂探针(每个都不含靶结合部分)略微降低效果。不希望受理论束缚,这可能是由于抑制剂探针的链之间发生连接,这阻止了链抑制扩增反应。这些数据表明抑制剂探针的寡核苷酸结构域可成功地阻止连接时的扩增。
[0844]
实验2:细胞系ev中的抑制剂探针的评估:图29中的细胞系数据表明添加包含与寡核苷酸结构域缀合的靶结合部分(例如,抗体剂)而不含引物位点(例如,包含不含引物位点的双链dna部分)的抑制剂探针可成功且选择性地减弱测定信号。不希望受理论束缚,信号的适度减少可能是靶标2的同源二聚体性质的结果。鉴于大部分测定信号可能来自靶标2二聚体(它们本质上紧密接近),抑制剂探针对靶标3的作用可能会降低。然而,这些数据证明,可通过部署抑制剂探针来在靶实体检测测定(例如,如本文所述)中选择性地减少和/或消除来自的交叉反应组织的信号。例如,这由下表8中的示例概述。
[0845]
表8.使用抑制剂探针消除交叉反应组织。
[0846][0847]
引用文献
[0848]
balaj,l.,lessard,r.,dai,l.,cho,y.j.,pomeroy,s.l.,breakefield,x.o.and skog,j.,2011.tumour microvesicles contain retrotransposon elements and amplified oncogene sequences.nature communications,2,p.180
[0849]
bebelman,m.p.,smit,m.j.,pegtel,d.m.,and baglio,s.r.,2018.biogenesis and function of extracellular vesicles in cancer.pharmacology & therapeutics,188,pp.1
‑
11.
[0850]
buys,s.s.,partridge,e.,black,a.,johnson,c.c.,lamerato,l.,isaacs,c.,reding,d.j.,greenlee,r.t.,yokochi,l.a.,kessel,b.and crawford,e.d.,2011.effect of screening on ovarian cancer mortality:the prostate,lung,colorectal and ovarian(plco)cancer screening randomized controlled trial.jama,305(22),pp.2295
‑
2303.
[0851]
darmanis,s.,nong,r.y.,hammond,m.,gu,j.,alderborn,a.,vanelid,j.,siegbahn,a.,gustafsdottir,s.,ericsson,o.,landegren,u.and kamali
‑
moghaddam,m.,2010.sensitive plasma protein analysis by microparticle
‑
based proximity ligation assays.molecular&cellular proteomics,9(2),pp.327
‑
335.
[0852]
howlader n,noone am,krapcho m,miller d,brest a,yu m,ruhl j,tatalovich z,mariotto a,lewis dr,chen hs,feuer ej,cronin ka(eds).seer cancer statistics review,1975
‑
2016,national cancer institute.bethesda,md,https://seer.cancer.gov/csr/1975_2016/,based on november 2018 seer data submission,posted to the seer web site,april 2019.
[0853]
im,h.,shao,h.,park,y.i.,peterson,v.m.,castro,c.m.,weissleder,r.and lee,h.,2014.label
‑
free detection and molecular profiling of exosomes with a nano
‑
plasmonic sensor.nature biotechnology,32(5),p.490.
[0854]
jeong,s,park,j.,pathania,d.,castro,c.m.,weissleder,r.and lee,h.,2016.integrated magneto
‑
electrochemical sensor for exosome analysis.acs nano,10(2),pp.1802
‑
1809.
[0855]
shao,h.,im,h.,castro,c.m.,breakefield,x.,weissleder,r.and lee,h.,2018.new technologies for analysis of extracellular vesicles.chemical reviews,118(4),pp.1917
‑
1950.
[0856]
sun,l.,brentnall,a.,patel,s.,buist,d.s.,bowles,e.j.,evans,d.g.r.,eccles,d.,hopper,j.,li,s.,southey,m.and duffy,s.,2019.a cost
‑
effectiveness analysis of multigene testing for all patients with breast cancer.jama oncology.
[0857]
torre,l.a.,trabert,b.,desantis,c.e.,miller,k.d.,samimi,g.,runowicz,c.d.,gaudet,m.m.,jemal,a.and siegel,r.l.,2018.ovarian cancer statistics,2018.ca:a cancer journal for clinicians,68(4),pp.284
‑
296.
[0858]
等效方案
[0859]
本领域技术人员仅仅使用常规试验将认识到或者能够确定本文所描述的发明的具体实施方案的很多等效方案。应当理解,本发明涵盖所有变体、组合和排列,其中来自所列权利要求中的一个或多个的一个或多个限制、要素、条款、描述性术语等被引入从属于相同基本权利要求的另一权利要求中(或如相关的任何其他权利要求),除非另有说明或除非本领域普通技术人员很明显会出现矛盾或不一致。此外,还应理解,本发明的任何实施方案或方面都可明确地从权利要求中排除,而不管具体的排除是否在说明书中陈述。本发明的范围并不旨在限于上述描述,而是如以下权利要求中所述。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。