1.本发明属于药物制剂技术领域,具体涉及一种吸入用布地奈德混悬液的制备方法。
背景技术:
2.哮喘是以气道炎症、支气管收缩、气道高反应性为特征的肺部慢性疾病,中国当前约有4570万成人哮喘患者(kewu huang,et al.,2019,prevalence,risk factors,and management of asthma in china:a national cross
‑
sectional study),面临严峻的哮喘疾病负担。当疾病控制不佳时,会发生哮喘急性发作,重度急性发作可威胁患者生命。吸入用布地奈德混悬液是短效速效糖皮质激素,抗炎作用强,它能有效抑制支气管收缩物质的合成和释放从而减轻支气管平滑肌的收缩反应,减少炎性介质释放,降低气道高反应性,减少腺体分泌;同时全身性副作用较小,因此广泛应用于哮喘的治疗。
3.吸入用布地奈德混悬液包括布地奈德、表面活性剂、稳定剂、ph调节剂、渗透压调节剂及注射用水等。由于需要反复使用,且水性介质容易滋生微生物;因此吸入混悬液应是无菌制剂。
4.现有技术常用的灭菌方法有,如专利cn1173702c中所披露的原料药干热灭菌法,又如专利cn1098680c中所披露的总混悬液湿热蒸汽灭菌法。但这两种灭菌方法对热不稳定布地奈德会造成药物活性成份降解、有关物质增加的问题,或者使原料药粒径明显增加(使d
90
涨幅大于3μm),影响其吸入性能。即使采用后续二次分散步骤(如高压均质等)也很难将粒径减小至原料药初始粒径。
5.专利cn108403638a公开了一种将鼻用糖皮质激素原料药与表面活性剂及注射用水混合后湿热灭菌的方法,能制备有关物质含量较低的产品。鼻喷剂原料药粒径要求相对宽松,较大粒径更有利于原料药在鼻粘膜的吸附从而改善治疗效果;灭菌后需采用较为繁琐的助悬剂、主药分别进行均质分散才将其粒度恢复到灭菌前。但吸入制剂原料药粒径要求更小更严格,过大粒子在口腔、上呼吸道就发生沉积,而不能有效在肺部沉积,且灭菌后的粒径增长较难通过均质分散恢复到灭菌前,故该专利的方法并不适用于吸入用布地奈德混悬液的制备。
技术实现要素:
6.为了克服现有技术的不足,本发明提供了一种吸入用布地奈德混悬液的制备方法。该制备方法能够保证布地奈德粒径适于吸入途径用药,同时减少布地奈德的降解,进一步优化药液含量均匀度,提高产品质量。
7.为了实现上述发明目的,本发明采用的技术方案如下:
8.一种吸入用布地奈德混悬液的制备方法,所述吸入用布地奈德混悬液包括布地奈德、表面活性剂、稳定剂、ph调节剂、渗透压调节剂和注射用水;
9.所述制备方法包括将布地奈德与部分表面活性剂及部分注射用水混合后得到浓
配液,将剩余辅料混合得到辅料溶液;对浓配液进行湿热灭菌,然后和经过滤灭菌的辅料溶液混匀;
10.其中,所述浓配液中,布地奈德与注射用水的质量比为1:1~1:6,表面活性剂与注射用水的质量比为1:60~1:300,表面活性剂占总表面活性剂的质量百分比为1%~30%。
11.优选地,所述布地奈德的粒径d
90
不大于5μm。
12.更优选地,所述布地奈德的粒径d
90
为1~5μm。
13.优选地,所述浓配液中,布地奈德与注射用水的质量比为1:2.5~1:5.5。
14.优选地,所述浓配液中,表面活性剂与注射用水的质量比为1:100~1:260。
15.优选地,所述浓配液中,表面活性剂占总表面活性剂的质量百分比为1%~10%。
16.优选地,所述湿热灭菌的温度为100~140℃,更优选为115~127℃。
17.优选地,所述湿热灭菌的时间为8~60min,更优选为8~17min。
18.作为一个优选地实施方案,本发明提供的所述吸入用布地奈德混悬液的制备方法还包括控制湿热灭菌过程中的升温和灭菌完成后的降温速度。发明人在进一步的优化研究过程中发现,当控制湿热灭菌过程中的升温和灭菌完成后的降温速度时,布地奈德吸入混悬液产品中药物的粒度及有关物质水平增加幅度更小,产品的稳定性更高。根据阿伦尼乌斯经验方程k=ae
‑
ea/rt
,反应速率常数k是温度的函数,温度越高,反应速率常数越大。对于温度敏感的混悬灭菌产品,药物粒度的增长及降解有可能会发生在高温灭菌过程中,采用不同的灭菌升温和降温速度会影响药物的粒度及有关物质水平。同时,升降温过程的优化控制对浓配液的可分散性有明显改善作用,可进一步明显提高药液含量均匀度。
19.优选地,所述浓配液湿热灭菌过程中升温速度为4~30℃/min,更优选为4~25℃/min。
20.优选地,所述浓配液湿热灭菌完成后降温速度为2~30℃/min,更优选为2~20℃/min。
21.优选地,经过湿热灭菌的所述浓配液和过滤灭菌的所述辅料溶液通过搅拌或均质混匀;更优选通过均质混匀。
22.优选地,所述浓配液与所述辅料溶液混匀时,混合体系温度控制在20~50℃,更优选40~45℃。
23.所述辅料溶液按照本领域常规方法进行过滤除菌。
24.优选地,所述吸入用布地奈德混悬液,ph=4.0~5.0,布地奈德的终浓度为0.01%~0.20%,所述表面活性剂的终浓度为0.005%~0.020%,所述稳定剂的终浓度为0.005%~0.020%,所述渗透压调节剂的终浓度为0.5%~1.0%。
25.优选地,所述表面活性剂选自吐温20、司盘20、司盘80、吐温80、卵磷脂、聚氧乙烯烷基醚、聚氧硬脂酸盐、聚乙二醇、聚氧乙烯蓖麻油和泊洛沙姆的一种或几种。
26.优选地,所述稳定剂选自乙二胺四乙酸、乙二胺四乙酸钠盐和乙二胺四乙酸钙盐中的一种。
27.优选地,所述渗透压调节剂选自氯化钠、葡萄糖、甘露醇中的一种或几种。
28.优选地,所述ph调节剂选自枸橼酸/枸橼酸钠、磷酸二氢钠/磷酸氢二钠中的一种。
29.作为一个优选地实施方案,本发明提供的所述吸入用布地奈德混悬液的制备方法还包括无菌灌装的步骤。
30.本发明还有一个目的在于提供一种吸入用布地奈德混悬液,所述吸入用布地奈德混悬液通过上述制备方法制备得到。
31.本发明的有益效果在于:
32.与现有技术相比,本发明提供的吸入用布地奈德混悬液的制备方法通过灭菌过程的精细调控(控制浓配液中表面活性剂的添加比例,同时控制浓配液中原料药与注射用水、表面活性剂与注射用水的比例,并进一步优化灭菌过程的升温速度和灭菌完成后的降温速度)以及浓配液与辅料溶液的混匀温度控制,使得产品原料粒径适宜于吸入途径用药,同时减少布地奈德的降解,显著优化药液含量均匀度,从而提高产品质量。
具体实施方式
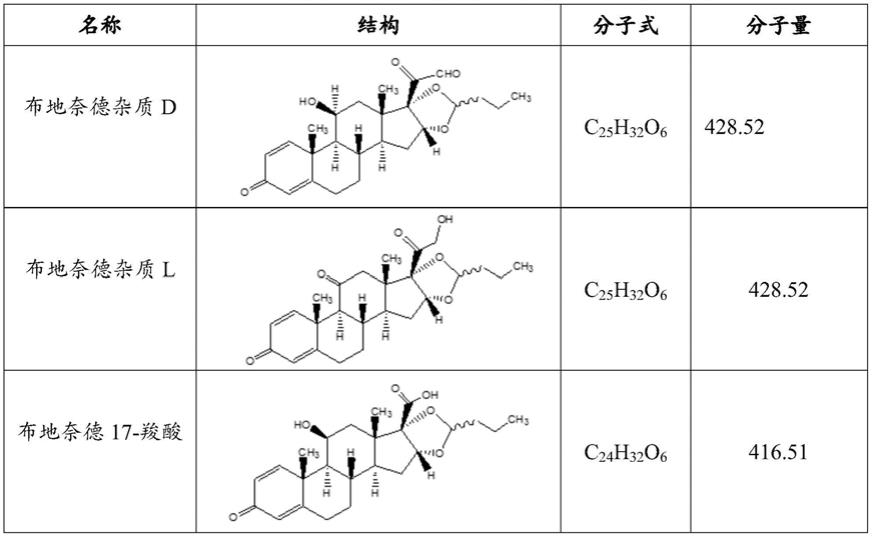
33.布地奈德属于热不稳定产品,在制备制剂过程中容易出现降解杂质及工艺杂质,因此需要严格控制产品中关键杂质的含量。吸入用布地奈德混悬液产品中常出现的关键杂质有3个,详情如表1所示。
34.表1 吸入用布地奈德混悬液产品中常出现的关键杂质
[0035][0036]
本发明人经深入研究发现,将布地奈德原料药与部分表面活性剂及部分注射用水混合后得到浓配液,对其单独进行湿热灭菌;将处方中的其它辅料混合后得到的辅料溶液进行过滤灭菌;然后将两种经过不同灭菌处理的液体混匀。这样制备得到的吸入用布地奈德混悬液能有效改善原料药(布地奈德)热降解及粒径增大的问题。值得注意的是,本发明所述制备方法中,浓配液的组分配置、浓配液与辅料溶液的混匀温度,共同对其后续灭菌过程中原料药的有关物质及粒径变化产生决定性的影响。首先,浓配液中原料药与注射用水、表面活性剂与注射用水的比例尤为关键。合适的比例能显著降低有关物质的产生,并且使浓配液在辅料溶液中较易分散均匀,获得理想原料药粒度。而超出本发明保护范围的比例时,则会出现原料药粒度异常增长且基本无法进一步减小的现象。
[0037]
同时,浓配液与辅料溶液混匀时,辅料溶液的温度对布地奈德粒径及杂质水平影
响显著,当辅料溶液温度高于50℃或低于20℃时,都会影响终产品中有关物质含量和/或布地奈德的粒径。
[0038]
发明人经过进一步优化研究发现,浓配液灭菌过程中升温和灭菌完成后降温的速度,对布地奈德粒径及杂质水平的控制也有一定的影响。当升温过程升温速度低于4℃/min或高于30℃/min时,会对终产品中有关物质水平和/或布地奈德的粒径产生一定的影响;降温过程降温速度低于2℃/min或高于30℃/min也会影响终产品中有关物质水平和/或布地奈德的粒径。同时,升降温过程的优化控制对浓配液的可分散性有明显改善作用,可进一步明显提高药液含量均匀度。
[0039]
基于上述研究和发现,本发明提供一种吸入用布地奈德混悬剂的制备方法。所述吸入用布地奈德混悬剂包括布地奈德、表面活性剂、稳定剂、渗透压调节剂、ph调节剂和注射用水,ph=4.0~5.0,布地奈德的终浓度为0.01%~0.20%,所述表面活性剂的终浓度为0.005%~0.020%,所述稳定剂的终浓度为0.005%~0.020%,所述渗透压调节剂的终浓度为0.5%~1.0%。所述制备方法包括如下步骤:
[0040]
i.浓配液的制备和灭菌
[0041]
将布地奈德和部分表面活性剂、部分注射用水混合,得到浓配液,其中布地奈德与注射用水的质量比为1:1~1:6,优选为1:2.5~1:5.5,表面活性剂占总表面活性剂质量的1%~30%,优选为1%~10%,表面活性剂与注射用水的质量比为1:60~1:300,优选为1:100~1:200;
[0042]
将上述浓配液在100~140℃,优选115~127℃下,灭菌8~60min,优选8~17min,即得湿热灭菌的浓配液;
[0043]
ii.辅料溶液的制备和灭菌
[0044]
将剩余的辅料和剩余的注射用水混合均匀,过滤灭菌,得到过滤灭菌的辅料溶液;
[0045]
iii.混合
[0046]
将步骤i制备得到的湿热灭菌的浓配液和步骤ii制备得到的过滤灭菌的辅料溶通过搅拌或均质混合,控制体系温度在20℃~50℃,优选40℃~45,得到吸入用布地奈德混悬液;
[0047]
iv.无菌灌装
[0048]
步骤iii制备得到的吸入用布地奈德混悬液在无菌条件下灌装入ldpe(低密度聚乙烯)瓶中。
[0049]
进一步的,作为优选实施方案,上述浓配液湿热灭菌过程中升温速度为4~30℃/min,优选4~25℃/min;湿热灭菌完成后降温速度为2~30℃/min,优选2~20℃/min。
[0050]
以下参照具体的实施例来说明本发明。本领域技术人员能够理解,这些实施例仅用于说明本发明,其不以任何方式限制本发明的范围。此外应理解,在阅读本文讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
[0051]
下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的原料、试剂、材料等,如无特殊说明,均为市售购买产品。
[0052]
下述实施例中,如无特殊说明,采用行业内湿热灭菌的常规较快的升温、降温控制速度,目的是提高产品的生产效率。一般地,控制升温和降温的速度为不低于35℃/min。
[0053]
实施例1
‑
5:吸入用布地奈德混悬液的制备
[0054]
实施例1
‑
5的吸入用布地奈德混悬液的处方组成(单支)见表2。
[0055]
表2 实施例1
‑
5处方组成及制备工艺关键参数
[0056][0057]
a
:布地奈德在混悬液中的终浓度(质量百分比)。
[0058]
制备工艺包括以下步骤:
[0059]
(1)按照表2所示的单支处方准备1000支的各原辅料;
[0060]
(2)取计算量的注射用水溶解计算量的表面活性剂(吐温80),加入全部的布地奈德中并在转速200~700rpm的条件下搅拌5~30min,得浓配液;
[0061]
(3)对浓配液进行高温121℃湿热灭菌,灭菌12~16min;
[0062]
(4)将剩余表面活性剂和其他辅料溶解在剩余的注射用水中,得到辅料溶液,经过两级过滤器(孔径0.2μm)进行过滤除菌;
[0063]
(5)将过滤除菌后的辅料溶液与经过灭菌处理的浓配液混合,搅拌或高压均质,制得无菌的吸入用布地奈德混悬液;
[0064]
(6)进行无菌操作灌装,每支2ml。
[0065]
实施例6
‑
7:吸入用布地奈德混悬液的制备
[0066]
实施例6
‑
7的吸入用布地奈德混悬液的处方组成(单支)见表3。
[0067]
表3 实施例6
‑
7处方组成及制备工艺关键参数
[0068][0069]
a
:布地奈德在混悬液中的终浓度(质量百分比)。
[0070]
制备工艺包括以下步骤:
[0071]
(1)按照表3所示的单支处方准备1000支的各原辅料;
[0072]
(2)取计算量的注射用水溶解计算量的表面活性剂(司盘或卵磷脂),加入全部的布地奈德中并在转速200~700rpm的条件下搅拌5~30min,得浓配液;
[0073]
(3)对浓配液进行高温121℃湿热灭菌,灭菌12~16min;
[0074]
(4)将剩余表面活性剂和其他辅料溶解在剩余的注射用水中,得到辅料溶液,经过两级过滤器(孔径0.2μm)进行过滤除菌;
[0075]
(5)将过滤除菌后的辅料溶液与经过灭菌处理的浓配液混合,搅拌或高压均质,制得无菌的吸入用布地奈德混悬液;
[0076]
(6)进行无菌操作灌装,每支2ml。
[0077]
实施例8:吸入用布地奈德混悬液的制备
[0078]
实施例8的吸入用布地奈德混悬液的处方组成(单支)见表4。
[0079]
制备工艺包括以下步骤:
[0080]
(1)按照表2所示的单支处方准备1000支的各原辅料;
[0081]
(2)取计算量的注射用水溶解计算量的表面活性剂(吐温80),加入全部的布地奈德中并在转速200~700rpm的条件下搅拌5~30min,得浓配液;
[0082]
(3)对浓配液进行高温121℃湿热灭菌,灭菌12~16min;
[0083]
(4)将剩余表面活性剂和其他辅料溶解在剩余的注射用水中,得到辅料溶液,经过两级过滤器(孔径0.2μm)进行过滤除菌;
[0084]
(5)将过滤除菌后的辅料溶液与经过灭菌处理的浓配液混合,搅拌或高压均质,制得无菌的吸入用布地奈德混悬液;
[0085]
(6)进行无菌操作灌装,每支2ml。
[0086]
表4 实施例8处方组成及制备工艺关键参数
[0087][0088]
a
:布地奈德在混悬液中的终浓度(质量百分比)。
[0089]
对比例1
‑
5:吸入用布地奈德混悬液的制备
[0090]
对比例1
‑
5的处方组成(单支)与实施例1的相同,制备方法也与实施例1的类似,不同之处在于浓配液的组成配比和浓配液与辅料溶液混合时的温度不同,具体见表5。
[0091]
表5 对比例1
‑
5制备工艺关键参数
[0092][0093]
测试例1:实施例1
‑
8及对比例1
‑
5的粒度、有关物质和微细粒子测定
[0094]
粒度测定方法:照粒度和粒度分布测定法(中国药典2020年版四部通则0982第三法)光衍射法测定。
[0095]
有关物质:照高效液相色谱法(中国药典2020年版四部通则0512)试验,用十八烷基硅烷键合硅胶为填充剂;以乙醇
‑
乙腈
‑
磷酸盐缓冲液1(2:34:66)为流动相a,乙腈
‑
磷酸盐缓冲液1(50:50)为流动相b;按下表进行梯度洗脱;检测波长为240nm。
[0096][0097]
微细粒子剂量:照吸入制剂微细粒子空气动力学特性测定法(中国药典2020年版四部通则0951),采用装置3测定。
[0098]
含量均匀度:照中国药典2020年版四部通则0941含量均匀度检查法测定,计算药液含量的a 2.2s值。
[0099]
测定结果见表6和表7。
[0100]
表6 实施例1
‑
8及对比例1
‑
5粒度、有关物质和微细粒子剂量(fpf)测定结果
[0101][0102]
表7 实施例1
‑
8药液含量均匀度测定结果
[0103]
实施例含量均匀度实施例15.3实施例25.6实施例35.9实施例45.6实施例55.1
实施例65.0实施例74.0实施例80.9
[0104]
本领域技术人员可知,吸入混悬液的含量均匀度通常应控制在a 2.2s≤l(l=20.0)(来源:中国药典2020版四部通则0941含量均匀度检查法),a 2.2s越小,药液含量均一性越佳。表7的药液含量均匀度结果显示,当各项工艺参数在本发明的权要范围内时,产品的含量均匀度均已优于行业内通用要求。其中浓配液灭菌过程中升温和降温的速度,对产品的药液含量均匀度影响较为明显,优化控制后会进一步明显提升混悬液的药液含量均匀度。
[0105]
测试例2:实施例1
‑
8、对比例1
‑
2加速6个月样品的粒度及有关物质测定
[0106]
将实施例1
‑
8和对比例1
‑
2制备的吸入用布地奈德混悬液进行6个月加速稳定性考察;观察结束时,按照测试例1的测定方法,分别测定各样品的湿法粒度和有关物质含量。结果见表8。
[0107]
表8 实施例1
‑
8及对比例1
‑
2加速6月样品粒度及有关物质测定
[0108][0109]
上述测试例1和测试例2的结果表明,本发明提供的吸入用布地奈德混悬液的制备方法,通过控制浓配液中各组分的配比以及浓配液稀释时的相关参数,产品的湿法粒度和有关物质均未见明显增加(实施例1
‑
实施例8),完全适于吸入途径给药。且加速稳定性考察6个月,布地奈德粒径和有关物质也没有明显变化(测试例2),说明本发明制备方法得到的布地奈德混悬液的稳定性好。
[0110]
当浓配液中原料药与注射用水的比例、浓配液中表面活性剂与注射用水的比例、浓配液中表面活性剂占总表面活性剂的比例、湿热灭菌过程升温/降温速度、以及浓配液和辅料液混匀温度超出本发明限定的范围时(对比例1
‑
对比例6),混悬液中原料药粒度明显增大,有关物质有明显增加且单杂超限(单杂≤0.30%)。此外,加速条件下放置6个月(测试例2),混悬液中原料药的粒度增大且超出限度(d90≤9μm)或有关物质有明显变化。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。