1.本发明是涉及用于对生物相关物质进行修饰的用途的在细胞内分解的分支型分解性聚乙二醇衍生物的发明。
背景技术:
2.使用激素、细胞因子、抗体、酶等生物相关物质的药品,通常在给药至生物体内时,由于肾脏中的肾小球过滤、肝脏或脾脏等中的巨噬细胞的摄取,迅速从生物体内被排出。因此,血液半衰期缩短、难以获得充分的药理效果的情况多。为解决该问题,已经进行了通过糖链、聚乙二醇等亲水性高分子或白蛋白等对生物相关物质进行化学修饰的尝试。其结果是由于分子量的增大、水合层的形成等,能够延长生物相关物质的血液半衰期。此外,通过以聚乙二醇进行修饰,可获得生物相关物质的毒性或抗原性的降低、难水溶性药剂的溶解性提高等效果也广为人知。
3.被聚乙二醇修饰的生物相关物质由于被由聚乙二醇的醚键与水分子的氢键所形成的水合层覆盖,分子尺寸增大,因此可避免肾脏中的肾小球过滤。进一步地,已知其与调理素、构成各组织的细胞表面之间的相互作用降低,向各组织中的迁移减少。已知聚乙二醇是能够延长生物相关物质的血液半衰期的优异材料,其性能是分子量越大则效果越高。迄今为止,较多地进行了以分子量4万以上的高分子量的聚乙二醇进行修饰的生物相关物质的研究,获得了能够显著地延长其血液半衰期的结果。
4.聚乙二醇被作为用于生物相关物质的性能改善的修饰剂中的最佳标准,现在已经有多个聚乙二醇修饰制剂上市,并用于医疗场所。另一方面,2012年欧洲药品管理局(ema)报道了,在长时间用规定的给药量以上对动物给药以分子量4万以上的高分子量的聚乙二醇修饰的生物相关物质时,一部分的组织的细胞内将产生空泡这样的现象(非专利文献1)。当前,考虑到尚无空泡的产生本身对人体带来不良影响的报道,此外,上述ema的报道中所使用的给药量相比于医疗场所中通常所适用的给药量为极高的用量等,可以说目前制造销售的分子量4万以上的聚乙二醇所修饰的治疗制剂的安全性没有问题。然而,也能够设想到在非常特殊的疾病(例如侏儒症等)的治疗中,采用高用量且长时间向患者给药聚乙二醇修饰制剂的治疗方案。因此,预计在开发这样的特殊状况中也能够适用的、在细胞中不产生空泡的聚乙二醇修饰制剂方面存在潜在需求。
5.非专利文献2中,在将相比于通常的聚乙二醇修饰制剂的给药量大幅过量的聚乙二醇,长时间单独向动物给药时,在分子量2万时未发现空泡,而在分子量4万时确认到空泡的产生。作为抑制空泡的一个手段,想到缩小聚乙二醇的分子量,但产生如果缩小分子量则不能充分改善生物相关物质的血液半衰期这一问题。
6.关于促进高分子量的聚乙二醇在体内分解为低分子量的聚乙二醇,从肾脏排出的技术,有报道例子。专利文献1中记载了具有能在生物体内被切断的硫醚键或肽键部位的聚乙二醇衍生物。记载了该聚乙二醇衍生物在生物体内被分解至适于从肾脏排出的分子量。然而,完全没有显示出有关具体分解的数据,也没有自肾脏的排出得到促进这样的数据。进
一步地,没有关于细胞的空泡的记载。
7.专利文献2中记载了具有在生物体内的低ph环境下能够水解的缩醛部位的聚乙二醇衍生物。记载了该聚乙二醇衍生物在生物体内被分解至适于从肾脏排出的分子量。然而,没有具体地促进从肾脏的排出的数据,进一步也没有有关细胞的空泡的记载。此外,已知这些能够水解的缩醛部位在血液中也缓慢分解,预计不能充分改善修饰后的生物相关物质的血液半衰期。
8.另一方面,存在为有效地释放药物而导入有分解性寡肽的聚乙二醇衍生物或在体内进行分解的水凝胶等的报道例子。
9.非专利文献3记载了具有通过酶而进行分解的寡肽部位的聚乙二醇衍生物。其中报道了,寡肽作为抗癌剂与聚乙二醇间的接头(linker)而被导入,通过在肿瘤周围特异性表达的酶,寡肽分解,可高效地释放抗癌剂。其目的在于抗癌剂的释放,并非出于抑制细胞空泡的目的而向聚乙二醇赋予分解性。
10.非专利文献4记载了使用具有通过酶进行分解的寡肽部位的交联分子和多分支型聚乙二醇衍生物的水凝胶。其中,寡肽被用作为连接多分支型聚乙二醇衍生物的交联分子,进一步地可以赋予水凝胶以经由酶的分解性。其目的在制备分解性的水凝胶,并非出于抑制细胞空泡的目的而向聚乙二醇赋予分解性。
11.专利文献3中记载了以寡肽作为骨架的分支型聚乙二醇衍生物。其中寡肽被用作为聚乙二醇衍生物的基本骨架,而非赋予经由酶的分解性。此外,其特征在于寡肽中包含赖氨酸、天冬氨酸等在侧链具有氨基或羧基的氨基酸,其目的在于合成将这些氨基酸利用于反应的分支型聚乙二醇衍生物。并不是以抑制细胞的空泡为目的的聚乙二醇衍生物。
12.进一步在用于对生物相关物质进行修饰的用途的聚乙二醇衍生物中,一般有直链型和分支型,非专利文献5中记载了分支型比直链型显著使生物相关物质的血液半衰期延长。近年来,上市的聚乙二醇修饰制剂大多采用分支型。然而,迄今为止,在该领域还没有关于抑制细胞空泡的分支型聚乙二醇衍生物的报道。
13.如上所述地,需要一种分支型的高分子量的聚乙二醇衍生物,其在血液中稳定,可改善修饰的生物相关物质的血液半衰期,在被摄取至细胞中时可在细胞内特异性分解,抑制细胞的空泡的产生。现有技术文献专利文献
14.专利文献1:日本特表2009
‑
527581号公报专利文献2:国际公布第2005/108463号专利文献3:国际公布第2006/088248号非专利文献
15.非专利文献1:ema/chmp/swp/647258/2012非专利文献2:daniel g.rudmann,et al.,toxicol.pathol.,41,970
‑
983(2013)非专利文献3:francesco m veronese,et al.,bioconjugate chem.,16,775
‑
784(2005)非专利文献4:jiyuan yang,et al.,marcomol.biosci.,10(4),445
‑
454(2010)非专利文献5:yulia vugmeysterang,et al.,bioconjugate chem.,23,1452
‑
1462(2012)
技术实现要素:
发明所要解决的问题
16.本发明的问题在于提供一种不引起细胞的空泡的高分子量的分支型聚乙二醇衍生物。更具体地,能够以工业化生产的制造方法来提供一种能够有效地用于对生物相关物质进行修饰的用途、在生物体内血液中稳定且在细胞内被分解的分支型分解性聚乙二醇衍生物。用以解决问题的手段
17.本发明人为了解决上述问题而进行了深入研究,结果发明了具有在细胞内进行分解的寡肽的分支型分解性聚乙二醇衍生物。
18.即,本发明为如下所示。[1]一种下式(1)所示的分解性聚乙二醇衍生物:
[0019]
[化1]
[0020]
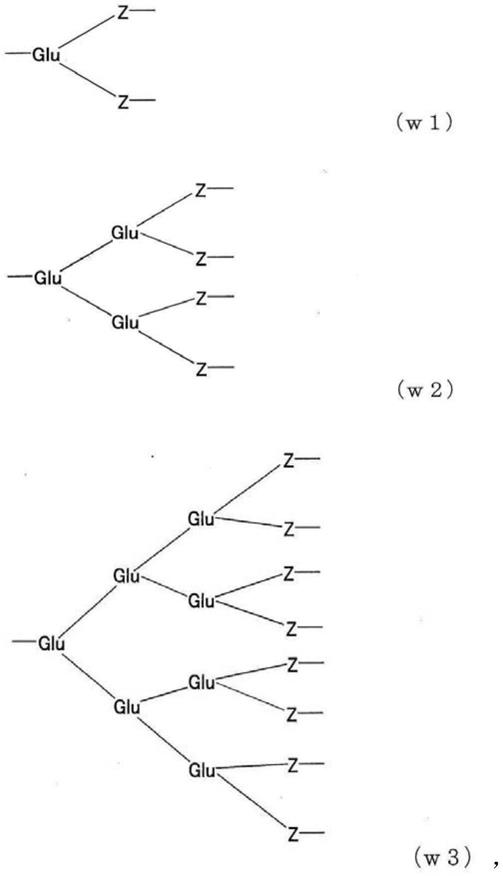
(式中,n为45~950,w为以谷氨酸为中心的对称结构的5~47个残基的寡肽,a为2~8,x为能够与生物相关物质反应的官能团,以及l1和l2分别独立地为2价间隔基团)。[2]根据[1]所述的分解性聚乙二醇衍生物,其中,w的以谷氨酸为中心的对称结构的寡肽是具有以下w1、w2或w3的结构的寡肽。
[0021]
[化2]
[0022]
[化3]
[0023]
[化4]
[0024]
(式中,glu为谷氨酸的残基,以及z为由不包括半胱氨酸的中性氨基酸构成的2~5个残基的分解性寡肽)[3]根据[2]所述的分解性聚乙二醇衍生物,其中,z的分解性寡肽是具有甘氨酸作为c末端的氨基酸的寡肽。[4]根据[2]或[3]中任一项所述的分解性聚乙二醇衍生物,其中,z的分解性寡肽是具有至少1个亲水指数为2.5以上的疏水性的中性氨基酸的寡肽。[5]根据[1]~[4]中任一项所述的分解性聚乙二醇衍生物,其中,总分子量为20,000以上。[6]根据[1]~[5]中任一项所述的分解性聚乙二醇衍生物,其中,l1是羰基、氨基甲酸酯键、酰胺键、醚键、硫醚键、仲氨基或脲键;或可包含这些键和/或基团的亚烷基。[7]根据[1]~[6]中任一项所述的分解性聚乙二醇衍生物,其中,l2是亚烷基;或包含选自羰基、氨基甲酸酯键、酰胺键、醚键、硫醚键、仲氨基和脲键中的至少一个键和/或基团的亚烷基。[8]根据[1]~[7]中任一项所述的分解性聚乙二醇衍生物,其中,x选自由活性酯基、活性碳酸酯基、醛基、异氰酸酯基、异硫氰酸酯基、环氧化物基、马来酰亚胺基、取代马来酰亚胺基、乙烯基磺酰基、丙烯酸基、取代磺酸酯基、磺酰氧基、羧基、巯基、二硫代吡啶基、α
‑
卤代乙酰基、烷基羰基、碘乙酰胺基、烯基、炔基、取代炔基、氨基、氧基氨基、酰肼基和叠氮基组成的群组。发明效果
[0025]
本发明的分支型分解性聚乙二醇衍生物在生物体内的血液中稳定,在结构内具有经由细胞内的酶而分解的寡肽。因此,该分解性聚乙二醇衍生物在血液中稳定,可以赋予生物相关物质以与现有的不具有分解性的聚乙二醇衍生物等同的血液半衰期。进一步地,该分解性聚乙二醇衍生物在被摄取至细胞内时,寡肽部位迅速被分解,因而可以抑制细胞空泡的产生这一悬而未决的问题。此外,构成分解性聚乙二醇衍生物的寡肽具有以谷氨酸为中心的对称结构,在所有聚乙二醇链的末端键合有相同的分解性寡肽z。因此在细胞内分解时产生的聚乙二醇分解产物具有相同的分子量和相同的结构,具有从组织和细胞均匀排出的特点。聚乙二醇引起的细胞的空泡化由于聚乙二醇的分子量越大,越容易发生,因此分解性聚乙二醇期望的分子设计是在细胞内分解成分子量更小的分子。然而,使分子量小的
聚乙二醇经分解性寡肽依次连接起来来制造高分子量的分解性聚乙二醇时,工序数增多。此外,需要以具有两种不同官能团的聚乙二醇作为原料,副产出来的杂质也变得复杂,因此不适合工业化生产。另一方面,本发明的分支型分解性聚乙二醇以廉价易得的甲氧基聚乙二醇衍生物作为原料,使其与分解性寡肽键合,然后,在与谷氨酸衍生物的反应中可以一次性将2根聚乙二醇链导入结构中,因此在其制造中能够大为减少工序数。此外,通过使用甘氨酸作为寡肽的c末端的氨基酸,可以减少制造工序中产生的杂质,从而能够工业化制造本发明的分支型分解性聚乙二醇衍生物。
附图说明
[0026]
图1表示实施例1的化合物(p3)(nh2‑
e(fg
‑
200me)2)的gpc分析结果。图2表示在实施例8的使用细胞的分解性试验中,从细胞内回收的化合物(p3)(nh2‑
e(fg
‑
200me)2)的gpc分析结果。图3表示实施例5的化合物(p13)(nh2‑
e{e(fg
‑
100me)2}2)的gpc分析结果。图4表示在实施例8的使用细胞的分解性试验中,从细胞内回收的化合物(p13)(nh2‑
e{e(fg
‑
100me)2}2)的gpc分析结果。图5表示实施例9的长期给药甲氧基peg(聚乙二醇)胺40kda的小鼠脑脉络丛的切片的图像(箭头指示空泡)。图6表示实施例9的长期给药化合物(p3)(nh2‑
e(fg
‑
200me)2)的小鼠脑脉络丛的切片的图像。图7表示实施例10的长期给药pbs、甲氧基peg胺40kda、甲氧基peg胺20kda、化合物(p3)(nh2‑
e(fg
‑
200me)2)的小鼠脑脉络丛的切片的图像(被染色的部分显示peg的蓄积)。图8表示实施例11的放射性同位素标记的nh2‑
e(fg
‑
200me)2、2分支型peg胺40kda、2分支型peg胺20kda的药代动力学结果(血液中浓度)。
具体实施方式
[0027]
以下详细说明本发明。本发明所涉及的分解性聚乙二醇衍生物如下式(1)所示。
[0028]
[化5]
[0029]
(式中,n为45~950,w为以谷氨酸为中心的对称结构的5~47个残基的寡肽,a为2~8,x为能够与生物相关物质反应的官能团,以及l1和l2分别独立地为2价间隔基团)
[0030]
本发明的式(1)的聚乙二醇衍生物的总分子量通常为4,000~160,000,优选为10,000~120,000,进一步优选为20,000~80,000。本发明的一个优选的实施方式中,本发明的式(1)的聚乙二醇衍生物的总分子量为20,000以上。此处所称的分子量是指数均分子量(mn)。
[0031]
式(1)中的n为聚乙二醇的重复单元数,通常为45~950,优选为110~690,进一步优选为220~460。
[0032]
式(1)中的a为与寡肽键合的聚乙二醇链的根数,通常为2~8,优选为2或4或8,进一步优选为2或4。
[0033]
式(1)中的l1和l2分别独立地为2价间隔基团,这些间隔基团只要是能够形成共价键的基团,就没有特别限制,l1优选为酰胺键、醚键、硫醚键、氨基甲酸酯键、仲氨基、羰基或脲键;或可包含这些键和/或基团的亚烷基。另外,l2优选为亚烷基;或包含选自酰胺键、醚键、硫醚键、氨基甲酸酯键、仲氨基、羰基和脲键中的至少一个键和/或基团的亚烷基。l2优选以碳原子与聚乙二醇的重复单元键合。l1和l2的特别优选方式如下述的群组(i)所示。此外,也可以将群组(i)的间隔基团2个至5个组合。作为2价间隔基团,酯键和碳酸酯键由于在生物体内血液中缓慢分解因而并不合适。
[0034]
群组(i):
[0035]
[化6]
[0036]
(z1)~(z11)中,式中的s表示0~10的整数,优选表示0~6的整数,进一步优选表示0~3的整数。此外,(z2)~(z11)中,式中的s可相同,也可不同。l1为非对称性2价间隔基团时,与相邻的其他基团的键合位置并没有特别限定,如果上述群组(i)的由上式表示的间隔基团的右侧表示与w的键合位置、左侧表示与x的键合位置时,则可采取左侧表示与w的键合位置、右侧表示与x的键合位置时的两个键合位置。同样地,l2为非对称性2价间隔基团时,如果上述群组(i)的由上式表示的间隔基团的右侧表示与och2ch2的键合位置、左侧表示与w的键合位置时,则也可采取左侧表示与och2ch2的键合位置、右侧表示与w的键合位置时的两个键合位置。
[0037]
作为式(1)中的l1,优选群组(i)的(z3)、(z4)、(z6)、(z7)、(z8)、(z9)或(z10)所示
的基团,更优选(z3)、(z6)、(z9)或(z10)所示的基团。作为式(1)中的l2,优选群组(i)的(z1)、(z2)、(z3)、(z4)、(z5)、(z6)、(z7)、(z8)或(z11)所示的基团,更优选团(z3)、(z5)或(z11)所示的基团。
[0038]
式(1)中的w只要是以谷氨酸为中心的对称结构的5~47个残基的寡肽,在生物体内血液中稳定,且经细胞内的酶进行分解的寡肽,就没有特别限制,作为构成寡肽的氨基酸,除了构成中心部分的谷氨酸以外,优选由不包括半胱氨酸的中性氨基酸构成。此处所称的以谷氨酸为中心的对称结构的寡肽是指在谷氨酸的α位的羧基与γ位的羧基上键合有相同肽的化合物,以谷氨酸为中心成对的肽是采用对称结构的寡肽。作为该寡肽中的中性氨基酸与谷氨酸数目的构成比(中性氨基酸的数目/谷氨酸的数目),通常为2~10,优选为2~8,进一步优选为2~6。构成w的氨基酸基本上为l型。
[0039]
w的特别优选的方式如下述的群组(ii)所示。
[0040]
群组(ii):
[0041]
[化7]
[0042]
[化8]
[0043]
[化9]
[0044]
(式中,glu为谷氨酸的残基,以及z为由不包括半胱氨酸的中性氨基酸构成的2~5个残基的分解性寡肽。)
[0045]
(w1)~(w3)中的z优选为在侧链上具有氨基或羧基的氨基酸,具体地为由不含赖氨酸、天冬氨酸、或谷氨酸的中性氨基酸构成的寡肽。本发明的式(1)的分支型分解性聚乙二醇衍生物的合成中,在通过反应键合作为原料的聚乙二醇衍生物与寡肽时,将寡肽的c末
端的羧基利用于与聚乙二醇衍生物的缩合反应中。然而,当该寡肽具有在侧链上具有氨基或羧基的氨基酸时,发生通过缩合反应在寡肽之间的副反应、聚乙二醇衍生物不被导入至作为目标的c末端的羧基,而是还导入至侧链的羧基的杂质。由于该杂质难以通过通常的萃取、析晶等提纯工序去除,因而为获得纯度良好的目标物,理想的是使用由侧链上不具有氨基或羧基的氨基酸构成的寡肽。构成z的氨基酸为α
‑
氨基酸,此外基本上为l型。
[0046]
由于作为中性氨基酸的半胱氨酸具有巯基,与其他巯基形成双硫键,因此(w1)~(w3)中的z优选为由不含半胱氨酸的中性氨基酸构成的寡肽。
[0047]
而且,(w1)~(w3)中的z优选为具有甘氨酸作为c末端的氨基酸的寡肽。在使c末端的羧基与聚乙二醇衍生物进行反应时,基本上需要用缩合剂等使c末端的羧基活性化。已知的是在该活性化的工序中,甘氨酸以外的氨基酸易于发生差向异构化,生成副产物立体异构体。通过使寡肽的c末端的氨基酸为非手性的甘氨酸,可以得到不会有立体异构体副产出来的高纯度的目标物。
[0048]
进一步地,(w1)~(w3)中的z是亲水指数为2.5以上的疏水性的中性氨基酸,具体地优选为具有至少1个苯丙氨酸、亮氨酸、缬氨酸、异亮氨酸的寡肽,进一步优选为具有苯丙氨酸的寡肽。由凯特(kyte)和杜利特尔(doolittle)所完成的定量表示氨基酸的疏水性的亲水指数(hydropathy index),其值越大,表示越为疏水性氨基酸(kyte j&doolittle rf,1982,j mol biol,157:105
‑
132.)。
[0049]
(w1)~(w3)中的z只要是在生物体内血液中稳定,且具有经细胞内的酶进行分解的性能,由不包括半胱氨酸的中性氨基酸构成的2~5个残基的寡肽,就没有特别限制,作为具体的例子,为甘氨酸
‑
苯丙氨酸
‑
亮氨酸
‑
甘氨酸、甘氨酸
‑
甘氨酸
‑
苯丙氨酸
‑
甘氨酸、甘氨酸
‑
苯丙氨酸
‑
甘氨酸、甘氨酸
‑
亮氨酸
‑
甘氨酸、缬氨酸
‑
瓜氨酸
‑
甘氨酸、缬氨酸
‑
丙氨酸
‑
甘氨酸、苯丙氨酸
‑
甘氨酸等,优选为甘氨酸
‑
苯丙氨酸
‑
亮氨酸
‑
甘氨酸、甘氨酸
‑
甘氨酸
‑
苯丙氨酸
‑
甘氨酸、甘氨酸
‑
苯丙氨酸
‑
甘氨酸、缬氨酸
‑
瓜氨酸
‑
甘氨酸、缬氨酸
‑
丙氨酸
‑
甘氨酸或苯丙氨酸
‑
甘氨酸,更优选为甘氨酸
‑
苯丙氨酸
‑
亮氨酸
‑
甘氨酸、甘氨酸
‑
苯丙氨酸
‑
甘氨酸、缬氨酸
‑
瓜氨酸
‑
甘氨酸或苯丙氨酸
‑
甘氨酸,进一步更优选为甘氨酸
‑
苯丙氨酸
‑
亮氨酸
‑
甘氨酸或苯丙氨酸
‑
甘氨酸。
[0050]
式(1)中的x只要是与存在于作为化学修饰对象的生理活性蛋白质、肽、抗体、核酸等生物相关物质中的官能团进行反应而形成共价键的官能团,就没有特别限制。例如,可举出“harris,j.m.poly(ethylene glycol)chemistry;plenum press:new york,1992(j.m.哈里斯,聚乙二醇化学;普莱南出版社:纽约,1992)”、“hermanson,g.t.bioconjugate techniques,2nd ed.;academic press:san diego,ca,2008(g.t.赫曼森,生物偶联技术,第二版;学术出版社:加利福尼亚州圣地亚哥,2008)”和“pegylated protein drugs:basic science and clinical applications;veronese,f.m.,ed.;birkhauser:basel,switzerland,2009(聚乙二醇化蛋白药物:基础科学和临床应用,f.m.韦罗内塞编;博克豪斯出版社:瑞士巴塞尔,2009)”等所记载的官能团。
[0051]
式(1)中的x所示的“能够与生物相关物质反应的官能团”,只要是能够与生物相关物质所具有的氨基、巯基、醛基、羧基、不饱和键或叠氮基等官能团化学键合的官能团,就没有特别限制。
具体可举出活性酯基、活性碳酸酯基、醛基、异氰酸酯基、异硫氰酸酯基、环氧化物基、羧基、巯基、马来酰亚胺基、取代马来酰亚胺基、酰肼基、二硫代吡啶基、取代磺酸酯基、乙烯基磺酰基、氨基、氧基氨基(h2n
‑
o
‑
基)、碘乙酰胺基、烷基羰基、烯基(例如烯丙基、乙烯基)、炔基、取代炔基(例如后述的被碳原子数1~5的烃基取代的炔基)、叠氮基、丙烯酸基、磺酰氧基(例如烷基磺酰氧基)、α
‑
卤代乙酰基等,优选为活性酯基、活性碳酸酯基、醛基、异氰酸酯基、异硫氰酸酯基、环氧化物基、马来酰亚胺基、取代马来酰亚胺基、乙烯基磺酰基、丙烯酸基、磺酰氧基(例如碳原子数1~5的烷基
‑
磺酰氧基)、取代磺酸酯基、羧基、巯基、二硫代吡啶基、α
‑
卤代乙酰基、炔基、取代炔基(例如后述的被碳原子数1~5的烃基取代的碳原子数2~5的炔基)、烯丙基、乙烯基、氨基、氧基氨基、酰肼基和叠氮基,更优选为活性酯基、活性碳酸酯基、醛基、马来酰亚胺基、氧基氨基和氨基,特别优选为醛基、马来酰亚胺基和氧基氨基。
[0052]
其他适宜的实施方式中,所述官能团x可分类为下述的群组(iii)、群组(iv)、群组(v)、群组(vi)、群组(vii)和群组(viii)。
[0053]
群组(iii):能够与生物相关物质所具有的氨基反应的官能团可举出下述的(a)、(b)、(c)、(d)、(e)、(f)、(g)、(j)或(k)所示的基团。
[0054]
群组(iv):能够与生物相关物质所具有的巯基反应的官能团可举出下述的(a)、(b)、(c)、(d)、(e)、(f)、(g)、(h)、(i)、(j)、(k)或(l)所示的基团。
[0055]
群组(v):能够与生物相关物质所具有的醛基反应的官能团可举出下述的(h)、(m)、(n)或(p)所示的基团。
[0056]
群组(vi):能够与生物相关物质所具有的羧基反应的官能团可举出下述的(h)、(m)、(n)或(p)所示的基团。
[0057]
群组(vii):能够与生物相关物质所具有的不饱和键反应的官能团可举出下述的(h)、(m)或(o)所示的基团。
[0058]
群组(viii):能够与生物相关物质所具有的叠氮基反应的官能团可举出下述的(l)所示的基团。
[0059]
[化10]
[0060]
官能团(j)中,式中的w1表示氯原子(cl)、溴原子(br)或碘原子(i)等卤素原子,优选为br或i,更优选为i。
[0061]
另外,官能团(e)和官能团(l)中,式中的y1和y3分别独立地表示氢原子或碳原子数1~5的烃基,优选为碳原子数1~5的烃基。作为碳原子数1~5的烃基,具体地可举出甲基、乙基、丙基、异丙基、丁基、叔丁基等,优选为甲基或乙基。
[0062]
另外,官能团(k)中,式中的y2表示可含有氟原子的碳原子数为1~10的烃基,具体地可举出甲基、乙基、丙基、异丙基、丁基、叔丁基、己基、壬基、乙烯基、苯基、苄基、4
‑
甲基苯基、三氟甲基、2,2,2
‑
三氟乙基、4
‑
(三氟甲氧基)苯基等,优选为甲基、乙烯基、4
‑
甲基苯基或2,2,2
‑
三氟乙基。
[0063]
活性酯基是指具有离去能力高的烷氧基的酯基。作为离去能力高的烷氧基,可举出衍生自硝基苯酚、n
‑
羟基琥珀酰亚胺、五氟苯酚等的烷氧基。活性酯基优选为具有衍生自n
‑
羟基琥珀酰亚胺的烷氧基的酯基。
[0064]
活性碳酸酯基是指具有离去能力高的烷氧基的碳酸酯基。作为离去能力高的烷氧基,可举出衍生自硝基苯酚、n
‑
羟基琥珀酰亚胺、五氟苯酚等的烷氧基。活性碳酸酯基优选为具有衍生自硝基苯酚或n
‑
羟基琥珀酰亚胺的烷氧基的碳酸酯基。
[0065]
取代马来酰亚胺基是指在马来酰亚胺基的双键之一的碳原子上键合有烃基的马来酰亚胺基。烃基具体地可举出甲基、乙基、丙基、异丙基、丁基、叔丁基等,优选为甲基或乙基。
[0066]
取代磺酸酯基是指在磺酸酯基的硫黄原子上键合有可含有氟原子的烃基的磺酸酯基。作为可含有氟原子的烃基,具体地可举出甲基、乙基、丙基、异丙基、丁基、叔丁基、己基、壬基、乙烯基、苯基、苄基、4
‑
甲基苯基、三氟甲基、2,2,2
‑
三氟乙基、4
‑
(三氟甲氧基)苯基等,优选为甲基、乙烯基、4
‑
甲基苯基或2,2,2
‑
三氟乙基。
[0067]
式(1)的优选方式之一是w为w1和a=2的下式(2)所示的2分支型分解性聚乙二醇衍生物。
[0068]
[化11]
[0069]
(式中,glu、z、n、x、l1和l2与上述含义相同)
[0070]
式(1)的优选方式之一是w为w2以及a=4的下式(3)所示的4分支型分解性聚乙二醇衍生物。
[0071]
[化12]
[0072]
(式中,glu、z、n、x、l1和l2与上述含义相同)
[0073]
式(1)的优选方式之一是w为w3以及a=8的下式(4)所示的8分支型分解性聚乙二醇衍生物。
[0074]
[化13]
[0075]
(式中,glu、z、n、x、l1和l2与上述含义相同)
[0076]
本发明的分支型分解性聚乙二醇衍生物例如可以经过以下工序来制造。
[0077]
[化14]
[0078]
(工序中的peg为聚乙二醇链,肽为寡肽,pro为保护基,以及l3为2价间隔基团。)
[0079]
工序中的peg为聚乙二醇链,分子量如作为上述的聚乙二醇的重复单元数的n所定义地,即由于n为45~950,其分子量的范围为2000~42000。
[0080]
工序中的肽是与上述z含义相同的寡肽。本工序中使用n末端的氨基被保护基所保护的寡肽。
[0081]
工序中的pro为保护基,此处保护基是指防止或阻止某一反应条件下分子中的能够进行特定化学反应的官能团的反应的成分。保护基根据所保护的能够进行化学反应的官能团的种类、所使用的条件和分子中的其他官能团或保护基的存在而有所改变。保护基的具体例子可以在很多通常的书籍中找到,例如记载于“wuts,p.g.m.;greene,t.w.protective groups in organic synthesis,4th ed.;wiley
‑
interscience:new york,2007(p.g.m.伍斯;t.w.格林,有机合成中的保护基,第四版;wiley
‑
interscience:纽约,2007)”。此外,被保护基保护的官能团通过使用适于各自保护基的反应条件进行脱保护、即进行化学反应,可再次产生原有的官能团。保护基的典型的脱保护条件如上述文献中所记载。
[0082]
工序中的l3是与上述l1和l2相同含义的2价间隔基团。
[0083]
反应a是通过缩合反应使n末端的氨基被保护基所保护的寡肽的羧基与单个末端为甲氧基的聚乙二醇衍生物的氨基键合而获得聚乙二醇衍生物(1)的工序。寡肽的n末端的氨基的保护基没有特别限制,例如可举出酰基系保护基和氨基甲酸酯系保护基,具体地可举出三氟乙酰基、9
‑
芴基甲氧基羰基(fmoc)、叔丁氧基羰基等。作为缩合反应,没有特别限制,但理想的是使用缩合剂的反应。作为缩合剂,可单独使用二环己基碳二亚胺(dcc)、1
‑
乙基
‑3‑
(3
‑
二甲基氨基丙基)碳二亚胺盐酸盐(edc)等碳二亚胺系的缩合剂,也可与n
‑
羟基琥珀酰亚胺(nhs)、1
‑
羟基苯并三唑(hobt)、1
‑
羟基
‑7‑
氮杂苯并三唑(hoat)等试剂一起使用。此外,也可使用反应性更高的hatu或hbtu、tatu,tbtu、comu、4
‑
(4,6
‑
二甲氧基
‑
1,3,5
‑
三嗪
‑2‑
基)
‑4‑
甲基吗啉盐酸盐n水合物(dmt
‑
mm)等缩合剂。此外为了促进反应,也可使用三乙胺或二甲基氨基吡啶等碱。反应中副反应生成的杂质或反应中未被消耗而残留的寡肽和缩合剂等优选进行提纯而去除。提纯没有特别限制,能够以萃取、重结晶、吸附处理、再沉淀、柱色谱法、超临界萃取等进行提纯。
[0084]
[化15]
[0085]
脱保护b是将反应a中所得的聚乙二醇衍生物(1)的保护基进行脱保护而获得聚乙二醇衍生物(2)的工序。作为脱保护反应,可以使用现有公知的方法,但需要使用寡肽和l3的2价间隔基团不分解的条件。此外,本工序也可以作为反应a的工序的一部分来实施。脱保护反应中副反应生成的杂质等优选进行提纯而去除。提纯没有特别限制,能够以萃取、重结晶、吸附处理、再沉淀、柱色谱法、超临界萃取等进行提纯。
[0086]
[化16]
[0087]
反应c是通过缩合反应使脱保护b中所得的聚乙二醇衍生物(2)的氨基与氨基被保护基所保护的谷氨酸衍生物的两个羧基键合,从而获得2根分解性聚乙二醇链被谷氨酸残基连接的结构的分支型聚乙二醇衍生物(3)的工序。与上述反应a同样地,理想的是使用缩合剂的反应,为了促进反应,也可使用三乙胺或二甲基氨基吡啶等碱。谷氨酸的氨基的保护基没有特别限制,例如可举出酰基系保护基和氨基甲酸酯系保护基,具体地可举出三氟乙酰基、9
‑
芴基甲氧基羰基(fmoc)、叔丁氧基羰基等。反应中副反应生成的杂质或反应中未被消耗而残留的聚乙二醇衍生物等优选进行提纯而去除。提纯没有特别限制,能够以萃取、重结晶、吸附处理、再沉淀、柱色谱法、超临界萃取等进行提纯。
[0088]
[化17]
[0089]
脱保护d是将反应c中所得的聚乙二醇衍生物(3)的保护基脱保护而获得聚乙二醇衍生物(4)的工序。作为脱保护反应,可以使用现有公知的方法,但需要使用寡肽和l3的2价间隔基团不分解的条件。此外,本工序也可以作为反应c的工序的一部分来实施。脱保护反应中副反应生成的杂质等优选进行提纯而去除。提纯没有特别限制,能
够以萃取、重结晶、吸附处理、再沉淀、柱色谱法、超临界萃取等进行提纯。
[0090]
[化18]
[0091]
反应e是通过缩合反应使脱保护d中所得的聚乙二醇衍生物(4)的氨基与氨基被保护基所保护的谷氨酸衍生物的两个羧基键合,从而获得4根分解性聚乙二醇链被谷氨酸残基连接的结构的分支型聚乙二醇衍生物(5)的工序。可以在与上述反应c相同条件下反应和提纯。作为从聚乙二醇衍生物(5)中除去子量或官能团不同的聚乙二醇杂质的方法,可以使用日本专利特开2014
‑
208786号公报或日本专利特开2011
‑
79934号公报中记载的提纯技术。
[0092]
[化19]
[0093]
脱保护f是将反应e中所得的聚乙二醇衍生物(5)的保护基脱保护而获得聚乙二醇衍生物(6)的工序。作为脱保护反应,可以使用现有公知的方法,但需要使用寡肽和l3的2价间隔基团不分解的条件。能够在与上述脱保护d相同条件下反应和提纯。此外,本工序也可以作为反应e的工序的一部分来实施。
[0094]
[化20]
[0095]
反应g是通过缩合反应使脱保护f中所得的聚乙二醇衍生物(6)的氨基与氨基被保护基所保护的谷氨酸衍生物的两个羧基键合,从而获得8根分解性聚乙二醇链被谷氨酸残基连接的结构的分支型聚乙二醇衍生物(7)的工序。可以在与上述反应c相同条件下反应和提纯。
[0096]
[化21]
[0097]
脱保护h是将反应g中所得的聚乙二醇衍生物(7)的保护基脱保护而获得聚乙二醇衍生物(8)的工序。能够在与上述脱保护f相同条件下反应和提纯。此外,本工序也可以作为反应g的工序的一部分来实施。
[0098]
通过进行以上的反应a、脱保护b、反应c和脱保护d,可得到2分支型分解性聚乙二
醇衍生物(4)。将2分支型分解性聚乙二醇衍生物(4)作为原料,继续通过进行反应e和脱保护f,可得到4分支型分解性聚乙二醇衍生物(6)。进一步继续通过进行反应g和脱保护h,可得到8分支型分解性聚乙二醇衍生物(8)。
[0099]
脱保护d、脱保护f和脱保护h中所得的聚乙二醇衍生物(4)、(6)和(8)均具有一个氨基,可利用其转换为各种官能团。
[0100]
关于将聚乙二醇衍生物的末端的氨基转换为其他官能团的工序,没有特别限制,基本上可以通过使用具有能够与氨基反应的活性酯基的化合物或酸酐、酰氯等通常的反应试剂,容易地转换为各种官能团。
[0101]
例如,在希望将聚乙二醇衍生物的末端的氨基转换为马来酰亚胺基时,可以通过使其与如下的试剂进行反应而获得目标物。
[0102]
[化22]
[0103]
例如,在希望将聚乙二醇衍生物的末端的氨基转换为羧基时,可以通过使其与琥珀酸酐或戊二酸酐进行反应而获得目标物。
[0104]
例如,在希望将聚乙二醇衍生物的末端的氨基转换为水酸基时,通过与己内酯等环状酯的开环物进行缩合反应而获得目标物。
[0105]
这些反应试剂是低分子量的试剂,由于与高分子量聚合物的聚乙二醇衍生物有很大的溶解性差别,因此可以通过萃取或析晶等通常的提纯方法容易地去除。
[0106]
要求经由如上所述的工序而获得的分解性聚乙二醇在血液中稳定,具有仅在细胞内进行分解的性能。为了恰当地评价其性能,例如可以进行如下所示的试验,评价分解性聚乙二醇在血液中的稳定性、以及在细胞内的分解性。此外,在这些评价中,考虑聚乙二醇衍生物所具有的官能团种类引起的影响,评价试样全部对具有一个氨基的聚乙二醇衍生物统一进行了试验。
[0107]
关于用于评价分解性聚乙二醇衍生物在血液中的稳定性的试验方法,没有特别限制,例如可举出使用小鼠、大鼠、人等血清的试验等。具体地,可以通过在血清中溶解聚乙二醇衍生物至浓度成为1~10mg/ml,在37℃下孵育96小时后,回收血清中所含的聚乙二醇衍生物,测定gpc,从而评价分解率。分解率基于稳定性试验前的聚乙二醇衍生物的gpc主馏分(main fraction)的峰面积%和稳定性试验后的聚乙二醇衍生物的gpc主馏分的峰面积%进行计算。具体地使用下式。分解率=(试验前的峰面积%
‑
试验后的峰面积%)
÷
试验前的峰面积%
×
100例如,如果稳定性试验前的分解性聚乙二醇衍生物的gpc主馏分的峰面积%为95%,试验后的gpc主馏分的峰面积%变为90%时,分解率如下地进行计算。分解率=(95
‑
90)
÷
95
×
100=5.26(%)分解性聚乙二醇衍生物一旦在血液中分解,则不能获得目标的血液半衰期,因此在稳定性试验中,96小时后的分解率优选10%以下,进一步优选5%以下。
[0108]
关于用于评价分解性聚乙二醇衍生物在细胞内的分解性的试验方法,没有特别限制,例如可举出使用含有分解性聚乙二醇衍生物的培养基,培养细胞的试验等。关于此处使用的细胞或培养基,没有特别限制,具体地,可以通过在培养基rpmi
‑
1640中溶解聚乙二醇衍生物至浓度成为1~20mg/ml,使用该培养基,在37℃下培养96小时巨噬细胞raw264.7后,回收细胞中的聚乙二醇衍生物,测定gpc,从而评价分解率。分解率与稳定性试验同样地,可以使用试验前后的聚乙二醇衍生物的gpc主馏分的峰面积%进行计算。例如,如果使用细胞的分解性试验前的分解性聚乙二醇衍生物的gpc主馏分的峰面积%为95%,试验后的gpc主馏分的峰面积%变为5%时,分解率如下地进行计算。分解率=(95
‑
5)
÷
95
×
100=94.7(%)如果分解性聚乙二醇衍生物不能在细胞内高效地分解,则不能抑制作为目标的细胞的空泡,因此在分解性试验中,96小时后的分解率优选90%以上,进一步优选95%以上。
[0109]
关于用于评价分解性聚乙二醇衍生物的血液半衰期和体内分布的试验方法,没有特别限制,例如可举出用放射性同位素或荧光物质标记,对小鼠或大鼠给药,并进行监测的试验等。认为导入至聚乙二醇衍生物的分解性肽对聚乙二醇赋予在细胞内的分解性,但因该肽结构而存在改变聚乙二醇的药代动力学的可能性。因此,为了确认导入的肽结构对药代动力学的影响,对于血液半衰期及其体内分布,需要与不具有分解性的相同分子量的聚乙二醇衍生物进行比较。具体地,可以将用放射性同位素标记的不具有分解性的聚乙二醇衍生物和分解性聚乙二醇衍生物向小鼠给药,在多个时间点测定血液、各脏器的辐射剂量,进行定量测定。
[0110]
关于用于评价分解性聚乙二醇衍生物的细胞的空泡抑制的试验方法,没有特别限制,例如可举出如非专利文献2所记载地,持续长期间、高频度、高给药量地向小鼠或大鼠给药,对被认为易于产生空泡的脏器或器官的切片图像进行确认的试验等。具体地,可在生理盐水中溶解聚乙二醇衍生物至浓度成为10~250mg/ml,通过小鼠尾静脉,持续每周3次、4周以上、20~100μl的给药,制作被认为易于产生空泡的器官的脑脉络丛或脾脏等的石蜡切片进行染色后,通过病理学方法确认切片图像,进行空泡抑制的评价。此外,本评价中聚乙二醇的给药量相比于该技术领域中的通常的聚乙二醇的给药量,需要给予过量很大的聚乙二醇。
[0111]
非专利文献2中有高分子量的聚乙二醇引起的细胞的空泡化与聚乙二醇在组织中的蓄积有关这样的记载。关于用于评价分解性聚乙二醇衍生物的细胞中的蓄积性的试验方法,没有特别限制,可以通过与以上述空泡评价相同方法制作的切片图像进行评价。可以通过病理学方法确认被认为易于产生空泡的器官的脑脉络丛或脾脏等的染色后的切片图像,进行聚乙二醇的蓄积性的评价。此外,本评价中聚乙二醇的给药量相比于该技术领域中的通常的聚乙二醇的给药量,需要给予过量很大的聚乙二醇。实施例
[0112]
下述实施例中获得的1h
‑
nmr得自捷欧迪拓姆(jeoldatum)株式会社制造的jnm
‑
ecp400或jnm
‑
eca600。测定中使用样品管,氘代溶剂中使用d2o或含有四甲基硅烷
(tms)作为内标物的cdcl3和d6‑
dmso。获得的聚乙二醇衍生物的分子量和胺纯度使用液相色谱(gpc和hplc)进行计算。液相色谱的系统是在gpc中使用东曹株式会社制造的“hlc
‑
8320gpc ecosec”,在hplc中使用waters公司制造的“alliance”。以下示出gpc和hplc的分析条件。gpc分析(分子量测定)标准聚合物:使用分子量为8,000、20,000、50,000和100,000的聚乙二醇作为标准聚合物进行利用gpc分析的分子量测定。检测器:示差折光仪色谱柱:ultrahydrogel 500和ultrahydrogel 250(waters公司制造)流动相:100mm乙酸盐缓冲液(acetate buffer) 0.02%nan3(ph5.2)流速:0.5ml/min样品量:5mg/ml,20μl色谱柱温度:30℃hplc分析(胺纯度测定)检测器:示差折光仪色谱柱:tskgel sp
‑
5pw(东曹株式会社制造)流动相:1mm磷酸钠缓冲液(sodium phosphate buffer)(ph6.5)流速:0.5ml/min注入量:5mg/ml,20μl色谱柱温度:40℃
[0113]
[实施例1]化合物(p3)(nh2‑
e(fg
‑
200me)2)的合成
[0114]
[化23]
[0115]
[实施例1
‑
1]
[0116]
[化24]
[0117]
向n末端被9
‑
芴基甲氧基羰基(fmoc基)保护的l
‑
苯丙氨酰
‑
甘氨酸(fmoc
‑
phe
‑
gly)(0.267g,6.0
×
10
‑4mol,渡边化学工业株式会社制造)和末端具有丙基氨基的甲氧基peg(6.0g,2.8
×
10
‑4mol,数均分子量=21,120,日油株式会社制造的“sunbright mepa
‑
20t”)中添加脱水n,n
’‑
二甲基甲酰胺(60g),在30℃下加温溶解。然后,添加二异丙基乙胺(192μl,1.2
×
10
‑3mol,关东化学株式会社制造)和(1
‑
氰基
‑2‑
乙氧基
‑2‑
氧代亚乙基氨基氧基)二甲基氨基
‑
吗啉
‑
碳鎓六氟磷酸盐(comu)(0.321g,7.5
×
10
‑4mol,sigma
‑
aldrich公司制造),使其在室温下氮气气氛下反应1小时。反应结束后,用氯仿(600g)进行稀释,添加饱和碳酸氢钠水溶液(240g),在室温下搅拌15分钟进行清洗。分离水层和有机层后,再次向有机层中添加饱和碳酸氢钠水溶液(240g),在室温下搅拌15分钟进行清洗,回收有机层。向获得的有机层(氯仿溶液)中添加硫酸镁(2.4g),搅拌30分钟进行脱水,然后使用在5a滤纸上铺有oplite的桐山漏斗进行抽滤。在40℃下浓缩获得的滤液,向浓缩物中添加乙酸乙酯(240g)搅拌至均匀,然后加入己烷(120g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后再次溶解于乙酸乙酯(240g)中,加入己烷(120g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用己烷(120g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p1)(me
‑
200gf
‑
fmoc)。产量为5.1g。
[0118]1h
‑
nmr(d6‑
dmso):1.62ppm(m,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),2.80ppm(m,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.04ppm(m,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.10ppm(m,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.24ppm(s,3h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.48ppm(m,约1,900h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.20ppm(m,4h),7.33ppm(m,9h),7.66ppm(m,4h,ar),7.88ppm(d,2h,ar),8.27ppm(t,1h)
[0119]
[实施例1
‑
2]
[0120]
[化25]
[0121]
向实施例1
‑
1中所得的me
‑
200gf
‑
fmoc(4.9g,2.3
×
10
‑4mol)中添加n,n
’‑
二甲基甲酰胺(29.4g),在30℃下加温溶解。添加哌啶(1.55g,1.8
×
10
‑2mol,和光纯药工业株式会社制造),在室温下氮气气氛下反应2小时。反应结束后,加入乙酸乙酯(300g)搅拌至均匀,添加己烷(150g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后再次溶解于乙酸乙酯(300g)中,加入己烷(150g),在室温下搅拌15分钟使生成物析出。使
用5a滤纸进行抽滤,回收析出物,然后用己烷(150g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p2)(me
‑
200gf
‑
nh2)。产量为3.9g。
[0122]1h
‑
nmr(d6‑
dmso):1.62ppm(m,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),1.64ppm(宽,1h),2.59ppm(dd,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),2.98ppm(dd,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.10ppm(q,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.24ppm(s,3h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.48ppm(m,约1,900h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),7.24ppm(m,6h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5,
‑
nh
‑
),7.73ppm(t,1h),8.12ppm(宽,1h)
[0123]
[实施例1
‑
3]
[0124]
[化26]
[0125]
向n末端被fmoc基保护的l
‑
谷氨酸(fmoc
‑
glu
‑
oh)(16.0mg,4.3
×
10
‑5mol,渡边化学工业株式会社制造)和实施例1
‑
2中所得的me
‑
200gf
‑
nh2(2.0g,1.0
×
10
‑4mol)中添加脱水n,n
’‑
二甲基甲酰胺(10g),在30℃下加温溶解。然后,添加二异丙基乙胺(19.2μl,1.1
×
10
‑4mol,关东化学株式会社制造)和4
‑
(4,6
‑
二甲氧基
‑
1,3,5
‑
三嗪
‑2‑
基)
‑4‑
甲基吗啉盐酸盐n水合物(dmt
‑
mm)(39.0mg,1.1
×
10
‑4mol,和光纯药工业株式会社制造),在室温下氮气气氛下反应1小时。然后,添加哌啶(0.5g,5.9
×
10
‑
3mol,和光纯药工业株式会社制造),在室温下氮气气氛下反应2小时。反应结束后,反应液用甲苯(80g)进行稀释,然后加入己烷(40g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后再次溶解于甲苯(80g)中,加入己烷(40g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用己烷(40g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p3)(nh2‑
e(fg
‑
200me)2)。产量为1.6g。分子量示于表1中。hplc:胺纯度92%。
[0126]1h
‑
nmr(d6‑
dmso):1.54ppm(m,2h,
‑
nh
‑
co
‑
ch(nh2)
‑
ch2‑
ch2‑
),1.62ppm(m,4h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
),1.97ppm(m,2h,
‑
nh
‑
co
‑
ch(nh2)
‑
ch2‑
ch2‑
),2.74ppm(dd,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),2.81ppm(dd,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),3.11ppm(m,11h),3.24ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.49ppm(m,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),4.57ppm(m,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.25ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.74ppm(m,2h),8.44ppm(m,2h),8.61ppm(m,2h)
[0127]
[实施例2]化合物(p4)(ma
‑
e(fg
‑
200me)2)的合成
[0128]
[化27]
[0129]
将实施例1中所得的化合物(p3)(200mg,5.0
×
10
‑6mol)溶解于乙腈(160mg)和甲苯(1.0g)中。然后,添加n
‑
甲基吗啉(10mg,1.0
×
10
‑5mol,关东化学株式会社制造)和3
‑
马来酰亚胺丙酸n
‑
羟基琥珀酰亚胺酯(8.0mg,3.0
×
10
‑5mol,大阪合成有机化学研究所株式会社制造),在室温下氮气气氛下和遮光下反应6小时。反应结束后,反应液用含2,6
‑
二叔丁基对甲酚(bht)(10mg)的乙酸乙酯(50g)进行稀释,然后加入己烷(25g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用含bht(5mg)的己烷(25g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p4)(ma
‑
e(fg
‑
200me)2)。产量为137mg。分子量示于表1中。马来酰亚胺纯度为90%(1h
‑
nmr)。
[0130]1h
‑
nmr(d6‑
dmso):1.62ppm(m,6h),1.99ppm(m,2h,
‑
nh
‑
co
‑
ch(nh2)
‑
ch2‑
ch2‑
),2.34ppm(m,2h,
‑
nh
‑
co
‑
ch2‑
ch2‑
马来酰亚胺),2.75ppm(dd,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),2.82ppm(dd,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),3.11ppm(m,11h),3.24ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.04ppm(m,2h,
‑
nh
‑
co
‑
ch2‑
ch2‑
马来酰亚胺),4.49ppm(m,2h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),6.98ppm(s,2h,
‑
co
‑
ch
‑
ch
‑
co
‑
),7.25ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.69ppm(dt,2h),8.04ppm(d,1h),8.29ppm(dd,2h),8.41ppm(dt,2h)
[0131]
[实施例3]化合物(p8)(al
‑
e(fg
‑
200me)2)的合成
[0132]
[化28]
[0133]
[实施例3
‑
1]化合物(p5)(ho
‑
e(fg
‑
200me)2)的合成
[0134]
[化29]
[0135]
将ε
‑
己内酯(114mg,1.0
×
10
‑3mol,东京化成工业株式会社制造)溶解于1n naoh(0.8ml,8.0
×
10
‑4mol,关东化学株式会社制造)中反应2小时,配制成6
‑
羟基己酸水溶液(0.88m)。此外,将实施例1中所得的化合物(p3)(2.0g,5.0
×
10
‑5mol)溶解于乙腈(8.0g)中。然后,将上述6
‑
羟基己酸水溶液(114μl,1.0
×
10
‑4mol)、二异丙基乙胺(20μl,1.2
×
10
‑4mol,关东化学株式会社制造)和dmt
‑
mm(21mg,6.0
×
10
‑5mol,和光纯药工业株式会社制造)添加到上述(p3)的乙腈溶液中,在室温下氮气气氛下反应1小时。反应结束后,将反应液在40℃下浓缩,向获得的浓缩物中添加氯仿(24g)进行溶解。添加饱和碳酸氢钠水溶液(10g),在室温下搅拌15分钟进行清洗。分离水层和有机层后,再次向有机层中添加饱和饱和碳酸氢钠水溶液(10g),在室温下搅拌15分钟进行清洗,回收有机层。向获得的有机层(氯仿溶液)中添加硫酸镁(1.2g),搅拌30分钟进行脱水,然后使用在5a滤纸上铺有oplite的桐山漏斗进行抽滤。在40℃下浓缩获得的滤液,向浓缩物中添加甲苯(50g)并搅拌至均匀,然后加入己烷(25g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后再次溶解于甲苯(50g)中,加入己烷(25g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用含bht(2mg)的己烷(10g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p5)(ho
‑
e(fg
‑
200me)2)。产量为1.5g。
[0136]1h
‑
nmr(cdcl3):1.37ppm(m,2h,ho
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.55ppm(m,4h,ho
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.77ppm(m,4h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),1.85ppm(m,1h),2.01ppm(m,2h,ho
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),3.01ppm(m,1h),3.24ppm(m,8h),3.38ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.03ppm(m,4h),4.14ppm(m,1h),4.48ppm(m,2h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),6.95ppm(宽,1h),7.00ppm(宽,1h),7.26ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.66ppm(宽,1h),8.29ppm(宽,1h)
[0137]
[实施例3
‑
2]化合物(p6)(sc
‑
e(fg
‑
200me)2)的合成
[0138]
[化30]
[0139]
将实施例3
‑
1中所得的化合物(p5)(500mg,1.3
×
10
‑5mol)溶解于二氯甲烷(3.5g)中。然后,添加n,n
’‑
二琥珀酰亚胺基碳酸酯(51mg,2.0
×
10
‑4mol,东京化成工业株式会社制造)和吡啶(24μl,3.0
×
10
‑4mol,关东化学株式会社制造),在室温下氮气气氛下反应8小时。反应结束后,用5%食盐水清洗反应液并加入硫酸镁(0.1g),在25℃下搅拌30分钟,然后使用在5a滤纸上铺有oplite的桐山漏斗进行抽滤。将获得的滤液浓缩后,向浓缩物中添加甲苯(50g)进行溶解,然后加入己烷(25g)并在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后再次溶解于甲苯(50g)中,加入己烷(25g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用含bht(5mg)的己烷(25g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p6)(sc
‑
e(fg
‑
200me)2)。产量为286mg。活性碳酸酯纯度为92%(1h
‑
nmr)。
[0140]1h
‑
nmr(cdcl3):1.38ppm(m,2h,琥珀酰亚胺
‑
oco
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.59ppm(m,2h,琥珀酰亚胺
‑
oco
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.75ppm(m,6h),1.85ppm(m,1h),2.13ppm(m,2h,琥珀酰亚胺
‑
oco
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),2.83ppm(s,4h,
‑
co
‑
ch2‑
ch2‑
co
‑
),3.01ppm(m,1h),3.19ppm(m,6h),3.38ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.03ppm(m,3h),4.18ppm(m,1h),4.31ppm(t,2h,琥珀酰亚胺
‑
oco
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),4.50ppm(m,2h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),6.98ppm(宽,1h),7.15ppm(宽,1h),7.26ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.81ppm(宽,1h),8.37ppm(宽,1h)
[0141]
[实施例3
‑
3]化合物(p7)(de
‑
e(fg
‑
200me)2)的合成
[0142]
[化31]
[0143]
将实施例3
‑
2中所得的化合物(p6)(250mg,6.3
×
10
‑6mol)溶解于氯仿(2g)中。然后,添加1
‑
氨基
‑
3,3
‑
二乙氧基丙烷(10μl,6.3
×
10
‑5mol,acros organics公司制造),在室温下氮气气氛下反应3小时。反应结束后,反应液用甲苯(25g)进行稀释,加入己烷(12.5g)并在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用含bht(2.5mg)的己烷(12.5g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p47)(de
‑
e(fg
‑
200me)2)。产量为185mg。
[0144]1h
‑
nmr(cdcl3):1.20ppm(t,6h,(ch3‑
ch2‑
o)2‑
ch
‑
),1.32ppm(m,2h,(ch3‑
ch2‑
o)2‑
ch
‑
ch2‑
ch2‑
nh
‑
coo
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.58ppm(m,2h,(ch3‑
ch2‑
o)2‑
ch
‑
ch2‑
ch2‑
nh
‑
coo
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.76ppm(m,4h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),1.82ppm(m,2h,(ch3‑
ch2‑
o)2‑
ch
‑
ch2‑
ch2‑
nh
‑
coo
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),2.11ppm(m,2h,(ch3‑
ch2‑
o)2‑
ch
‑
ch2‑
ch2‑
nh
‑
coo
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),2.16ppm(m,1h),2.70ppm(m,1h),3.06ppm(m,2h),3.25ppm(m,11h),3.38ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.02ppm(m,8h),4.17ppm(m,1h),4.51ppm(m,2h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),4.55ppm(t,1h,(ch3‑
ch2‑
o)2‑
ch
‑
),5.36ppm(宽,1h),6.47ppm(宽,1h),6.98ppm(宽,2h),7.26ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.81ppm(宽,1h),8.36ppm(宽,1h)
[0145]
[实施例3
‑
4]化合物(p8)(al
‑
e(fg
‑
200me)2)的合成
[0146]
[化32]
[0147]
将实施例3
‑
3中所得的化合物(p7)(150mg,3.8
×
10
‑6mol)溶解于调节ph至1.90的磷酸盐缓冲液(2.25g)中,在室温下氮气气氛下反应3小时。反应后,添加0.1n氢氧化钠水溶液(0.89g),调节ph至6.40后,添加氯化钠(0.56g)进行溶解。向获得的溶液中滴加0.1n氢氧化钠水溶液(0.60g),调节ph至7.06后,添加含bht(0.6mg)的氯仿(3g),在室温下搅拌20分钟,将生成物萃取至有机层。分离有机层和水层,回收有机层,然后向水层中再次添加含bht(0.6mg)的氯仿(3g),在室温下搅拌20分钟,将生成物萃取至有机层。将第1次萃取和第2次萃取中所得的有机层合并且在40℃下浓缩,将获得的浓缩物用甲苯(30g)稀释,加入己烷(15g)并在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用含bht(3.0mg)的己烷(15g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p8)(al
‑
e(fg
‑
200me)2)。产量为84mg。分子量示于表1中。醛纯度为92%(1h
‑
nmr)。
[0148]1h
‑
nmr(cdcl3):1.32ppm(m,2h,cho
‑
ch2‑
ch2‑
nh
‑
coo
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.57ppm(m,2h,cho
‑
ch2‑
ch2‑
nh
‑
coo
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.76ppm(m,4h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),1.82ppm(m,1h),2.10ppm(m,2h,cho
‑
ch2‑
ch2‑
nh
‑
coo
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),2.16ppm(m,1h),2.71ppm(m,2h,cho
‑
ch2‑
ch2‑
nh
‑
coo
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),3.02ppm(m,1h),3.26ppm(m,8h),3.38ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.01ppm(m,4h),4.16ppm(m,1h),4.49ppm(m,2h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),5.59ppm(宽,1h),6.36ppm(宽,1h),6.93ppm(宽,2h),7.08ppm(宽,1h),7.26ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.80ppm(宽,1h),8.37ppm(宽,1h),9.79ppm(s,1h,cho
‑
ch2‑
ch2‑
nh
‑
coo
‑
)
[0149]
[实施例4]化合物(p9)(nh2o
‑
e(fg
‑
200me)2)的合成
[0150]
[化33]
[0151]
将实施例3
‑
1中所得的化合物(p5)(300mg,7.5
×
10
‑6mol)在30℃下加温溶解于甲苯(2.4g)中,减压下共沸脱水。然后,将浓缩物溶解于氯仿(2.4g)中,添加n
‑
羟基邻苯二甲酰亚胺(7.3mg,4.5
×
10
‑5mol,和光纯药工业株式会社制造)、三苯基膦(35mg,1.4
×
10
‑4mol,关东化学株式会社制造)和偶氮二羧酸二异丙酯(22μl,1.1
×
10
‑4mol,acros organics公司制造),在室温下氮气气氛下反应4小时。反应结束后,向反应液中添加甲醇(9.1μl)并在25℃下搅拌30分钟,在40℃下浓缩。将浓缩物用甲苯(3.0g)稀释并共沸,然后将浓缩物溶解于甲苯(1.5g)中,添加乙二胺一水合物(24μl,3.0
×
10
‑4mol,关东化学株式会社制造),在室温下氮气气氛下反应1小时。反应结束后,反应液用甲苯(50g)进行稀释,然后加入己烷(25g)并在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用己烷(20g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p9)(nh2o
‑
e(fg
‑
200me)2)。产量为156mg。分子量示于表1中。hplc:氧化胺纯度91%。
[0152]1h
‑
nmr(cdcl3):1.32ppm(m,2h,h2n
‑
o
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.56ppm(m,4h,h2n
‑
o
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),1.76ppm(m,4h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),1.85ppm(m,1h),2.10ppm(m,2h,h2n
‑
o
‑
ch2‑
ch2‑
ch2‑
ch2‑
ch2‑
co
‑
nh
‑
),2.17ppm(m,1h),3.01ppm(m,1h),3.24ppm(m,8h),3.38ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.03ppm(m,2h),4.17ppm(m,1h),4.49ppm(m,2h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),5.37ppm(宽,2h),6.40ppm(宽,1h),6.95ppm(宽,2h),7.12ppm(宽,1h),7.26ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.74ppm(宽,1h),8.31ppm(宽,1h)
[0153]
[实施例5]化合物(p13)(nh2‑
e{e(fg
‑
100me)2}2)的合成
[0154]
[化34]
[0155]
[实施例5
‑
1]化合物(p10)(me
‑
100gf
‑
fmoc)的合成
[0156]
[化35]
[0157]
按照与实施例1
‑
1相同的制造方法,使用n末端被fmoc基保护的l
‑
苯丙氨酰
‑
甘氨酸(fmoc
‑
phe
‑
gly)(533mg,1.2
×
10
‑3mol,渡边化学工业株式会社制造)和末端具有丙基氨基的甲氧基peg(9.9g,1.0
×
10
‑3mol,数均分子量=9,896,日油株式会社制造的“sunbright mepa
‑
10t”)作为原料,获得上述化合物(p10)(me
‑
100gf
‑
fmoc)。产量为9.2g。
[0158]1h
‑
nmr(d6‑
dmso):1.62ppm(m,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),2.80ppm(m,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.04ppm(m,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.10ppm(m,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.24ppm(s,3h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.48ppm(m,约900h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.20ppm(m,4h),7.33ppm(m,9h),7.66ppm(m,4h,ar),7.88ppm(d,2h,ar),8.27ppm(t,1h)
[0159]
[实施例5
‑
2]化合物(p11)(me
‑
100gf
‑
nh2)的合成
[0160]
[化36]
[0161]
按照与实施例1
‑
2相同的制造方法,使用实施例5
‑
1中所得的化合物(p10)(9.2g,4.6
×
10
‑4mol)进行脱保护反应,获得上述化合物(p11)(me
‑
100gf
‑
nh2)。产量为8.7g。
[0162]1h
‑
nmr(d6‑
dmso):1.62ppm(m,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),1.64ppm(宽,1h),2.59ppm(dd,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),2.98ppm(dd,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.10ppm(q,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.24ppm(s,3h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.48ppm(m,约900h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),7.24ppm(m,6h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5,
‑
nh
‑
),7.73ppm(t,1h),8.12ppm(宽,1h)
[0163]
[实施例5
‑
3]化合物(p12)(nh2‑
e(fg
‑
100me)2)的合成
[0164]
[化37]
[0165]
按照与实施例1
‑
3相同的制造方法,使用n末端被fmoc基保护的l
‑
谷氨酸(fmoc
‑
glu
‑
oh)(135mg,3.7
×
10
‑4mol,渡边化学工业株式会社制造)和实施例5
‑
2中所得的化合物(p11)(8.5g,8.5
×
10
‑4mol)作为原料,连续进行反应和脱保护,获得上述化合物(p12)(nh2‑
e(fg
‑
100me)2)。产量为6.6g。hplc:胺纯度95%。
[0166]1h
‑
nmr(d6‑
dmso):1.54ppm(m,2h,
‑
nh
‑
co
‑
ch(nh2)
‑
ch2‑
ch2‑
),1.62ppm(m,4h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
),1.97ppm(m,2h,
‑
nh
‑
co
‑
ch(nh2)
‑
ch2‑
ch2‑
),2.74ppm(dd,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),2.81ppm(dd,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),3.11ppm(m,11h),3.24ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约1,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.49ppm(m,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),4.57ppm(m,1h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.25ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.74ppm(m,2h),8.44ppm(m,2h),8.61ppm(m,2h)
[0167]
[实施例5
‑
4]化合物(p13)(nh2‑
e{e(fg
‑
100me)2}2)的合成
[0168]
[化38]
[0169]
按照与实施例1
‑
3相同的制造方法,使用n末端被fmoc基保护的l
‑
谷氨酸(fmoc
‑
glu
‑
oh)(15.2mg,4.1
×
10
‑5mol,渡边化学工业株式会社制造)和实施例5
‑
3中所得的化合物(p12)(2.0g,1.0
×
10
‑4mol)作为原料,连续进行反应和脱保护,获得上述化合物(p13)(nh2‑
e{e(fg
‑
100me)2}2)。产量为1.2g。分子量示于表1中。hplc:胺纯度94%。
[0170]1h
‑
nmr(d6‑
dmso):1.62ppm(m,14h),2.00ppm(m,6h,
‑
nh
‑
co
‑
ch(nh2)
‑
ch2‑
ch2‑
),2.78ppm(m,4h),3.11ppm(m,14h),3.24ppm(s,16h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,600h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.19ppm(m,2h),4.51ppm(m,4h),7.25ppm(m,20h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.71ppm(m,4h),7.89ppm(m,1h),8.45ppm(m,9h)
[0171]
[实施例6]
[0172]
化合物(p16)(nh2‑
e(gflg
‑
200me)2)的合成
[0173]
[化39]
[0174]
[实施例6
‑
1]化合物(p14)(me
‑
200glfg
‑
fmoc)的合成
[0175]
[化40]
[0176]
按照与实施例1
‑
1相同的制造方法,使用n末端被fmoc基保护的l
‑
甘氨酰
‑
苯丙氨酰
‑
亮氨酰
‑
甘氨酸(fmoc
‑
gly
‑
phe
‑
leu
‑
gly)(66mg,1.1
×
10
‑4mol,渡边化学工业株式会社制造)和末端具有丙基氨基的甲氧基peg(1.5g,7.1
×
10
‑5mol,数均分子量=21,120,日油株式会社制造的“sunbright mepa
‑
20t”)作为原料,获得上述化合物(p14)(me
‑
200glfg
‑
fmoc)。产量为1.2g。
[0177]1h
‑
nmr(cdcl3):0.89ppm(d,3h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2)、0.91ppm(d,3h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1.53ppm(m,2h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1,70ppm(m,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1.80ppm(m,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.10ppm(dd,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.18ppm(dd,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.33ppm(m,7h),3.74ppm(m,约1,900h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.31ppm(宽,1h),4.55ppm(t,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),6.91ppm(宽,1h),7.00ppm(宽,1h),7.28ppm(m,5h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),7.33ppm(t,2h,ar),7.41ppm(m,3h,ar),7.73ppm(m,3h,ar),7.89ppm(d,2h,ar),7.98ppm(宽,1h)
[0178]
[实施例6
‑
2]化合物(p15)(me
‑
200glfg
‑
nh2)的合成
[0179]
[化41]
[0180]
按照与实施例1
‑
2相同的制造方法,使用实施例6
‑
1中所得的化合物(p14)(1.2g,5.7
×
10
‑5mol)进行脱保护反应,获得上述化合物(p15)(me
‑
200glfg
‑
nh2)。产量为1.0g。
[0181]1h
‑
nmr(cdcl3):0.89ppm(d,3h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2)、0.91ppm(d,3h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1.53ppm(m,2h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1,70ppm(m,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1.80ppm(m,2h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.10ppm(dd,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.18ppm(dd,1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),3.33ppm(m,7h),3.74ppm(m,约1,900h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.31ppm(宽,1h),4.55ppm(t,
1h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),6.91ppm(宽,1h),7.00ppm(宽,1h),7.28ppm(m,5h,
‑
nh
‑
co
‑
ch
‑
ch2‑
c6h5),7.98ppm(宽,1h)
[0182]
[实施例6
‑
3]化合物(p16)(nh2‑
e(gflg
‑
200me)2)的合成
[0183]
[化42]
[0184]
按照与实施例1
‑
3相同的制造方法,将n末端被fmoc基保护的l
‑
谷氨酸(fmoc
‑
glu
‑
oh)(8.3mg,2.3
×
10
‑5mol,渡边化学工业株式会社制造)和实施例6
‑
2中所得的化合物(p15)(1.0g,4.8
×
10
‑5mol)用作原料,连续进行反应和脱保护,获得上述化合物(p16)(nh2‑
e(gflg
‑
200me)2)。产量为0.5g。分子量示于表1中。hplc:胺纯度90%。
[0185]1h
‑
nmr(cdcl3):0.89ppm(d,6h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2)、0.91ppm(d,6h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1.53ppm(m,4h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1,70ppm(m,2h,
‑
nh
‑
co
‑
ch
‑
ch2‑
ch(ch3)2),1.77ppm(m,4h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),1.85ppm(m,1h),3.01ppm(m,1h),3.24ppm(m,8h),3.38ppm(s,6h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.64ppm(m,约3,800h,
‑
co
‑
nh
‑
ch2‑
ch2‑
ch2‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.03ppm(m,4h),4.14ppm(m,1h),4.48ppm(m,2h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),6.95ppm(宽,1h),7.00ppm(宽,1h),7.26ppm(m,10h,
‑
co
‑
nh
‑
ch
‑
ch2‑
c6h5),7.66ppm(宽,2h),8.29ppm(宽,2h)
[0186]
[比较例1]
[0187]
化合物(p18)(ly
‑
400nh2)的合成
[0188]
[化43]
[0189]
[比较例1
‑
1]
化合物(p17)(ly
‑
400bo)的合成
[0190]
[化44]
[0191]
将已上市的聚乙二醇修饰剂中使用的赖氨酸骨架的2分支型聚乙二醇活化酯(3.0g,7.5
×
10
‑5mol,数均分子量=39,700,日油株式会社制造的“sunbright ly
‑
400ns”)在40℃下加温溶解于甲苯(15g)中,添加n
‑
(叔丁氧基羰基)
‑
1,2
‑
二氨基乙烷(48μl,3.0
×
10
‑4mol,东京化成工业株式会社制造),在40℃下在氮气气氛下反应1小时。反应结束后,反应液用乙酸乙酯(12g)进行稀释,然后加入己烷(14g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后再次溶解于乙酸乙酯(27g)中,加入己烷(14g),在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用己烷(30g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p17)(ly
‑
400bo)。产量为2.7g。
[0192]1h
‑
nmr(cdcl3):1.37ppm(m,2h),1.43ppm(s,9h,
‑
ch2‑
nh
‑
co2‑
c
‑
(ch3)3),1.51ppm(m,2h),3.15ppm(m,2h),3.38ppm(s,6h,
‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.65ppm(m,约3,650h,
‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.21ppm(m,4h)
[0193]
[比较例1
‑
2]化合物(p18)(ly
‑
400nh2)的合成
[0194]
[化45]
[0195]
将比较例1
‑
1中所得的化合物(p17)(1.0g,2.5
×
10
‑6mol)溶解于离子交换水(4.0g)中,添加甲磺酸(57μl,8.8
×
10
‑4mol,关东化学株式会社制造),在40℃下在氮气气氛下反应6小时。反应后,用离子交换水(6.0g)进行稀释,添加1n氢氧化钠水溶液(0.9g),调节ph至12后,添加氯化钠(2.5g)进行溶解。向获得的溶液中添加含bht(1.0mg)的氯仿(10g),在室温下搅拌20分钟,将生成物萃取至有机层。分离有机层和水层,回收有机层,然后在40℃下进行浓缩,将获得的浓缩物用甲苯(30g)进行稀释,加入己烷(15g)并在室温下搅拌15分钟使生成物析出。使用5a滤纸进行抽滤,回收析出物,然后用含bht(3.0mg)的己烷(15g)进行清洗,使用5a滤纸进行抽滤,真空干燥而获得上述化合物(p18)(ly
‑
400nh2)。产量为0.7g。分子量示于表1中。hplc:胺纯度97%。
[0196]1h
‑
nmr(cdcl3):1.37ppm(m,2h),1.51ppm(m,2h),3.15ppm(m,2h),3.38ppm(s,6h,
‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),3.65ppm(m,约3,650h,
‑
o
‑
(ch2‑
ch2‑
o)n
‑
ch3),4.21ppm(m,4h)
[0197]
[表1] 样品名分子量(m
n
)实施例1化合物(p3)42,417实施例2化合物(p4)42,534实施例3化合物(p8)42,334实施例4化合物(p9)42,190实施例5化合物(p13)38,234实施例6化合物(p16)42,398比较例1化合物(p 18)39,654
[0198]
[实施例7]在血清中的稳定性试验向1.5ml的微型离心管中,加入小鼠或人血清1ml,添加各种聚乙二醇衍生物至浓度成为5.0mg/ml。在37℃下孵育96小时后,取样200μl,向其中添加乙腈,用旋涡搅拌器搅拌1分钟,使血清中的蛋白质析出,离心分离后,回收上清液。接着为了去除脂肪酸等疏水性物质,向回收液中添加己烷,用旋涡搅拌器搅拌1分钟,离心分离后,回收下层。将该溶液在真空条件下进行浓缩,从血清中回收聚乙二醇衍生物。然后,进行gpc分析,计算分解性聚乙二醇衍生物的分解率。分解率按下式进行计算:分解率=(试验前的40kda的峰面积%
‑
试验后的40kda的峰面积%)
÷
(试验前的40kda的峰面积%)
×
100结果示于下表2中。
[0199]
[表2]
[0200]
根据表2,作为分解性聚乙二醇衍生物的化合物(p3)、(p13)、(p16)与作为非分解性的聚乙二醇衍生物的化合物(p18)、甲氧基peg胺40kda同样地,在血清中未观察到分解。即表示该分解性聚乙二醇衍生物在血液中稳定。
[0201]
[实施例8]使用细胞的分解性试验使用培养基rpmi
‑
1640(10%fbs pn/st)10ml,向100mm培养皿中接种10
×
106细胞的raw264.7,在37℃下培养24小时后,更换到溶解有各种聚乙二醇衍生物至浓度成为10mg/ml的培养基,在37℃下培养96小时。培养后,将细胞溶解于1%sds溶液中,用磷酸盐缓冲生
理盐水(pbs)进行稀释,向其中添加乙腈,用旋涡搅拌器搅拌1分钟,使细胞溶解液中的蛋白质析出,离心分离后,回收上清液。接着为了去除脂肪酸等疏水性物质,向回收液中添加己烷,用旋涡搅拌器搅拌1分钟,离心分离后,回收下层。将该溶液在真空条件下进行浓缩,从细胞内回收聚乙二醇衍生物。另外,为了确认在用于细胞培养的培养基中的分解,在37℃下仅在溶解有各种聚乙二醇衍生物至浓度成为10mg/ml的培养基中培养96小时,按照与上述相同操作进行聚乙二醇衍生物的回收。然后,进行回收的各种聚乙二醇衍生物的gpc分析,按照与实施例7相同的计算式,计算分解性聚乙二醇衍生物的分解率。结果示于下表3中。此外,化合物(p3)、(p13)的细胞实验前后的gpc图谱分别示于图1和图2、图3和图4中。
[0202]
[表3]
[0203]
根据表3,作为分解性聚乙二醇衍生物的化合物(p3)和(p16)可确认到在细胞内有效地分解(分解率99%),从分子量4万分解至2万。此外,在化合物(p13)中,可确认到以分解率99%从分子量4万分解至1万。这些分解性聚乙二醇衍生物由于在用于细胞培养的培养基中不分解,因此确认在细胞内被特异性分解。另一方面,在作为非分解性的聚乙二醇衍生物的化合物(p18)和甲氧基peg胺40kda中,均未观察到在细胞内的分解。
[0204]
[实施例9]利用动物试验的空泡形成评价试验使用作为在末端具有氨基的分子量4万的分解性聚乙二醇衍生物的化合物(p3)nh2‑
e(fg
‑
200me)2和具有非分解性的甲氧基peg胺40kda,进行利用动物实验的空砲形成评价。小鼠品种为balb/c(8周龄,雄性),聚乙二醇溶液使用生理盐水配制聚乙二醇衍生物至浓度成为100mg/ml,经由小鼠尾静脉给药20μl。持续进行每周3次、4周的连续给药,给药完成后,用4%多聚甲醛水溶液对小鼠进行灌注固定,制作石蜡切片。进行he染色和利用抗peg抗体的免疫染色,评价脑脉络丛上皮细胞中的空泡形成。作为免疫染色,使用免疫染色试剂盒(bond refine polymer detection kit,徕卡公司制造)和抗peg抗体(b
‑
47抗体,abcam公司制造)来实施。进行利用抗peg抗体的免疫染色的脑脉络丛切片的图像示于图5(甲氧基peg胺40kda)和图6(nh2‑
e(fg
‑
200me)2)中。其结果,作为分解性聚乙二醇的nh2‑
e(fg
‑
200me)2相比于甲氧基peg胺40kda,显著地抑制了空泡的形成。此外,本实施例中给药的聚乙二醇的量终归是为了评价空泡化而优化后的量,相比于该技术领域中的通常的聚乙二醇的给药量,是非常多的量。
[0205]
[实施例10]利用动物实验的聚乙二醇的蓄积性评价试验使用作为在末端具有氨基的分子量4万的分解性聚乙二醇衍生物的化合物(p3)nh2‑
e(fg
‑
200me)2和具有非分解性的甲氧基peg胺20kda、甲氧基peg胺40kda和作为对照的pbs,进行利用动物实验的聚乙二醇的蓄积性评价。小鼠品种为balb/c(8周龄,雄性),聚乙二醇溶液使用生理盐水配制聚乙二醇衍生物至浓度成为62.5mg/ml,经由小鼠尾静脉给药100μl。持续进行每周3次、4周的连续给药,给药完成后,用4%多聚甲醛水溶液对小鼠进行灌注固定,制作石蜡切片。进行利用抗peg抗体的免疫染色,评价脑脉络丛上皮细胞中的蓄积性。进行免疫染色后的各脑脉络丛切片的图像示于图7中。根据图7,在给予不含聚乙二醇的pbs的小鼠脉络丛切片中未被染色,与此相对,在作为非分解性的甲氧基peg胺40kda中,确认到切片大范围被染色为褐色。该染色部分表示peg出现蓄积。另一方面,在作为分解性聚乙二醇的nh2‑
e(fg
‑
200me)2的切片中,被染成褐色的部分较少,显示出与分子量为其一半的甲氧基peg胺20kda相同的蓄积。作为结果,分解性聚乙二醇由于其分解性,相比于作为相同分子量的非分解性的甲氧基peg胺40kda,显著地抑制了聚乙二醇在组织中的蓄积。此外,本实施例中给药的聚乙二醇的量终归是为了评价蓄积性而优化后的量,相比于该技术领域中的通常的聚乙二醇的给药量,是非常多的量。
[0206]
[实施例11]利用动物实验的药代动力学试验(放射性同位素)将作为在末端具有氨基的分子量4万的分解性聚乙二醇衍生物的nh2‑
e(fg
‑
200me)2、作为非分解性2分支型peg胺40kda(平均分子量=约42,000,日油株式会社制造的“sunbright gl2
‑
400pa”)和作为非分解性2分支型peg胺20kda(平均分子量=约20,000,日油株式会社制造的“sunbright gl2
‑
200pa”)分别以浓度为10mg/ml地溶解于50mm碳酸氢钠水溶液中,向其中添加bolton
‑
hunter(羟苯基丙酸n
‑
羟基琥珀酰亚胺酯)试剂(0.4625mbq),用旋涡搅拌器搅拌后,室温反应过夜。反应溶液经pd
‑
10柱分离,对各馏分使用聚乙二醇显色剂(使用硫氰酸铵和硝酸钴)和γ计数器,确认含有
125
i的馏分并回收。使用获得的放射性同位素标记的聚乙二醇衍生物,在动物实验中评价药代动力学。小鼠品种为balb/c(8周龄,雄性),聚乙二醇溶液使用生理盐水配制未标记的聚乙二醇衍生物至浓度成为10mg/ml,微量添加放射性同位素标记的聚乙二醇衍生物,经由小鼠尾静脉给药100μl。然后,在第1、3、6、24、48、72小时时从小鼠取出血液、各脏器,使用γ计数器测定标记的聚乙二醇衍生物的滞留量。作为放射性同位素标记的分解性聚乙二醇衍生物的nh2‑
e(fg
‑
200me)2、作为非分解性的聚乙二醇衍生物的2分支型peg胺40kda和2分支型peg胺20kda的药代动力学试验的结果,将血液中浓度示于图8中。根据图8,nh2‑
e(fg
‑
200me)2相比于作为相同分子量的非分解性2分支型peg胺40kda,显示出相同程度的血液半衰期。另一方面,nh2‑
e(fg
‑
200me)2相比于分子量20kda的非分解性2分支型peg胺20kda,显示出显著长的血液半衰期。产业上的可利用性
[0207]
本发明的分解性聚乙二醇衍生物是不引起细胞的空泡的高分子量的聚乙二醇衍
生物,能够有效地用于对生物相关物质进行修饰的用途、在生物体内血液中稳定且在细胞内被分解。
[0208]
本技术以在日本技术的日本专利特愿2019
‑
069449(申请日:2019年3月29日)为基础,其内容全部包含在本说明书中。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。