用于癌症治疗的脑信号蛋白
‑
4d拮抗剂
背景技术:
1.脑信号蛋白4d(sema4d),也称作cd100,是一种属于脑信号蛋白基因家族的跨膜蛋白。sema4d在细胞表面上表达为同二聚体,但在细胞激活之后,sema4d可通过蛋白水解切割从细胞表面上释放以生成该蛋白质的溶解形式ssema4d,其也是有生物活性的。参见suzuki等,nature rev.immunol.3:159
‑
167(2003);kikutani等,nature immunol.9:17
‑
23(2008)。
2.sema4d在包括脾脏、胸腺和淋巴结的淋巴器官中以及如脑、心脏和肾脏的非淋巴器官中以高水平表达。在淋巴器官中,sema4d在静息t细胞上大量表达,但是仅在静息b细胞和抗原呈递细胞(apc)如树突细胞(dc)上弱表达。然而,在用各种免疫刺激激活之后,其表达在这些细胞中上调。细胞激活也增加了可溶性sema4d从免疫细胞的释放。sema4d已与某些癌症的发展密切关联(ch’ng等,cancer 110:164
‑
72(2007);campos等,oncology letters,5:1527
‑
35(2013);kato等,cancer sci.102:2029
‑
37(2011))。
3.之前我们已经报道了抗
‑
sema4d拮抗物单克隆抗体vx15/2503派比奈单抗(pepinemab)单独(参见例如,美国专利号9,605,055)或与包括检查点阻断的各种其他癌症免疫疗法治疗组合(参见例如,美国专利号9,243,068)在治疗多种癌症中有效。这些结果已经拓展到临床,参见例如,patnaik,a.,等clin.cancer res.22:827
‑
836(2016)。此外,我们已经表明,与其他癌症患者相比,当患有癌症的对象在治疗前t细胞(例如,cd8 t细胞)、b细胞或t细胞和b细胞的水平升高时,他们的情况往往会更好(参见例如,美国专利号9,243,068)。
4.髓源性抑制细胞(mdsc)是一组异质性髓源细胞,具有肿瘤促进和/或免疫抑制活性。参见lang,s.,等clin.cancerres.24:4834
‑
4844(2018)。人mdsc的不同群体以不同表面标志物为特征。例如,循环多形核mdsc(pmn
‑
mdsc)表达cd15和/或cd66b,缺乏单核标志物cd14,且cd33呈阳性。与pmn
‑
mdsc相比,单核mdsc(m
‑
mdsc)通常表达较高水平cd33,呈cd14 ,并且hla
‑
dr水平较低甚至不存在。同上。mdsc特征还在于不存在其他细胞谱系典型标志物,例如它们的特征在于不存在标志物cd3、cd19和/或cd56。参见例如,gabrilovich等cancer immunol res.5:3
‑
8(2017).
5.本领域仍然需要定义癌症患者群体的其他方法,这些癌症患者群体可能受益于使用派比奈单抗单独治疗或与其他免疫治疗剂组合治疗。
技术实现要素:
6.本发明涉及用于治疗癌症和选择进行治疗的患癌对象的方法。本发明提供了用于治疗和选择患癌对象的方法,用于治疗、抑制、延迟或减少对象中恶性肿瘤细胞生长,通过给予对象有效量的癌症免疫治疗方案,其包括给予特异性结合脑信号蛋白
‑
4d(sema4d)的分离抗体或其抗原结合片段。该方法包括确定对象中循环mdsc的水平,如果mdsc水平低于预定阈值水平,则选择对象进行治疗。在某些方面,循环mdsc水平通过获得或已经获得生物样品测定,例如来自对象的血液样品或肿瘤活检,并进行或已经进行测定,例如对生物样品
biomedicine and molecular biology),juo,pei
‑
show,第2版,2002,crc出版社(crc press);《细胞和分子生物学词典》(the dictionary of cell and molecular biology),第5版,2013,学术出版社(academic press);和《牛津生物化学和分子生物学辞典》(oxford dictionary of biochemistry and molecular biology),第2版,2008,牛津大学出版社(oxford university press),向技术人员提供了本发明使用的很多术语的常用词典。
18.单位、前缀和符号以它们的国际单位制(si)接受的形式表示。数值范围包括限定该范围的数值。除非另外说明,氨基酸以氨基到羧基的取向从左到右书写。本文提供的标题不是本发明各种方面或某方面的限制,可以参考说明书整体理解本发明的各种方面或实施方式。因此,下面紧接着定义的术语完全参考说明书全文定义。
19.本文所用的术语“多肽”意在包括单数形式“多肽”和复数形式“多肽”,指由酰胺键(也称肽键)线性连接的多个单体(氨基酸)所组成的分子。术语
″
多肽
″
指的是两个或更多个氨基酸的任何一条链或多条链,并且不表示特定长度的产物。因此,肽、二肽、三肽、寡肽、“蛋白质”、“氨基酸链”或其它任何用于指两个或多个氨基酸的一条或多条链的术语均包含于“多肽”的定义内,术语“多肽”可与任意这些术语替代或互换使用。术语“多肽”还指多肽表达后修饰的产物,所述修饰包括但不限于糖基化、乙酰基化、磷酸化、酰胺化,和通过已知保护/阻断基团、蛋白酶切割或非天然产生氨基酸修饰的衍生化。多肽可由生物来源衍生或由重组技术产生,但不必定由指定核酸序列翻译而来。其可以任何方式产生,包括通过化学合成。
20.多肽可具有确定的三维结构,但它们不必定具有这种结构。本文所用的术语糖蛋白指偶联至至少一个糖部分的蛋白质,所述糖部分通过某一氨基酸如丝氨酸或天冬酰胺的含氧或含氮侧链连接于该蛋白质。
21.述及“分离的”多肽或其片段、变体或衍生物指不处于其天然环境中的多肽。对具体纯化水平没有要求。例如,可从其原生或天然环境中移出分离的多肽。在宿主细胞中表达的重组产生多肽和蛋白质被认为是如本文公开的分离的,通过任何合适技术分离、分级,或者部分或基本上纯化的天然或重组多肽也如此。
22.本文中所用的术语“非天然产生的多肽”或其任何语法变化形式,是条件性的限定,其明确地排除,但仅排除,被法官或管理部门或司法机关或可能会被法官或管理部门或司法机关确定或解释为“天然产生的”那些多肽形式。
23.本文公开的其它多肽是前述多肽的片段、衍生物、类似物或变体,及其任何组合。本文所述的术语
″
片段
″
、
″
变体
″
、
″
衍生物
″
和
″
类似物
″
包括保持对应的原始抗体或多肽的至少一些性质(例如,特异性结合至抗原)的任何多肽。除本文他处讨论的具体抗体片段外,多肽的片段还包括,例如,蛋白酶水解片段以及缺失片段。例如,多肽的变体包括如上所述的片段,以及因氨基酸取代、缺失或插入而具有改变的氨基酸序列的多肽。变体多肽可包含保守或非保守性氨基酸取代、缺失或添加。衍生物是经改变从而显示原始多肽上不存在的其它特征的多肽。例子包括融合蛋白。
[0024]“保守性氨基酸取代”是其中一个氨基酸被具有相似侧链的另一个氨基酸替代的情况。本领域中已定义了具有类似侧链的氨基酸的家族,包括碱性侧链(如赖氨酸、精氨酸、组氨酸)、酸性侧链(如天冬氨酸、谷氨酸)、不带电荷的极性侧链(如天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、酪氨酸、半胱氨酸)、非极性侧链(如甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨
酸、脯氨酸、苯丙氨酸、甲硫氨酸、色氨酸)、β
‑
分支侧链(如苏氨酸、缬氨酸、异亮氨酸)和芳族侧链(如酪氨酸、苯丙氨酸、色氨酸、组氨酸)。例如,苯丙氨酸取代成酪氨酸是保守取代。在某些实施方式中,本发明的多肽和抗体的序列中的保守取代不废除包含所述氨基酸序列的多肽或抗体与所述结合分子结合的抗原的结合。鉴定不消除抗原结合的核苷酸和氨基酸保守取代的方法是本领域熟知的(参见,例如,brummell等,biochem.32:1180
‑
1 187(1993);kobayashi等,protein eng.12(10):879
‑
884(1999);和burks等,proc.natl.acad.sci.usa 94:.412
‑
417(1997))。
[0025]
术语“多核苷酸”意在包括单个核酸和多个核酸,指分离的核酸分子或构建物,例如信使rna(mrna)、cdna或质粒dna(pdna)。多核苷酸可包含常规磷酸二酯键或非常规键(如酰胺键,如肽核酸(pna)中发现的酰胺键)。术语“核酸”或“核酸序列”指多核苷酸中存在的任何一种或多种核酸区段,如dna或rna片段。
[0026]
述及
″
分离的
″
核酸或多核苷酸意为与其原始环境分离的核酸或多核苷酸的任何形式。例如,凝胶纯化的多核苷酸,或载体中编码所含多肽的重组多核苷酸将被视作是“分离的”。并且,认为已被工程改造以具有供于克隆的限制性位点的多核苷酸区段,例如,pcr产物,是“分离的”。分离的多核苷酸的其它示例包括在异源性宿主细胞中维持的重组多核苷酸或在非原始溶液(例如缓冲液或盐水)中(部分地或基本上)纯化的重组多核苷酸。分离的rna分子包括多核苷酸的体内或体外rna转录本,其中,所述转录本不是自然中存在的转录本。分离的多核苷酸或核酸还包括通过合成方式产生的此类分子。此外,多核苷酸或核酸可以是或可包括调节元件例如启动子、核糖体结合位点,或转录终止子。
[0027]
本文中所用的术语“非天然产生的多核苷酸”或其任何语法变化形式,是条件性的限定,其明确地排除,但仅排除,被判定机构或管理部门或司法机关或可能会被被判定机构或管理部门或司法机关确定或解释为“天然产生的”那些核酸或多核苷酸形式。
[0028]
本文所用的术语“编码区”指由翻译成氨基酸的密码子组成的核酸部分。虽然“终止密码子”(tag、tga或taa)不翻译成氨基酸,但它可被认为是编码区的一部分,而任何侧接序列如启动子、核糖体结合位点、转录终止子、内含子等均不是编码区的一部分。
[0029]
在某些实施方式中,所述多核苷酸或核酸是dna。对dna而言,包含多肽编码核酸的多核苷酸通常包含启动子和/或其它转录或翻译控制元件,这些元件与一个或多个编码区操作性连接。操作性连接指当基因产物如多肽的编码区与一个或多个调控序列以此方式连接时,将该基因产物的表达置于所述调控序列的影响或控制下。如果启动子功能的诱导使编码所需基因产物的mrna转录,且如果两个dna片段间连接的属性不干扰表达调控序列指导基因产物表达或不干扰转录dna模板的能力,则两个dna片段(如多肽编码区及其相连的启动子)“操作性连接”。因此,如果启动子能够影响核酸的转录,则启动子区域与多肽编码核酸操作性连接。启动子可以是在预定细胞中指导dna实质转录的细胞特异性启动子。启动子以外的其它转录控制元件如增强子、操纵基因、阻遏物和转录终止信号,能与多核苷酸可操作连接以指导细胞特异性转录。
[0030]
在其它实施方式中,多核苷酸可以是rna,例如,信使rna(mrna)、转移rna或核糖体rna的形式。
[0031]
本文中所用的术语“结合分子”以其最宽泛的含义指特异性结合至受体(例如,表位或抗原决定簇)的分子。如本文进一步描述,结合分子可包含本文所述的多种“抗原结合
结构域”之一。结合分子的非限制性示例是抗体或其保持抗原
‑
特异性结合性的片段。
[0032]
本文中所用的术语“结合结构域”或“抗原
‑
结合结构域”指的是必需且足以特异性结合至表位的结合分子的区域。例如,“fv",例如,抗体的可变重链和可变轻链,以两个分开多肽亚基或作为单一链形式,被视作是“结合结构域”。其它结合结构域包括,但不限于,源自骆驼科物种的抗体的可变重链(vhh),或在纤连蛋白支架上表达的六个免疫球蛋白互补决定区(cdr)。
[0033]
抗体(或其抗原结合片段、变体或衍生物,或其多聚片段、变体或衍生物,如本文所述)包括:至少重链的可变区(对于骆驼科物种而言)或至少重链和轻链的可变区。脊椎动物系统中的基本免疫球蛋白结构是相对较好地了解的。参见例如,harlow等,《抗体:实验室手册》(antibodies:a laboratory manual)(冷泉港实验室出版社(cold spring harbor laboratory press),第2版,1988)。除非另有说明,术语“抗体”涵盖从抗体的小抗原结合片段到全尺寸抗体范围内的任何物质,例如,igg抗体,其包括两个完整重链和两个完整轻链。
[0034]
正如下文中更详细讨论,术语“免疫球蛋白”包括可通过生化性质区分的各种类型多肽。本领域技术人员将理解,重链被分类为γ、μ、α、δ或ε(γ、μ、α、δ、ε),其中还有一些亚类(例如γ1
‑
γ4或α1
‑
α2)。该链的特性决定抗体“同种型”分别为igg、igm、iga、igg或ige。免疫球蛋白亚类(亚型)如igg1、igg2、igg3、igg4、iga1、iga2等已被充分表征,且已知提供功能性特化。根据本文公开内容,本领域技术人员不难区分这些免疫球蛋白各自的修饰形式,因此,它们涵盖在本发明范围内。
[0035]
轻链分类为κ或λ(kappa或lambda)。各重链类别可与κ或λ轻链结合。通常,轻链和重链互相共价键合,并且当由例如杂交瘤、b细胞或遗传工程改造的宿主细胞表达免疫球蛋白时,两条重链的“尾”部分通过共价二硫键或非共价连接键合在一起。在重链中,氨基酸从y构型的分叉末端处的n
‑
端到各条链的底部处的c
‑
端。某些抗体(例如,igg抗体)的基础结构包括两个重链亚基和两个轻链亚基,其通过二硫键共价连接以形成“y”结构,也在本文中称为“h2l2”结构。
[0036]
术语“表位”包括任意能够特异性结合抗体的分子决定簇。在某些方面,表位可包括有化学活性的成组表面分子(例如氨基酸、糖侧链、磷酰基或磺酰基(sulfonyl)),以及,在某些方面,可具有三维结构特点和或特定的荷电特点。表位是被抗体结合的靶标的区域。
[0037]
术语“靶标”以最广泛的含义使用以包括可被结合分子结合的物质。靶标可以是例如多肽、核酸、碳水化合物、脂质或其他分子。另外,“靶标”可以是,例如,包含可被结合分子结合的表位界限的细胞、器官或生物体。
[0038]
轻链和重链都被划分成具有结构和功能同源性的区域。从功能角度使用术语“恒定”和“可变”。在这方面,应理解可变轻(vl)链或可变重(vk)链部分的可变区决定抗原识别和特异性。相反,轻链(cl)和重链(例如ch1、ch2、ch3或ch4(如果存在))的恒定区赋予生物学特性,例如分泌、跨胎盘移动、fc受体结合、补体结合等。按照习惯,恒定区结构域的编号随着远离抗原结合位点或抗体的n末端而增加。n末端部分是可变区,并且c末端部分是恒定区;ch3和cl结构域实际上分别包括重链和轻链的羧基端。
[0039]
如上所述,可变区允许结合分子选择性地识别并特异性地结合抗原上的表位。也就是说,例如抗体的结合分子的vl结构域和vh结构域、或这些互补决定区(cdr)亚组组合形成抗原结合结构域。更具体地,抗原结合结构域可由各vh和vl链上的三个cdr确定。
[0040]
抗体抗原结合结构域中存在的六个“互补决定区”或“cdr”是氨基酸的非连续短序列,其特异性地定位,以随着抗体在水性环境中采用其三维构型而形成结合结构域。结合结构域中的其余氨基酸称为“构架”区,显示较小的分子间差异。构架区主要采用β
‑
片层构象,并且cdr形成连接β
‑
片层结构且在某些情况下形成β
‑
片层结构的部分的环。因此,构架区用于通过链间非共价相互作用形成为cdr提供正确方向位置的支架。由定位的cdr形成的结合结构域确定了与免疫反应性抗原上的表位互补的表面。这种互补表面促进了抗体与其互补表位的非共价结合。任何给定的重或轻链可变区中分别组成cdr和构架区域的氨基酸均可由本领域普通技术人员容易地鉴定,因为它们已以多种不同的方式被定义(参见,
″
免疫学热门蛋白质序列(sequences of proteins of immunological interest)
″
,kabat,e.等,美国卫生及公共服务部(u.s.department of health and human services),(1983);和chothia和lesk,j.mol.biol.,196:901
‑
917(1987),其通过引用其全文纳入本文)。
[0041]
如本文所用术语“免疫表型测定”是指用于研究细胞表达的蛋白质的技术。该技术可以在组织切片(新鲜的或固定的组织)、细胞悬液、血样等上进行。应用于研究和临床设置中的免疫表型技术和应用的集锦详细描述于《免疫表型:方法与方案》(immunophenotyping:methods and protocols),:mccoy,jr.,j.philip(编著)(2019),通过引用纳入本文。
[0042]
除非明确表述为相反的含义,否则在本领域内所使用和/或接受的某一术语有两种或多种定义的情况下,本文所用的术语定义应包括所有这些含义。具体示例是使用术语“互补决定区”(“cdr")描述在重链和轻链多肽的可变区内发现的非毗连抗原结合位点。这些具体的区域已被描述,例如,由kabat等,美国卫生及公共服务部,
″
免疫学热门蛋白质序列(sequences of proteins of immunological interest)
″
(1983),和由chothia等,j.mol.biol.196:901
‑
917(1987),其通过引用纳入本文。kabat和chothia定义包括氨基酸在彼此比较时的重叠或子集。不过,除非另有说明,述及抗体或其变体的cdr的定义(或本领域普通技术人员已知的其它定义)意图落在本文定义或所用的术语范围之内。合适的氨基酸残基包括上文引用的各参考文献中定义的cdr,如下表1所示以作对比。涵盖具体cdr的确切氨基酸编号将根据cdr的序列和大小而变化。鉴于抗体的可变区氨基酸序列,本领域技术人员能够常规地确定哪些氨基酸包含具体cdr。
[0043]
表1 cdr定义
*
[0044] kabatchothiavh cdr131
‑
3526
‑
32vh cdr250
‑
6552
‑
58vh cdr395
‑
10295
‑
102vl cdr124
‑
3426
‑
32vl cdr250
‑
5650
‑
52vl cdr389
‑
9791
‑
96
[0045]
*
表1中所有cdr定义的编号均按照kabat等所述的编号规则(见下文)。
[0046]
抗体可变结构域也可以例如使用imgt信息系统分析(www://imgt.cines.fr/)(/v
‑
quest)以鉴定包括cdr的可变区域段。(参见,例如,brochet等,nucl.acids res.,36:w503
‑
508,2008)。
[0047]
kabat等还定义了适用于任何抗体的可变区序列的编号系统。本领域普通技术人员能明确地将所述“kabat编号”系统应用于任何可变区序列,而不依赖序列本身外的任何实验数据。本文所用的“kabat编号”指由kabat等,美国卫生与公众服务部,“免疫学热门蛋白质序列(sequences of proteins of immunological interest)”(1983)中所述的编号系统。除非明确注明采用kabat编号系统,否则,本公开的全部氨基酸序列采用连贯的编号。
[0048]
结合分子,例如,抗体或其抗原结合片段、变体或衍生物,或其多聚片段、变体或衍生物,包括但不限于,多克隆、单克隆、人、人源化的或嵌合抗体、单链抗体、表位
‑
结合片段,例如,fab、fab
′
和f(ab
′
)2、fd、fv、单链fv(scfv)、单链抗体、二硫键连接的fv(sdfv)、包含vl或vh结构域的片段、通过fab表达文库产生的片段。scfv分子是本领域已知的,并且描述于例如美国专利号5,892,019。
[0049]
述及“特异性结合”一般表示结合分子,例如抗体或其片段、变体或衍生物通过其抗原结合结构域结合表位,并且该结合需要抗原结合结构域和表位之间的一些互补性。按照这一定义,当结合分子通过其抗原结合结构域与表位结合比其与随机、无关的表位结合更容易时,称该结合分子“特异性结合”该表位。本文中使用术语“特异性”定性分析某一抗体与某一表位结合的相对亲和性。例如,可认为结合分子“a”比结合分子“b”对给定表位具有更高特异性,或者可以说结合分子“a”以比其对相关表位“d”的特异性更高的特异性结合表位“c”。
[0050]
可以说本文公开的结合分子,例如,抗体或其片段、变体或衍生物,以小于或等于5x10
‑2秒
‑1、10
‑2秒
‑1、5x10
‑3秒
‑1、10
‑3秒
‑1、5x10
‑4秒
‑1、10
‑4秒
‑1、5x10
‑5秒
‑1、或10
‑5秒
‑15x10
‑6秒
‑1、10
‑6秒
‑1、5x10
‑7秒
‑1或10
‑7秒
‑1的解离速率(k(off))结合靶标抗原。
[0051]
可以说本文公开的结合分子,例如,抗体或抗原结合片段、变体或衍生物,以大于或等于103m
‑1秒
‑1、5x103m
‑1秒
‑1、104m
‑1秒
‑1、5x104m
‑1秒
‑1、105m
‑1秒
‑1、5x105m
‑1秒
‑1、106m
‑1秒
‑1、或5x106m
‑1秒
‑1或107m
‑1秒
‑1的结合速率(k(on))结合靶标抗原。
[0052]
如果结合分子,例如抗体或其片段、变体或衍生物,以一定程度上阻断参比抗体或抗原结合片段与表位的结合的程度优先结合该表位,则可以说,该结合分子,例如,抗体或其片段、变体或衍生物竞争性地抑制参比抗体或抗原结合片段与给定的表位的结合。可通过本领域已知的任意方法确定竞争性抑制,例如,竞争elisa试验。可以说,结合分子竞争性地抑制参比抗体或抗原结合片段与给定表位的至少90%、至少80%、至少70%、至少60%或至少50%的结合。
[0053]
本文所用的术语“亲和力”指单独表位与例如免疫球蛋白分子的一个或多个结合结构域结合的强度量度。参见例如,harlow等,《抗体:实验室手册》(antibodies:a laboratory manual)(冷泉港实验室出版社(cold spring harbor laboratory press),第2版,1988),第27
‑
28页。本文中所用的术语“亲合力(avidity)”指的是结合结构域的群和抗原之间的复合物的总体稳定性。参见,例如,harlow,第29
‑
34页。亲合力既与群体中单独结合结构域与特定表位的亲和力相关,也与免疫球蛋白分子和抗原的价态相关。例如,二价单克隆抗体和具有高度重复表位结构的抗原例如多聚体之间的相互作用是具有高亲合力的一个例子。二价单克隆抗体与以高密度存在于细胞表面上的受体之间的相互作用也将具有高亲和力。
[0054]
本文公开的结合分子,例如抗体或其抗原结合片段、变体或衍生物,也可就其交叉
反应性进行描述或说明。本文所用的术语“交叉反应性”指,结合分子(例如抗体或其片段、变体或衍生物)对某一种抗原具有特异性、与第二种抗原发生反应的能力;它是两种不同抗原性物质之间关联性的量度。因此,如果结合分子与诱导其形成的表位以外的其他表位结合,则具有交叉反应性。交叉反应性表位通常含有许多与诱导表位相同的互补结构特征,在某些情况下甚至比原始表位更匹配。
[0055]
结合分子,例如,抗体或其片段、变体或衍生物还可就它们与抗原的结合亲和性来描述或说明。例如,结合分子可以不超过5x10
‑2m、10
‑2m、5x10
‑3m、10
‑3m、5x10
‑4m、10
‑4m、5x10
‑5m、10
‑5m、5x10
‑6m、10
‑6m、5x10
‑7m、10
‑7m、5x10
‑8m、10
‑8m、5x10
‑9m、10
‑9m、5x10
‑
10
m、10
‑
10
m、5x10
‑
11
m、10
‑
11
m、5x10
‑
12
m、10
‑
12
m、5x10
‑
13
m、10
‑
13
m、5x10
‑
14
m、10
‑
14
m、5x10
‑
15
m或10
‑
15
m的解离常数或k
d
结合抗原。
[0056]
如本文所用术语“亚基”是指与其他相同或异源多肽链结合产生结合分子,例如,抗体或其抗原结合片段的单多肽链。
[0057]
本文中所用的术语“重链亚基”包括这样的氨基酸序列,其源自免疫球蛋白重链、结合分子,例如,包含重链亚基的抗体,可包括如下至少一项:vh结构域、ch1结构域、铰链(例如,上部、中部和/或下部铰链区)结构域、ch2结构域、ch3结构域、ch4
‑
tp结构域,或其变体或片段。
[0058]
本文所用的术语“轻链亚基”包括衍生自免疫球蛋白轻链的氨基酸序列。轻链亚基至少包括vl,还可包括cl(例如,cκ或cλ)结构域。
[0059]
结合分子,例如,抗体或其抗原结合片段、变体或衍生物可就它们识别或特异性结合的表位或抗原部分进行描述或说明。靶抗原与抗体的抗原结合结构域特异性相互作用的部分是“表位”或“抗原决定簇”。靶抗原可包含单个表位,或至少两个表位,并可包括任意数量的表位,这取决于抗原的大小、构象和类型。
[0060]
本文所用术语“癌症”和“癌”是指或描述哺乳动物中的生理病症,其中细胞群的特征在于不受调控的细胞生长。可以对癌症进行分类,例如,实体瘤或恶性病或血液癌或恶性病。这些类型都可能迁移到远端成为转移瘤。可以对实体瘤进行分类,例如,肉瘤、癌、黑色素瘤或其转移。
[0061]
术语“增殖性病症”和“增殖性紊乱”是指与异常细胞增殖相关的病症,如癌症。本文所用的“肿瘤”和“瘤
″
是指由良性(非癌性)或恶性(癌性)的过度细胞生长或增殖产生的任意组织块,包括癌前病灶。
[0062]
本文所用术语“转移”、“转移癌”、“转移性”或其他语法同义词是指从最初位置(例如,原发肿瘤)或身体的其他区域扩散或转移并在新位置处发展类似的癌病灶的癌细胞。“转移性”或“转移中”的细胞是丧失与相邻细胞的粘合接触并且通过血流或淋巴从疾病的原发部位迁移以侵入相邻的身体结构。该术语也指转移的过程,其包括但不限于癌细胞从原发肿瘤的癌细胞上脱落,癌细胞进入血管到循环中,它们存活并迁移到不同部位,从循环中粘附并外渗到新的部位,并且在不同的部位微定植,并且在不同的部位肿瘤生长和发展。
[0063]
这类实体瘤的实例可以包括,例如,鳞状细胞癌,腺癌,基底细胞癌,肾细胞癌,乳腺导管癌,软组织肉瘤,骨肉瘤,黑素瘤,小细胞肺癌,非小细胞肺癌(nsclc),肺腺癌,腹膜癌,肝细胞癌,胃肠癌,胃癌,胰腺癌,神经内分泌癌,胶质母细胞瘤,宫颈癌,卵巢癌,肝癌,膀胱癌,脑癌,肝细胞瘤,乳腺癌,结肠癌,结直肠癌,子宫内膜癌或子宫癌,食道癌,唾液腺
癌,肾癌,肝癌,前列腺癌,外阴癌,甲状腺癌,头颈癌,其任何转移,或其任意组合。
[0064]
血液癌症或恶性病的实例包括但不限于,白血病,淋巴瘤,骨髓瘤,急性髓性白血病,慢性髓性白血病,急性淋巴细胞白血病,慢性淋巴细胞白血病,毛细胞白血病,霍奇金淋巴瘤,非霍奇金淋巴瘤,多发性骨髓瘤,其任何转移,或其任意组合。
[0065]
在某些实施方式中,适于通过本文提供的方法治疗的癌症包括但不限于肉瘤,乳腺癌,卵巢癌,宫颈癌,头颈癌,nsclc,食道癌,胃癌,肾癌,肝癌,膀胱癌,结直肠癌和胰腺癌。
[0066]
术语“免疫调节剂”是指免疫疗法的活性试剂。免疫调节剂包括各种各样的重组、合成和天然的制备物的组合。免疫调节剂的示例包括但不限于白介素如il
‑
2、il
‑
7、il
‑
12;细胞因子如粒细胞集落刺激因子(g
‑
csf)、干扰素;各种趋化因子如cxcl13、ccl26、cxcl7;免疫检查点阻断的拮抗剂,如抗
‑
ctla
‑
4、抗
‑
pd
‑
1或抗
‑
pd
‑
l1(pd
‑
1的配体)、抗
‑
lag3、抗
‑
b7
‑
h3、合成胞嘧啶磷酸酯
‑
鸟嘌呤(cpg)寡脱氧核苷酸、葡聚糖;和调节性t细胞(treg)的调节剂如环磷酰胺。
[0067]
术语“治疗有效量”是指对对象(例如人)的疾病或病症而言有效“治疗”或在一些情况中“预防”的抗体、多肽、多核苷酸、小有机分子或其他药物的量。在癌症的情况中,治疗有效量的药物可减少癌细胞的数量;阻滞或停止癌细胞分裂、降低或阻滞肿瘤尺寸增加;抑制,例如,压制、阻滞、防止、停止、延迟或逆转癌细胞浸润至周边器官,包括,例如,癌症扩散到软组织和骨;抑制,例如,压制、阻滞、防止、收缩、停止、延迟或逆转肿瘤转移;抑制,例如,压制、阻滞、防止、停止、延迟或逆转肿瘤生长;一定程度上缓解与癌症相关的一种或多种症状,降低发病率和死亡率;改善生活质量;或这些效果的组合。就药物预防生长和/或杀伤现存的癌细胞的程度而言,其可以指代抑制细胞生长的和/或细胞毒性的。
[0068]
术语例如“处理”或“治疗”或“以治疗”或“缓解”或“以缓解
″
指的是1)治愈、减缓、减少已经诊断的病理病症或紊乱的症状,逆转和/或截停已经诊断的病理病症或紊乱的进展的治疗性措施和2)预防和/或减缓目标病理病症或紊乱的发展的预防或预防性措施。因此,需要治疗的那些(对象)包括已经患有疾病的那些(对象);易于患有疾病的那些(对象);和需要预防疾病的那些(对象)。如果患者表现出以下一种或多种情况,则根据本发明的方法成功地“治疗”了对象:癌细胞数量减少或完全不存在;减小肿瘤大小;或延缓或逆转肿瘤生长,抑制,例如抑制、预防、延缓、缩小、延迟或逆转转移,例如癌细胞浸润到外周器官,包括例如癌症扩散到软组织和骨中;抑制,例如,抑制、延缓、预防、缩小、逆转、延迟或不存在肿瘤转移;抑制,例如,抑制、延缓、防止、缩小、逆转、延迟或不存在肿瘤生长;缓解与特定癌症相关的一种或多种症状;降低发病率和死亡率;改善生活质量;或某种效果的组合。有益的或期望的临床结果包括但不限于症状的缓解、疾病程度的减轻、疾病的稳定(即,不恶化)状态、疾病进展的延迟或减缓、疾病状态的改善或缓解,以及缓解(无论是部分还是全部),无论是可检测的还是不可检测的。“治疗”也可以指与不接受治疗的期望存活相比延长生存期。因此,需要治疗的那些(对象)包括已经患有疾病或紊乱的那些(对象);易于患有疾病或紊乱的那些(对象);和需要预防疾病或紊乱的那些(对象)。
[0069]
述及“对象”或“个体”或“动物”或“患者”或“哺乳动物”,其指需要诊断、预防或治疗的任何对象,特别是哺乳动物对象。哺乳动物对象包括人、家养动物、家畜和动物园动物、竞技动物或宠物,如犬、猫、豚鼠、兔、大鼠、小鼠、马、猪、奶牛、熊等。
[0070]
如本文所用,短语例如“将受益于治疗的对象”和“需要治疗的动物”包括将从给予结合分子(例如抗体,包括一个或多个抗原结合结构域)中获益的对象(例如哺乳动物对象)。这种结合分子(例如抗体)可被用于例如诊断过程和/或用于治疗或预防疾病。
[0071]
靶多肽描述
‑
sema4d
[0072]
本文所用术语“脑信号蛋白
‑
4d”、“sema4d”和“sema4d多肽”可互换使用,如“sema4d”和“sema4d”。在某些实施方式中,sema4d是膜结合的。在其他实施方式中,sema4d是可溶的,例如ssema4d。在其他实施方式中,sema4d可包括完整大小的sema4d或其片段,或sema4d变体多肽,其中sema4d或sema4d变体多肽的片段保留完整大小的sema4d的一些或全部功能性质。
[0073]
完整大小的人sema4d蛋白质是由2条150kda的多肽链组成的同二聚体跨膜蛋白。sema4d属于脑信号蛋白家族细胞表面受体并且也称为cd100。人和小鼠sema4d/sema4d从其跨膜形式经蛋白水解切割以形成120
‑
kda可溶性形式,产生两种sema4d同种型(kumanogoh等,j.cell science 116(7):3464(2003))。脑信号蛋白由原始定义为轴突引导因子的可溶性和膜结合蛋白组成,所述轴突引导因子在建立神经元与其合适靶标的精确连接中起到重要作用。
[0074]
sema4d已知具有至少3个功能性受体,丛蛋白
‑
b1、丛蛋白
‑
b2和cd72。丛蛋白
‑
b1在非淋巴组织中表达并且已经显示为sema4d的高亲和性(1nm)受体(tamagnone等,cell 99:71
‑
80(1999))。丛蛋白
‑
b2对sema4d具有重等亲和力并且最近的报告指出plxnb2在角质细胞上表达并且激活sema4d阳性γδt细胞以有助于上皮细胞修复(witherden等immunity 2:314
‑
25(2012))。在淋巴组织中,cd72用作低亲和性(300nm)sema4d受体(kumanogoh等,immunity 13:621
‑
631(2000))。
[0075]
sema4d在包括脾脏、胸腺和淋巴结的淋巴器官中以及如脑、心脏和肾脏的非淋巴器官中以高水平表达。在淋巴器官中,sema4d在静息t细胞上大量表达,但是仅在静息b细胞和抗原呈递细胞(apc)如树突细胞(dc)上弱表达。细胞激活增加了sema4d的表面表达以及可溶性sema4d(ssema4d)的生成。
[0076]
抗
‑
sema4d抗体
[0077]
已经在本领域中描述了结合sema4d的抗体。参见例如,美国专利号7,919,594、8,496,938、8,816,058、9,605,055、9,676,840、9,243,068和9,828,43,国际专利申请wo 93/14125和herold等,int.immunol.7(1):1
‑
8(1995),其各自通过引用全文纳入本文。
[0078]
本发明一般涉及治疗和选择接受治疗的患有癌症的对象的方法,以抑制、延缓或减少患者(例如人癌症患者)体内肿瘤生长或转移,包括测定对象体内循环mdsc的水平,如果mdsc的水平低于预定阈值水平,则选择该对象接受治疗。循环mdsc水平通过从对象中获得或已经获得生物样品测定,例如血液样品或肿瘤活检,并进行或已经进行测定,例如对生物样品的免疫表型测定以确定生物样品中mdsc的水平。如果确定mdsc的水平低于预定阈值水平,则向患者给药有效量的包括特异性结合脑信号蛋白
‑
4d(sema4d)的分离抗体或其抗原结合片段、变体或衍生物的癌症免疫治疗方案,从而治疗对象。在某些实施方式中,抗体阻断sema4d与其受体中的一种或多种,例如丛蛋白
‑
b1和/或丛蛋白
‑
b2的相互作用。在某些实施方式中,癌细胞表达丛蛋白
‑
b1和/或丛蛋白
‑
b2。具有这些性质的抗
‑
sema4d抗体可用于本文提供的方法。可使用的抗体包括,但不限于mab vx15/2503,67,76,2282及其抗原结
合片段、变体或衍生物,其全部描述于例如美国专利号8,496,938中。可用于本文提供的方法的其他抗体包括us 2006/0233793 a1中所述的bd16抗体及其抗原结合片段、变体或衍生物;或mab 301、mab 1893、mab 657、mab 1807、mab 1656、mab 1808、mab 59、mab 2191、mab 2274、mab 2275、mab 2276、mab 2277、mab 2278、mab 2279、mab 2280、mab 2281、mab 2282、mab 2283、mab 2284和mab 2285中的任意种,及其任意片段、变体或衍生物,如美国专利号7,919,594所述。在某些实施方式中,用于本文提供的方法的抗
‑
sema4d抗体结合人、鼠、或人和鼠sema4d。还可使用与任意前述抗体结合相同表位的抗体和/或竞争性抑制任意前述抗体的结合或活性的抗体。
[0079]
在某些方面,抗
‑
sema4d抗体或其抗原结合片段包括以下的六个cdr:鼠抗体mab 67和人源化抗体vx15/2503,其作为人igg4抗体在本领域中称为派比奈单抗(pepinemab)。这些抗体的可变重链(vh)包含分别含有seq id no:2、3和4的vh cdr 1
‑
3,而可变轻链(vl)包含分别含有seq id no:6、7和8的vl cdr 1
‑
3。在某些方面中,抗体包含分别含有氨基酸序列seq id no:1和seq id no:5的人源化vh和vl区。在某些方面中,抗体包含分别含有氨基酸序列seq id no:9和seq id no:10的鼠vh和vl区。
[0080]
使用治疗性抗
‑
sema4d抗体作为单药或与至少一种免疫调节疗法组合的治疗方法
[0081]
本发明的方法涉及使用sema4d拮抗剂,例如抗
‑
sema4d抗体或其抗原结合片段、变体和衍生物,作为单药或与至少一种其他免疫调节疗法组合,以抑制、延迟或减少需要这种抑制、延缓或减少的对象(例如癌症患者)体内肿瘤生长或转移。在本文提供的某些方面,将要接受治疗的对象包括那些治疗前mdsc水平降低的,例如,mdsc水平低于某个阈值水平,例如,在外周血或在肿瘤微环境中。
[0082]
在一个方面,本发明提供了用于选择患癌对象的方法,用于治疗、抑制、延缓或减少患者体内恶性肿瘤细胞生长,包括:测定对象的循环髓源性抑制细胞(mdsc)水平,如果mdsc的水平低于预定阈值水平,向对象给予有效量的包括sema4d拮抗剂的癌症免疫治疗方案,例如特异性结合sema4d的分离抗体或其抗原结合片段,从而治疗对象。
[0083]
mdsc可以通过任何已知方法测定,其水平可以表达为,例如,在外周血或肿瘤微环境中细胞的绝对数量,或外周血细胞的百分比,或外周血细胞亚群的百分比。如本文他处所述,细胞通常通过流式细胞仪测定。述及“预定阈值水平”是指对象中测定的mdsc细胞的水平低于限定的水平,例如,低于在相当的癌症患者中观察到的平均水平或等同于或低于在正常健康捐献者中测定的通常水平。在某些方面“预定阈值水平”可以是mdsc特定的绝对值(例如在外周血或肿瘤微环境中),或细胞群的百分比(例如在总外周血单核细胞中mdsc的百分比)。在某些方面,mdsc的预定阈值水平包括,治疗前低于对象总外周血单核细胞的50%、40%、30%、20%或10%。
[0084]
在某些方面,mdsc是单核mdsc(m
‑
mdsc)。在某些方面,m
‑
mdsc含有细胞表面标志物的表型。例如,某些m
‑
mdsc群表达cd14、cd11b和cd33,但不表达或仅表达低水平的hla
‑
dr标志物。表达某些细胞表面标志物(例如cd3、cd19和cd56)的细胞可被排除在mdsc群之外。在某些方面,m
‑
mdsc包括cd14
、hla
‑
dr
‑
/低
、cd11b
、cd33
、ln
‑
表型,其中ln是界定非mdsc的标志物混合。典型的混合包括但不限于cd3、cd19和/或cd56的任意组合。在某些方面,m
‑
mdsc表达cd14和高水平的hla
‑
dr,但不表达cd16(参见krieg等,nature med.24:144
‑
154(2018))。在某些方面,mdsc是表达cd15 cd66b和/或cd33,但不表达cd14的多形核mdsc
(pmn
‑
mdsc)。其他mdsc表型对本领域普通技术人员显而易见。
[0085]
在某些方面,作为癌症免疫治疗方案的一部分给药抗
‑
sema4d抗体或其片段,抑制sema4d与其受体例如丛蛋白
‑
b1、丛蛋白
‑
b2、cd72或其任意组合的相互作用。在某些方面,作为癌症免疫治疗方案的一部分给药抗
‑
sema4d抗体或其抗原结合片段,抑制sema4d介导的信号转导。合适的抗
‑
sema4d抗体公开于本文他处,包括但不限于派比奈单抗。
[0086]
在某些方面,癌症免疫治疗方案是组合治疗,且进一步包括给药其他癌症免疫治疗剂,其可以是例如至少一种免疫调节剂。合适的免疫治疗和免疫调节剂如本文他处所述。在某些方面,其他癌症免疫治疗剂是免疫检查点阻断,例如特异性结合ctla4、pd
‑
1、pd
‑
l1、lag3、tim3、b7
‑
h3或其任何组合的抗体或其抗原结合片段。在某些方面,检查点阻断抗体是抗
‑
pd
‑
l1抗体阿维鲁单抗。
[0087]
所提供的方法可用于选择和治疗患有任何癌症的对象,所述癌症例如,实体瘤,血液恶性肿瘤,其任何转移,或其任意组合。在某些方面,实体瘤是肉瘤,癌,黑色素瘤,其任何转移,或其任意组合。在某些方面,实体瘤可以是,鳞状细胞癌,腺癌,基底细胞癌,肾细胞癌,乳腺导管癌,软组织肉瘤,骨肉瘤,黑素瘤,小细胞肺癌,非小细胞肺癌,肺腺癌,腹膜癌,肝细胞癌,胃肠癌,胃癌,胰腺癌,神经内分泌癌,胶质母细胞瘤,宫颈癌,卵巢癌,肝癌,膀胱癌,脑癌,肝细胞瘤,乳腺癌,结肠癌,结直肠癌,子宫内膜癌或子宫癌,食道癌,唾液腺癌,肾癌,肝癌,前列腺癌,外阴癌,甲状腺癌,头颈癌,其任何转移,或其任意组合。在某些方面中,所述癌症是非小细胞肺癌。在某些方面中,血液恶性肿瘤是白血病,淋巴瘤,骨髓瘤,急性髓性白血病,慢性髓性白血病,急性淋巴细胞白血病,慢性淋巴细胞白血病,毛细胞白血病,霍奇金淋巴瘤,非霍奇金淋巴瘤,多发性骨髓瘤,其任何转移,或其任意组合。
[0088]
本发明所提供的方法可以进一步包括给予其他癌症疗法,包括但不限于手术,化疗,放疗,给予癌症疫苗,给予免疫刺激剂,过继性t细胞疗法,给予调节性t细胞(treg)调节剂及其任意组合。
[0089]
在某些方面,癌细胞或癌细胞附近的细胞表达sema4d受体,在某些实施方式中,受体是丛蛋白
‑
b1。虽然以下说明涉及给予抗
‑
sema4d抗体,本文所述的方法也同样适用于任何sema4d拮抗剂,即抑制sema4d和其受体之一的相互作用的药剂,包括例如,保留本发明的抗体的所需性质的抗
‑
sema4d抗体的抗原结合片段、变体和衍生物,所述性质例如,能够特异性结合sema4d(例如,人、小鼠或人和小鼠sema4d)、具有sema4d中和/拮抗活性、和/或阻断sema4d与其任意一种或多种受体的相互作用。本文所述方法也适用于保留sema4d拮抗剂所需性质的其他生物制剂或小分子药物,所述特性例如能够特异性结合sema4d(例如人、小鼠或人和小鼠sema4d)、具有sema4d中和/拮抗活性、和/或阻断sema4d与其受体的相互作用。
[0090]
在一个实施方式中,sema4d拮抗剂(例如抗
‑
sema4d抗体或其片段、变体或衍生物)可被用作单药以抑制、延缓或减少需要这种抑制、减缓或减少的对象(例如癌症患者)中的肿瘤生长,其中在某些方面对象被定义为在治疗前具有低于某阈值水平的mdsc。在其他方面,sema4d拮抗剂(例如抗
‑
sema4d抗体或其片段、变体或衍生物)可与其他癌症疗法组合给予,包括癌症免疫疗法,例如但不限于癌症疫苗、免疫刺激剂、过继t细胞或抗体疗法和免疫检查点抑制剂。
[0091]
癌症疫苗。癌症疫苗激活身体的免疫系统和对异常细胞(例如癌)的天然抵抗,从
而根除或控制疾病。癌症疫苗通常由免疫原性制剂中的肿瘤抗原组成,其激活肿瘤抗原特异性辅助细胞和/或ctl和b细胞。疫苗可以在各种制剂中,包括但不限于树突细胞,尤其是用肿瘤细胞或肿瘤抗原脉冲的自体树突细胞,用免疫刺激剂(例如gm
‑
csf)转染的异源肿瘤细胞,重组病毒,或蛋白质或肽,通常与强力免疫佐剂例如cpg一起给药。
[0092]
免疫刺激剂。免疫刺激剂作用以增强或增加对肿瘤的免疫反应,其在许多癌症患者中通过各种机制被抑制。免疫调节疗法可靶向淋巴细胞、巨噬细胞、树突细胞、自然杀伤细胞(nk细胞)、或这些细胞的亚群,例如细胞毒性t淋巴细胞(ctl)或自然杀伤t(nkt)细胞。由于免疫级联反应相互作用,在一群免疫细胞上的作用通常会通过传播给其他细胞被放大,例如增强抗原呈递细胞活性促进t和b淋巴细胞反应。免疫刺激剂的实例包括但不限于her2、细胞因子例如g
‑
csf、gm
‑
csf和il
‑
2、来自细菌的细胞膜组分、与cd1d结合以激活自然杀伤t(nkt)细胞的糖脂、cpg寡核苷酸。
[0093]
巨噬细胞是免疫系统的髓噬细胞(myelophagocytic cell),是先天防御机制的基本组成部分,可以通过诱导t细胞募集和激活来促进特异性免疫。尽管如此,它们在肿瘤微环境中的存在与增强的肿瘤进展有关,并显示出促进癌细胞生长和扩散、血管生成和免疫抑制。巨噬细胞表型设置的关键因素是巨噬细胞所暴露的微环境信号,这些信号在包括m1极(肿瘤抑制巨噬细胞)和m2极(肿瘤促进巨噬细胞)的功能谱内选择性地调整它们的功能。sica等,seminars in cancer biol.18:349
‑
355(2008)。癌症期间巨噬细胞数量增加通常与不良预后有关(qualls和murray,curr.topics in develop.biol.94:309
‑
328(2011))。在实体瘤常见的多种独特基质细胞类型中,肿瘤相关巨噬细胞(tam)对促进肿瘤进展具有重要意义。靶向调节tam极化的分子通路为抗癌治疗提供了广阔的前景。ruffell等,trends in immunol.33:119
‑
126(2012).
[0094]
过继细胞转移。过继细胞转移可以利用基于t细胞的细胞毒性反应来攻击癌细胞。对患者的癌症具有天然的或基因工程改造的反应性的自体t细胞在体外产生和扩增,然后转移回患者体内。一项研究表明,体外扩增自体肿瘤浸润淋巴细胞的过继转移是转移性黑色素瘤的患者的有效治疗方法。(rosenberg sa,restifo np,yang jc,morgan ra,dudley me(2008年4月).nat.rev.cancer 8(4):299
‑
308)。这可以通过获取在切除的患者肿瘤中发现的t细胞实现。这些t细胞被称为肿瘤浸润性淋巴细胞(til),并且由于它们对肿瘤抗原的特异性,被推定为已转运到肿瘤中。可以使用高浓度il
‑
2、抗
‑
cd3和同种异体反应性饲养细胞在体外诱导此类t细胞扩增。然后将这些t细胞同外源性il
‑
2给药一起转移回患者体内,以进一步增强其抗癌活性。在其他研究中,自体t细胞已经用嵌合抗原受体转导(“car
‑
t细胞”),使它们对靶向肿瘤抗原具有反应性(参见,例如,liddy等,nature med.18:980
‑
7,(2012);grupp等,new england j.med.368:1509
‑
18,(2013);petitt,等,mol ther.26:342
‑
353(2018))。
[0095]
其他过继细胞转移疗法采用离体的暴露于天然或修饰的肿瘤抗原自体树突细胞,其被回输到患者体内。普列威(provenge)是fda批准的疗法,其中自体细胞与前列腺酸性磷酸酶和gm
‑
csf的融合蛋白一起孵育,以治疗前列腺肿瘤患者。gm
‑
csf被认为促进了抗原呈递树突细胞的分化和活性(small等,j.clin.oncol.18:3894
‑
903(2000);us专利7,414,108))。
[0096]
免疫检查点抑制剂。免疫检查点抑制剂疗法通过消除正在进行的免疫反应的负反
馈控制来增强t细胞免疫。这些类型的疗法针对免疫系统中的抑制通路以减少旁系组织损伤,其对于调节外周组织中(抗
‑
ctla4)或表达pd
‑
l1的肿瘤组织中(抗
‑
pd
‑
1或抗
‑
pd
‑
l1)的生理免疫反应的持续和波动至关重要。肿瘤可进化为利用某些免疫检查点通路作为针对肿瘤抗原特异的t细胞的免疫抵抗的主要机制。因为许多免疫检查点被配体
‑
受体相互作用引发,所以这些检查点可以被受体或配体的抗体阻断,或可以通过配体或受体的可溶性重组形式调节。免疫检查点的中和允许肿瘤特异性t细胞继续作用于其他免疫抑制的肿瘤微环境。免疫检查点阻断疗法的实例为靶向细胞毒性t淋巴细胞相关抗原4(ctla
‑
4)、pd
‑
1、它的配体pd
‑
l1、lag3和b7
‑
h3的那些。
[0097]
环磷酰胺。环磷酰胺,常规使用的化疗药剂,可以增强免疫反应。相对于效应t细胞,环磷酰胺对调节性t细胞的功能有不同的抑制作用(treg)。treg在调节抗癌免疫反应中十分重要。肿瘤浸润treg以前与不良预后相关。然而目前还没有获得特异靶向treg的药剂,但环磷酰胺已成为临床上可行的药物,相对于其他t细胞,它可以优先抑制treg,因此可以更有效地诱导抗肿瘤免疫反应。
[0098]
其他免疫调节疗法。在另一个实施方式中,sema4d拮抗剂,例如sema4d抗体或其抗原结合片段、变体或衍生物,可以与低剂量化疗或放疗组合治疗。虽然标准化疗通常是免疫抑制的,但是低剂量化疗药例如环磷酰胺、多柔比星和紫杉醇已经证明增强了对癌症疫苗疗法的反应(machiels等,cancerres.61:3689
‑
3697(2001))。在一些情况下,化疗可差异地失活调节性t细胞(treg)和髓源性抑制细胞(mdsc),其负调节肿瘤环境中的免疫反应。放射治疗已普遍用于利用电离辐射的直接杀肿瘤作用。实际上,与化疗类似,高剂量放疗可以是免疫抑制性的。然而,大量的观察表明,在适当的剂量分级和测序条件下,放射治疗可以增强肿瘤特异性免疫反应和免疫调节剂的作用。促成这种作用的几种机制之一是树突细胞和其他抗原呈递细胞交叉呈递由辐射诱导的肿瘤细胞死亡释放的肿瘤抗原(higgins等,cancer biol.ther.8:1440
‑
1449(2009))。实际上,放疗可以原位诱导针对肿瘤的疫苗接种(ma等,seminar immunol.22:113
‑
124(2010)),且这可以通过与sema4d拮抗剂(例如,sema4d抗体或其抗原结合片段、变体或衍生物)组合治疗而放大。
[0099]
在一个实施方式中,免疫调节疗法可以是免疫调节剂,包括但不限于白介素如il
‑
2、il
‑
7、il
‑
12;细胞因子如粒细胞
‑
巨噬细胞集落刺激因子(gm
‑
csf)、干扰素;各种趋化因子如cxcl13、ccl26、cxcl7;免疫检查点阻断的拮抗剂,如抗
‑
ctla
‑
4、抗
‑
pd
‑
1、抗
‑
pd
‑
l1、抗
‑
lag3和抗
‑
b7
‑
h3;合成胞嘧啶磷酸酯
‑
鸟嘌呤(cpg)、寡脱氧核苷酸、葡聚糖、调节性t细胞(treg)的调节剂如环磷酰胺,或其他免疫调节剂。在一个实施方式中,免疫调节剂是4
‑
1bb(cd137)的激动剂抗体。如最近所报道的,这类4
‑
1bb的激动剂抗体可产生一类新型klrg1 t细胞,其对肿瘤具有高度细胞毒性(curran等,j.exp.med.210:743
‑
755(2013))。在所有情况下,在sema4d拮抗剂(例如抗
‑
sema4d抗体或其抗原识别片段、变体或衍生物)治疗之前、期间或之后给予其他免疫调节治疗。在组合疗法包括将抗
‑
sema4d结合分子(例如抗体或其抗原结合片段、变体或衍生物)的给予与另一种免疫调节剂的给予相组合的情况中,本发明的方法涵盖共同给予、使用单独制剂或单药制剂、同时或以任意顺序连续给予。
[0100]
在一个实施方式中,免疫调节疗法可以是癌症治疗剂,包括但不限于手术或外科手术(例如脾切除术、肝切除术、淋巴结切除术、白细胞移植术、骨髓移植等);放射治疗;化疗,可选地与自体骨髓移植或其他癌症治疗组合;其中在sema4d拮抗剂(例如抗
‑
sema4d抗
体或其抗原结合片段、变体或衍生物)治疗之前、期间或之后给予其他癌症疗法。在组合疗法包括将抗
‑
sema4d抗体或其抗原结合片段、变体或衍生物的给予与另一种治疗剂的给予相组合的情况中,本发明的方法涵盖共同给予、使用单独制剂或单药制剂,同时或以任意顺序连续给予。
[0101]
在另一个实施方式中,本发明内容涉及sema4d拮抗剂(例如抗sema4d抗体或其抗原结合片段、变体或衍生物)作为单药或与至少一种其他免疫调节疗法组合用于治疗癌症患者的用途,所述患者与其他患有实体瘤的患者(例如在脑、肺、卵巢、乳腺、结肠和其他组织中发现的实体瘤或其他血液癌症患者)相比,治疗前循环中的mdsc水平降低,例如低于预定阈值水平。如本文所用,术语“降低”是指与其他癌症患者相比,癌症患者的循环中mdsc的平均数量的低于90%、低于80%、低于70%、低于60%、低于50%、低于40%、低于30%或低于20%。可以测定mdsc的数量,例如外周血中的绝对值,例如测定每μl中的细胞,或占外周血中总细胞群的百分比,例如单核细胞的百分比或多形核细胞的百分比(即为mdsc)。还可以测定患者肿瘤微环境中mdsc的数目(作为总细胞或细胞群的百分比)。mdsc可以是m
‑
mdsc,例如具有cd14
、hla
‑
dr
‑
/低
、cd11b
、cd33
、ln
‑
表型的mdsc,其中ln是界定非
‑
mdsc的标志物混合,例如,cd3、cd19和/或cd56的一种或多种。
[0102]
在另一个实施方式中,本发明涉及sema4d拮抗剂(例如抗
‑
sema4d抗体或其抗原结合片段、变体或衍生物)作为单药或与至少一种其他免疫调节疗法组合的用途,用于治疗在治疗前循环中mdsc的水平降至正常个体范围内或低于正常个体范围的癌症患者。如本文所用,术语“正常”是指在健康、非癌症患者中发现的mdsc或任何特定mdsc群体的水平。如本文所用,术语“之内”是指mdsc水平的10%差异。当然,本领域技术人员将理解mdsc的水平可根据各种因素变化,例如,癌症类型、癌症分期等,因此,高于以上提供的水平的水平可以也构成某些类型或分期的癌症的降低水平。可以测定mdsc的数量,例如外周血中的绝对值,例如测定每μl细胞中的,或占外周血中总细胞群的百分比,例如单核细胞的百分比或多形核细胞的百分比(即为mdsc)。还可以测定患者肿瘤微环境中mdsc的数目(作为总细胞或作为细胞群的百分比)。mdsc可以是m
‑
mdsc,例如具有cd14
、hla
‑
dr
‑
/低
、cd11b
、cd33
、ln
‑
表型的mdsc,其中ln是界定非
‑
mdsc的标志物混合,例如,cd3、cd19和/或cd56的一种或多种。在一些实施方式中,mdsc细胞绝对计数或相对计数可以使用免疫表型试验测定,例如基于标准流式细胞术的免疫表型试验。
[0103]
本文所述方法可用于任何sema4d拮抗剂,包括例如抗
‑
丛蛋白
‑
b1抗体或其抗原结合片段,其中抗
‑
丛蛋白
‑
b1抗体可被用于通过阻断sema4d与丛蛋白
‑
b1的结合和/或通过防止丛蛋白
‑
b1被sema4d激活抑制sema4d和丛蛋白
‑
b1的相互作用。本文所述方法也可用于小分子sema4d拮抗剂或其他抑制sema4d或丛蛋白
‑
b1活性的生物制剂的使用。在一些实施方式中,除抗
‑
sema4d结合分子以外小分子药物或生物制剂可用于通过阻断sema4d与丛蛋白
‑
b1的结合和/或通过防止丛蛋白b1被sema4d激活抑制sema4d和丛蛋白b1的相互作用。
[0104]
在一个实施方式中,治疗包括以单药或与至少一种其他免疫调节疗法组合施用或给予本文所述抗
‑
sema4d抗体或其抗原结合片段,或以单药或与至少一种其他免疫调节治疗组合向来自患者的分离的组织或细胞系施用或给予抗
‑
sema4d抗体,其中患者具有癌细胞的转移或具有发展癌细胞的转移的风险。在某些方面患者在治疗之前具有低于预定阈值水平的降低水平的mdsc。在另一个实施方式中,治疗还旨在包括向患者施用或给予包含抗
‑
sema4d抗体或其抗原结合片段的药物组合物,与至少一种其他免疫调节治疗组合,或将包含抗
‑
sema4d抗体和至少一种其他免疫调节治疗的药物组合物施用或给予来自患者的分离的组织或细胞系,其中所述患者具有癌细胞的转移或具有发展癌细胞的转移的风险。
[0105]
如本文所述的抗
‑
sema4d抗体或其结合片段,作为单药或与至少一种其他免疫调节疗法组合有助于多种恶性肿瘤和非恶性肿瘤的治疗。在某些方面,患者在治疗之前具有低于预定阈值水平的降低水平的mdsc。述及“抗肿瘤活性”意指sema4d产生或累积速率的降低,其与肿瘤直接相关或与肿瘤环境的基质细胞间接相关,并因此使存在的肿瘤或在治疗过程中产生的肿瘤的增长率下降,和/或破坏存在的瘤性(肿瘤)细胞或新形成的瘤性细胞,并因此在治疗期间降低肿瘤的总尺寸和/或转移灶的数量。例如,采用至少一种抗
‑
sema4d抗体作为单药或与至少一种其他免疫调节疗法组合引起生理反应,例如转移减少,其就与人体中表达sema4d的细胞相关的疾病状态的治疗而言是有益的。
[0106]
在一个实施方式中,本发明涉及抗
‑
sema4d抗体或其抗原结合片段、变体或衍生物,作为单药或与至少一种其他免疫调节疗法组合作为药物,在治疗或预防癌症中的用途,或用于癌前病症或病灶,抑制、减少、预防、延缓或最小化肿瘤细胞的生长和转移。在某些方面,患者在治疗之前具有低于预定阈值水平的降低水平的mdsc。
[0107]
根据本发明的方法,可采用至少一种抗
‑
sema4d结合分子,例如抗体或其抗原结合片段、变体或衍生物,作为单药或与至少一种其他免疫调节疗法组合来促进关于人恶性肿瘤细胞的积极治疗反应。述及“积极治疗反应”,就癌症治疗而言,意指与这些结合分子(抗体或其片段)抗肿瘤活性相关的疾病改善和/或与疾病相关的症状改善。具体地,本文提供的方法涉及抑制、预防、减少、延迟或减弱患者中肿瘤的生长和/或原发肿瘤的转移灶进展。即可以观察到预防远端肿瘤的长出。因此,例如,疾病的改善可表征为完全缓解。述及“完全缓解”意指没有临床可检测的转移,并且任何先前异常的放射学研究正常化,例如在原发肿瘤部位或骨髓中存在肿瘤转移。或者,疾病的改善可归类为部分缓解。述及“部分缓解”意指至少约所有可测量的转移灶(即在远离原发肿瘤的部位存在于对象中的肿瘤细胞的数量)至少减少约50%。或者,疾病的改善可归类为无复发生存期或“无进展生存期”。述及“无复发生存期”意指直到肿瘤在任何部位复发的时间。“无进展生存期”是指直到某部位的肿瘤进一步生长至可被检测到的时间。
[0108]
转移的抑制、延迟或减少可以使用筛查技术来评估,例如成像,例如荧光抗体成像、骨扫描成像和肿瘤活检取样,包括骨髓抽吸(bma)或免疫组织化学。除了这些积极治疗反应之外,接受抗
‑
sema4d结合分子(例如抗体或其抗原结合片段、变体或衍生物)治疗的对象可以经历改善与疾病相关的症状的有益效果。
[0109]
可以使用筛查技术评估临床反应,例如磁共振成像(mri)扫描、x射线成像、计算机断层扫描(ct)扫描、流式细胞术或荧光活化细胞分选仪(facs)分析、组织学、总体病理学和血液学化学,包括但不限于可通过elisa、ria、色谱等检测的变化。
[0110]
为了在某些实施方式中应用本发明的方法和系统,向患有实体瘤或血液学癌症的对象单独给予或与有效量的至少一种其他免疫调节疗法组合给予包含有效量的sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)的疗法之前或之后获取来自患者的样品。可以根据本文别处提供的方法筛选样品的某些生物标志物,例如mdsc水平。在一些情况下,可以在治疗开始后或治疗停止后从患者获取连续样品,并且同样可以针对某
些生物标志物例如mdsc水平筛选此类样品。例如,样品可以由医疗服务提供者(例如,医生)或医疗服务益处提供者请求,由相同或不同的医疗服务提供者(例如,护士、医院)或临床实验室获得和/或处理,处理后,结果可以转递给另一个医疗服务提供者、医疗服务益处提供者或患者。类似地,一个或多个评分的测量/确定、评分之间的比较、评分的评估和治疗决定可以由一个或多个医疗服务提供者、医疗服务益处提供者和/或临床实验室执行。
[0111]
本文所用术语“医疗服务提供者”是指直接接触或向活的对象(例如人类患者)给予治疗的个人或机构。医疗服务提供者的非限制性示例包括医生、护士、技师、治疗师、药师、顾问、替代医学从业者、医学设备、医生办公室、医院、急救室、诊所、急救中心、替代医学诊所/设备、和提供关于患者健康状态的全部或任意部分的一般和/或特殊治疗、评价、维持、疗法、医药和/或建议的任意其它实体,包括但不限于一般医学、特殊医学、手术、和/或任何其它类型治疗、评价、维持、疗法、医药和/或建议。
[0112]
在一些方面,医疗服务提供者可以给予治疗,或指导另一个医疗服务提供者给予治疗,其包括向患有或怀疑患有癌症的对象单独给予或与有效量的至少一种其他免疫调节疗法组合给予包含有效量的sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)的疗法。医疗服务提供者可执行或指示其他医疗服务提供者或患者进行以下动作:获取样品、处理样品、提交样品、接收样品、转移样品、分析或测量样品、定量样品、提供样品分析/测量/定量样品后获得的结果、接收分析/测量/定量样品后获得的结果、对分析/测量/定量一个或多个样品后获得的结果进行比较/评分、提供一个或多个样品的比较/评分样品、从一个或多个样品获得比较/评分、向对象给予治疗(例如有效量的sema4d拮抗剂,例如单独的分离抗体或与有效量的至少一种其他免疫调节疗法组合),其中对象患有或怀疑患有癌症,开始给予治疗、减轻给予治疗、继续给予治疗、暂时中断给予治疗、增加给予的治疗剂的量、减少给予的治疗剂的量、继续给予一定量的治疗剂、增加治疗剂的给药频率、降低治疗剂的给药频率、维持治疗剂的相同给药频率、用至少另一种治疗或治疗剂替代治疗或治疗剂、联合治疗或治疗剂与至少另一种治疗或附加治疗剂。在一些方面中,医疗服务益处提供者可授权或拒绝例如,收集样品、处理样品、提交样品、接收样品、转移样品、分析或测量样品、定量样品、提供在分析/测量/定量样品之后得到的结果、转移在分析/测量/定量样品之后得到的结果、比较/评分在分析/测量/定量一个或多个样品之后得到的结果、转移来自一个或多个样品的比较/得分、给予治疗或治疗剂、开始给予治疗或治疗剂、停止给予治疗或治疗剂、持续给予治疗或治疗剂、暂时中断给予治疗或治疗剂、增加给予的治疗剂的量、减少给予的治疗剂的量、继续给予一定量的治疗剂、增加给予治疗剂的频率、降低给予治疗剂的频率、维持治疗剂的相同给药频率、由至少一种其它治疗或治疗剂取代治疗或治疗剂、或将治疗或治疗剂与至少一种其它治疗或治疗剂组合。
[0113]
另外,医疗益处提供者可以,例如授权或拒绝治疗处方,授权或拒绝治疗覆盖范围,授权或拒绝治疗成本的退还,确定或拒绝治疗合格性等。
[0114]
在一些方面中,临床实验室可以,例如,收集或获取样品、处理样品、提交样品、接收样品、转移样品、分析或测量样品、定量样品、提供在分析/测量/定量样品之后得到的结果、接收在分析/测量/定量样品之后得到的结果、比较/评分在分析/测量/定量一个或多个样品之后得到的结果、提供来自一个或多个样品的比较/得分、获取来自一个或多个样品的比较/得分或其它相关活动。
[0115]
诊断和治疗的方法
[0116]
在某些实施方式中,本发明提供治疗对象(例如癌症患者,其中对象具有低于预定阈值水平的mdsc水平)的方法,包括如果对象的mdsc水平低于预定阈值水平或等于或低于一个或多个对照样品中的mdsc水平(对照样品可以包括但不限于来自其他癌症患者或健康的非癌症患者的样品),则给予sema4d拮抗剂,例如抗
‑
sema4d抗体或其抗原结合片段、变体或衍生物,其单独给予或与本文别处提供的至少一种其他免疫调节剂组合。mdsc水平,无论是绝对水平还是占其他细胞群的百分比,可由医疗服务提供者或临床实验室测量,其中样品,例如血液样品或肿瘤活检,由医疗服务提供者或由临床实验室从患者获取。一方面,患者的mdsc水平可以在免疫表型试验中测量,例如基于细胞计数的免疫表型试验。
[0117]
本发明还提供了方法、试验和试剂盒以促进医疗服务提供者、医疗服务益处提供者或临床实验室确定对象(例如癌症患者)是否将受益于单独给予或与有效量的至少一种其他免疫调节疗法组合给予有效量的sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)的治疗,其中所述对象患有或怀疑患有癌症。本文中提供的所述方法、试验和试剂盒也将促进医疗服务提供者、医疗服务益处提供者或临床实验室确定对象(例如癌症患者)是否将受益于单独给予或与有效量的至少一种其他免疫调节疗法组合给予有效量的sema4d拮抗剂(例如分离抗体或其特异性结合sema4d的抗原结合片段)的治疗。
[0118]
本发明提供了一种治疗对象(例如癌症患者)的方法,其包括如果在治疗前取自患者的样品中的mdsc水平低于预定阈值水平,或者低于或等于一个或多个对照样品中的mdsc水平,则单独给予或与有效量的至少一种其他免疫调节疗法组合给予有效量的sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)。在某些方面,样品从患者中获取并提交用于测量样品中的mdsc水平,例如,提交给临床实验室。
[0119]
还提供了一种治疗对象(例如癌症患者)的方法,包括(a)提交从对象中获取的样品用于测量样品中的mdsc水平;和(b)如果在治疗前患者的mdsc水平低于预定阈值水平,或者低于或等于一个或多个对照样品中的mdsc水平,则单独给予或与有效量的至少一种其他免疫调节疗法组合给予有效量的sema4d拮抗剂(例如特异性结合sema4d的分离抗体其抗原结合片段)。
[0120]
本发明还提供了治疗对象(例如癌症患者)的方法,包括(a)测量从对象(例如癌症患者)获得的样品中的mdsc水平,其中,例如,在基于细胞计数的免疫表型试验中测量对象的样品中的mdsc水平;(b)确定样品中mdsc的水平是否低于预定阈值水平,或低于或等于一个或多个对照样品中的mdsc水平;和(c)如果对象的mdsc水平低于预定阈值水平,或低于或等于一个或多个对照样品中的mdsc水平,则建议、指导或授权医疗服务提供者向对象单独给予或与有效量的至少一种其他免疫调节疗法组合给予有效量的sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)。
[0121]
在某些方面,对象的mdsc水平可以在基于细胞计数的免疫表型试验中测量。在某些方面,可以由治疗患者的医疗服务专业人员对从对象获得的样品进行测定,例如,使用如本文所述的试验,配制为“护理点”诊断试剂盒。在某些方面,样品可以从对象获得并且可以提交给例如临床实验室,用于根据医疗服务专业人员的说明测量样品中mdsc的水平,包括但不限于使用如本文所述的基于细胞计数的免疫表型试验。在某些方面,进行测定的临床实验室可以为医疗服务提供者或医疗服务益处提供者提供建议,如果对象的mdsc水平低于
预定阈值水平,或者低于或等于一个或多个对照样品中的mdsc水平,对象是否可以受益于使用有效量的与脑信号蛋白
‑
4d(sema4d)特异性结合的分离结合分子和有效量的至少一种其他免疫调节疗法的治疗。
[0122]
在某些方面,如本文提供的免疫测定的结果可以提交给医疗服务益处提供者,以确定患者的保险是否将涵盖用有效量的sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)单独治疗或与有效量的至少一种其他免疫调节疗法组合治疗。
[0123]
药物组合物和给药方法
[0124]
本领域技术人员熟知或不难确定制备和向有需要的对象给予sema4d拮抗剂(例如抗
‑
sema4d抗体或其抗原结合片段、变体或衍生物)的方法,其作为单药或与至少一种其他免疫调节疗法组合。sema4d拮抗剂,例如与sema4d特异性结合的分离抗体或其抗原结合片段,其单独给药或与有效量的至少一种其他免疫调节疗法的给药的途径可以是例如口服、肠胃外给药,对于每种治疗剂,在相同或不同时间通过吸入或局部给药。本文所用的术语胃肠外包括例如,静脉内、动脉内、腹膜内、肌肉内、皮下、直肠或阴道给药。虽然所有这些给药形式均明确认为在本发明范围内,但给药形式的例子是注射液,特别是用于静脉内或动脉内注射或滴注。合适的注射用药物组合物可包含缓冲剂(如乙酸盐、磷酸盐或柠檬酸盐缓冲剂)、表面活性剂(如聚山梨酯),以及任选的稳定剂(如人白蛋白)等。然而,在与本文所教授内容相容的其它方法中,单独分离的sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)或与有效量的至少一种其他免疫调节疗法组合,可直接递送到不良细胞群的位点,从而增加患病组织与治疗剂的接触。
[0125]
如本文所讨论的,单独的sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)或与有效量的至少一种其他免疫调节疗法组合,可以针对体内治疗例如肿瘤性疾病,包括实体瘤的疾病的药学有效量给予。可以配制所公开的药剂以便于促进给药和促进活性剂的稳定性。在某些实施方式中,本发明的药物组合物包含药学上可接受的无毒无菌运载体,如生理盐水、无毒缓冲液、防腐剂等。出于本技术的目的,药学有效量的单独sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)或与有效量的至少一种其他免疫调节疗法组合应认为是指足以实现与靶标的有效结合并实现益处的量,所述益处即抑制、延迟或减少癌症患者中的转移。
[0126]
本发明所用的药物组合物包含药学上可接受的运载体,包括例如,离子交换剂、氧化铝、硬脂酸铝、卵磷脂,血清蛋白质如人血清白蛋白,缓冲物质如磷酸盐、甘氨酸、山梨酸、山梨酸钾、饱和植物脂肪酸的部分甘油酯混合物、水、盐或电解质,如硫酸鱼精蛋白、磷酸氢二钠、磷酸氢钾、氯化钠、锌盐、胶体二氧化硅、三硅酸镁、聚乙烯吡咯烷酮、纤维素基物质、聚乙二醇、羧甲基纤维素钠、聚丙烯酸酯、蜡、聚乙烯
‑
聚氧丙烯
‑
段聚合物、聚乙二醇和羊毛脂。
[0127]
胃肠道外给药制剂包括无菌的水性或非水性溶液、悬液和乳液。非水性溶剂的示例是丙二醇,聚乙二醇,植物油如橄榄油,和可注射的有机酯如油酸乙酯。水性运载体包括例如,水、醇/水溶液、乳液或悬液,包括盐水和缓冲介质。药学上可接受的运载体包括但不限于:0.01
‑
0.1m,或0.05m的磷酸盐缓冲液或0.8%盐水。其它常见的胃肠外载剂包括磷酸钠溶液、林格右旋糖、右旋糖和氯化钠、乳酸林格溶液或固定油。静脉内载剂包括液体和营养补充剂、电解质补充剂,例如基于林格右旋糖的那些物质等。也可存在防腐剂和其它添加
剂,例如,抗微生物剂、抗氧化剂、螯合剂和惰性气体等。
[0128]
更具体地,适于注射应用的药物组合物包括无菌水溶液(水溶性时)或分散液,以及用于临时制备无菌注射液或分散液的无菌粉末。在这种情况下,该组合物可以是无菌的,并应该是达到存在易注射性(easy syringability)程度的流体。它应该在制造和储存条件下稳定,并且应该在保存过程中能够抵抗微生物如细菌和真菌的污染作用。运载体可以是包含如水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇等)及其合适混合物的溶剂或分散介质。可维持合适的流动性,例如通过使用诸如卵磷脂的涂料、分散系情况下保持某种粒度以及通过使用表面活性剂。适用于本文所述治疗方法的制剂可参见《雷明顿药物科学》(remington
′
s pharmaceutical sciences)(马克出版公司(mack publishing co.))第21版(2005)。
[0129]
也可通过各种抗菌剂和抗真菌剂(如对羟基苯甲酸酯类、氯丁醇、苯酚、抗坏血酸、硫柳汞等)实现防止微生物的作用。在某些实施方式中,例如,组合物中可包含等渗剂,例如糖、多元醇如甘露醇、山梨糖醇、或氯化钠。可在组合物中包含延迟吸收的物质(如单硬脂酸铝和明胶)以延长可注射组合物的吸收。
[0130]
在任何情况下,制备无菌可注射溶液可通过将特定量的活性化合物(如抗
‑
sema4d抗体或其抗原结合片段、变体或衍生物,本身或与至少一种其它免疫调节疗法组合)掺入含有本文所列一种成分或多种成分组合的合适溶剂,然后进行过滤除菌。通常,将活性活化物掺入含有碱性分散介质和上述其它成分的无菌载剂中制备分散液。在用于制备无菌注射液的无菌粉末情况中,制备方法可包括真空干燥或冷冻干燥,可得到由其之前无菌过滤的溶液得到活性组分和任何其它所需组分的粉末。注射制剂在无菌条件下按照本领域已知方法加工,装入容器(如安瓿、袋、瓶、注射器或小管)中,并密封。此外,可以试剂盒的形式包装并销售制剂。这类制品可具有标签或药品说明书,表明相关组合物可用于治疗患有或倾向于患有疾病或病症的对象。
[0131]
胃肠外制剂可以是单次推注剂量,输注或负荷推注剂量,随后是维持剂量。可在具体固定或可变的间隔处给予这些组合物,例如,每天一次或者按需基础。
[0132]
某些药物组合物可以可接受的剂型口服给予,包括例如,胶囊、片剂、水性悬液或溶液。也可通过鼻气溶胶或吸入来给予某些药物组合物。这类组合物可制备成盐水溶液,其中采用苯甲醇或其他合适的防腐剂、提高生物利用度的吸收促进剂和/或其他常规增溶剂或分散剂。
[0133]
sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)单独或与有效量的至少一种其他免疫调节疗法组合以与运载体材料组合以产生单一剂型的量将根据所治疗的宿主和特定的给药方式而变化。可以单剂型、多剂型或在确立的时间段内的输注中给予组合物。也可调整给药方案,以提供最优所需反应(例如,治疗或预防性反应)。
[0134]
在本发明范围内,可以按照上述治疗方法给予人或其他动物足以产生治疗效果的量的单独sema4d拮抗剂(例如特异性结合sema4d的分离抗体或其抗原结合片段)或与有效量的至少一种其他免疫调节疗法的组合。sema4d拮抗剂(例如与sema4d特异性结合的分离抗体或其抗原结合片段)可以单独或与有效量的至少一种其他免疫调节疗法组合以常规剂型给予于此类人或其他动物,所述常规剂型根据已知技术通过将本文提供的抗体与常规药学上可接受的运载体或稀释剂组合来制备。本领域技术人员应认识到,药学上可接受运载
cloning a laboratory manual)(第4版;冷泉港实验室出版社(cold spring harbor laboratory press));sambrook等编(1992)《分子克隆:实验室手册》(molecular cloning:a laboratory manual),(冷泉港实验室出版社,纽约(cold springs harbor laboratory,ny));d.n.glover和b.d.hames编(1995)《dna克隆》(dna cloning)第2版(irl出版社(irl press)),第1
‑
4卷;gait编(1990)《寡核苷酸合成》(oligonucleotide synthesis)(irl 出版社);mullis等美国专利号4,683,195;hames和higgins编(1985)《核酸杂交》(nucleic acid hybridization)(irl出版社);hames和higgins编(1984)《转录和翻译》(transcription and translation)(irl出版社);freshney(2016)《动物细胞培养》(culture of animal cells)第七版,(约翰威立出版社(wiley
‑
blackwell));woodward,j.,《固定的细胞和酶》(immobilized cells and enzymes)(irl出版社)(1985);perbal(1988)《分子克隆实践指南》(a practical guide to molecular cloning);第2版(约翰威立出版社);miller和calos编(1987)《哺乳动物细胞的转基因载体》(gene transfer vectors for mammalian cells)(冷泉港实验室出版社);s.c.makrides(2003)《哺乳动物细胞中的基因转移和表达》(gene transfer and expression in mammalian cells)(爱思唯尔科学出版社(elsevier science));《酶学方法》(methods in enzymology)第151
‑
155卷(学术出版社公司,纽约(academic press,inc.,n.y.));mayer和walker编(1987)《细胞和分子生物学中的免疫化学方法》(immunochemical methods in cell and molecular biology)(学术出版社,伦敦(academic press,london));weir和blackwell编;和ausubel等(1995)《新编分子生物学实验指南》(current protocols in molecular biology)(约翰韦利父子公司(john wiley and sons))。
[0140]
抗体工程的一般原理可参见例如strohl,w.r.和l.m.strohl(2012)《治疗性抗体工程》(therapeutic antibody engineering)(伍德海德出版社(woodhead publishing))。蛋白质工程的一般原理可参见例如park和cochran编(2009)《蛋白质工程与设计》(protein engineering and design)(cdc出版社(cdc press))。免疫学的一般原理可参见例如abbas和lichtman(2017)《细胞和分子免疫学》(cellular and molecular immunology)第9版(爱思唯尔出版社(elsevier))。此外,本领域已知的免疫学标准方法可按照:例如,《新编免疫学实验指南》(current protocols in immunology)(威力在线图书馆(wiley online library));wild,d.(2013)《免疫测定手册》(the immunoassay handbook)第4版(爱思唯尔科学出版社);greenfield编(2013)《抗体:实验室手册》(antibodies,a laboratory manual)第2版(冷泉港实验室出版社);和ossipow和fischer编(2014)《单克隆抗体:方法和方案》(monoclonal antibodies:methods and protocols)(humana出版社(humana press))。
[0141]
将上文中引用的所有参考文献以及其中引用的所有参考文献通过引用全文纳入本文。
[0142]
通过说明的方式,而非限制性方式提供以下实施例。
[0143]
实施例
[0144]
实施例1:mdsc水平作为基于sema4d的癌症免疫疗法的生物标志物
[0145]
阻断pd
‑
1/pd
‑
l1通路是用于nsclc的有效免疫疗法,但是仍然需要合理的组合疗法以克服耐药性机制。classical
‑
肺临床试验正在测试派比奈单抗和阿维鲁单抗组合,将
检查点抑制导致的免疫激活与派比奈单抗对肿瘤免疫微环境的有益改善结合起来。
[0146]
目前正在进行一项1b/2期、开放标签、单臂、首次人体组合研究,以评估派比奈单抗与阿维鲁单抗组合在62名患有晚期(iiib/iv)nsclc的对象中的安全性、耐受性和功效。
[0147]
派比奈单抗(vx15/2503)是igg4人源化单克隆抗体,靶向脑信号蛋白4d(sema4d,cd100)。vh包含氨基酸序列seq id no:1,vl包含氨基酸序列seq id no:5。体内临床前模型证明,抗体阻断sema4d促进了cd8 t细胞和树突细胞的浸润,并减少肿瘤内免疫抑制性骨髓细胞和调节性t细胞(treg)的功能和招募。重要的是,临床前抗
‑
sema4d与各种免疫疗法的组合增强了t细胞活性和肿瘤消退。参见例如美国专利第9,243,068号,该专利通过引用完全纳入本文。
[0148]
阿维鲁单抗是完全人抗
‑
pd
‑
l1的igg1抗体,已被批准用于治疗默克尔(merkel)细胞癌和尿路上皮癌。阿维鲁单抗抑制pd
‑
l1
‑
pd
‑
1相互作用,也有可能诱发adcc。阿维鲁单抗的重链和轻链以seq id no:11和seq id no:12表示。
[0149]
研究设计
[0150]
该试验分为剂量递增(n=12)和剂量扩展(n=50)阶段。剂量递增部分包括未接受免疫治疗并且已经进展或拒绝标准一线或二线全身抗癌治疗的患者。剂量递增群组中的患者接受了递增剂量的派比奈单抗(5、10、20mg/kg,q2w)与阿维鲁单抗(10mg/kg,q2w)的组合。
[0151]
扩展阶段包括类似的患者群组以及第二个在免疫治疗期间或之后肿瘤进展的患者群组。
[0152]
人口统计学特征
[0153]
所有对象在基线时都患有iv期癌。腺癌和鳞状细胞癌对象分布均匀。67%的对象接受了在先的全身治疗。
[0154]
免疫细胞基线水平与研究时间的相关性
[0155]
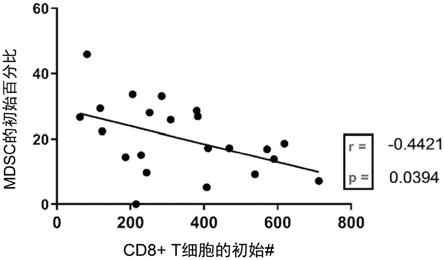
对基线与研究周的外周血免疫细胞亚群的初步分析表明,较高水平的t细胞和较低水平的mdsc与研究时间的长度相关。
[0156]
在治疗之前,对对象的cd8 t细胞和cd14
、hla
‑
dr
低
、cd11b
、cd33
、ln
‑
表型mdsc细胞的初始水平进行评估。“ln”是一组排除细胞群的标志物,包括cd3、cd19、cd56。在研究的这一初步阶段,“研究天数”是基于死亡、自主退出或疾病进展。基线和研究周的细胞亚群之间的斯皮尔曼等级相关性。相关性图表的截止值为2019年1月28日。
[0157]
在中心实验室通过流式细胞术在基线处测量外周血中的绝对细胞亚群或细胞亚群百分比。描绘直至疾病进展的每周给予的派比奈单抗剂量数与基线处外周血亚群的绝对值(个细胞/μl)(图1a,对于cd8 t细胞)或mdsc(单核细胞的)百分比(图1b)的关系(筛选访视和基线访视的平均值)。图1c描绘了外周血中初始cd8 t细胞与初始mdsc的百分比。提供了每个分析相应的斯皮尔曼等级相关系数(r)和p值。“研究周”定义为从第一剂到治疗结束或到分析截止日期(2019年1月25日)的时间。
[0158]
表2序列
[0159]
[0160]
[0161]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。