1.本发明属于肿瘤生物学领域,具体涉及一种肿瘤内分泌治疗药物诱导的休眠或复发细胞株的构建方法。
背景技术:
2.乳腺癌是目前发病率和死亡率最高的妇科恶性肿瘤,且于2020年发病率首次取代肺癌成为全球第一大癌症,占所有新增癌症患者的11.7%,其中,超过50%的乳腺癌患者雌激素受体阳性,该类乳腺癌的治疗也成为人们关注的焦点。传统的化疗和放疗由于缺乏特异性,取得疗效的同时往往也给患者带来较大的毒副作用,临床结局不佳。因此,为了使疗效达到最优化、毒性最低化,针对不同分子遗传学背景的群体和/或个体,根据其分子特点进行有选择性的“个体化”治疗具有重要临床意义。目前,内分泌治疗成为雌激素受体阳性患者临床治疗中的主流疗法,雌激素受体阳性的乳腺癌患者有多种内分泌治疗临床药物选择,且表现出了良好的疗效,能够有效改善预后,改善患者临床结局。但是大部分患者在接受内分泌治疗肿瘤消退后的5年甚至更长时间后出现复发,针对此类晚期乳腺癌患者,氟维斯群作为其主流临床的内分泌药物,在改善患者预后方面非常有限,这类患者通常即使服用药物,生存期也只有1
‑
2年,临床结局不佳。药物治疗下肿瘤细胞的休眠,是促使肿瘤耐药、复发和转移的一大过程和特性。
3.目前尚无模拟临床体内构建的针对休眠和复发特性的细胞株,仅有一些具有耐药特性的细胞株,且这些耐药特性细胞株产生多药耐药,致使耐药机制复杂,不利于对单一药物引起的肿瘤休眠、耐药、复发及转移的研究。
4.随着肿瘤研究的深入,应用传统方法(如卡尺测量肿瘤体积、肿瘤组织切片等)进行肿瘤研究已存在诸多限制。例如,进行组织切片观测前需要处死小鼠取出肿瘤组织,因此,在不同时间点或不同实验组都需要处死一批实验小鼠以获取足够的统计学数据,这样不但大大增加了实验成本,而且很难消除由于小鼠个体差异而产生的误差,无法获取可靠的重复性数据,并且在制作切片时也无法保证实验的准确性。此外,微小转移灶也很难被传统手段检测到。
5.荧光素酶(luciferase)是一类产生生物发光的氧化酶,可以在实验室中通过基因工程生产,并被用于多种目的,荧光素酶基因可以被合成并插入到生物体中或转染到细胞中。在萤光素酶反应中,当萤光素酶作用于合适的萤光素底物时会发光,而发出的光子可以通过光敏设备,如光度计或改进的光学显微镜检测,这就使得对于生物过程观察成为可能。由于荧光素酶生物发光不需要光激发,因此自发荧光很小,因此几乎没有背景荧光。表达荧光素酶的细胞移植到动物身上时,可进行全动物体内活体成像,是研究活体动物(如小鼠)细胞群的强大技术。这种技术已被应用于动物模型中跟踪肿瘤发生和肿瘤对治疗的反应,尤其对微小转移灶具有更高敏感性。
技术实现要素:
6.本发明为了解决现有技术中的不足和缺点,提出一种肿瘤内分泌治疗药物诱导的休眠或复发细胞株的构建方法,具体技术方案如下:
7.本发明第一方面提供一种肿瘤内分泌治疗药物诱导的休眠或复发细胞株的构建方法,包括如下步骤:
8.(1)转染表达荧光素酶基因的载体进入肿瘤细胞,筛选稳定表达荧光素酶基因的肿瘤细胞;
9.(2)将步骤(1)所述稳定表达荧光素酶基因的肿瘤细胞进行裸鼠原位异种移植成瘤实验,裸鼠成瘤后,注射肿瘤内分泌治疗药物治疗;
10.(3)步骤(2)治疗结束后,取出不增殖的肿瘤块或残留灶,进行原代培养,验证细胞休眠特性,得到休眠样细胞株,即为肿瘤内分泌治疗药物诱导的休眠细胞株;
11.(4)步骤(2)治疗结束后,待肿瘤恢复增殖,取出肿瘤块,进行原代培养,验证细胞复发特性,得到复发样细胞株,即为肿瘤内分泌治疗药物诱导的复发细胞株。
12.进一步地,本发明的上述技术方案中,所述肿瘤内分泌治疗药物的治疗周期按照药物临床治疗周期和人与小鼠平均寿命比率换算确定。
13.进一步地,本发明的上述技术方案中,所述肿瘤细胞为人源雌激素受体阳性乳腺癌细胞;优选地,所述人源雌激素受体阳性乳腺癌细胞选自mcf7细胞株;
14.所述肿瘤内分泌治疗药物为氟维斯群;优选地,每kg小鼠体重注射所述氟维斯群的剂量为25~35mg;优选地,每kg小鼠体重注射所述氟维斯群的剂量为30mg。
15.进一步地,本发明的上述技术方案中,步骤(2)中所述裸鼠为4
‑
6周龄balb/c雌性裸鼠;
16.优选地,步骤(2)中肿瘤内分泌治疗药物治疗4周;
17.优选地,步骤(4)中肿瘤恢复增殖至步骤(2)中所述裸鼠成瘤体积的5~15倍。
18.本发明第二方面提供上述构建方法构建的肿瘤内分泌治疗药物诱导的休眠或复发细胞株
19.本发明第三方面提供一种氟维斯群诱导的人源雌激素受体阳性乳腺癌的休眠细胞株,命名为人源雌激素受体阳性乳腺癌细胞mcf7
‑
fd,保藏编号为cctcc no:c2021199。
20.进一步地,所述休眠细胞株细胞大小和形状较为一致,成铺路石样,呈现出偏向间充质的形态。所述休眠细胞极性小且圆润的细胞比例大。所述休眠细胞的细胞周期相对于亲本细胞呈现出g0/g1周期阻滞特性,高度耐受氟维斯群,耐受程度约是亲本细胞的2500倍。
21.本发明第四方面提供一种氟维斯群诱导的人源雌激素受体阳性乳腺癌的复发细胞株,命名为人源雌激素受体阳性乳腺癌细胞mcf7
‑
fr,保藏编号为cctcc no:c2021200。
22.进一步地,所述复发细胞株细胞大小不一,有梭形与多角形,多有突起,且多角形形态各异,呈现出偏向上皮样的形态。所述复发细胞极性强且有触角的细胞比例大。所述复发细胞的细胞周期相对于亲本细胞未呈现出g0/g1周期阻滞,恢复细胞周期和细胞增殖,高度耐受氟维斯群,耐受程度约是亲本细胞的2500倍。
23.本发明第五方面提供所述细胞株作为肿瘤耐药、休眠、复发或转移机制研究的细胞模型的用途。
24.本发明第六方面提供所述细胞株作为肿瘤靶向治疗位点筛选的细胞模型的用途;优选地,作为肿瘤复发的靶向治疗位点筛选的细胞模型的用途;优选地,作为晚期雌激素受体阳性乳腺癌靶向治疗位点筛选的细胞模型的用途。
25.本发明第七方面提供所述细胞株作为肿瘤靶向治疗药物筛选的细胞模型的用途;优选地,作为肿瘤复发的靶向治疗药物筛选的细胞模型的用途;优选地,作为晚期雌激素受体阳性乳腺癌治疗药物筛选的细胞模型的用途。
26.本发明的有益效果:
27.1、本发明提供的肿瘤内分泌治疗药物诱导的休眠或复发细胞株的构建方法,通过生物学手段,转染表达荧光素酶基因的载体进入肿瘤细胞,筛选稳定表达荧光素酶基因的肿瘤细胞进行裸鼠原位异种移植成瘤实验,裸鼠成瘤后,注射肿瘤内分泌治疗药物治疗。治疗结束后,取出不增殖的肿瘤块或残留灶,进行原代培养,验证细胞休眠特性,得到休眠样细胞株;取出恢复增殖的肿瘤块,进行原代培养,验证细胞复发特性,得到复发样细胞株。本发明构建方法通过模拟临床给药,创新性地从体内构建休眠或复发细胞模型,且该构建方法可以针对单一药物引起的肿瘤耐药、休眠、复发及转移进行研究,专一性强。同时,细胞内稳定表达的荧光素酶也有利于稳定标记与活体示踪,尤其对微小转移灶具有更高敏感性。
28.2、本发明提供的氟维斯群诱导的人源雌激素受体阳性乳腺癌的休眠或复发细胞株的构建方法,通过转染表达荧光素酶基因的载体进入人源雌激素受体阳性乳腺癌细胞,筛选稳定表达荧光素酶基因的乳腺癌细胞进行裸鼠原位异种移植成瘤实验,裸鼠成瘤后,注射氟维斯群。治疗结束后,取出不增殖的肿瘤块和恢复增殖的肿瘤块,分别进行原代培养,得到休眠样细胞株和复发样细胞株。一方面,该构建方法模拟晚期雌激素受体阳性乳腺癌患者主要内分泌药物氟维斯群的临床给药,创新性地从体内构建休眠和复发细胞模型,克服了当前从人体直接分离雌激素受体阳性乳癌病灶组织难以在小鼠体内成瘤建模的问题;另一方面,细胞内稳定表达的荧光素酶可稳定标记与活体示踪,尤其对微小转移灶具有更高敏感性,便于后期氟维斯群治疗压力下复发转移等方向的深入研究,为开发晚期雌激素受体阳性乳腺癌患者的新治疗策略提供参考。
29.3、本发明提供的氟维斯群诱导的人源雌激素受体阳性乳腺癌的休眠细胞株mcf7
‑
fd和复发细胞株mcf7
‑
fr,相对于亲本细胞的氟维斯群耐受性明显增强,休眠样mcf7
‑
fd呈现出明显的细胞周期g1/g0阻滞等细胞休眠特性,复发样mcf7
‑
fr细胞周期进程得到恢复。一方面,建模过程和临床给药高度贴合,有利于研发雌激素受体阳性乳腺癌晚期患者内分泌治疗抵抗的临床肿瘤休眠、转移、复发和耐药的分子机制,进行相关生物学研究和挖掘新的治疗策略,期望有效改善晚期雌激素受体阳性乳腺癌患者的预后和临床结局。另一方面,细胞内稳定表达的荧光素酶可稳定标记与活体示踪,进行肿瘤早期观测及微小转移灶的观测,既能对活体癌组织生长进行连续监测并进行定量分析,又能在离体的肿瘤组织及体外共培养体系中标识癌细胞以便于准确的定性和定量,还能更灵敏的发现残余病灶点或尽早发现肿瘤的复发,从而更准确的对药物治疗效果进行判定。氟维斯群诱导的人源雌激素受体阳性乳腺癌的休眠细胞株mcf7
‑
fd和复发细胞株mcf7
‑
fr可视化效果更佳,为研究相关机制、靶点探索和新药筛选提供了更为合理的实验模型。
附图说明
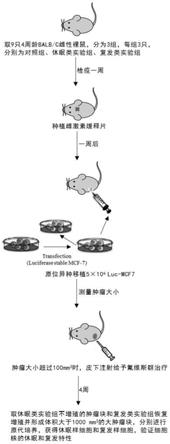
30.图1为人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞的构建流程图;
31.图2为人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞的形态学观察;
32.图3为不同浓度氟维斯群下亲本细胞、休眠细胞株mcf7
‑
fd和复发细胞株mcf7
‑
fr的细胞存活情况;
33.图4为亲本细胞、休眠细胞株mcf7
‑
fd和复发细胞株mcf7
‑
fr的细胞周期图。
34.保藏说明
35.人源雌激素受体阳性乳腺癌细胞mcf7
‑
fd,分类命名为人源雌激素受体阳性乳腺癌细胞mcf7
‑
fd,于2021年7月30日保藏于中国典型培养物保藏中心,地址为中国.武汉.武汉大学,保藏编号为cctcc no:c2021199;
36.人源雌激素受体阳性乳腺癌细胞mcf7
‑
fr,分类命名为人源雌激素受体阳性乳腺癌细胞mcf7
‑
fr,于2021年7月30日保藏于中国典型培养物保藏中心,地址为中国.武汉.武汉大学,保藏编号为cctcc no:c2021200。
具体实施方式
37.为了更清楚地理解本发明,现参照下列实施例及附图进一步描述本发明。实施例仅用于解释而不以任何方式限制本发明。实施例中,各原始试剂材料均可商购获得,未注明具体条件的实验方法为所属领域熟知的常规方法和常规条件,或按照仪器制造商所建议的条件。
38.在一个优选的实施方案中,本发明构建的氟维斯群诱导的人源雌激素受体阳性乳腺癌的休眠细胞株mcf7
‑
fd和复发细胞株mcf7
‑
fr作为肿瘤耐药、休眠、复发或转移机制研究的细胞模型的用途,用于研究氟维斯群促进肿瘤耐药、休眠、复发或转移的机制。
39.在一个优选的实施方案中,本发明构建的氟维斯群诱导的人源雌激素受体阳性乳腺癌的休眠细胞株mcf7
‑
fd和复发细胞株mcf7
‑
fr作为肿瘤靶向治疗位点筛选或靶向治疗药物筛选的细胞模型的用途,尤其是针对有耐药、休眠、复发或转移的肿瘤细胞进行靶向治疗,筛选靶向治疗药物,为晚期雌激素受体阳性乳腺癌患者提供新的治疗策略。
40.术语:
41.mcf7细胞:人乳腺癌细胞
42.fbs:胎牛血清
43.g418:遗传霉素
44.d
‑
luciferin:萤虫素(d
‑
虫荧光素)
45.实施例1:人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞的构建
46.人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞的构建流程如图1。
47.(1)筛选稳定表达荧光素酶基因的mcf7细胞
48.构建含荧光素酶基因的表达载体,备用。载体的构建参照试剂盒中说明书。
49.将mcf7细胞接种于6孔板,当细胞汇合度达80%时进行瞬时转染。6孔板各孔以质粒dna2ug、脂质体6ul进行转染,37℃、5%co2孵育24h。mcf7细胞转染72h后吸弃上清液,加入含有10%fcs、800μg/ml g418的rpmi 1640培养基,培养约3周,期间换液,去除死亡的细胞,筛选出稳定表达luciferase的细胞(命名为luc
‑
mcf7)。
50.检测稳定表达luciferase细胞系生物发光:活性消化计数luc
‑
mcf7细胞,以0.25
×
106个、0.5
×
106个、1
×
106个、1.5
×
106个、2
×
106个细胞分别接种至6孔板,预留一孔仅添加培养基作为空白对照。细胞贴壁过夜后,于6孔板每孔添加15mg/ml d
‑
luciferin,轻轻摇匀置于lumina成像系统进行检测。lumina成像结果表明,筛选的luc
‑
mcf7细胞能够稳定表达luciferase。
51.(2)原位异种移植物成瘤实验
52.取9只4周龄balb/c雌性裸鼠,分为3组,每组3只,分别为对照组、休眠类实验组、复发类实验组,检疫一周,种植雌激素缓释片,一周后在裸鼠身上通过原位移植进行接种肿瘤细胞luc
‑
mcf7(1000万细胞/只),每天用游标卡尺测量肿瘤大小,每周进行2次活体成像观察肿瘤大小。当肿瘤大小超过100mm3时,休眠类实验组和复发类实验组按照30mg/kg剂量皮下注射给予氟维斯群治疗,持续4周,肿瘤在治疗期间形成不发生明显增殖的肿瘤块或残留灶。
53.对照组当肿瘤大小超过100mm3时,给予与休眠类实验组、复发类实验组等量的药物溶剂,持续4周,待肿瘤长大至1000mm3时,牺牲小鼠,取出肿瘤进行原代培养,此细胞为亲本细胞。
54.(3)获得休眠样细胞株和复发样细胞株
55.4周治疗结束后,取出休眠类实验组不增殖的残留肿瘤块进行原代培养,获得的细胞即为人源雌激素受体阳性乳腺癌休眠样细胞,命名为mcf7
‑
fd。
56.对复发类实验组接受完4周氟维斯群治疗后停止给药,待其恢复增殖并形成体积大于1000mm3的大肿瘤块时取出肿瘤进行原代培养,获得的细胞即为人源雌激素受体阳性乳腺癌复发样细胞,命名为mcf7
‑
fr。
57.实验例1:人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞的形态学观察
58.使用倒置相差显微镜观察活细胞形态:取对数生长期的休眠样mcf7
‑
fd细胞和复发样mcf7
‑
fr细胞,在倒置显微镜放大200倍下观察活细胞形态,如图2所示。
59.通过光镜可以观察到mcf7
‑
fd细胞大小和形状较为一致,成铺路石样,呈现出更偏向间充质的形态,极性更小偏圆润的细胞比例更大。
60.通过光镜可以观察到mcf7
‑
fr细胞大小不一,有梭形与多角形,多有突起,且多角形形态各异,呈现出更偏向上皮样的形态,极性更强,能看到明显的触角。
61.实验例2:人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞对氟维斯群耐药指数的测定
62.取实施例1获取的休眠样细胞mcf7
‑
fd、复发样细胞mcf7
‑
fr和亲本细胞,在含有2%胎牛血清的rpmi1640培养基中培养,培养至对数生长期,用0.25%腆蛋白酶消化并计数,用1640培养液调整细胞浓度至2
×
104/ml。同时设置仅接种细胞的无药对照孔和仅加培养液的调零孔。在96孔板的每个孔中分别接种0.1ml单细胞悬液,每个孔含2000个细胞,置于培养箱中培养过夜。吸弃每孔中的上清液,pbs洗一次,之后加入含氟维斯群的细胞培养液0.1m1,氟维斯群的浓度梯度如表1,每一种药物的浓度设3个复孔。表中的化疗药物浓度是经过多次测定确定的稳定浓度范围,每次耐药指数测定3次,该范围可能根据会有小幅度的调整,以利于更准确的测定耐药指数。
63.表1氟维斯群的给药浓度
[0064][0065]
96孔板放入培养箱培养72h后,在200倍倒置显微镜下计数每孔活细胞数量,每3个复孔取其平均值。不同浓度氟维斯群下亲本细胞、休眠细胞株mcf7
‑
fd和复发细胞株mcf7
‑
fr的细胞存活,如图3。用软件graphpad primer 5计算药物的半数抑制率ic50,结果如表2。结果表明休眠样细胞mcf7
‑
fd和复发样细胞mcf7
‑
fr对氟维斯群的耐受程度约是亲本细胞的2500倍,皆为高度耐受氟维斯群的细胞。
[0066]
表2氟维斯群对不同组细胞的半数抑制浓度测定
[0067][0068]
实验例3:人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞的细胞周期分析
[0069]
用流式细胞仪分析细胞周期。将实施例1的人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞培养至对数生长期,用不含edta的胰酶消化计数,各取2
×
106个,用预冷的pbs洗细胞2次,每次800g/min离心5分钟,加入1ml预冷的70%浓度的乙醇,
‑
20℃下过夜固定16小时。用4℃预冷的pbs洗细胞1次,800g/min离心5min。细胞沉淀中加200ul pbs溶液,重悬细胞,再加入2ul 10mg/ml的pi染色液混匀,4℃避光孵育30min。
[0070]
采用标准程序进行流式细胞仪检测,记录激发波长488nm处红色荧光。本实施例的人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞的细胞周期分析,如图4。两者的细胞周期分布见表3。
[0071]
表3人源雌激素受体阳性乳腺癌mcf7
‑
fd/mcf7
‑
fr细胞周期分布表
[0072][0073]
结果显示,亲本细胞的g0/g1细胞为38.84%,而休眠样mcf7
‑
fd细胞的g0/g1细胞为55.23%,差异有统计学意义(p<0.001),呈现出明显的细胞周期g1/g0阻滞等细胞休眠特性。复发样mcf7
‑
fr的g0/g1细胞为41.05%,与亲本细胞没有统计学差异,未呈现出明显g0/g1周期阻滞,细胞周期得到一定恢复,细胞一定程度上恢复增殖属性。
[0074]
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。

