1.本公开涉及微流控芯片技术领域,具体涉及一种用于集成核酸提取、扩增、检测于一体的微流控芯片,还包括其制备方法、使用方法及用途。
背景技术:
2.结核病(tb)是由结核分枝杆菌(mtbc)引起的严重危害人类健康的世界性传染病,也是致死亡率最高的单一传染性病原体。据世界卫生组织(who)发布的《2019年全球结核病报告》统计,2019年新增了1000万的感染病例,新增140万的死亡病例。而我国的结核病总人数在全球30个结核病高负担国家中位于第二名。因此,为了阻止其传播,降低疾病死亡率,需要开发结核病的快速诊断技术。在一些设备齐全的三级医院,自动化结核病检测仪器如genexpert、genedrive和cobas已经被广泛应用。虽然这些设备具有自动化和用户友好的特点,但由于其检测原理均是基于荧光定量pcr(qpcr)技术,需要配备精确的温度控制模块和光学检测模块,因此为仪器的开发与生产带来了高昂的成本。以genexpert为例,17500$的仪器价格,10$的单次检测费用,超出了基础设施匮乏的地区的经济承受能力。而且,这些仪器均要求专业人员在标准实验室进行样品制备、核酸扩增和检测等复杂操作,从而阻碍了它们在偏远地区的应用。因此,急需设计一种低成本、易操作、鉴定准确的即时平台(poct)能够在资源匮乏地区进行广泛的使用。
3.核酸快速扩增技术为poc平台的设计奠定了基础,而常用的核酸扩增技术qpcr存在一些固有的缺点,如精确的热循环温度和较长的热循环周期(2小时),使其难以应用于poc平台。目前,重组酶聚合酶扩增(recombinase polymerase amplification,rpa)、环介导等温扩增(loop-mediated isothermal amplification,lamp)等的等温核酸扩增技术可以替代传统的pcr方法。特别是rpa技术,可以在生理温度下(37~42℃)快速扩增核酸,而不需要精确的温度控制,非常适用于poc平台。
4.poc平台诊断的另一个关键因素在于设备的结构。在结核病的检测中存在交叉污染的风险,因此需要在完全密封的环境下进行“样本输入-结果输出”的过程,这对不同模块的设计和协调提出了挑战,包括样本输入、结核病原体dna提取、核酸扩增和结果读出。目前,已经有报道将微流控芯片与rpa扩增技术结合实现了自动检测,如law设计了一种自动旋转芯片,在注入样本后利用离心力驱动液体流到相应位置,通过监测rpa荧光检测结核杆菌的耐药性。然而,这种微流控芯片仍然需要离心装置或外部驱动泵,不足以满足无仪器的要求。
技术实现要素:
5.(一)要解决的技术问题
6.针对上述问题,本公开提供了一种集成核酸提取、扩增、检测于一体的微流控芯片,用于至少部分解决传统核酸检测难以实现便携、无仪器的现场快速检测等技术问题。
7.(二)技术方案
8.本公开一方面提供了一种集成核酸提取、扩增、检测于一体的微流控芯片,包括:芯片基底,和设置在芯片基底上的进样口1,dna洗涤缓冲液储存室2、rpa扩增缓冲液储存室3,dna提取区10和至少两个核酸扩增室13、14,至少两个核酸扩增室13、14平行并置,进样口1、dna洗涤缓冲液储存室2和rpa扩增缓冲液储存室3中的每一个与dna提取区10之间,以及dna提取区10和至少两个核酸扩增室13、14之间通过微通道连接,其中dna洗涤缓冲液储存室2和rpa扩增缓冲液储存室3的上表面分别覆有弹性材料;dna提取区10填充有二氧化硅。
9.进一步地,进样口1、dna洗涤缓冲液2、rpa扩增缓冲液3与dna提取区10之间分别设置有防回流结构4、5、6。
10.进一步地,防回流结构4、5、6为悬臂式挡板微阀的设计,靠近正向出液口的一侧设置有挡板,以及有一定间距的弹性膜瓣。
11.进一步地,还包括:废液池11,通过微通道连接于dna提取区10之后、核酸扩增室13之前;废液池11底部设有透气孔12。
12.进一步地,每个核酸扩增室13包括“y”形通道、反应池18;核酸扩增室13、14之间通过“y”形通道相连接,最后一个“y”形通道之后设置有透气孔23。
13.进一步地,反应池18中存储有rpa扩增反应原料、荧光标记探针;rpa扩增反应原料包括引物、rpa酶反应冻干粉、rpa反应启动子,荧光标记探针为fam探针。
14.进一步地,dna提取区10为“w”蛇形通道,二氧化硅为用盐酸胍预处理过的二氧化硅珠。
15.本公开另一方面提供了一种用于核酸扩增检测的微流控芯片的制备方法,包括:在芯片基底上刻蚀出进样口1,dna洗涤缓冲液储存室2、rpa扩增缓冲液储存室3,dna提取区10,至少两个核酸扩增室13、14,微通道,至少两个核酸扩增室13、14平行并置;进样口1、dna洗涤缓冲液储存室2和rpa扩增缓冲液储存室3中的每一个与dna提取区10之间,以及dna提取区10和至少两个核酸扩增室13、14之间通过微通道连接;在dna洗涤缓冲液储存室2和rpa扩增缓冲液储存室3的上表面分别覆上弹性材料;dna提取区10中填充有二氧化硅。
16.本公开还有一方面提供了根据前述用于核酸扩增检测的微流控芯片的使用方法,包括:从进样口1进样,样品进入dna提取区10进行dna提取;按压dna洗涤缓冲液储存室2上的弹性材料,使dna洗涤缓冲液进入dna提取区10,去除dna提取过程中的杂质和抑制剂;按压rpa扩增缓冲液储存室3上的弹性材料,使rpa扩增缓冲液洗脱dna并将该dna输送至每个核酸扩增室13中;将该微流控芯片置于37~42℃下进行rpa扩增,获取该rpa扩增的荧光检测结果。
17.本公开还有一方面提供了前述用于核酸扩增检测的微流控芯片在人类结核分枝杆菌、结核分枝杆菌复合体、分枝杆菌检测中的应用。
18.(三)有益效果
19.本公开的集成核酸提取、扩增、检测于一体的微流控芯片,包括制备方法及用途,通过简单的手指按压来驱动液体流动,能够在一个完全封闭的芯片中完成结核病的诊断过程,包括进样、提取dna、基于rpa的核酸扩增、以及结果的直接读出;这样的设计摆脱了对电力、外部泵的需求,能够在资源有限的地区使用。其次,为了消除交叉污染的风险,在rpa反应体系中添加了fam修饰的探针,使得结果能够在芯片内通过原位荧光的方式读出。最后,还设计了多个平行的检测室,能够同时识别人类结核分枝杆菌(mtb)、结核分枝杆菌复合体
(mtbc)和分枝杆菌(mb),从而鉴别结核感染/非结核感染,人结核分枝杆菌/牛分枝杆菌。
附图说明
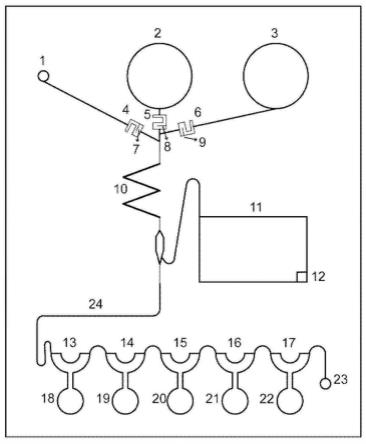
20.图1示意性示出了根据本公开实施例中集成核酸提取、扩增、检测于一体的微流控芯片的结构示意图;
21.图2示意性示出了根据本公开实施例中pdms可压缩弹性膜的制作示意图;
22.图3示意性示出了根据本公开实施例中防回流结构的示意图;
23.图4示意性示出了根据本公开实施例中二氧化硅吸附dna的原理示意图;
24.图5示意性示出了根据本公开实施例中可视化rpa的扩增原理示意图;
25.图6示意性示出了根据本公开实施例中用于检测结核病的rpa引物和探针的序列;
26.图7示意性示出了根据本公开实施例中手指驱动微流控芯片的4种临床结果诊断照片;
27.图8示意性示出了根据本公开实施例中手指驱动微流控芯片的灵敏度检测结果照片;
28.附图标记说明:
29.1进样口;
30.2dna洗涤缓冲液储存室;
31.3rpa扩增缓冲液储存室;
32.4~6防回流结构;
33.7~9弹性膜瓣;
34.10dna提取区;
35.11废液池;
36.12、23透气孔;
37.13~17核酸扩增室;
38.18~22小圆柱腔室;
39.24微流控通道。
具体实施方式
40.为使本公开的目的、技术方案和优点更加清楚明白,以下结合具体实施例,并参照附图,对本公开进一步详细说明。
41.为了解决上述问题,本公开设计了一种低成本、便携、“从样本-结果”的手指驱动微流控芯片。
42.本公开的实施例提供了一种用于核酸扩增检测的微流控芯片,请参见图1,包括:芯片基底,和设置在芯片基底上的进样口1,dna洗涤缓冲液储存室2、rpa扩增缓冲液储存室3,dna提取区10和至少两个核酸扩增室13、14,至少两个核酸扩增室13、14平行并置,进样口1、dna洗涤缓冲液储存室2和rpa扩增缓冲液储存室3中的每一个与dna提取区10之间,以及dna提取区10和至少两个核酸扩增室13、14之间通过微通道连接,其中dna洗涤缓冲液储存室2和rpa扩增缓冲液储存室3的上表面分别覆有弹性材料;dna提取区10填充有二氧化硅。
43.芯片基底可采用聚甲基丙烯酸甲酯pmma,pmma是一种具有低成本、易加工和良好
的生物相容性的特点,具有更好的传热速率,缩短加热时间。dna洗涤缓冲液和rpa扩增缓冲液分别填充到dna洗涤缓冲液储存室2、rpa扩增缓冲液储存室3,该两种缓冲液储存室上表面覆有弹性材料,通过按压该弹性材料可驱使dna洗涤缓冲液、rpa扩增缓冲液在微通道内流动;dna洗涤缓冲液用于去除dna提取过程中的杂质和抑制剂,rpa扩增缓冲液用于进行rpa扩增。dna提取区10用于提取样品中的dna,将dna被吸附于二氧化硅颗粒上。
44.本公开以重组酶聚合酶扩增rpa为检测技术,结合微流控芯片技术,设计了手指驱动液体的核酸检测装置。目的在于提供一种无仪器需求的核酸检测芯片,制作过程简单,所需成本低,用户操作简单,在便携的基础上做到多指标的检测,检测结果肉眼可见,非常适合病原体的现场快速检测。
45.在上述实施例的基础上,dna洗涤缓冲液2、rpa扩增缓冲液3上分别固定有pdms制作的弹性膜,用于手指按压驱动膜内液体流动。
46.图2示意性示出pdms可压缩弹性膜的制作示意图。将pdms混合液注入一个10.5mm的腔体1,然后将另一个腔体压在上面2,80℃固定2h,制成200μm的弹性膜。最后固定在dna洗涤缓冲液2、rpa扩增缓冲液3的对应位置。
47.在进样口1、dna洗涤缓冲液2、rpa扩增缓冲液3与dna提取区10这三个进液口的微通道内嵌入了pdms制成的悬臂式挡板结构,可以通过阀的变形防止液体回流。
48.图3示意性示出了防回流结构的示意图,为悬臂式挡板微阀的设计,通过阀的变形防止液体回流。将在pmma上刻蚀的悬臂阀作为挡板,用pdms制成弹性膜瓣粘在挡板下方。当微阀处于液体正向压力时,挡板与弹性膜瓣之间的间隙可使流体顺利流动,微阀处于向前导流状态。然而,当微阀受到流体反向压力时,弹性膜瓣有向挡板移动的趋势。随着反压逐渐增加,膜瓣与挡板紧密接触,阻断流体通过,微阀呈现反向阻塞状态。因此,这种悬臂式挡板结构可以有效地防止流体的逆流。当然这里还可以是其他形状或者材料制作的微阀,只要能实现当通道内收到反向压力,液体不能通过微阀均可。
49.在上述实施例的基础上,dna提取区10为“w”蛇形通道,二氧化硅为盐酸胍预处理过的二氧化硅珠。
50.在dna提取区内填充有二氧化硅珠,基于二氧化硅对病原体的核酸进行固相萃取。dna提取区设计为“w”形通道,能够增大样品与二氧化硅珠的接触面,使两者充分混合。当样品进入到微通道与硅粒子混合时,在高浓度的盐离子作用下,样品中带负电荷的dna分子通过阳离子盐桥与硅粒子结合,从而被吸附于二氧化硅珠上。图4为dna提取区中二氧化硅对核酸的固相提取原理。将二氧化硅颗粒1用6m盐酸胍预处理30分钟,填充在“w”形微通道中,二氧化硅颗粒能够以盐桥2的形式吸附dna3。
51.在上述实施例的基础上,还包括:废液池11,通过微通道连接于dna提取区10之后、核酸扩增室13之前;废液池11底部设有透气孔12。
52.废液池11,通过微通道连接于dna提取区10之后、核酸扩增室13之前(请参见图1),用于接收进样液体和dna洗涤缓冲液2;废液池11底部设有透气孔12,当该废液池11装满液体后,液体才会流至核酸扩增室13。同时dna提取区10之后设置有一类似菱形的结构,液体先流至该菱形腔中,然后通过两个微通道分流,分别流向废液池11、核酸扩增室13,菱形腔与核酸扩增室13之间的微通道24由两端粗细不同的微通道组成,靠近菱形腔的一段微通道比靠近核酸扩增室13的微通道更细,进一步使得液体先流向废液池11。同时,废液池11的容
积等于或大于从进样口1进样液体的体积与dna洗涤缓冲液2的体积之和,但是废液池11的容积也不宜过大,以便于废液池装满之后,使核酸洗脱液流入到细的通道,再进一步流向核酸扩增室13。
53.在上述实施例的基础上,每个核酸扩增室13包括“y”形通道、反应池18;核酸扩增室13、14之间通过“y”形通道相连接,最后一个“y”形通道之后设置有透气孔23。
54.核酸扩增区设计成多个平行的“y”形通道,并在最后连接了一个通气孔。“y”形通道下方设计为圆柱形储液池,作为核酸扩增反应池。设置至少核酸扩增室13、14,其中一个用作对照组,以防止假阴性结果。去除杂质后,废液池11基本装满液体,按压rpa扩增缓冲液储存室3上的弹性材料,rpa扩增缓冲液将纯化后的dna洗脱到5个平行的“y”形检测区,当液体先充满一个“y”形后,会随即流入到另一个“y”形通道。轻甩芯片后,“y”形通道中的液体才会流入到圆柱形的反应池进行扩增。
55.在上述实施例的基础上,反应池18中存储有rpa扩增反应原料、荧光标记探针;rpa扩增反应原料包括引物、rpa酶反应冻干粉、rpa反应启动子,荧光标记探针为fam探针。
56.反应池中提前固定了引物、冻干rpa酶反应干粉、rpa反应启动子mg
2
。rpa等温扩增技术能在恒温状态下(37~42℃),利用重组酶与引物结合,形成蛋白-dna复合物。接着在dsdna中寻找同源序列,一旦引物定位了同源序列,就会发生链交换反应形成并启动dna合成,对模板上的目标区域进行指数式扩增。本公开还设计了fam修饰的探针对扩增结果进行原位可视化观察。简单地说,fam探针的荧光信号首先被淬灭剂bhq淬灭。一旦目标基因与探针结合,外切酶nfo就会将探针裂解,将fam和bhq分离,从而在480nm的激发源下可观察到fam荧光(520nm)。fam荧光可以通过肉眼直接观察到,无需重新打开密封的反应室,从而消除了交叉污染的风险。图5为可视化rpa的原理图,fam探针的荧光信号首先被淬灭剂bhq淬灭(1),当目标基因与探针结合,外切酶nfo将探针裂解(2),将fam和bhq分离,从而在480nm的激发源下可观察到fam荧光(520nm)(3)。
57.本公开提供一种快速、低成本、便携式、手指驱动微流控芯片,基于重组酶聚合酶扩增(rpa)可用于结核病的现场鉴定。该微流控芯片可通过简单的手指按压来驱动芯片中预储存的液体在微流道中的流动,并利用二氧化硅颗粒对病原体中的核酸实现固相萃取,最后通过重组酶聚合酶技术实现核酸的等温扩增。该芯片被设计用于多重检测,基于fam的探针可对检测结果实现荧光原位观察。该公开基于样本前处理和核酸恒温扩增的集成化技术,通过手指驱动液体流动,将核酸提取、扩增、检测集于一体,研发了一款便携式多功能核酸检测芯片,实现了快速便携、无仪器的现场快速检测。
58.本公开还提供了一种用于核酸扩增检测的微流控芯片的制备方法,包括:在芯片基底上刻蚀出进样口1,dna洗涤缓冲液储存室2、rpa扩增缓冲液储存室3,dna提取区10,至少两个核酸扩增室13、14,微通道,至少两个核酸扩增室13、14平行并置;进样口1、dna洗涤缓冲液储存室2和rpa扩增缓冲液储存室3中的每一个与dna提取区10之间,以及dna提取区10和至少两个核酸扩增室13、14之间通过微通道连接;在dna洗涤缓冲液储存室2和rpa扩增缓冲液储存室3的上表面分别覆上弹性材料;向dna提取区10填充二氧化硅。
59.(1)设计所需要的微流控管道的图形,绘制cad图纸,利用激光刻蚀技术在聚甲基丙烯酸甲酯pmma基底进行刻蚀,制备出带有进样口1、液体储存室2和3、dna提取区10、废液池11、核酸扩增室13~17、微通道24的多功能微流控芯片。
60.(2)用聚二甲基硅氧烷pdms制作成可压缩的弹性膜,固定在pmma液体储存室的对应位置,并提前储存一定量的dna洗涤缓冲液和rpa扩增缓冲液。用于按压驱动弹性膜中的液体在微通道内流动。对于可按压式的pdms膜,其制作过程如图2所示:将pdms的弹性体基和固化剂按照10∶1的比例进行混合,真空脱气后,将混合液注入一个10.5mm的腔体(1),然后将另一个腔体压在上面(2),80℃固定2h,制成200μm的弹性膜。最后粘在dna洗涤缓冲液2、rpa扩增缓冲液3的对应位置,80℃固定2h。
61.(3)在三个进液口的微通道内嵌入了pdms制成的悬臂式挡板结构,可以通过阀的变形防止液体回流。将在pmma上刻蚀的悬臂阀作为挡板,用pdms制成200μm的弹性膜瓣粘在距离挡板200μm左右的地方。当液体正向流动时,挡板与弹性膜瓣之间的间隙可使流体顺利通过。然而,当液体反向流动时,弹性膜瓣与挡板紧密接触,阻断流体通过。因此,这种悬臂式挡板结构可以有效地防止流体的逆流。
62.(4)dna洗涤缓冲液成分为70%乙醇和10mm tris(ph=8)。rpa缓冲液的成分为重组酶聚合酶扩增(rpa)扩增试剂盒中提供的复水缓冲液。
63.(5)dna提取区设计为“w”蛇形通道,填充有用6m盐酸胍预处理过的二氧化硅珠,对病原体的核酸进行固相萃取。
64.(6)废液池底部刻蚀了一个通气孔,以便液体先流入废液池。
65.(7)核酸扩增区设计成多个平行的“y”形通道,并在最后连接了一个通气孔。
66.(8)“y”形通道下方设计为圆柱形储液池,作为核酸扩增反应池。
67.(9)核酸扩增反应池中预粘附引物、rpa酶反应冻干粉、rpa反应启动子mg
2
。
68.(10)芯片用单面封口膜进行封闭,形成封闭环境,避免不同检测位点之间的相互串扰,有效提高检测准确度。
69.本公开还提供了一种根据前述用于核酸扩增检测的微流控芯片的使用方法,包括:从进样口进样,样品进入dna提取区10进行dna提取;按压dna洗涤缓冲液储存室2上的弹性材料,使dna洗涤缓冲液进入dna提取区10,去除dna提取过程中的杂质和抑制剂;按压rpa扩增缓冲液储存室3上的弹性材料,使rpa扩增缓冲液洗脱dna并将该dna输送至每个核酸扩增室13中;将该微流控芯片置于37~42℃下进行rpa扩增,获取该rpa扩增的荧光检测结果。
70.步骤1,微流控芯片预填充。预先在液体储存室中储存dna洗涤液和的rpa缓冲液。二氧化硅珠填充到dna提取区。引物、冻干rpa酶反应干粉、rpa反应启动子mg
2
填充到圆柱形反应池,芯片用单面封口膜进行封闭,形成封闭环境。
71.步骤2,进样。痰液样品经过简单的净化后通过进样口注入到芯片中。在流经预先装有二氧化硅颗粒的dna提取区后,样品中的病原体被裂解,dna被吸附于二氧化硅颗粒上。废液流入废液池。
72.步骤3,提取结核病原体dna。直接用手指按压pdms膜,使膜中预先装好的dna洗涤缓冲液被压入微通道,进入到dna提取区,去除dna提取过程中的杂质和抑制剂,废液流入废液池;
73.步骤4,rpa反应。用手指按压pdms膜,挤出预填充的rpa扩增缓冲液,将纯化后的dna洗脱到5个平行的“y”形检测区。然后将芯片置于37~42℃的水浴锅中进行rpa扩增,20min后在手持蓝色激发灯下对扩增结果进行判断。
74.其中,重组酶聚合酶扩增技术(rpa技术)具体包括:
75.(1)利用primer premier 5.0分别针对mtb的靶基因mts9025,mtbc的靶基因is108138,mb的靶基因16s rrna设计特异性引物,gapdh为阳性对照。
76.(2)在目的扩增序列的中间设计检测探针,并用fam、碱基核苷酸类似物和bhq1修饰。
77.(3)在恒温状态下(37~42℃)进行核酸等温扩增,时间为20分钟。扩增结束后,在488nm的激光灯下观察fam发射出来的绿色荧光。
78.与现有技术相比,本公开的有益效果是:
79.1、体积小,携带方便,无需仪器设备。
80.2、试剂及样本消耗量小。
81.3、易于操作,对操作者操作水平简单。
82.4、效率高,多指标同时检测。
83.5、成本低,采用普通生产工艺即可批量生产。
84.本公开还提供了前述用于核酸扩增检测的微流控芯片在人类结核分枝杆菌、结核分枝杆菌复合体、分枝杆菌检测中的应用。
85.本公开将该微流控芯片应用于结核病检测中。结核相关病原体mtb、mtbc、mb能够从结核分枝杆菌复合体中识别人类结核分枝杆菌,并从非结核分枝杆菌中区分结核分枝杆菌复合体。gapdh为阳性对照,以防止假阴性结果。从genbank中获得了mtb、mtbc和mb基因组片段,利用primer premier 5.0分别针对mtb的靶基因mts9025,mtbc的靶基因is108138,mb的靶基因16s rrna设计特异性引物。检测探针的核苷酸序列设计在扩增序列的中间,进行fam、碱基核苷酸类似物和bhq1修饰。所有引物和探针在生工生物技术公司合成(图6)。
86.本公开涉及一种快速便携式的核酸等温检测芯片,用于结核病的现场鉴定。具体的说是基于样本前处理和核酸恒温扩增的集成化技术,通过手指驱动液体的微流控芯片,将核酸提取、扩增、检测集于一体,研发了一款便携式多功能核酸检测芯片,检测结果可直接肉眼读取,实现了快速便携、无仪器的现场快速检测。
87.下面通过具体实施方式对本公开作进一步说明。
88.我们利用autocad 2020和solidworks 2017设计了手指驱动微流控芯片的结构,并在pmma上进行激光刻蚀。图1示出手指驱动微流控芯片的设计原理图。该芯片被设计为长度55毫米,宽度66毫米和厚度5毫米的巴掌大小的芯片。样品的进样口1直径为1.6毫米;两个圆柱形液体储存室2和3用于储存相应的缓冲液,直径为10毫米;为了防止液体回流,在三个进液口的微通道内嵌入了pdms制成的悬臂式挡板结构。将在pmma上刻蚀的悬臂阀作为挡板4、5、6,用pdms将200μm的弹性膜瓣7、8、9粘在距离挡板200μm左右的位置,80℃固定2h;dna提取区10为“w”形微通道,填充了二氧化硅颗粒,用于dna提取,微通道宽度1.5毫米,深度1.5毫米;废液池11的深度为4毫米,体积为680μl;在废液池上有一个通气孔12;核酸扩增区设计了五个平行的“y”形通道13~17,5个用于多重检测结核病相关病原体的小圆柱腔室直径为4毫米,深度为2毫米18~22,在扩增区最后设置一个通气孔23;微流控通道24的宽度为0.5毫米,深度为0.5毫米。还制作了可按压式的pdms膜;悬臂式挡板微阀,通过阀的变形防止液体回流,当微阀处于液体正向压力,挡板与弹性膜瓣之间的间隙可使流体顺利流动;当微阀受到流体反向压力,膜瓣与挡板紧密接触,阻断流体通过。
89.dna洗涤缓冲液2和rpa扩增缓冲液3预封装于两个pmma的液体储存室。dna洗涤缓
冲液的体积为350μl,其成分为70%乙醇和10mmtris(ph=8)。rpa缓冲液的体积为130μl,其成分为rpa扩增试剂盒中提供的复水缓冲液。
90.将二氧化硅颗粒用6m盐酸胍预处理30分钟,填充在“w”形微通道中,二氧化硅颗粒能够以盐桥的形式吸附dna。
91.微流控芯片的检测区的五个腔室中分别预封装mtbc,mtb,mb,gapdh四种引物,无菌水作为空白对照;冻干rpa酶反应干粉;rpa反应启动子醋酸镁(mgoac)。将混合物与0.1%琼脂糖在室温下干燥30分钟。一旦含有目标的样品进入密封的腔室,就会引发多重rpa反应。
92.以上所有试剂和材料准备完成后,芯片用单面封口膜进行封闭,形成封闭环境,在-20℃下保存使用。
93.在使用时,从痰中提取dna之前,需要进行简单的净化。50μl痰液添加到macl缓冲液中(1.5%柠檬酸钠,2%氢氧化钠,0.25%n-acetyl-l-cysteine),37℃加热15分钟,然后在95℃煮沸10分钟。随后,添加1毫克溶菌酶,将混合物在37℃下加热15分钟。然后,将混合物从芯片的进样口注射进样,dna被二氧化硅颗粒吸附。
94.rpa荧光扩增试剂盒购自杭州众测生物科技公司。rpa扩增时,反应混合液体积为25μl,其中复水缓冲液20.45μl,正向和反向引物各1μl,探针0.3μl,mgoac 1.25μl,dna模板1μl,以及冻干酶反应颗粒。对于手指驱动微流控芯片上的rpa反应,用复水缓冲液洗脱dna,然后转移到每个密封室,与引物、mgoac和冻干试剂颗粒混合。随后,将手指驱动微流控芯片置于42℃中水浴加热15分钟,最后在手持蓝绿灯下直接用肉眼读取结果。
95.为了提供准确的结核病感染类型信息,将手指驱动微流控芯片诊断结果分为4组,包括健康样本、mb感染、mtbc感染和mtb感染(图7):
96.(1)当芯片的四个孔均显示绿色荧光时,说明该样本为人类结核分枝杆菌,为mtb感染。
97.(2)孔2、孔3、孔4显示荧光,表示样品可能是牛分枝杆菌或其他分枝杆菌复合物,为mtbc感染。
98.(3)孔3和孔4显示荧光,说明样本可能感染了非结核分枝杆菌,为mb感染。
99.(4)当只有孔4有反应时,可能是一个健康的样本。
100.(5)但当所有的孔都没有荧光时,可能是样本中提取的dna不足以进行rpa扩增,或者芯片无法进行诊断。
101.图8测量了手指驱动微流控芯片的检出限(lod)。将合成的mtb、mtbc、mb、gapdh的质粒用tv缓冲液进行10倍梯度浓度(10
9-102copies/ml)稀释作为dna模板。随着模板浓度的降低,检测室中的绿色荧光强度降低,最终lod达到103copies/ml。
102.因此,在这项工作中,设计了一种低成本、便携式和无电的微流控芯片,以满足快速、现场检测结核病的需求,特别是在资源有限的地区。其优势在于:
103.(1)手指驱动微流控芯片通过简单的手指按压就可以完成包括固相dna提取和rpa扩增在内的整个过程,无需专业的技术人员。
104.(2)手指驱动微流控芯片实现了mb、mtbc和mtb的多重检测,不仅可以用于鉴别tb/非tb感染,而且同时对人mtb/m.bovis进行区分。
105.(3)手指驱动微流控芯片易于生产,成本较低,我们估计手指驱动微流控芯片的总
成本低于8美元,包括微流控芯片的制备、rpa缓冲液、酶和引物等所有元素。
106.(4)检测时间小于30分钟,包括dna提取和rpa扩增,有利于结核病的快速筛查。
107.综合所述,证明拟议的装置对于扩大我们在资源有限的环境中快速和大规模筛查传染性病原体引起的流行病的能力具有重要意义。
108.以上的具体实施例,对本公开的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上仅为本公开的具体实施例而已,并不用于限制本公开,凡在本公开的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本公开的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。