1.本发明属于医药生物技术领域,具体涉及宿萼木中一种二萜化合物及其制备方法和在神经保护药物开发中的应用。
背景技术:
2.宿萼木(strophioblachia fimbricalyx boerl.)为大戟科宿萼木属多年生灌木植物。主要分布于中国海南,云南,广西以及泰国。泰国民间用于治疗癌症,发烧,偏头痛等。然而国内外关于宿萼木的化学成分的报道较少。目前,主要报道从中分离得到变形菲、萜,黄酮苷等三十多个化合物,物质基础尚不明确。因此亟待对宿萼木的化学成分进行深入研究,分离制备其活性成分并研发新型药物。
技术实现要素:
3.本发明针对上述现有技术存在的问题,提供了一种从宿萼木中提取分离的strophiofimbrins类新型二萜化合物及其制备方法和应用,经研究发现本发明的新骨架结构化合物对pc12细胞凋亡具有较好的抑制作用。同时提供一种针对本发明新化合物的简便、快速、纯度高的提取分离方法。
4.本发明的目的是通过以下技术方案来实现的,一种二萜化合物,其通式如式(i)所示:
[0005][0006]
其中r1为-h或=o;r2为-oh、-och3或-nh2,r3为-oh或-och3。
[0007]
本发明具有神经保护活性的新型5/6/7三环系统的strophiofimbrins类化合物及其衍生物,本发明中式(i)所示化合物的酸加成的盐、水合物或前药也包括在本发明之中。
[0008]
优选的,所述的二萜化合物,其中r1为=o,r2为-nh2,r3为-och3,其结构式如式1所示:
[0009][0010]
[0011]
式1的化学名为strophiofimbrin a。
[0012]
优选的,所述的二萜化合物,其中r1为-h,r2为-och3,r3为-och3,其结构式如式2所示:
[0013][0014]
式2的化学名为strophiofimbrin b。
[0015]
其中strophiofimbrin a二萜化合物的制备方法,包括以下步骤:
[0016]
步骤a.将宿萼木药材剪碎,用乙醇回流提取,回收提取液,减压浓缩干燥,得到总浸膏;
[0017]
步骤b.将总浸膏用蒸馏水分散,依次用等体积石油醚、乙酸乙酯萃取,得到石油醚部位、乙酸乙酯部位;
[0018]
步骤c.将乙酸乙酯部位浸膏进行硅胶柱层析,用体积比为30∶1、15∶1、8∶1、5∶1、3∶1、2∶1、1∶1、1∶2、1∶5、0∶1的石油醚-乙酸乙酯梯度洗脱,合并后得11个流份;
[0019]
流份11经硅胶柱层析,用体积比为1∶0、50∶1、30∶1、20∶1、15∶1、10∶1、5∶1、1∶1、0∶1的二氯甲烷-甲醇梯度洗脱,合并后得9个流份;
[0020]
流份1经mci柱层析,用体积比为2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1、1∶0的甲醇-水梯度洗脱,合并后得10个流份;
[0021]
流份9经半制备高效液相色谱纯化,用体积比为41∶59的乙腈-水洗脱,收集主峰,得到化合物strophiofimbrin a。
[0022]
优选的,所述步骤a中乙醇采用体积分数为95%的乙醇水溶液85℃回流提取4次。
[0023]
其中strophiofimbrin b二萜化合物的制备方法,包括以下步骤:
[0024]
步骤s1:将宿萼木药材剪碎,用乙醇回流提取,回收提取液,减压浓缩干燥,得到总浸膏;
[0025]
步骤s2:将总浸膏用蒸馏水分散,依次用等体积石油醚、乙酸乙酯萃取,得到石油醚部位、乙酸乙酯部位;
[0026]
步骤s3:将乙酸乙酯部位浸膏进行硅胶柱层析,用体积比为30∶1、15∶1、8∶1、5∶1、3∶1、2∶1、1∶1、1∶2、1∶5、0∶1的石油醚-乙酸乙酯梯度洗脱,合并后得11个流份;
[0027]
流份11经硅胶柱层析,用体积比为1∶0、50∶1、30∶1、20∶1、15∶1、10∶1、5∶1、1∶1、0∶1的二氯甲烷-甲醇梯度洗脱,合并后得9个流份;
[0028]
流份1经mci柱层析,用体积比为2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1、1∶0的甲醇-水梯度洗脱,合并后得10个流份;
[0029]
流份8经半制备高效液相色谱纯化,用体积比为3∶2的甲醇-水洗脱,收集主峰,得到化合物strophiofimbrin b。
[0030]
优选的,所述步骤s3中乙醇采用体积分数为95%的乙醇水溶液85℃回流提取4次。
[0031]
本发明所述的二萜化合物或其互变异构体、区域异构体、立体异构体、对映异构体、非对映异构体以及其骨架相同或包含该骨架的结构或药学上可接受的盐在制备用于神经保护药物中的应用。
[0032]
术语“药学上可接受的盐”是指,在可靠的医学判断范围内,适合与人和低等动物的组织接触而没有过度毒性、刺激性、变态反应等等,并且与合理的益处/危险比例相称的那些盐。药学上可接受的盐在本领域是众所周知的。例如,berge等人在j.pharmaceutical sciences(1977)66:1-19中详细描述的药学上可接受的盐。
[0033]
本发明化合物可包括一个或多个不对称中心,且因此可以存在多种立体异构体形式,例如,对映异构体和/或非对映异构体形式。例如,本发明化合物可为单独的对映异构体、非对映异构体或几何异构体(例如顺式和反式异构体),或者可为立体异构体的混合物的形式,包括外消旋混合物和富含一种或多种立体异构体的混合物。异构体可通过本领域技术人员已知的方法从混合物中分离,所述方法包括:手性高压液相色谱法(hplc)以及手性盐的形成和结晶;或者优选的异构体可通过不对称合成来制备。
[0034]
本发明具有以下有益效果:(1)本发明提供来源于宿萼木的新化合物strophiofimbrins类二萜化合物及一种针对本发明新化合物的提取分离纯化方法,采用醇提取、硅胶柱层析、mci柱层析及半制备hplc进行分离纯化,成功获得新的化合物,操作方法简便及快速,且经该方法分离得到的化合物纯度较高,均大于95%。
[0035]
(2)本发明所述的新化合物strophiofimbrins类二萜化合物,经研究表明能够显著提高模型损伤神经细胞pc12的存活率,对pc12神经细胞凋亡有较好的抑制效果,因此本发明的化合物具有较显著的神经保护活性,能够在制备新型神经保护药物中应用,如用于治疗包括但不限于抑郁症、焦虑症、脑卒中及改善神经退行性疾病患者的认知障碍和运动迟缓。
附图说明
[0036]
图1为化合物1和化合物2的hmbc二维相关图;
[0037]
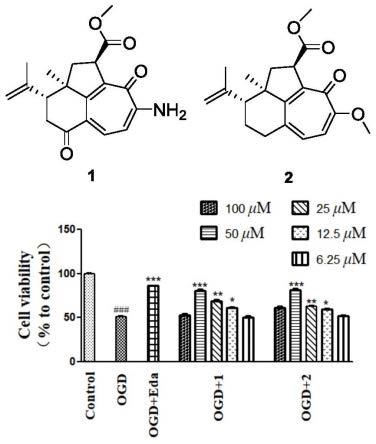
图2为化合物1和化合物2的结构及其对ogd损伤的pc12细胞的神经保护效果(平均值
±
sd,n=4)。与对照组相比,
###
p《0.001,*p《0.05,**p《0.01,***p《0.001。阳性对照:依达拉奉(eda);
[0038]
图3为化合物1和化合物2的实验与计算的ecd谱图;
[0039]
图4为化合物1的1h-nmr谱图;
[0040]
图5为化合物1的
13
c-nmr谱图;
[0041]
图6为化合物1的hmbc谱图;
[0042]
图7为化合物1的hsqc谱图;
[0043]
图8为化合物1的1h-1
h cosy谱图;
[0044]
图9为化合物1的noesy谱图
[0045]
图10为化合物1的高分辨质谱图
[0046]
图11为化合物1的单晶数据
[0047]
图12为化合物2的1h-nmr谱图;
[0048]
图13为化合物2的
13
c-nmr谱图;
[0049]
图14为化合物2的hmbc谱图;
[0050]
图15为化合物2的hsqc谱图;
[0051]
图16为化合物2的1h-1
h cosy谱图;
[0052]
图17为化合物2的noesy谱图;
[0053]
图18为化合物2的高分辨质谱图。
具体实施方式
[0054]
提供下列实施例进一步举例说明本发明,它们不应当认为是对本发明范围的限定。
[0055]
一种二萜化合物,其通式如式(i)所示:
[0056][0057]
其中r1为-h或=o;r2为-oh、-och3或-nh2,r3为-oh或-och3。
[0058]
实施例1:化合物1(strophiofimbrin a)的制备
[0059]
将宿萼木药材18kg,剪碎,95%乙醇85℃回流提取4次,合并提取液,减压浓缩干燥,得到总浸膏(472g)。将总浸膏用10倍量的蒸馏水分散,依次用等体积石油醚、乙酸乙酯、萃取,得到石油醚部位(123g)、乙酸乙酯部位(55g)。将乙酸乙酯部位浸膏进行硅胶柱层析,用体积比为30∶1、15∶1、8∶1、5∶1、3∶1、2∶1、1∶1、1∶2、1∶5、0∶1的石油醚-乙酸乙酯梯度洗脱,合并后得11个流份;流份11经硅胶柱层析,用体积比为1∶0、50∶1、30∶1、20∶1、15∶1、10∶1、5∶1、1∶1、0∶1的二氯甲烷-甲醇梯度洗脱,合并后得9个流份;流份1经mci柱层析,用体积比为2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1、1∶0的甲醇-水梯度洗脱,合并后得10个流份;流份9经半制备高效液相色谱纯化,用体积比为41∶59的乙腈-水洗脱,收集主峰,得到该化合物1。
[0060]
实施例2:化合物2(strophiofimbrin b)的制备
[0061]
将宿萼木药材18kg,剪碎,95%乙醇85℃回流提取4次,合并提取液,减压浓缩干燥,得到总浸膏(472g)。将总浸膏用10倍量的蒸馏水分散,依次用等体积石油醚、乙酸乙酯、萃取,得到石油醚部位(123g)、乙酸乙酯部位(55g)。将乙酸乙酯部位浸膏进行硅胶柱层析,用体积比为30∶1、15∶1、8∶1、5∶1、3∶1、2∶1、1∶1、1∶2、1∶5、0∶1的石油醚-乙酸乙酯梯度洗脱,合并后得11个流份;流份11经硅胶柱层析,用体积比为1∶0、50∶1、30∶1、20∶1、15∶1、10∶1、5∶1、1∶1、0∶1的二氯甲烷-甲醇梯度洗脱,合并后得9个流份;流份1经mci柱层析,用体积比为2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1、1∶0的甲醇-水梯度洗脱,合并后得10个流份;流份8经半制备高效液相色谱纯化,用体积比为3∶2的甲醇-水洗脱,收集主峰,得到该化合物2。
[0062]
化合物1和化合物2的结构式如下:
1.87,3h,s;δ
c 24.2)和甲基酯羰基(δ
c 177.4,52.5)。其余五个烯烃季碳(δ
c 177.5、164.3、160.8、146.5和138.4)和两个烯烃次甲基(δ
h 7.05和7.23,2h、d、j=10.2hz)构成另外三对双键和一个共轭羰基(δ
c 177.5)。上述官能团占9个不饱和度中的6个。因此,剩余的3个不饱和度要求是分子中的三环系统。
[0068]
在hmbc谱(图1)中,相关性起源于me-20(δ
h 1.11)到c-5、c-9,从典型异丙烯基的me-18和h-19到c-5,从h-5(δ
h 2.44)到c-4、c-10和c-20,从h-7(δ
h 3.11,2.92)到c-5、c-6、c-8和c-9,以及连续相关性1h-1
h cosy谱中的h-5/h-6α/h-7α/h-7β,建立了由c-10处的甲基和典型的异丙烯基取代的六元碳环b的片段c-5,它是三环结构的部分链段。1h-1
h cosy谱还显示存在一个自旋系统h-2/h-1α/h-1β,以及从h-2(δ
h 4.15)到c-1、c-11和c-的hmbc相关性3个甲酸甲酯基团,从me-20到c-1和c-9,从h-1(δ
h 2.25,2.01)到c-20、c-9、c-11和c-3,构建了一个五元环a在c-2处被甲基酯羰基取代,它与环b在共同的c-9和c-10处结合。然后,通过对α,β不饱和酮基团(δ
c 160.8,c-9;δ
c 146.5,c-11;δc177.5,c-17或δ
c 115.1,c-13;δ
c 164.3,c-12;δ
c 177.5,c-17)和从其他ome-12到c-12(δc164.3),从两个烯属次甲基h-13(δ
h 7.05)到c-8,c-12和c-17,以及h-14(δ
h 7.23)到c-9和c-12,以及一个自旋系统h-13/h-14的hmbc相关性的综合分析,构建了七元环c。h-14/c-7、h-7/c-14和h-2/c-17的hmbc交叉峰进一步表明环c与环b共享c-8和c-9,与环a共享c-9和c-11。因此,阐明了具有新型5/6/7环系统的平面结构。我们另外通过计算圆二色谱(图2)确定其构型同样为(2r,5r,10r)。综上,确定了该化合物的结构,并命名为strophiofimbrin b。
[0069]
表1:化合物1和化合物2的1h nmr和
13
c nmr数据
[0070][0071]arecorded in cdcl3;brecorded in meod.
[0072]
活性部分:
[0073]
实验材料:细胞培养液dmem、透气细胞培养瓶、96孔细胞培养板、pc12细胞、胎牛血清、胰蛋白酶、cck8试剂盒、青霉素-链霉素双抗溶液(青霉素工作浓度100u/ml,链霉素工作浓度为0.1mg/l)、strophiofimbrin a、strophiofimbrin b、依达拉奉、磷酸盐缓冲液pbs(0.03mol/l、ph=7.2)、微孔滤器、注射器、乙醇、dmso、离心管、ep管、1ml枪头、200ul枪头、手套、口罩等。
[0074]
购买的pc12细胞在37℃、5%co2培养箱中适应性培养。培养液为dmem培养液(含5%胎牛血清和1%双抗)。在37℃、5%co2饱和湿度培养箱中培养,待细胞长满培养瓶底后,倒掉培养液,用pbs洗涤2次,加入胰蛋白酶消化2min,再向其中加入dmem培养液终止消化,
轻柔吹打,以1200r/min离心5min,重悬细胞沉淀,接种于培养瓶,显微镜下观察拍照,待细胞长满单层,即可用于实验。
[0075]
实验模型的建立、分组、造模及给药:
[0076]
建立氧糖剥夺/复氧(oxygen glucose deprivation-reoxygenation,ogd/r)模型,用dmem培养液将经处理后的细胞稀释为5
×
104个/ml的细胞悬液,接种于96孔板,每孔加入200μl,适应性培养24h。分为正常对照组(对照组)、模型组(ogd组)、实验组(strophiofimbrin a、strophiofimbrin b药物组)、阳性药物对照组(依达拉奉edaravone组)进行实验:正常对照组全量换液成全量换液成dmem培养液(含10%胎牛血清),在恒温培养箱培养;模型组、实验组、阳性药物对照组全量换成dmem无糖培养液,在含1%o2、94%n2和5%co2的三气培养箱中低氧处理6h,实验组每孔分别加入终浓度分别为6.25μm、12.5μm、25μm、50μm和100μm的样品,阳性对照组加入对应浓度的依达他奉,然后恢复常氧,复氧24h。每孔加入10μl cck8,37℃孵育2h,酶标仪检测各组细胞在450nm下的吸光度值(od值)。
[0077]
计算公式为:
[0078]
细胞存活率=[(od给药组-od空白组)/(od对照组-od空白组)]
×
100%。
[0079]
以细胞活力评价其保护作用,与ogd对照(dmso,细胞活力50.82
±
1.99%)相比,化合物1(50μm)和2(50μm)表现出明显的神经保护作用,细胞活力分别为80.23
±
3.14%和81.25
±
3.83%,阳性对照药edaravone(50μm)的细胞活力为85.95
±
1.07%(图2)。实验结果显示,化合物1~2对ogd损伤的pc12细胞具有神经保护作用。
[0080]
本发明涉及到的新化合物能够显著提高模型损伤神经细胞pc12的存活率,对pc12神经细胞凋亡有较好的抑制效果,能够在制备新型神经保护药物中应用,如用于治疗包括但不限于抑郁症、焦虑症、脑卒中及改善神经退行性疾病患者的认知障碍和运动迟缓。以上结合附图对本发明的具体实施方式作了说明,但这些说明不能被理解为限制了本发明的范围,本发明的保护范围由随附的权利要求书限定,任何在本发明权利要求基础上的改动都是本发明的保护范围。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。