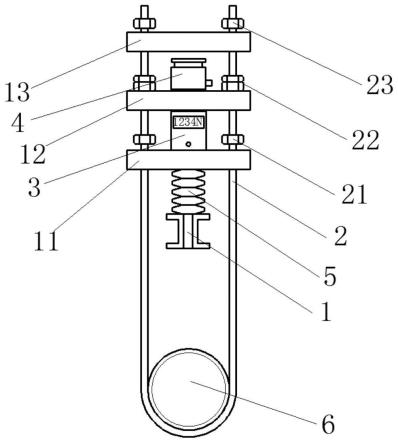
一种具有ph敏感和活性氧敏感的智能药物载体及其制备方法和应用
技术领域
1.本发明属于物理化学领域,具体涉及一种具有ph敏感和ros敏感的智能响应型药物载体的制备方法及应用,应用于增加抗癌药物溶解度以及药物的肿瘤微环境响应释放。
背景技术:
2.当前,癌症已经成为威胁人类生命健康的主要疾病之一,癌症治疗形势十分严峻。开发药物生物利用度高并且生物友好的新型智能药物递送系统是目前癌症治疗新方法的重要方向。
3.肿瘤微环境由癌细胞、血管系统、间质细胞和细胞外基质组成。肿瘤微环境不仅包括周围的成纤维细胞、干细胞和免疫细胞等,还包括肿瘤组织内的氧含量,ph值和氧化还原特性等生物学特征。肿瘤基质的细胞组分是肿瘤细胞增殖、凋亡和代谢的重要调控因子,控制着肿瘤细胞对治疗的敏感性。当肿瘤组织快速增殖时,其微环境会发生改变,生物学行为表现为组织氧含量降低、ph值降低和ros浓度升高等特征
1.。
4.介孔二氧化硅纳米颗粒由于其具有均匀且可控的介孔孔径、稳定的骨架结构、比表面积大和容易修饰的表面在药物载体领域广泛应用。介孔二氧化硅纳米颗粒的孔道内表面及颗粒外表面具有很多可以进行烷基化修饰的硅羟基,通过对其进行官能化修饰,如引入巯基、氨基、羧基以及更多复杂的有机官能团,这些官能团可以改变介孔二氧化硅纳米颗粒的生化性质或者可以与大分子聚合物连接,聚合物在介孔二氧化硅表面缠绕包覆形成纳米阀,减少负载药物的提前释放
2.。
5.为了实现载体在肿瘤组织部位的控制释放,用于药物载体的聚合物往往具有刺激响应性,例如ph,温度,ros,gsh和超声等。聚丙烯酸、聚甲基丙烯酸和聚谷氨酸等聚合物表现出ph响应特性,在酸性ph时发生质子化,碱性ph时发生去质子化,从而发生亲疏水的转变,控制药物载体组装与解组装。这类聚合物可以作为msn的封堵材料,利用其疏水时的收缩状态,包覆缠绕在介孔二氧化硅的表面,将药物封堵在孔道内部。当进入肿瘤组织后,聚合物发生质子化而伸展,药物从孔道中释放,从而实现在特定环境下的药物控制释放。参考文献:
6.[1]rahmanian m.,seyfoori a.,ghasemi m.,et al.in-vitro tumor microenvironment models containing physical and biological barriers for modelling multidrug resistance mechanisms and multidrug delivery strategies[j].journal of controlledrelease,2021,334(10):164-77.
[0007]
[2]fenton o.s.,olafson k.n.,pillai p.s.,et al.advances in biomaterials for drug delivery[j].adv mater,2018,30(29):1705328.
技术实现要素:
[0008]
为了解决部分化疗药物溶解度低、毒副作用强等问题,本发明提供了一种具有ph
敏感和ros敏感的介孔二氧化硅纳米药物载体及其制备方法,同时提供了该药物载体在增加药物溶解度以及肿瘤微环境响应释放中的应用。
[0009]
本发明技术方案为:
[0010]
本发明提供的纳米药物载体,由peg和pdpa-nh2封装介孔二氧化硅得到。通过可逆加成-断裂链转移聚合法,制备了一种具有ph敏感的聚合物pdpa,之后在两端修饰具有ros敏感特性的tk键得到pdpa-nh2。peg和介孔二氧化硅经羧基化修饰后,可与pdpa-nh2链端的氨基通过酰胺化反应连接,pdpa-nh2和peg连接的聚合物链在介孔二氧化硅表面缠绕包覆,从而达到封装药物的目的。上述纳米药物载体在酸性ph以及ros存在下,tk键氧化断裂,聚合物链从介孔二氧化硅表面脱落,促使负载在介孔二氧化硅孔道内的药物大量释放。
[0011]
本发明中包封介孔二氧化硅所用的pdpa-nh2嵌段同时具有ros响应和ph响应特性,该嵌段的中间部分为pdpa,即聚(2-二异丙基氨基甲基丙烯酸乙酯),两端修饰有缩硫基团tk,peg为聚乙二醇,pdpa-nh2与介孔二氧化硅以及peg之间通过tk基团相连接。所述tk键,其主体结构为-s-c(ch3)-s-,并以缩硫基团为中心的对称结构,其具有ros响应特性,在ros作用下可氧化断裂。
[0012]
本发明所述药物载体msn-pdpa-peg的平均粒径为150-200nm,如附图2所示。
[0013]
进一步,所述纳米药物载体在ros存在下,聚合物pdpa由疏水状态转化为亲水状态,起包封作用的聚合物链伸展,从而实现药物的响应性释放。
[0014]
进一步,所述的纳米药物载体在ros存在下,tk键被氧化断裂,表面起包封作用的pdpa-nh2嵌段和peg嵌段脱落,从而实现药物的响应性释放。
[0015]
本发明中所述的ros,即活性氧(reactive oxygen species),包括h2o2,单线态氧等。
[0016]
本发明还提供一种所述的具有ph敏感和活性氧敏感的智能药物载体的制备方法,具体如下:
[0017]
步骤1:聚合物pdpa-nh2的合成
[0018]
在β-巯基乙胺中加入浓盐酸,置于冰水浴中,搅拌至固体溶解,加入丙酮与二氯甲烷。将产物进行抽滤,洗涤,收集上层滤饼。将其用甲醇溶解,于冰乙醚中沉降。析出的固体中加入氢氧化钠溶液后,经搅拌、萃取、旋蒸得到产物tk连接体。
[0019]
将dpa、aibn和双(羧甲基)三硫代碳酸盐用1,4-二氧六环溶解,除水除氧。在65℃下搅拌反应,产物用乙醇和超纯水进行透析,冷冻干燥得产物pdpa。
[0020]
将pdpa溶解于thf中,并加入dcc和nhs。将tk溶解于thf中,逐滴滴加至上述体系,产物用乙醇和超纯水透析。真空冷冻干燥得产物pdpa-nh2。
[0021]
步骤2:msn的制备及其表面功能化
[0022]
将ctab(十六烷基三甲基溴化铵)溶解在超纯水中,逐滴加入naoh溶液,加热并搅拌。加入teos(正硅酸四乙酯),继续搅拌,产物经离心、洗涤后真空干燥。马弗炉煅烧得到产物msn。
[0023]
将msn超声分散于异丙醇中,加入aptes,加热至85℃反应。离心、洗涤后真空干燥得msn-nh2。将msn-nh2分散于dmf中,加入溶解与dmf的丁二酸酐。离心、真空干燥得产物msn-cooh。
[0024]
步骤3:载体msn-pdpa-peg的制备
[0025]
将msn-cooh分散于thf中,加入dcc和nhs,将pdpa-nh2溶解于thf中,加入上述体系。离心、洗涤后真空干燥得msn-pdpa。
[0026]
将peg-cooh分散于thf中,加入dcc和nhs,将msn-pdpa分散于thf中,加入至上述体系中。离心、洗涤后真空干燥得msn-pdpa-peg。
[0027]
优选地,所述步骤1中二氯甲烷与丙酮的体积比为1:2.5;
[0028]
优选地,所述步骤1中aibn、双(羧甲基)三硫代碳酸盐与dpa的摩尔比为1:1:500;
[0029]
优选地,所述步骤1中透析过程所用的透析袋截留分子量分别为3500和5000;
[0030]
优选地,所述步骤1和步骤3中nhs与dcc的质量比为1.5-2.5,优选1:2;
[0031]
优选地,所述步骤1中tk与pdpa-nh2的质量比为1:2-2.5,优选1:2.5;
[0032]
优选地,所述步骤3中pdpa-nh2与msn-cooh的质量比为1:1.5-2.0,优选1:1.75。
[0033]
本发明具有ros敏感和ph敏感的多重响应型纳米药物载体的制备方法,所述pdpa-nh2,以聚合物链pdpa为主体,两端通过化学修饰,引入含tk基团的末端带氨基的小分子,得到pdpa-nh2,末端的氨基与peg链的羧基和msn上修饰的羧基通过酰胺偶联反应,得到目标载体。
[0034]
本发明还提供了一种所述ros敏感和ph敏感介孔二氧化硅纳米药物载体在智能药物递送以及靶向释放等领域的应用。
[0035]
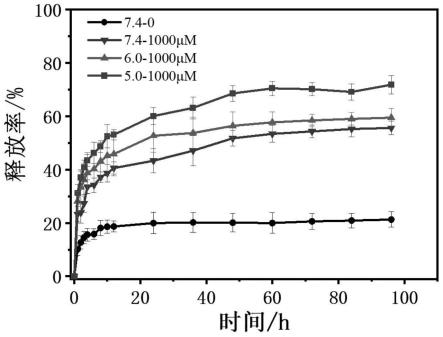
本发明以dox/icg为模板药物进行共装载,研究了h2o2和ph同时作用时的药物释放情况,结果如附图7所示,h2o2浓度设置为1000μm,探究在不同ph下的释放情况。随着ph的降低,其累积释放率逐渐升高,分别可以达到53%,56%和70%。ph为5.0和h2o2浓度为1000μm共同作用时的dox释放率高于仅有ph 5.0(60%)和仅有h2o2(53%)作用时的情况。药物释放结果呈现出ph/ros协同响应释放,当载体进入到低ph和过量ros表达的癌细胞内时,可以发挥这种协同作用,释放更多的药物进行治疗。此外,共装载icg后的载体呈现出nir(808nm)控制的突释效果,可实现定时、迅速、大量的药物释放。
[0036]
本发明相对于现有技术,具有以下有益效果:
[0037]
(1)本发明以介孔二氧化硅作为载体进行药物负载,与其他载体相比,介孔二氧化硅具有丰富且可调节的孔道、良好的生物相容性等优点,以其为药物载体,因epr效应的影响,使得载体在肿瘤组织部位富集,提高药物的生物利用度。
[0038]
(2)本发明以pdpa-nh2和peg作为纳米阀门包封介孔二氧化硅,pdpa-nh2的ph敏感点为6.50,以其为包封聚合物,提高了载体稳定性,减少了载体在非肿瘤部位的提前释放,在肿瘤部位酸性ph环境,pdpa-nh2的叔胺基质子化导致聚合物链伸展,促进药物释放。修饰在介孔二氧化硅表面的peg具有良好的生物相容性,可避免载体在血液循环过程中被捕获清除。如附图5所示,含dox的msn-pdpa-peg在两种介质中的粒径均维持在190nm左右,可以在所检测的时间里(96小时)里维持稳定。
[0039]
(3)本发明以tk键连接msn、pdpa-nh2和peg,tk键具有ros敏感特性,在ros浓度大于50μm时,tk键氧化断裂,从而导致聚合物链从介孔二氧化硅表面脱落,载体负载的药物释放。本发明提供了一种pdpa-nh2嵌段的制备方法,该嵌段同时具有ros敏感和ph敏感,是一种理想的具备多响应特性的聚合物嵌段,为刺激响应型智能药物载体的制备提供了一种可行的策略。
[0040]
(4)本发明提供了一种纳米介孔二氧化硅药物载体,并以pdpa-nh2和peg聚合物进
行包封。该药物载体在正常组织环境中表现出极高的稳定性,进入肿瘤组织后,低ph和高ros浓度促使载体裂解,药物迅速释放。本发明提供的智能药物递送体系具有载药量高,稳定性好,敏感性强等特点,是一种可以有效提高药物生物利用度、增强癌症治疗效果的策略。
附图说明
[0041]
图1为本发明中聚合物pdpa-nh2的合成流程图。
[0042]
图2为msn,msn-nh2,msn-cooh,msn-pdpa和msn-pdpa-peg的粒径分布图。
[0043]
图3为msn-pdpa-peg的tem图。
[0044]
图4为msn-pdpa-peg的sem图。
[0045]
图5为msn-pdpa-peg@dox在含10%fbs的dmem和1mm pbs中粒径随时间变化图。
[0046]
图6为msn-pdpa-peg@dox/icg溶液在nir照射10分钟前后的溶液图片。
[0047]
图7为msn-pdpa-peg@dox在h2o2浓度均为1000μm,ph分别为7.4,6.0和5.0下的dox的累积释放率。
具体实施方式
[0048]
为了使本发明所针对的研究背景、提供的技术方案以及所具备的有益效果更加直观的体现,以下结合具体实施实例,对本发明在药物递送领域的应用进行进一步的说明。以下实例仅仅是对本发明最佳实施方式的描述,并不对本发明在智能药物载体等领域的应用有任何限制。
[0049]
实施例1pdpa-nh2和peg包封的双重响应型纳米介孔二氧化硅药物载体的制备
[0050]
(1)msn的制备
[0051]
称取500mg ctab溶解于240ml超纯水中,超声溶解,然后在搅拌下逐滴滴加1.75ml的2mnaoh溶液。将溶液加热至80℃并持续搅拌30分钟,搅拌转速不要过快。提高转速,使用恒流泵缓慢滴加2.5ml teos,滴加速度为167μl/min,观察到体系变为乳白色后继续搅拌2小时。冷却至室温后,离心收集产物,并用乙醇和去离子水交替洗涤,使用广泛ph试纸检测离心上清液的ph,ph呈中性即洗涤完成。产物于60℃真空干燥箱中真空干燥24小时。使用马弗炉550℃煅烧6小时以除去模板分子ctab。最终得到白色产物msn。
[0052]
(2)msn表面氨基化
[0053]
称取400mg合成的msn,超声分散于50ml异丙醇,通氮气除氧除水20分钟后,逐滴滴加80μl(3-氨丙基)-三乙氧基硅烷偶联剂,85℃回流反应24小时。离心收集产物,并用异丙醇洗涤,以除去未反应的硅烷偶联剂。产物于真空干燥箱中常温干燥12小时,得到白色产物msn-nh2。
[0054]
(3)msn的表面羧基化
[0055]
称取300mg msn-nh2超声分散于40ml dmf溶剂中,搅拌20分钟,称取300mg丁二酸酐,溶解于5mldmf中,逐滴滴加至体系中,继续搅拌反应24小时。离心收集产物,产物用dmf洗涤三次,以除去未反应的丁二酸酐,乙醇洗涤三次,除去dmf,产物于真空干燥箱干燥12小时,得到白色产物msn-cooh。
[0056]
(4)tk连接体的制备
[0057]
称取5.78gβ-巯基乙胺,滴加4ml的12m浓盐酸,反应在冰水浴中搅拌,加入10ml丙酮与4ml二氯甲烷的混合溶剂,反应约10分钟,观察到有大量白色固体析出。将产物进行抽滤,并用少量二氯甲烷洗涤,收集上层滤饼。将滤饼用50ml甲醇溶解,然后浓缩至少量,于适量冰乙醚中沉降,并置于低温下沉降4小时,离心收集产物。产物加入10ml 6m氢氧化钠溶液,反应12小时。加入适量二氯甲烷,分液收集下层有机相,用超纯水洗涤、分液三次,无水硫酸镁干燥除水后抽滤。通过旋蒸得到产物,产物为黄白色透明油状物,于真空干燥箱中干燥12小时,产率为62%。
[0058]
(5)聚合物pdpa的合成
[0059]
分别称取dpa、aibn和双(羧甲基)-三硫代碳酸盐2g(9.38mmol),3mg(0.0188mmol)和43mg(0.188mmol)至史莱克瓶中,加入20ml1,4-二氧六环使固体完全溶解。通氮气15分钟,液氮冷冻,抽真空15分钟,充氮气解冻15分钟,如此循环三次,以除水除氧,然后加热至65℃搅拌反应12小时。所得产物为黄色粘稠状,将产物置于透析袋(mw:3500)中,使用乙醇和超纯水透析48小时,冷冻干燥得到白色固体产物pdpa。
[0060]
(6)pdpa-nh2的合成
[0061]
称取300mg pdpa-cooh,溶解于20ml thf中,通氮气搅拌20分钟,加入dcc 38mg活化15分钟,然后加入19mg nhs,继续搅拌反应3小时。将120mg tk溶解于5ml thf中,逐滴滴加至上述体系,继续反应24小时。所得产物过滤除去不溶物,然后将其置于透析袋中(mw=5000),用乙醇和超纯水透析48小时。产物真空冷冻干燥得到黄色固体pdpa-nh2。
[0062]
(7)msn-pdpa的制备
[0063]
称取350mg msn-cooh,分散于thf中,加入52mg dcc进行活化,15分钟后,加入26mg nhs,继续通氮气3小时。称取200mg pdpa-nh2,溶解于适量thf中,滴加至上述体系,继续搅拌反应24小时。离心收集产物,并用thf洗涤三次,置于真空干燥箱中干燥12小时,得到产物msn-pdpa。
[0064]
(8)msn-pdpa-peg的制备
[0065]
称取peg-cooh(mw=2000)98.6mg和dcc 46mg溶解于thf中,通氮气活化15-20分钟后,加入23mg nhs。3小时后,将msn-pdpa分散于适量thf中,加入至上述体系中,室温下继续反应24小时。离心收集产物并用thf洗涤三次,真空干燥12小时得到所述的多重响应型纳米药物载体msn-pdpa-peg。
[0066]
实施例2多重响应型纳米介孔二氧化硅药物载体装载与释放dox的研究
[0067]
(1)dox装载
[0068]
称取100mg载体msn-pdpa-peg,超声分散于30ml ph=7.4的1mm pbs缓冲溶液中,调节体系ph至6.0,搅拌30分钟。配制浓度为2mg/ml的dox溶液,向上述体系中滴加10ml,室温下避光搅拌24小时,使其充分装载。调节体系ph至7.4,搅拌2小时,离心收集负载dox的载体,用pbs缓冲溶液洗涤至上清液澄清。使用紫外可见光谱确定上清液dox含量,dox的紫外特征吸收波长为488nm。真空冷冻干燥得到载药后的载体msn-pdpa-peg@dox,载体颜色为红色。
[0069]
(2)药物控制释放
[0070]
ph响应释放:称取适量msn-pdpa-peg@dox,置于50ml离心管。设置ph分别为7.4,6.0和5.0的1mm pbs缓冲溶液作为释放体系。将释放体系置于37℃恒温震荡箱中,每隔一定
时间,吸取上清液,通过荧光分光光度计测量其荧光强度,激发波长为488nm,发射波长为550nm,狭缝宽度均为5nm,然后放回原体系,释药时间为96小时。
[0071]
h2o2响应释放:称取适量msn-pdpa-peg@dox,置于50ml离心管,设置浓度分别为0μm,50μm,100μm和1000μm的h2o2作为释放条件,溶液为ph 7.4的pbs缓冲溶液(1mm),检测方法同上。
[0072]
ph和h2o2双重响应释放:设置ph分别为7.4,6.0和5.0,含有1000μmh2o2的pbs缓冲溶液作为释放介质。其他检测方法同上。
[0073]
实施例3多重响应型纳米介孔二氧化硅药物载体装载与释放dox和icg的研究
[0074]
(1)icg和dox的共装载
[0075]
称取100mg载体msn-pdpa-peg,分散于20ml含1%dmso的pbs缓冲溶液中,并调节ph至6.0。分别配制浓度为2mg/ml的dox溶液和icg溶液,所用溶液为含1%dmso的pbs缓冲溶液,向上述体系中滴加10mldox溶液,15ml icg溶液。体系避光搅拌24小时,调节ph至7.4后,继续搅拌2小时,离心收集产物,用pbs缓冲溶液洗涤多次,去除未载入的dox和icg。通过紫外检测上清液药物含量,检测波长分别为488nm(dox)和780nm(icg)。真空冷冻干燥,得到载药后的载体msn-pdpa-peg@dox/icg,载体颜色为深绿色。
[0076]
(2)药物控制释放实验
[0077]
nir刺激释放:称取适量msn-pdpa-peg@dox/icg,置于50ml离心管中,设置释放介质为ph 7.4和5.0的pbs缓冲溶液。将释放体系置于37℃恒温震荡箱中。测量不同时间下的荧光强度,在特定时间进行nir光照,测定其荧光强度,以计算不同时间下的累积释放率。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。