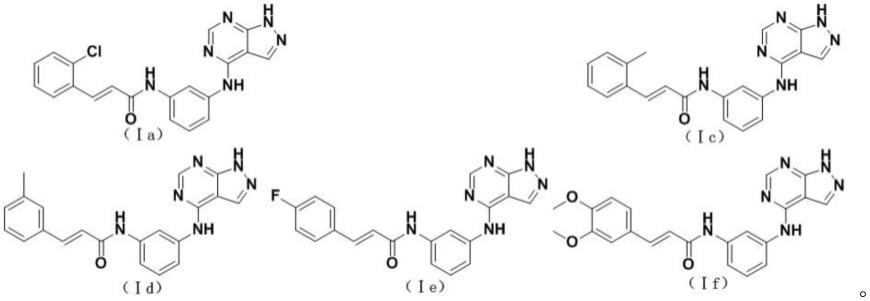
1.本发明涉及肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物及其制备方法,以及所述化合物在制备治疗或预防癌症的药物中的应用。
背景技术:
[0002]
吡唑并[3,4-d]嘧啶作为一种重要的药物骨架,与嘌呤的结构相似,吡唑并[3,4-d]嘧啶类化合物在许多药理活性中起着重要作用,例如抗炎活性、抗菌活性、抗病毒活性和抗结核活性等。1955年,skipper等人首先对吡唑并[3,4-d]嘧啶化合物进行了抗肿瘤活性探究,发现4-氨基吡唑并[3,4-d]嘧啶类化合物对实验性肿瘤具有杀伤性,从此,对吡唑并[3,4-d]嘧啶类化合物的研究引起了研究者的广泛兴趣。因此,吡唑并[3,4-d]嘧啶类化合物具有广阔的发展前景。
技术实现要素:
[0003]
本发明的第一个目的在于提供了一种具有良好抗癌活性的新型肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物。
[0004]
本发明的第二个目的是提供所述肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物的制备方法,该制备方法简便,易于操作,原料易得,且生产成本较低,适于工业化应用。
[0005]
本发明的第三个目的是提供所述肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物或其药学上可接受的盐在制备治疗或预防癌症的药物中的应用,所述的癌症为人恶性黑素瘤、人肺癌、人肝癌、人胃癌、人乳腺癌或人结肠癌,所述的癌症的癌细胞为人恶性黑素瘤细胞a375、人肝癌细胞hepg2、人胃癌细胞ags、人乳腺癌细胞t47d、人乳腺癌细胞mda-mb-231、人结肠癌细胞sw620。
[0006]
下面对本发明所采用的技术方案做具体说明。
[0007]
第一方面,本发明提供了一种肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物,其具有下列结构式(ⅰ):
[0008][0009]
式(ⅰ)中,r为2-cl、2-甲基、3-甲基、4-f或3,4-二甲氧基。
[0010]
本发明特别优选所述的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物选自下列之一:
[0011][0012]
第二方面,本发明提供了一种式(i)所示的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物的制备方法,所述制备方法为:将4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)加入有机溶剂a中,在-10~40℃搅拌条件下,滴加盐酸,反应5~50分钟,再滴加含有化合物(ⅲ)的有机溶剂a溶液,滴加完毕,升温至回流温度搅拌反应0.5~5小时,所得反应液经分离纯化得到式(ⅰ)所示的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物;
[0013][0014]
式(iii)中,r的定义同式(i)。
[0015]
进一步,所述的4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)与盐酸、化合物(ⅲ)的投料物质的量之比为1﹕0.1~1﹕0.8~1.2,优选为所述的4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)与盐酸、化合物(ⅲ)的的投料物质的量之比为1﹕0.1~0.5﹕0.9~1.2。
[0016]
进一步,所述有机溶剂a选自下列之一:甲醇、乙醇或异丙醇。所述有机溶剂a的用量以能够溶解4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)、化合物(ⅲ)即可。优选有机溶剂a总体积用量以4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)的物质的量计为10~50ml/mmol,其中溶解4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)所用有机溶剂a体积用量以4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)的物质的量计为5~25ml/mmol,溶解化合物(ⅲ)所用有机溶剂a体积用量以4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)的物质的量计为5~25ml/mmol。
[0017]
进一步,在0~30℃搅拌条件下,滴加盐酸。
[0018]
进一步,在0~30℃搅拌条件下,滴加含有化合物(ⅲ)的有机溶剂a溶液。
[0019]
进一步,反应过程用tlc跟踪检测(展开剂为体积比1~30:1的二氯甲烷和甲醇混合溶液),以确定反应终点,一般回流反应时间在0.5~5小时。
[0020]
进一步,所述分离纯化采用如下步骤:反应结束后,反应液冷却至室温,过滤,水洗,滤饼干燥后柱层析得到式(ⅰ)所示的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物。
[0021]
更进一步,所述柱层析的操作步骤具体如下:取滤饼于单口瓶中,加入有机溶剂b将其溶解,获得溶解液,然后向溶解液中加入滤饼质量1~2倍量的柱层析硅胶(优选300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的滤饼与硅胶的混合物,将混合物装柱上样,然后以体积比1~30:1的二氯甲烷和甲醇混合溶液为洗脱剂,进行洗脱,tlc跟踪检测(展开剂为体积比1~30:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含
式(ⅰ)所示化合物的洗脱液,将洗脱液浓缩干燥,获得式(ⅰ)所示化合物;所述有机溶剂b为下列之一:石油醚、二氯甲烷、甲醇或乙酸乙酯;所述有机溶剂b用量以能够溶解滤饼即可。
[0022]
本发明所述的有机溶剂a、有机溶剂b,所表示的都是指用于反应或柱层析的有机溶剂,这里的字母并没有特指某一些有机溶剂的含义,字母只是为了便于表达清楚,用来区分这些出现在不同的步骤中的有机溶剂。上述有机溶剂a或b可以为同一溶剂,也可为不同种溶剂。.
[0023]
第三方面,本发明提供了式(ⅰ)所示的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物或其药学上可接受的盐在制备治疗或预防癌症的药物中的应用,所述的癌症的癌细胞为人恶性黑素瘤细胞a375、人肝癌细胞hepg2、人胃癌细胞ags、人乳腺癌细胞t47d、人乳腺癌细胞mda-mb-231、人结肠癌细胞sw620。
[0024]
作为优选,所述癌细胞为a375、hepg2、ags、t47d、sw620细胞。
[0025]
作为优选,所述式(ⅰ)所示的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物中,r为2-cl。
[0026]
作为优选,所述癌细胞为hepg2,所述式(ⅰ)所示的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物中,r为2-cl、4-f或3,4-二甲氧基。
[0027]
作为优选,所述癌细胞为t47d,所述式(ⅰ)所示的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物中,r为2-cl。
[0028]
术语"药学上可接受的"在本技术中是指:化合物在化学上和/或在毒理学上与构成制剂的其它成分和/或与用其预防或治疗疾病或病症的人类或哺乳动物相容。
[0029]
术语"药学上可接受的盐"是指本发明化合物的相对无毒、无机酸或有机酸加成盐。例如,参见s.m.berge等人"pharmaceutical salts",j.pharm.sci.1977,66,1-19。其中,无机酸例如盐酸、氢溴酸、氢碘酸、硫酸、磷酸或硝酸等;有机酸例如甲酸、乙酸、乙酰乙酸、丙酮酸、三氟乙酸、丙酸、丁酸、己酸、庚酸、十一酸、月桂酸、苯甲酸、水杨酸、2-(4-羟基苯甲酰基)-苯甲酸、樟脑酸、肉桂酸、环戊烷丙酸、二葡萄糖酸、3-羟基-2-萘甲酸、烟酸、巴莫酸、果胶酯酸、3-苯基丙酸、苦味酸、特戊酸、2-羟基乙磺酸、衣康酸、胺基磺酸、三氟甲磺酸、十二烷基硫酸、乙磺酸、苯磺酸、对-甲苯磺酸、甲磺酸、2-萘磺酸、萘二磺酸、樟脑磺酸、柠檬酸、酒石酸、硬脂酸、乳酸、草酸、丙二酸、琥珀酸、苹果酸、己二酸、海藻酸、马来酸、富马酸、d-葡萄糖酸、扁桃酸、抗坏血酸、葡庚糖酸、甘油磷酸、天冬胺酸、磺基水杨酸等。
[0030]
与现有技术相比,本发明的有益效果主要体现在:(1)提供了一种新型的、具有良好的抗癌(尤其是人肝癌或人乳腺癌)活性的肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物;(2)提供了该肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物的制备方法,该制备方法简单,易于操作,原料易得且生产成本较低,适于实用,有望应用于制备预防或治疗肿瘤疾病的药物中;(3)提供了一类新型肉桂酰氨基吡唑并[3,4-d]嘧啶类化合物或其药学上可接受的盐在制备治疗或预防癌症的药物中的应用,该类化合物对于人恶性黑素瘤细胞a375、人肝癌细胞hepg2、人胃癌细胞ags、人乳腺癌细胞t47d、人乳腺癌细胞mda-mb-231、人结肠癌细胞sw620具有良好的抑制作用。
具体实施方式
[0031]
为使本发明的目的、技术方案和优点更加清楚,下面将进一步通过实施例对技术
方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0032]
4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ)的制备参照文献(organic letters,2013,15(8),1882-1885)的方法制备得到。
[0033][0034]
化合物(ⅲa)~(ⅲg)的制备反应式如下,反应式中r1的结构见上面化合物(ⅲa)~(ⅲg):
[0035][0036]
实施例制备的化合物(ia)~(if)的结构式如下:
[0037][0038]
实施例1:化合物(ⅲg)的制备
[0039]
三口烧瓶中加入7.4g(50mmol)肉桂酸和100ml无水二氯甲烷,冰浴条件下,滴加含有70.0g(551mmol)草酰氯的无水二氯甲烷溶液100ml,滴毕,加入dmf 2.0g,室温反应12小时,蒸除有机溶剂,得4.8g(29mmol)淡黄色油状物肉桂酰氯。
[0040]
三口烧瓶中加入4.8g(29mmol)肉桂酰氯和100ml无水二氯甲烷,冰浴条件下,滴加含有5.5g(40mmol)间硝基苯胺和4.2g(42mmol)三乙胺的二氯甲烷溶液100ml,滴毕室温反应10小时,蒸除有机溶剂,加入ph为1的稀盐酸100ml,过滤,100ml
×
3水洗涤滤饼,干燥得
5.6g(21mmol)n-(3-硝基苯基)肉桂酰胺。
[0041]
三口烧瓶中加入5.4g(20mmol)n-(3-硝基苯基)肉桂酰胺、15.2g(80.0mmol)二氯化锡和1.1g(21mmol)氯化铵,再加入200ml无水乙醇,磁力搅拌下,回流反应1.5小时,冷却至室温,将反应液用饱和碳酸氢钠水溶液调节ph至弱碱性,乙酸乙酯萃取(100ml
×
3),合并有机相,无水硫酸镁干燥,过滤,蒸除有机溶剂,得3.2g(13mmol)化合物(ⅲg)。
[0042]
化合物(ⅲa)~(ⅲf)的制备:将肉桂酸替换为相应的取代肉桂酸,参照实施例1的方法制备得到化合物(ⅲa)~(ⅲf)。
[0043]
实施例2:化合物(ⅰa)的制备
[0044]
用25.0ml的乙醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),-10℃磁力搅拌条件下,滴加1.0ml盐酸(1.0mol/l),反应5分钟,再滴加含有0.245g(0.9mmol)化合物(ⅲa)的25.0ml的乙醇溶液,滴完后反应液升温,回流反应0.5小时(反应过程采用tlc跟踪检测,展开剂为体积比1:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml石油醚溶剂将其溶解,获得溶解液,然后向溶解液中加入0.7克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比1:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比1:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰa)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰa),收率35%(以化合物(ⅲa)物质的量计),熔点287~290℃。1h nmr(500mhz,dmso-d6)δ13.64(s,1h),10.38(s,1h),10.06(s,1h),8.39(s,1h),8.28(d,j=9.5hz,2h),7.87(d,j=15.7hz,1h),7.78-7.75(m,1h),7.62(d,j=8.1hz,1h),7.57-7.54(m,1h),7.46-7.42(m,3h),7.33(t,j=8.1hz,1h),6.93(d,j=15.6hz,1h).
13
c nmr(125mhz,dmso-d6)δ163.17,155.27,154.82,154.41,139.78,139.45,135.43,133.56,132.66,131.30,130.18,129.07,127.97,127.81,125.58,116.69,114.61,112.27,100.73.esi-ms:(m/z)calcd for c
20h15
cln6o[m h]
391.1;found 391.2。
[0045]
实施例3:化合物(ⅰa)的制备
[0046]
用5.0ml的甲醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),40℃磁力搅拌条件下,滴加0.1ml盐酸(1.0mol/l),反应50分钟,再滴加含有0.327g(1.2mmol)化合物(ⅲa)的5.0ml的甲醇溶液,滴完后反应液升温,回流反应5小时(反应过程采用tlc跟踪检测,展开剂为体积比30:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml二氯甲烷溶剂将其溶解,获得溶解液,然后向溶解液中加入0.8克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比30:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比30:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰa)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰa),收率44%(以化合物(ⅱ)物质的量计),熔点287~290℃。1hnmr,
13
c nmr和ms同实施例1。
[0047]
实施例4:化合物(ⅰa)的制备
[0048]
用10.0ml的异丙醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),30℃磁力搅拌条件下,滴加0.5ml盐酸(1.0mol/l),反应30分钟,再滴加含有0.218g(0.8mmol)化
合物(ⅲa)的10.0ml的异丙醇溶液,滴完后反应液升温,回流反应1小时(反应过程采用tlc跟踪检测,展开剂为体积比15:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml乙酸乙酯溶剂将其溶解,获得溶解液,然后向溶解液中加入0.7克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比15:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比15:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰa)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰa),收率38%(以化合物(ⅲa)物质的量计),熔点287~290℃。1hnmr,
13
c nmr和ms同实施例1。
[0049]
实施例5:化合物(ⅰa)的制备
[0050]
用20.0ml的乙醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),0℃磁力搅拌条件下,滴加0.2ml盐酸(1.0mol/l),反应20分钟,再滴加含有0.273g(1.0mmol)化合物(ⅲa)的20.0ml的乙醇溶液,滴完后反应液升温,回流反应3小时(反应过程采用tlc跟踪检测,展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml甲醇溶剂将其溶解,获得溶解液,然后向溶解液中加入0.7克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比10:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰa)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰa),收率41%(以化合物(ⅱ)物质的量计),熔点287~290℃。1hnmr,
13
c nmr和ms同实施例1。
[0051]
实施例6:化合物(ⅰb)的制备
[0052]
用20.0ml的乙醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),0℃磁力搅拌条件下,滴加0.2ml盐酸(1.0mol/l),反应20分钟,再滴加含有0.307g(1.0mmol)化合物(ⅲb)的20.0ml的乙醇溶液,滴完后反应液升温,回流反应2.5小时(反应过程采用tlc跟踪检测,展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml甲醇溶剂将其溶解,获得溶解液,然后向溶解液中加入0.8克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比10:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰb)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰb),收率48%(以化合物(ⅱ)物质的量计),熔点273~275℃。esi-ms:m/z calcd for c
20h14
cl2n6o[m h]
425.1;found425.2。
[0053]
实施例7:化合物(ⅰc)的制备
[0054]
用20.0ml的乙醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),0℃磁力搅拌条件下,滴加0.2ml盐酸(1.0mol/l),反应20分钟,再滴加含有0.252g(1.0mmol)化合物(ⅲc)的20.0ml的乙醇溶液,滴完后反应液升温,回流反应3.5小时(反应过程采用tlc跟踪检测,展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml甲醇溶剂将其溶解,获
得溶解液,然后向溶解液中加入0.7克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比10:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰc)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰc),收率22%(以化合物(ⅱ)物质的量计),熔点258~259℃。1h nmr(500mhz,dmso-d6)δ13.63(s,1h),10.31(s,1h),10.06(s,1h),8.38(s,1h),8.27(d,j=15.3hz,2h),7.80(d,j=15.6hz,1h),7.60-7.57(m,2h),7.44(d,j=8.4hz,1h),7.33-7.23(m,4h),6.80(d,j=15.6hz,1h),2.39(s,3h).
13
c nmr(125mhz,dmso-d6)δ163.69,155.22,154.91,154.44,139.72,139.61,137.71,137.02,133.65,132.46,130.85,129.55,128.98,126.52,126.20,123.64,116.53,114.57,112.29,100.69,19.51.esi-ms:(m/z)calcd for c
21h18
n6o[m h]
371.2;found 371.2。
[0055]
实施例8:化合物(ⅰd)的制备
[0056]
用20.0ml的乙醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),0℃磁力搅拌条件下,滴加0.2ml盐酸(1.0mol/l),反应20分钟,再滴加含有0.252g(1.0mmol)化合物(ⅲd)的20.0ml的乙醇溶液,滴完后反应液升温,回流反应4小时(反应过程采用tlc跟踪检测,展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml甲醇溶剂将其溶解,获得溶解液,然后向溶解液中加入0.7克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比10:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰd)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰd),收率34%(以化合物(ⅱ)物质的量计),熔点254~259℃。1h nmr(500mhz,dmso-d6)δ13.62(s,1h),10.23(s,1h),10.04(s,1h),8.39(s,1h),8.28(d,j=15.9hz,2h),7.62(d,j=7.9hz,1h),7.55(d,j=15.7hz,1h),7.45-7.40(m,3h),7.35-7.30(m,2h),7.22(d,j=7.5hz,1h),6.87(d,j=15.7hz,1h),2.34(s,3h).
13
c nmr(125mhz,dmso-d6)δ163.72,155.19,154.95,154.45,140.25,139.74,139.64,138.25,134.79,132.49,130.53,128.98,128.95,128.28,125.02,122.36,116.53,114.53,112.22,100.71,20.99.esi-ms:(m/z)calcd for c
21h18
n6o[m h]
371.2;found 371.2。
[0057]
实施例9:化合物(ⅰe)的制备
[0058]
用20.0ml的乙醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),0℃磁力搅拌条件下,滴加0.2ml盐酸(1.0mol/l),反应20分钟,再滴加含有0.256g(1.0mmol)化合物(ⅲe)的20.0ml的乙醇溶液,滴完后反应液升温,回流反应4小时(反应过程采用tlc跟踪检测,展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml甲醇溶剂将其溶解,获得溶解液,然后向溶解液中加入0.7克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比10:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰe)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰe),收率38%(以化合物(ⅱ)物质的量计),熔点297~298
℃。1h nmr(500mhz,dmso-d6)δ13.62(s,1h),10.30(s,1h),10.06(s,1h),8.37(s,1h),8.27(d,j=23.2hz,2h),7.67(dd,j=8.6,5.6hz,2h),7.56(s,2h),7.41(d,j=8.4hz,1h),7.28(dt,j=24.4,8.5hz,3h),6.84(d,j=15.7hz,1h).
13
c nmr(125mhz,dmso-d6)δ163.92,163.61,161.95,155.19,154.97,154.44,139.74,139.61,138.98,132.48,131.51,131.49,130.01,129.95,128.96,122.42,116.54,116.17,115.99,114.55,112.23,100.72.esi-ms:(m/z)calcdfor c
20h15
fn6o[m h]
375.1;found 375.4。
[0059]
实施例10:化合物(ⅰf)的制备
[0060]
用20.0ml的乙醇溶解0.155g(1.0mmol)4-氯-1h-吡唑并[3,4-d]嘧啶(ⅱ),0℃磁力搅拌条件下,滴加0.2ml盐酸(1.0mol/l),反应20分钟,再滴加含有0.298g(1.0mmol)化合物(ⅲf)的20.0ml的乙醇溶液,滴完后反应液升温,回流反应4.5小时(反应过程采用tlc跟踪检测,展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),反应液冷却至室温,反应液过滤,滤饼用(10ml
×
3)水洗涤后,80℃干燥,干燥后的滤饼加入5.0ml甲醇溶剂将其溶解,获得溶解液,然后向溶解液中加入0.8克硅胶(300~400目粗孔(zcx.ii)型柱层析硅胶),混匀后,蒸除溶剂,得干燥的残留物与硅胶的混合物,将混合物装柱,然后以体积比10:1的二氯甲烷和甲醇混合溶液为洗脱剂,洗脱,tlc跟踪检测(展开剂为体积比10:1的二氯甲烷和甲醇混合溶液),根据tlc检测收集含式(ⅰf)所示的化合物的洗脱液,收集的洗脱液蒸除溶剂,干燥得到白色固体产物,即化合物(ⅰf),收率82%(以化合物(ⅱ)物质的量计),熔点260~263℃。1h nmr(500mhz,dmso-d6)δ13.62(s,1h),10.27(s,1h),10.03(s,1h),8.39(s,1h),8.28(d,j=10.7hz,2h),7.78(d,j=15.8hz,1h),7.60(d,j=8.0hz,1h),7.43(d,j=8.7hz,1h),7.32(t,j=8.1hz,1h),7.19(dd,j=7.7,1.5hz,1h),7.15-7.08(m,2h),6.91(d,j=15.8hz,1h),3.82(s,3h),3.77(s,3h).
13
c nmr(125mhz,dmso-d6)δ163.85,155.28,154.84,154.44,153.00,147.69,139.73,139.65,134.81,132.65,129.02,128.42,124.57,123.65,118.87,116.56,114.59,114.24,112.29,100.71,60.82,55.90.esi-ms:(m/z)calcd for c
22h20
n6o3[m h]
417.2;found417.2。
[0061]
实施例11:抗癌活性体外测试
[0062]
将制得的化合物(ⅰa)~(ⅰf)分别进行了人恶性黑素瘤细胞a375、人肺癌细胞a549、人肝癌细胞hepg2、人胃癌细胞ags、人乳腺癌细胞t47d、人乳腺癌细胞mda-mb-231、人结肠癌细胞sw620生物活性测试,其中化合物(ⅰa)由实施例5方法制备得到。
[0063]
测试方法:四氮唑盐还原法(mtt法)。
[0064]
细胞株:人恶性黑素瘤细胞a375、人肺癌细胞a549、人肝癌细胞hepg2、人胃癌细胞ags、人乳腺癌细胞t47d、人乳腺癌细胞mda-mb-231、人结肠癌细胞sw620。上述细胞株购自中国科学院上海生命科学院细胞库。
[0065]
实验步骤如下:
[0066]
(1)肿瘤细胞的培养
[0067]
实验所用的细胞代数均在5代以内。细胞培养所用的耗材和试剂均经过严格的灭菌操作,并且所有实验操作均在无菌操作台内进行。
[0068]
(a)肿瘤细胞的复苏
[0069]
实验开始前先把要使用的物品,如培养瓶、离心管、移液枪、枪头、废液桶等放入超净台打开紫外灯灭菌,并将细胞培养所用的试剂放入37℃恒温水浴锅内预热。一切准备工
作就绪后关掉紫外灯,开启超净台日光灯及通风扇。从-80℃冰箱内取出冻存的肿瘤细胞,在37℃水浴中振摇快速解冻,保证冻存管内冻存液仍有少部分未解冻的情况下,喷酒精放入超净台,然后立即将冻存管内的细胞全部转移至已加入含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620)的15ml离心管中,用移液枪轻轻吹打混匀。将离心管置于离心机中,转速1000rpm离心5min,在超净台内吸掉上清液。用移液枪吸取2ml含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620)至含有细胞沉淀的离心管中制成细胞悬液,并将细胞悬液吹打混匀转移到瓶底面积为25cm2的透气培养瓶中,再补加含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620)4ml,轻轻摇晃培养瓶混匀细胞,将培养瓶放至5%co2、37℃恒温培养箱中培养2~3天。
[0070]
(b)肿瘤细胞的传代
[0071]
当细胞生长状态良好并且铺满培养瓶瓶底70%~80%时,即可进行传代。传代操作步骤均在超净台内完成,将准备工作做好后即可开始传代。首先将培养瓶中的原有培养液用移液枪吸掉打进废液桶内,加2ml的pbs反复洗涤几次吸掉,然后加入600~700μl左右的胰蛋白酶(含0.02%edta、酚红和0.25%胰酶),保证瓶底完全被胰蛋白酶覆住,轻轻摇动培养瓶,放入37℃恒温培养箱中孵育1~2min,在显微镜下观察细胞脱落情况,如有少量细胞仍贴在壁上,可以用指肚轻轻敲打甁壁,直至细胞大部分能从瓶底脱落。加入2ml的含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620)终止消化后用移液枪轻轻吹打细胞,将细胞从瓶底全部吹落,并将细胞悬液转移至15ml离心管中,1000rpm,离心5min。吸掉上清液,用含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620)稀释吹打均匀后平均分配到2~3个培养瓶中继续在5%co2、37℃恒温培养箱内培养2~3天。
[0072]
(c)肿瘤细胞的冻存
[0073]
预先按照fbs(胎牛血清):dmso=9:1的体积比例配置好细胞冻存液,置于4℃冰箱备用。冻存操作步骤均在超净台内完成,将准备工作做好后即可开始冻存。首先将培养瓶中的原有培养液吸掉,加2ml的pbs缓冲液反复洗涤几次倒掉,然后加入600~700μl左右的胰蛋白酶(含0.02%edta、酚红和0.25%胰酶),轻轻摇动培养瓶,保证胰酶能够把培养瓶瓶底覆盖,放入37℃恒温培养箱中孵育1~2min,在显微镜下观察细胞脱落情况,如有少量细胞仍贴在壁上,可以用指肚轻轻敲打甁壁,直至细胞能大部分从瓶底脱落。加入2ml的含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620)终止消化后用移液枪轻轻吹打细胞,将细胞从瓶底全部吹落,并将细胞悬液转移至15ml离心管中,1000rpm,离心5min。倒掉上清液。加入1ml刚从4℃冰箱取出的冻存液,并吹打均匀形成细胞悬液,转移至冻存管内。在标记好细胞种类、细胞代数、冻存日期后放入4℃中静置30min,-20℃中静置1小时后放入-80℃超低温冰箱内保存。
[0074]
(2)mtt实验方法
[0075]
(a)细胞计数:将培养瓶中生长状态良好的肿瘤细胞经消化、离心后,用4ml含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620)重悬,取10μl细胞悬液至细胞计数板,计数后,细胞稀释到5
×
104个/ml。
[0076]
(b)铺板:取96孔板,实验孔加入100μl稀释过的细胞悬液,空白孔加入100μl含
10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620),周围补加100μl pbs缓冲液,在co2恒温培养箱中培养24h。
[0077]
(c)配制化合物加药:用含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620)将dmso配置的10μmol/ml化合物以及阳性对照药索拉菲尼稀释到指定浓度,分别为20μm、10μm、5μm、2.5μm、1.25μm,采用换液法进行上药。将原有培养液弃去,向实验孔中加入100μl含化合物或者阳性对照药的含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620),向对照组以及空白孔中加入100μl含10%fbs的dmem培养液(a375、hepg2、t47d、mda-mb-231)或含10%fbs的1640培养液(a549、ags、sw620),加药后把96孔板放入5%co2、37℃恒温培养箱内继续培养。
[0078]
(d)加mtt:48小时后,取出96孔板放入超净台内,避光条件下每孔加入10μl,5mg/ml的mtt溶液,之后放入5%co2、37℃恒温培养箱内继续培养。
[0079]
(e)检测:加入mtt的96孔板在培养箱中孵育3.5~4h取出,将每孔中的溶液小心地吸出,每孔加入150μl的dmso溶解生成的甲臜,然后放至平板振荡器上震荡10min,使用酶标仪检测490nm下的吸光度值。
[0080]
(f)实验数据处理:按照以下公式计算细胞存活率,细胞存活率50%的值即为ic
50
。
[0081]
细胞存活率(%)=[(as-ab)/(ac-ab)]
×
100%
[0082]
as:实验孔(含有细胞的培养液、mtt、毒性物质)
[0083]
ac:对照孔(含有细胞的培养液、mtt、没有毒性物质)
[0084]
ab:空白孔(含mtt、不含细胞和毒性物质的培养液)。
[0085]
测试的结果如表1所示:
[0086]
表1.化合物(ⅰ)对癌细胞生长的抑制作用
[0087][0088]
以上所述仅为本技术的实施例而已,并不用于限制本技术的保护范围,对于本领域的技术人员来说,本技术可以有各种更改和变化。凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。